Соединения, оптимизирующие утилизацию кислорода и обмен энергетических субстратов в кардиомиоцитах, получили название миокардиальных цитопротекторов, наиболее изученным из которых является триметазидин. Этот препарат путем селективного ингибирования митохондриальной 3–кетоацилКоА–тиолазы (3–КАТ) и, возможно, карнитин–пальмитол–трансферазы–1 (СРТ–1) уменьшает окисление жирных кислот и стимулирует использование глюкозы. Под действием триметазидина в условиях дефицита кислорода восстанавливается сопряжение гликолиза и окислительного декарбоксилирования, уменьшается внутриклеточный ацидоз, увеличивается количество пирувата, трансформирующегося в ацетил–КоА, что в конечном итоге приводит к увеличению продукции АТФ.
Триметазидин, способствуя синтезу большего количества молекул АТФ на одну потребляемую молекулу кислорода, улучшает баланс между потребностью миокарда в кислороде и его поступлением. Устранение дефицита внутриклеточного уровня АТФ, возникающего в условиях ишемии миокарда, составляет основу антиишемического кардиопротективного действия препарата. Кроме того, триметазидин активно участвует в утилизации сохраняющихся жирных кислот, стимулируя обмен фосфолипидов в сарколемме. Следствием этого являются уменьшение содержания свободных жирных кислот и создание благоприятных условий для восстановления структурной целостности клеточных мембран. Важный результат действия триметазидина – устранение ацидоза и высокой концентрации внутриклеточного кальция, характерных для ишемии, гипоксии и перерастяжения кардиомиоцитов, наблюдающихся при стенокардии и хронической сердечной недостаточности (ХСН). Протективное действие триметазидина в отношении кардиомиоцитов и эндотелиальных клеток снижает механическую и эндотелиальную дисфункцию, характерную для ишемии и ХСН. Это обеспечивает защиту миокарда от некроза и апоптоза. Поскольку эффекты триметазидина не связаны с влиянием на гемодинамику, его применение в отличие от традиционных антиангинальных препаратов не увеличивает риск артериальной гипотензии, брадикардии, нарушений проводимости и усугубления ХСН.
Антиангинальная эффективность
триметазидина
Оценке антиангинальной эффективности триметазидина было посвящено большое количество исследований. P. Sellier отметил, что на фоне приема препарата у 32 больных с ИБС достоверно увеличивалась толерантность к физической нагрузке и повышался порог ишемии по данным нагрузочных тестов: объем выполненной работы (+25%, р=0,012), продолжительность нагрузки (+114 с, р=0,016) и время до появления депрессии сегмента ST на 1 мм ниже изолинии (+90, р=0,034). J. Passeron у 54 больных со стабильной стенокардией, получавших триметазидин, продемонстрировал достоверное увеличение объема выполненной работы (+62%) и значительное уменьшение количества ангинозных приступов в неделю (–64%) при отсутствии каких–либо изменений параметров гемодинамики или развития выраженных побочных эффектов.
По данным ряда исследований, оптимизируя метаболизм кардиомиоцитов, триметазидин обладает не только антиангинальным действием, но и способствует сохранению жизнеспособности и функциональной активности хронически ишемизированного миокарда. Продемонстрировано положительное влияние триметазидина при нарушении локальной сократимости миокарда по данным стресс–эхокардиографии с добутамином. Известно, что нарушение локальной сократимости миокарда является более ранним признаком ишемии миокарда, чем изменения ЭКГ. Результаты эхокардиографии (увеличение индекса подвижности стенок левого желудочка (ЛЖ)) свидетельствуют о том, что, в отличие от плацебо, триметазидин достоверно уменьшал ишемию миокарда во время фармакологической пробы. Более того, на фоне приема препарата значительно увеличивались время инфузии (р=0,019) и доза добутамина (р=0,003). Это позволило предположить, что триметазидин защищает миокард от повреждения во время ишемии.
Результаты двойных слепых контролируемых исследований подтверждают целесообразность применения триметазидина как второго компонента комбинированной терапии стабильной стенокардии. Воздействие на различные звенья патогенеза ишемии миокарда (потребность миокарда в кислороде, его доставка и утилизация), с одной стороны, является физиологической основой для развития аддитивного эффекта компонентов такой комбинации, а с другой – уменьшает вероятность развития побочных эффектов терапии.
В ряде исследований продемонстрировано, что комбинированная терапия триметазидином и b–блокатором или антагонистом кальция позволила существенно улучшить состояние пациентов со стабильной стенокардией. В многоцентровом плацебо–контролируемом исследовании 67 пациентов со стабильной стенокардией, у которых предшествующее лечение дилтиаземом (180 мг/сут.) было недостаточно эффективным, были рандомизированы на дополнительный прием триметазидина (60 мг/сут.) или плацебо. Через 6 мес. комбинированной терапии у 87,5 (р<0,001) и 78% (р<0,01) больных соответственно на 25% уменьшилось количество приступов стенокардии и принимаемых таблеток нитроглицерина в сравнении с предшествующей монотерапией дилтиаземом.
Продолжительность нагрузочных тестов в обеих группах была схожей, за исключением порога ишемии, определяемого по времени нагрузки до появления депрессии сегмента ST на 1 мм ниже изолинии. Так, в основной группе этот показатель возрастал на 2 мин. 41 с (р<0,001) и достоверно не изменялся в группе плацебо. Кроме того, объем выполненной работы также был большим в группе триметазидина (1445,9 кГм; p<0,001), чем в группе плацебо (563,7 кГм; p=0,012).
В исследовании A. Michaelides и соавт. у 53 пациентов со стабильной стенокардией сравнивали эффективность триметазидина (60 мг/сут.) и изосорбида динитрата (40 мг/сут.), назначаемых дополнительно к пропранололу (120 мг/сут.) при недостаточной эффективности предшествующей терапии последним. Продемонстрировано, что комбинация пропранолола с триметазидином достоверно в большей степени, чем комбинация пропранолола с изосорбида динитратом, снижает количество приступов стенокардии (на 63%; р<0,01 и 31%; р<0,01 соответственно) и улучшает показатели велоэргометрии (время до появления депрессии сегмента ST на 1 мм возросло на 81 с (p<0,05); время до развития болевого приступа увеличилось на 125 с, p<0,05 по сравнению с монотерапией). Отмечены хорошая переносимость триметазидина и отсутствие влияния на параметры гемодинамики. Результаты этого исследования показали большую эффективность комбинации триметазидина с пропранололом, чем двух антиангинальных препаратов с гемодинамическим механизмом действия.
Способность триметазидина усиливать антиангинальную эффективность b–блокаторов, антагонистов кальция и нитратов, обеспечивая дополнительный клинический эффект и повышение толерантности к физической нагрузке у больных стабильной стенокардией через 4 нед. лечения, продемонстрирована в исследовании TRIMPOL. Исследование TRIMPOL–2, в которое было включено 347 больных стабильной стенокардией, резистентной к терапии метопрололом (100 мг/сут.), позволило подтвердить не только антиангинальную эффективность триметазидина (60 мг/сут.) и целесообразность его применения в качестве второго компонента комбинированной терапии, но и сохранение позитивного воздействия препарата на показатели нагрузочного теста через 3 мес. лечения.
Кроме того, значительное улучшение течения заболевания наблюдалось также среди больных ИБС, которым ранее была проведена баллонная коронарная ангиопластика или аортокоронарное шунтирование. Близкие результаты были получены в исследовании TACT (Trimetazidine in Angina Combination Therapy), включавшем 177 пациентов со стабильной стенокардией, которым в течение недели проводилась монотерапия нитратами пролонгированного действия (52%) или b–блокаторами (48%). Далее дополнительно к антиангинальной терапии назначался триметазидин (90 пациентов) или плацебо (n=87). Через 12 нед. терапии наблюдалось снижение количества приступов стенокардии с 5,6±0,6 до 2,7±0,5 в группе триметазидина и в группе плацебо – с 6,8±0,7 до 5,1±0,7 (p<0,05), а также числа потребляемых короткодействующих нитратов – с 5,2±0,9 до 2,8±0,8 и с 5,5±0,8 до 4,1±0,9 (р>0,05) соответственно. На фоне терапии триметазидином наблюдалось более значимое возрастание продолжительности нагрузочной пробы (с 417,7±14,2 до 506,8±17,7 с в основной группе и с 435,3±14,8 до 458,9±16,2 с в группе плацебо (p<0,05)), времени до появления депрессии сегмента ST на 1 мм (с 389,0±15,3 до 479,6±18,6 с в основной группе и в группе плацебо – с 411,8±15,2 до 428,5±17,3 с (p<0,05)) и времени до появления приступа стенокардии (с 417,0±16,9 до 517,3±21,0 с в основной группе и в группе плацебо – с 415,1±16,5 до 436,4±18,5 с (p<0,005)) при отсутствии влияния на параметры гемодинамики.
В российском исследовании ТРИУМФ, включавшем 846 пациентов со стабильной стенокардией, недостаточно контролируемой антиангинальными препаратами гемодинамического действия, 3–месячная терапия триметазидином (70 мг/сут.) в дополнение к комбинированной традиционной антиангинальной терапии, наряду со снижением количества приступов стенокардии и потребления короткодействующих нитратов в неделю (более чем в 3 раза) достоверно улучшала оценку пациентами качества жизни. Эти данные подтверждают, что триметазидин может быть назначен на любом этапе терапии стабильной стенокардии для усиления антиангинальной эффективности b–блокаторов, антагонистов кальция и нитратов.
M. Marzilli и соавт. в обзоре 23 крупных рандомизированных двойных слепых исследований (1378 пациентов со стабильной стенокардией), в которых сравнивалась эффективность триметазидина с плацебо или другими антиангинальными препаратами, продемонстрировали большую эффективность триметазидина в сравнении с плацебо по влиянию на клиническое состояние: количество приступов стенокардии в неделю (в среднем – 1,44, 95% ДИ от –2,10 до –0,79; p<0,0001) и число потребляемых таблеток нитроглицерина в неделю (–1,47 95% ДИ от –2,20 до –0,73; p<0,0001) и толерантность к физической нагрузке – увеличение времени до появления депрессии сегмента ST на 1 мм (p=0,0002). Триметазидин эффективен при лечении стабильной стенокардии как в качестве монотерапии, так и в сочетании с препаратами, обладающими гемодинамическим механизмом действия. В сочетании с традиционной терапией ИБС триметазидин демонстрирует аддитивный эффект, что дает дополнительные преимущества больным на фоне сохранения безопасности лечения.
Применение триметазидина
у пациентов с коронарной
ангиопластикой
В греческом исследовании проанализирована эффективность триметазидина у пациентов до и после чрескожного коронарного вмешательства (ЧКВ). 52 пациента, госпитализированные с острым коронарным синдромом, были рандомизированы на прием триметазидина (60 мг/сут.) или плацебо дополнительно к традиционной антиангинальной терапии за 15 дней до ЧКВ и в течение 3 мес. после процедуры. Продемонстрировано, что триметазидин минимизирует реперфузионное повреждение миокарда во время ЧКВ и улучшает глобальную и региональную контрактильность через 1 и 3 мес. после операции.
Применение триметазидина
при лечении ИБС у больных
с сахарным диабетом (СД)
Более высокая заболеваемость и смертность среди больных СД по сравнению с лицами, не имеющими этого заболевания, связана с нарушениями энергетического метаболизма миокарда. Даже при отсутствии ишемии кардиомиоциты больных СД поглощают меньше глюкозы и лактата. Абсолютно доминирующую роль в качестве источника энергии у этой категории больных играет бета–окисление жирных кислот. Лечение больных СД и ИБС должно быть направлено на снижение интенсивности бета–окисления жирных кислот и восстановление сопряженности между гликолизом и окислительным декарбоксилированием пирувата.
В связи с этим представляет интерес эффективность триметазидина у больных ИБС с СД. В открытом многоцентровом исследовании TRIMPOL–1 (Trimetazidine in Poland) у 50 пациентов со стабильной стенокардией и СД оценивали эффективность и переносимость комбинации триметазидина и антиангинального препарата. На фоне приема триметазидина (60 мг/сут.) в течение 4 нед. достоверно улучшались клинические показатели (частота приступов стенокардии составила 3,06 против 4,79 в неделю; p<0,01; потребность в нитроглицерине – 2,29 против 4,2 дозы/нед.) и параметры пробы с дозированной физической нагрузкой: общей выполненной работы (9,39 против 8,67 МЕТ, p<0,01), продолжительности нагрузки (440,2 против 383,2 с; p<0,01), максимальной величины депрессии сегмента ST (1,82 против 1,91 мм), времени нагрузки до появления депрессии сегмента ST на 1 мм ниже изолинии (358,3 против 301,6 с; p<0,01) и развития ангинозного приступа (400,0 против 238,3 с; p<0,01) в сравнении с исходными данными. При этом отмечена хорошая переносимость препарата.
Эти данные подтверждают, что у пациентов с ИБС в сочетании с СД триметазидин может быть эффективным и безопасным дополнением к препарату с гемодинамическим механизмом действия. Fragasso, Rosano и соавт. продемонстрировали улучшение общего состояния и фракции выброса (ФВ) левого желудочка (ЛЖ) при ишемической кардиомиопатии у пациентов с СД на фоне приема триметазидина.
Применение триметазидина
при лечении ИБС у больных
пожилого возраста
По мере старения у пациентов увеличивается количество сопутствующих заболеваний, а одновременное назначение нескольких препаратов увеличивает риск негативного лекарственного взаимодействия. Более того, имеются данные, что у пожилых больных на фоне приема антиангинальных препаратов чаще развиваются побочные эффекты. Оптимизируя энергетический обмен в миокарде, цитопротективные препараты не оказывают при этом отрицательного инотропного или хронотропного действия. Благодаря указанным свойствам препараты этого класса могут быть особенно эффективны при лечении ИБС у пациентов пожилого возраста (старше 65 лет). Так, в исследовании TRIMPOL–1 у 71 больного старше 65 лет прием триметазидина в течение 4 нед. достоверно улучшал клинические показатели и параметры нагрузочных тестов: продолжительность нагрузки (р<0,01); время нагрузки до появления депрессии сегмента ST на 1 мм ниже изолинии (на 50 с), время нагрузки до возникновения приступа стенокардии (на 126 с). Побочные эффекты отмечены у 3% пациентов. В исследовании TRIMEP (Trimetazidine in Elderly People), включавшем пациентов старше 65 лет, из которых 20% были старше 70 лет, отмечены эффективность комбинации триметазидина с традиционной терапией и повышение качества жизни обследуемых на фоне лечения данным препаратом.
Применение триметазидина
при лечении ИБС у больных
с метаболическим синдромом (МС)
Leonardo и соавт. в рандомизированном двойном слепом перекрестном исследовании у 16 пациентов с МС, получавших триметазидин (60 мг/сут.) или атенолол (100 мг/сут.) в течение двух 2–недельных периодов, продемонстрировали благоприятные эффекты атенолола на клиническое состояние, переносимость нагрузок и диастолическую функцию ЛЖ и отсутствие существенного изменения указанных показателей на фоне терапии триметазидином. Авторы предположили, что полученные данные могут быть следствием различных механизмов, ответственных за развитие клинической симптоматики при МС.
В польском исследовании изучена эффективность 6–месячной терапии триметазидином у 34 пациентов с МС. Оценка клинического состояния и толерантности к физической нагрузке проводилась через 1 и 6 мес. Отрицательные результаты тредмил–теста отмечены у 4 (11,76%) и 5 пациентов (14,71%) через 1 и 6 мес. терапии триметазидином соответственно. Продемонстрировано уменьшение количества приступов стенокардии через 6 мес. терапии (приступы стенокардии регистрировались у 76,47% до начала терапии и у 38,23% через 6 мес. лечения). Не выявлено влияния триметазидина на АД и ЧСС. Продолжительность нагрузки существенно возрастала через 1 мес. (652,9±206,2 против 563,4±190,4 с, p=0,0047) и 6 мес. (650,3±207,8 с, p=0,0094) терапии. Эта данные позволили авторам сделать вывод, что терапия триметазидином улучшает клиническое течение заболевания и повышает толерантность к нагрузке у больных с МС.
Применение триметазидина
при лечении ХСН
Лечение ХСН представляет собой одну из актуальных проблем современной медицины в связи с неуклонным ростом заболеваемости, инвалидизации и смертности. Основу фармакотерапии ХСН составляют ингибиторы АПФ (иАПФ), диуретики, b–блокаторы. В большинстве случаев рациональное использование комбинации препаратов с различными механизмами действия повышает эффективность и качество жизни больных с ХСН. Однако применение только препаратов данных групп не позволяет полностью решить проблему медикаментозной терапии ХСН, поэтому в настоящее время происходит не только совершенствование уже существующих подходов, но и разработка новых направлений лечения ХСН.
На сегодняшний день накоплен целый ряд доказательств, что триметазидин при добавлении к гемодинамической терапии оказывает благоприятное влияние на ФВ ЛЖ у пациентов с ишемической кардиомиопатией и систолической дисфункцией ЛЖ.
Влияние длительной терапии триметазидином на показатели сократительной способности ЛЖ у больных с ишемической кардиомиопатией оценена D. Napoli и соавт. Пациенты (61 человек) с ишемической кардиомиопатией и ХСН II–IV ФК по NYHA c систолической дисфункцией (ФВ ЛЖ 30±1%) были рандомизированы для проведения двойного слепого плацебо–контролируемого исследования. 30 пациентам дополнительно к традиционной терапии назначался триметазидин (60 мг/сут.). Через 18 мес. лечения отмечены уменьшение ФК ХСН по NYHA, улучшение контрактильности миокарда ЛЖ (прирост ФВ ЛЖ составил 7%, р<0,001, тогда как в группе сравнения этот показатель уменьшился на 5%, р>0,05), замедление процесса ремоделирования ЛЖ (конечно–диастолический объем ЛЖ в основной группе незначительно уменьшился, тогда как в группе сравнения возрастал (р<0,001)). Этому соответствовали стабильный уровень С–реактивного белка в плазме крови (маркера воспаления) в группе триметазидина и увеличение этого показателя в группе сравнения (разница между группами оказалась достоверной – р<0,001). Авторы предположили, что подавление воспаления способствует улучшению обмена веществ в кардиомиоцитах и эндотелиальных клетках, что ведет к повышению сократимости и коронарного кровотока соответственно, предупреждает повреждение клеток и, в конечном итоге, уменьшает тканевую реакцию и воспаление.
В плацебо–контролируемом исследовании изучено влияние триметазидина на сократительную функцию миокарда у 38 больных с постинфарктной дисфункцией ЛЖ (ФВ ЛЖ в среднем 33%), рандомизированных на прием триметазидина или плацебо. Перед началом и через 2 мес. лечения всем пациентам проводили стресс– эхокардиографию с введением малой дозы добутамина и нагрузочный тест. У пациентов, получавших триметазидин, наблюдались значительное снижение индекса нарушения сегментарной сократимости в покое и при нагрузке (р<0,001) и увеличение ФВ (р<0,001) без изменения ЧСС и АД. Кроме того, у больных, получавших триметазидин, по сравнению с группой плацебо отмечено достоверное увеличение объема кислорода при нагрузке (р=0,001). Vitale и соавт. показали, что добавление триметазидина к традиционной терапии улучшает систолическую и диастолическую функции ЛЖ, а также повышает качество жизни пожилых пациентов, страдающих ишемической кардиомиопатией.
В двойном слепом плацебо–контролируемом исследовании, включавшем 20 пациентов с ХСН III и IV функциональных классов (ФК) по NYHA, изучены преимущества добавления триметазидина (60 мг/сут.) в классическую схему лечения ХСН. Через 6 мес. у больных, получавших триметазидин, наблюдалось значительное улучшение состояния по показателям тяжести одышки, величины ФВ ЛЖ и объема сердечного выброса (соответственно р<0,001, р<0,018 и р<0,034) в сравнении с группой плацебо.
В другом двойном слепом перекрестном исследовании с участием 15 пациентов с ИБС и умеренно сниженной ФВ ЛЖ в течение 2 нед. назначался триметазидин (60 мг/сут.) или плацебо. Критериями оценки эффективности терапии были: повышение устойчивости миокарда к ишемии, определяемое с помощью дозы добутамина и времени его инфузии при проведении стресс–эхокардиографии, и улучшение функции ЛЖ по индексу нарушения сегментарной сократимости в покое и на пике введения добутамина. Длительность исследования составила 30 дней. В группе триметазидина индекс нарушения сегментарной сократимости как в покое, так и на пике введения добутамина значительно снижался (р=0,013 и р=0,018 соответственно), существенно увеличивались время инфузии добутамина (с 15,3 до 17,9 мин., р=0,019) и введенная доза добутамина (с 22,7 до 28,7 мкг/кг/мин., р=0,003). Триметазидин не только защищал миокард от ишемического повреждения во время нагрузки, но и улучшал локальную сократимость миокарда ЛЖ в покое (это связано со снижением количества участков гибернации миокарда), при этом он не влиял на показатели гемодинамики и потребления миокардом кислорода.
В.С. Задионченко и соавт. изучали роль триметазидина (Предизин, «Гедеон Рихтер», Венгрия) в составе комплексной терапии больных ХСН. Было обследовано 60 больных ХСН II–III ФК (NYHA) с ФВ ЛЖ <45%. Все исследуемые были распределены на 2 группы, сравнимые по базисной терапии, тяжести недостаточности кровообращения: 1–ю группу составили 40 больных, находившихся на терапии иАПФ, диуретиками и b–блокаторами, во 2–ю группу вошли 20 пациентов, дополнительно получавших Предизин. Доза Предизина составила 35 мг 2 раза/сут., длительность лечения – 5 нед. В ходе исследования оценивались клиническая эффективность комплексной терапии, качество жизни пациентов, динамика состояния микроциркуляции, морфофункциональные параметры сердца. На фоне комплексной терапии с добавлением Предизина улучшение ФК ХСН отмечалось в 78% случаев, клиническая эффективность терапии была хорошей; в 18% – удовлетворительной (однако ФК ХСН не претерпел изменений), неудовлетворительной – в 4% случаев. В контрольной группе результаты клинической эффективности были хорошими у 66% пациентов, удовлетворительными – у 24% и неудовлетворительными – у 10%.
Отмечено улучшение (р<0,05) показателей качества жизни под влиянием обоих методов лечения, но существенно более выраженное – при включении в терапию Предизина. Так, под влиянием традиционной терапии происходит достоверное улучшение качества жизни (КЖ) в 1–й группе больных, уменьшение среднего суммарного балла КЖ с 69,1±6,0 до 55,8±5,2 (р<0,05) (согласно Миннесотскому опроснику, уменьшение суммарного балла КЖ означает улучшение качества жизни). Дополнительное включение в традиционный лечебный комплекс Предизина сопровождалось более выраженными положительными сдвигами в показателях КЖ во 2–й группе больных, отмечено достоверное (р<0,05) уменьшение среднего суммарного балла КЖ с 69,1±6,0 до 43,7±5,0 (табл. 1).
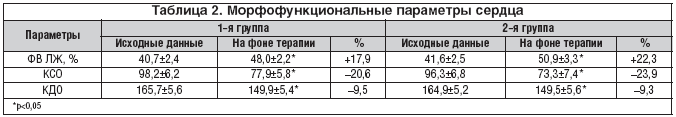
Морфофункциональные параметры сердца в большей степени улучшились у больных 2–й группы: ФВ составила 41,6±2,5 и 50,9±3,3% до и через 5 нед. лечения соответственно (р<0,05). КСО (конечный систолический объем) и КДО (конечный диастолический объем) уменьшились на 23,9 и 9,3% соответственно. У больных 1–й группы ФВ составила 40,7±2,4 и 48,0±2,2% до и в конце лечения (р<0,05), КСО и КДО уменьшились на 20,6 и 9,5% соответственно (табл. 2).
Комбинированная терапия с добавлением Предизина привела к достоверному увеличению ФВ ЛЖ и уменьшению объема сердца, что говорит об улучшении сократительной способности миокарда.
На фоне лечения у всех больных достоверно возрос средний показатель микроциркуляции (ПМ). У пациентов, получавших традиционную терапию ХСН, средний ПМ возрос на 7,3%. Однако наиболее выраженный прирост ПМ произошел в группе, получавшей Предизин, – на 28,2% (р<0,05). Во 2–й группе достоверно снизилось внутрисосудистое сопротивление – на 13,9% (р<0,05), в 1–й – на 11,2% (р<0,05). Обращает на себя внимание снижение эндотелиальной активности при терапии Предизином – на 24,3%, в то время как без нее – на 15,3%.
При распределении пациентов с ХСН по гемодинамическим типам микроциркуляции (ГТМ) исходно преобладали стазический, который составил в среднем по группам 36%, и спастический – 32%. На долю гиперемического и застойного ГТМ пришлось 12 и 10% соответственно. Нормоциркуляционный ГТМ был выявлен у 10% обследованных больных ХСН.
На фоне терапии тяжелые формы нарушения микрогемодинамики частично регрессировали. В контрольной группе количество пациентов со стазическим ГТМ не претерпело изменений, однако при лечении Предизином встречаемость стазического типа ГТМ уменьшилась на 8%. Количество пациентов со спастическим типом уменьшилось на 8% в 1–й группе и на 12% – во 2–й, с застойным ГТМ – на 8%, и он полностью исчез на фоне лечения Предизином. Распределение гиперемического ГТМ в среднем по группам осталось постоянным. На фоне лечения в обеих группах увеличилось (на 20–25%) число больных с нормоциркуляторным ГТМ, что убедительно свидетельствует об улучшении состояния микроциркуляции, которое происходит за счет как уменьшения стаза крови в периферических сосудах, так и за счет нормализации собственной гладкомышечной активности микрососудов. Положительная динамика всех показателей микроциркуляции была более выражена на фоне применения Предизина.
Заключение
Во всех исследованиях продемонстрирована хорошая переносимость терапии триметазидином. Побочные эффекты препарата развивались редко и не требовали отмены терапии. Так, в исследовании ТРИУМФ переносимость терапии триметазидином была оценена как отличная и хорошая и врачами (98,4%), и пациентами (97,6%).
Таким образом, результаты исследований подтверждают, что триметазидин, улучшая клеточный энергетический метаболизм, снижает тяжесть и длительность периодов ишемии, повышает сократимость «спящего» миокарда и улучшает систолическую и диастолическую функцию ЛЖ. Препарат способен усиливать лечебное действие традиционных антиангинальных препаратов, не влияя на параметры гемодинамики. Полученные результаты убедительно свидетельствуют о том, что добавление триметазидина к традиционной терапии больных ХСН II–III ФК улучшает клиническое состояние больных, сократительную функцию миокарда, уменьшает нарушения микроциркуляции в большей степени, чем при применении комплекса лекарственных средств, не включающего миокардиальные цитопротекторы. Все это позволяет назвать триметазидин (Предизин, «Гедеон Рихтер», Венгрия) перспективным лекарственным средством и рекомендовать его данной категории больных.

Литература
1. Бранько В.В., Вахляев В.Д., Камшилина Л.С., Маколкин В.И. Влияние ингибиторов ангиотензинпревращающего фермента на состояние микроциркуляции у больных с хронической сердечной недостаточностью // Кардиология. 1999. Т. 39. № 3.
2. Бузиашвили Ю.И., Маколкин В.И., Осадчий К.К., Асымбекова Э.У., Ахмедярова Н.К., Старовойтова С.П. Влияние триметазидина на обратимую дисфункцию миокарда при ишемической болезни сердца // Кардиология. 1999. Т. 39. № 6.
3. Задионченко В.С., Шехян Г.Г., Ялымов А.А., Заседателева Л.В. Микроциркуляция и морфофункциональный статус больных хронической сердечной недостаточностью при лечении триметазидином // Кардиоваскулярная терапия и профилактика. 2004. Т. 3. № 5. С. 74–80.
4. Саркисов К.Г, Дуфак Г.В. Лазерная допплеровская флоуметрия как метод оценки состояния кровотока в микрососудах // Методология флоуметрии. 1999. С. 9–14.
5. Терещенко С.Н., Акимова О.С., Демидова И.В., Борисова Н.Е., Моисеев В.С. Цитопротектор триметазидин в комплексной терапии тяжелой постинфарктной хронической сердечной недостаточности // Кардиология. 1999.Т. 39. № 9.
6. Маколкин В.И., Глезер М.Г., Жарова Е.А., Капелько В.И., Карпов Ю.А., Ланкин В.З., Сыркин А.Л. Ишемия миокарда: от понимания механизмов к адекватному лечению // Кардиология. 2009. Т. 40. № 9.
7. Оганов Р.Г., Глезер М.Г. Кардиология. 2007. № 3. С. 4–13.
8. Belardinelli R., Purcaro A. Effects of trimetazidine on the contractile response of chronically dysfunctional myocardium to low–dose dobutamine in ischemic cardiomyopathy // Eur. Heart J. 2001. Vol. 22. P. 2164–2170.
9. Colantuoni A., Bertuglia S., Integlietta M.Microvascular vasomotion: origin of laser doppler flux motion // Int. Microcirc.Clin. Exp. 1994. Vol. 23. Р. 151–158.
10. Dalla–Volta S., Maraglino G., Della–Valentina P. et al. Comparison of trimetazidine with nife–dipine in effort angina. A double–blind crossover study // Cardiovasc. Drugs Therap. 1990. Vol. 4. P. 853–860.
11. Detry J.M., Leclerca P.J. on behalf of the TEMS Steering Committee. Trimetazidine European Multicenter Study versus Propranolol in stable angina pectoris: combination of Holter electrocardiographic ambulatory monitoring // Am. J. Cardiol. 1995. Vol. 76. P. 8–11.
12. Fagrell B., Intaglietta M.Microcirculation: its significance in clinical and molecular medicine // J. Intern. Medicine. 1997. Vol. 241. N 5. Р. 349–362.
13. Kantor P.F., Lucien A., Kozak R., Lopaschuk G.D. The antianginal drug Trimetazidine shifts cardiac energy metabolism from fatty acid oxidation to glucose oxidation by inhibiting mitochondrial long–chain 3–ketoacyl CoenzymeAthiolase // Circ. Res. 2000. Vol. 86. P. 580–588.
14. Manchanda S.C., Krishnaswami S. Combination treatment with trimetazidine and diltiazem in stable angina pectoris // Heart. 1997. Vol. 78. Р. 353–357.
15. Passeron J. Clinical efficacy of trimetazidine in stable angina pectoris // Press. Med. 1986. Vol. 15. P. 1775–1778.
16. Sellier P. Chronic effects of trimetazidine on ergometric parameters in effort angina // Cardio–vasc. Drugs Ther. 1990. Vol. 4. P. 822–823.












