2) кардиоселективные, преимущественно взаимодействующие с β-1-адренорецепторами (бисопролол, метопролол, атенолол, эсмолол);
3) препараты, обладающие вазодилатирующими свойствами (карведилол, небиволол);
4) препараты с внутренним симпатомиметическим действием (пиндолол, ацебутолол, окспренолол).
Препараты из четвертой подгруппы из-за отсутствия положительного влияния на прогноз жизни больных ИБС в настоящее время не рекомендованы для их лечения. В связи c наличием нескольких групп β-адреноблокаторов врачу очень важно располагать информацией по сравнительной оценке их эффективности.
Целью данного анализа является предоставление сравнительных результатов, которые были получены в контролируемых исследованиях с использованием плацебо у больных с наиболее распространенными проявлениями сердечно-сосудистых заболеваний. К ним относятся: документированная хроническая ишемическая болезнь сердца (ИБС) (стабильная форма стенокардии напряжения, перенесенный инфаркт миокарда), систолическая форма нарушения функции левого желудочка (сниженная фракция его выброса, застойная сердечная недостаточность), артериальная гипертония (АГ). Этими формами проявления заболеваний сердечно-сосудистой системы представлено большинство случаев смерти вне стационаров. Поэтому только эффективное лечение данных патологий может снизить высокую летальность, которая сохраняется в нашей стране.
Большинство исследований с блокаторами β-адренорецепторов было выполнено с включением больных, перенесших инфаркт миокарда, и весьма малое количество – среди больных стабильной стенокардией. В определенной степени это обусловлено тем, что преимущественно проводились исследования по оценке эффективности аортокоронарного шунтирования, а затем – коронарной ангиопластики.
В обзорной статье M.J. Everly и соавт. [1] приведены опубликованные с января 1966 г. по октябрь 2002 г. результаты всех исследований, оценивавших эффективность β-блокаторов у больных, перенесших инфаркт миокарда. Полученные данные продемонстрировали наличие положительного действия этой группы препаратов, что проявилось уменьшением летальности на 19– 48% и частоты повторного инфаркта – на 28%. Из этих исследований самым большим было американское многоцентровое исследование ВНАТ, в которое спустя 5–21 день после перенесенного инфаркта миокарда были включены 3 837 больных, получавших пропранолол в дозе 60 или 80 мг 3 раза/сут. или плацебо. В течение в среднем 25 мес. наблюдения установлено, что общая летальность составила 7,2% в группе, получавшей β–блокатор, и 9,8 % – в группе плацебо, т.е. отмечено относительное снижение риска смерти на 26% (р<0,005), а внезапной смерти – на 28% (р<0,05). В дальнейшем дополнительный анализ показал, что среди больных с высоким риском смерти (383 чел.), получавших пропранолол, этот риск был меньше на 43% по сравнению с теми, кто принимал плацебо (р<0,01). Показатели летальности в группах больных низкого или промежуточного риска, получавших в течение 1 года β–блокатор или плацебо, существенно не отличались [2] .
В другом обзоре [3] было установлено, что β-блокаторы без вазодилатирующего действия сохраняют свою эффективность также и у больных старше 80 лет, в частности летальность на фоне терапии cреди них была на 32% меньше, чем у тех, кто не получал данных препаратов. Эти данные очень важны для сравнительной оценки пользы от терапии небивололом пожилых больных.
В двойном слепом рандомизированном исследовании SMT [4] было установлено, что желудочковые аритмии достоверно чаще, особенно в первые 6 мес., регистрировались в группе, получавшей плацебо. Наличие депрессии сегмента ST во время проведения исходной пробы с нагрузкой ассоциировалось с риском реинфаркта только в группе, получавшей плацебо. Доза метопролола в первые 3 дня составляла 50 мг 3 раза/сут., далее – 100 мг 2 раза/сут. Наблюдение в течение 3 лет после отмены β-блокатора продемонстрировало наличие двухкратного увеличения летальности в данной группе больных.
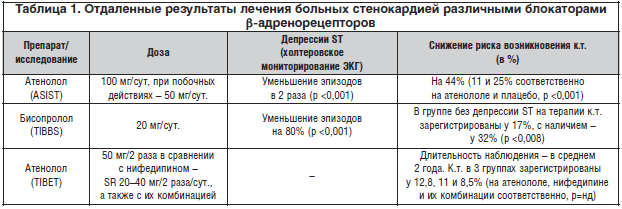
Среди больных, перенесших инфаркт миокарда и не подвергавшихся инвазивному вмешательству по реваскуляризации миокарда, в дальнейшем при обследовании примерно в 50% случаев выявляется стенокардия напряжения или безболевая ишемия миокарда. Поэтому положительные результаты, полученные среди всех больных, перенесших инфаркт миокарда, позволили сформулировать рекомендации по лечению также и тех, кто имеет стенокардию и не перенес инфаркта миокарда. Целесообразность такой рекомендации была подтверждена в сравнительно небольших исследованиях (ASIST, TIBBS, IMAGE, FEMINA, TIBET), которые были проведены в 1996–1999 гг. В этих исследованиях (табл. 1) было показано, что β-блокаторы в адекватных дозах позволяют в определенной степени контролировать возникновение преходящей ишемии миокарда, провоцируемой стрессом. В некоторых из них были также получены доказательства их положительного влияния на частоту возникновения комбинированной конечной точки (к.т.).
Изучали также эффективность комбинированной терапии, в частности в двойном слепом рандомизированном исследовании TIBВS [5] сравнили эффективность бисопролола в дозе 10 мг и 20 мг с нифедипином SR 20 мг и 40 мг 2 раза/сут. у больных с положительной пробой на нагрузке и имевших более двух эпизодов депрессии сегмента ST во время регистрации холтер- ЭКГ в течение 48 ч. На первых дозах препаратов антиишемический эффект бисопролола был достоверно выраженнее, чем у нифедипина, в отношении продолжительности эпизодов депрессии сегмента ST, которая уменьшилась в среднем с 99±10 до 32±5 мин./48 ч и с 101±9 до 73±8 мин. соответственно (р=0,0001). Удвоение дозы достоверно увеличило только эффект бисопролола. Частота ритма сердца на β-блокаторе снизилась на 14±1 уд./мин. (р <0,001) и не изменилась на терапии нифедипином. Количество эпизодов депрессии сегмента ST на терапии бисопрололом в дозе 20 мг уменьшилось на 80,5%, а на нифедипине – на 49% (р<0,0001). Конечные точки (смерть, инфаркт миокарда, госпитализация в связи с возникновением нестабильной стенокардии) среди больных на терапии бисопрололом в течение 1 года были зарегистрированы у 22%, а на терапии нифедипином – у 33%, различия достоверны (р=0,03). Конечные точки возникали почти в 2 раза чаще среди тех, у кого были депрессии сегмента ST после начала терапии (32%), по сравнению с не имевшими их (17,5%), различия достоверны (р=0,03). В группе больных, имевших более 6 эпизодов депрессии сегмента ST, по сравнению с теми, кто имел меньше 2 эпизодов, частота конечных точек была в 2,5 раза больше ( 32,5 и 13% соответственно, р<0,001).
Таким образом, терапия бисопрололом улучшила исходы у больных в течение 1 года. Маркером более плохого прогноза являются сохраняющиеся на терапии депрессии сегмента ST.
В контролируемом рандомизированном исследовании FEMINA [6] замена метопролола на терапию только фелодипином сопровождалась увеличением частоты сердечного ритма, двойного произведения и достоверным увеличением числа побочных реакций (р<0,01).
В двойном слепом рандомизированном исследовании IMAGE [7] с использованием теста с нагрузкой сравнили эффективность комбинированной терапии метопрололом и нифедипином с монотерапией спустя 6 и 10 нед. от начала терапии. В конце 6 нед. на приеме нифедипина-ретард в дозе 20 мг 2 раза/сут. продолжительность нагрузки до появления депрессии сегмента ST увеличилась в среднем на 43 с (р<0,01), а на терапии метопрололом в дозе 200 мг/сут. – достоверно возросла в большей степени (70 с). На их комбинации прирост продолжительности нагрузки увеличился до 107 с, в основном за счет тех больных, у которых монотерапия была малоэффективной. Эти данные подтвердили результаты наших исследований, выполненных в начале 80–х гг. прошлого века, в которых было показано, что комбинированная терапия препаратами из группы β-блокаторов и антагонистов кальция оказывает более выраженное антиишемическое действие. В механизме более выраженного антиангинального эффекта комбинации препаратов, вероятно, существенную роль играет уменьшение уровня артериального давления в покое и во время нагрузки, дальнейшее снижение потребности миокарда в кислороде, улучшение кровоснабжения в зоне, подвергающейся ишемии [8]. Кроме того, было также доказано с помощью повторных нагрузок, что для значительного повышения толерантности к нагрузке и предупреждения развития ишемии миокарда у больных стабильной стенокардией с депрессией сегмента ST на нагрузке требуется назначение индивидуальных доз β–блокатора. В частности, индивидуальная разовая доза пропранолола в среднем составила 80 мг. А т.к. продолжительность действия препарата не превышала 8 ч, то суточная доза при его приеме 3 раза в течение 24 ч достигала 240 мг. При сравнении эффекта пропранолола с атенололом средние их разовые дозы не отличались, но суточная доза была меньше на терапии тенормином (в среднем 186 мг и 258 мг соответственно), который оказывает антиишемическое действие в течение до 12 ч, что предполагает его прием больным не менее 2 раз/сут.
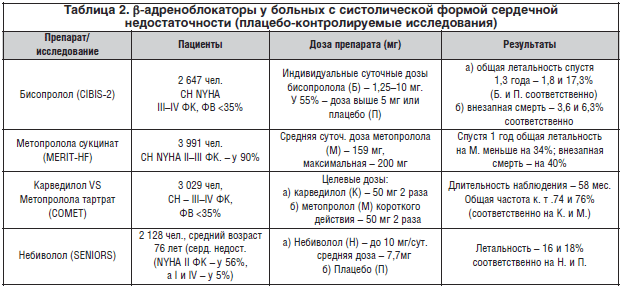
В отношении β-блокаторов в настоящее время также получены доказательства их положительного влияния на отдаленные исходы у больных с систолической формой сердечной недостаточности, хотя на начальных этапах их изучения у данной группы больных результаты были отрицательными (табл. 2). Последнее было обусловлено тем, что тактика их назначения была неправильной. В частности, терапию начинали без предварительного обеспечения стабилизации состояния больных и титрования дозы, начиная с очень малой. К сожалению, это и сегодня не всегда учитывается, что демонстрируется тем, что в принятых в нашей стране рекомендациях предлагается начинать терапию β-блокаторами даже у больных с острой декомпенсацией хронической застойной сердечной недостаточности до того, как будет обеспечена относительная компенсация.
В двойном слепом исследовании СIBIS-2 [9] доза бисопролола постепенно увеличивалась с 1,25 до 10 мг (при условии ее переносимости). Все больные получали вазодилататоры (преимущественно иАПФ), диуретики и при необходимости дигоксин. Длительность наблюдения в среднем составила 1,3 года. Исследование было досрочно остановлено, т.к. общая летальность была достоверно меньше на терапии бисопрололом (11,8 и 17,3% соответственно; р <0,0001). Препарат обеспечил положительные результаты терапии при сердечной недостаточности различной этиологии и, более того, при III, IV ФК в одинаковой степени. Почти половина больных (43%) получали бисопролол в дозе 10 мг, и лишь меньшая часть (32%) – в дозе менее 5 мг. Эти данные позволяют объяснить, почему в первом исследовании CIBIS, в котором использовались меньшие дозы бисопролола (1,25–5 мг), не было отмечено снижения летальности; меньшие дозы улучшили лишь функциональный класс больных, а для обеспечения блокады β-адренорецепторов у многих требуются более высокие дозы.
Исследование MERIT- HF [10] было также досрочно прекращено из-за достоверного снижения общей летальности на терапии метопрололом. Доза его титровалась, начиная с 12,5–25 мг/сут., и постепенно повышалась до максимальной – 200 мг 1 раз/сут. (при хорошей переносимости). Средняя суточная доза его составила 159 мг. По сравнению с плацебо общая летальность высокодостоверно снизилась в группе больных, получавших метопролол (11 и 7,2% в течение 1 года, р =0,0009).
В исследование CAPRICON [11] доза карведилола также титровалась, начиная с 6,25 мг, и повышалась до 25 мг 2 раза/сут. Кроме того, все больные получали ингибитор АПФ. Наблюдение продолжалось 1,3 года. В результате не было установлено значимых различий между группами больных в частоте конечных точек (35 и 37%), хотя общая смертность была несколько меньше на терапии карведилолом (12 и 15 соответственно). В качестве конечных точек были приняты общая летальность и частота госпитализации по кардиальным причинам. Это позволяет предположить, что наличие вазодилатирующего действия у препарата уменьшило его влияние на летальность больных. Но особенно важным для понимания роли вазодилатирующего действия является исследование COMET [12]. В группе больных, получавших оптимальную дозу карведилола (25 мг 2 раза/сут.), общая летальность составила 34%, а среди тех, кто получал метопролол короткого действия в малых дозах (25–50 мг только 2 раза/сут.), оказалась умеренно выше – 40%. Оптимальная доза этой формы метопролола должна составлять до 200 мг, разделенных на 3 приема в сутки. Частота комбинированной конечной точки была одинаковой (74 и 76 соответственно, р=0,1). Сравнительная оценка результатов демонстрирует, что оптимальное лечение карведилолом весьма умеренно превышает эффективность метопролола, использованного в недостаточной дозировке. C практической точки зрения полученные результаты не свидетельствуют в пользу карведилола. Вероятно, это можно объяснить тем, что препарат кроме свойств β-блокатора обладает также свойством блокировать α-адренорецепторы. Этот эффект присущ празозину, который в плацебо-контролируемом исследовании DIG оказал отрицательное влияние на выживаемость больных с сердечной недостаточностью, из-за чего в настоящее время он не рекомендован для лечения больных с данной патологией. Практические наблюдения также свидетельствуют, что пульсурежающее действие карведилола меньше, чем у бисопролола и метопролола при их использовании в целевых дозах.
Эффективность небиволола, обладающего также вазодилатирующим действием, изучалась у больных старше 70 лет с хронической сердечной недостаточностью преимущественно II ФК (56 %) или III ФК (39%), а IV ФК имели лишь 2% больных. Огромное число больных выбыло из исследования (35 и 36% соответственно). Общая летальность в течение 21 мес. составила 16 и 18% (на препарате или плацебо, р=0,2). Эти данные указывают на наличие весьма сомнительной эффективности небиволола у больных с сердечной недостаточностью [13].
Таким образом, имеющиеся в настоящее время данные, полученные в проспективных рандомизированных и контролируемых исследованиях, являются доказательством пользы терапии кардиоселективными β–блокаторами, не имеющими вазодилатирующего действия, что позволило включить их в рекомендации по лечению больных с кардиоваскулярными заболеваниями. В принятых в последние годы руководствах были только уточнены некоторые положения о степени обоснованности применения этой группы препаратов среди кардиологических больных. В частности, в Британском руководстве от 2011 г. по лечению больных ИБС (стенокардией) β-блокаторы рекомендуется назначать больным, которые отнoсятся к группе повышенного риска возникновения сердечно-сосудистых событий независимо от наличия или отсутствия систолической дисфункции левого желудочка [14].
В американском руководстве β-блокаторы рекомендованы как препараты, имеющие доказательства положительного влияния на летальность (кл. 1А) у больных ИБС, включая перенесших инфаркт миокарда, со сниженной фракцией выброса (≤40%), с сердечной недостаточностью [15]. У больных, не имеющих нарушения сократительной функции левого желудочка, в т.ч. перенесших инфаркт миокарда, терапия β-блокатором должна продолжаться не менее 3 лет (доказательства класса 1В). Более длительное их применение у больных, перенесших инфаркт миокарда и не имеющих сниженной фракции выброса, отнесено к доказательствам класса IIА. Доказательства пользы от их применения класса IIв имеются у больных хронической ИБС и другими сосудистыми заболеваниями.
Неожиданно в октябре 2012 г. в журнале JAMA [16] были опубликованы результаты анализа наблюдений за больными, включенными в REACH регистр (Reduction of Atherothrombosis for Continued Heart). Это нерандомизированное и неконтролируемое исследование, база данных, из которой была взята информация о 44 708 больных с различными заболеваниями, отвечавших избранным критериям отбора. Из них 14 043 пациента перенесли инфаркт миокарда, 12 012 больных имели документированную ИБС и 18 653 чел. были с факторами риска ИБС. Результаты длительного наблюдения за этими больными были получены в срок до апреля 2009 г. Первичной конечной точкой наблюдения был комбинированный показатель, включавший случаи смерти от кардиоваскулярных заболеваний, а также случаи нефатального инфаркта миокарда и инсульта. Вторичная конечная точка объединяла первичную со случаями госпитализации в связи с развитием заболеваний, обусловленных атеротромбозом, а также включала больных с реваскуляризационными вмешательствами на коронарных артериях. Средний срок наблюдения составил 44 мес. Из 44 708 больных почти половина (21 860 чел.) были избраны с помощью метода определения двойников (Score – matched). Такого рода исследования характеризуются малой степенью доказательности. Сравнение отдаленных результатов среди «меченых двойников» выявило увеличение конечных точек на терапии β–блокаторами среди больных ИБС и лиц с факторами риска ее развития. Только у больных после инфаркта миокарда в течение первого года наблюдения отмечено уменьшение количества вторичной конечной точки. В дополнительном анализе результатов исследования [17] обращается внимание на то, что почти у половины больных (44%) частота ритма сердца была более 70 уд./мин. Это указывает на то, что у данных больных не обеспечивалось эффективное лечение β-блокаторами. В заключение авторы отметили, что среди больных, включенных в международный REACH регистр, прием (но не адекватное и контролируемое лечение) в течение 44 мес. β-адреноблокатора не ассоциировался с более низкой частотой кардиоваскулярных конечных точек.
В связи с данной публикацией следует обратить внимание на то, что в Американском исследовании с β–блокаторами (BHAT), где была установлена польза при их применении у больных, перенесших инфаркт миокарда, в 1993 г. при дополнительном анализе результатов было установлено, что положительное влияние на отдаленные исходы получено в основном только в подгруппе больных, имевших высокий риск плохого исхода. В подгруппах умеренного или низкого риска терапия β-блокаторами не ассоциировалась с уменьшением летальности. Этот анализ полностью подтвердил результаты нашего проспективного рандомизированного и контролируемого исследования с пропранололом, которое было выполнено в 1982 г. и включало только больных с высоким риском внезапной смерти [18].
Значение публикации S. Bangalore и соавт. [16] в том, что в ней отмечена важность разделения больных ИБС на группы риска и что в соответствии с этим должен осуществляться выбор метода лечения, имеющего доказательства снижения риска общей летальности за счет уменьшения летальности от кардиоваскулярных заболеваний. Кроме того, данная публикация должна послужить важным стимулом к тому, чтобы при организации исследований выделять группы с различной величиной риска фатального исхода [19]. Такой подход позволит повысить качество полученных результатов, даже при включении в исследования меньшего количества больных, подобно нашему исследованию с пропранололом у больных после инфаркта миокарда. Важным является также вопрос о длительности лечения больных с помощью β-блокаторов. Ответ на него очевиден в случае наличия у больного ишемии миокарда или стабильно существующих нарушений (АГ, аритмия), которые требуют проведения терапии в течение всей жизни больного, включая также использование β-блокаторов. Именно β-блокаторы в отличие от ивабрадина, угнетающего только функцию синусового узла, обеспечивают не только урежение частоты ритма сердца, но и оказывают положительное влияние на многие патофизиологические нарушения, имеющиеся у этих больных. Поэтому у больных ИБС, относящихся к группе высокого риска смерти, терапия β-блокаторами должна проводиться пожизненно. Внезапное прекращение их приема, как это было установлено давно, приводит к ухудшению состояния больных (учащению приступов стенокардии, повышению артериального давления, увеличению количества желудочковых экстрасистол) и к увеличению также риска внезапной смерти [20]. В связи с этим актуальной является проблема доступности такой терапии, что особенно важно для больных в нашей стране. В определенной степени эта проблема решается при назначении качественного дженерика, стоимость которого в 2–3 раза меньше. Одним из таких препаратов является Бипрол, который был изучен Ю.Б. Белоусовым и соавт. В их исследовании было доказано, что Бипрол идентичен по терапевтической эффективности оригинальному бисопрололу.
β-адреноблокаторы не потеряли своего значения и у больных АГ. В последние годы уточнены показания для их назначения в данной группе больных. В частности, Национальным институтом здоровья (NICE) совместно с Британским обществом по изучению артериальной гипертонии в 2006 г. были подготовлены новые клинические рекомендации [21]. Основным изменением, по сравнению с предыдущими вариантами, является то, что β-блокаторы рекомендованы в качестве первой линии в лечении АГ, ассоциированной с другими заболеваниями (ИБС, ХСН). Такое отношение к применению β–блокаторов для лечения всех больных АГ основывается на результатах исследования ASCOT и нескольких метаанализов [22]. Например, в исследовании ASCOT было установлено, что современная антигипертензивная стратегия, основанная на использовании антагонистов кальция и ингибиторов АПФ, достоверно снижает общую и сердечно-сосудистую смертность, а также другие сердечно-сосудистые осложнения по сравнению с атенололом в сочетании с диуретиком (бендрофлуметиазидом). В этом исследовании терапия агонистом имидазолиновых рецепторов была досрочно прекращена.
Основанием для пересмотра существовавших руководств по лечению больных АГ явились накопившиеся к концу XX в. данные, свидетельствовавшие о наличии преимуществ для больного при использовании для лечения АГ антагонистов кальция и ингибиторов АПФ. В частности, полученные в проведенных исследованиях результаты свидетельствовали о более значимом снижении у больных риска инсульта на терапии антагонистами кальция и снижении риска возникновения инфаркта миокарда – на терапии ингибиторами АПФ [22]. Такие результаты можно объяснить тем, что антагонисты кальция более эффективно снижают уровень артериального давления и не оказывают отрицательного влияния на другие факторы риска развития атеросклероза, а ингибиторы АПФ улучшают функцию эндотелия, не вызывают гипокалиемии (в сравнении с диуретиками) и не оказывают также отрицательного влияния на липидный и углеводный обмен.
Все имеющиеся сегодня данные свидетельствуют, что использование диуретиков для лечения больных АГ в качестве препаратов первого выбора при сравнении не только с ингибиторами АПФ, но и с β-адреноблокаторами,оказывается менее эффективным, особенно в отношении возникновения ИБС и внезапной кардиальной смерти, риск которых может увеличиться на терапии диуретиком. Поэтому следует считать, что диуретики должны стать препаратами выбора лишь на последней ступени комбинированной терапии больных АГ [23]. Возможно, исключение составляют больные негроидной расы, но и в этих случаях предпочтение следует отдать антагонистам кальция.
Исходя из имеющихся в настоящее время данных, можно предложить следующий алгоритм выбора терапии больного АГ, который представлен в таблице 3.
Таким образом, представленные результаты проведенных контролируемых исследований позволяют прийти к заключению, что наибольшими доказательствами положительного влияния на выживаемость больных ИБС, сердечной недостаточностью обладают бисопролол и метопролол в случае использования их в целевых дозах (до 10–20 мг бисопролол и до 200 мг – метопролол). Карведилол в целевой дозе (50 мг) по эффективности несколько превышает эффект неоптимальной дозы метопролола короткого действия (до 100 мг), что следует учитывать врачу при выборе терапии. Небиволол не получил доказательств положительного влияния на выживаемость больных ИБС, а у больных с сердечной недостаточностью его влияние на летальность сопоставимо с эффектом плацебо. Кроме перечисленных показаний β-блокаторы широко используются для лечения некоторых нарушений сердечного ритма, мигрени, АГ у беременных.

Литература
1. Everly M.J., Heaton P.C., Cluxton R.J. Beta-blocker underuse in secondary prevention of myocardial infarction // Ann. Pharmacother. 2004. Vol. 38(2). P. 286–293.
2. Viscoli C.M., Horwitz R.I., Singer B.H. Beta-blockers after myocardial infarction: influenceof first-year clinical course on long- term effectiveness (BHAТ) // Ann. Intern. Med. 1993. Vol. 118. P. 89–105.
3. Aronow W.S. Prevalence of use of beta-blockers and of calcium channel blockers in older patients with prior myocardial infarction at the time of admission to a nursing home // J..Am. Geriatr. Soc. 1996. Vol. 44. P. 1075–1077.
4. Olsson G., Rehngist N., Evaluation of antiarrhythmic effect of metoprolol treatment after myocardial infarction: relationship between treatment responses and survival during a 3-year follow-up (SMT) // Eur. Heart J. 1986. Vol. 7. P. 312–319.
5. Weber F., Schneider H., von Armin T. et al. Total ischemie Burden Bisoprolol study (TIBBS) // Eur. Heart J. 1999. Vol. 20. P. 38–50.
6. Dunselman P., Liem A.H., Verdel G. et al. Felodipine ER and Metoprolol CR in Anginа (FEMINA) // Eur. Heart J. 1997. Vol. 18. P. 1755– 1764.
7. Savonitto A., Ardissino D., Egstrup K. et al. Combination therapy with metoprolol and nifedipine vs monotherapy in patients with stable angina pectoris. Results of the international Multicenter Angina Exercisе (IMAGE) // Study J. Am. Coll. Cardiol. 1996. Vol. 27. P. 311–316.
8. Mazur N.A. Basic clinical pharmacology and pharmacotherapy in cardiology. M. Meditsina, 1988, 302 p. Russian (Мазур Н.А. Основы клинической фармакологии и фармакотерапии в кардиологии. М.: Медицина, 1988, 302 с.).
9. CIBIS-II Investigators Committees. The Cardiac Insufficiency Bisoprolol Study II (CIBIS-II): a randomised trial // Lancet. 1999. Vol. 353. P. 9–13.
10. Hjalmarson A., Goldstein S., Fagerberg B. et al. Effects of controlled – release metoprolol on total mortality, hospitalisation, and well – being in patients with heart failure. The metoprolol CR/XL Randomised international Trial in Congestive heart failure (MERIT–HF) // JAMA. 2000. Vol. 283. P. 1295–1302.
11. Dargie H.J., Colucei W.S., Ford I. et al. Effect of carvedilol on outcome after myocardial infarction in patients with left-ventricular dysfunction: the CAPRICORN randomised trial // Lancet. 2001. Vol. 357. P. 1385–1390.
12. Poole-Wilson Ph.A., Swedbery K., Cleland J G.F. et al. Comparison of carvedilol and metoprolol European trial (COMET): randomised controlled trial // Lancet. 2003. Vol. 362 (9377). P. 7–3 .
13. Flather M.D., Shibata M.C., Coats A.J et al. SENIORS Investigators. Randomized trial to determine the effect of nebivolol on mortality аnd cardiovascular hospital admission in elderly patients with heart failure (SENIORS) // Eur. Heart J. 2005. Vol. 26. P. 215–225.
14. National Clinical Guidelines Centre, Stable angina: FULL guideline (July 2011). 468 p.
15. AHA/ACCF Secondary Prevention and Risk reduction Therapy for patients with Coronary and other Atherosclerotic Vascular Disease // J. Am. Coll. Cardiol. 2012. Vol. 60. e44 –164.
16. Bangalore Sripal. Beta-Blocker Use Not Associated With Lower Risk of Cardiovascular Events // JAMA. 2012.
17. Steg Ph.G., Ferrari R., Ford I. et al. for the CLARIFY Investigators Heart Rate and Use of Beta-Blockers in Stable Outpatients with Coronary Artery Disease. PLoS One. 2012; 7(5): e36284. Published online 2012 May 3. doi: 10.1371/journal.pone.0036284.
18. Mazur N.A., Ostrovskaya T.P., Dokuchaeva E.A. et al. Long-term propranolol (obzidan) treatment patients with ischemic heart desease with high risk of sudden death // Cardiol. 1982. Vol. 8. P. 64–68. Russian (Мазур Н.А., Островская Т.П., Докучаева Е.А. и др. Длительное лечение обзиданом больных ИБС с высоким риском внезапной смерти // Кардиология. 1982. № 8. С. 64–68).
19. Mazur N.A. Sudden death patients with ischemic heart desease. M. Meditsina, 1985.189 p. Russian (Мазур Н.А. Внезапная смерть у больных ишемической болезнью сердца. М.: Медицина, 1985. 189 с.).
20. Marimoto S., Shimisu K., Yamada K. et al. Can beta-blockers therapy be withdrawn from patients with dilated cardiomyopathy? // Am. Heart J. 1999. Vol. 138. P. 456–459.
21. www. nice. org. uk / CGO 34 NICE guid-line.
22. Staessen J.A., Ji-Guan Wang, Tija L. Cardiiovascular protection and blood pressure reduction: a meta-analysis // Lancet. 2001. Vol. 358. P. 1305–1313.
23. Mazur N.A. Practical Cardiology. M. Medpractica, 2012. 678 p. Russian (Мазур Н.А. Практическая кардиология, 2012. 678 с.).












