Целью нашего исследования стало выявление особенностей адаптации к жаре больных ишемической болезнью сердца (ИБС) и больных с умеренным/высоким риском ССО без ИБС.
Материалы и методы
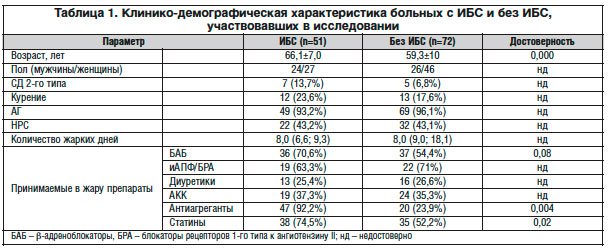
В исследование были включены 123 больных, обратившихся в научно-диспансерный отдел Института клинической кардиологии им. А.Л. Мясникова в мае 2012 г. У 51 больного была ИБС, а у 72 ИБС не было, но имелся умеренный и высокий риск ССО по шкале SCORE [4]. Их клинико-демографическая характеристика представлена в таблице 1. Как и следовало ожидать, больные ИБС были старше, чаще получали терапию статинами и дезагрегантами. В то же время группы были сопоставимы по полу, уровню АД, доле больных СД, артериальной гипертензией (АГ), нарушениями ритма сердца (НРС), курящих и некурящих, количеству дней, проведенных под влиянием жары. Больные обеих групп одинаково часто во время жары получали терапию ингибиторами ангиотензинпревращающего фермента (иАПФ), антагонистами кальциевых каналов (АКК), диуретиками. В ходе исследования терапия не менялась. Следует отметить, что цифры, приведенные в таблице 1, отражают истинную картину приема препаратов. Так, например, статины назначали на исходном визите 100% больных ИБС, реально же во время жары их принимали только 74,5% пациентов.
Всем больным проводилось комплексное клинико-инструментальное обследование, включающее сбор анамнеза, ЭКГ в 12 отведениях, измерение «офисного» АД, частоты сердечных сокращений (ЧСС), определение концентрации калия (К+) и натрия (Nа+), сфигмографию (определение скорости пульсовой волны (СПВ)). Больным также предлагался для заполнения ряд опросников:
1. Визуально-аналоговая шкала (ВАШ): оценивалось качество жизни как по состоянию на приеме, так и (ретроспективно) на период аномальной жары.
2. Опросник, специально разработанный нами для этого исследования. Вопросы касались местонахождения больного во время волны жары, его самочувствия, продолжительности рабочего дня, количества гипертонических кризов, вызовов скорой медицинской помощи (СМП), обращений к врачу, характера терапии и т. д.
Для оценки уровня окислительного стресса определялось содержание окисленных липопротеинов низкой плотности (окЛПНП) в плазме крови с использованием иммуноферментного набора Mercodia Oxidized LDL ELISA (Швеция). Содержание продуктов, реагирующих с 2-тиобарбитуровой кислотой (преимущественно малоновый диальдегид (МДА)), определялось в плазме крови с помощью диагностических тест-наборов фирмы «АГАТ» (Россия). Активность супероксиддисмутазы (СОД) в эритроцитах определяли, используя диагностические тест-наборы RANSOD фирмы RANDOX (США). На основании результатов анализов рассчитывали отношение МДА/СОД, характеризующее «окислительный потенциал» крови (для расчетов использовали показатели содержания МДА в нмолл/л и активности СОД в ед/гHb).
Дизайн исследования
Исходная точка – отбор пациентов (исходная точка, май 2012 г.).
1 визит. В первой декаде июля 2012 г. была зафиксирована дневная температура воздуха 29°С и выше. Такая температура рассматривается как «пороговая» для жителей зоны умеренного климата [5]. За период с 9 июля по 9 августа 2012 г. температура, равная и превышающая «пороговую», наблюдалась в течение 8 дней, причем зафиксирована была одна волна жары (3 дня) с 30.06.12 по 1.08.12 г. с максимальной температурой 32°С (http://meteoinfo.ru). В этот период (период жары) проводились активный вызов участников исследования и их повторное обследование.
2 визит. Заключительное обследование в сентябре – октябре 2012 г.
Статистический анализ. При анализе достоверности различий средних величин между группами, при условии нормального распределения, рассчитывали значения t-критерия Стьюдента для независимых выборок в предположении равенства дисперсий. Сравнение значений с распределением признаков, отличным от нормального, проводилось с помощью критерия Мак–Уитни. Различия считали статистически достоверными при вероятности абсолютно случайного их характера, не превышающей 5% (p<0,05). Сравнение распределения качественных признаков проводили с использованием точного критерия Фишера. Непрерывные переменные, имеющие нормальное распределение, представлялись как М±σ, где М – среднее и σ – стандартное отклонения. Непрерывные переменные, распределение которых отличалось от нормального, представлялись медианой и 95% доверительным интервалом Mе (–95% ДИ; 95% ДИ). Для оценки динамики показателей проводился однофакторный анализ динамики в контрольных и основных группах. Для критерия Даннета представлены p-значения.
Результаты исследования
Метеоусловия в период исследования. В мае 2012 г. среднемесячная температура составляла 15,1°С (отклонение от нормы +1,9°С). В период 1-го визита среднемесячная температура была равна 20,9°С в июле (отклонение от нормы +1,7°С) и 17,7°С – в августе (отклонение от нормы +0,7°С). «Пороговой» среднесуточной температурой в Московском регионе в это время принято считать среднесуточную температуру +22,7°С, за максимальную температуру принимают 29°С. Число дней со среднесуточной температурой > +22,7°С составило 11 в июле и 2 – в августе. Такая температура держалась 4 дня подряд с 8.07.12 по 12.07.12 г., а затем 3 дня подряд в период 30.07.12–1.08.12. Максимальная температура (+29°С и выше) наблюдалась в течение 8 дней, максимальная температура +32,5°С была зафиксирована 7 августа (+7,1°С от нормы).
В сентябре 2012 г. среднемесячная температура была 12,9°С при норме 11,3°С.
ССО во время жары и в период после ее окончания
(с середины августа по сентябрь 2012 г.)
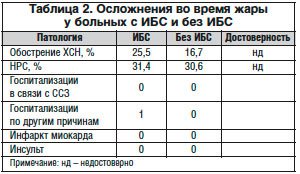
За весь период наблюдения у участников исследования не было ни одного случая инфаркта миокарда или острого нарушения мозгового кровообращения. На пике жары был госпитализирован один больной ИБС по причинам некардиального характера. Еще 4 госпитализации в той же группе зафиксированы в период после окончания жары (2 госпитализации связаны с ССЗ, 2 – по некардиальным причинам) (табл. 2). 25,5% больных ИБС и 16,7% без ИБС отметили нарастание одышки во время жары, расцениваемое как нарастание сердечной недостаточности 31,4% больных ИБС и 30,6% без ИБС отмечали появление или усугубление перебоев в работе сердца и сердцебиений во время жары (НРС).
Качество жизни и изменение гемодинамических
и электролитных показателей во время жары
и после ее окончания
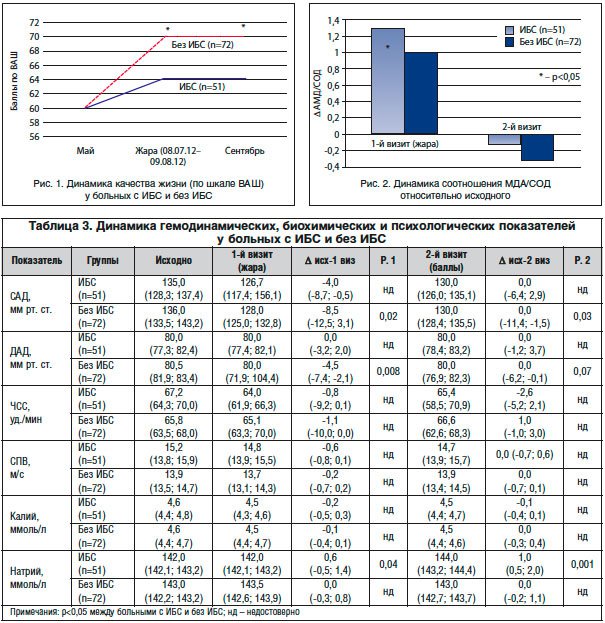
Как видно из таблицы 3, реакция на летнюю жару у больных с ИБС и без ИБС существенно отличалась. У больных без ИБС отмечалось снижение систолического АД на 8,5 мм рт. ст. и диастолического – на 4,5 мм рт. ст. во время жары и систолического АД на 2-м визите. У них же отмечалось улучшение качества жизни, выражающееся в увеличении количества баллов по ВАШ с 60,1 (56,0; 66,1) до 70,0 (64,1; 71,3) во время жары, сохранявшееся и после ее окончания, на 2-м визите (рис. 1). Электролитный баланс крови у этих больных существенно не изменялся.
У больных ИБС отсутствовала динамика изучаемых гемодинамических показателей, а также качества жизни, однако отмечалось повышение концентрации натрия в жару на 0,6 ммоль/л (р=0,04) и на 2-м визите – на 1,0 ммоль/л от исходного. У больных ИБС прослеживалась тесная положительная корреляция между приростом концентрации натрия в летний период и обострением хронической сердечной недостаточности (ХСН) в жару (r=0,453, p=0,000). У больных без ИБС такая связь не наблюдалась. Только у больных ИБС динамика качества жизни отрицательно коррелировала с количеством дней, проведенных под действием жары (r= -0,311, p=0,045).
Состояние окислительного стресса во время жары и после ее окончания
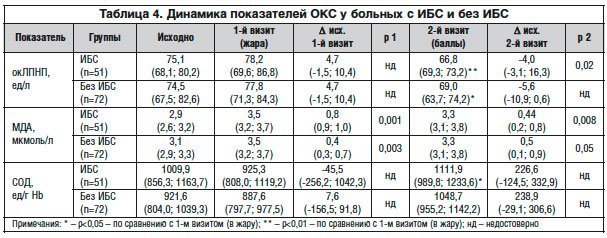
Данные, отражающие влияние повышенной температуры на параметры окислительного стресса, представлены в таблице 4. На пике летней жары у обследуемых пациентов как с ИБС, так и без ИБС возрастал уровень продуктов свободнорадикального окисления в плазме крови (∆МДА +0,8 мкмоль/л у больных ИБС и +0,4 мкмоль/л у больных без ИБС, разница между группами недостоверна), тогда как активность антиоксидантного фермента – эритроцитарной СОД – практически не изменяется. В период осеннего понижения температуры (2-й визит) содержание МДА оставалось повышенным в обеих группах, однако отмечается прирост активности СОД, недостоверный в группе без ИБС, и достоверный у больных ИБС по сравнению с показателями во время жары. В то же время отмечено достоверное снижение уровня окЛПНП в группе больных ИБС (∆окЛПНП -4,0 ед/л).
Динамика отношения МДА/СОД, характеризующего «окислительный потенциал» крови, была однонаправленной. Однако если у больных ИБС оно достоверно возрастало в период летней жары и снижалось до исходных значений в период осеннего понижения температуры, то у больных без ИБС эти изменения были статистически незначимы (рис. 2).
Таким образом, летняя жара, даже не выходящая за границы климатической нормы, вызывает у больных ИБС такие признаки напряжения адаптации, как повышение уровня натрия плазмы и окислительный стресс, качество жизни коррелирует с количеством дней, проведенных под действием жары. В то же время у больных без ИБС отмечаются улучшение качества жизни и снижение уровня АД.
Обсуждение
Тепловая адаптация обусловлена совокупностью специфических физиологических изменений. Первой реакцией на наступление жары является активация симпатико-адреналовой системы: увеличиваются ЧСС и минутный выброс крови, возможно повышение АД. По мере адаптации в условиях жаркого климата отклонения в нейроэндокринной регуляции выравниваются, терморегуляционные процессы становятся более стабильными и соответствующими интенсивности термического воздействия. Обмен веществ устанавливается на нормальном уровне, то же самое относится к другим физиологическим функциям. АД обычно устанавливается на более низких величинах нормального уровня, пульс при физической работе снижается на 20–30 уд./мин, а температура тела – на 0,5–1°С [6].
Многочисленные исследования, проведенные на здоровых добровольцах и спортсменах в условиях пустынного климата, показали, что в ходе адаптации к жаре происходит увеличение концентрации солей, прежде всего натрия, в крови и тканях, в то время как изменения объема циркулирующей крови незначительны [7]. Это происходит вследствие увеличения реабсорбции натрия в потовых железах и почечных канальцах под действием альдостерона и антидиуретического гормона, а также симпатического возбуждения, которое вызывает сужение почечных сосудов и, как следствие, уменьшение почечного кровотока и скорости клубочковой фильтрации. В итоге выделительная функция почек снижается. В результате акклиматизированный человек теряет натрий с потом и мочой в несколько раз меньше, чем неакклиматизированный. Причем эти защитные механизмы включаются довольно быстро. Параллельно происходит увеличение содержания катехоламинов в плазме и активности ренина и ангиотензина II [8]. Повышение секреции ангиотензина II приводит к снижению выделения почками натрия как непосредственно, так и путем стимуляции секреции альдостерона. Результатом вышеописанных изменений становится повышение осмолярности крови [9]. Повышенная осмолярность, в свою очередь, вызывает сильное ощущение жажды, которая является механизмом, направленным на компенсацию потерь жидкостей организмом.
У больных ССЗ изменения гемодинамических, биохимических и электролитных параметров крови соответствуют адаптивным реакциям, описанным у здоровых людей: снижение АД, повышение концентрации натрия плазмы, уменьшение клубочковой фильтрации. Однако летняя жара, даже не выходящая за границы климатической нормы, ассоциируется с увеличением числа ССО у части больных ССЗ [8].
В нашем исследовании больные ССЗ без ИБС хорошо перенесли жару, более того, их самочувствие улучшилось. В этой группе не было ни одной госпитализации за весь летний период. Изменения гемодинамических параметров носили положительный характер и соответствовали адаптивным реакциям, описанным у здоровых людей. Сохранение более низкого уровня АД в сентябре, бесспорно, является положительным моментом для больных АГ, которые составляют 96,1% всей группы.
У больных ИБС уже при «обычной», характерной для данной местности, летней жаре появляются признаки напряжения адаптивных механизмов, что свидетельствует об их несовершенстве. Динамика концентрации натрия, присущая нормальной адаптивной реакции, не всегда «выгодна» больным ССЗ. С одной стороны, как было сказано, поддерживается постоянство водного баланса организма. С другой, активация ренин-альдостерон-ангиотензиновой системы может вести к нарастанию явлений сердечной недостаточности, что и отмечается у части пациентов. Кроме того, в литературе есть данные об ассоциации гипернатриемии с увеличением риска тромбозов [10]. Это объясняет корреляцию, казалось бы, адаптивного повышения уровня натрия с количеством и частотой обострения ХСН у больных ИБС в нашем исследовании. Летняя жара, даже остающаяся в пределах климатической нормы, ведет к возникновению у пациентов с ССЗ окислительного стресса, более выраженного у больных ИБС. Пациенты с более быстрым «включением» защитной антиоксидантной системы клинически лучше переносили жару: у них реже возникали НРС, реже появлялись или усугублялись явления ХСН, что позволяет предполагать ассоциацию высокой активности антиоксидантной системы с лучшей адаптацией больных ССЗ к жаре [11].
Естественным ограничением нашего исследования стал более пожилой возраст больных ИБС. Пожилые люди во время волн жары подвержены более высокому риску, поскольку с возрастом ухудшаются функции ряда важных респираторных защитных механизмов, снижается васкуляризация кожного покрова, ухудшается перераспределение крови к коже, необходимое для эффективной теплоотдачи во время жары, уменьшаются плотность потовых желез, их ответная реакция, объем вырабатываемого пота. Указанные возрастные изменения в сочетании с ИБС уменьшают адаптационные резервы организма. Однако, по данным эпидемиологических исследований, риск смерти, ассоциированной с жарой, максимален для лиц старше 80 лет [3], средний возраст наших пациентов с ИБС был 66 лет, самому пожилому участнику исследования было 75 лет. Не отмечено статистически значимых корреляций между возрастом и изучаемыми параметрами. Таким образом, главную роль в снижении адаптационных способностей играло, по-видимому, все же наличие ИБС, а не возраст.
Выводы:
1. У больных без ИБС летняя жара (в пределах климатической нормы) способствует снижению АД и ассоциируется с улучшением качества жизни.
2. У больных ИБС воздействие жары вызывает повышение натриемии и смещение баланса МДА/СОД в сторону окисления, качество жизни коррелирует с количеством дней, проведенных под действием жары.
Литература
1. Climate change and communicable diseases in the EU Member States. Hand-book for national vulnerability, impact and adaptation assessments // European Centre for Diseases Prevention and Control. 2010. 42 p.
2. Планы действий по защите здоровья населения от воздействия аномальной жары. Руководство под редакцией F. Matthies, Gr. Bickler, N.C. Marn, S. Hales. Всемирная организация здравоохранения, 2011. 66 с.
3. Bouchama A., Dehbi M., Mohamed G. et al. Prognostic factors in heat wave-related deaths; a meta-analysis // Arch. Intern. Med. 2007. Vol. 167. P. 2170–2176.
4. Kalkstein L.S., Smoyer K.E. The impact of climate change on human health: Some international implications // Experiencia. 1993. Vol. 49. P. 469–479.
5. Ревич Б.А., Малеев В.В. Изменения климата и здоровье населения России: анализ ситуации и прогнозные оценки. М.: Ленанл, 2011. 208 с.
6. Умидова З.И. Физиология и патология сердечно-сосудистой систем в условиях жаркого климата. Ташкент: Госиздат УзСССР, 1949. 296 с.
7. Гора Е.П. Экология человека. М.: Дрофа, 2007. 145 с.
8. Lammintausta R., Syvalahti E., Pekkarinen A. The change in hormones reflecting sympathetic activity in the Finnish sauna // Ann. Clin. Res. 1976. Vol. 8. P. 266–271.
9. Агеев Ф.Т., Смирнова М.Д., Галанинский П.В. Оценка непосредственного и отсроченного воздействия аномально жаркого лета 2010 г. на течение сердечно-сосудистых заболеваний в амбулаторной практике // Терапевтический архив. 2012. № 8. С. 45–51.
10. Grant P.J., Tate G.M., Hughes J.R. et al. Does hypernatraemia promote thrombosis? // Thromb. Res. 1985. Vol.1; 40(3). P. 393–9.19
11. Смирнова М.Д., Коновалова Г.Г., Тихазе А.К., Агеев Ф.Т. и др. Влияние летней жары на показатели окислительного стресса у пациентов с сердечно-сосудистыми заболеваниями // Кардиологический вестник. 2013. № 1. С. 18–22.












