–ö —Ā–ĺ–∂–į–Ľ–Ķ–Ĺ–ł—é, –≤ —É—Ā–Ľ–ĺ–≤–ł—Ź—Ö –Ĺ–į—ą–Ķ–Ļ —Ā—ā—Ä–į–Ĺ—č –Ņ–ĺ–ī—ä–Ķ–ľ —É—Ä–ĺ–≤–Ĺ—Ź –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ķ–ľ–ĺ—Ā—ā–ł –≤ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —Ā—ā–Ķ–Ņ–Ķ–Ĺ–ł –ĺ–Ī—É—Ā–Ľ–ĺ–≤–Ľ–Ķ–Ĺ —Ā—ā—Ä–Ķ–ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ –ĺ–ľ–ĺ–Ľ–ĺ–∂–Ķ–Ĺ–ł–Ķ–ľ –ĺ–Ī–Ľ–ł—ā–Ķ—Ä–ł—Ä—É—é—Č–Ķ–≥–ĺ –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ–∑–į (–ě–ź) –ļ–į–ļ —Ā–į–ľ–ĺ–Ļ —á–į—Ā—ā–ĺ–Ļ —Ą–ĺ—Ä–ľ—č –ě–ó–ź–Ě–ö, –ľ–į–Ľ–ĺ–Ņ–ĺ–ī–≤–ł–∂–Ĺ—č–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ –∂–ł–∑–Ĺ–ł, –ļ—É—Ä–Ķ–Ĺ–ł–Ķ–ľ, –Ĺ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–į–Ľ—Ć–Ĺ—č–ľ –Ņ–ł—ā–į–Ĺ–ł–Ķ–ľ (—É–Ņ–ĺ—ā—Ä–Ķ–Ī–Ľ–Ķ–Ĺ–ł–Ķ –Ī–ĺ–Ľ—Ć—ą–ĺ–≥–ĺ –ļ–ĺ–Ľ–ł—á–Ķ—Ā—ā–≤–į —Ā–į—Ö–į—Ä–ĺ–≤ –ł —Ö–ĺ–Ľ–Ķ—Ā—ā–Ķ—Ä–ł–Ĺ—Ā–ĺ–ī–Ķ—Ä–∂–į—Č–ł—Ö –Ņ—Ä–ĺ–ī—É–ļ—ā–ĺ–≤), –į —ā–į–ļ–∂–Ķ –ĺ—ā—Ā—É—ā—Ā—ā–≤–ł–Ķ–ľ –ī–ĺ–Ľ–∂–Ĺ–ĺ–≥–ĺ –į–ľ–Ī—É–Ľ–į—ā–ĺ—Ä–Ĺ–ĺ-–Ņ–ĺ–Ľ–ł–ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ «–Ĺ–į–ī–∑–ĺ—Ä–į», –ī–ĺ—Ā—ā—É–Ņ–Ĺ–ĺ–Ļ —ą–ł—Ä–ĺ–ļ–ł–ľ —Ā–Ľ–ĺ—Ź–ľ –Ĺ–į—Ā–Ķ–Ľ–Ķ–Ĺ–ł—Ź –ļ–≤–į–Ľ–ł—Ą–ł—Ü–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ –į–Ĺ–≥–ł–ĺ—Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ņ–ĺ–ľ–ĺ—Č–ł. –Ď–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–ĺ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –≥–į–Ĺ–≥—Ä–Ķ–Ĺ–ĺ–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ (–Ě–ö) —Ä–į–Ĺ–Ķ–Ķ –Ĺ–Ķ –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –į–ī–Ķ–ļ–≤–į—ā–Ĺ–ĺ–≥–ĺ –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź –ł –Ĺ–Ķ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł—Ā—Ć —É —Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–≥–ĺ —Ö–ł—Ä—É—Ä–≥–į [5–7].
–Ě–Ķ–ľ–į–Ľ–ĺ–≤–į–∂–Ĺ—č–ľ —Ą–į–ļ—ā–ĺ—Ä–ĺ–ľ, —É—Ā—É–≥—É–Ī–Ľ—Ź—é—Č–ł–ľ –ł –Ī–Ķ–∑ —ā–ĺ–≥–ĺ —ā—Ź–∂–Ķ–Ľ–ĺ–Ķ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –ī–į–Ĺ–Ĺ–ĺ–Ļ –ļ–į—ā–Ķ–≥–ĺ—Ä–ł–ł (–ļ–į–ļ –Ņ—Ä–į–≤–ł–Ľ–ĺ, —ć—ā–ĺ –Ľ–ł—Ü–į –Ņ—Ä–Ķ–ļ–Ľ–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –≤–ĺ–∑—Ä–į—Ā—ā–į —Ā «–Ī—É–ļ–Ķ—ā–ĺ–ľ» —ā—Ź–∂–Ķ–Ľ—č—Ö —Ā–ĺ–ľ–į—ā–ł—á–Ķ—Ā–ļ–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł–Ļ, –≤ –Ņ–Ķ—Ä–≤—É—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć –ļ–į—Ä–ī–ł–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ą–ł–Ľ—Ź), —Ź–≤–Ľ—Ź—é—ā—Ā—Ź —á–į—Ā—ā—č–Ķ —Ä–į–Ĺ–Ķ–≤—č–Ķ –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł—Ź: –Ĺ–į–≥–Ĺ–ĺ–Ķ–Ĺ–ł—Ź (9–44,8%), –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ĺ–Ķ–ļ—Ä–ĺ–∑—č (3–18%) –ł –≥–Ķ–ľ–į—ā–ĺ–ľ—č –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –ļ—É–Ľ—Ć—ā–ł (5–15%) [4, 6, 9]. –ü–ĺ—á—ā–ł –≤—Ā–Ķ –ĺ–Ĺ–ł, —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤—É—Ź –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä–ĺ–≤–į–Ĺ–ł—é —Ā–ł—Ā—ā–Ķ–ľ–Ĺ–ĺ–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —Ä–Ķ–į–ļ—Ü–ł–ł –ĺ—Ä–≥–į–Ĺ–ł–∑–ľ–į –ł –Ņ–ĺ–Ľ–ł–ĺ—Ä–≥–į–Ĺ–Ĺ–ĺ–Ļ –Ĺ–Ķ–ī–ĺ—Ā—ā–į—ā–ĺ—á–Ĺ–ĺ—Ā—ā–ł (–ü–ě–Ě), –∑–į–ľ–Ķ—ā–Ĺ–ĺ —É—ā—Ź–∂–Ķ–Ľ—Ź—é—ā –ł –Ī–Ķ–∑ —ā–ĺ–≥–ĺ –Ĺ–Ķ–∑–į–≤–ł–ī–Ĺ–ĺ–Ķ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł–Ķ —Ā—ā—Ä–į–ī–į—é—Č–ł—Ö, —É—Ö—É–ī—ą–į—é—ā –ĺ–Ī—Č–ł–Ļ –Ņ—Ä–ĺ–≥–Ĺ–ĺ–∑; –ĺ–Ĺ–ł –∂–Ķ —Ź–≤–Ľ—Ź—é—ā—Ā—Ź –Ņ—Ä–ł—á–ł–Ĺ–ĺ–Ļ –Ņ–ĺ–≤—ā–ĺ—Ä–Ĺ—č—Ö –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤ (—ć—ā–į–Ņ–Ĺ—č—Ö –Ĺ–Ķ–ļ—Ä—ć–ļ—ā–ĺ–ľ–ł–Ļ, —Ä–Ķ–į–ľ–Ņ—É—ā–į—Ü–ł–Ļ –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–ł –≤ 12–35% –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–Ļ). –ü–ĺ-–Ņ—Ä–Ķ–∂–Ĺ–Ķ–ľ—É –≤—č—Ā–ĺ–ļ–į –ł –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–į—Ź –Ľ–Ķ—ā–į–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć – –ĺ—ā 18 –ī–ĺ 40% [8].
–ö–į–ļ –≤ –Ĺ–į—ą–Ķ–Ļ —Ā—ā—Ä–į–Ĺ–Ķ, —ā–į–ļ –ł –∑–į —Ä—É–Ī–Ķ–∂–ĺ–ľ –Ĺ–Ķ–ľ–į–Ľ–ĺ–≤–į–∂–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ–Ī–Ľ–Ķ–ľ–ĺ–Ļ –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ —É—Ö–ĺ–ī–į –∑–į –Ī–ĺ–Ľ—Ć–Ĺ—č–ľ–ł, –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā—ą–ł–ľ–ł –ź–Ě–ö –Ĺ–į —É—Ä–ĺ–≤–Ĺ–Ķ –Ī–Ķ–ī—Ä–į –ł–Ľ–ł –≤–Ķ—Ä—Ö–Ĺ–Ķ–Ļ —ā—Ä–Ķ—ā–ł –≥–ĺ–Ľ–Ķ–Ĺ–ł, —Ź–≤–Ľ—Ź–Ķ—ā—Ā—Ź —ā—Ź–∂–Ķ–Ľ—č–Ļ —Ą–į–Ĺ—ā–ĺ–ľ–Ĺ–ĺ-–Ī–ĺ–Ľ–Ķ–≤–ĺ–Ļ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ. –ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ –Ľ–ł—ā–Ķ—Ä–į—ā—É—Ä—č, –ĺ—ā –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ –≤ —Ä–į–Ĺ–Ĺ–Ķ–ľ –Ņ–Ķ—Ä–ł–ĺ–ī–Ķ —Ā—ā—Ä–į–ī–į—é—ā –ĺ—ā 30 –ī–ĺ 75% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ [9, 10]. –°–į–ľ–ł –Ņ–ĺ —Ā–Ķ–Ī–Ķ –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ—č–Ķ –Ī–ĺ–Ľ–Ķ–≤—č–Ķ –ĺ—Č—É—Č–Ķ–Ĺ–ł—Ź –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź—é—ā —ā–ĺ–Ľ—Ć–ļ–ĺ –≤–ł–ī–ł–ľ—É—é —á–į—Ā—ā—Ć «–į–Ļ—Ā–Ī–Ķ—Ä–≥–į», —Ź–≤–Ľ—Ź—Ź—Ā—Ć –Ņ–Ķ—Ä–≤–ĺ–Ņ—Ä–ł—á–ł–Ĺ–ĺ–Ļ —Ä–į–∑–≤–ł—ā–ł—Ź –Ņ–į—ā–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–ĺ–ļ–ĺ–ľ–Ņ–Ľ–Ķ–ļ—Ā–į. –ü–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł–Ļ –≤–ļ–Ľ—é—á–į–Ķ—ā –≤ —Ā–Ķ–Ī—Ź –Ľ–Ķ–≥–ĺ—á–Ĺ—É—é –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł—é, —Ā—ā–ĺ–Ļ–ļ—É—é –≥–ł–Ņ–Ķ—Ä–į–ļ—ā–ł–≤–į—Ü–ł—é —Ā–ł–ľ–Ņ–į—ā–ĺ–į–ī—Ä–Ķ–Ĺ–į–Ľ–ĺ–≤–ĺ–Ļ —Ā–ł—Ā—ā–Ķ–ľ—č, –ľ–Ĺ–ĺ–∂–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ—č–Ķ –ĺ—Ä–≥–į–Ĺ–ĺ—ā—Ä–ĺ–Ņ–Ĺ—č–Ķ —Ä–Ķ–į–ļ—Ü–ł–ł. –Ě–į —Ą–ĺ–Ĺ–Ķ –Ĺ–Ķ–į–ī–Ķ–ļ–≤–į—ā–Ĺ–ĺ –ļ—É–Ņ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –ě–ó–ź–Ě–ö, –≤ 100% –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–Ļ —Ā—ā—Ä–į–ī–į—é—Č–ł—Ö –ľ—É–Ľ—Ć—ā–ł—Ą–ĺ–ļ–į–Ľ—Ć–Ĺ—č–ľ –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ–∑–ĺ–ľ, –≤—č—Ā–ĺ–ļ–į –≤–Ķ—Ä–ĺ—Ź—ā–Ĺ–ĺ—Ā—ā—Ć —Ä–Ķ–∑–ļ–ĺ–≥–ĺ —É–≤–Ķ–Ľ–ł—á–Ķ–Ĺ–ł—Ź –Ņ–ĺ—ā—Ä–Ķ–Ī–Ĺ–ĺ—Ā—ā–ł –ľ–ł–ĺ–ļ–į—Ä–ī–į –ł –≥–ĺ–Ľ–ĺ–≤–Ĺ–ĺ–≥–ĺ –ľ–ĺ–∑–≥–į –≤ –ļ–ł—Ā–Ľ–ĺ—Ä–ĺ–ī–Ķ, —á—ā–ĺ —á—Ä–Ķ–≤–į—ā–ĺ, –≤ —Ā–≤–ĺ—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć, –ĺ–Ņ–į—Ā–Ĺ–ĺ—Ā—ā—Ć—é —Ä–į–∑–≤–ł—ā–ł—Ź –ĺ—Ā—ā—Ä—č—Ö —Ā–ĺ–Ī—č—ā–ł–Ļ –≤ –ļ–ĺ—Ä–ĺ–Ĺ–į—Ä–Ĺ–ĺ–ľ –ł –Ī—Ä–į—Ö–ł–ĺ—Ü–Ķ—Ą–į–Ľ—Ć–Ĺ–ĺ–ľ —Ā–ĺ—Ā—É–ī–ł—Ā—ā—č—Ö –Ī–į—Ā—Ā–Ķ–Ļ–Ĺ–į—Ö [1, 10].
–Ě–į IV –ļ–ĺ–Ĺ–≥—Ä–Ķ—Ā—Ā–Ķ –Ķ–≤—Ä–ĺ–Ņ–Ķ–Ļ—Ā–ļ–ł—Ö –į—Ā—Ā–ĺ—Ü–ł–į—Ü–ł–Ļ –Ņ–ĺ –ł–∑—É—á–Ķ–Ĺ–ł—é –Ī–ĺ–Ľ–ł (–ü—Ä–į–≥–į, —Ā–Ķ–Ĺ—ā—Ź–Ī—Ä—Ć 2003 –≥.) –Ī—č–Ľ–ĺ –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ–ĺ, —á—ā–ĺ –Ĺ–Ķ –ľ–Ķ–Ĺ–Ķ–Ķ 65% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā—ą–ł—Ö –Ņ–Ľ–į–Ĺ–ĺ–≤—č–Ķ –ź–Ě–ö, —Ā—ā—Ä–į–ī–į—é—ā –ĺ—ā —ā—Ź–∂–Ķ–Ľ–ĺ–Ļ –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –Ī–ĺ–Ľ–ł. –ü—É—ā–ł —Ä–Ķ—ą–Ķ–Ĺ–ł—Ź –ī–į–Ĺ–Ĺ–ĺ–Ļ –Ņ—Ä–ĺ–Ī–Ľ–Ķ–ľ—č, –Ņ–ĺ–ľ–ł–ľ–ĺ —Ā–ĺ–≤–Ķ—Ä—ą–Ķ–Ĺ—Ā—ā–≤–ĺ–≤–į–Ĺ–ł—Ź —ā–Ķ—Ö–Ĺ–ł–ļ–ł –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤–į –ł –≤–Ĺ–Ķ–ī—Ä–Ķ–Ĺ–ł—Ź –Ĺ–ĺ–≤—č—Ö —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ł—Ö —ā–Ķ—Ö–Ĺ–ĺ–Ľ–ĺ–≥–ł–Ļ, –≤–ł–ī—Ź—ā—Ā—Ź –≤ —Ā–ĺ–≤–Ķ—Ä—ą–Ķ–Ĺ—Ā—ā–≤–ĺ–≤–į–Ĺ–ł–ł –ľ–Ķ—ā–ĺ–ī–ł–ļ –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ –ľ–Ķ–ī–ł–ļ–į–ľ–Ķ–Ĺ—ā–ĺ–∑–Ĺ–ĺ–Ļ –į–Ĺ–į–Ľ—Ć–≥–Ķ–∑–ł–ł. –° —ć—ā–ĺ–Ļ —Ü–Ķ–Ľ—Ć—é –Ņ—Ä–ł–ľ–Ķ–Ĺ—Ź–Ķ—ā—Ā—Ź –į–Ĺ–į–Ľ—Ć–≥–Ķ—ā–ł–ļ –Ĺ–ĺ–≤–ĺ–≥–ĺ –Ņ–ĺ–ļ–ĺ–Ľ–Ķ–Ĺ–ł—Ź –ó–į–Ľ–ī–ł–į—Ä, –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź—é—Č–ł–Ļ —Ā–ĺ–Ī–ĺ–Ļ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł—é –≤ –ĺ–ī–Ĺ–ĺ–Ļ —ā–į–Ī–Ľ–Ķ—ā–ļ–Ķ –Ĺ–Ķ–≤—č—Ā–ĺ–ļ–ł—Ö –ī–ĺ–∑ –ĺ–Ņ–ł–ĺ–ł–ī–Ĺ–ĺ–≥–ĺ –į–Ĺ–į–Ľ—Ć–≥–Ķ—ā–ł–ļ–į —ā—Ä–į–ľ–į–ī–ĺ–Ľ–į (37,5 –ľ–≥) –ł —Ā–į–ľ–ĺ–≥–ĺ –Ī–Ķ–∑–ĺ–Ņ–į—Ā–Ĺ–ĺ–≥–ĺ –į–Ĺ–į–Ľ—Ć–≥–Ķ—ā–ł–ļ–į/–į–Ĺ—ā–ł–Ņ–ł—Ä–Ķ—ā–ł–ļ–į –Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į (325 –ľ–≥). –Ď–Ľ–į–≥–ĺ–ī–į—Ä—Ź —Ā–ł–Ĺ–Ķ—Ä–≥–ł—á–Ĺ–ĺ–ľ—É –ī–Ķ–Ļ—Ā—ā–≤–ł—é –ļ–ĺ–ľ–Ņ–ĺ–Ĺ–Ķ–Ĺ—ā–ĺ–≤ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –ī–ĺ—Ā—ā–ł–≥–į–Ķ—ā—Ā—Ź –ľ–Ĺ–ĺ–≥–ĺ–ļ—Ä–į—ā–Ĺ–ĺ–Ķ —É—Ā–ł–Ľ–Ķ–Ĺ–ł–Ķ –ĺ–Ī—Č–Ķ–≥–ĺ –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į—é—Č–Ķ–≥–ĺ –ī–Ķ–Ļ—Ā—ā–≤–ł—Ź [9–11].
–í 2-—Ö —Ä–į–Ĺ–ī–ĺ–ľ–ł–∑–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –ī–≤–ĺ–Ļ–Ĺ—č—Ö —Ā–Ľ–Ķ–Ņ—č—Ö –Ņ–Ľ–į—Ü–Ķ–Ī–ĺ-–ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ–ł—Ä—É–Ķ–ľ—č—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö –Ī—č–Ľ–į –ĺ—Ü–Ķ–Ĺ–Ķ–Ĺ–į —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć —Ą–ł–ļ—Ā–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —ā—Ä–į–ľ–į–ī–ĺ–Ľ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į 37,5/325 –ľ–≥ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł–Ľ–ł –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –Ī–ĺ–Ľ—Ć—é, –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā—ą–ł—Ö –ĺ—Ä—ā–ĺ–Ņ–Ķ–ī–ł—á–Ķ—Ā–ļ—É—é –ł–Ľ–ł –į–Ī–ī–ĺ–ľ–ł–Ĺ–į–Ľ—Ć–Ĺ—É—é –ĺ–Ņ–Ķ—Ä–į—Ü–ł—é [12, 13]. –í —ć—ā–ł –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –≤–ļ–Ľ—é—á–į–Ľ–ł—Ā—Ć –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č —Ā –Ī–ĺ–Ľ—Ć—é –Ī–ĺ–Ľ–Ķ–Ķ 4 –Ī–į–Ľ–Ľ–ĺ–≤ –Ņ–ĺ –≤–ł–∑—É–į–Ľ—Ć–Ĺ–ĺ-–į–Ĺ–į–Ľ–ĺ–≥–ĺ–≤–ĺ–Ļ —ą–ļ–į–Ľ–Ķ, –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā—ą–ł–Ķ –į—Ä—ā—Ä–ĺ—Ā–ļ–ĺ–Ņ–ł—á–Ķ—Ā–ļ—É—é –ĺ–Ņ–Ķ—Ä–į—Ü–ł—é –Ĺ–į –ļ–ĺ–Ľ–Ķ–Ĺ–Ķ –ł–Ľ–ł –Ņ–Ľ–Ķ—á–Ķ, –Ľ–ł–Ī–ĺ –ĺ–Ņ–Ķ—Ä–į—Ü–ł—é –Ņ–ĺ –Ņ–ĺ–≤–ĺ–ī—É –Ņ–į—Ö–ĺ–≤–ĺ–Ļ –ł–Ľ–ł –≤–Ķ–Ĺ—ā—Ä–į–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—č–∂–ł. –ě–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į–Ĺ–ł–Ķ –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ĺ—Ā—Ć –Ĺ–į –Ņ—Ä–ĺ—ā—Ź–∂–Ķ–Ĺ–ł–ł 6 —Ā—É—ā —ā–Ķ—Ä–į–Ņ–ł–ł —É –≤–∑—Ä–ĺ—Ā–Ľ—č—Ö –Ľ–ł—Ü, –Ņ–ĺ–Ľ—É—á–į–≤—ą–ł—Ö –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł—Ź–ľ–ł —ā—Ä–į–ľ–į–ī–ĺ–Ľ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į, –ļ–ĺ–ī–Ķ–ł–Ĺ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į 30/300 –ľ–≥ –ł–Ľ–ł –Ņ–Ľ–į—Ü–Ķ–Ī–ĺ [12, 13]. –Ę—Ä–į–ľ–į–ī–ĺ–Ľ/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ –Ī—č–Ľ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ—č–ľ –ł —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ–ĺ –Ĺ–Ķ –ĺ—ā–Ľ–ł—á–į–Ľ—Ā—Ź –ĺ—ā –ļ–ĺ–ī–Ķ–ł–Ĺ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į —Ā —ā–ĺ—á–ļ–ł –∑—Ä–Ķ–Ĺ–ł—Ź –į–Ĺ–į–Ľ—Ć–≥–Ķ—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ —ć—Ą—Ą–Ķ–ļ—ā–į —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ā —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł–Ľ–ł –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ–Ļ –Ī–ĺ–Ľ—Ć—é –Ņ–ĺ—Ā–Ľ–Ķ –Ĺ–Ķ–Ī–ĺ–Ľ—Ć—ą–ł—Ö –ĺ—Ä—ā–ĺ–Ņ–Ķ–ī–ł—á–Ķ—Ā–ļ–ł—Ö –ł–Ľ–ł –į–Ī–ī–ĺ–ľ–ł–Ĺ–į–Ľ—Ć–Ĺ—č—Ö –ĺ–Ņ–Ķ—Ä–į—Ü–ł–Ļ. –ö–į—Ā–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ –ī—Ä—É–≥–ł—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ–Ķ–Ļ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –ļ–į—á–Ķ—Ā—ā–≤–ĺ –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į–Ĺ–ł—Ź –Ī—č–Ľ–ĺ –∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ –Ľ—É—á—ą–Ķ —É —ā—Ä–į–ľ–į–ī–ĺ–Ľ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į –≤ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł–ł —Ā –Ņ–Ľ–į—Ü–Ķ–Ī–ĺ –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –≤—Ā–Ķ—Ö 6 –ī–Ĺ–Ķ–Ļ –≤ –ĺ–Ī–ĺ–ł—Ö –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź—Ö [12, 13]. –ě–Ī—Č–į—Ź –ĺ—Ü–Ķ–Ĺ–ļ–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–į–ľ–ł –ļ–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł–ł —ā—Ä–į–ľ–į–ī–ĺ–Ľ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į –Ī—č–Ľ–į «–ĺ—á–Ķ–Ĺ—Ć —Ö–ĺ—Ä–ĺ—ą–ĺ» –ł «—Ö–ĺ—Ä–ĺ—ą–ĺ». –í –Ņ—Ä–ĺ—ā–ł–≤–ĺ–Ņ–ĺ–Ľ–ĺ–∂–Ĺ–ĺ—Ā—ā—Ć —ć—ā–ĺ–ľ—É –Ĺ–Ķ –Ī—č–Ľ–ĺ –Ĺ–ł–ļ–į–ļ–ł—Ö —Ā—É—Č–Ķ—Ā—ā–≤–Ķ–Ĺ–Ĺ—č—Ö —Ä–į–∑–Ľ–ł—á–ł–Ļ –ľ–Ķ–∂–ī—É –ļ–ĺ–ī–Ķ–ł–Ĺ–ĺ–ľ/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–ĺ–ľ –ł –Ņ–Ľ–į—Ü–Ķ–Ī–ĺ –≤ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź—Ö —Ā—Ä–Ķ–ī–Ĺ–Ķ–≥–ĺ —É—Ä–ĺ–≤–Ĺ—Ź –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į–Ĺ–ł—Ź –ł–Ľ–ł –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ī–ĺ–Ľ–ł.
–ė–Ĺ—ā–Ķ—Ä–Ķ—Ā –Ņ—Ä–Ķ–ī—Ā—ā–į–≤–Ľ—Ź—é—ā –ī–į–Ĺ–Ĺ—č–Ķ –Ī–ĺ–Ľ—Ć—ą–ĺ–≥–ĺ –ľ–Ĺ–ĺ–≥–ĺ—Ü–Ķ–Ĺ—ā—Ä–ĺ–≤–ĺ–≥–ĺ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź ELZA, –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–Ĺ–ĺ–≥–ĺ –≤–ĺ –§—Ä–į–Ĺ—Ü–ł–ł –≤ 2006–2007 –≥–≥., –≤ –ļ–ĺ—ā–ĺ—Ä–ĺ–ľ —ā–į–ļ–∂–Ķ –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–į—Ā—Ć —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –ó–į–Ľ–ī–ł–į—Ä–į [14]. –í –Ĺ–Ķ–ľ –Ņ—Ä–ł–Ĺ—Ź–Ľ–ł —É—á–į—Ā—ā–ł–Ķ 1158 –≤—Ä–į—á–Ķ–Ļ –ĺ–Ī—Č–Ķ–Ļ –Ņ—Ä–į–ļ—ā–ł–ļ–ł –ł 5495 –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≤–ĺ–∑—Ä–į—Ā—ā–Ķ —Ā—ā–į—Ä—ą–Ķ 12 –Ľ–Ķ—ā, –ļ–ĺ—ā–ĺ—Ä—č–Ķ –Ņ–ĺ–Ľ—É—á–į–Ľ–ł –ó–į–Ľ–ī–ł–į—Ä –Ņ—Ä–ł —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ—č—Ö –ł —Ā–ł–Ľ—Ć–Ĺ—č—Ö –ľ—č—ą–Ķ—á–Ĺ–ĺ-—Ā–ļ–Ķ–Ľ–Ķ—ā–Ĺ—č—Ö –Ī–ĺ–Ľ—Ź—Ö (–ĺ—Ā—ā–Ķ–ĺ–į—Ä—ā—Ä–ĺ–∑ – 24,9%, –Ī–ĺ–Ľ–ł –≤ —Ā–Ņ–ł–Ĺ–Ķ – 20,1% –ł —Ä–į–ī–ł–ļ—É–Ľ–ĺ–Ņ–į—ā–ł—Ź – 13,9%). –°—Ä–Ķ–ī–Ĺ—Ź—Ź –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –Ī–ĺ–Ľ–ł —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 7,3 –ī–Ĺ—Ź (n=5108), 44,0% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł—Ā–Ņ—č—ā—č–≤–į–Ľ–ł –Ī–ĺ–Ľ—Ć –ľ–Ķ–Ĺ–Ķ–Ķ 5 –ī–Ĺ–Ķ–Ļ, 70,3% – –ľ–Ķ–Ĺ–Ķ–Ķ 30 –ī–Ĺ–Ķ–Ļ, 15,6% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ł–ľ–Ķ–Ľ–ł —Ö—Ä–ĺ–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ķ –Ī–ĺ–Ľ–ł –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –Ī–ĺ–Ľ–Ķ–Ķ 90 –ī–Ĺ–Ķ–Ļ. –°—Ä–Ķ–ī–Ĺ—Ź—Ź –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć —ā–Ķ—Ä–į–Ņ–ł–ł —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 16,6 –ī–Ĺ—Ź, —Ā—Ä–Ķ–ī–Ĺ—Ź—Ź —Ā—É—ā–ĺ—á–Ĺ–į—Ź –ī–ĺ–∑–į – 3,7 —ā–į–Ī–Ľ–Ķ—ā–ļ–ł. –ě—ā–ī–Ķ–Ľ—Ć–Ĺ—É—é –Ņ–ĺ–ī–≥—Ä—É–Ņ–Ņ—É —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź–Ľ–ł –Ņ–į—Ü–ł–Ķ–Ĺ—ā—č –≤ –≤–ĺ–∑—Ä–į—Ā—ā–Ķ —Ā—ā–į—Ä—ą–Ķ 75 –Ľ–Ķ—ā (n=89). –°—Ä–Ķ–ī–Ĺ—Ź—Ź –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć –Ī–ĺ–Ľ–ł —É —ć—ā–ł—Ö –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –Ī—č–Ľ–į 2,1 –≥–ĺ–ī–į, 51% –ł—Ā–Ņ—č—ā—č–≤–į–Ľ–ł –Ī–ĺ–Ľ—Ć –ľ–Ķ–Ĺ–Ķ–Ķ 1 –ľ–Ķ—Ā., 22% – –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 1 –≥–ĺ–ī–į –ł –Ī–ĺ–Ľ–Ķ–Ķ, —Ā—Ä–Ķ–ī–Ĺ—Ź—Ź –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā—Ć —ā–Ķ—Ä–į–Ņ–ł–ł —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–į 20,8 –ī–Ĺ—Ź, –į —Ā—Ä–Ķ–ī–Ĺ—Ź—Ź —Ā—É—ā–ĺ—á–Ĺ–į—Ź –ī–ĺ–∑–į – 3,8 —ā–į–Ī–Ľ–Ķ—ā–ļ–ł.
–ź–Ĺ–į–Ľ–ł–∑ —Ä–Ķ–∑—É–Ľ—Ć—ā–į—ā–ĺ–≤ —ā–Ķ—Ä–į–Ņ–ł–ł –Ņ–ĺ–ļ–į–∑–į–Ľ, —á—ā–ĺ –∑–Ĺ–į—á–ł–ľ–ĺ–Ķ (—Ä<0,001) —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ī–ĺ–Ľ–ł –Ņ–ĺ —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—é —Ā –ł—Ā—Ö–ĺ–ī–Ĺ—č–ľ —É—Ä–ĺ–≤–Ĺ–Ķ–ľ –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ĺ—Ā—Ć –≤ –ĺ–Ī—Č–Ķ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ (6,3 –Ī–į–Ľ–Ľ–į –≤ –Ĺ–į—á–į–Ľ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł—Ź –ł 2,3 – –Ņ–ĺ –ĺ–ļ–ĺ–Ĺ—á–į–Ĺ–ł–ł, —ā.–Ķ. —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ī–ĺ–Ľ–ł –Ĺ–į 63%) –ł —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≤–ĺ–∑—Ä–į—Ā—ā–Ķ —Ā—ā–į—Ä—ą–Ķ 75 –Ľ–Ķ—ā (6,1 –Ņ—Ä–ĺ—ā–ł–≤ 2,9 –Ī–į–Ľ–Ľ–į; 52% —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł—Ź –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ī–ĺ–Ľ–ł). –ö—Ä–ĺ–ľ–Ķ —ā–ĺ–≥–ĺ, –≤ –ĺ–Ī—Č–Ķ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ 63,6% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ĺ—Ü–Ķ–Ĺ–ł–Ľ–ł —É—Ä–ĺ–≤–Ķ–Ĺ—Ć –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į–Ĺ–ł—Ź –ļ–į–ļ «–∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ», 13,8% – –ļ–į–ļ «–Ņ–ĺ–Ľ–Ĺ—č–Ļ»; 66% –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –≤–ĺ–∑—Ä–į—Ā—ā–Ķ —Ā—ā–į—Ä—ą–Ķ 75 –Ľ–Ķ—ā –ĺ—Ü–Ķ–Ĺ–ł–Ľ–ł —É—Ä–ĺ–≤–Ķ–Ĺ—Ć –ĺ–Ī–Ķ–∑–Ī–ĺ–Ľ–ł–≤–į–Ĺ–ł—Ź –ļ–į–ļ «–∑–Ĺ–į—á–ł—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ» –ł–Ľ–ł «–Ņ–ĺ–Ľ–Ĺ—č–Ļ» [14].
–ú–į—ā–Ķ—Ä–ł–į–Ľ –ł –ľ–Ķ—ā–ĺ–ī—č
–ó–į –Ņ–ĺ—Ā–Ľ–Ķ–ī–Ĺ–ł–Ķ 8 –ľ–Ķ—Ā. –≤ –ļ–Ľ–ł–Ĺ–ł–ļ–Ķ —Ą–į–ļ—É–Ľ—Ć—ā–Ķ—ā—Ā–ļ–ĺ–Ļ —Ö–ł—Ä—É—Ä–≥–ł–ł ‚ĄĖ 2 –ü–Ķ—Ä–≤–ĺ–≥–ĺ –ú–ď–ú–£ –ł–ľ–Ķ–Ĺ–ł –ė.–ú. –°–Ķ—á–Ķ–Ĺ–ĺ–≤–į –Ĺ–į –Ī–į–∑–Ķ –ĺ—ā–ī–Ķ–Ľ–Ķ–Ĺ–ł—Ź —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ł—Ö –ł–Ĺ—Ą–Ķ–ļ—Ü–ł–Ļ –ď–ö–Ď ‚ĄĖ 61 –≥. –ú–ĺ—Ā–ļ–≤—č 31 –Ņ–į—Ü–ł–Ķ–Ĺ—ā—É –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ–į –≤—č—Ā–ĺ–ļ–į—Ź –į–ľ–Ņ—É—ā–į—Ü–ł—Ź –Ĺ–į —É—Ä–ĺ–≤–Ĺ–Ķ –≤–Ķ—Ä—Ö–Ĺ–Ķ–Ļ —ā—Ä–Ķ—ā–ł –≥–ĺ–Ľ–Ķ–Ĺ–ł (2) –ł —Ā—Ä–Ķ–ī–Ĺ–Ķ–Ļ —ā—Ä–Ķ—ā–ł –Ī–Ķ–ī—Ä–į (29). –í—Ā–Ķ –ĺ–Ĺ–ł – 27 –ľ—É–∂—á–ł–Ĺ –ł 4 –∂–Ķ–Ĺ—Č–ł–Ĺ—č – –Ņ–ĺ—Ā—ā—É–Ņ–ł–Ľ–ł —Ā –∑–į–Ņ—É—Č–Ķ–Ĺ–Ĺ–ĺ–Ļ —Ā—ā–į–ī–ł–Ķ–Ļ –ě–ó–ź–Ě–ö (IV —Ā—ā–į–ī–ł—Ź –Ņ–ĺ –ļ–Ľ–į—Ā—Ā–ł—Ą–ł–ļ–į—Ü–ł–ł –ü–ĺ–ļ—Ä–ĺ–≤—Ā–ļ–ĺ–≥–ĺ––§–ĺ–Ĺ—ā–Ķ–Ļ–Ĺ–į), –Ņ—Ä–ĺ—Ź–≤–Ľ—Ź–≤—ą–Ķ–Ļ—Ā—Ź –≤ –≤–ł–ī–Ķ –Ņ—Ä–ĺ—ā—Ź–∂–Ķ–Ĺ–Ĺ—č—Ö –Ĺ–Ķ–ļ—Ä–ĺ–∑–ĺ–≤ –Ĺ–į —Ā—ā–ĺ–Ņ–Ķ, —Ą–Ľ–ł–ļ—ā–Ķ–Ĺ –ł –ĺ–Ī—ą–ł—Ä–Ĺ—č—Ö –≥–Ĺ–ĺ–Ļ–Ĺ–ĺ-–Ĺ–Ķ–ļ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö —ā—Ä–ĺ—Ą–ł—á–Ķ—Ā–ļ–ł—Ö —Ź–∑–≤ –Ĺ–į —Ā—ā–ĺ–Ņ–Ķ –ł/–ł–Ľ–ł –≥–ĺ–Ľ–Ķ–Ĺ–ł. –í–ĺ–∑—Ä–į—Ā—ā–Ĺ–ĺ–Ļ –ī–ł–į–Ņ–į–∑–ĺ–Ĺ –≤–į—Ä—Ć–ł—Ä–ĺ–≤–į–Ľ –ĺ—ā 57 –ī–ĺ 84 –Ľ–Ķ—ā (71,5±3,2); –Ņ–ĺ–ī–į–≤–Ľ—Ź—é—Č–Ķ–Ķ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–ĺ (85%) – –Ľ–ł—Ü–į –Ņ–ĺ–∂–ł–Ľ–ĺ–≥–ĺ –ł —Ā—ā–į—Ä—á–Ķ—Ā–ļ–ĺ–≥–ĺ –≤–ĺ–∑—Ä–į—Ā—ā–į.
–ü–ĺ –ī–į–Ĺ–Ĺ—č–ľ —É–Ľ—Ć—ā—Ä–į–∑–≤—É–ļ–ĺ–≤–ĺ–≥–ĺ –į–Ĺ–≥–ł–ĺ—Ā–ļ–į–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ņ—Ä–ł—á–ł–Ĺ–ĺ–Ļ –≥–į–Ĺ–≥—Ä–Ķ–Ĺ—č –Ě–ö –Ī—č–Ľ–į –Ņ—Ä–ĺ—ā—Ź–∂–Ķ–Ĺ–Ĺ–į—Ź –ĺ–ļ–ļ–Ľ—é–∑–ł—Ź –ľ–į–≥–ł—Ā—ā—Ä–į–Ľ—Ć–Ĺ–ĺ–≥–ĺ —Ā–ĺ—Ā—É–ī–ł—Ā—ā–ĺ–≥–ĺ —Ä—É—Ā–Ľ–į: –Ī–Ķ—Ä—Ü–ĺ–≤–ĺ-—Ā—ā–ĺ–Ņ–Ĺ—č–Ļ –ł/–ł–Ľ–ł –Ī–Ķ–ī—Ä–Ķ–Ĺ–Ĺ–ĺ-–Ņ–ĺ–ī–ļ–ĺ–Ľ–Ķ–Ĺ–Ĺ—č–Ļ —Ā–Ķ–≥–ľ–Ķ–Ĺ—ā—č. –ě—Ā–Ĺ–ĺ–≤–Ĺ—č–Ķ –Ĺ–ĺ–∑–ĺ–Ľ–ĺ–≥–ł—á–Ķ—Ā–ļ–ł–Ķ —Ą–ĺ—Ä–ľ—č –ě–ó–ź–Ě–ö: –ě–ź –≤ «—á–ł—Ā—ā–ĺ–ľ» –≤–į—Ä–ł–į–Ĺ—ā–Ķ (24) –Ľ–ł–Ī–ĺ –Ķ–≥–ĺ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–Ķ —Ā –ī–ł–į–Ī–Ķ—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ľ–į–ļ—Ä–ĺ–į–Ĺ–≥–ł–ĺ–Ņ–į—ā–ł–Ķ–Ļ (7). –ü–ĺ–ī–į–≤–Ľ—Ź—é—Č–Ķ–Ķ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–ĺ –ł–ľ–Ķ–Ľ–ł 3 –ł –Ī–ĺ–Ľ–Ķ–Ķ —Ā–Ķ—Ä—Ć–Ķ–∑–Ĺ—č—Ö —Ā–ĺ–ľ–į—ā–ł—á–Ķ—Ā–ļ–ł—Ö –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź; –Ĺ–į–ł–Ī–ĺ–Ľ–Ķ–Ķ —á–į—Ā—ā–ĺ – –ļ–į—Ä–ī–ł–ĺ–≤–į—Ā–ļ—É–Ľ—Ź—Ä–Ĺ—č–Ķ —Ä–į—Ā—Ā—ā—Ä–ĺ–Ļ—Ā—ā–≤–į (—ā—Ź–∂–Ķ–Ľ–į—Ź —Ą–ĺ—Ä–ľ–į –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –Ī–ĺ–Ľ–Ķ–∑–Ĺ–ł —Ā–Ķ—Ä–ī—Ü–į, –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–į—Ź –≥–ł–Ņ–Ķ—Ä—ā–Ķ–Ĺ–∑–ł—Ź –ł –Ņ—Ä.), –ī–Ķ–ļ–ĺ–ľ–Ņ–Ķ–Ĺ—Ā–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ļ —Ā–į—Ö–į—Ä–Ĺ—č–Ļ –ī–ł–į–Ī–Ķ—ā (–°–Ē), –Ņ–Ķ—á–Ķ–Ĺ–ĺ—á–Ĺ–ĺ-–Ņ–ĺ—á–Ķ—á–Ĺ—č–Ķ –ī–ł—Ā—Ą—É–Ĺ–ļ—Ü–ł–ł. –ü—Ä–į–ļ—ā–ł—á–Ķ—Ā–ļ–ł —É –≤—Ā–Ķ—Ö –Ľ–ł—Ü –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ—č –ļ–Ľ–ł–Ĺ–ł–ļ–ĺ-–Ľ–į–Ī–ĺ—Ä–į—ā–ĺ—Ä–Ĺ—č–Ķ –Ņ—Ä–ĺ—Ź–≤–Ľ–Ķ–Ĺ–ł—Ź —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į —Ā–ł—Ā—ā–Ķ–ľ–Ĺ–ĺ–Ļ –≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ļ —Ä–Ķ–į–ļ—Ü–ł–ł (SIRS), –≤ 1/3 —Ā–Ľ—É—á–į–Ķ–≤ – –ü–ě–Ě.
–ź–ľ–Ņ—É—ā–į—Ü–ł–ł –≤—č–Ņ–ĺ–Ľ–Ĺ—Ź–Ľ–ł—Ā—Ć –Ĺ–į–ľ–ł –Ņ–ĺ–ī —Ā–Ņ–ł–Ĺ–į–Ľ—Ć–Ĺ–ĺ–Ļ –į–Ĺ–Ķ—Ā—ā–Ķ–∑–ł–Ķ–Ļ –Ņ–ĺ —ā—Ä–į–ī–ł—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –ī–≤—É—Ö–Ľ–ĺ—Ā–ļ—É—ā–Ĺ–ĺ–Ļ —Ą–į—Ā—Ü–ł–ĺ-–ľ–ł–ĺ–Ņ–Ľ–į—Ā—ā–ł—á–Ķ—Ā–ļ–ĺ–Ļ –ľ–Ķ—ā–ĺ–ī–ł–ļ–Ķ. –í 1-–ľ –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł–ł –≤—č–Ņ–ĺ–Ľ–Ĺ–Ķ–Ĺ—č –Ī–ł–Ľ–į—ā–Ķ—Ä–į–Ľ—Ć–Ĺ—č–Ķ –≤–ľ–Ķ—ą–į—ā–Ķ–Ľ—Ć—Ā—ā–≤–į —Ā —É—Ā–Ķ—á–Ķ–Ĺ–ł–Ķ–ľ –Ě–ö –Ĺ–į –ĺ–ī–Ĺ–ĺ–ľ –ł —ā–ĺ–ľ –∂–Ķ —É—Ä–ĺ–≤–Ĺ–Ķ. –ü—Ä–į–≤–į—Ź –ł –Ľ–Ķ–≤–į—Ź –Ě–ö –Ņ—Ä–ł–ľ–Ķ—Ä–Ĺ–ĺ –ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤–ĺ –Ņ–ĺ–ī–≤–Ķ—Ä–≥–į–Ľ–ł—Ā—Ć –ĺ–Ņ–Ķ—Ä–į—Ü–ł–ł. –í—Ā–Ķ–ľ –Ī–ĺ–Ľ—Ć–Ĺ—č–ľ –≤ –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–ľ –Ņ–Ķ—Ä–ł–ĺ–ī–Ķ –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–į—Ā—Ć –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź (–į–Ĺ—ā–ł–Ī–ł–ĺ—ā–ł–ļ–ł, –ł–Ĺ—Ą—É–∑–ł–ĺ–Ĺ–Ĺ–į—Ź —ā–Ķ—Ä–į–Ņ–ł—Ź, –Ņ—Ä—Ź–ľ—č–Ķ –į–Ĺ—ā–ł–ļ–ĺ–į–≥—É–Ľ—Ź–Ĺ—ā—č, –ī–Ķ–∑–į–≥—Ä–Ķ–≥–į–Ĺ—ā—č, —Ą–Ľ–Ķ–Ī–ĺ—ā–ĺ–Ĺ–ł–ļ–ł, –ľ–Ķ—ā–į–Ī–ĺ–Ľ–ł—á–Ķ—Ā–ļ–ł–Ķ —Ā—Ä–Ķ–ī—Ā—ā–≤–į –ł –ī—Ä.) –≤ —Ā–ĺ—á–Ķ—ā–į–Ĺ–ł–ł —Ā –ľ–Ķ–ī–ł–ļ–į–ľ–Ķ–Ĺ—ā–ĺ–∑–Ĺ–ĺ–Ļ –ļ–ĺ—Ä—Ä–Ķ–ļ—Ü–ł–Ķ–Ļ —Ā–ĺ–ľ–į—ā–ł—á–Ķ—Ā–ļ–ł—Ö –Ī–ĺ–Ľ–Ķ–∑–Ĺ–Ķ–Ļ –Ņ–ĺ —Ä–Ķ–ļ–ĺ–ľ–Ķ–Ĺ–ī–į—Ü–ł—Ź–ľ —ā–Ķ—Ä–į–Ņ–Ķ–≤—ā–į.
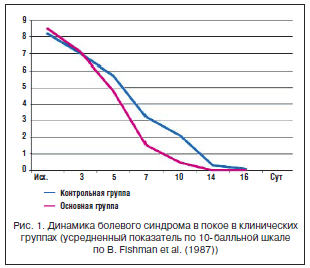
–ü–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–į—Ź –į–Ĺ–į–Ľ—Ć–≥–Ķ–∑–ł—Ź –≤–ĺ –≤—Ā–Ķ—Ö –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź—Ö –Ĺ–ĺ—Ā–ł–Ľ–į –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–Ļ —Ö–į—Ä–į–ļ—ā–Ķ—Ä –ł –≤–ļ–Ľ—é—á–į–Ľ–į –ĺ–Ī—Ź–∑–į—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ –Ņ—Ä–ł–Ķ–ľ –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į –ó–į–Ľ–ī–ł–į—Ä –Ņ–ĺ —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ–ĺ–Ļ —Ā—Ö–Ķ–ľ–Ķ (–Ņ–ĺ 1 —ā–į–Ī–Ľ–Ķ—ā–ļ–Ķ 2 —Ä./—Ā—É—ā –≤–Ĺ–Ķ —Ā–≤—Ź–∑–ł —Ā –Ķ–ī–ĺ–Ļ) –Ĺ–į—á–ł–Ĺ–į—Ź —Ā 1-—Ö —Ā—É—ā –ł –ī–į–Ľ–Ķ–Ķ –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ 10 –ī–Ĺ–Ķ–Ļ. –≠—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –į–Ĺ–į–Ľ—Ć–≥–Ķ–∑–ł–ł –ĺ—Ü–Ķ–Ĺ–ł–≤–į–Ľ–ł –Ņ—Ä–ĺ—Ā–Ņ–Ķ–ļ—ā–ł–≤–Ĺ–ĺ. –Ē–Ľ—Ź —Ā–į–ľ–ĺ–ĺ—Ü–Ķ–Ĺ–ļ–ł –Ī–ĺ–Ľ–Ķ–≤–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į –Ņ–ĺ –Ķ–≥–ĺ –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –≤ –Ņ–ĺ–ļ–ĺ–Ķ –ļ–į–∂–ī–ĺ–ľ—É –Ņ–į—Ü–ł–Ķ–Ĺ—ā—É —Ā –ě–ó–ź–Ě–ö –Ņ—Ä–Ķ–ī–Ľ–į–≥–į–Ľ–į—Ā—Ć –≤–ł–∑—É–į–Ľ—Ć–Ĺ–ĺ-–į–Ĺ–į–Ľ–ĺ–≥–ĺ–≤–į—Ź 10-–Ī–į–Ľ–Ľ—Ć–Ĺ–į—Ź —ą–ļ–į–Ľ–į –Ņ–ĺ B. Fishman et al. (1987). –ü–ĺ–Ľ—É—á–Ķ–Ĺ–Ĺ—č–Ķ –ī–į–Ĺ–Ĺ—č–Ķ —Ā—Ä–į–≤–Ĺ–ł–≤–į–Ľ–ł —Ā —ā–į–ļ–ĺ–≤—č–ľ–ł —É 25 —á–Ķ–Ľ–ĺ–≤–Ķ–ļ, —ā–į–ļ–∂–Ķ –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā—ą–ł—Ö –≤—č—Ā–ĺ–ļ—É—é –į–ľ–Ņ—É—ā–į—Ü–ł—é –Ņ–ĺ –Ņ–ĺ–≤–ĺ–ī—É –≤–Ľ–į–∂–Ĺ–ĺ–Ļ –≥–į–Ĺ–≥—Ä–Ķ–Ĺ—č –Ĺ–į —Ą–ĺ–Ĺ–Ķ –ě–ó–ź–Ě–ö, –Ĺ–ĺ –Ņ—Ä–ł–Ĺ–ł–ľ–į–≤—ą–ł—Ö —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ—É—é —ā–Ķ—Ä–į–Ņ–ł—é (–Ĺ–Ķ—Ā—ā–Ķ—Ä–ĺ–ł–ī–Ĺ—č–ľ–ł –Ņ—Ä–ĺ—ā–ł–≤–ĺ–≤–ĺ—Ā–Ņ–į–Ľ–ł—ā–Ķ–Ľ—Ć–Ĺ—č–ľ–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–į–ľ–ł) –≤ —ā–Ķ –∂–Ķ —Ā—Ä–ĺ–ļ–ł. –ě–Ĺ–ł —Ā–ĺ—Ā—ā–į–≤–ł–Ľ–ł –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ—É—é –≥—Ä—É–Ņ–Ņ—É. –ė—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –ī–į–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź –Ņ—Ä–ĺ–≤–ĺ–ī–ł–Ľ–ĺ—Ā—Ć –Ņ—Ä–ł –≥–ĺ—Ā–Ņ–ł—ā–į–Ľ–ł–∑–į—Ü–ł–ł, –į —ā–į–ļ–∂–Ķ –Ĺ–į 3, 5, 7, 10, 14 –ł 16-–Ķ —Ā—É—ā –Ņ–ĺ—Ā–Ľ–Ķ –į–ľ–Ņ—É—ā–į—Ü–ł–ł. –Ď–ĺ–Ľ–Ķ–≤–ĺ–Ļ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ —Ā—á–ł—ā–į–Ľ–ł –Ņ–ĺ–Ľ–Ĺ–ĺ—Ā—ā—Ć—é –ļ—É–Ņ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č–ľ –Ņ—Ä–ł —Ā–į–ľ–ĺ–ĺ—Ü–Ķ–Ĺ–ļ–Ķ «0 –Ī–į–Ľ–Ľ–ĺ–≤». –ü–ĺ –ī–į–Ĺ–Ĺ–ĺ–Ļ —ą–ļ–į–Ľ–Ķ —Ā—Ä–Ķ–ī–Ĺ–ł–Ļ –Ī–į–Ľ–Ľ –Ņ—Ä–ł –Ņ–ĺ—Ā—ā—É–Ņ–Ľ–Ķ–Ĺ–ł–ł —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ —Ā –ö–ė–Ě–ö –≤ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ —Ā–ĺ—Ā—ā–į–≤–ł–Ľ 8,5±0,3 –Ī–į–Ľ–Ľ–į, –≤ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ – 8,2±0,2 –Ī–į–Ľ–Ľ–į (p>0,05). –ė–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ī–ĺ–Ľ–Ķ–Ļ –≤ –Ĺ–į—ą–ł—Ö –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź—Ö –Ĺ–Ķ –ļ–ĺ—Ä—Ä–Ķ–Ľ–ł—Ä–ĺ–≤–į–Ľ–į —Ā —É—Ä–ĺ–≤–Ĺ–Ķ–ľ –ĺ–ļ–ļ–Ľ—é–∑–ł–ł –ľ–į–≥–ł—Ā—ā—Ä–į–Ľ—Ć–Ĺ—č—Ö –į—Ä—ā–Ķ—Ä–ł–Ļ. –ě–Ī–Ķ –≥—Ä—É–Ņ–Ņ—č – –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–į—Ź –ł –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–į—Ź – –ł–ī–Ķ–Ĺ—ā–ł—á–Ĺ—č –Ņ–ĺ —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ—č–ľ –ī–Ķ–ľ–ĺ–≥—Ä–į—Ą–ł—á–Ķ—Ā–ļ–ł–ľ –Ņ–į—Ä–į–ľ–Ķ—ā—Ä–į–ľ, —ć—ā–ł–ĺ–Ľ–ĺ–≥–ł–ł, —ā—Ź–∂–Ķ—Ā—ā–ł —ā–Ķ—á–Ķ–Ĺ–ł—Ź –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–≥–ĺ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź, –ĺ–Ī—Č–Ķ–ľ—É —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł—é –ł —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–ł–ľ –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ. –ú–Ķ–∂–≥—Ä—É–Ņ–Ņ–ĺ–≤—č–Ķ —Ä–į–∑–Ľ–ł—á–ł—Ź –Ĺ–ĺ—Ā–ł–Ľ–ł –Ĺ–Ķ–ī–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ—č–Ļ —Ö–į—Ä–į–ļ—ā–Ķ—Ä.
–†–Ķ–∑—É–Ľ—Ć—ā–į—ā—č –ł –į–Ĺ–į–Ľ–ł–∑
–° —É—á–Ķ—ā–ĺ–ľ –Ņ—Ä–ł–ĺ—Ä–ł—ā–Ķ—ā–ĺ–≤ –ľ–ł–Ĺ–ł–ľ–į–Ľ—Ć–Ĺ–ĺ–Ļ –ł–Ĺ–≤–į–∑–ł–≤–Ĺ–ĺ—Ā—ā–ł –≤–į–∂–Ĺ–Ķ–Ļ—ą–ł–ľ –ļ—Ä–ł—ā–Ķ—Ä–ł–Ķ–ľ —ć—Ą—Ą–Ķ–ļ—ā–ł–≤–Ĺ–ĺ—Ā—ā–ł —Ö–ł—Ä—É—Ä–≥–ł—á–Ķ—Ā–ļ–ł—Ö —ā–Ķ—Ö–Ĺ–ĺ–Ľ–ĺ–≥–ł–Ļ —Ā—á–ł—ā–į–Ķ—ā—Ā—Ź –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ—Ā—ā—Ć –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ –≤ —Ä–į–Ĺ–Ķ –ļ—É–Ľ—Ć—ā–ł –Ě–ö. –ú–ł–Ĺ–ł–ľ–į–Ľ—Ć–Ĺ–į—Ź –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ī–ĺ–Ľ–Ķ–≤–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į –ĺ—ā–ľ–Ķ—á–į–Ľ–į—Ā—Ć —É –Ľ–ł—Ü —Ā —Ā–ĺ–Ņ—É—ā—Ā—ā–≤—É—é—Č–ł–ľ –°–Ē –Ĺ–į —Ą–ĺ–Ĺ–Ķ –≤—č—Ä–į–∂–Ķ–Ĺ–Ĺ–ĺ–Ļ –Ņ–ĺ–Ľ–ł–Ĺ–Ķ–Ļ—Ä–ĺ–Ņ–į—ā–ł–ł (7,7±0,4 –Ī–į–Ľ–Ľ–į), –į –ľ–į–ļ—Ā–ł–ľ–į–Ľ—Ć–Ĺ–į—Ź – –Ņ—Ä–ł –Ņ—Ä–ĺ–≥—Ä–Ķ—Ā—Ā–ł—Ä—É—é—Č–Ķ–Ļ –≤–Ľ–į–∂–Ĺ–ĺ–Ļ –≥–į–Ĺ–≥—Ä–Ķ–Ĺ–Ķ —Ā—ā–ĺ–Ņ—č –ł –≥–ĺ–Ľ–Ķ–Ĺ–ł –Ĺ–į —Ą–ĺ–Ĺ–Ķ –ĺ—Ā—ā—Ä–ĺ–Ļ –į—Ä—ā–Ķ—Ä–ł–į–Ľ—Ć–Ĺ–ĺ–Ļ –ĺ–ļ–ļ–Ľ—é–∑–ł–ł (3 –Ĺ–į–Ī–Ľ—é–ī–Ķ–Ĺ–ł—Ź), –Ņ—Ä–ł–Ī–Ľ–ł–∂–į—Ź—Ā—Ć –ļ —ā–į–ļ –Ĺ–į–∑—č–≤–į–Ķ–ľ–ĺ–Ļ «–Ĺ–Ķ—Ā—ā–Ķ—Ä–Ņ–ł–ľ–ĺ–Ļ» (9,5 –Ī–į–Ľ–Ľ–į).
–ė–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā—Ć –Ī–ĺ–Ľ–Ķ–Ļ –≤ –ļ—É–Ľ—Ć—ā–Ķ –Ě–ö –≤ —ā–Ķ—á–Ķ–Ĺ–ł–Ķ –Ņ–Ķ—Ä–≤—č—Ö 3 —Ā—É—ā –Ĺ–Ķ –ł–ľ–Ķ–Ľ–į –ľ–Ķ–∂–≥—Ä—É–Ņ–Ņ–ĺ–≤–ĺ–Ļ —Ä–į–∑–Ĺ–ł—Ü—č (—Ä–ł—Ā. 1). –ü—Ä–ł—á–ł–Ĺ–į–ľ–ł —ć—ā–ĺ–≥–ĺ, –Ĺ–į –Ĺ–į—ą –≤–∑–≥–Ľ—Ź–ī, –Ī—č–Ľ–ł –Ņ—Ä–ł–ľ–Ķ—Ä–Ĺ–ĺ –ĺ–ī–ł–Ĺ–į–ļ–ĺ–≤—č–Ķ —Ā—ā–Ķ–Ņ–Ķ–Ĺ—Ć —Ä–į—Ā–Ņ—Ä–ĺ—Ā—ā—Ä–į–Ĺ–Ķ–Ĺ–ł—Ź –≥–Ĺ–ĺ–Ļ–Ĺ–ĺ-–Ĺ–Ķ–ļ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ĺ–≥–ĺ –Ņ—Ä–ĺ—Ü–Ķ—Ā—Ā–į –Ĺ–į —Ą–ĺ–Ĺ–Ķ –ě–ó–ź–Ě–ö –ł —ā—Ź–∂–Ķ—Ā—ā—Ć –ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ —ā—Ä–į–≤–ľ—č.
–ě–ī–Ĺ–į–ļ–ĺ –≤ –Ņ–ĺ—Ā–Ľ–Ķ–ī—É—é—Č–ł–Ķ –ī–Ĺ–ł –Ĺ–į —Ą–ĺ–Ĺ–Ķ –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ —ā–Ķ—Ä–į–Ņ–ł–ł —Ā –ł—Ā–Ņ–ĺ–Ľ—Ć–∑–ĺ–≤–į–Ĺ–ł–Ķ–ľ –ó–į–Ľ–ī–ł–į—Ä–į —É –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–į –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ—č –Ĺ–į–Ī–Ľ—é–ī–į–Ľ–ł —Ā—ā–į—ā–ł—Ā—ā–ł—á–Ķ—Ā–ļ–ł –ī–ĺ—Ā—ā–ĺ–≤–Ķ—Ä–Ĺ–ĺ–Ķ (—Ä<0,05) —Ā–Ĺ–ł–∂–Ķ–Ĺ–ł–Ķ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ź –ł–Ĺ—ā–Ķ–Ĺ—Ā–ł–≤–Ĺ–ĺ—Ā—ā–ł –Ī–ĺ–Ľ–Ķ–Ļ –≤ –ļ—É–Ľ—Ć—ā–Ķ –Ě–ö. –ö 5–6 —Ā—É—ā –ĺ–Ĺ —Ā–Ĺ–ł–∂–į–Ľ—Ā—Ź, —Ā–ĺ—Ā—ā–į–≤–Ľ—Ź—Ź –≤ —Ā—Ä–Ķ–ī–Ĺ–Ķ–ľ 4,8±0,3 –Ī–į–Ľ–Ľ–į («—É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ—č–Ķ –Ī–ĺ–Ľ–ł»). –£—Ā–ļ–ĺ—Ä–Ķ–Ĺ–Ĺ–į—Ź —Ä–Ķ–≥—Ä–Ķ—Ā—Ā–ł—Ź –Ī–ĺ–Ľ–Ķ–≤–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į –∑–į —Ā—á–Ķ—ā –ļ–ĺ–ľ–Ī–ł–Ĺ–ł—Ä–ĺ–≤–į–Ĺ–Ĺ–ĺ–Ļ –į–Ĺ–į–Ľ—Ć–≥–Ķ–∑–ł–ł –Ņ–ĺ–∑–≤–ĺ–Ľ—Ź–Ľ–į –Ĺ–į–ľ —Ä–į—Ā—ą–ł—Ä–ł—ā—Ć –ī–≤–ł–≥–į—ā–Ķ–Ľ—Ć–Ĺ—č–Ļ —Ä–Ķ–∂–ł–ľ –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≤ –Ī–ĺ–Ľ–Ķ–Ķ —Ä–į–Ĺ–Ĺ–ł–Ķ —Ā—Ä–ĺ–ļ–ł. –Ď—č–Ľ–ł –ĺ—ā–ľ–Ķ—á–Ķ–Ĺ—č —É–Ľ—É—á—ą–Ķ–Ĺ–ł–Ķ –ĺ–Ī—Č–Ķ–≥–ĺ —Ā–ĺ—Ā—ā–ĺ—Ź–Ĺ–ł—Ź –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö –≤ —Ā–≤—Ź–∑–ł —Ā –ļ—É–Ņ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ–ľ –Ī–ĺ–Ľ–Ķ–≤–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į, –Ĺ–ĺ—Ä–ľ–į–Ľ–ł–∑–į—Ü–ł—Ź –Ĺ–ĺ—á–Ĺ–ĺ–≥–ĺ —Ā–Ĺ–į –ł –į–Ņ–Ņ–Ķ—ā–ł—ā–į. –≠—ā–ĺ –≤ —Ā–≤–ĺ—é –ĺ—á–Ķ—Ä–Ķ–ī—Ć —Ā–Ņ–ĺ—Ā–ĺ–Ī—Ā—ā–≤–ĺ–≤–į–Ľ–ĺ —É–Ľ—É—á—ą–Ķ–Ĺ–ł—é —Ä–Ķ–≥–ł–ĺ–Ĺ–į—Ä–Ĺ–ĺ–≥–ĺ –ļ—Ä–ĺ–≤–ĺ–ĺ–Ī—Ä–į—Č–Ķ–Ĺ–ł—Ź –ł —Ä–į–Ĺ–Ĺ–Ķ–Ļ —Ä–Ķ–į–Ī–ł–Ľ–ł—ā–į—Ü–ł–ł.
–í —ā–Ķ –∂–Ķ —Ā—Ä–ĺ–ļ–ł –≤ –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ —É –Ņ–ĺ–ī–į–≤–Ľ—Ź—é—Č–Ķ–≥–ĺ –Ī–ĺ–Ľ—Ć—ą–ł–Ĺ—Ā—ā–≤–į –ĺ–Ņ–Ķ—Ä–ł—Ä–ĺ–≤–į–Ĺ–Ĺ—č—Ö –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć –≤–į—Ä—Ć–ł—Ä–ĺ–≤–į–Ľ –≤ –Ņ—Ä–Ķ–ī–Ķ–Ľ–į—Ö –ĺ—ā 5 –ī–ĺ 7 –Ī–į–Ľ–Ľ–ĺ–≤ (–≤ —Ā—Ä–Ķ–ī–Ĺ–Ķ–ľ 5,7±0,5 –Ī–į–Ľ–Ľ–į –ļ 5 —Ā—É—ā).
–ö –ļ–ĺ–Ĺ—Ü—É 1-–Ļ –Ĺ–Ķ–ī. –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –Ņ–Ķ—Ä–ł–ĺ–ī–į –≤ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ –Ņ–ĺ—Ä–ĺ–≥ –Ī–ĺ–Ľ–Ķ–≤–ĺ–Ļ —á—É–≤—Ā—ā–≤–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ—Ā—ā–ł –≤ —Ä–į–Ĺ–Ķ –ļ—É–Ľ—Ć—ā–ł –Ě–ö –ī–ĺ—Ā—ā–ł–≥ —É—Ä–ĺ–≤–Ĺ—Ź «–Ķ–ī–≤–į –ĺ—Č—É—ā–ł–ľ—č—Ö –Ī–ĺ–Ľ–Ķ–Ļ» (1,5±0,1 –Ī–į–Ľ–Ľ–į). –í –ļ–ĺ–Ĺ—ā—Ä–ĺ–Ľ—Ć–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ –≤ —ā–Ķ –∂–Ķ —Ā—Ä–ĺ–ļ–ł —Ā—Ä–Ķ–ī–Ĺ–ł–Ļ –Ņ–ĺ–ļ–į–∑–į—ā–Ķ–Ľ—Ć –Ņ–ĺ 10-–Ī–į–Ľ–Ľ—Ć–Ĺ–ĺ–Ļ —ą–ļ–į–Ľ–Ķ —Ā–ĺ—Ā—ā–į–≤–ł–Ľ 3,2±0,2 –Ī–į–Ľ–Ľ–į («—Ā–Ľ–į–Ī–į—Ź –Ī–ĺ–Ľ—Ć») (p<0,05). –ě–ļ–ĺ–Ĺ—á–į—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –ļ—É–Ņ–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ –Ī–ĺ–Ľ–Ķ–Ļ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤ –≥—Ä—É–Ņ–Ņ—č —Ā—Ä–į–≤–Ĺ–Ķ–Ĺ–ł—Ź –Ņ—Ä–ĺ–ł—Ā—Ö–ĺ–ī–ł–Ľ–ĺ –≤ —Ā—Ä–Ķ–ī–Ĺ–Ķ–ľ –ļ 16,5±0,6 —Ā—É—ā –ĺ—ā –Ĺ–į—á–į–Ľ–į –Ľ–Ķ—á–Ķ–Ĺ–ł—Ź (–ĺ—ā 10 –ī–ĺ 16 —Ā—É—ā), —á—ā–ĺ –∑–į–Ĺ—Ź–Ľ–ĺ –Ī–ĺ–Ľ–Ķ–Ķ –Ņ—Ä–ĺ–ī–ĺ–Ľ–∂–ł—ā–Ķ–Ľ—Ć–Ĺ–ĺ–Ķ –≤—Ä–Ķ–ľ—Ź, —á–Ķ–ľ –≤ –ĺ—Ā–Ĺ–ĺ–≤–Ĺ–ĺ–Ļ –≥—Ä—É–Ņ–Ņ–Ķ (–ĺ—ā 8 –ī–ĺ 13 —Ā—É—ā, –≤ —Ā—Ä–Ķ–ī–Ĺ–Ķ–ľ – 10,8±0,3 —Ā—É—ā).
–Ę–į–ļ–ł–ľ –ĺ–Ī—Ä–į–∑–ĺ–ľ, –Ņ—Ä–ĺ–≤–Ķ–ī–Ķ–Ĺ–Ĺ–ĺ–Ķ –ł—Ā—Ā–Ľ–Ķ–ī–ĺ–≤–į–Ĺ–ł–Ķ –Ņ–ĺ–ļ–į–∑–į–Ľ–ĺ –ĺ—á–Ķ–≤–ł–ī–Ĺ—č–Ķ –Ņ—Ä–Ķ–ł–ľ—É—Č–Ķ—Ā—ā–≤–į –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –į–Ĺ–į–Ľ—Ć–≥–Ķ–∑–ł–ł –Ņ—Ä–Ķ–Ņ–į—Ä–į—ā–ĺ–ľ –ó–į–Ľ–ī–ł–į—Ä –Ņ–ĺ —Ā—ā–į–Ĺ–ī–į—Ä—ā–Ĺ–ĺ–Ļ —Ā—Ö–Ķ–ľ–Ķ –≤ —Ä–į–Ĺ–Ĺ–Ķ–ľ –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–ľ –Ņ–Ķ—Ä–ł–ĺ–ī–Ķ —É –Ņ–į—Ü–ł–Ķ–Ĺ—ā–ĺ–≤, –Ņ–Ķ—Ä–Ķ–Ĺ–Ķ—Ā—ą–ł—Ö –≤—č—Ā–ĺ–ļ—É—é –į–ľ–Ņ—É—ā–į—Ü–ł—é –≤ —Ā–≤—Ź–∑–ł —Ā –ł—ą–Ķ–ľ–ł—á–Ķ—Ā–ļ–ĺ–Ļ –≥–į–Ĺ–≥—Ä–Ķ–Ĺ–ĺ–Ļ –Ě–ö. –ü—Ä–ł —ć—ā–ĺ–ľ —Ā—Ä–ĺ–ļ–ł –ļ—É–Ņ–ł—Ä–ĺ–≤–į–Ĺ–ł—Ź –Ņ–ĺ—Ā–Ľ–Ķ–ĺ–Ņ–Ķ—Ä–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–≥–ĺ –Ī–ĺ–Ľ–Ķ–≤–ĺ–≥–ĺ —Ā–ł–Ĺ–ī—Ä–ĺ–ľ–į —Ā–ĺ–ļ—Ä–į—ā–ł–Ľ–ł—Ā—Ć –≤ 1,5 —Ä–į–∑–į.
–õ–ł—ā–Ķ—Ä–į—ā—É—Ä–į
1. –°–į–≤–Ķ–Ľ—Ć–Ķ–≤ –í.–°., –ö–ĺ—ą–ļ–ł–Ĺ –í.–ú., –ö–į—Ä–į–Ľ–ļ–ł–Ĺ –ź.–í. –ü–į—ā–ĺ–≥–Ķ–Ĺ–Ķ–∑ –ł –ļ–ĺ–Ĺ—Ā–Ķ—Ä–≤–į—ā–ł–≤–Ĺ–ĺ–Ķ –Ľ–Ķ—á–Ķ–Ĺ–ł–Ķ —ā—Ź–∂–Ķ–Ľ—č—Ö —Ā—ā–į–ī–ł–Ļ –ĺ–Ī–Ľ–ł—ā–Ķ—Ä–ł—Ä—É—é—Č–Ķ–≥–ĺ –į—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ–∑–į –į—Ä—ā–Ķ—Ä–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ. –ú.: –ú–ė–ź, 2010. –°. 21–22.
2. TASC II // Working Group Inter-Society Consensus for the Management of Peripheral Arterial disease // Eur. J. Vasc. Endovasc. Surg. 2007. Vol. 33 (Suppl.1).
3. Chaturvedi N., Stevens L., Fuller J. Risk factors, ethnic differences and mortality associated with lower-extremity gangrene and amputation in diabetes. // The WHO Multinational Study of Vascular Disease in Diabetes // Diabetologia. 2001. Vol. 44 (2). –†. 65–71.
4. –ď–ĺ—Ā—ā–ł—Č–Ķ–≤ –í.–ö., –õ–ł–Ņ–į—ā–ĺ–≤ –ö.–í., –ź—Ā–į—ā—Ä—Ź–Ĺ –ź.–ď., –í–≤–Ķ–ī–Ķ–Ĺ—Ā–ļ–į—Ź –ě.–í. –ü—Ä–ĺ–≥–Ĺ–ĺ–∑–ł—Ä–ĺ–≤–į–Ĺ–ł–Ķ —Ä–ł—Ā–ļ–į –≥–Ĺ–ĺ–Ļ–Ĺ–ĺ-–Ĺ–Ķ–ļ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–ł—Ö –ĺ—Ā–Ľ–ĺ–∂–Ĺ–Ķ–Ĺ–ł–Ļ –į–ľ–Ņ—É—ā–į—Ü–ł–ĺ–Ĺ–Ĺ–ĺ–Ļ –ļ—É–Ľ—Ć—ā–ł –Ī–Ķ–ī—Ä–į. // –•–ł—Ä—É—Ä–≥–ł—Ź. –Ė—É—Ä–Ĺ–į–Ľ –ł–ľ. –Ě.–ė. –ü–ł—Ä–ĺ–≥–ĺ–≤–į. 2013. ‚ĄĖ 11. –°. 4-8.
5. –°—ā–Ķ–Ņ–į–Ĺ–ĺ–≤ –Ě.–ď. –ź–ľ–Ņ—É—ā–į—Ü–ł–ł –≥–ĺ–Ľ–Ķ–Ĺ–ł –ł –Ī–Ķ–ī—Ä–į (–ļ–Ľ–ł–Ĺ–ł—á–Ķ—Ā–ļ–ł–Ļ –ĺ–Ņ—č—ā) / –Ě. –Ě–ĺ–≤–≥–ĺ—Ä–ĺ–ī: –Ē–Ķ–ļ–ĺ–ľ, 2003. 212 —Ā.
6. –ź–Ī—č—ą–ĺ–≤ –Ě.–°., –ó–į–ļ–ł—Ä–ī–∂–į–Ķ–≤ –≠.–Ē. –Ď–ĺ–Ľ—Ć—ą–ł–Ķ –į–ľ–Ņ—É—ā–į—Ü–ł–ł —É –Ī–ĺ–Ľ—Ć–Ĺ—č—Ö —Ā –ĺ–ļ–ļ–Ľ—é–∑–ł–ĺ–Ĺ–Ĺ—č–ľ–ł –∑–į–Ī–ĺ–Ľ–Ķ–≤–į–Ĺ–ł—Ź–ľ–ł –į—Ä—ā–Ķ—Ä–ł–Ļ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ // –•–ł—Ä—É—Ä–≥–ł—Ź. 2005. ‚ĄĖ 12. –°. 59–64.
7. –ė—Ā–ľ–į–ł–Ľ–ĺ–≤ –Ě.–Ď., –í–Ķ—Ā–Ĺ–ł–Ĺ –ź.–í. –ź—ā–Ķ—Ä–ĺ—Ā–ļ–Ľ–Ķ—Ä–ĺ—ā–ł—á–Ķ—Ā–ļ–į—Ź –≥–į–Ĺ–≥—Ä–Ķ–Ĺ–į –ī–ł—Ā—ā–į–Ľ—Ć–Ĺ—č—Ö –ĺ—ā–ī–Ķ–Ľ–ĺ–≤ –Ĺ–ł–∂–Ĺ–ł—Ö –ļ–ĺ–Ĺ–Ķ—á–Ĺ–ĺ—Ā—ā–Ķ–Ļ – –≤—Ā–Ķ–≥–ī–į –Ľ–ł –Ĺ–Ķ–ĺ–Ī—Ö–ĺ–ī–ł–ľ–į –≤—č—Ā–ĺ–ļ–į—Ź –į–ľ–Ņ—É—ā–į—Ü–ł—Ź? // –•–ł—Ä—É—Ä–≥–ł—Ź. –Ė—É—Ä–Ĺ–į–Ľ –ł–ľ. –Ě.–ė. –ü–ł—Ä–ĺ–≥–ĺ–≤–į. 2008. ‚ĄĖ 9. –°. 51-55.
8. Campbell W.B., Marriott S., Eve R. Amputation for acute ischemia is associated with increased co morbidity and higher amputation level // Cardiovase Surg. 2003. Vol. 11 (2). –†. 121–123.
9. Perrot S., Krause D., Crozes P. Efficacy and tolerability of —Äaracetamol/tramadol (325 mg/37.5 mg) combination treatment compared with tramadol (50 mg) monotherapy in patients with subacute low back pain: a multicenter, randomized, double-blind, parallel-group, 10-day treatment study // Clin Ther. 2006. Oct. Vol. 28 (10).–†. 1592–606.
10. Edwards J.E., McQuay H.J., Moore R.A. Combination analgesic efficacy: individual patient data meta-analysis of single-dose oral tramadol plus acetaminophen in acute postoperative pain // J Pain Symptom Manage. 2002. Feb. Vol. 23 (2). –†. 121–130.
11. Jung Y.S., Kim D.K., Kim M.K. Onset of analgesia and analgesic efficacy of tramadol/acetaminophen and codeine/acetaminophen/ibuprofen in acute postoperative pain: a single-center, single-dose, randomized, active-controlled, parallel-group study in a dental surgery pain model // Clin. Ther. 2004. Jul. Vol. 26 (7). –†. 1037–1045.
12. Bourne M.H., Rosenthal N.R., Xiang J. Tramadol/acetaminophen tablets in the treatment of postsurgical orthopedic pain [published erratum appears in Am. J. Orthop. 2006. Sep; Vol. 35 (9). –†. 410] // Am. J. Orthop. 2005. Dec. Vol. 34 (12). –†. 592–597.
13. Smith A.B., Ravikumar T.S., Kamin M. Combination tramadol plus acetaminophen for postsurgical pain // Am. J. Surg. 2004. Apr. Vol. 187 (4). –†. 521–527.
14. Dhillon S. –ö–ĺ–ľ–Ī–ł–Ĺ–į—Ü–ł—Ź —ā—Ä–į–ľ–į–ī–ĺ–Ľ–į/–Ņ–į—Ä–į—Ü–Ķ—ā–į–ľ–ĺ–Ľ–į –≤ —ā–Ķ—Ä–į–Ņ–ł–ł —É–ľ–Ķ—Ä–Ķ–Ĺ–Ĺ–ĺ–Ļ –ł —Ā–ł–Ľ—Ć–Ĺ–ĺ–Ļ –Ī–ĺ–Ľ–ł (—Ä–Ķ—Ą–Ķ—Ä–į—ā–ł–≤–Ĺ—č–Ļ –Ņ–Ķ—Ä–Ķ–≤–ĺ–ī) // Manage pain. 2013, –Ĺ–ĺ—Ź–Ī—Ä—Ć. ‚ĄĖ 1. –°. 77.












