В настоящее время ЖКБ принято рассматривать с позиций липидного дистресс–синдрома Савельева (ЛДС) в виде калькулезного холестероза желчного пузыря (ЖП), а термины «калькулезный холестероз ЖП» и «ЖКБ» считаются синонимами одного и того же заболевания [1,4,12].
Любая морфологическая форма холестероза, включая бескаменную и полипозную, сопровождается нарушением моторно–эвакуаторной функции ЖП и/или несвоевременным (замедленным) поступлением желчи в кишечник [9,10,11]. Согласно Римским критериям II (1999), эти изменения являются основными признаками внепеченочных билиарных дисфункций (ВБД), включающих все заболевания, связанные с нарушениями моторики билиарного тракта вне зависимости от их этиологии (ВБД Е1 – дисфункции ЖП и ВБД Е2 – дисфункции сфинктера Одди) [19,23].
Различают первичные и вторичные ВБД. Первичные встречаются редко (10–15%) и связаны со снижением чувствительности рецепторного аппарата ЖП и сфинктеров желчных путей к нейрогуморальной стимуляции. Ограниченное количество функционирующих рецепторов может быть генетически детерминированным либо приобретенным вследствие различных воспалительных, дистрофических и метаболических расстройств [16,21].
Вторичные ВБД наблюдаются при психоэмоциональных перегрузках, стрессовых ситуациях, общих неврозах, гормональных расстройствах, при беременности, системных заболеваниях, диабете, гепатите, циррозе печени, а также при ЛДС Савельева вследствие инфильтрации эфирами холестерина стенки ЖП и сфинктеров внепеченочных желчных путей (холестероз), а также при воспалении ЖП [8,31].
Другие наиболее частые причины вторичных ВБД обусловлены различными хирургическими вмешательствами на органах желудочно–кишечного тракта: резекцией желудка и ваготомией, приводящих к ослаблению гормональной регуляции и гипотонии ЖП, еюностомией, холецистэктомией (ХЭ) и др. [3].
Известно, что удаление ЖП по поводу ЖКБ не избавляет больных от метаболических нарушений, в том числе от гепатоцитарной дисхолии, сохраняющейся и после операции [14]. Выпадение физиологической роли ЖП, а именно концентрация желчи в межпищеварительный период и выброс ее в двенадцатиперстную кишку во время еды, часто сопровождается нарушением пассажа желчи в кишечник и расстройством пищеварения [5].
Объяснения возникновения ВБД после операции ХЭ достаточно разноречивы: одни авторы считают, что после ХЭ (особенно в первые месяцы после операции) происходит временное усиление тонуса сфинктера Одди [14], другие, напротив, доказывают длительную недостаточность сфинктера Одди с непрерывным истечением желчи в просвет двенадцатиперстной кишки [3].
Изменение химического состава и объема желчи, хаотическое ее поступление в двенадцатиперстную кишку нарушают переваривание и всасывание жира и других веществ липидной природы, уменьшают бактерицидность дуоденального содержимого, что приводит к микробному обсеменению и нарушению моторики двенадцатиперстной кишки, развитию синдрома избыточного бактериального роста в кишечнике (особенно в подвздошной кишке), расстройству печеночно–кишечной циркуляции и снижению синтеза желчных кислот в печени [5]. Как следствие – синдром нарушенного пищеварения, симптомы которого часто трактуются, как постхолецистэктомический синдром (ПХС), ассоциирующийся хирургами в первую очередь с нераспознанными до операции или не устраненными во время ХЭ механическими препятствиями желчеоттоку (оставленными или возникшими вновь камнями в холедохе, стенозом фатерова сосочка и т.д.) [5,8].
В настоящее время термином «ПХС» принято обозначать только вторичную дисфункцию сфинктера Одди (Е2 по Римским критериям), обусловленную (при отсутствии органических изменений) нарушением его моторной функции, препятствующей нормальному оттоку желчи и панкреатического секрета в двенадцатиперстную кишку при отсутствии органических препятствий [23]. У 25–65% больных, перенесших ХЭ, сохраняются или через некоторое время возобновляются абдоминальные боли и диспептические расстройства, требующие коррекции. У большинства из них (58%) причиной жалоб являются функциональные, а у 42% – органические нарушения работы сфинктера Одди, из которых только 1,5% можно отнести к последствиям оперативного вмешательства. Важно, что лишь 0,5% больных с ПХС нуждаются в проведении повторного хирургического лечения [3,23].
К основным причинам патологических состояний у больных, перенесших ХЭ, относят функциональные расстройства сфинктера Одди (ВБД Е2) в результате потери функционирующего ЖП, реже – органические (стриктуры желчных протоков (6,5–20%), стенозы в области дуоденального сосочка (11–14%), нераспознанные или рецидивирующие камни общего желчного протока (5–20%), длинный пузырный проток, невринома в области рубца (0,1–1,9%); заболевания органов желудочно–кишечного тракта (синдром раздраженной кишки, язвенная болезнь желудка и двенадцатиперстной кишки и др.)) [13,16,26,35].
Диагностике механических препятствий желчеоттоку в двенадцатиперстную кишку при подготовке к операции ХЭ при ЖКБ всегда уделяется большое внимание [33]. По–иному обстоит дело с дооперационной верификацией ВБД. Отсутствие косвенных признаков функциональных нарушений сфинктера Одди в виде расширения холедоха при УЗ исследовании, повышения печеночных ферментов, болевых приступов и т.д. совсем не исключает наличия ВБД Е2, формирующихся задолго до поступления пациента на хирургическое лечение.
Цель исследования: оценка диагностических и лечебных возможностей гиосцина бутилбромида (Бускопан®) при желчно–каменной болезни, бескаменном холестерозе ЖП и внепеченочных билиарных дисфункциях.
Материал и методы исследования
В исследование включены 132 пациента, составивших две группы. В группе пациентов с ЖКБ (n=102) 68 человек (66%) были оперированы: 36 (35%) из них выполнялась лапароскопическая ХЭ (ЛХЭ), 32 (31%) – традиционная открытая ХЭ (ТХЭ), а 34 пациента (34%) отказались от хирургического лечения. 30 пациентов с верифицированным бескаменным холестерозом ЖП, клинически характеризовавшимся пузырными коликами, обследованы в качестве контрольной группы. У всех пациентов в анамнезе не было эпизодов острого холецистита, механической желтухи.
Функциональное состояние гепатобилиарной системы было изучено с помощью стандартной гепатобилисцинтиграфии (ГБСГ) у оперированных пациентов (n=68) до и через 12 месяцев после хирургического вмешательства, у неоперированных (n=64) – до и после консервативного лечения.
ГБСГ позволяет объективно оценивать наиболее важные с позиций желчекамнеобразования процессы: желчесинтетическую и желчеэкскреторную функции печени. Она основана на регистрации пассажа короткоживущих радионуклидов по билиарному тракту, проводилась на гамма–камере «Diakam» фирмы «Simens» (Германия) с обработкой данных на компьютере «Icon». Исследование проводилось натощак, в горизонтальном положении пациента после введения 3 мКм Тс–99м+бромезида внутривенно. Длительность исследования составила 60 минут. В качестве желчегонного завтрака пациенты принимали желтки куриных яиц через 30 минут от начала процедуры.
Нормальными показателями ГБСГ считалось время полувыведения (Т1/2) радиофармпрепарата (РФП) из печени менее 35 минут, Т1/2 из холедоха менее 50 минут, время поступления РФП в 12–перстную кишку – менее 40 минут. Признаком адекватного поступления РФП в кишечник считалось преобладание активности РФП в 12–перстной кишке по сравнению с таковой в холедохе к концу исследования.
По результатам стандартной ГБСГ больные были разделены на две группы. В первую группу вошли 59 пациентов со своевременным (не нарушенным) пассажем РФП по холедоху (время полувыведения РФП из общего желчного протока не превышало 50 мин.), из них 41 – больные с ЖКБ, а 18 – с бескаменным холестерозом ЖП. 2 группа была составлена из 73 пациентов с выявленными нарушениями пассажа РФП по холедоху, обусловленными нарушениями желчеоттока (время полувыведения РФП из общего желчного протока превышало 50 мин.). 61 их них были пациенты с ЖКБ, 12 – с бескаменным холестерозом ЖП.
Общепринятая методика ГБСГ с желчегонным завтраком не всегда позволяет конкретизировать характер функциональных изменений желчеоттока. Это объясняется тем, что после пищевой нагрузки вследствие раздражения I–клеток двенадцатиперстной кишки и интрамурального нервного сплетения увеличивается концентрация в кровотоке холецистокинина (ХК) [22,24]. Однако активность пищеварительных ферментов и чувствительность сфинктерного аппарата желчевыводящих путей к интестинальным гормонам вариабельна и на практике трудноопределима [2], а тонус интрамуральных нервных волокон зависит от физиологической активности органов верхних отделов пищеварительного тракта [38].
В этой связи для исключения возможных аббераций при радионуклидной диагностике ВБД часто применяется внутривенное введение гормона холецистокинина, но релаксирующий эффект этого препарата также зависит от состояния центральной нервной системы, гормонального фона пациента и нарушается при холестерозе ЖП и внепеченочных желчных путей, поскольку локализация рецепторов к холецистокинину совпадает с местами отложений эфиров холестерина в стенке пузыря и желчных протоков, что затрудняет точное определение дозы вводимого гормона [3,40].
Пациентам второй группы для уточнения характера нарушений желчеоттока по холедоху были выполнены ГБСГ с аминокислотным холекинетическим тестом, разработанным в нашей клинике (ГБСГ–АХТ, патент РФ №2166333) и ГБСГ с гиосцином бутилбромидом (Бускопан®–тест) (Берингер Ингельхайм, Германия).
В связи с тем, что ГБСГ–АХТ и ГБСГ – Бускопан®–тест являются новыми и малоизвестными методиками, остановимся подробнее на технических особенностях их проведения.
Исследование проводится натощак. Через 30 минут после введения РФП и начала исследования в периферическую вену вводится раствор аминокислот «Вамин–14» или «Фреамин», не содержащие глюкозы и электролитов. Последнее условие мы считаем весьма важным, так как возникающая при инфузии глюкозы гипергликемия полностью или частично ингибирует секрецию холецистокинина [20]. Доза препарата выбиралось из расчета 1,5–2 мл/кг массы тела (80–130 мл). Продолжительность инфузии составляла 5–7 минут, поскольку введение раствора аминокислот более 10 минут (независимо от дозы) не приводило к увеличению выброса эндогенного холецистокинина, а наоборот, снижало инкрецию гормона [28]. ВБД и причина замедленной экскреции радиофармпрепарата гепатоцитами оценивались на основании различий показателей стандартной ГБСГ и ГБСГ–АХТ (рис. 1).
В последнее время в нашей клинике для диагностики ВБД применяется оригинальная методика ГБСГ с использованием гиосцина бутилбромида (Бускопан®) – четвертичного аммониевого производного. Гиосцина бутилбромид – алкалоид, полученный из растения Duboisia. Его химически перерабатывают с помощью добавления бутиловой группы для получения четвертичной аммониевой структуры. Эта модификация формирует молекулу, которая по–прежнему обладает антихолинергическими свойствами. Но в отличие от третичных аммониевых соединений, четвертичные аммониевые соединения, такие как гиосцина бутилбромид, ограничивают системное поглощение и значительно уменьшают число побочных реакций. Гиосцина бутилбромид – антихолинергический препарат с высокой степенью сродства к мускариновым рецепторам, расположенным на клетках гладких мышц желудочно–кишечного тракта, который вызывает спазмолитический эффект. Кроме того, препарат связывается с никотиновыми рецепторами, что вызывает эффект блокировки нервных узлов.
Техническая сторона исследования мало отличается от вышеизложенного АХТ–теста. По окончании стандартной ГБСГ пациент вместо инфузии раствора аминокислот per os принимал 20 мг гиосцина бутилбромида. Через 20 минут выполнялись повторная запись и обработка данных (рис. 2, 3).
Таким образом, 37 пациентам с нарушениями, обусловленными нарушениями желчеоттока, была выполнена ГБСГ – АХТ (2А подгруппа), а 36 больным – ГБСГ – Бускопан®–тест (2Б подгруппа).
Лечение ВБД проводилось комплексно по разработанной в клинике методике [7,8,10].
Базовой была энтеросорбция отечественным сорбентом ФИШант–С® (ПентаМед, Россия), представляющим композицию биологически инертных компонентов (белое масло) и пребиотиков (пектин, агар–агар) в виде сложной капсулированной микроэмульсии. Удаление эндотоксинов из химуса (энтеросорбент ФИШант–С® обладает наибольшей сорбционной способностью по отношению к эндотоксину грамотрицательной микрофлоры по сравнению с рыночными энтеросорбентами) оказывает положительное влияние на течение многих метаболических процессов [7,11].
При верифицированных ВБД пациентам назначали прием спазмолитического средства на натуральной основе гиосцина бутилбромида (Бускопан®) по 20 мг/сут. в течение 2 месяцев. Оперированным пациентам (холецистэктомия при ЖКБ) лечение начинали на следующий день после ХЭ с приема Бускопана®, затем через 10 суток им предписывалась полная схема.
Растительный гепатопротекторный препарат гепабене® (Ратиофарм, Германия) обладает комбинированным действием: холеретический эффект обусловлен наличием в его составе экстракта плодов расторопши пятнистой, содержащих группу флавоидных соединений – силимарина и силибинина. Холекинетические свойства гепабене связаны с экстрактом дымянки аптечной, содержащим алкалоид фумарин.
Для нормализации микробиоценоза кишечника дополнительно к приему Бускопана®, ФИШант–С® и гепабене® использовался хилак–форте® (Ратиофарм, Германия) – стерильный концентрат продуктов жизнедеятельности микроорганизмов–синбионтов тонкой и толстой кишок, образующих молочную кислоту, аминокислоты, лактозу, короткоцепочечные жирные кислоты.
Исследования выполнены до операции ХЭ, через 12 месяцев после ХЭ и через 6 месяцев непрерывной комплексной терапии. Статистическая обработка данных проведена на персональном компьютере по стандартному пакету программ.
Результаты и их обсуждение
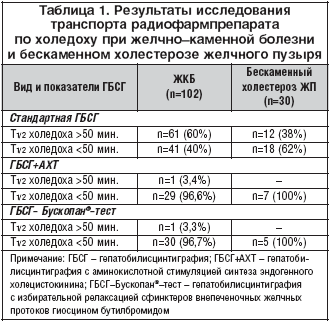
Всем пациентам была выполнена стандартная ГБСГ, которая явилась скрининговым исследованием для определения ВБД. Результаты приведены в таблице 1 и на рисунке 4. У 60% пациентов с ЖКБ и у 38% пациентов с бескаменным холестерозом ЖП время полувыведения РФП их холедоха достоверно превышало нормальные значения (45,7±6,1 мин.), у этих больных были заподозрены ВБД (Е2), для исключения органического характера нарушений транспорта РФП из общего желчного протока им были произведены ГБСГ – АХТ (n=37) и ГБСГ–Бускопан®–тест (n=36). По их результатам (табл.1) лишь у 2–х пациентов с ЖКБ (3,3%) были получены данные, свидетельствующие о нарушении транспорта РФП в двенадцатиперстную кишку. Эндоскопическая ретроградная панкреатохолангиография подтвердила механический характер ВБД (стеноз фатерова сосочка). У 59 пациентов с ЖКБ при ГБСГ в обеих модификациях были диагностированы функциональные нарушения сфинктера Одди, 47 из них в дальнейшем были оперированы (26 произведена лапароскопическая холецистэктомия, 21 – традиционная), а 12 пациентов отказались от хирургического лечения.
Необходимо отметить, что показатели ГБСГ–АХТ и технически более простого и легковоспроизводимого ГБСГ–Бускопан®–теста достоверно не различались между собой, что свидетельствует о бОльшем информационном потенциале последнего.
Практический интерес представляла сравнительная оценка результатов радионуклидной ГБСГ в традиционном и модифицированных вариантах у пациентов с ВБД и ЖКБ (n=61) и ВБД и бескаменным холестерозом ЖП (n=12). Она позволила решить несколько важных задач: определить особенности билидинамики при различных формах холестероза, оценить взаимосвязь внепеченочных билиарных расстройств типа Е2 и метаболических функций печени, изучить влияние длительности желчекамненосительства на процессы формирования функциональных нарушений сфинктера Одди.
Известно, что ведущими факторами нарушения желчесекреторной и желчеэкскреторной функций гепатоцитов являются колебания гидростатического давления в желчных путях [13]. Оценка этих функций при ЖКБ было проведена в специальной части исследования раздельно у больных со своевременным (1 группа) и нарушенным пассажем РФП по холедоху (2 группа) в сравнении с пациентами 3 группы (бескаменный холестероз ЖП с нарушением транспорта РФП по холедоху), данные приведены в таблице 2.
Желчесекреторная функция гепатоцитов анализирована по трем категориям: нормальная секреция желчи (Тmax печени <10 мин.), снижение до 50% от нормы (Тmax печени 10–15 мин.), выраженные нарушения (Тmax печени >15 мин.). У 58% пациентов с ЖКБ с нормальным транспортом РФП по холедоху синтез желчи гепатоцитами не был изменен, умеренно снижен у 25% обследованных, а выраженное снижение установлено у 17% пациентов (рис. 5).
В ходе исследования было установлено, что нарушения транспорта желчи во холедоху в одинаковой степени влияют на изменения метаболических функций гепатоцитов. Так, лишь у 26 и 28% пациентов 2–й и 3–й групп, соответственно, было установлено нормальное время накопления РФП в печени, умеренные нарушения выявлены у 39 и 40%, а тяжелые – у 35 и 32% соответственно группам. Аналогичные результаты были получены при изучении желчеэкскреторной функции гепатоцитов (рис. 6).
Таким образом, конкременты в ЖП не влияют на снижение синтеза желчи гепатоцитами. Эти нарушения формируются на более ранних стадиях желчекамнеобразования – при бескаменном холестерозе ЖП, который справедливо считается «предстадией» ЖКБ [8].
У половины пациентов с нормальным пассажем желчи по холедоху экскреция РФП гепатоцитами была своевременной. Напротив, у 75% больных с дисфункцией сфинктера Одди (2 и 3 группы) отмечалось нарушение желчевыделительной функции печени.
При изучении взаимосвязи длительности заболевания с выявленными нарушениями функции печени было установлено следующее. У пациентов с нормальным пассажем желчи по холедоху снижение желчесекреторной функции гепатоцитов было одинаковым (32–34%) при любой длительности заболевания; напротив, у пациентов с дисфункцией сфинктера Одди (2 и 3 группы) нарушение функций гепатоцитов наиболее часто (более 50%) наблюдались при длительности заболевания свыше 5 лет, реже – у пациентов с длительностью до 5 лет (27–31%) (рис. 7).
При исследовании желчеоттока по долевым и внепеченочным протокам были выявлены два вида нарушения. На основании анализа сцинтиграфических кривых и визуализации протоков в виде широкой полосы сцинтиляций задержка РФП во внутрипеченочных желчных протоках была установлена у 26 пациентов только с замедленным пассажем РФП по холедоху в равных пропорциях при калькулезном и бескаменном холестерозе ЖП.
Замедленное опорожнение долевых желчных протоков можно объяснить дискоординацией сфинктера Мирризи, с одной стороны, с другой – нарушением экскреторной функции гепатоцитов. Детальный анализ результатов ГБСГ показал, что при задержке РФП во внутрипеченочных желчных протоках снижение секреторной активности гепатоцитов отмечается значительно чаще. Это позволяет подтвердить негативную роль дискинезии сфинктера Мирризи в формировании нарушений метаболических функций печени при холестерозе ЖП. В связи с тем, что эти изменения установлены лишь при нарушении транспорта РФП по холедоху (т.е. при дискинезии сфинктера Одди), можно вполне обоснованно утверждать о сочетанном нарушении функций различных сфинктеров внепеченочных желчных протоков при холестерозе ЖП (рис. 8).
Как было отмечено выше, у 72 пациентов с калькулезным холестерозом ЖП при стандартной ГБСГ было выявлено замедление пассажа РФП по холедоху, что явилось поводом для проведения повторных ГБСГ–АХТ и ГБСГ–Бускопан®–тест. Результаты приведены в таблице 2.
Анализ данных радионуклидной гепатобилисцинтиграфии позволяет утверждать, что ГБСГ–тесты обладают различными точками приложения. Так, уменьшение времени полувыведения РФП из холедоха при ГБСГ–АХТ до нормальных значений необходимо расценивать, как результат ликвидации нейрогенного спазма сфинктерного аппарата под действием стимулированного эндогенного холецистокинина вследствие устранения влияния интестинального пейсмекера на сфинктер Одди. Это сопровождалось ускоренным выведением РФП из печени, что может быть связано с нормализацией давления желчи во внутрипеченочных желчных протоках на фоне восстановления функции сфинктера Мирризи. При этом время максимального накопления РФП в печени не изменилось, т.е. желчесинтетическая функция гепатоцитов осталась прежней. Это свидетельствует о том, что аминокислотный холекинетический тест не обладает холеретическим эффектом, что подчеркивает его физиологичность, важную для оценки характера нарушений желчеоттока при гепатобилиарной патологии.
Необходимо учитывать, что функционирование сфинктера Одди находится под контролем собственных водителей ритма, расположенных в проксимальном отделе сфинктера, осуществляющих фазовую и перистальтическую активность. Авторы объясняют болевой синдром после ХЭ именно дисфункцией сфинктера Одди [6,18,26,32,34,36,39].При этом было доказано, что если до операции ХЭ при ЖКБ инъекции холецистокинина снимали спазм сфинктера Одди (т.е. сохранялась его функциональная активность), то через 6 месяцев после хирургического лечения реакция сфинктера Одди на такие же дозы гормона была резко снижена [17,25,27,30]. Это означает, что при обследовании пациентов после ХЭ на предмет ВБД необходимо использовать альтернативные (не «холецистокининовые») способы воздействия на сфинктеры внепеченочных желчных путей. В настоящее время этой цели позволяет достичь применение ГБСГ–Бускопан®–теста.
При проведении ГБСГ Бускопан®–теста релаксирущее действие осуществляется не только на сфинктерный аппарат внепеченочных желчных путей, но и на моторику 12–перстной кишки. Это, в частности, было показано при изучении гормонального ответа сфинктера Одди после операции холецистэктомии: даже через 1 год после вмешательства моторика 12–ти перстной кишки была нарушена, установлено снижение на 60% реакции сфинктера Одди на инъекцию холецистокинина и на 175% в ответ на пищевую нагрузку [43]. Авторы считают, что после удаления ЖП нарушается не только синтез холецистокинина, но и рецепторная активность к нему 12–перстной кишки. В этой связи при ЖКБ патогенетически показано воздействие на моторику 12–перстной кишки как в диагностических, так и в лечебных целях.
Детальный анализ кривых выведения РФП из холедоха у пациентов с нарушенным транспортом РФП по холедоху позволил установить, что период быстрого выведения РФП во время введения «Вамина–14» у части больных сменялся прекращением снижения (26% случаев) или повышением «активности» в проекции холедоха (17%).
Это было расценено в виде парадоксальной реакции папиллярных мышц сфинктера Одди в ответ на холецистокининовую стимуляцию – развитие спазма вместо периода релаксации. Такая реакция может быть обусловлена инактивацией «релаксирующих» рецепторов к холецистокинину, расположенных в подслизистом слое Фатерова соска, где преимущественно скапливаются эфиры холестерина в виде «пенистых клеток» при холестерозе внепеченочных желчных путей, и активацией «сокращающих» рецепторов, локализованных непосредственно в папиллярных мышцах [27,29].
Для изучения взаимосвязи вида дисфункции сфинктера Одди (нейрогенный гипертонус или парадоксальный спазм) с морфологической формой холестероза были анализированы результаты ГБСГ с АХТ у больных калькулезным (2 группа) и бескаменным (3 группа) холестерозом ЖП (рис. 9).
Частота регистрации вышеуказанных видов дисфункции сфинктера Одди при ЖКБ и бескаменном холестерозе ЖП достоверно не различались.
Отложения эфиров холестерина, по имеющимся данным, локализуются преимущественно в подслизистом слое билиарного тракта, там же расположены релаксирующие рецепторы к холецистокинину [2,37]. В этой связи парадоксальный спазм можно вполне обоснованно считать подтверждением липидной инфильтрации Фатерова соска, то есть его холестероза.
У 45 пациентов (76%) 1–й группы, у 16 пациентов (26%) 2–й группы и у 6 пациентов (58%) 3–й группы при стандартной ГБСГ выявлена нормальная накопительная функция ЖП (рис. 10). При ГБСГ с АХТ частота «визуализации» желчного пузыря увеличивалась в два раза по сравнению с традиционной методикой (52 и 38%, соответственно группам), кроме того, обнаружено увеличение сократимости желчного пузыря на 51–60% от исходных значений.
Основной причиной нарушенного накопления РФП в ЖП при проходимости пузырного протока считается гипертонус сфинктера Люткенса [16]. Для изучения взаимосвязи дисфункции сфинктеров Одди и Люткенса проведен анализ зависимости накопительной и сократительной функции желчного пузыря от состояния транспорта желчи по холедоху. У пациентов с функциональными нарушениями оттока желчи по холедоху (2–я и 3–я группы) чаще определялись нарушения сократительной функции ЖП по сравнению с пациентами с нормальным желчеоттоком (табл. 2, рис. 11). Их средние значения достоверно не различались между собой. Это свидетельствует о том, что основной причиной нарушения моторно–эвакуаторной функции ЖП являются не конкременты, а липидная инфильтрация пузырной стенки.
Установленное в результате исследования сочетанное изменение функций сфинктеров Одди и Мирризи и Люткенса свидетельствует об общем происхождении этих нарушений. Для холестероза ЖП характерно значительное преобладание парадоксального спазма сфинктера Одди, это позволяет вполне обоснованно считать, что функциональные нарушения желчеоттока при холестерозе ЖП в том числе и ЖКБ, как одной из его форм, обусловлены холестерозом желчевыводящих путей, в частности, сфинктера Одди. Одинаковая частота дисфункции сфинктерного аппарата внепеченочных желчных путей при ЖКБ и бескаменном холестерозе ЖП значительно уменьшает роль механического фактора (травму сфинктеров мигрирующими конкрементами) в генезе функциональных нарушений желчеоттока.
Как было сказано выше, 68 пациентов с ЖКБ были оперированы, 36 из них произведена лапароскопическая ХЭ (ЛХЭ), 32 – традиционная «открытая» ХЭ (ТХЭ). Через 12 месяцев после операции части больных (выборка обусловлена верифицированными до хирургического вмешательства ВБД) повторно произведена стандартная ГБСГ (табл. 3). Все параметры, характеризующие синтез желчи и ее транспорт по холедоху, практически не изменились и достоверно превышали значения нормы (р<0,05).
Это позволило сделать вывод о том, что удаление ЖП любым из существующих сегодня в хирургии вариантов не устраняет нарушения метаболических функций печени и транспорт желчи по внепеченочным желчным путям, т.е. сохраняются ВБД, требующие медикаментозной коррекции.
Для устранения подобных изменений 90 пациентам после холецистэктомии, а также 11 пациентам с ЖКБ, отказавшимся от хирургического лечения (группа контроля), проведена консервативная терапия по разработанному в клинике факультетской хирургии РГМУ методу в рамках стратегии лечения ЛДС Савельева [7,8].
При контрольных исследованиях, сделанных через 6 месяцев непрерывного лечения (табл. 3), установлено достоверное улучшение функций печени, нормализовался транспорт желчи по холедоху. Исключение составили 16 пациентов (14 (22%) из группы оперированных больных и 2 (18%) из числа отказавшихся от операции), у которых 6–месячная терапия не улучшила исходные показатели. Для достижения искомого эффекта этим пациентам потребовалось продолжение терапии до 12 месяцев.
Таким образом, для дехолестеринизации сфинктеров внепеченочных желчных путей и нормального поступления желчи в 12–перстную кишку 22% пациентов после операции холецистэктомии необходима длительная (более 1 года) непрерывная этиопатогенетическая терапия.
В виде специальной задачи в данном исследовании была изучена необходимость применения Бускопана® при лечении бескаменного холестероза желчного пузыря, так как единого мнения по этому вопросу до сих пор нет, а имеющиеся данные разноречивы и не подкреплены фактическими доказательствами. С этой целью были обследованы сопоставимые по всем параметрам две группы пациентов с бескаменной пузырной коликой (холестероз ЖП).
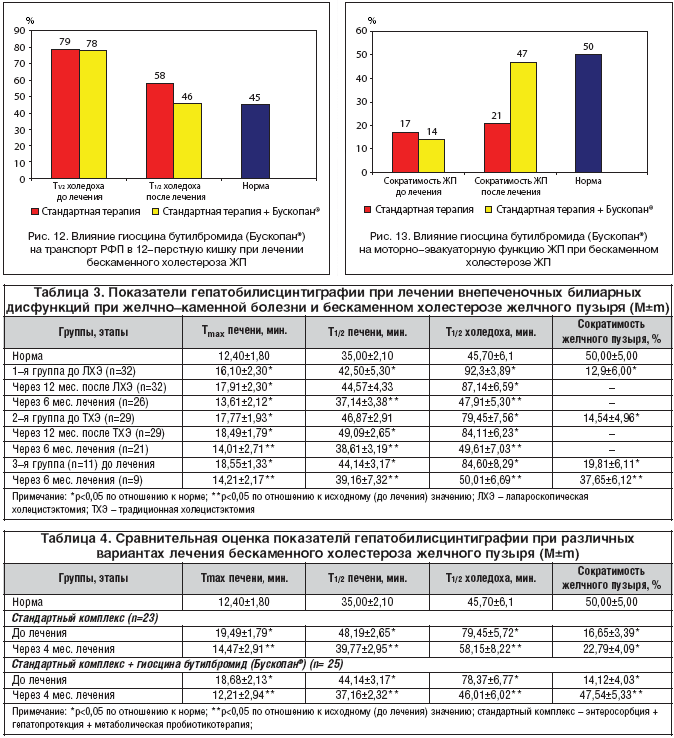
Пациентам одной из групп (n=23) проводилась стандартная комплексная терапия, в лечение другой (n=25) был включен гиосцина бутилбромид (Бускопан®) в стандартной суточной дозе. Исходные и контрольные результаты ГБСГ приведены в таблице 4 и иллюстрированы на рисунках 12 и 13.
При анализе данных видно, что имеются достоверные различия по двум показателям – времени транспорта РФП по холедоху и моторно–эвакуаторной функции ЖП. При стандартной терапии поступление РФП в 12–ти перстную кишку значительно улучшилось по сравнению с исходными значениями, но не достигло нормальных значений (p>0,05). Моторная функция ЖП также улучшилась. При включении в комплекс лечения избирательного спазмолитического средства направленного действия на натуральной основе Бускопан® отмечена нормализация вышеизложенных показателей транспорта желчи и эвакуаторной функции ЖП.
Выводы
1. ВБД при желчно–каменной болезни и бескаменном холестерозе ЖП обусловлены поражением всех сфинктеров внепеченочных желчных путей. Нарушения транспорта желчи в 12–ти перстную кишку, связанные с парадоксальным спазмом сфинктера Одди, существенно ухудшают метаболические функции гепатоцитов и пищеварение в целом.
2. Для диагностики внепеченочных билиарных дисфункций необходимо применять радионуклидную гепатобилисцинтиграфию с аминокислотным либо Бускопан®–тестами.
3. Операция холецистэктомии при ЖКБ не восстанавливает нарушения функций печени и не устраняет внепеченочные билиарные дисфункции.
4. Длительная консервативная терапия внепеченочных билиарных дисфункций комплексом, включающим энтеросорбент ФИШант–С®, растительный гепатопротектор гепабене®, метаболический пребиотик хилак–форте® и спазмолитическое средство направленного действия на натуральной основе Бускопан®, устраняет нарушение синтеза и транспорта желчи при желчно–каменной болезни, восстанавливает моторно–эвакуаторную деятельность желчного пузыря при бескаменном холестерозе.








Литература
1. Беглярова С.В. // Нарушения функции печени при липидном дистресс–синдроме//. Дисс. на соискание ученой степении кандидата медицинских наук. М.,2000.
2. Высоцкая Р.А. // Простагландины и гастроинтестинальные гормоны при хронических заболеваниях печени // дисс. докт. биол. наук М. 1992, 340 с.
3. Гальперин Э.И., Волкова Н.В. // Заболевания желчных путей после холецистэктомии.// М. Медицина 1988. 272 с.
4. Думпе Л.Э. // Инструментальная и радионуклидная диагностика поражений органов пищеварения при липидном дистресс–синдроме. // Дисс. на соискание ученой степении кандидата медицинских наук. М.,2002.
5. Каретерс Д.М. Мальабсорбция: В кн. Хендерсон Д.М. «Патофизиология органов пищеварения». М., 1997.
6. И.В.Маев, Е.С.Вьючнова, Е.Г.Лебедева. Коррекция проявлений холестаза у больных с калькулезным холециститом, перенесших холецистэктомию. // Практикующий врач »» №1 2006, Специальный выпуск, стр. 29
7. Петухов В.А. // Липидный дистресс–синдром. Под ред. В.С.Савельева, М., МАКС ПРЕСС, 256 с.
8. В.С.Савельев, В.А.Петухов, Б.В.Болдин // Холестероз желчного пузяря. М., ВЕДИ, 2002, 176 с.
9. Савельев В.С. // Липидный дистресс–синдром в хирургии. // Материалы 8–ой открытой сессии РАМН, М., с 56–57.
10. Савельев В.С. // Липидный дистресс–синдром в хирургии.// Материалы научн. практ. конф., посвященной 200 – летию ВМА. – С.–П. 1998.
11. Савельев В.С., Яблоков Е.Г., Петухов В.А. // Липидный дистресс–синдром в хирургии.// Бюллетень экспериментальной биологии и медицины. – 1999.–т.127.– №6.–с.604–611.
12. Тугдумов Б.В. // Результаты хирургической коррекции дислипопротеидемии при липидном дистресс–синдроме.// Дисс. на соискание ученой степении кандидата медицинских наук. М., 1999.
13. Хендерсон Д.М. Патофизиология органов пищеварения. М., 1997.
14. Bar–Meir S, Halpern Z,Barden E, et all. Frequency of papillary dysfunction among cholecystectomized patients. Hepatology 1984;4:328–30.
15. Basso L., McCollum P.T., Darling M.R. et al. A descriptive study of pregnant women with gallstones. Relation to dietary and social habits, education, physical activity, height and weight // Eur. J. Epidemiol. – 1992. – Vol. 8. – P. 629–633.
16. Bechar J., Biancani P. // Effect of cholecystokinin and the octapeptid of cholecystokinin on the feline sphincter of Оddi and gallbladder // J.Clin. Invest. 1980 vol. 66 p. 1231–9.
17. Behar J, Corazziari E, Guelrud M. Functional gallbladder and sphincter of oddi disorders. // Gastroenterology. 2006 Apr; 130(5): 1498–509.
18. Becker JM. Physiology of motor function of the sphincter of Oddi. // Surg Clin North Am. 1993 Dec;73(6):1291–309.
19. Corazziarei E., Shaffer E., Hogan W. et al // Functional disorders of the biliary tract and pancreas //Gut. 1999 Vol 45(Suppl 2) p. 1148–1154/
20. De Boer SY, Masclee AA, Lam WF, Jansen JB, Lamers CB // Effect of intravenous glucose on intravenous amino acid–induced gallbladder contraction and CCK secretion. //Dig Dis Sci 1994 Feb;39(2): p. 268–274.
21. Den Hertig A., Van den Akker J. // Modification of a1–receptor–operated channels in smooth muscle cells of guinea–pig taenia caeci. // Eur. J. Pharmacol. 1987; 138: 367–374.
22. Grasing–K; Freedholm–D; Murphy–MG; Swigar–M; Russer–T; Nosher–J; Lin–J; Frame–V; Clarke–L; Seibold–JR // Selective blockade of cholecystokinin type B receptors with L–365,260 does not impair gallbladder contraction in normal humans. // Am–J–Gastroenterol. 1996 Mar; 91(3): p. 569–573.
23. Drossman DA. The functional gastrointestinal disorders and the Rome II process. Gut 1999;45(suppl. II):1–5.
24. Houda R., Tooli J., Dodds W.J. // Effect of enteric hormons on sphincter of Oddi and gastrointestinal myoelectric activity in fasted conscious opossums // Gastroenterol. 1983 vol. 84 p. 1–9.
25. Madacsy L, Fejes R, Kurucsai G. Characterization of functional biliary pain and dyspeptic symptoms in patients with sphincter of Oddi dysfunction: effect of papillotomy. // World J Gastroenterol. 2006 Nov 14;12(42):6850–6.
26. Scott GW, Smallwood RE. Rowlands S. Flow through the bile duct after cholecystectomy. Surg Gynecol Obstet. 1975 Jun;140(6):912–8.
27. Grace PA, Pitt HA. Cholecystectomy alters the hormonal response of the sphincter of Oddi. // Surgery. 1987 Aug;102(2):186–94.
28. Kalfarentzos F, Vagenas C, Michail A, Vasilakos P, Markoy S, Kordossis T, Androulakis J // Gallbladder contraction after administration of intravenous amino acids and long–chain triacylglycerols in humans. // Nutrition 1991 Sep;7(5): p. 347–349.
29. Krishnamurthy–S; Krishnamurthy–GT // Cholecystokinin and morphine pharmacological intervention during 99mTc–HIDA cholescintigraphy: a rational approach. // Semin–Nucl–Med. 1996 Jan; 26(1): p.16–24.
30. Luman W, Williams AJ, Pryde A. Influence of cholecystectomy on sphincter of Oddi motility. // Gut. 1997 Sep;41(3):371–4.
31. Naruse S, Kitagava M, Ishiguro H, et al. Chronic pancreatitis: Overview of medical aspects. Pancreas 1998;16:323–28.
32. Nils G., Kock, M.D., Jan Kewenter. The Influence of the Motor Activity of the Duodenum on the Pressure in the Common Bile Duct. //
33. Sherman S, Troiano FP, Hawes RH, et al. Frequency of abnormal of sphincter Oddi manometry compared with the clinical suspicion of sphincter Oddi dysfunction. Am J Gastroenterol 1991;86:586–90.
34. Sonoda Y, Dong M, Konomi H. Role of duodenum on sphincter of Oddi motility in conscious dogs. // Dig Dis Sci. 2003 Sep;48(9):1693–700.
35. Sostre–S; Kalloo–AN; Spiegler–EJ; Camargo–EE; Wagner–HN Jr // A noninvasive test of sphincter of Oddi dysfunction in postcholecystectomy patients: the scintigraphic score // J–Nucl–Med. 1992 Jun; 33(6): p. 1216–1222.
36. Tanaka M. Advances in research and clinical practice in motor disorders of the sphincter of Oddi. // J Hepatobiliary Pancreat Surg. 2002;9(5):564–8.
37. Toouli J. // Sphincter of Oddi motility // Br. J. Surg. 1984 vol. 71 p. 251–256.
38. Weechsler–JG. // Bedeutung der Gallenblase in der Regulation des duodenogastralen Refluxes // Z–Gastroenterol. 1987 Aug. 25 Suppl 3: p. 15–21.
39. Zhang XM, Dong L, Liu LN. Changes of gastrointestinal myoelectric activity and bile acid pool size after cholecystectomy in guinea pigs. // World J Gastroenterol. 2005 Jun 28;11(24):3665–70.
40. Wood JD, Alpers DH, Andrews PLR. Fundamentals of neurogastroenterology. Gut 1999;45(suppl. II):6–16.












