Таким образом, несмотря на различные организационные подходы и используемые хирургические вмешательства, для медицинских центров, оказывающих специализированную флебологическую помощь по разным системам медицинского страхования и на платной основе, сохраняет свою актуальность быстрая медико–социальная реабилитация. Многочисленные исследования доказывают, что скорость последней как раз и определяется частотой послеоперационных осложнений, которая находится в обратной пропорции от стадии болезни. Таким образом, пациенты с ВБНК С6 по СЕАР (открытая трофическая язва) имеют больший риск послеоперационных осложнений в сравнении с больными с С5 (закрытая язва). Та же закономерность характерна для групп пациентов с С3 (хронический венозный отек) и С2 (только варикозный синдром).
Таким образом, одной из главных задач врача, проводящего подготовку пациента с ВБВНК к хирургическому вмешательству, должно быть снижение класса хронического заболевания вен (ХЗВ), а также адаптация венозной и лимфатической систем к предстоящей операционной травме.
Актуальность предоперационной подготовки подтверждают результаты многочисленных эпидемиологических исследований, согласно которым более половины российских пациентов на момент хирургического вмешательства имеют декомпенсированные и осложненные формы варикозной болезни. Хирургический «героизм» в таких условиях оборачивается для больного гнойно–некротическими осложнениями, лимфореей, косметическими и функциональными потерями.
Очевидно, что целенаправленная, патогенетически обоснованная флеботропная терапия позволяет не только снизить выраженность хронической венозной недостаточности (ХВН), но и сократить частоту послеоперационных осложнений.
Справедливость этого положения подтверждает ряд клинических исследований. Одно из первых исследований, посвященных периоперационной флеботропной терапии, проведено в Чешской Республике [2], когда в 15 медицинских центрах 181 пациенту в возрасте от 18 до 60 лет был выполнен стриппинг большой подкожной вены бедра на одной нижней конечности. После рандомизации 92 пациента за 14 дней до и в течение 14 дней после флебэктомии получали микронизированную очищенную фракцию флавоноидов (МОФФ) в суточной дозе 1000 мг (1 таблетка х 2 р./сут.). 89 пациентов составили контрольную группу. На 4–е сут. послеоперационного периода в основной группе 96% пациентов не нуждались в приеме анальгетиков, в то время как в группе контроля 12,5% больных продолжали получать обезболивающие препараты. Кроме того, у пациентов, получавших МОФФ (Детралекс), на 7–е сут. послеоперационного периода площадь кровоизлияний (экхимозов) в зоне хирургического вмешательства была достоверно меньше (110 см2 против 131 см2, p<0,001), а интегральный показатель качества жизни, определяемый с помощью болезнь–специфического опросника CIVIQ, оказался на 18% выше (62% в основной группе против 44% – в контрольной группе) [2,3].
В 2006 г. в Российской Федерации было проведено схожее по дизайну мультицентровое рандомизированное исследование, получившее название ДЕФАНС (ДЕтралекс – оценка эФфективности и безопАсНоСти при комбинированной флебэктомии). В исследование ДЕФАНС вошли 245 женщин в возрасте от 25 до 60 лет, перенесших стриппинг большой подкожной вены на бедре по поводу варикозной болезни одной из нижних конечностей, соответствующей клиническому классу С2S (S – наличие субъективных жалоб) международной классификации СЕАР [4,5].
200 пациенток, рандомизированных в основную группу, получали МОФФ (500 мг х 2 р./сут.) за 2 нед. до операции и в течение 4–х нед. после нее. В контрольной группе (n=45) флеботропные средства не использовали вообще.
Сравнение течения послеоперационного периода у пациенток основной и контрольной групп осуществляли с помощью веноспецифического опросника CIVIQ, визуальных аналоговых шкал для субъективных жалоб, а также специально разработанной балльной оценки площади послеоперационных кровоизлияний.
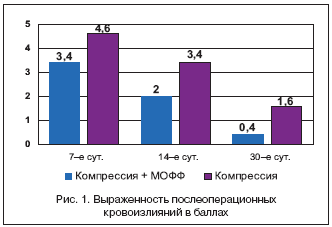
При обработке результатов исследования оказалось, что при схожих показателях качества жизни у всех пациенток, включенных в исследование, площадь послеоперационных кровоизлияний у получавших МОФФ на 7,14 и 30–е сут. послеоперационного периода была достоверно меньше (p<0,05). Максимальные различия, составившие 70% в пользу основной группы, были зафиксированы на 30–е сут. после операции (рис. 1).
Еще одним важным показателем, характеризующим комфортность послеоперационного периода, служит болевой синдром. На 7–е сут. после флебэктомии его интенсивность у пациентов основной группы составила 2,9±0,2 балла против 3,5±0,1 балла в группе контроля (p<0,05). При дальнейшем наблюдении – к 14–м сут. – болевой синдром постепенно уменьшался и к концу наблюдения практически полностью исчез.
Интересно, что пациенты, получавшие МОФФ, демонстрировали более высокую толерантность к статическим нагрузкам, меньшую выраженность послеоперационного отека и дискомфорта в оперированной конечности.
Исследование ДЕФАНС подтвердило, что периоперационная флеботропная терапия позволяет снизить выраженность нежелательных последствий операции и увеличить скорость медико–социальной реабилитации пациентов, перенесших флебэктомию.
А.А. Шульц и соавт. [6] обобщили результаты хирургического лечения 65 пациентов с варикозной болезнью, у которых были отмечены наличие продолжительного рефлюкса по стволу большой подкожной вены и выраженный варикозный синдром. Авторы разделили больных на 3 группы: контрольная (n=20), в которой флебопротекторы не назначались; 1–ая основная группа (n=22), где в периоперационном периоде была назначена МОФФ в стандартной дозировке (1000 мг/сут.) и 2–ая основная группа (n=23), пациенты которой в послеоперационном периоде первые 7 сут. получали 3000 мг/сут., а затем – 1000 мг/сут. МОФФ [6].
В качестве референтных методов были использованы визуальные аналоговые шкалы, болезнь–специфичный опросник CIVIQ, супрамалеолярная окружность голени, а также оценка эхогенности подкожно–жировой клетчатки на голени.
После обработки результатов у пациентов 1–ой и 2–ой основных групп были зафиксированы значимые позитивные отличия от больных из группы контроля. При этом отмечено, что респонденты, получавшие «ударную» дозу МОФФ, невзирая на значимо большую операционную травму, уже к 5–м сут. не испытывали дискомфорта, ограничивающего их бытовую и социальную активность. В этой же группе по данным УЗИ были зафиксированы минимальные отек и воспалительные изменения в подкожно–жировой клетчатке.
Авторы сделали вывод о полезности назначения МОФФ в послеоперационном периоде, подчеркивая, что в стандартной дозировке (1000 мг/сут.) МОФФ уменьшает нежелательные проявления послеоперационного периода, но, тем не менее, достоверно не влияет на сроки реабилитации пациентов. В то же время, прием «ударной» суточной дозы (3000 мг) МОФФ в течение 7 дней значимо улучшает течение послеоперационного периода и обеспечивает быстрейшую реабилитацию.
Следует отметить, что флеботропная терапия в пред– и послеоперационном периоде постепенно становится modus operandi в практике специализированных европейских флебологических клиник.
Так, Р. Pitalluga – основоположник нового направления в хирургическом лечении варикозной болезни, получившего название ASVAL (Ambulatory Selective Varicose vein Ablation under Local anesthesia), рекомендует назначать МОФФ в течение 3–6 мес. послеоперационного периода. Р. Pitalluga считает, что благодаря ряду специфических и плейотропных терапевтических эффектов МОФФ не только нивелирует последствия операционной травмы, но и благодаря доказанному венотонизирующему эффекту способствует уменьшению диаметра и восстановлению дееспособности сохраненных в результате ASVAL поверхностных вен [7].
Из клинической фармакологии известно понятие «синергизм лекарственных веществ» (от греч. synergia – сотрудничество, содействие), подразумевающее одновременное действие в одном направлении двух или нескольких веществ, обеспечивающее более высокий общий эффект, чем действие каждого из них в отдельности. В последние годы понятие синергизм стали использовать по отношению к разнородным лечебным методикам.
Так, F. Allaert и соавт. [8] на примере 2862 пациентов с ВБВНК С1S–С3S клинических классов по CEAP, пролеченных в 2 флебологических центрах Франции, продемонстрировали выраженный синергизм флебосклерозирующего и флеботропного лечения (МОФФ 1000 мг/сут. в течение месяца) в отношении основных симптомов ХЗВ [8].
Еще одним подтверждением целесообразности периоперационной флеботропной терапии при ВБВНК служит исследование DECISION, которое было проведено в 8 клинических центрах РФ в период с 27.01 по 21.09.2011 г. В исследование были включены 230 пациентов (52 мужчины и 178 женщин) в возрасте от 20 до 62 лет (43,1±10,7) с показаниями для эндоваскулярного лечения варикозной болезни одной нижней конечности (C2–4sEpPr по CEAP), давшие информированное согласие на участие в исследовании. Принципиальным критерием включения служило наличие не менее трех симптомов, связанных с ХЗВ.
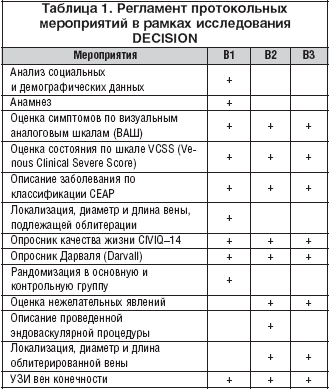
Дизайн исследования предполагал на первом визите к врачу (В1) регламентированное протоколом клиническое обследование пациента и его рандомизацию в основную или контрольную группу. Второй (В2) и третий (В3) визиты планировались соответственно через 2 и 4 нед. после проведения эндоваскулярного лечения. Мероприятия, предусмотренные протоколом, представлены в таблице 1.
Все 230 пациентов, включенных в исследование, были разделены на 2 группы. В основную группу – Д+ вошло 126 человек, которым в качестве средства фармакологической защиты за 2 нед. до предполагаемого эндоваскулярного вмешательства и в течение 4 нед. после него была назначена МОФФ в стандартной суточной дозировке 1000 мг. 104 больных были рандомизированы в контрольную группу – Д–, где осуществлялось стандартное послеоперационное ведение – бандажирование оперированной конечности с помощью компрессионных бинтов или медицинского трикотажа.
Статистическая обработка результатов исследования была проведена с помощью параметрических и непараметрических методов с вероятностью ошибки не более 5%.
В качестве референтных методов, позволяющих оценить влияние приема МОФФ в периоперационном периоде, расматривались шкала VCSS и опросник по качеству жизни – CIVIQ–14.
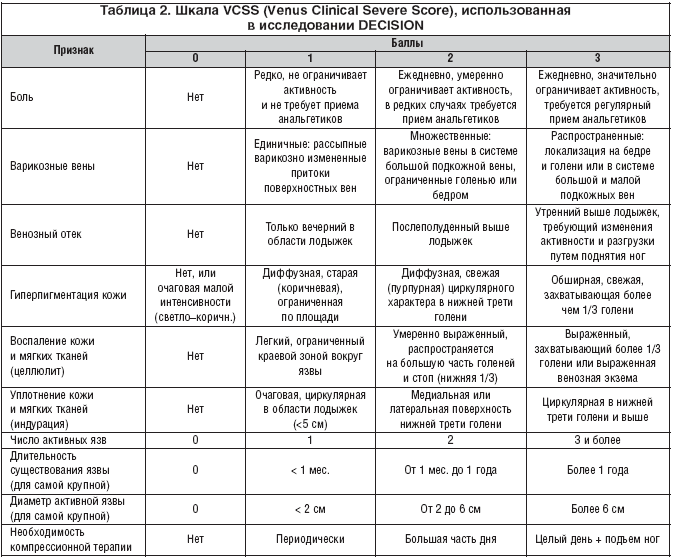
Клиническая шкала тяжести ХЗВ – VCSS – служит неотъемлемой частью классификации СЕАР и предназначена для динамической оценки течения заболевания. Последняя редакция шкалы VCSS представлена в таблице 2.
Исходные средние значения VCSS для пациентов, рандомизированных в МОФФ+ и МОФФ–, составили 4,2±2,1 и 4,0±2,1 соответственно (р=0,55), что свидетельствует об отсутствии значимых различий между основной и контрольной группами.
Сравниваемые группы пациентов МОФФ+ и МОФФ– не имели значимых различий по конституциональным признакам, факторам риска, характеру и тяжести заболевания, а также использованным методам эндоваскулярного лечения.
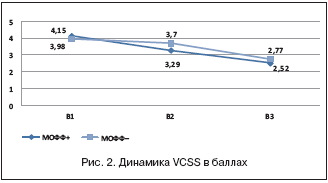
При оценке динамики суммы баллов по шкале VCSS отмечено ее статистически значимое снижение через первые 2 нед. после эндоваскулярного лечения (визит В2) как во всей популяции в целом (p<0,00001), так и отдельно в группе МОФФ+ (p<0,00001), но не в группе МОФФ– (p=0,15) (рис. 2).
Через 4 нед. (В3) после эндоваскулярного вмешательства сумма баллов по шкале VCSS статистически достоверно снизилась как во всей популяции в целом (p<0,00001), так и отдельно в группах МОФФ+ (p<0,00001) и МОФФ– (p<0,00001) (рис. 2). Уменьшение разницы по показателю VCSS вполне логично и легкообъяснимо. Это связано с естественной адаптацией пациентов контрольной группы и постепенным размыванием различий с пациентами МОФФ+ по критериям VCSS.
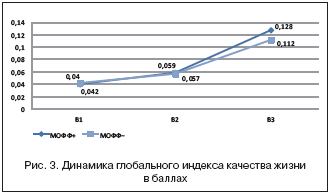
Что касается динамики глобального индекса качества жизни, то тут ситуация оказалась более сложной. При 2–ом и 3–ем визитах не было зафиксировано значимых различий в группах МОФФ+ и МОФФ–, хотя на графиках отмечается четкая дивергенция в пользу пациентов основной группы (рис. 3). В связи с этим можно предположить, что для получения статистически достоверных различий необходимо было увеличить либо число респондентов, либо длительность наблюдения.
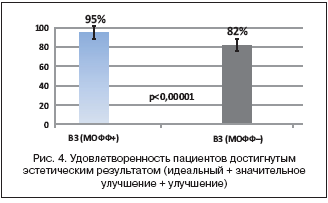
Исследование DECISION было интересно и тем, что в нем впервые в российской практике была проведена сравнительная оценка ожиданий пациента и его удовлетворенности исходом лечения. Для этого был использован опросник Дарваля (Darvall), согласно которому респонденты на 1–ом визите должны были в баллах оценить свои ожидания по исчезновению различных проявлений ВБВНК, а на 2–ом и 3–ем визитах зафиксировать достигнутый эффект. Например, на 3–ем визите 95% пациентов основной группы были удовлетворены достигнутым эстетическим результатом. В контрольной группе этот показатель составил 82% (рис. 4).
Таким образом, исследование DECISION продемонстрировало, что прием МОФФ в периоперационном периоде достоверно снижает степень клинической тяжести заболевания (VCSS), а также оказывает синергическое с эндоваскулярным вмешательством действие на основные симптомы варикозной болезни. Важно, что и удовлетворенность пациентов результатами лечения значимо выше в группе, где был назначен флеботропный препарат.
С.И. Ларин и соавт. [9] на основании результатов динамической компьютерной термографии продемонстрировали более быструю нормализацию температуры кожи и менее выраженный болевой синдром после эндовазальной лазерной облитерации у пациентов, получавших в течение 60 сут. МОФФ, в сравнении с больными у которых использовали только компрессионную терапию. Авторы делают вывод о том, что МОФФ приводит к статистически значимому улучшению физического благополучия, что связано с уменьшением уровня воспалительных явлений в проекции облитерированных вен [9].
МОФФ является единственным флеботропным лекарственным препаратом, ускоряющим заживление венозных трофических язв [10]. В связи с этим прием МОФФ рекомендован в рамках предоперационной подготовки и послеоперационной реабилитации больных с тяжелыми формами ХВН, осложненными венозными язвами, которым планируется эндоскопическая диссекция перфорантных вен голени [11].
Таким образом, представленный обзор и анализ 5 клинических исследований, из которых 3 были рандомизированными, убедительно демонстрирует, что периоперационная флеботропная терапия на примере микронизированной очищенной фракции флавоноидов (Детралекса) позволяет улучшать результаты как традиционных, так и эндоваскулярных методов лечения самой распространенной сосудистой патологии – ВБВНК.
Литература
1. Савельев В.С., Кириенко А.И., Богачев В.Ю. Хронические заболевания вен в Российской Федерации. Результаты международной исследовательской программы VEIN CONSULT // Флебология. – 2010. – Т. 4, № 3. – С. 9–12.
2. Veverkova L., Kalac J., Jedlicka V., Wechsler J. Analysis of surgical procedures on the vena saphena magna in the Czech Republic and an effect Detralex during its stripping [in Czech] // Rozhl. Chir. 2005. Vol. 84. P. 410–416.
3. Veverkova L., Kalac J., Jedlicka V., Wechsler J. Analysis of surgical procedures used in great saphenous vein surgery in the Czech Republic and benefit of Daflon 500 to postoperative symptoms // Phlebolymphol. 2006. Vol. 13. P. 193–199.
4. Савельев В.С., Покровский А.В., Кириенко А.И. и др. Проведение оперативного вмешательства при варикозной болезни под прикрытием микронизированного диосмина // Ангиология и сосудистая хирургия. – 2007. – Т. 13, № 2. – С. 47–55.
5. Saveljev V., Pokrovsky A., Kirienko A. et al Striping of the great saphenous vein under micronized purified flavonoid fraction (MPFF) protection (results of the Russian multicenter controlled trial DEFANCE) // Phlebolymphol. 2008. Vol. 15 (2). P. 43–51.
6. Шульц А.А., Шульц О.Г., Грошевой Д.В. и др. Выбор оптимальной послеоперационной дозировки микронизированной очищенной флавоноидной фракции у пациентов с варикозной болезнью нижних конечностей // Флебология. – 2009. – Т. 3, № 2. – С. 12–17.
7. www.veinteachingcenter.com
8. Allaert F., Gobin J. Observation study on the synergy of action of sclerotherapy and Grade A phlebotonic agents in chronic venous disease of the lower limbs // Angiol. 2010. Vol. 29 (2 suppl.). P. 2.
9. Ларин С.И., Замечник Т.В., Андриянов А.Ю. Микронизированная очищенная флавоноидная фракция в комплексном лечении пациентов с варикозной болезнью после эндовазальной лазерной облитерации // Флебология. – 2011. – Т.5(1). – С. 36–40.
10. Colerige–Smith P., Lok C., Ramelet A.A. Venous leg ulcer: a meta–analysis of adjunctive therapy with micronized purified flavonoid fraction // Eur. J. Vasc. Endovasc. Surg. 2005. Vol. 30. P. 198–208.
11. Выборный М.И. Эндоскопическая субфасциальная диссекция перфорантных вен голени в лечении осложненных форм хронической венозной недостаточности: автореф. дисс... к. м.н. – М., 2012.












