Рассматривая этиологию этих заболеваний, можно отметить, что инфекции кожи и мягких тканей обычно являются следствием каких–либо механических повреждений или хирургических манипуляций и вызываются широким спектром бактериальных микроорганизмов. В этой ситуации они являются в некоторой степени «запрограммированными», и их выявление не представляет особых сложностей для практического врача. Гораздо реже подобные инфекции возникают спонтанно, и в таких случаях часто возникают проблемы своевременной диагностики и лечения.
Большинство инфекций кожи и мягких тканей являются самоограничивающимися и легко поддаются терапии, иногда заключающейся только в местном лечении и хирургическом пособии и, часто даже без использования антибактериальных препаратов. Другие варианты течения инфекций мягких тканей являются жизненноопасными и требуют максимально быстрой диагностики, экстренного оперативного вмешательства и выбора рациональной антибактериальной терапии для предотвращения повреждения тканей и сохранения жизни. Дефекты в диагностике и лечении тяжелых инфекций мягких тканей, приведшие к обширным потерям мягкотканных образований, существенно в дальнейшем влияют на качество жизни и требуют сложных реконструктивных пластических операций.
Рост антибиотикорезистентных штаммов грамотрицательной и грамположительной флоры, отражающий как общую тенденцию эволюции микроорганизмов, так и являющийся следствием нерационального использования антибактериальных препаратов, вызывает определенные трудности в лечении и негативно влияет на клинические результаты и при подобного рода инфекциях.
В выборе адекватной тактики лечения важную роль играет знание анатомии мягких тканей, уровень локализации инфекции, что в совокупности с анализом конкретной клинической ситуации, учетом факторов риска и знанием эпидемиологической обстановки позволяет с достаточно высокой долей вероятности определить потенциального возбудителя и назначить адекватную рациональную стартовую антибактериальную терапию. Необходимо подчеркнуть, что существенную помощь в выборе тактики лечения может оказать использование в клинической практике классификации инфекций мягких тканей по уровню поражения, достаточно распространенной в ряде стран, однако малоизвестной отечественному врачу [4].
Предлагаемая классификация имеет достаточно много положительных сторон. Главное ее значение заключается в том, что она нацеливает врача на конкретный уровень поражения (вовлечения тканей) в ходе инфекционного процесса, что определяет как хирургическую тактику, так и дополнительные методы лечения.
Изучая применение антибиотиков в ходе лечения хирургических инфекций мягких тканей, необходимо отметить несколько важных с нашей точки зрения моментов.
Прежде всего нет ни одного антибактериального препарата, который бы не использовался в ходе лечения инфекционного процесса в этой зоне. Начиная от первых поколений пенициллинов и заканчивая фторхинолонами III поколения и карбапенемами и представителем оксазалидинонов. Вторым, принципиальным, моментом, является то, что в доступной нам литературе мы не нашли описания систематизирующих принципов применения тех или иных антибактериальных препаратов при рассматриваемом типе инфекций. Необходимо отметить также, что присутствие анаэробных возбудителей как этиологических агентов ряда заболеваний, относящихся к хирургическим инфекциям мягких тканей, заставляет зачастую использовать антианаэробные препараты при всех патологиях, невзирая на отсутствие микробиологического подтверждения и обоснованности. Именно этот факт привел к значительному снижению чувствительности анаэробной микрофлоры к клиндамицину, долгое время выступавшему в качестве «золотого стандарта» антианаэробной терапии. К счастью, механизм действия нитроимидазолов (НИМЗ) носит принципиально другой характер, и сообщения о развивающейся резистентности микроорганизмов крайне редки и носят весьма противоречивый характер. Механизм действия после проникновения НИМЗ в микробную клетку связан с восстановлением нитрогруппы под влиянием нитроредуктаз микроорганизмов и с активностью уже восстановленного нитромидазола. НИМЗ характеризуются благоприятной фармакокинетикой и высокой степенью биодоступности, медленно выводятся из организма и могут обеспечить после однократной дозы терапевтический уровень в крови и органах в течение 2 дней. НИМЗ выводятся почками (главным образом) и с желчью.
Первым высокоактивным препаратом, примененным в клинике в 1960 г., был метронидазол. Метронидазол сначала рассматривался только как антипротозойный препарат; в 1962 г. была доказана его активность и в отношении большинства анаэробных бактерий.
Метронидазол (Метрогил) сохраняет свою активность против разных групп анаэробов (исключение составляют актиномицеты и пропионобактерии) и имеет целый ряд преимуществ по сравнению с другими антианаэробными препаратами. Обладая бактерицидной активностью, метронидазол хорошо сочетается с антибиотиками разных групп, что особенно важно при комбинированной терапии инфекций полимикробной этиологии. К тому же комбинированная терапия с метронидазолом имеет и фармакоэкономические преимущества. Хорошее проникновение в органы и ткани (70–94% от сывороточных концентраций) выгодно отличает метронидазол от других антимикробных средств и позволяет применять его практически при любой локализации инфекции или гнойно–воспалительного процесса.
Рассматриваемая классификация Ahrenholz D.H., 1991, с нашей точки зрения, может в некоторой степени решить указанную проблему (табл. 1). Это определяется тем, что в большинстве случаев имеется четкая связь уровня инфекционного поражения и определенного набора микроорганизмов, что позволяет выбрать те или иные препараты.
К примеру: основным возбудителем целлюлита является Str. pyogenes; фасциита – Str. pyogenes, St. aureus и анаэробные возбудители; миозита – St. аureus; мионекроза – B. fragilis, Clostridium spp [5].
Распределение основных возбудителей инфекций мягких тканей в зависимости от уровня поражения.
Уровень I – Str. pyogenes
Уровень II – St. aureus, Str. pyogenes
Уровень III – (Смешанная) St. aureus, E. сoli, Pr. mirab, Ps. aerug., Enterobacter, Анаэробные возбудители
Уровень IV – (Смешанная) B. fragilis, Clostridium spp. St. aureus.
Знание такой уровнево–микробиологической зависимости помогает в выборе рационального стартового лечения, в дальнейшем корригируемого при анализе каждой конкретной клинической ситуации и получении результатов культуральных исследований [6].
К примеру, изучение такой патологии как рожистое воспаление, являющейся инфекцией только первого уровня – собственно кожи, показывает крайнюю неудовлетворенность результатами лечения [7].
Большое число проведенных на протяжении последних лет микробиологических исследований показало значительный рост устойчивости возбудителей заболеваний к антибактериальным препаратам [8,9,10]. В то же самое время чувствительность b–гемолитического стрептококка группы А, признаваемого до настоящего времени основным этиологическим фактором рожистого воспаления, к b–лактамным антибиотикам, включая природные пенициллины, остается абсолютной [11,12]. При анализе результатов лечения пациентов с неосложненными формами рожистого воспаления (эритематозная, эритематозно–буллезная) отмечено, что в большинстве случаев показана достаточная эффективность природных пенициллинов, использование которых ведет к быстрому купированию общей и местной симптоматики.
Проведенные бактериологические исследования того, что принято называть осложненными формами рожистого воспаления, показали преобладание микробных ассоциаций, в которых Str. pyogenes уже не играет ведущего значения, что уже в плане стартовой терапии требует исходного назначения антибактериальных препаратов более широкого спектра действия, включающих также и противоанаэробную активность (ингибиторзащищенные пенициллины и цефалосорины, карбепенемы, аминогликозиды III пок., цефалоспорины III и IV пок.; последние две группы препаратов целесообразно комбинировать с метронидазолом) [11].
К первому уровню поражений, помимо рожистого воспаления (точнее его неосложненных форм), относятся фурункул и эризипилоид.
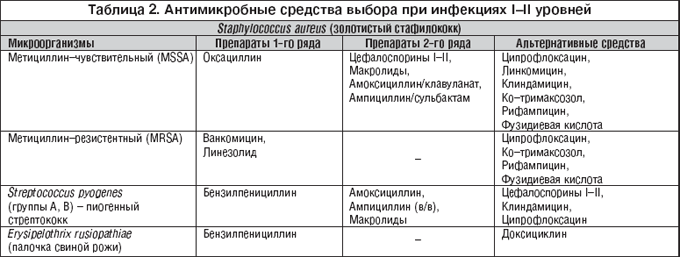
Ко второму уровню поражений относятся карбункул, гидраденит, целлюлит, абсцесс. Перечисленные нозологии вызываются стафилококком, чаще золотистым. Как видно из вышеизложенного, основными возбудителями инфекций первого и второго уровней являются стрептококк и стафилококк. Следовательно, антибактериальным препаратам, назначаемым при лечении инфекций первого и второго уровней, в своем спектре достаточно иметь антистрептококковую и антистафилококковую активность (табл. 2). Применение препаратов более широкого спектра действия нецелесообразно как с микробиологической позиции (выше риск развития таких побочных эффектов, как дисбактериозы, антибиотик–ассоциированные колиты), так и с экономической (неоправданное повышение стоимости лечения).
Из перечисленных патологий много проблем возникает при диагностике и лечении целлюлита. В клинике чаще всего встречается целлюлит, обусловленный Str. рyogenes и St. аureus, но в редких случаях развитие целлюлита может быть связано и с другими более вирулентными микроорганизмами, как грамположительными, так и грамотрицательными. Инфекция может иметь моно– и полимикробный характер, быть аэробной, анаэробной или смешанной. Подобный спектр возбудителей и определяет характер начальной антибактериальной терапии, заключающийся в назначении пенициллиназа–устойчивых пенициллинов или цефалоспоринов I поколения. При аллергии на пенициллин или при высоком риске инфекции MRSA препаратами выбора являются ванкомицин, линезолид [5].
Серьезной клинической проблемой инфекций второго уровня является некротический целлюлит. Непосредственно анаэробные микроорганизмы являются причиной развития данной патологии лишь у 10% пациентов с некротическим целлюлитом и обычно входят в состав поликультуры [5]. Основным же возбудителем инфекций данного уровня остается стрептококк. Развитие заболевания связано с травматизацией и нарушением целостности кожного покрова, ранами, а также может являться результатом инфекции области хирургического вмешательства, особенно в абдоминальной хирургии при операциях, сопровождающихся вскрытием просвета кишечного тракта. Основными анаэробными микроорганизмами, ответственными за развитие некротического целлюлита, являются Clostridium, Bacteroides и Peptostreptococcus. Диагностике помогают данные микробиологического исследования. Существенную роль в диагностике клостридиальной инфекции оказывает выполнение мазка–отпечатка с окраской по Граму, результаты которого могут быть получены в течение ближайшего часа. Обнаружение в мазке грамположительных палочек с закругленными концами с высокой вероятностью указывает на наличие клостридий в ране.
Клостридии высокочувствительны к пенициллину. Однако прежде чем начинать его использование в конкретной клинической ситуации, необходимо иметь в виду, что инфекции кожи и подкожной клетчатки редко протекают как моноинфекция (табл. 3). Значительно чаще они выступают в виде «микстов», поэтому в случае госпитальной полимикробной инфекции, включающей грамотрицательную флору и St. аureus, схемами выбора являются: защищенные цефалоспорины (цефоперазон/сульбактам); клиндамицин с аминогликозидом; цефалоспорины IV поколения в сочетании с метронидазолом; карбапенемы [5,13,17].
Инфекции третьего уровня – инфекции фасций. В настоящее время все процессы, связанные с бактериальными инфекциями, протекающими в фасциальных выстилках, объединяют общим генерическим термином «некротизирующий фасциит». Некротизирующий фасциит может вызываться полимикробной флорой, но отдельно выделяется стрептококковый некротизирующий фасциит ввиду выраженных особенностей клинической картины. Основными факторами риска являются пожилой возраст, заболевания периферических сосудов, диабет. В качестве непосредственных причин могут служить повреждение кожных покровов, травма или хирургическое вмешательство, что характерно для всех глубоких поражений.
Особо тяжелая ситуация в случае инфекции высоковирулентными штаммами b–гемолитических стрептококков группы А, вызывающими синдром токсического шока, хотя и в остальных случаях стрептококковые некротизирующие фасцииты протекают крайне тяжело и характеризуются быстро прогрессирующим некрозом кожного покрова. Они могут быть как внебольничной этиологии, так и являться осложнениями послеоперационного периода.
Несмотря на высокую чувствительность стрептококка к пенициллину G, в плане антибактериальной терапии рекомендуется использовать цефтриаксон, обладающий активностью и в отношении стрептококков, продуцирующих пенициллин–связывающий белок [11]. В схемы терапии некротических фасциитов стрептококковой и микст–этиологии рекомендуется включать клиндамицин, который обладает способностью ингибировать продукцию белкового токсина стрептококком (табл. 4) [5]. При клостридиальной и стрептококковой этиологии инфекции рекомендуемая стартовая терапия: пенициллин + клиндамицин [5]. При внебольничных смешанных инфекциях – препараты выбора – защищенные пенициллины широкого спектра действия, клиндамицин с аминогликозидом [5]. При нозокомиальных инфекциях предпочтительнее цефалоспорины IV поколения в сочетании с метронидазолом; карбапенемы [5]. Раннее хирургическое вмешательство и своевременное начало рациональной антибиотикотерапии снижают риск смерти при столь тяжелой патологии.
Поражение мышц и глубоких фасциальных структур рассматривается как четвертый уровень. Основными возбудителями мионекроза являются – B. fragilis, Clostridium spp. Неклостридиальные миозиты вызываются смешанной аэробной и анаэробной флорой, изолированно данную патологию могут вызывать St. аureus, инвазивные штаммы Str. рyogenes, и обычно газообразования при данной инфекции не определяется. Миозит, или пиомиозит, чаще встречается в тропических регионах и возникает у пациентов с имуннодефицитом на фоне ВИЧ–инфекции или диабетом. Клиническая картина заключается в мышечных болях, спазмах, лихорадке, при пальпации мышцы кажутся деревянными, что заставляет в плане дифференциальной диагностики исключать глубокий венозный тромбоз. Ультразвуковое исследование и компьютерная томография помогают в обнаружении внутримышечных абсцессов.
Хирургическое лечение дополняется использованием пенициллиназа–устойчивых пенициллинов, цефалоспоринов I поколения или (крайне редко, при специальных показаниях!) ванкомицина. Часто смешанный характер инфекции, исходная иммуноскомпрометированность пациентов с данной патологией, характеризующейся высокой летальностью, заставляет в плане стартовой терапии рекомендовать антибактериальные препараты широкого и ультраширокого спектра действия, что принято относить к группе антибиотиков резерва – цефалоспорины IV + метронидазол и карбапенемы (табл. 5).
Некротический миозит, мионекроз, или газовая гангрена – одна из самых тяжелых инфекций, протекающая с выраженной токсемией и быстро распространяющимся некрозом мышечных структур, в подавляющем большинстве случаев вызывается Clostridium perfringens (инфекция Clostridium septicum чаще связана с текущей патологией колоректальной области – рак, полипы или дивертикулит). Половина случаев развития газовой гангрены связана с травмой, треть случаев – последствия абдоминальных хирургических вмешательств, реже развитие столь серьезной патологии происходит спонтанно. Важным методом диагностики клостридиального характера инфекции является выполнение мазка–отпечатка во время операции, который уже в самое ближайшее время даст ответ о присутствии в ране грамположительных палочек, подтверждая диагноз анаэробной клостридиальной инфекции. И как при лечении любой тяжелой инфекции мягких тканей, проведение рациональной антибактериальной терапии является одним из основных мероприятий, обеспечивающих успех проводимого лечения. При клостридиальной моноинфекции, несмотря на высокую чувствительность клостридий к пеницилллину, терапию следует дополнять клиндамицином для обеспечения синергизма в воздействии и торможения продукции токсина. С учетом того, что в более чем 50% случаев имеет место смешанная инфекция с участием грамотрицательной флоры [5], антибактериальную терапию следует проводить с использованием цефалоспоринов III поколения (цефотаксим, цефтриаксон) при внебольничном характере процесса, в то время как при нозокомиальном – IV поколения или карбапенемами [14]. Эти же препараты должны быть использованы при наличии у больного клиники тяжелого сепсиса и/или септического шока, как обладающие минимальной эндотоксинвысвобождающей активностью.
Важным фактором, осложняющим антибактериальную терапию тяжелых смешанных инфекций мягких тканей, особенно госпитальных форм, остается неблагоприятная динамика антибиотикорезистентности основных возбудителей [15,16,17]. Нерациональная антибактериальная терапия, широкомасштабное и бесконтрольное применение антибактериальных препаратов группы резерва, отсутствие в широкой клинической практике четких критериев к назначению и строгих стандартов по применению антибактериальных препаратов привели к резкому росту антибиотикорезистентности микроорганизмов.
Анализируя вышепредставленные данные, в эмпирической терапии тяжелых инфекций мягких тканей смешанной этиологии или преимущественно грамотрицательной природы нозокомиального происхождения рекомендуется использовать цефалоспорины IV поколения и карбапенемы, сохраняющие наибольшую активность в отношении основных возбудителей.
В заключении необходимо отметить, что в успешном лечении тяжелых инфекций мягких тканей основную роль играет своевременная диагностика, адекватное оперативное пособие, рациональная антибактериальная терапия, полноценная интенсивная терапия, включающая нутриционную и иммунную коррекцию, для чего крайне необходимо правильное понимание анатомопатофизиологических и микробиологических особенностей течения инфекций мягких тканей. Использование классификации по уровню поражения мягких тканей инфекцией оказывает практическую помощь при выборе лечебной тактики и позволяет производить дифференцированный подход как к хирургической тактике, так и к выбору антибактериальной терапии.



Литература
1. Green J, Wenzel RP. Postoperative wound infection. Ann Surg.1977;185:264–268.
2. Haley RW. The scientific basis for using surveillance and risk factor data to
reduce nosocomial infection rates. J Hosp Infect.1995;30(suppl):3–14.
3. Everett JE, Wahoff DC, Statz CL, et al. Characterization and impact of wound
infection after pancreas transplantation. Arch Surg.1994;129:1310–1317.
4. Ahrenholz DH Necrotizing fasciitis and other infections. In: Rippe J.M., Irwin R.S., Alpert J.S., Fink M.P. (eds)Intensive Care Medicine, 2nd ed Boston, Little, Brown, 1991, p.1334.
5. “Severe Skin and Soft–Tissue Infections”, David R. Stone, Sherwood L.Gorbach in : “Infectious Diseases in Critical Care Medicine”, Burke A. Cunha`, 1998.
6. Giuliano A., Lewis F. Jr., Hadley K., Blaisdel FW// Bacteriology of necrotizing fasciitis Am J Surg 134:52, 1977
7. Королев М.П., Спесивцев Ю.А., Толстов О.А., Чуликов О.А., Бечвая Л.Д. Тактика лечения различных форм рожистого воспаления // Тезисы докладов научно–практической ежегодной конференции Ассоциации хирургов Санкт–Петербурга, 28–29 января 2000 г., Санкт–Петербург, 2000 г.– 7 – 9.
8. Навасардян А.С. Оптимизация комплексного лечения больных с рожистым воспалением на госпитальном этапе: Автореф. дис. канд. мед. наук: 14.00.27 / Самарский медицинский университет.–Самара, 2000 г.– 24 с.
9. Амбалов Ю.М., Левина Л.Д., Коваленко А.П. Использование клинических, иммуногенетических и иммунологических показателей для прогноза развития рецидивирующей формы рожистого воспаления // Врачеб. дело, 1992, № 9. –60–65 с.
10. С.В. Сидоренко, С.П. Резван, С.А. Грудинина, Г.В. Стерхова. Динамика антибиотикорезистентности возбудителей госпитальных инфекций в отделении реанимации // Consilium medicum журн., 2001.
11. Антибактериальная терапия. Практическое руководство. Под редакцией Л.С Страчунского, Ю.Б. Белоусова, С.Н. Козлова, 2002 г.
12. Сидоренко С.В., Яковлев С.В. Инфекции в интенсивной терапии. Москва 2000 г.
13.. Charles E. Edmiston, Jr., Candace J. Krepel, Gary R Seabrook, and William G. Jochimsen. “Anaerobic Infections in the Surgical Patient: Microbial Etiology and Therapy”. Clinical Infectious Diseases, 2002;35(Suppl 1): S 112–8
14. В.А. Руднов. Место карбапенемов в лечении тяжелого сепсиса // Consilium medicum журн., 2001.
15. С.В. Яковлев. Клиническое значение резистентности микроорганимов для выбора режима антибактериальной терапии в хирургии // Consilium medicum журн., 2001.
16. С.В. Сидоренко, С.П. Резван, С.А. Грудинина, Г.В. Стерхова. Динамика антибиотикорезистентности возбудителей госпитальных инфекций в отделении реанимации // Consilium medicum журн., 2001.
17. Современное значение цефалоспоринов IV поколения. Редакционная статья // Инфекции и антимикробная терапия, 2001, том 3, № 2.












