Феномен усугубления кардиоваскулярных заболеваний, ассоциированных с сексуальной активностью, хорошо изучен [3]. Больные ЭД, подверженные риску сердечно-сосудистых заболеваний, могут быть разделены на категории низкого, среднего и высокого риска. Данная классификация может быть широко использована в клинической практике для восстановления сексуальной активности у такой категории больных.
Несмотря на множество эффективных методов лечения ЭД, в большинстве случаев она не может быть вылечена полностью. Исключением являются психогенная ЭД, посттравматическая артериогенная ЭД у молодых, а также ЭД, вызванная гормональными причинами. Так, у молодых пациентов с тазовой или промежностной травмой хирургическая пенильная реваскуляризация имеет длительный положительный эффект в 60–70% случаев [4].
Физиология эректильной функции
Понимание механизма эрекции – ключевой момент выбора метода лечения. Во время сексуальной стимуляции полового члена в центре эрекции спинного мозга, который располагается на уровне S2–S4, возникает нервный импульс [5]. Оттуда по эфферентным нервным волокнам, которые находятся в составе тазового нерва, он достигает тазового сплетения. В дальнейшем по постганглионарным неадренергическим, нехолинергическим (NANC – nonadrenergic noncholinergic) нервным волокнам, находящимся в составе кавернозных нервов, нервный импульс достигает кавернозных тел полового члена [5]. В результате этого в терминалиях NANC волокон высвобождается оксид азота. Последний также вырабатывается клетками эндотелия кавернозных тел в ответ на выработку ацетилхолина в парасимпатических эндотелиальных нервных волокнах. Установлено, что оксид азота нервной ткани инициирует процесс эрекции посредством эндотелиального оксида азота, что приводит к усиленной выработке последнего и, как следствие, к поддержанию максимальной эрекции [6]. Дополнительное количество оксида азота вырабатывается вследствие возникшего напряжения в кавернозных телах после усиленного кровенаполнения [5, 7].
На молекулярном уровне оксид азота продуцируется за счет фермента NO-синтетазы, который, вступая во взаимодействие с L-аргинином, высвобождает оксид азота. NO-синтетазу выявляют в нервных окончаниях и клетках эндотелия. Оксид азота проникает сквозь мембраны гладкомышечных клеток кавернозных синусов и активирует растворенную в цитоплазме гуанилатциклазу. Последняя катализирует процесс образования циклического гуанозинмонофосфата (цГМФ) из внутриклеточного гуанозин-трифосфата. цГМФ активирует протеинкиназу, способствуя гиперполяризации мембран гладкомышечных клеток, а в мембранах эндоплазматического ретикулума происходит усиленное потребление ионов кальция [5, 7]. Гиперполяризация клеточных мембран ведет к закрытию кальциевых каналов, и ионы кальция концентрируются внутри эндоплазматического ретикулума гладкомышечных клеток, что приводит к расслаблению последних.
Вместе с этим другие нейротрасмиттеры, такие как вазоактивный интестинальный пептид, простагландин Е, взаимодействуют с различными гладкомышечными рецепторами и способствуют повышению уровня циклического аденозинмонофосфата (цАМФ), что также приводит к накоплению ионов калия в клетках и их расслаблению [5, 8]. Такое расслабление гладкомышечных клеток артерий и артериол влечет за собой активное кровенаполнение кавернозных синусов в систолическую и диастолическую фазы. Кавернозные синусы остаются расширенными до тех пор, пока продолжается приток крови [8]. Компрессия венозного сплетения, расположенного между белочной оболочкой и кавернозными синусами, препятствует оттоку крови от полового члена [9]. Белочная оболочка адаптируется к растяжению кавернозных тел, тем самым дополнительно окклюзируя эмиссарные вены между внутренними циркулярными и продольными венами [10].
Участие андрогенов в поддержании эректильной функции заключается в регуляции продукции и взаимодействия нейрогенной и эндотелиальной NO-синтетаз в ткани каверозных тел [11]. Так, установлено, что у мужчин пожилого возраста в связи со снижением уровня тестостерона имеет место затрудненное возникновение или поддержание эрекции [12]. Фермент цГМФ-специфическая фосфодиэстераза (5 типа) прекращает превращение цГМФ из гуанозинтрифосфата, а также гиперполяризацию клеточных мембран, тем самым тормозя релаксацию гладкомышечных клеток, вызывая детумесценцию [13]. Дополнительное давление приводит также к сокращению седалищно-кавернозных мышц за счет соматической нервной стимуляции. В это время интракавернозное давление приводит к повышению системного артериального давления [10].
Парасимпатический механизм поддержания эрекции сменяется активацией симпатических нервных волокон. Симпатический нервный центр локализуется на уровне Th4-L2, и его активация способствует поддержанию полового члена в «пассивном» состоянии. Это происходит за счет высвобождения норадреналина из нервных терминалей, который взаимодействует с α-адренорецепторами кавернозных гладкомышечных клеток [5].
Норадреналин, эндотелин-1 и простагландин F2α активируют рецепторы гладкомышечных клеток за счет повышения уровня инозитолтрифосфата (ИТФ) и диаглицерола. Накопление этих веществ внутри клетки способствует открытию кальциевых каналов эндоплазматического ретикулума и накоплению кальция внутри клетки. Ионы кальция взаимодействуют с белком кальмодулином и активируют работу легких цепей миозина, приводя к сокращению гладкомышечных клеток и прекращению эрекции [5, 14, 15].
Медикаментозное лечение
Ингибиторы фосфодиэстеразы 5 типа (ФДЭ-5) оказывают воздействие на расслабление гладкомышечных клеток за счет конкурентного взаимодействия с ферментом ФДЭ-5. Этот фермент отвечает за расщепление цГМФ в 5’-ГМФ. Ингибиторы ФДЭ-5 способствуют накоплению цГМФ внутри гладкомышечных кавернозных клеток, а также в клетках гладкомышечного слоя артерий полового члена [7, 13, 16]. Расслабление гладкомышечных клеток усиливает приток артериальной крови, в результате чего наступает эрекция. Известно, что ФДЭ–5 – это одна из 11 открытых ФДЭ в организме человека [7]. ФДЭ-5 обеспечивает поддержание физиологической концентрации цГМФ в кавернозных телах полового члена. Это объясняет тот факт, почему ФДЭ-5 селективна лишь в отношении эректильной функции и не имеет системного влияния [17].
Действие препаратов – ингибиторов ФДЭ-5 основано на взаимодействии оксида азота с NO-синтетазами нервных окончаний и эндотелия кавернозных тел. Вот почему эти лекарства не так эффективны у больных с сосудистыми заболеваниями, когда имеет место дисфункция эндотелия, или биодоступость оксида азота снижена, например, в результате повреждения нервных путей или после радикальной простатэктомии [7, 13, 16].
В соответствии с рекомендациями EAU выбор одного из одобренных к применению ингибитора ФДЭ-5 во многом зависит от предпочтений пациента. Задача врача заключается в предоставлении полной информации больному в отношении ингибиторов ФДЭ-5. Эффективность в отношении ЭД и безопасность ингибиторов ФДЭ-5 на сегодняшний день являются доказанными. В ходе постмаркетинговых исследований установлено, что связи между увеличением числа сердечно-сосудистых заболеваний и приемом ингибиторов ФДЭ-5 не существует [18]. Хотя очевидно, что противопоказаниями к приему ингибиторов ФДЭ-5 являются нестабильная стенокардия, недавно перенесенный инфаркт миокарда, постоянная аритмия и злокачественная артериальная гипертензия. Ингибиторы ФДЭ-5 полностью не совместимы с приемом донаторов оксида азота, учитывая риск развития серьезной гипотонии и сосудистого коллапса.
Одним из ингибиторов ФДЭ-5 является силденафил. С уверенностью можно сказать, что силденафил – наиболее изученное медикаментозное средство лечения ЭД. На сегодняшний день существует 27 клинических исследований, посвященных эффективности и безопасности этого препарата. В этой статье мы представляем отдельные, но авторитетные с точки зрения доказательной медицины публикации, посвященные применению силденафила у разных категорий больных с ЭД.
Так, уже в 2002 г. был проведен крупный метаанализ многочисленных данных, опубликованных к тому моменту в мировой литературе [19]. Авторы проанализировали 27 клинических исследований, которые включали в себя 6659 пациентов с ЭД. Исследования, посвященные сравнению силденафила и плацебо, подтверждают достоверную эффективность препарата по сравнению с плацебо в отношении улучшения эректильной функции. Что касается работ, посвященных сравнению различных доз силденафила, то установлено, что немного более эффективными являются высокие дозы препарата. Существенным является тот факт, что силденафил не был связан с развитием каких-либо серьезных сердечно-сосудистых заболеваний или летальных исходов.
Важной категорией больных ЭД являются пациенты после радикальной простатэктомии. Так, по данным Mulhall (2009), распространенность заболевания среди таких пациентов составляет от 14 до 90%. На эти цифры, безусловно, влияет множество факторов, таких как возраст пациента, качество эректильной функции до операции, то, какая операция была выполнена (одно- или двусторонняя нервосберегающая радикальная простатэктомия), и, конечно, опыт хирурга. Известно, что пациенты в большинстве случаев нуждаются в восстановлении эректильной функции после радикальных оперативных вмешательств на органах малого таза. Наиболее простым способом является назначение ингибиторов ФДЭ–5. Механизм действия препаратов в данном случае полностью зависит от присутствия в клетках гладкой мускулатуры артерий и кавернозных тел цГМФ, а также от способности клеток эндотелия продуцировать оксид азота. Основным звеном патогенеза в данном случае является нейропраксия (повреждение кавернозного нерва), поэтому способность выработки оксида азота может быть значительно снижена или полностью утрачена.
В 2008 г. Bannowsy et al. опубликовали результаты применения низких доз силденафила у мужчин, перенесших радикальную нервосберегающую простатэктомию. 23 пациента принимали 25 мг силденафила на ночь, а контрольная группа не получала медикаментозного лечения. В группе, принимавшей силденафил, индекс IIEP снизился по сравнению с дооперационным с 20,8 до 3,6 (после 6 нед. приема препарата) и затем поднялся до 14,1 (после 52 нед. приема препарата). У пациентов контрольной группы этот же индекс снизился с 21,2 до 2,4 (через 6 нед.), а затем поднялся до 9,3 (через 52 нед.). Таким образом, авторы установили значительное улучшение эректильной функции у больных, которые принимали силденафил после радикальной простатэктомии, а также значительное укорочение времени реабилитации в послеоперационном периоде в результате медикаментозного лечения [20].
В том же 2008 г. Padma-Nathan et al. опубликовали данные первого широкомасштабного плацебо-контролируемого исследования применения силденафила у больных после радикальной нервосберегающей простатэктомии. В исследование было включено 76 мужчин через 4 нед. после оперативного лечения. Участники были разделены на 3 группы: 1-я получала силденафил в дозе 50 мг, 2-я – также силденафил, но в дозировке 100 мг, а 3-я – плацебо. Препарат принимался ежедневно на ночь в течение 36 нед. Было отмечено появление спонтанных ночных эрекций у 4% плацебо-группы и 27% больных, получавших силденафил (р≤0,01). Исследователями был сделан вывод о том, что ежедневный прием силденафила после оперативного лечения способствует восстановлению нормальных спонтанных эрекций [21].
Существуют также данные о том, что длительный прием ингибиторов ФДЭ-5, в частности силденафила, влияет на восстановление эндотелиальной функции [22]. В исследование вошли 20 больных с СД 2-го типа без ЭД. Обе группы вначале на протяжении 3 дней получали 100 мг силденафила. Затем 1-я группа принимала 25 мг силденафила 3 р./сут на протяжении 4 нед. 2-я группа принимала 25 мг силденафила 3 р./сут на протяжении 4 дней, затем перешла на прием плацебо. Через 1 нед. после начала исследования был оценен показатель пенильного кровотока FMD (flow mediated dilatation). У всех пациентов он улучшился более чем на 50% (на 62% в 1-й группе и на 64% – во 2-й). У больных 1-й группы было отмечено дальнейшее улучшение FMD через 2, 3 и 4 нед. (78, 86 и 94% соответственно). У пациентов, получавших плацебо, подобных изменений не наблюдалось: 45, 18 и 6% соответственно. Также у больных, длительно принимавших силденафил, было выявлено снижение эндотелина 1 (мощного сосудосуживающего фактора) и значительное увеличение донаторов азота. Авторы пришли к заключению, что длительный прием силденафила у больных, страдающих СД, способствует восстановлению эндотелиальной функции.
В настоящее время в мире известно несколько препаратов – ингибиторов ФДЭ-5, которые обладают рядом особенностей и отличий. Вот почему очень важным является ретроспективное исследование, опубликованное в 2005 г. в США, посвященное сравнительному анализу 3–х препаратов: силденафила, варденафила и тадалафила [23]. В исследование было включено 146 619 пациентов, принимавших данные препараты в период с 1996 по 2004 г. Анализу подверглись следующие параметры: необходимость продолжить прием того же препарата, с которого было начато лечение; смена препарата на другой ингибитор ФДЭ-5; возможность и удобство титрования дозы. В результате было установлено, что 52% пациентов, принимавших силденафил, считали необходимым продолжить прием этого же препарата, в отличие от варденафила и тадалафила (30 и 29% соответственно) (р<0,001). Меньшее количество больных из группы силденафила (6,4%) имели желание сменить препарат на другой, по сравнению с группами тадалафила (9,0%) и варденафила (10,4%) (р<0,001). Принимая во внимание тот факт, что пациенты с ЭД во многом представляют собой неоднородную популяцию, возможность титрования дозы в сторону увеличения или уменьшения для улучшения результатов лечения является крайне актуальной. Безусловно, данные показатели позволяют сделать многообещающий вывод о том, что силденафил может наиболее соответствовать потребностям пациентов в лечении ЭД. Для более точной и значимой оценки требуются новые рандомизированные плацебо-контролируемые исследования в данном направлении.
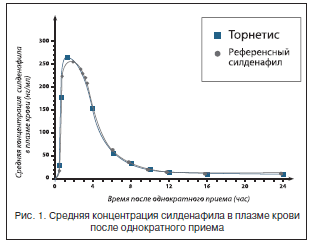
В 2013 г. на российский рынок был выпущен препарат Торнетис. Это медикаментозное средство является дженерическим силденафилом. Данный препарат обладает теми же фармакодинамическими и фармакокинетическими параметрами, что и оригинальный силденафил (рис. 1). По этой причине не вызывает сомнений тот факт, что его эффективность и безопасность должны соответствовать хорошо известному силденафилу. Удобство применения препарата состоит в возможности многократного титрования дозы (25, 50, 75 и 100 мг). Торнетис производится в виде таблеток по 100 мг. Для удобства применения таблетка имеет специальные насечки, которые позволяют как разделить ее на 4 равные части по 25 мг каждая, так и выбрать дозу в 50 и 75 мг. Таким образом, компания-производитель при помощи такой простой оригинальной конструкции таблетки решает задачу титрования дозы. Пациент приобретает Торнетис в дозе 100 мг и имеет шанс использовать все возможные дозы силденафила, а именно 25, 50, 75 и 100 мг. С экономической точки зрения ввиду оригинальной возможности деления таблетки Торнетис также имеет явные преимущества.
Таким образом, медикаментозная терапия ингибиторами ФДЭ-5 остается основным методом лечения ЭД и обеспечивает доказанную высокую эффективность. Появление препарата Торнетис (силденафил) с новым и простым решением подбора дозы препарата упрощает наши возможности эффективного лечения больных ЭД.
RU1312160911
Литература
1. Feldman H.A., Goldstein I., Hatzichristou D.G., Krane R.J., McKinlay J.B. Impotence and its medical correlates: results of the Massacusetts Male Aging Study // О Urol. 1994. Vol. 151. Р. 54–61.
2. Montorsi F., Briganti A., Salonia A. et al. Erectile dysfunction prevalence, time of oneset and association with risk factors in 300 consecutive patients with accute chest pain and angiographically documented coronary artery disease // Eur Urol. 2003. Vol. 44. Р. 360–365.
3. Jackson J., Rosen R.C., Kloner R.A., Kostis J.B. The second Princeton consensus on sexual dysfunction and cardiac risc: new guidelines for sexual medicine // J Sex Med. 2006. Vol. 3. Р. 28–36.
4. Rao D.S., Donatucci C.F. Vasculogenic impotence. Arterial and venous surgery // Urol Clin North Am. 2001. Vol. 3. Р. 28–36.
5. Steers W.D. Neural pathways and sentral sites involved in penile erection: neuroanatomy and clinical implications // Neurosci Biobehav Rev. 2000. Vol. 24. Р. 507–516.
6. Hurt K.J., Musicki B., Palese M.A. et al. Akt-dependent phosphorylation of endothelial nitric-oxide synthase mediates penile erection // Proc Natl Acad Sci USA. 2002. Vol. 99. Р. 4061–4066.
7. Burnett A.L., Ricker D.D., Chamness S.L. et al. Localization of nitric oxide synthase in the reproductive organs of the male rate // Biol Reprod. 1995. Vol. 52. Р. 1–7.
8. Lue T.F. Erectile dysfunction // N Engl О Med. 2003. Vol. 342. Р. 1802–1813.
9. Fournier Jr. G.R., Juenemann K.P., Lue T.F., Tanagho E.A. Mechanism of venous occlusion during canine penile erection: an anathomic demonstration // О Urol. 1987. Vol. 137. Р. 163–167.
10. Wespes E., Schulman C.C. Study of human penile venous system and hypothesis on its behavior during erection // Urology. 1990. Vol. 36. Р. 68–72.
11. Martin R., Escrig A., Abreu P., Mass M. Androgen-dependent nitric oxide release in rat penis correlated with levels of constitutive nitric oxide synthase isoenzymes // Biol Reprod. 1999.Vol. 61. Р. 1012–1016.
12. Pinsky M.R., Hellstrom W.J. Hypogonadism, ADAM and hormone replacement // Ther Adv Urol. 2010. Vol. 2. Р. 99–104.
13. Carson C.C., Lue T.F. Phosphodiesterase type 5 inhibitors for erectile dysfunction // Br О Urol Int. 2005. Vol. 96. Р. 257–280.
14. Dean R.C., Lue T.F. Physiology of penile erection and pathophysiology of erectile dysfunction // Urol Clin North Am. 2005. Vol. 32. Р. 379–395.
15. Andersson K.-E., Nehra A., Lue T., Burnett A., Goldstein I., Morales A. Erectile physiological and pathophysiological pathways involved in erectile dysfunction // О Urol. 2003. Vol. 170. Р. 6–14.
16. Bivalacqua T.J., Champion H.C., Hellstrom W.J.G., Kadowitz P.J. Pharmacotherapy for erectile dysfunction // Trends Pharmacol Sci. 2000. Vol. 21. Р. 484–489.
17. Gopal V.K., Francis S.H., Corbin J.D. Allosteric sites of phosphodiesterase-5 (PDE5). A potential role of cGMP signaling in corpus cavernosum // Eur О Biochem. 2001. Vol. 268. Р. 3304–3312.
18. Patterson D., Kloner R., Effron M. et al. The effect of tadalafil on the time to exercise-induced myocardial ischemia in subjects with coronary artery disease // Br J Clin Pharmacol. 2005. Vol. 60. Р. 459–468.
19. Fink H.A., Mac Donald R., Rutks I.R. et al. Sildenafil for male erectile dysfunction: a systemic review and metaanaysis // Arch Intern Med. 2002 Jun 24. Vol. 162 (2). Р. 1349–1360.
20. Bannowsky A., Schulze H., van der Horst C., Hautmann S., Junemann K.P. Recovery of erectile function after nerve-sparing radical prostatectomy: improvement with nightly low-dose sildenafil // BJU Int. 2008. Vol. 101. Р. 1279–1283.
21. Padma-Nathan H., McCullough A.R., Levine L.A. et al. Randomized, double-blind, placebo-controlled study of postoperative nightly sildenafil citrate for the prevention of erectile dysfunction after bilateral nerve-sparing radical prostatectomy // Int J Impot Res. 2008. Vol. 20. Р. 479–486.
22. Aversa A., Vitale C., Volterrani M. et al. Chronic administration of sildenafil improves markers of endothelial function in men with type 2 diabetes // Diabet Med. 2008. Vol. 25. Р. 37–44.
23. Mulhall J.P., McLaughlin T.P., Harnett J.P. et al. Medication utilization behavior in patients receiving phosphodiesterase type 5 inhibitors for erectile dysfunction // JSexMed. 2005 Nov. Vol. 2 (6). Р. 848–855.












