–Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є —А–Њ–ї—М –≥–Є–њ–Њ–≤–Њ–ї–µ–Љ–Є–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є —В—П–ґ–µ–ї—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ –њ—А–µ–і–Њ–њ—А–µ–і–µ–ї—П–µ—В –≤–ї–Є—П–љ–Є–µ —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –≤–Њ–ї–µ–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–∞ –Є—Б—Е–Њ–і –Њ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ, –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–—В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –≤–µ–і—Г—Й–∞—П —А–Њ–ї—М –≤ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є –Є –њ–Њ–і–µ—А–ґ–∞–љ–Є–Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–Љ –Ј–∞–њ—А–Њ—Б–∞–Љ –Њ–±—К–µ–Љ–∞ —Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–є –Ї—А–Њ–≤–Є (–Ю–¶–Ъ), –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –≥–µ–Љ–Њ—А–µ–Њ–ї–Њ–≥–Є–Є –Є –≤–Њ–і–љ–Њ-—Н–ї–µ–Ї—В—А–Њ–ї–Є—В–љ–Њ–≥–Њ –±–∞–ї–∞–љ—Б–∞. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–—В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–≥–Њ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є—П –µ–µ –њ—А–Њ–≥—А–∞–Љ–Љ—Л, —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л—Е —Б—А–µ–і, –Є—Е —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є.
–У–Є–њ–Њ–≤–Њ–ї–µ–Љ–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤–Њ–Ј–≤—А–∞—В–∞ –Ї—А–Њ–≤–Є –Ї —Б–µ—А–і—Ж—Г, —Б–љ–Є–ґ–µ–љ–Є—О –Љ–Є–љ—Г—В–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–Є. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н—В–Њ–≥–Њ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —Б–Є–Љ–њ–∞—В–Є–Ї–Њ––∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є –Є –≥–Є–њ–Њ—В–∞–ї–∞–Љ–Њ––≥–Є–њ–Њ—Д–Є–Ј–∞—А–љ–Њ––љ–∞–і–њ–Њ—З–µ—З–љ–Є–Ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Я–µ—А–≤–∞—П —П–≤–ї—П–µ—В—Б—П –љ–µ–є—А–Њ–≥–µ–љ–љ—Л–Љ, —В–Њ –µ—Б—В—М —Б–∞–Љ—Л–Љ –±—Л—Б—В—А—Л–Љ, —А–µ–≥—Г–ї—П—В–Њ—А–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ, –≤—В–Њ—А–∞—П – –≥—Г–Љ–Њ—А–∞–ї—М–љ—Л–Љ, –≤–Ї–ї—О—З–∞—О—Й–Є–Љ—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –њ–Њ–Ј–ґ–µ, –љ–Њ –і–µ–є—Б—В–≤—Г—О—Й–Є–Љ –і–Њ–ї—М—И–µ –њ–Њ –≤—А–µ–Љ–µ–љ–Є. –Т —Б–ї–Њ–ґ–љ–Њ–Љ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, —А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П –њ–Њ—Б–ї–µ –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А–Є, –≤–∞–ґ–љ–Њ–µ –Љ–µ—Б—В–Њ –Њ—В–≤–Њ–і–Є—В—Б—П –љ–∞—А—Г—И–µ–љ–Є—П–Љ –Ї–Є—Б–ї–Њ—А–Њ–і–љ–Њ–≥–Њ —А–µ–ґ–Є–Љ–∞ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є –Є –≥–µ–Љ–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–Њ–Ї—Б–Є–Є. –Ґ–∞–Ї, –њ—А–Є –Љ–∞—Б—Б–Є–≤–љ–Њ–є –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А–µ –љ–µ–Є–Ј–±–µ–ґ–љ–Њ –њ–∞–і–µ–љ–Є–µ —Б–Є—Б—В–µ–Љ–љ–Њ–≥–Њ —В—А–∞–љ—Б–њ–Њ—А—В–∞ –Ї–Є—Б–ї–Њ—А–Њ–і–∞, –Ї–Њ—В–Њ—А—Л–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Б—Е–Њ–і–љ—Л–Љ —Г—А–Њ–≤–љ–µ–Љ –Љ–Њ–ґ–µ—В —Г–Љ–µ–љ—М—И–∞—В—М—Б—П –≤ 3–5 —А–∞–Ј, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –њ–∞–і–µ–љ–Є–µ–Љ –Љ–Є–љ—Г—В–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П. –Я–Њ–≤—Л—И–µ–љ–љ–Њ–µ –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –∞—А—В–µ—А–Є–Њ––≤–µ–љ–Њ–Ј–љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л –Є —А–Њ—Б—В—Г –Ї–Њ—Н—Д—Д–Є—Ж–µ–љ—В–∞ —Г—В–Є–ї–Є–Ј–∞—Ж–Є–Є –µ–≥–Њ –≤ —В–Ї–∞–љ—П—Е. –Ґ–Ї–∞–љ–µ–≤–∞—П –і–Є–Ј–Њ–Ї—Б–Є—П —Б–ї—Г–ґ–Є—В –±–∞–Ј–Њ–є –і–ї—П —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –∞–љ–Њ–Љ–∞–ї—М–љ–Њ–≥–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ —Н–Ї—Б—В—А–∞–Ї—Ж–Є–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–Љ–Є —В–Ї–∞–љ—П–Љ–Є. –Я—А–Њ–Є—Б—Е–Њ–і–Є—В —Н—В–Њ –Ј–∞ —Б—З–µ—В –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –і–µ—Б–∞—В—Г—А–∞—Ж–Є–Є –њ–Њ—Б—В—Г–њ–∞—О—Й–µ–≥–Њ –≤ –Ї–∞–њ–Є–ї–ї—П—А—Л –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞. –°–Є—Б—В–µ–Љ–љ—Л–є –≤—Л–±—А–Њ—Б —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤, –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–Њ–≤, –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II, –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О —В–Ї–∞–љ–µ–≤–Њ–≥–Њ —И—Г–љ—В–∞ —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–µ—А—Д—Г–Ј–Є–Є.
–Ъ–ї–µ—В–Ї–Є –Ї—А–Њ–≤–Є (–љ–µ–є—В—А–Њ—Д–Є–ї—Л, –±–∞–Ј–Њ—Д–Є–ї—Л –Є –і—А.) –Є —Н–љ–і–Њ—В–µ–ї–Є–Њ—Ж–Є—В—Л –њ–µ—А–µ–≤–Њ–і—П—В —Д–∞–Ї—В–Њ—А—Л –∞–≥—А–µ—Б—Б–Є–Є, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –Є—Е —Е–∞—А–∞–Ї—В–µ—А–∞, –≤ —Б–Њ—Б—В–Њ—П–љ–Є–µ «–Ї–Є—Б–ї–Њ—А–Њ–і–љ–Њ–≥–Њ –≤–Ј—А—Л–≤–∞». –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Љ–Њ—Й–љ—Л–є –≤—Л–±—А–Њ—Б —Н—В–Є–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є –≤ –Ї—А–Њ–≤–Њ—В–Њ–Ї –Њ–≥—А–Њ–Љ–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –њ–Њ–ї–Є–Њ—А–≥–∞–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (—Ж–Є—В–Њ–Ї–Є–љ—Л, —Н–є–Ї–Њ—Б–∞–љ–Њ–Є–і—Л, –Њ–Ї—Б–Є–і –∞–Ј–Њ—В–∞, —Д–Є–±—А–Њ–љ–µ–Ї—В–Є–љ, –Ї–Є—Б–ї–Њ—А–Њ–і–љ—Л–µ —А–∞–і–Є–Ї–∞–ї—Л, –њ—А–Њ–і—Г–Ї—В—Л –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤, —Н–љ–Ј–Є–Љ—Л –Є –і—А.) – —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ–Њ–є –Њ—Б–љ–Њ–≤—Л –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є. –Р–Ї—В–Є–≤–∞—Ж–Є—П –Ї–Њ–Љ–њ–ї–µ–Љ–µ–љ—В–∞, –Ї–∞—Б–Ї–∞–і–Њ–≤ –Ї–∞–ї–Є–Ї—А–µ–Є–љ––Ї–Є–љ–Є–љ–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, –≤—Л–±—А–Њ—Б –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –Є–љ–Є—Ж–Є–Є—А—Г—О—В —А–∞–Ј–≤–Є—В–Є–µ –љ–µ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е, —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –і–ї—П –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –ї—О–±–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є, —А–µ–∞–Ї—Ж–Є–є –≥–Є–њ–µ—А–Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ —Б –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Њ–±–Љ–µ–љ–∞ –±–µ–ї–Ї–Њ–≤, —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –ї–Є–њ–Є–і–Њ–≤, —Г—Б–Є–ї–µ–љ–љ—Л–Љ —А–∞—Б—Е–Њ–і–Њ–Љ —Г–≥–ї–µ–≤–Њ–і–љ–Њ––ї–Є–њ–Є–і–љ—Л—Е —А–µ–Ј–µ—А–≤–Њ–≤ –Є —А–∞—Б–њ–∞–і–Њ–Љ —В–Ї–∞–љ–µ–≤—Л—Е –±–µ–ї–Ї–Њ–≤.
–Т —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б–Њ —Б–ї–Њ–ґ–Є–≤—И–µ–є—Б—П –Ї–Њ–љ—Ж–µ–њ—Ж–Є–µ–є –љ–∞—А—Г—И–µ–љ–Є—П —Г–≥–ї–µ–≤–Њ–і–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П —Б–њ–Њ–љ—В–∞–љ–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–µ–є –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –≥–ї—О–Ї–Њ–Ј—Л –≤ —В–Ї–∞–љ—П—Е. –Я—А–Є —Н—В–Њ–Љ –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤—Л—А–∞–±–Њ—В–Ї–Є –≥–ї—О–Ї–Њ–Ј—Л –≤ –њ–µ—З–µ–љ–Є –Њ—В–Љ–µ—З–∞—О—В—Б—П –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј, —Г—Б—В–Њ–є—З–Є–≤—Л–є –Ї –≤–≤–µ–і–µ–љ–Є—О —Н–Ї–Ј–Њ–≥–µ–љ–љ–Њ–є –≥–ї—О–Ї–Њ–Ј—Л, —Б–Њ—З–µ—В–∞–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ —Б —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М—О –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —В–Ї–∞–љ–µ–є (–Љ—Л—И—Ж) –Ї –≥–ї—О–Ї–Њ–Ј–µ.
–†–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –±–µ–ї–Ї–Њ–≤–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П —Г—Б–Ї–Њ—А–µ–љ–љ—Л–Љ —А–∞—Б–њ–∞–і–Њ–Љ –њ—А–Њ—В–µ–Є–љ–Њ–≤, –Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є–µ–є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Є–Ј –Љ–Є–Њ—Ж–Є—В–Њ–≤ —Б–Ї–µ–ї–µ—В–љ–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –і–ї—П –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –њ–µ—З–µ–љ–Њ—З–љ–Њ–≥–Њ –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ –Є —Б–Є–љ—В–µ–Ј–∞ –Њ—Б—В—А–Њ—Д–∞–Ј–љ—Л—Е –±–µ–ї–Ї–Њ–≤. –Ю–і–љ–∞–Ї–Њ —Б–Є–љ—В–µ–Ј –±–µ–ї–Ї–∞ –љ–µ –Ї–Њ–Љ–њ–µ–љ—Б–Є—А—Г–µ—В –≤–Њ–Ј—А–∞—Б—В–∞—О—Й–Є–є –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ –Љ—Л—И–µ—З–љ—Л—Е –Є –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л—Е –±–µ–ї–Ї–Њ–≤, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–Љ—Г –∞–Ј–Њ—В–Є—Б—В–Њ–Љ—Г –±–∞–ї–∞–љ—Б—Г. –Я–Њ—В–µ—А–Є –±–µ–ї–Ї–Њ–≤ –Љ–Њ–≥—Г—В –і–Њ—Б—В–Є–≥–∞—В—М –±–Њ–ї–µ–µ 20 –≥ –≤ —Б—Г—В–Ї–Є –Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–є –њ–Њ—В–µ—А–µ–є –Љ–∞—Б—Б—Л —В–µ–ї–∞.
–Ы–Є–њ–Є–і—Л –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б—Е–Њ–і—Г–µ–Љ—Л–Љ –Є—Б—В–Њ—З–љ–Є–Ї–∞–Љ —Н–љ–µ—А–≥–Є–Є. –Я—А–Њ—Ж–µ—Б—Б –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –ї–Є–њ–Є–і–Њ–≤ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ґ–Є—А–Њ–≤, –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –ї–Є–њ–Њ–ї–Є–Ј–∞, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ––ї–Є–њ–∞–Ј—Л. –Ц–Є—А–Њ–≤–∞—П —В–Ї–∞–љ—М —А–∞—Б–њ–∞–і–∞–µ—В—Б—П –љ–∞ –ґ–Є—А–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л, –њ–Њ–њ–∞–і–∞—О—Й–Є–µ –≤ —Б–Є—Б—В–µ–Љ–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –Є –њ–µ—З–µ–љ—М. –Я–Њ–≤—Л—И–µ–љ–љ–Њ–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –≤ —Б–Є—Б—В–µ–Љ–љ—Л–є –Ї—А–Њ–≤–Њ—В–Њ–Ї —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Б–љ–Є–ґ–µ–љ–Є—О —Г—В–Є–ї–Є–Ј–∞—Ж–Є–Є —В–Ї–∞–љ—П–Љ–Є –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ –Ј–∞ —Б—З–µ—В –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–љ––ї–Є–њ–∞–Ј—Л.
–Э–∞—А—Г—И–µ–љ–Є—П –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞ –њ—А–Њ—П–≤–ї—П—О—В—Б—П –Ј–∞–Љ–µ—В–љ—Л–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –≤ –Ї—А–Њ–≤–Є —Г—А–Њ–≤–љ—П –∞–і—А–µ–љ–∞–ї–Є–љ–∞, –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞, –≥–ї—О–Ї–Њ–≥–µ–љ–∞ –Є –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤. –Т –њ—А–Њ—В–Є–≤–Њ–≤–µ—Б —Г–≤–µ–ї–Є—З–µ–љ–Є—О —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В–Є –Ї –Є–љ—Б—Г–ї–Є–љ—Г –µ–≥–Њ —Г—А–Њ–≤–µ–љ—М –≤ –Ї—А–Њ–≤–Є –њ–Њ–≤—Л—И–∞–µ—В—Б—П. –†–µ–Ј–Ї–Њ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —Г—В–Є–ї–Є–Ј–∞—Ж–Є—П —Н–љ–µ—А–≥–Њ–Є—Б—В–Њ—З–љ–Є–Ї–Њ–≤ – –Њ—Б–љ–Њ–≤–љ–Њ–є –Њ–±–Љ–µ–љ –њ–Њ–≤—Л—И–∞–µ—В—Б—П –љ–∞ 10–100% (–≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –∞–≥—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞).
–Ш–Ј–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤, —А–∞–Ј–≤–Є–≤–∞—О—Й–µ–µ—Б—П –≤ –њ–Њ—Б—В–≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–Љ –њ–µ—А–Є–Њ–і–µ, —П–≤–ї—П–µ—В—Б—П –Њ—В—А–∞–ґ–µ–љ–Є–µ–Љ –Њ–±—Й–Є—Е –љ–µ–є—А–Њ—Н–љ–і–Њ–Ї—А–Є–љ–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ –Ю–¶–Ъ –Є —Д—Г–љ–Ї—Ж–Є–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –љ–∞ —Г—А–Њ–≤–љ–µ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є —В–Ї–∞–љ–µ–є. –Т —Г—Б–ї–Њ–≤–Є—П—Е —А–∞–Ј–≤–Є–≤—И–µ–є—Б—П –≥–Є–њ–Њ–Ї—Б–Є–Є –∞—Н—А–Њ–±–љ—Л–є –њ—Г—В—М –Њ–±–Љ–µ–љ–∞ –Љ–µ–љ—П–µ—В—Б—П –љ–∞ –∞–љ–∞—Н—А–Њ–±–љ—Л–є, –Ї–Њ—В–Њ—А—Л–є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ–Љ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤. –Ю–і–љ–Є–Љ –Є–Ј –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –∞–љ–∞—Н—А–Њ–±–љ–Њ–є –Є–љ–≤–µ—А—Б–Є–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –њ—А–Є —Н—В–Њ–Љ —П–≤–ї—П–µ—В—Б—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –Љ–Њ–ї–Њ—З–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≤–Љ–µ—Б—В–Њ –°–Ю2, —З—В–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –Љ–µ–љ—М—И–Є–Љ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ–Љ –њ–Є—А—Г–≤–∞—В–∞ –≤ —Ж–Є–Ї–ї –Ъ—А–µ–±—Б–∞ –њ—А–Є –≥–Є–њ–Њ–Ї—Б–Є–Є –Є –±–Њ–ї—М—И–Є–Љ –њ–µ—А–µ–≤–Њ–і–Њ–Љ –µ–≥–Њ –≤ –ї–∞–Ї—В–∞—В. –Я—А–Є —Н—В–Њ–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –ї–∞–Ї—В–∞—В/–њ–Є—А—Г–≤–∞—В –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –ї–∞–Ї—В–∞—В–∞ –Љ–Њ–ґ–µ—В –≤–Њ–Ј—А–∞—Б—В–∞—В—М –≤ 4–5 —А–∞–Ј.
–Т–Њ–Ј—А–Њ—Б—И–∞—П –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М –≤ —Н–љ–µ—А–≥–Є–Є –Є –Њ–≥—А–∞–љ–Є—З–µ–љ–љ–Њ—Б—В—М –Ј–∞–њ–∞—Б–Њ–≤ —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –≤—Л–Ј—Л–≤–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Є –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –ґ–Є—А–Њ–≤ –Є –±–µ–ї–Ї–Њ–≤. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ —Н—В–Њ–≥–Њ –≤ –Ї—А–Њ–≤–Є –љ–∞–Ї–∞–њ–ї–Є–≤–∞—О—В—Б—П –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ—Л–µ –Є –Ї–Њ–љ–µ—З–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є, –њ—А–Є–≤–Њ–і—П –Ї —А–∞–Ј–≤–Є—В–Є—О –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –∞—Ж–Є–і–Њ–Ј–∞ –Є —Б–Є—Б—В–µ–Љ–љ–Њ–є —Н–љ–і–Њ—В–Њ–Ї—Б–µ–Љ–Є–Є. –Я—А–Є —Н—В–Њ–Љ –Ј–љ–∞—З–µ–љ–Є–µ —А–Э –Ї—А–Њ–≤–Є –љ–∞ –њ–Њ–Ј–і–љ–Є—Е —Б—В–∞–і–Є—П—Е –Љ–Њ–ґ–µ—В –і–Њ—Б—В–Є–≥–∞—В—М 7,0 —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –і–µ—Д–Є—Ж–Є—В–∞ –±—Г—Д–µ—А–љ—Л—Е –Њ—Б–љ–Њ–≤–∞–љ–Є–є, –∞ —А–∞–Ј–≤–Є–≤–∞—О—Й–∞—П—Б—П —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–∞—П –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є—П –Ј–∞—З–∞—Б—В—Г—О –±—Л–≤–∞–µ—В –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ—Б—В—А–∞—П –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А—П —П–≤–ї—П–µ—В—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ –∞–≥—А–µ—Б—Б–Є–Є, —Б–њ–Њ—Б–Њ–±–љ—Л–Љ –њ—А–Є–≤–Њ–і–Є—В—М –Ї –Њ—А–≥–∞–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є –≥–ї—Г–±–Њ–Ї–Є–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞, —З—В–Њ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–µ–Є–Ј–±–µ–ґ–љ–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —И–Њ–Ї–∞, –њ–Њ–ї–Є–Њ—А–≥–∞–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є —Б –≤—Л—Б–Њ–Ї–Њ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М—О –ї–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞.
–Ь–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В –љ–∞ —Б—В—А–µ—Б—Б –љ–Њ—Б–Є—В —Д–∞–Ј–Њ–≤—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Я–µ—А–≤–∞—П —Д–∞–Ј–∞ (ebb phase) – –њ–µ—А–≤—Л–µ 12–24 —З –њ–Њ—Б–ї–µ –∞–≥—А–µ—Б—Б–Є–Є – —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л —В–µ–ї–∞, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –Ї–Є—Б–ї–Њ—А–Њ–і–∞, –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є–µ–є. –Т–Њ –≤—В–Њ—А–Њ–є —Д–∞–Ј–µ (flow phase) –њ—А–Њ–Є—Б—Е–Њ–і—П—В –∞–Ї—В–Є–≤–∞—Ж–Є—П –∞–і—А–µ–љ–∞–ї–Њ–≤–Њ–є —Б–Є—Б—В–µ–Љ—Л, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–∞—В–∞–±–Њ–ї–Є–Ј–Љ–∞, –њ–Њ–≤—Л—И–µ–љ–Є–µ –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –Ї–Є—Б–ї–Њ—А–Њ–і–∞, –±—Л—Б—В—А–∞—П –њ–Њ—В–µ—А—П –∞–Ј–Њ—В–∞. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –љ–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–Ј–Њ—В–Є—Б—В–Њ–≥–Њ –±–∞–ї–∞–љ—Б–∞ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≤–ї–Є—П–љ–Є–µ –љ–∞—А—Г—И–µ–љ–Є–µ –њ–Є—В–∞–љ–Є—П –±–Њ–ї—М–љ–Њ–≥–Њ (—В—П–ґ–µ–ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ, –Ї–Њ–Љ–∞, –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–є –Ц–Ъ–Ґ –Є —В. –і.) –Є –њ—А—П–Љ–∞—П –њ–Њ—В–µ—А—П –±–µ–ї–Ї–∞ (–Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А—П, –њ—А–Њ—В–µ–Є–љ—Г—А–Є—П, —А–∞–љ—Л, –љ–µ–Ї—А–Њ–Ј—Л, –Њ–ґ–Њ–≥–Є –Є –њ—А.). –Я—А–Є —Н—В–Њ–Љ —В—П–ґ–µ—Б—В—М –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–∞–њ—А—П–Љ—Г—О –Ј–∞–≤–Є—Б—П—В –Њ—В —Б—В–µ–њ–µ–љ–Є –∞–≥—А–µ—Б—Б–Є–Є, –≤–Є–і–∞ –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
–Ф–ї—П –њ–µ—А–≤–Њ–є —Д–∞–Ј—Л —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –љ–∞–њ—А—П–ґ–µ–љ–Є–µ –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Љ–Њ–±–Є–ї–Є–Ј–∞—Ж–Є—П —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є—Е —А–µ—Б—Г—А—Б–Њ–≤ –≤ –Є–љ—В–µ—А–µ—Б–∞—Е –ґ–Є–Ј–љ–µ–љ–љ–Њ –≤–∞–ґ–љ—Л—Е –Њ—А–≥–∞–љ–Њ–≤ –Є —Б–Є—Б—В–µ–Љ (–¶–Э–°, –і—Л—Е–∞–љ–Є–µ –Є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є–µ). –†–µ–∞–Ї—Ж–Є—П –љ–∞ —Б—В—А–µ—Б—Б – —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ —Н–љ–µ—А–≥–Њ–µ–Љ–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б. –Ю—Б–љ–Њ–≤–љ—Л–Љ —Н–љ–і–Њ–≥–µ–љ–љ—Л–Љ –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ —Н–љ–µ—А–≥–Є–Є —П–≤–ї—П—О—В—Б—П –Љ—Л—И–µ—З–љ—Л–µ –±–µ–ї–Ї–Є –Є –ґ–Є—А–Њ–≤—Л–µ –і–µ–њ–Њ. –Э–µ—Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ –љ–∞—З–∞—В–Њ–µ –Є –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –≤–µ–і–µ—В –Ї —Б—А—Л–≤—Г –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –Є —В–Њ–≥–і–∞ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –њ—А—П–Љ–∞—П —Г–≥—А–Њ–Ј–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ–Њ–≥–Њ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –µ–≥–Њ –љ–∞—З–∞–ї–∞, –њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ—Б—В–Є –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤—Б–µ–Љ–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ–Є –љ—Г—В—А–Є–µ–љ—В–∞–Љ–Є –Є –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —Б—А–Њ–Ї–Њ–≤ –њ—А–Њ–≤–µ–і–µ–љ–Є—П. –Я–Њ—Б–ї–µ–і–љ–µ–µ –Њ–Ј–љ–∞—З–∞–µ—В, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –Я–Я –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П —Б—А–Њ–Ї–∞–Љ–Є —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞.
–Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М —А–µ—И–µ–љ–Є–µ —Н—В–Њ–є –Ј–∞–і–∞—З–Є –≤ –њ–µ—А–≤–Њ–є —Д–∞–Ј–µ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П —Б—А–µ–і—Б—В–≤–∞–Љ–Є –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–є –љ–∞ —Г—Б—В—А–∞–љ–µ–љ–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є, –љ–∞—А—Г—И–µ–љ–Є–є –Ї–Є—Б–ї–Њ—В–љ–Њ-–Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П (–Ъ–Ю–°), –Ї–Њ—А—А–µ–Ї—Ж–Є—О –≥–Є–њ–Њ–≤–Њ–ї–µ–Љ–Є–Є –Є –≥–∞–Ј–Њ–≤–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞, –∞ —В–∞–Ї–ґ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є —В—А–∞–љ—Б–њ–Њ—А—В–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –Ї—А–Њ–≤–Є. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ —В–µ–љ–і–µ–љ—Ж–Є–Є –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Њ–±—К–µ–Љ–∞ –≥–µ–Љ–Њ—В—А–∞–љ—Б—Д—Г–Ј–Є–Є, –≤—Л—П–≤–ї–µ–љ–љ—Л–µ –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —А–∞—Б—В–≤–Њ—А–Њ–≤ –љ–∞ –Њ—Б–љ–Њ–≤–µ –і–µ–Ї—Б—В—А–∞–љ–∞, –њ–ї–∞–Ј–Љ—Л –Є –∞–ї—М–±—Г–Љ–Є–љ–∞ —З–µ–ї–Њ–≤–µ–Ї–∞ –і–Є–Ї—В—Г—О—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ —Б–Њ–≤–µ—А—И–µ–љ—Б—В–≤–Њ–≤–∞–љ–Є—П –Љ–µ—В–Њ–і–Њ–≤ –Є —Б—А–µ–і—Б—В–≤ –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–—В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–Њ –≤—А–µ–Љ—П –Њ–њ–µ—А–∞—Ж–Є–Є –Є –≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ. –†–∞–Ј—А–∞–±–Њ—В–Ї–∞ –Є –њ—А–Њ–Є–Ј–≤–Њ–і—Б—В–≤–Њ –љ–Њ–≤—Л—Е –Ї–Њ–ї–ї–Њ–Є–і–љ—Л—Е –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л—Е —А–∞—Б—В–≤–Њ—А–Њ–≤ –љ–∞ –Њ—Б–љ–Њ–≤–µ –≥–Є–і—А–Њ–Ї—Б–Є—Н—В–Є–ї–Ї—А–∞—Е–Љ–∞–ї–∞ (—А–µ—Д–Њ—А—В–∞–љ, —Б—В–∞–±–Є–Ј–Њ–ї, –•–Р–Х–°, –≤–Њ–ї—О–≤–µ–љ) –Є –Љ–Њ–і–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –ґ–µ–ї–∞—В–Є–љ—Л (–≥–µ–ї–Њ—Д—Г–Ј–Є–љ) —Б—В–∞–ї–Є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –Ї–Њ–ї–ї–Њ–Є–і–љ—Л—Е –њ–ї–∞–Ј–Љ–Њ–Ј–∞–Љ–µ–љ–Є—В–µ–ї–µ–є –љ–∞ –Њ—Б–љ–Њ–≤–µ –і–µ–Ї—Б—В—А–∞–љ–∞.
–Э–∞ –≤—В–Њ—А–Њ–Љ —Н—В–∞–њ–µ —Б —Ж–µ–ї—М—О —Б–љ–Є–ґ–µ–љ–Є—П –Ї–∞—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–Ї—Ж–Є–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є—П —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞—В—А–∞—В –Є –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤ –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Г—О —В–µ—А–∞–њ–Є—О –≤–Ї–ї—О—З–∞—О—В —Б—А–µ–і—Л –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П. –Ю–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ–Є —Г—Б–ї–Њ–≤–Є—П–Љ–Є –љ–∞—З–∞–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П (–Я–Я) –Є —Г—Б–≤–Њ–µ–љ–Є—П –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е –≤–µ—Й–µ—Б—В–≤, –≤–≤–Њ–і–Є–Љ—Л—Е –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ, —П–≤–ї—П—О—В—Б—П:
- –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–µ —Г—Б—В—А–∞–љ–µ–љ–Є–µ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤;
- –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є–µ –і–µ—Д–Є—Ж–Є—В–∞ –≥–ї–Њ–±—Г–ї—П—А–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞, –Њ–±—К–µ–Љ–∞ –њ–ї–∞–Ј–Љ—Л –Є –Ю–¶–Ъ;
- –ї–Є–Ї–≤–Є–і–∞—Ж–Є—П –≥—А—Г–±—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Ъ–Ю–°;
- —Г–ї—Г—З—И–µ–љ–Є–µ —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є;
- —Г–ї—Г—З—И–µ–љ–Є–µ –Љ–∞–Ї—А–Њ– –Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є.
–Т—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П –Я–Я –і–Њ–ї–ґ–µ–љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞—В—М –µ–≥–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ –Ј–∞–і–∞—З–∞–Љ – –≤–Њ–і–љ–Њ–—Н–ї–µ–Ї—В—А–Њ–ї–Є—В–љ–Њ–Љ—Г, —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–Љ—Г –Є –њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–Љ—Г –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—О –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Ю–±—К–µ–Љ –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л—Е —Б—А–µ–і –Є —В–µ–Љ–њ –≤–≤–µ–і–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї—П—О—В—Б—П –≤–∞—А–Є–∞–љ—В–Њ–Љ –Я–Я (–њ–Њ–ї–љ–Њ–µ, —З–∞—Б—В–Є—З–љ–Њ–µ –Є–ї–Є —Б–Љ–µ—И–∞–љ–љ–Њ–µ), –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Я–Я, –Є—Б—Е–Њ–і–љ—Л–Љ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Д–Њ–љ–Њ–Љ, –≤—А–µ–Љ–µ–љ–µ–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —В—А–∞–≤–Љ—Л (—А–∞–љ–µ–љ–Є—П, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П) –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М—О –љ–∞—А—Г—И–µ–љ–Є–є –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞ (–≥–Є–њ–Њ–≥–Є–і—А–∞—В–∞—Ж–Є—П, –≥–Є–њ–Њ–Ї–∞–ї–Є–µ–Љ–Є—П, –≥–Є–њ–µ—А–Њ—Б–Љ–Њ–ї—П—А–љ–Њ—Б—В—М, –±–µ–ї–Ї–Њ–≤–Њ–—Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–є –ї–µ–≥–Ї–Є—Е, –њ–µ—З–µ–љ–Є, –њ–Њ—З–µ–Ї).
–Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ, –Ї–∞–Ї –Є –Њ–±—Л—З–љ–Њ–µ –Њ—А–∞–ї—М–љ–Њ–µ, –і–Њ–ї–ґ–љ–Њ –±—Л—В—М —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–Њ –Є –њ–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г, –Є –њ–Њ –Ї–∞—З–µ—Б—В–≤—Г –Є–љ–≥—А–µ–і–Є–µ–љ—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Б–Њ–і–µ—А–ґ–∞—В—М –∞–Ј–Њ—В—Б–Њ–і–µ—А–ґ–∞—Й–Є–µ –Є —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–µ –≤–µ—Й–µ—Б—В–≤–∞, —Н–ї–µ–Ї—В—А–Њ–ї–Є—В—Л, –≤–Є—В–∞–Љ–Є–љ—Л. –Т–µ—Б—М –љ–∞–±–Њ—А –љ—Г—В—А–Є–µ–љ—В–Њ–≤, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –і–ї—П —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –њ–Њ–ї–љ–Њ–≥–Њ –Я–Я –Љ–Њ–ґ–љ–Њ –њ—А–µ–і—Б—В–∞–≤–Є—В—М –і–≤—Г–Љ—П –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –≥—А—Г–њ–њ–∞–Љ–Є: –Є—Б—В–Њ—З–љ–Є–Ї–Є —Н–љ–µ—А–≥–Є–Є (—Г–≥–ї–µ–≤–Њ–і—Л, –ї–Є–њ–Є–і—Л) –Є –њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–є –Љ–∞—В–µ—А–Є–∞–ї –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞ (—А–∞—Б—В–≤–Њ—А—Л –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В), –≤–Њ–і–∞, —Н–ї–µ–Ї—В—А–Њ–ї–Є—В—Л, –≤–Є—В–∞–Љ–Є–љ—Л, –Љ–Є–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В—Л. –Т–Њ–і–∞ –Є —А—П–і —Н–ї–µ–Ї—В—А–Њ–ї–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –Є –Љ–Є–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Њ—В–љ–Њ—Б—П—В—Б—П –Ї —А–∞–Ј—А—П–і—Г –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –≤–µ—Й–µ—Б—В–≤. –Ґ–µ—А–Љ–Є–љ «–љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ» –њ—А–Є–Љ–µ–љ–Є–Љ –Ї —В–µ–Љ —Б—Г–±—Б—В–∞–љ—Ж–Є—П–Љ, –Ї–Њ—В–Њ—А—Л–µ —П–≤–ї—П—О—В—Б—П –ґ–Є–Ј–љ–µ–љ–љ–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–Љ–Є –Є –љ–µ —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В—Б—П —Б–∞–Љ–Є–Љ –Њ—А–≥–∞–љ–Є–Ј–Љ–Њ–Љ –Є–ї–Є —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В—Б—П –≤ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ.
–†–∞—Б—В–≤–Њ—А—Л –Ї—А–Є—Б—В–∞–ї–ї–Є—З–µ—Б–Ї–Є—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В – –Њ—Б–љ–Њ–≤–љ–Њ–є –Є—Б—В–Њ—З–љ–Є–Ї –∞–Ј–Њ—В–∞, –њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Љ–∞—В–µ—А–Є–∞–ї–∞ –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞.
–°–Њ—Б—В–∞–≤ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л—Е —Б–Љ–µ—Б–µ–є –Њ—Ж–µ–љ–Є–≤–∞—О—В –њ–Њ –Є—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Ж–µ–љ–љ–Њ—Б—В–Є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–Њ–≥–Њ –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј–∞. –С–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Ж–µ–љ–љ–Њ—Б—В—М –љ–∞—В—Г—А–∞–ї—М–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –µ–≥–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –≤–Њ—Б–њ–Њ–ї–љ–Є—В—М –±–µ–ї–Ї–Њ–≤—Л–µ –њ–Њ—В–µ—А–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Я—А–Є —Н—В–Њ–Љ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ –≤–≤–Њ–і–Є–Љ—Л–є –Њ–±—К–µ–Љ –і–Њ–ї–ґ–µ–љ –Њ–±–µ—Б–њ–µ—З–Є—В—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є –∞–Ј–Њ—В–Є—Б—В—Л–є –±–∞–ї–∞–љ—Б.
–Р–і–µ–Ї–≤–∞—В–љ–Њ—Б—В—М –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л—Е —Б–Љ–µ—Б–µ–є (–±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Ж–µ–љ–љ–Њ—Б—В—М) –Њ—Ж–µ–љ–Є–≤–∞—О—В –њ–Њ –љ–∞–ї–Є—З–Є—О –Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—О –≤ –Є—Е —Б–Њ—Б—В–∞–≤–µ –Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –Є –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –∞–Ј–Њ—В–∞. –†–∞—Б—В–≤–Њ—А—Л –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –Њ—Б–љ–Њ–≤–∞–љ–љ—Л–µ –љ–∞ —Б—Е–µ–Љ–µ W.C. Rose, –Њ–±—Л—З–љ–Њ —Б–Њ–і–µ—А–ґ–∞—В —В–Њ–ї—М–Ї–Њ 25% –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–µ—В –Є—Е –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Ж–µ–љ–љ–Њ—Б—В—М. –° —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ–Њ–Ј–Є—Ж–Є–є –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ–Є —Б—З–Є—В–∞—О—В —В–µ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л–µ —Б–Љ–µ—Б–Є, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–і–µ—А–ґ–∞—В –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–µ –Є –Ј–∞–Љ–µ–љ–Є–Љ—Л–µ L––∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –≤ —В–µ—Е –ґ–µ –њ—А–Њ–њ–Њ—А—Ж–Є—П—Е, –≤ –Ї–∞–Ї–Є—Е –Њ–љ–Є –љ–∞—Е–Њ–і—П—В—Б—П –≤ —П–Є—З–љ–Њ–Љ –±–µ–ї–Ї–µ. –Ч–љ–∞—З–µ–љ–Є–µ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Ж–µ–љ–љ–Њ—Б—В–Є –≤—Л—А–∞–ґ–∞–µ—В—Б—П –≤ –њ—А–Њ—Ж–µ–љ—В–∞—Е –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —Б–Њ—Б—В–∞–≤–∞ —Ж–µ–ї—М–љ–Њ–≥–Њ —П–Є—З–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ (100%), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —В–Њ—З–љ–Њ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞—В—М –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Ж–µ–љ–љ–Њ—Б—В—М –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л—Е —Б–Љ–µ—Б–µ–є. –І–µ–Љ –≤—Л—И–µ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Ж–µ–љ–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞, —В–µ–Љ –±–Њ–ї—М—И–µ –µ–≥–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –Њ–±–µ—Б–њ–µ—З–Є—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є —Н–љ–і–Њ–≥–µ–љ–љ—Л–є —Б–Є–љ—В–µ–Ј –±–µ–ї–Ї–∞.
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Ж–µ–љ–љ–Њ—Б—В–Є —А–∞—Б—В–≤–Њ—А–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Њ—В—А–∞–ґ–∞–µ—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–Ї–∞–Ј–∞—В—М –≤–ї–Є—П–љ–Є–µ –љ–∞ –∞–Ј–Њ—В–Є—Б—В—Л–є –±–∞–ї–∞–љ—Б. –Ъ–Њ—А—А–µ–Ї—Ж–Є—П –∞–Ј–Њ—В–Є—Б—В–Њ–≥–Њ –±–∞–ї–∞–љ—Б–∞, –Є –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Г—Б—В—А–∞–љ–µ–љ–Є—П –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–Ј–Њ—В–Є—Б—В–Њ–≥–Њ –±–∞–ї–∞–љ—Б–∞, —П–≤–ї—П–µ—В—Б—П —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ—Л–Љ –Њ–±—Б—В–Њ—П—В–µ–ї—М—Б—В–≤–Њ–Љ –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Я–Я –≤ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є. –Т–≤–µ–і–µ–љ–Є–µ —А–∞—Б—В–≤–Њ—А–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –љ–Є–Ј–Ї–Њ–є –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Ж–µ–љ–љ–Њ—Б—В–Є –Є —Б –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –∞–Ј–Њ—В–∞ –Є–ї–Є –љ–µ–њ–Њ–ї–љ–Њ—Ж–µ–љ–љ—Л–Љ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ—Л–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –±—Г–і–µ—В –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ—Л–є –∞–Ј–Њ—В–Є—Б—В—Л–є –±–∞–ї–∞–љ—Б. –Ю—Б–љ–Њ–≤–љ—Л–Љ —В—А–µ–±–Њ–≤–∞–љ–Є–µ–Љ, –њ—А–µ–і—К—П–≤–ї—П–µ–Љ—Л–Љ –Ї —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–Љ —А–∞—Б—В–≤–Њ—А–∞–Љ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, —П–≤–ї—П–µ—В—Б—П –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ 8 –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, 6 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В (–∞–ї–∞–љ–Є–љ, –≥–ї–Є—Ж–Є–љ, —Б–µ—А–Є–љ, –њ—А–Њ–ї–Є–љ, –≥–ї—О—В–∞–Љ–Є–љ–Њ–≤–∞—П –Є –∞—Б–њ–∞—А–∞–≥–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В—Л), —Б–Є–љ—В–µ–Ј–Є—А—Г–µ–Љ—Л—Е –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Є–Ј —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –Є 4 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В (–∞—А–≥–Є–љ–Є–љ, –≥–Є—Б—В–Є–і–Є–љ, —В–Є—А–Њ–Ј–Є–љ –Є —Ж–Є—Б—В–µ–Є–љ), –Ї–Њ—В–Њ—А—Л–µ —Б–Є–љ—В–µ–Ј–Є—А—Г—О—В—Б—П –≤ –љ–µ–Љ –≤ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ. –Ъ –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ —А–∞—Б—В–≤–Њ—А–Њ–≤ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Њ—В–љ–Њ—Б—П—В: —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –љ–µ –Љ–µ–љ–µ–µ 5%, –≤ —В–Њ–Љ —З–Є—Б–ї–µ 30% –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е, –њ—А–Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є –ї–µ–є—Ж–Є–љ/–Є–Ј–Њ–ї–µ–є—Ж–Є–љ (LEU/ILE) –Њ–Ї–Њ–ї–Њ 1,6, —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Є –Њ–±—Й–µ–≥–Њ –∞–Ј–Њ—В–∞ (–Х/–Ґ) –Њ–Ї–Њ–ї–Њ 3 –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Я–Я —Г —В—П–ґ–µ–ї—Л—Е –±–Њ–ї—М–љ—Л—Е –Є 1,4–1,8 –њ—А–Є –љ—Г—В—А–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –ї–µ–≥–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є.
–Ъ—А–Њ–≤—М, –њ–ї–∞–Ј–Љ–∞, –∞–ї—М–±—Г–Љ–Є–љ –љ–µ —П–≤–ї—П—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –≥–Є–і—А–Њ–ї–Є–Ј –Є—Е –±–µ–ї–Ї–Њ–≤—Л—Е –Љ–Њ–ї–µ–Ї—Г–ї –≤ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –Ј–∞–љ–Є–Љ–∞–µ—В –±–Њ–ї–µ–µ 24 —Б—Г—В.
–†–∞—Б—В–≤–Њ—А—Л –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –і–ї—П –Я–Я, –њ–Њ–і—А–∞–Ј–і–µ–ї—П—О—В –љ–∞ —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –Є —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ. –°—В–∞–љ–і–∞—А—В–љ—Л–µ —А–∞—Б—В–≤–Њ—А—Л –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ—Л –і–ї—П –≤–Ј—А–Њ—Б–ї—Л—Е –±–Њ–ї—М–љ—Л—Е. –°–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ —А–∞—Б—В–≤–Њ—А—Л –≤–Ї–ї—О—З–∞—О—В: –њ–Є—В–∞—В–µ–ї—М–љ—Л–µ —Б–Љ–µ—Б–Є –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –і–µ—В–µ–є, –і–ї—П –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А–Њ–є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–µ—З–µ–љ–Є –Є –і–ї—П –ї–µ—З–µ–љ–Є—П –њ–µ—З–µ–љ–Њ—З–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, –њ—А–µ–њ–∞—А–∞—В—Л —Б –≤—Л—Б–Њ–Ї–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–µ–є —А–∞–Ј–≤–µ—В–≤–ї–µ–љ–љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В – –і–ї—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –±–Њ–ї—М–љ—Л—Е –≤ –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≥–Є–њ–µ—А–Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ (—В—А–∞–≤–Љ–∞, —Б–µ–њ—Б–Є—Б, –Њ–ґ–Њ–≥–Є).
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б—Г—Й–µ—Б—В–≤—Г–µ—В –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—О –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –Є –Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В – –њ–Њ–ї–Є–∞–Љ–Є–љ, –∞–Љ–Є–љ–Њ—Б—В–µ—А–Є–ї –Ъ–Х 10%, –≤–∞–Љ–Є–љ, –≥–ї–∞–Љ–Є–љ, –Є–љ—Д–µ–Ј–Њ–ї 40, –∞–Љ–Є–љ–Њ–њ–ї–∞–Ј–Љ–∞–ї—М (5%, 10% –Х), –∞–Љ–Є–љ–Њ—Б–Њ–ї (600, 800, –Ъ–Х) («–•–µ–Љ–Њ—Д–∞—А–Љ», –Ѓ–≥–Њ—Б–ї–∞–≤–Є—П), —Д—А–µ–∞–Љ–Є–љ III 8,5%. –°–Њ—Б—В–∞–≤ —Б—В–∞–љ–і–∞—А—В–љ—Л—Е —А–∞—Б—В–≤–Њ—А–Њ–≤ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –њ—А–Є–≤–µ–і–µ–љ –≤ —В–∞–±–ї. 1 –Є 2. –°–Њ–і–µ—А–ґ–∞–љ–Є–µ 8 –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В 35–45%.
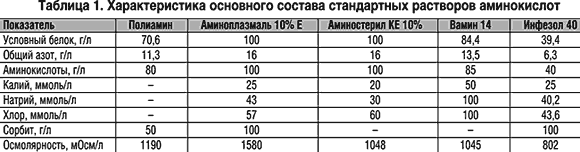

–Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤–≤–Њ–і–Є–Љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –і–ї—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –±–µ–ї–Ї–Њ–≤–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –∞–Ј–Њ—В–Є—Б—В—Л–Љ –±–∞–ї–∞–љ—Б–Њ–Љ. –Т –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е –і–Њ–Ј–∞ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В —Б–Њ—Б—В–∞–≤–ї—П–µ—В 0,8–1,5 –≥/–Ї–≥/—Б—Г—В, –њ—А–Є —В—П–ґ–µ–ї—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е, —Б–Є–љ–і—А–Њ–Љ–µ –≥–Є–њ–µ—А–Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ – 1,5–2,0 –≥/–Ї–≥/—Б—Г—В. –Э–µ –Љ–µ–љ–µ–µ –≤–∞–ґ–љ—Л–Љ –і–ї—П —Г—В–Є–ї–Є–Ј–∞—Ж–Є–Є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Є —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞ —П–≤–ї—П–µ—В—Б—П —Д–∞–Ї—В–Њ—А –≤—А–µ–Љ–µ–љ–Є – –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –≤–≤–µ–і–µ–љ–Є—П —А–∞—Б—В–≤–Њ—А–Њ–≤ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В. –Ю–њ—В–Є–Љ–∞–ї—М–љ–Њ–є —Б—З–Є—В–∞–µ—В—Б—П —Б–Ї–Њ—А–Њ—Б—В—М –≤–≤–µ–і–µ–љ–Є—П –і–Њ 0,1 –≥/–Ї–≥/—З–∞—Б.
–У–ї—О–Ї–Њ–Ј–∞ – –Њ—Б–љ–Њ–≤–љ–Њ–є –Є—Б—В–Њ—З–љ–Є–Ї —Н–љ–µ—А–≥–Є–Є –Є —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –∞ —В–∞–Ї–ґ–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –±–µ–ї–Ї–∞ –≤ –њ—А–∞–Ї—В–Є–Ї–µ –Я–Я. –Т –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –Њ—А–≥–∞–љ–Є–Ј–Љ –Є—Б–њ–Њ–ї—М–Ј—Г–µ—В –≤–≤–µ–і–µ–љ–љ—Л–µ –Є–ї–Є —Н–љ–і–Њ–≥–µ–љ–љ—Л–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є—Б—В–Њ—З–љ–Є–Ї–∞ —Н–љ–µ—А–≥–Є–Є, –∞ –љ–µ –і–ї—П –њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е —Ж–µ–ї–µ–є. –£—Б–Є–ї–µ–љ–Є–µ –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ –Є –Є—Б—В–Њ—Й–µ–љ–Є–µ –Ј–∞–њ–∞—Б–Њ–≤ —Б–≤–Њ–±–Њ–і–љ–Њ–≥–Њ –≥–ї–Є–Ї–Њ–≥–µ–љ–∞ —П–≤–ї—П–µ—В—Б—П —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ–Љ –љ–∞—А—Г—И–µ–љ–Є—П –Њ–±–Љ–µ–љ–∞ —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –њ—А–Є —Б—В—А–µ—Б—Б–µ. –Т —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –≥–ї—О–Ї–Њ–Ј—Л –≤ –µ—Й–µ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Г—Б–Є–ї–Є–≤–∞–µ—В –≥–ї—О–Ї–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј, –Ї–Њ—В–Њ—А—Л–є –љ–µ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ–љ –Є –≤–µ–і–µ—В –Ї –±—Л—Б—В—А–Њ–є –њ–Њ—В–µ—А–µ –±–µ–ї–Ї–∞ (100 –≥ –±–µ–ї–Ї–∞ –Њ–±—А–∞–Ј—Г—О—В 56 –≥ –≥–ї—О–Ї–Њ–Ј—Л). –У–ї—О–Ї–Њ–Ј–∞ –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї –Њ–і–љ–Њ–Љ—Г –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л—Е –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–≤ –±–µ–ї–Ї–Њ–≤–Њ–≥–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Љ–µ–ґ–і—Г –Њ–±–Љ–µ–љ–Њ–Љ —Г–≥–ї–µ–≤–Њ–і–Њ–≤, –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –Є –ї–Є–њ–Є–і–Њ–≤ —Б—Г—Й–µ—Б—В–≤—Г–µ—В —В–µ—Б–љ–∞—П –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М.
–Ф–Њ–ї—П –≥–ї—О–Ї–Њ–Ј—Л –≤ —Н–љ–µ—А–≥–Њ—Б–љ–∞–±–ґ–µ–љ–Є–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 45-50%. –≠–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–∞—П —Ж–µ–љ–љ–Њ—Б—В—М 1 –≥ –≥–ї—О–Ї–Њ–Ј—Л – 4,1 –Ї–Ї–∞–ї. –Ю–±–µ—Б–њ–µ—З–µ–љ–Є–µ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ —Г–≥–ї–µ–≤–Њ–і–∞–Љ–Є –Ј–∞–Љ–µ—В–љ–Њ —Б–љ–Є–ґ–∞–µ—В –∞–Ј–Њ—В–Є—Б—В—Л–µ –њ–Њ—В–µ—А–Є, –∞ –≤–≤–µ–і–µ–љ–Є–µ –і–Њ 100 –≥ –≥–ї—О–Ї–Њ–Ј—Л –≤ —Б—Г—В–Ї–Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Ї–µ—В–Њ–Ј–∞. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≥–ї—О–Ї–Њ–Ј—Г —И–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –≤ –њ—А–∞–Ї—В–Є–Ї–µ –Я–Я –Ї–∞–Ї –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –Є—Б—В–Њ—З–љ–Є–Ї –љ–µ–±–µ–ї–Ї–Њ–≤—Л—Е –Ї–∞–ї–Њ—А–Є–є –≤ –≤–Є–і–µ 20-50% —А–∞—Б—В–≤–Њ—А–∞. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –њ—А–Њ–≥—А–∞–Љ–Љ–∞—Е –Я–Я —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–Љ–µ–љ—П—В—М 20-30% —А–∞—Б—В–≤–Њ—А—Л –≥–ї—О–Ї–Њ–Ј—Л, —Б—В—А–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А–Њ–≤–∞—В—М –µ–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≤ –Ї—А–Њ–≤–Є, –і–Њ–±–∞–≤–ї—П—В—М –∞–і–µ–Ї–≤–∞—В–љ—Л–µ –і–Њ–Ј—Л —Н–Ї–Ј–Њ–≥–µ–љ–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞, –љ–µ –њ—А–µ–≤—Л—И–∞—П —Б—Г—В–Њ—З–љ—Г—О –і–Њ–Ј—Г 6 –≥/–Ї–≥.
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ–і—Е–Њ–і—Л –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –±–Њ–ї—М—И–Є—Е –Њ–±—К–µ–Љ–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е (>30%) —А–∞—Б—В–≤–Њ—А–Њ–≤ –≥–ї—О–Ї–Њ–Ј—Л –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М. –Т –ї–Є—В–µ—А–∞—В—Г—А–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –њ—А–Є–Љ–µ–љ—П—В—М –љ–µ –±–Њ–ї–µ–µ —З–µ–Љ 20–30% —А–∞—Б—В–≤–Њ—А—Л –≥–ї—О–Ї–Њ–Ј—Л. –Ю–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ —Н—В–Њ —А–∞–Ј–≤–Є—В–Є–µ–Љ –њ—А–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е –љ–Є–Ј–Ї–Њ–є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї –≥–ї—О–Ї–Њ–Ј–µ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –±–ї–Њ–Ї–∞–і—Л –≤—Л–і–µ–ї–µ–љ–Є—П –Є–љ—Б—Г–ї–Є–љ–∞ —Б –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є, –≥–ї—О–Ї–Њ–Ј—Г—А–Є–Є, –≥–Є–њ–µ—А–Њ—Б–Љ–Њ–ї—П—А–љ–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–Њ–ї—М—И–Є—Е –і–Њ–Ј –≥–ї—О–Ї–Њ–Ј—Л –≤ –≤—Л—Б–Њ–Ї–Њ–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ–љ—Л—Е —А–∞—Б—В–≤–Њ—А–∞—Е —З—А–µ–≤–∞—В–Њ —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ї–∞–Ї –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е, —В–∞–Ї –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–≥–Њ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Љ–Є–љ—Г—В–љ–Њ–≥–Њ –Њ–±—К–µ–Љ–∞ –і—Л—Е–∞–љ–Є—П (–Ь–Ю–Ф), –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Ш–Т–Ы, –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –ї–Є–њ–Њ–љ–µ–Њ–≥–µ–љ–µ–Ј–∞ –Є –ґ–Є—А–Њ–≤–Њ–є –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є–Є –њ–µ—З–µ–љ–Є, –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П —Б –≥–Є–њ–µ—А–Њ—Б–Љ–Њ–ї—П—А–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ, –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П –≤ —Б–≤—П–Ј–Є —Б –њ–µ—А–µ–і–Њ–Ј–Є—А–Њ–≤–Ї–Њ–є –Є–љ—Б—Г–ї–Є–љ–∞. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є 5% –Є 10% —А–∞—Б—В–≤–Њ—А–Њ–≤ –≥–ї—О–Ї–Њ–Ј—Л –Њ–≥—А–∞–љ–Є—З–µ–љ—Л –Є—Е –љ–Є–Ј–Ї–Њ–є —Н–љ–µ—А–≥–Њ–µ–Љ–Ї–Њ—Б—В—М—О –Є –Њ–±—К–µ–Љ–Њ–Љ –Є–љ—Д—Г–Ј–Є–є (—В–∞–±–ї.3). –Я–Њ–Љ–Є–Љ–Њ –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ —Н–љ–µ—А–≥–Њ–љ–Њ—Б–Є—В–µ–ї—П –Є –Є—Б—В–Њ—З–љ–Є–Ї–∞ —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В —Д—А—Г–Ї—В–Њ–Ј—Г, —Б–Њ—А–±–Є—В –Є –Ї—Б–Є–ї–Є—В.

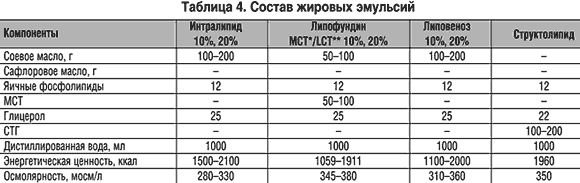
–Т –Ї–∞—З–µ—Б—В–≤–µ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—Г–±—Б—В—А–∞—В–∞ –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –ґ–Є—А–Њ–≤—Л–µ —Н–Љ—Г–ї—М—Б–Є–Є. –≠—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –љ–µ—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ—Б—В—М—О –ґ–Є—А–∞ –≤ –≤–Њ–і–µ, —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –Њ—Б–Љ–Њ—В–Є—З–µ—Б–Ї–Є –љ–µ–∞–Ї—В–Є–≤–љ—Л–Љ, –∞ —В–∞–Ї–ґ–µ —Б –≤—Л—Б–Њ–Ї–Њ–є —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–є —Ж–µ–љ–љ–Њ—Б—В—М—О (1 –≥ – 9,3 –Ї–Ї–∞–ї) –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –љ–µ–Ј–∞–Љ–µ–љ–Є–Љ—Л–Љ–Є –ґ–Є—А–љ—Л–Љ–Є –Ї–Є—Б–ї–Њ—В–∞–Љ–Є (–Ц–Ъ) –≤ –Љ–∞–ї–Њ–Љ –Њ–±—К–µ–Љ–µ –ґ–Є–і–Ї–Њ—Б—В–Є. –Ц–Є—А–Њ–≤—Л–µ —Н–Љ—Г–ї—М—Б–Є–Є –Є–Ј–Њ–Њ—Б–Љ–Њ–ї—П—А–љ—Л (280–380 –Љ–Њ—Б–Љ/–ї), —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤–≤–Њ–і–Є—В—М –Є—Е –Ї–∞–Ї –≤ —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ, —В–∞–Ї –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –≤–µ–љ—Л.
–Ц–Є—А–Њ–≤—Л–µ —Н–Љ—Г–ї—М—Б–Є–Є –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –≤ –њ—А–∞–Ї—В–Є–Ї–µ –Я–Я –±–Њ–ї–µ–µ 40 –ї–µ—В. –Я–µ—А–≤–Њ–є –ґ–Є—А–Њ–≤–Њ–є —Н–Љ—Г–ї—М—Б–Є–µ–є –±—Л–ї –њ—А–µ–њ–∞—А–∞—В –Є–љ—В—А–∞–ї–Є–њ–Є–і, —А–∞–Ј—А–∞–±–Њ—В–∞–љ–љ—Л–є A. Wretlind –≤ 1957 –≥. –Ъ –њ–µ—А–≤–Њ–Љ—Г –њ–Њ–Ї–Њ–ї–µ–љ–Є—О –ґ–Є—А–Њ–≤—Л—Е —Н–Љ—Г–ї—М—Б–Є–є –Њ—В–љ–Њ—Б–Є—В—Б—П –Є –ї–Є–њ–Њ–≤–µ–љ–Њ–Ј. –Ю—Б–љ–Њ–≤–љ—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ —Н—В–Є—Е —Н–Љ—Г–ї—М—Б–Є–є —П–≤–ї—П—О—В—Б—П —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–µ –Љ–∞—Б–ї–∞ –≤ –≤–Є–і–µ LCT. –Т 1985 –≥. –љ–∞—З–∞—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П –ґ–Є—А–Њ–≤—Л—Е —Н–Љ—Г–ї—М—Б–Є–є —Б–Њ–і–µ—А–ґ–∞—Й–Є—Е LCT –Є MCT (MCT/LCT) –≤ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є 50:50.
–°—В—А—Г–Ї—В–Њ–ї–Є–њ–Є–і –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —В—А–µ—В—М–µ–Љ—Г, –љ–∞–Є–±–Њ–ї–µ–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ—Г, –њ–Њ–Ї–Њ–ї–µ–љ–Є—О –ґ–Є—А–Њ–≤—Л—Е —Н–Љ—Г–ї—М—Б–Є–є. –Ю–Љ–µ–≥–∞–≤–µ–љ – 10% —Н–Љ—Г–ї—М—Б–Є—П —А—Л–±—М–µ–≥–Њ –ґ–Є—А–∞ —Б –≤—Л—Б–Њ–Ї–Є–Љ –њ—А–Њ—Ж–µ–љ—В–љ—Л–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ w–3 –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В. –Я—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –і–Њ–±–∞–≤–Ї–Є –Ї —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ —А–∞—Б—В–≤–Њ—А–∞–Љ –ґ–Є—А–Њ–≤—Л—Е —Н–Љ—Г–ї—М—Б–Є–є –Ї–∞–Ї –Є—Б—В–Њ—З–љ–Є–Ї –њ–Њ–ї–Є–љ–µ–љ–∞—Б—Л—Й–µ–љ–љ—Л—Е w–3 –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В —Б —Ж–µ–ї—М—О –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П. w–3, 6 –ґ–Є—А–љ—Л–µ –Ї–Є—Б–ї–Њ—В—Л —П–≤–ї—П—О—В—Б—П –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–∞–Љ–Є —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤, —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞, –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞, –ї–µ–є–Ї–Њ—В—А–Є–µ–љ–∞ (LTD5), —Б–љ–Є–ґ–∞—О—Й–µ–≥–Њ –њ—А–Њ–і—Г–Ї—Ж–Є—О —Ж–Є—В–Њ–Ї–Є–љ–Њ–≤ (IL–1, IL–6, TFN), –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б—Г–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л–є –Њ—В–≤–µ—В, –њ—А–Њ–і—Г–Ї—Ж–Є—О –∞–љ—В–Є—В–µ–ї –Є —Ж–Є—В–Њ–ї–Є–Ј –Ї–ї–µ—В–Њ–Ї, —Б—В–∞–±–Є–ї–Є–Ј–Є—А—Г—О—В –Ї–ї–µ—В–Њ—З–љ—Л–µ –Љ–µ–Љ–±—А–∞–љ—Л, –Њ–±–ї–∞–і–∞—О—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Є –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є.
–Я—А–Є –љ–∞–ї–Є—З–Є–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ–µ—А–µ–≤–∞—А–Є–≤–∞—О—Й–µ–є –Є –≤—Б–∞—Б—Л–≤–∞—О—Й–µ–є —Д—Г–љ–Ї—Ж–Є–є —В–Њ–љ–Ї–Њ–є –Ї–Є—И–Ї–Є –≤–Њ –≤—А–µ–Љ—П –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Љ–µ—А–Њ–њ—А–Є—П—В–Є–є –њ–Њ —Г—Б—В—А–∞–љ–µ–љ–Є—О –њ—А–Њ—П–≤–ї–µ–љ–Є–є —Б–Є–љ–і—А–Њ–Љ–∞ –Ї–Є—И–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і—П—В –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ. –Я–Њ –Љ–µ—А–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П —Д—Г–љ–Ї—Ж–Є–є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ —Б–љ–∞—З–∞–ї–∞ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–—Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ, –∞ –Ј–∞—В–µ–Љ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ. –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –і–Њ —В–µ—Е –њ–Њ—А, –Ї–Њ–≥–і–∞ –±–Њ–ї—М–љ–Њ–є —Б–Љ–Њ–ґ–µ—В –њ–Њ–ї—Г—З–∞—В—М 50–70% –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –µ—Б—В–µ—Б—В–≤–µ–љ–љ—Л–Љ –Є–ї–Є —Н–љ—В–µ—А–∞–ї—М–љ—Л–Љ –њ—Г—В–µ–Љ. –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Б–Њ–Ї—А–∞—Й–∞—О—В, —З—В–Њ–±—Л –љ–Є–Ј–Ї–∞—П –Ї–∞–ї–Њ—А–Є–є–љ–Њ—Б—В—М –њ–Є—Й–Є —Б—В–Є–Љ—Г–ї–Є—А–Њ–≤–∞–ї–∞ –∞–њ–њ–µ—В–Є—В. –Т –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Г–Љ–µ–љ—М—И–∞—О—В –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –ґ–Є—А–Њ–≤—Л—Е —Н–Љ—Г–ї—М—Б–Є–є, —В–∞–Ї –Ї–∞–Ї –Њ–љ–Є —Г–≥–љ–µ—В–∞—О—В –∞–њ–њ–µ—В–Є—В –Є —Н–≤–∞–Ї—Г–∞—В–Њ—А–љ—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –ґ–µ–ї—Г–і–Ї–∞ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ –≥–ї—О–Ї–Њ–Ј–∞ –Є –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В—Л. –Ъ–Њ—А–Љ–ї–µ–љ–Є–µ —З–µ—А–µ–Ј —В–Њ–љ–Ї–Є–є –љ–∞–Ј–Њ–≥–∞—Б—В—А–∞–ї—М–љ—Л–є –Ј–Њ–љ–і –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ—Л–Љ —Н—В–∞–њ–Њ–Љ –і–ї—П –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–≥–Њ –њ–µ—А–µ—Е–Њ–і–∞ –Њ—В –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Ї –Њ–±—Л—З–љ–Њ–Љ—Г.

–С–Њ–ї—М—И–Є–љ—Б—В–≤—Г –±–Њ–ї—М–љ—Л—Е –ґ–µ–ї–µ–Ј–Њ–і–µ—Д–Є—Ж–Є—В–љ–Њ–є –∞–љ–µ–Љ–Є–µ–є –њ–Њ–Ї–∞–Ј–∞–љ—Л –њ–µ—А–Њ—А–∞–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –ґ–µ–ї–µ–Ј–∞. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б–ї–µ –Њ–±—И–Є—А–љ—Л—Е –Њ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤ —Б –Љ–∞—Б—Б–Є–≤–љ–Њ–є –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А–µ–є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –ґ–µ–ї–µ–Ј–Њ–Љ –Њ—В–і–∞–µ—В—Б—П –њ—А–µ–і–њ–Њ—З—В–µ–љ–Є–µ. –†–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Љ–µ—Б—В–љ—Л—Е –Є —Б–Є—Б—В–µ–Љ–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –ґ–µ–ї–µ–Ј–∞. –Т –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–Њ—Б—В—М –і–µ–Ї—Б—В—А–∞–љ––ґ–µ–ї–µ–Ј—Г Fe(III)-–≥–Є–і—А–Њ–Ї—Б–Є–і-—Б–∞—Е–∞—А–Њ–Ј–љ—Л–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –ґ–µ–ї–µ–Ј–∞ –њ—А–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е. –°–∞—Е–∞—А–Њ–Ј–љ—Л–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б –ґ–µ–ї–µ–Ј–∞ –±—Л—Б—В—А–Њ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–∞–µ—В –ґ–µ–ї–µ–Ј–Њ, –Ї–Њ—В–Њ—А–Њ–µ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б —Н–љ–і–Њ–≥–µ–љ–љ—Л–Љ–Є –±–µ–ї–Ї–∞–Љ–Є (—В—А–∞–љ—Б—Д–µ—А—А–Є–љ, —Д–µ—А—А–Є—В–Є–љ), —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –і–Њ—Б—В—Г–њ–љ—Л–Љ –і–ї—П —А–µ—В–Є–Ї—Г–ї–Њ–—Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ–µ—З–µ–љ–Є, —Б–µ–ї–µ–Ј–µ–љ–Ї–Є, –Ї–Њ—Б—В–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –і–ї—П —Н—А–Є—В—А–Њ–њ–Њ—Н–Ј–∞. –Я–∞—А–∞–ї–ї–µ–ї—М–љ–Њ–µ –њ–µ—А–µ–ї–Є–≤–∞–љ–Є–µ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В –≤–µ–і–µ—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ —В—А–∞–љ—Б—Д–µ—А—А–Є–љ–∞ –Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Б –ґ–µ–ї–µ–Ј–Њ–Љ.
–Ф–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –њ–Њ—Б—В–≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–є –∞–љ–µ–Љ–Є–Є –Є –∞–Ї—В–Є–≤–Є–Ј–∞—Ж–Є–Є —Н—А–Є—В—А–Њ–њ–Њ—Н–Ј–∞ –≤–≤–µ–і–µ–љ–Є–µ –ґ–µ–ї–µ–Ј–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ —Б–Њ—З–µ—В–∞—В—М —Б —Н—А–Є—В—А–Њ–њ–Њ—Н—В–Є–љ–Њ–Љ. –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Н—А–Є—В—А–Њ–њ–Њ—Н—В–Є—З–µ—Б–Ї–Є–є –Њ—В–≤–µ—В —З–∞—Б—В–Є—З–љ–Њ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є —Б –Љ–∞—Б—Б–Є–≤–љ–Њ–є –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А–µ–є. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –њ—А–Є —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ –њ–Њ–≤—Л—И–µ–љ–Є—П –≥–µ–Љ–∞—В–Њ–Ї—А–Є—В–∞, –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П —Н—А–Є—В—А–Њ–њ–Њ—Н—В–Є–љ–Њ–Љ –±–Њ–ї—М–љ—Л–µ –љ—Г–ґ–і–∞—О—В—Б—П –≤ –Љ–µ–љ—М—И–µ–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ –≥–µ–Љ–Њ—В—А–∞–љ—Б—Д—Г–Ј–Є–є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ —В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –Є —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, –љ–∞—А—П–і—Г —Б —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–—В—А–∞–љ—Б—Д—Г–Ј–Є–Њ–љ–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є, —А–µ—Б–њ–Є—А–∞—В–Њ—А–љ–Њ–є –Є –Є–љ–Њ—В—А–Њ–њ–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Њ–є, —П–≤–ї—П—О—В—Б—П –љ–µ–Њ—В—К–µ–Љ–ї–µ–Љ–Њ–є —З–∞—Б—В—М—О –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є –Њ—Б—В—А–Њ–є –Ї—А–Њ–≤–Њ–њ–Њ—В–µ—А–µ.












