Данный вывод достаточно серьезен, т.к. именно данному классу аминокислотных смесей направленного действия отводится главная роль не только в устранении клинических проявлений ПЭ у больных с печеночной недостаточностью, но и в коррекции белкового и аминокислотного дисбаланса [10]. Хорошо известно, что нарушение синтеза мочевины в печени приводит к накоплению в крови аммиака и других токсичных азотистых соединений. Также нарушается аминокислотный состав в плазме. Особенно это касается аминокислот – предшественников центральных моноаминных нейротрансмиттеров, что сопровождается непременным снижением их уровня в центральной нервной системе (ЦНС), способствуя развитию энцефалопатии. Данные положения определяют роль специальных адаптированных аминокислотных смесей в коррекции аминокислотного дисбаланса, когда фракция ароматических аминокислот (фенилаланина и тирозина) снижена, а РА увеличена. На этом фоне искусственное питание, в том числе и ПП, должно не только максимально обеспечить суточную потребность организма больного в белках и других питательных веществах, но при этом не усиливать проявления энцефалопатии.
К настоящему времени специально разработаны и производятся различными фармацевтическими компаниями растворы кристаллических аминокислот категории «–Гепа», имеющие химический состав, ориентированный на пациентов с заболеваниями печени. При этом все растворы данного класса (в зависимости от производителя) не идентичны, хотя и имеют некоторое сходство. Клиницисту нужно знать принципиальные отличия состава растворов кристаллических аминокислот класса «–Гепа» от стандартных растворов аминокислот (АК) и не отождествлять их. Это не праздный вопрос, т.к. существует мнение о том, что аминокислотные растворы категории «–Гепа» способны заменить при проведении ПП стандартные растворы кристаллических аминокислот. Но это совершенно особые растворы кристаллических аминокислот, их целесообразно считать лекарственными препаратами для лечения печеночной недостаточности у больных с выраженными проявлениями ПЭ, чем донатором аминного азота, устраняющего белково–энергетическую недостаточность.
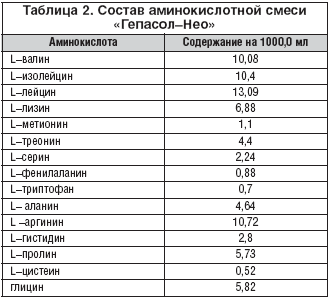
В качестве иллюстрации приведем пропись раствора «Гепасол–Нео» (HEMOFARM KONCERN, A.D.) (табл. 2). Как видим, в данной прописи присутствуют все 8 незаменимых аминокислот (L–валин, L–изолейцин, L–лейцин, L–лизин, L–метионин, L–треонин, L–фенилаланин, L–триптофан), 2 условно заменимые аминокислоты (L–аргинин и L–гистидин) и 5 заменимых аминокислот. По сравнению со стандартными прописями растворов кристаллических аминокислот, содержащих в своем составе до 20 АК, в Гепасол–Нео многие отсутствуют. Это относится к аспарагину, ацетилцистеину, глицил–тирозину, глутаминовой кислоте, тирозину, орнитину, таурину. В растворе отсутствуют электролиты, микроэлементы и водорастворимые витамины, что делает данный тип раствора АК по сущности несбалансированным для проведения полного ПП.
Но в то же время это не делает Гепасол–Нео менее ценным лекарственным препаратом для лечения больных с ПЭ. Рядом исследований доказано, что эти «несбалансированные» растворы обладают высокой фармакологической активностью [8], главным образом за счет того, что в их составе, как было указано выше, существенно увеличено содержание РА и понижено содержание ароматических АК и метионина. Общие показания для назначения препаратов группы «–Гепа» сводятся к следующим положениям:
• профилактика и лечение печеночной энцефалопатии;
• назначение пациентам, у которых печеночная энцефалопатия или является неизбежной, или уже имеет выраженные клинические проявления;
• нормализация аминокислотного дисбаланса, являющегося результатом заболеваний печени.
Почему при лечении ПЭ делается акцент на разветвленные аминокислоты и какова их роль в организме человека?
Изолейцин – ( α–амино–b–метилвалериановая кислота), C2H5CH(CH3)CH(NH2)COOH, был открыт Ф. Эрлихом (1904) в продуктах распада белка фибрина. Относится к группе алифатических моноаминокарбоновых кислот с разветвленной углеродной цепью. Для человека изолейцин является незаменимой аминокислотой, суточная потребность которой составляет около 1,5–2,0 г. Необходим для синтеза гемоглобина. Также стабилизирует и регулирует уровень сахара в крови и процессы энергообеспечения. Является источником энергии для мышечных клеток. Недостаток изолейцина приводит к проявлению гипогликемии, что проявляется вялостью и сонливостью. Дефицит изолейцина приводит к потере мышечной массы.
Лейцин, (CH3CH(CH3)CH2CH(NH2)COOH), незаменимая разветвленная алифатическая аминокислота. Необходима для построения и развития мышечной ткани, способствует синтезу белка в мышцах и печени и препятствует их разрушению. Также служит источником энергии на клеточном уровне.
Валин – (CH3)2CH(NH2)COOH) – a–аминоизовалериановая кислота, незаменимая аминокислота. Входит в состав всех белков, участвует в биосинтезе пантотеновой кислоты. Необходим для метаболизма в мышцах, восстановления поврежденных тканей и поддержания нормального обмена азота в организме. Помогает предотвратить неврологические заболевания, защищает миелиновую оболочку, окружающую нервные волокна в головном и спинном мозге. Вместе с лейцином и изолейцином служит источником энергии в мышечных клетках, а также препятствует снижению уровня серотонина.
L–изолейцин, L–лейцин и L–валин прямо усваиваются периферическими тканями (их метаболизм не зависит от степени поражения печени), снижают усвоение и поступление ароматических аминокислот в ЦНС, уменьшая проявления ПЭ, нормализуют энергетический и азотный баланс в организме.
Как было указано выше, при хронических заболеваниях печени в крови пациентов повышено содержание ароматических аминокислот (тирозина, фенилаланина, триптофана) и уменьшено содержание валина, лейцина, изолейцина. В этой связи становится понятной пропись «Гепасол–Нео», где существенно снижена концентрация фенилаланина, а триптофан исключен вовсе при существенном обогащении раствора валином, изолейцином и лейцином. Соотношение РА и ароматических АК обозначается как индекс Фишера (ИФ), который в норме должен составлять 3–3,5.
изолейцин + лейцин + валин
Индекс Фишера = ————————————————
фенилаланин + тирозин
Исходя из формулы Фишера становится понятным почему в препаратах класса «–Гепа» высоко содержание разветвленных аминокислот, препятствующих образованию аммиака [3], который также причастен к развитию ПЭ, т.к. способствует транспорту ароматических аминокислот в ЦНС [9]. При циррозе печени ИФ может снижаться до единицы [6,7].
В то же время отдельные публикации указывают на то, что не обнаружено корреляции между соотношением ароматических аминокислот и РА, с одной стороны, и выраженностью ПЭ – с другой [2]. Возможно, положительный клинический эффект инфузий РА обусловлен уменьшением белкового катаболизма в печени и мышцах, а также улучшением обменных процессов в головном мозге. Есть и иная точка зрения – устранение энцефалопатии с помощью РА необязательно является результатом адекватного питания, а использование РА–обогащенных растворов не оказывает влияния на выживание [8].
Проведение полного ПП определяет совместное применение растворов углеводов, жировых эмульсий как донаторов энергии, растворов аминокислот, витаминных комплексов, электролитов и микроэлементов. У пациентов с заболеваниями печени нет противопоказаний для назначения жира и углеводов. Положения Европейской ассоциации специалистов энтерального и парентерального питания [8] определяют, что жир является энергетическим источником для гепатоцитов и полезен пациентам с острой печеночной недостаточностью. Жировые эмульсии, введенные парентерально, эффективно выводятся из крови и утилизируются большинством пациентов с циррозом. Введение глюкозы в дозе равной 2 г на 1 кг массы тела в сутки обязательно для предотвращения и лечения гипогликемии. Необходимо добавлять электролиты (калий, магний). Белок вводится из расчета 1,0–1,5 г на 1 кг массы тела в сутки, при ПЭ уровень вводимого белка можно уменьшить до 0,8 г на 1 кг массы тела в сутки [13 ].
В заключение следует сказать, что лечение больных с острой и хронической печеночной недостаточностью является сложной и до конца не решенной проблемой. Проведение ПП при ПЭ также следует относить к категории проблемных и требует дальнейшего всестороннего изучения на основе многоцентровых рандомизированных исследований.

Литература
1. Арвид Вретлинд, Арам Суджан. Клиническое питание. – Стокгольм–Москва, 1990. – С. 354.
2. Буеверов А.О., Маевская М.В. Особенности течения и подходы к терапии различных вариантов печеночной энцефалопатии // Трудный пациент. 2006. №10. С. 41–46.
3. Костюченко Л.Н. Парентерально–энтеральная коррекция дисбаланса аминокислот у пациентов старческого возраста // Трудный пациент. №5. 2007. С. 32–36.
4. Котаев А.Ю. Принципы парентерального питания // Русский медицинский журнал. С. 1604–1612.
5. Луфт В.М., Костюченко А.Л., Лейдерман И.Н. Руководство по клиническому питанию больных в интенсивной медицине. Санкт–Петербург; Екатеринбург, 2003. – С. 310.
6. Манзюк Л.В., Салтанов А.И., Сельчук В.Ю., Снеговой А.В., Снигур П.В. Печеночная недостаточность и рациональная нутритивная поддержка // Русский медицинский журнал. 2007. №25. Том. 15. С. 1896–1899.
7. Надинская М.Ю. Печеночная энцефалопатия: патогенетические подходы к лечению // Consilium Medicum. 2004. №1. Том 6.
8. Основы клинического питания. Материалы лекций для курсов Европейской ассоциации парентерального и энтерального питания / Пер. с англ.; Гл. ред. Л. Соботка. – 2–е изд. – Петрозаводск: «ИнтелТек», 2004. – С. 416.
9. Чарльз В.Ван Вэй, Кэрол Айертон–Джонс. Секреты питания / Пер. с англ. под общ. ред. д.м.н. В.Н.Малаховского. «БИНОМ», 2006. – С. 320.
10. Шестопалов А.Е. Cовременные аспекты парентерального питания в интенсивной терапии и реанимации // Лекция на XVI школе–семинаре «Современные проблемы физиологии и патологии пищеварения, Пущино–на–Оке, 14–17 мая 2001 года. Приложение №14 к Российскому журналу гастроэнтерологии, гепатологии, колопроктологии «Материалы XVI сессии Академической школы–семинара имени А.М. Уголева «Современные проблемы физиологии и патологии пищеварения». 2001. Том XI. №4. С. 102–109.
11. Parrish C.R. Nutrition for Patients with Hepatic Failure // Practical Gastroenterology, june, 2003, р. 23–42.
12. Plauth M, Roske AE, Romaniuk P, Roth E, Ziebig R, Lochs H. Post–feeding hyperammonaemia in patients with transjugular intrahepatic portosystemic shunt and liver cirrhosis: role of small intestinal ammonia release and route of nutrient administration // Gut, 2000;46:849–855.
13. Plauth M., Cabre E., Riggio O., Assis–Camilo M., Pirlich M., J. Kondrup et.al. ESPEN Guidelines on Enteral Nutrition: Liver disease. // Clinical Nutrition, vol. 25, issue 2, April 2006, p. 285–294.
14. Stratton R. J. , Smith T. R. Role of enteral and parenteral nutrition in the patient with gastroin testinal and liver disease. // Clinical Gastroenterology, 2006, Volume 20, Issue 3. P. 441–466.








.gif)



