Гангрена нижних конечностей у больных СД развивается в 6 раз чаще, чем у недиабетиков; в 5 случаях из 6 причиной ампутации, не связанной с травмой, являются гнойно–некротические поражения нижних конечностей на фоне СД. Летальность от гнойных осложнений при синдроме диабетической стопы (СДС) составляет от 6 до 22% [3–5,8]. Более 60% пациентов с СД – лица пожилого и старческого возраста.
На фоне диабетической ангиопатии нарушение микроциркуляции отмечается не только в сосудах нижних конечностей, но и в паренхиматозных органах, вызывая гипоксию тканей. Степень снижения кровотока и нарастание гипоксии являются определяющими в развитии полиорганной дисфункции у больных этой группы, что определяет тяжесть состояния и влияет на результат хирургического лечения.
Материалы и методы исследования
Нами проанализированы результаты хирургического лечения 240 больных с осложненными формами СДС, находящихся на лечении в клинике факультетской хирургии им. С.Р. Миротворцева КБ № 3 СГМУ с 2000 по 2006 г.
В основную группу (I группа) входили 118 больных, группу сравнения (II группа) составили 122 больных. Больные в обеих группах были сопоставимы по полу, возрасту, длительности течения сахарного диабета и способам коррекции гликемии. Группы статистически сопоставимы по выраженности деструктивных изменений на стопе (классификация Wagner F.W. [9]). Пациенты основной группы лечились в клинике в 2003–2006 гг., когда сформировалось конкретное представление о важности коррекции полиорганной дисфункции у больных этой группы. Группу сравнения составили 122 пациента, которые лечились в клинике в 2000–2002 гг., когда исследование было на этапе выяснения частоты и выраженности полиорганной дисфункции у этих больных и определения способов коррекции выявленных нарушений. Всем пациентам I и II групп проводилось медикаментозное лечение в соответствии с принятым стандартом «Алгоритм специализированной медицинской помощи больным сахарным диабетом», утвержденном Министерством здравоохранения и социального развития Российской Федерации и Российской академией медицинских наук, ГУ Эндокринологическим научным центром РАМН (2006). Оно включало коррекцию гликемии дробным введением инсулина короткого действия, антибактериальную терапию, сосудистые препараты и антикоагулянты, спазмолитики. Больным I группы проводилась терапия с учетом степени полиорганной дисфункции, коррекции ее и включением в комплекс лечения ежедневных внутривенных инфузий 1000 мг Актовегина (из них у 46 пациентов она проводилась внутриартериально путем катетеризация a. epigastrica inferior). Курс лечения Актовегином составлял от 14 до 20 дней, в редких случаях более продолжительно, в зависимости от проявлений системной воспалительной реакции.
Среди пациентов было 168 (70%) женщин и 72 (30%) мужчины в возрасте от 40 до 82 лет. СД 1 типа был у 13% больных, СД 2 типа – у 87% больных. Большинство больных имели диабетический анамнез длительностью более 10 лет.
Тяжелая степень СД выявлена у 98 пациентов, средняя степень тяжести – у 124 пациентов. Все больные имели сопутствующие заболевания: ишемическую болезнь сердца, гипертоническую болезнь, облитерирующий атеросклероз сосудов конечностей, нарушения мозгового кровообращения и т.д.
Больные представлены с различными формами СДС: нейропатическая форма – 69 (28,8%) пациента, ишемическая – 13 (5,6%) и смешанная форма – 158 (65,6%) больных. По глубине деструктивных изменений (классификации Wagner F.W.) [9] 72 (30%) пациента с инфицированными глубокими язвами, с развитием абсцесса, флегмон и возможным присоединением остеомиелита – 54 (22,5%), с гангреной стопы или отдельного пальца 114 (46,9%) больных.
Больных с распространенной диабетической гангреной было большинство, многие поступали в крайне тяжелом состоянии, с декомпенсацией СД и сопутствующей патологией. Общая летальность – 3 человека (1,25%).
Больным выполнялись оперативные вмешательства различного объема: иссечение язв стопы и вскрытие флегмон у 132 (55%) больных, ампутация пальцев и резекция костей стопы у 75 (31,3%), ампутация бедра у 18 (7,5%), ампутация голени у 10 (4,2%), ампутация стопы у 5 (2,1%), повторные некрэктомии у 192 (80%) больных. Катетеризацию нижней надчревной артерии для селективного введения лекарственных препаратов проводили у 69 (28,8%) пациентов.
Анализируя течение хирургической инфекции и причины развития осложнений в послеоперационном периоде у больных с СДС, мы подтвердили вывод о значительной частоте тяжелого сепсиса при гнойных осложнениях диабетической стопы. Наличие и выраженность полиорганной дисфункции имеет существенное значение в данном процессе и в ряде случаев определяет исход заболевания. Во всех случаях, где имелось тяжелое течение гнойного процесса при осложнениях СДС, мы констатировали выраженные функциональные изменения органов и систем, метаболические изменения.
Как показали наши исследования, первостепенной задачей в комплексе лечения является коррекция гормональных, волемических и метаболических нарушений и, соответственно, макро– и микроциркуляторных расстройств, что является определяющим в эффективности антибактериальной терапии, эфферентной детоксикации и профилактики полиорганной недостаточности. Нами разработан математический алгоритм определения тяжести состояния больных с осложненными формами СДС, с помощью которого определялись критерии при выборе хирургической тактики лечения.
Для построения объективной системы оценки тяжести состояния больных с СДС были выявлены характеристики, наиболее влияющие на исход операции. Обработка исходной информации проводилась с помощью табличного редактора Excel, специализированного пакета программы обработки статистических данных Statistica.
При анализе частотного распределения с проверкой статистической достоверности связи полученных градаций баллов с результатом лечения суммарный показатель тяжести состояния больного I рассчитывался по формуле:
I =10n1 + 15n2 + 30n3,
где n1 – количество показателей, относящихся к первой (компенсированной) градации шкалы;
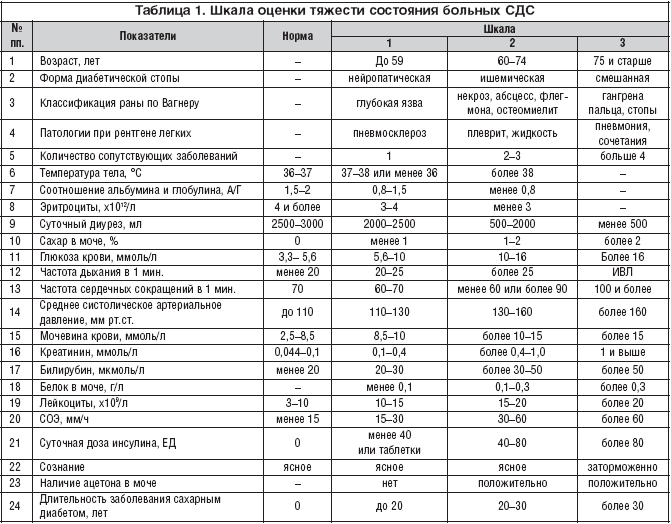
n2, n3 – количество показателей, относящихся соответственно ко второй (субкомпенсированной) и третьей (декомпенсированной) градациям шкалы (табл. 1).
Результаты исследования
В результате анализа значений суммарного показателя тяжести состояния I, определяемого по предложенной формуле, больные были распределены на три группы. Соответственно определялся оптимальный срок и объем операции: 1) до 250 баллов – лечение больных в хирургическом отделении было эффективно, сроки и объем операции не ограничены; прослеживалось гладкое течение послеоперационного периода, прогноз по заживлению раны благоприятный; 2) при сумме баллов I от 250 до 400 – рекомендовано выполнить отсроченные и плановые операции после предоперационной подготовки, направленной на стабилизацию показателей органов и систем; «большие» ампутации выполнялись в экстренном порядке при прогрессирующей влажной гангрене, объем прочих операций был минимальным; 3) при сумме баллов I более 400 баллов оперативные вмешательства целесообразно выполнять только после интенсивной предоперационной подготовки, уменьшения степени полиорганной дисфункции и эндотоксикоза и, как следствие – снижения показателя I. Эффект от лечения минимальный, прогноз неблагоприятный. Все 3 случая летального исхода возникли у больных этой группы.
Для того чтобы снизить суммарный показатель I, проводилось лечение полиорганной дисфункции. В зависимости от функционального состояния сердечно–сосудистой системы, функции почек, надпочечников, желудочно–кишечного тракта (и т.д.) назначалась этиотропная и симптоматическая терапия, направленная на коррекцию конкретных нарушений. Универсальным средством, повышающим толерантность органов к гипоксии (которая развивается у больных сахарным диабетом вследствие микро– и макроангиопатии) является Актовегин. Выраженный клинический эффект высоких доз Актовегина при лечении осложненных форм СД был отмечен многими отечественными и зарубежными авторами [1,5].
В наших наблюдениях у больных, которым проводилось введение Актовегина, было отмечено снижение среднесуточного уровня гликемии с первых суток применения препарата. Кроме того, при применении Актовегина наблюдались быстрая ликвидация болевого синдрома (на 2–3 сут. введения препарата) и ускорение процессов грануляции и эпителизации ран с заживлением последних.
В группе, где проводилось лечение полиорганной дисфункции с использованием Актовегина, количество «больших» ампутаций уменьшилось до 6 (4,9%) при увеличении количества органосохраняющих операций. Сократилась продолжительность нахождения в стационаре до 20,2±2,7 суток по сравнению с контрольной группой 28,5±8,4 суток. В группе сравнения была констатирована летальность 3 (2,5%) пациентов; в основной группе летальных исходов не было.
Заключение
Использование предложенной шкалы оценки тяжести состояния больных с осложненными формами СДС позволяет более адекватно оценивать тяжесть состояния больных, более корректно определить объем и сроки операции, оценить эффективность предоперационной подготовки, улучшить результаты хирургического лечения в данной группе больных.
Полученные результаты свидетельствуют о высокой эффективности применения внутриартериальной и внутривенной инфузии Актовегина (в составе комплексного лечения) для снижения степени полиорганной дисфункции, что в конечном итоге улучшает результаты хирургического лечения.
Литература
1. Балаболкин М.И., Клебанова Е.М., Креминская В.М. Микроангиопатия – одно из сосудистых осложнений сахарного диабета //Consilium medicum. – 2000. –Т. 2. № 5.
2. Гурьева И.В., Кузина И.В., Воронин А.В., Комелягина Е.Ю., Мамонтова Е.Ю. Синдром диабетической стопы. – М., 2000. – 40 с.
3. Дедов И.И. Сахарный диабет – проблема XXI // Врач. – М., 2000.– С. 4–5.
4. Дедов И.И., Шестакова М.В., Максимова М.А. Национальные стандарты оказания помощи больным сахарным диабетом //Министерство Здравоохранения РФ.– М., 2003.
5. Земляной А.Б., Светухин А.М. Стандарты диагностики и комплексного хирургического лечения гнойно–некротических форм диабетической стопы //Материалы научно– практической конференции. – М., 2001.– С. 44–48.
5. Львова Л.В. В центре внимания// Провизор. –2003. – № 6.
6. Светухин A.M., Прокудина М.В. Комплексное хирургическое лечение больных с синдромом диабетической стопы //Хирургия.–1998.– №10. – С. 64–66.
7. Труды научно–практической конференции «Современные аспекты диагностики, лечения, профилактики поражений нижних конечностей у больных с сахарным диабетом». – М., 1996. – 243 с.
8. Larsson J., Agardh C.D., Apelqvist J., Stenstron A. // Foot Ankle Int. – 2003. – Vol. 16(2). – P. 69–74.
9. Wagner F.W. A classification and treatment program for diabetic, neuropatic and dysvas–cular foot problems. In The American Academy of Ortopaedic Surgeons instructional course lectures. – St. Louis. – Mosby Year Book. – 1979. – P. 143–165.












