По данным отечественной и зарубежной литературы, частота возникновения пролежней у малоподвижных пациентов составляет от 3 до 40%, достигая 80% у спинальных больных [1–10]. К группе риска возникновения пролежней относятся все люди с ограниченной подвижностью вследствие многообразных причин: заболеваний или травм спинного мозга, параличей, комы, онкологической патологии, длительного послеоперационного периода, продолжительного пребывания в отделениях реанимации и интенсивной терапии.
Во многих работах последних лет пролежни определяются как участки ишемии и некроза тканей вследствие нейротрофических нарушений. Этим подчеркиваются отсутствие иннервации в зоне поражения, низкая резистентность тканей и их слабая репаративная способность [4, 5]. К числу факторов, повышающих риск возникновения пролежней, относятся: пожилой возраст, дефицит питания, мышечная атрофия, курение, недержание мочи или кала, заболевания, сопровождающиеся нарушением микроциркуляции в тканях (облитерирующий атеросклероз, сахарный диабет).
Независимо от причины в основе патогенеза пролежней лежат нарушения трофики и защитных свойств кожи, развивающиеся вследствие тканевой гипоксии. Пролежни обычно развиваются в тех местах, где ткани испытывают интенсивное и продолжительное давление, особенно в области подкожных костных выступов. В лежачем положении у человека наибольшее давление – 40–60 мм рт. ст. испытывают области крестца, ягодиц, пяток и затылка. Согласно результатам экспериментальных исследований, имевших целью количественную оценку сдавливающего действия внешних факторов, установлено, что непрерывное давление 70 мм рт. ст. в течение 2 ч вызывает необратимые изменения в тканях. В то же время при прекращении давления каждые 5 мин в тканях возникают минимальные изменения без каких-либо последствий [5].
В ответ на давление первоначально ишемические изменения вследствие большей чувствительности к гипоксии развиваются прежде всего в мышечном слое над костным выступом. В условиях тканевой гипоксии увеличивается проницаемость капилляров с нарастанием тканевого отека, снижается напряжение кислорода в тканях, развиваются грубые нарушения структуры. Все это в итоге приводит к развитию трофических нарушений, которые впоследствии распространяются по направлению к коже. Последующая травматизация вследствие трения, смещения, мацерации и бактериальная контаминация кожи приводят к быстрому прогрессированию воспаления и некрозу [3–7].
В зависимости от расположения пациента (на спине, на боку, сидя в кресле) места сдавления тканей изменяются. Чаще всего это области ушной раковины, грудного отдела позвоночника, крестца, большого вертела бедренной кости, выступа малоберцовой кости, седалищного бугра, локтя, пяток. Реже пролежни появляются в области затылка, сосцевидного отростка, акромиального отростка лопатки, ости лопатки, латерального мыщелка, пальцев стоп. Наиболее типичной локализацией пролежней является крестцовая область. Около 36% случаев пролежней у малоподвижных пациентов развивается в этой области, 21% случаев приходится на области ягодиц, 25% – на пяточные области, 2–4% – на другие области [4, 11].
Длительно незаживающая раневая поверхность становится причиной хронической интоксикации, ведущей к анемии, гипопротеинемии, амилоидозу органов [1, 4, 5]. Являясь входными воротами для инфекции, пролежни часто становятся причиной сепсиса, в 20% заканчивающегося летальным исходом [4]. Летальность у больных с пролежневыми язвами, по данным различных авторов, колеблется в широких пределах – от 21 до 88,1% [1–8].
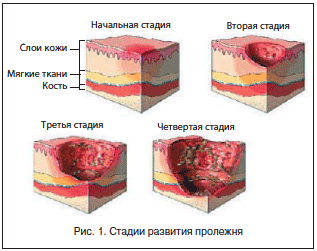
Течение пролежня подчиняется общим закономерностям раневого процесса, однако имеется и ряд особенностей, связанных с его развитием в условиях нервно-трофической дисфункции. Для определения исходного состояния пролежня и контроля за динамикой лечения оцениваются размер, форма пролежня, характер его краев и дна, состояние окружающих тканей. С целью объективизации данных о выраженности трофических расстройств была разработана классификация пролежней Pressure Ulcer Advisoriy Panel (1989), согласно которой выделяют 4 стадии пролежня (рис. 1) [9]:
• I стадия – кожный покров без повреждения, эпидермис интактен, отмечается эритема кожи в месте формирования пролежня, сохраняющаяся в течение 30 мин после изменения положения тела;
• II стадия – поверхностный дефект кожи в виде поражения эпидермиса, иногда с захватом дермы, что может проявляться в виде пузыря, который наполнен содержимым бурого цвета, на фоне эритемы кожи или в виде очага воспаления;
• III стадия – поражение кожи на всю ее толщину, образование язв с боковыми карманами; в центре язвенного образования, которое обращено внутрь, отмечаются очаги некроза и формирования свища за счет истончения кожного покрова;
• IV стадия – деструкция кожи и глубжележащих расположенных тканей; процесс некротизации захватывает подкожные структуры: фасции, мышцы и сухожилия, элементы сустава и костные образования.
В течении заболевания выделяют также этап первичной реакции, некротически-воспалительный этап и этап регенерации.
Проблема лечения пролежней у малоподвижных больных была и остается не только актуальной медицинской, но и социальной проблемой. При развитии пролежневых язв увеличивается продолжительность госпитализации пациента, появляется потребность в дополнительных перевязочных и лекарственных средствах, инструментарии, оборудовании. В ряде случаев требуется хирургическое лечение пролежней. Помимо экономических затрат, связанных с лечением пролежней, нужно учитывать и нематериальные затраты – тяжелые физические и моральные страдания, испытываемые пациентом.
Лечению пролежней посвящено большое количество работ как в отечественной, так и в зарубежной литературе [2–7, 9–11, 13, 14]. В них достаточно глубоко и подробно отражен патогенез развития пролежней, предлагаются многообразные классификации, методы профилактики и лечения, в т. ч. и хирургического, что свидетельствует о сложности и неоднозначности решения данной проблемы.
В лечении пролежней всегда необходим комплексный подход, направленный прежде всего на устранение основной причины – заболевания, вызвавшего появление пролежня, а также факторов, способствующих развитию пролежней. На каждой степени развития пролежня важно проводить профилактику его прогрессирования. Выбор локального лечения пролежней зависит от стадии процесса.
Пациенты с пролежнями I стадии не нуждаются в хирургическом лечении. Главными задачами лечения на этой стадии являются защита раны от инфекции и активная профилактика прогрессирования некротического изменения тканей. С целью предотвращения дальнейшего воздействия повреждающих факторов необходимо переворачивать пациента в кровати каждые 2 ч либо применять специальные средства для уменьшения локального давления на ткани. К последним относятся специальные кровати, матрацы, подушки, заполненные пеной, водой, воздухом, гелем или комбинацией этих материалов, оснащенные системами регулируемого давления и вибрации, обеспечивающие прерывистость давления. Следует соблюдать простые гигиенические правила ухода за лежачими больными, следить за чистотой и состоянием их кожи. Местное лечение формирующейся пролежневой язвы требует грамотного подхода и включает тщательную обработку области измененной кожи средствами, не обладающими ионообменными свойствами (физиологический раствор, камфорный спирт). Данный выбор средств имеет принципиальное значение, поскольку препараты, обладающие ионообменными свойствами (хлоргексидин, йодинол, повидон-йод и др.) нарушают проницаемость клеточных мембран, подавляют защитные функции клеток и создают благоприятные условия для развития микрофлоры и дальнейшего прогрессирования пролежня. После обработки пролежня важно применение средств, улучающих местное кровообращение и трофическое обеспечение тканей.
Пациенты с пролежнями II стадии также не нуждаются в хирургическом лечении. На этой стадии продолжается проведение активной профилактики прогрессирования некротического изменения тканей, достаточно ограничиться тщательной обработкой пролежневого дефекта, которая заключается в удалении общего загрязнения и эпидермиса в местах образования пузырей. Деэпителизированные участки кожи (так же как и на I стадии пролежневого процесса) не следует обрабатывать ионообменными антисептиками. Допустимо промывание раны физиологическим раствором, перекисью водорода. Для эпителизации измененных участков кожи в настоящее время в арсенале врача имеется широкое многообразие повязок, отличающихся по физическим свойствам, химическому составу, добавляемым в них лекарственным веществам [2] для лечения пролежневой раневой поверхности с учетом стадии, наличия или отсутствия некроза, площади поражения. Это и прозрачные пленочные повязки с клеящейся поверхностью, вафельные гидроколлоидные гидрогелевые повязки, полупроницаемые повязки на основе гидрополимера, губчатые повязки с верхним слоем из воздухопроницаемого полиуретана, который препятствует проникновению бактерий и жидкости.
Задачами лечения пролежней III стадии являются предупреждение дальнейшего прогрессирования некротического изменения подкожных тканей и удаление некрозов хирургическим путем, очищение пролежневой язвы от гнойного экссудата и остатков некроза, абсорбция отделяемого и предохранение заживающей раны от высыхания. Для местного лечения пролежней на этой стадии существует несколько групп препаратов, применение которых зависит от фазы раневого процесса. На этапе некротически-воспалительных изменений применяют местные антисептики (раствор Бeтaдина, мирамистин, перекись водорода, хлоргексидин), некролитические препараты (трипсин, химотрипсин, террилитин, коллагеназа), гиперосмолярные препараты и противовоспалительные средства (гидрокортизон, дексаметазон).
Значительное ослабление неприятного запаха из пролежневых язв достигается применением в качестве перевязочного материала 0,75% метронидазолового геля.
На этапе регенерации применяют стимуляторы репарации тканей (диоксометилтетрагидропиримидин, винилин, цинка гиалуронат, декспантенол).
На IV стадии формирования пролежня происходит глубокий некроз с вовлечением в патологический процесс мышц, сухожилий, суставных капсул и костей. Лечение заключается в некрэктомии, очищении пролежневой раны и стимуляции регенерации заживающей язвы. Медикаментозная терапия схожа с таковой, применяемой при лечении пролежней III стадии. Полное хирургическое иссечение всех мертвых тканей невозможно и нецелесообразно, поскольку точно определить границы некроза довольно сложно. Хирургическое очищение раны проводится с максимально возможным сохранением живых тканей в зонах суставных сумок, сосудисто-нервных пучков [4, 7].
В большинстве развитых стран мира, в т. ч. и у нас, пролежни у малоподвижных больных предпочитают лечить консервативно, что обусловлено экономическими причинами. Другой причиной низкой хирургической активности является высокий процент послеоперационных осложнений, обусловленных плохой подготовленностью пролежня к операции, остеомиелитом подлежащей кости, наличием высокопатогенной флоры, резистентной к большинству антибиотиков, большим натяжением краев раны, недостаточным уходом за больным после операции. В среднем, по данным разных авторов, только 50–75% пролежней после операции заживает первично. В остальных случаях необходима дополнительная, достаточно длительная консервативная терапия или повторная операция [2, 7, 9]. В ведущих клиниках мира, занимающихся проблемой лечения пролежней, пролежни II и III степени лечатся консервативно, операция выполняется только у больных с пролежнями IV степени.
По опыту лечения 695 пациентов с пролежнями различной локализации на фоне повреждения спинного мозга за период 1993–1997 гг. было показано, что основой лечения пролежней IV степени, длительно не заживающих или часто рецидивирующих пролежней II и III степени является оперативное вмешательство, что позволяет в десятки раз быстрее ликвидировать длительно существующие кожные язвы и значительно улучшить качество и продолжительность жизни пациентов [5]. Выбор метода хирургического лечения определяется размерами пролежня. Применяются иссечение пролежня с сопоставлением краев раны, свободная кожная пластика (аутодермопластика), пластика местными тканями, перемещенным кожным или кожно-мышечным лоскутом.
Обязательным условием для хирургического лечения пролежня является его тщательная комплексная предоперационная подготовка, которая может продолжаться от 2–3 мес. до 1 года.
Комплексное применение средств с рациональной антибактериальной терапией позволяет добиться быстрого очищения язвы и стабилизации состояния больного. Особенно эффективны мази на водорастворимой основе, поскольку они позволяют обеспечить выраженный дегидратационный эффект и положительно влияют на процессы заживления. Одним из эффективных антибактериальных препаратов является средство Бeтaдин, представляющее собой комплекс поливинилпирролидона и йода. Препарат обладает универсальным спектром активности: подавляет грамположительные бактерии, включая энтерококки и микобактерии, грамотрицательные бактерии, в т. ч. псевдомонады, ацинетобактерии, клебсиеллы, протей, споры бактерий, грибы, вирусы, включая вирусы гепатита В и С, энтеро- и аденовирусы, а также анаэробные, спорообразующие и аспорогенные бактерии [14–17].
Бактерицидное действие оказывает за счет образования белковых соединений йодаминов при контакте с белками бактериальной стенки или ферментными белками, в результате чего блокируется жизнедеятельность микроорганизмов. Благодаря большому размеру комплексной молекулы Бeтaдин плохо проникает через биологические барьеры, поэтому практически не проявляется системное действие йода. Проникновение в ткани на глубину около 1 мм не препятствует нормальным процессам регенерации. За счет постепенного высвобождения йода препараты Бeтaдина действуют длительно. Препарат выпускается в виде 10% раствора в зеленых пластмассовых флаконах по 30, 120 и 1000 мл; 10% мази в тубе по 20 г [17].
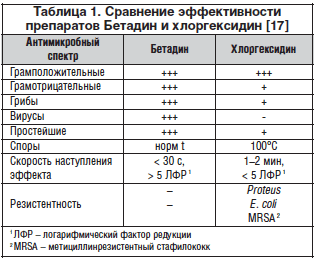
Исследования доказали высокую эффективность препарата Бeтaдин в сравнении с другими антисептиками (табл. 1) [17, 18].
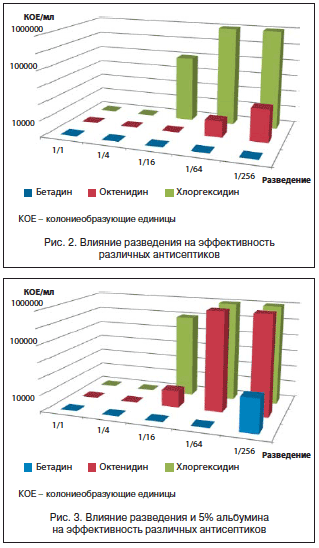
Бeтaдин эффективнее других антисептиков подавляет размножение микроорганизмов даже в большом разведении (рис. 2). Физико-химические условия в ране и очаге воспаления (рН, белок, кровь, ферменты) мало влияют на действие Бeтaдина (рис. 3) [19].
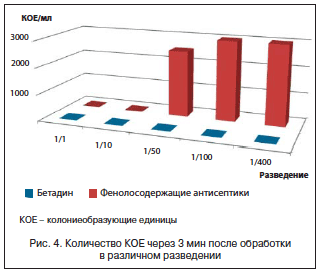
При стационарном лечении пролежней неэффективность консервативной терапии и предоперационной подготовки, а также большинство послеоперационных осложнений, как правило, связаны с высокопатогенной флорой, резистентной к большинству антибиотиков. Исследования 1998 г. подтверждают исключительно высокую эффективность Бeтaдина в профилактике и лечении инфекционных осложнений, вызванных высокорезистентной патогенной микрофлорой (рис. 4) [17].
В одно из исследований по оценке эффективности применения препарата Бeтaдин при лечении 156 больных с инфицированными ранами были включены пациенты с пролежнями. Бeтaдин продемонстрировал эффективность, способствовал отчетливому регрессу воспалительного процесса в течение первых 5–7 сут. На фоне лечения исследуемым препаратом исчезал отек тканей вокруг участка поражения, уменьшалось количество гнойного отделяемого, исчезали или становились менее интенсивными боли в ране, уменьшались размеры ран. При применении Бeтaдина отмечено снижение обсемененности ран ниже критического уровня – менее 103 КОЕ/г к 7,2 сут. Появление первых грануляций зафиксировано к 10,2 и 13,5 сут. Первые признаки краевой эпителизации в 1-й группе возникали через 13,9 сут. Клиническое исследование показало, что Бeтaдин является эффективным средством при лечении инфицированных ран в I–II фазах раневого процесса. Побочных эффектов, таких как аллергические общие и местные реакции, при использовании Бeтaдина не наблюдалось, препарат хорошо переносился пациентами [13].
Эффективность препарата Бeтaдин, помимо его применения в терапии пролежней, показана в лечении пациентов с ожогами, трофическими язвами, суперинфекционными дерматитами, вирусными заболеваниями кожи, в т. ч. вызванными вирусом герпеса и вирусом папилломы человека, у гинекологических больных и подтверждена многочисленными клиническими исследованиями [15, 17].
В настоящий момент проблема лечения пролежней у малоподвижных пациентов является трудной задачей. Дифференцированный подход к лечению в зависимости от стадии процесса, а также комбинированный способ ведения ран с использованием сочетанного применения групп препаратов в соответствии с фазой раневого процесса могут быть использованы в клинической практике как эффективный подход к лечению пролежней у малоподвижных больных.
Хирургические методы лечения пролежней являются методами выбора у пациентов с пролежнями IV степени и длительно не заживающими или часто рецидивирующими пролежнями II и III степени. Обязательным условием для хирургического лечения пролежня является тщательная его подготовка к операции, включающая рациональную антибиотикотерапию.
Среди антибактериальных препаратов местного применения Бeтaдин выделяют за счет его универсального спектра активности, что делает его незаменимым при лечении пролежней у малоподвижных пациентов. Высокая эффективность даже при разведении и изменении физико-химических условий в ране позволяет с успехом использовать препарат для лечения пролежневых ран. Удобные формы препарата Бeтaдин (раствор, мазь) позволяют широко применять его в клинической практике.












