–Ф–Њ–ї–≥–Њ–µ –≤—А–µ–Љ—П –Њ–њ–µ—А–∞—Ж–Є–µ–є –≤—Л–±–Њ—А–∞ —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е –њ—А–Є —А–∞–Ј–≤–Є—В–Є–Є –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –±—Л–ї–Є –≤—Л—Б–Њ–Ї–Є–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Ф–∞–љ–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ —Г –±–Њ–ї—М–љ—Л—Е –°–Ф –њ—А–Њ¬–Є–Ј–≤–Њ–і—П—В—Б—П –≤ 17–45 —А–∞–Ј —З–∞—Й–µ, —З–µ–Љ —Г –љ–∞—Б–µ–ї–µ–љ–Є—П –≤ —Ж–µ–ї–Њ–Љ, —В–Њ–≥–і–∞ –Ї–∞–Ї —З–∞—Б—В–Њ—В–∞ –Њ–Ї–Ї–ї—О–Ј–Є–Њ–љ–љ—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –њ—А–µ–≤—Л—И–∞–µ—В —В–∞–Ї–Њ–≤—Г—О —Г –ї–Є—Ж –±–µ–Ј –і–Є–∞–±–µ—В–∞ –ї–Є—И—М –≤ 4 —А–∞–Ј–∞. –°—В–Њ–ї—М –≤—Л—Б–Њ–Ї—Г—О —З–∞—Б—В–Њ—В—Г –∞–Љ–њ—Г—В–∞—Ж–Є–є –њ—А–Є –і–Є–∞–±–µ—В–µ –љ–µ–ї—М–Ј—П —Б—З–Є—В–∞—В—М –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –Њ–±–ї–Є—В–µ—А–Є—А—Г—О—Й–µ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є [1,4,5,9].
–Ш–Ј–Љ–µ–љ–µ–љ–Є—П —Б–Њ—Б—Г–і–Њ–≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞ –Є–Љ–µ—О—В –Њ—Б–Њ–±–µ–љ–љ–Њ –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –°–Ф–° –Є —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е –ї—О–±–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—П —Б–∞–Љ–∞ –њ–Њ —Б–µ–±–µ –љ–µ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —А–∞–Ј–≤–Є—В–Є—О —П–Ј–≤–µ–љ–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б¬—Б–∞ –љ–∞ —Б—В–Њ–њ–µ. –Т –Њ—Б–љ–Њ–≤–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –љ–µ–Ї—А–Њ–Ј–∞ –ї–µ–ґ–Є—В –љ–µ–і–Њ¬—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –Њ–±—Г—Б–ї–Њ–≤¬–ї–µ–љ–љ–∞—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є –Є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –Т–Љ–µ—Б—В–µ —Б —Н—В–Є–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Њ—В—П–≥–Њ—Й–∞—О—В –њ—А–Њ—П–≤–ї–µ–љ–Є—П –љ–µ–є—А–Њ– –Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є, —Б–Њ–Ј–і–∞–≤–∞—П —Г—Б–ї–Њ–≤–Є—П, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–µ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –≥–љ–Њ–є¬–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —В–Ї–∞–љ–µ–є —Б—В–Њ–њ—Л [2,3,6,11].
–Т –ї–Є—В–µ—А–∞—В—Г—А–µ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ —Г–і–µ–ї—П–µ—В—Б—П –Њ—Ж–µ–љ–Ї–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є –њ—А–Є –Є—Е –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –љ–∞ —Д–Њ–љ–µ –°–Ф, –Њ–і–љ–∞–Ї–Њ –Љ–љ–Њ–≥–Є–Љ–Є –∞–≤—В–Њ—А–∞–Љ–Є —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —А–∞–љ–љ—П—П –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф–° –њ–Њ–Ј–≤–Њ–ї—П–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ –Њ–њ—А–µ–і–µ–ї–Є—В—М —Г—А–Њ–≤–µ–љ—М –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –Є –≤—Л–±—А–∞—В—М –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –∞–Љ–њ—Г—В–∞—Ж–Є–Є, –љ–Њ –Є –≤—Л—П–≤–Є—В—М –љ–∞—З–∞–ї—М–љ—Л–µ —Б—В–∞–і–Є–Є –љ–∞—А—Г—И–µ–љ–Є—П –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –Њ–њ—А–µ–і–µ–ї–Є—В—М —В–∞–Ї—В–Є–Ї—Г –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ–≥–љ–Њ–Ј –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [11].
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Э–∞–Љ–Є –њ—А–Њ–∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П 214 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є –љ–∞ —Д–Њ–љ–µ –°–Ф–° –Ј–∞ –њ–µ—А–Є–Њ–і —Б 2002 –њ–Њ 2007 –≥–Њ–і. –£—Б–ї–Њ–≤–љ–Њ –≤—Б–µ –±–Њ–ї—М–љ—Л–µ –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л:
• 1 –≥—А—Г–њ–њ–∞ (105 —З–µ–ї–Њ–≤–µ–Ї) – –±–Њ–ї—М–љ—Л–µ, —Г –Ї–Њ—В–Њ—А—Л—Е –ї–µ—З–µ–±–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –і–∞–љ–љ—Л—Е –Є –і–∞–љ–љ—Л—Е –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–∞–Ї—А–Њ–≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є.
• 2 –≥—А—Г–њ–њ–∞ (109 —З–µ–ї–Њ–≤–µ–Ї) – –њ–∞—Ж–Є–µ–љ—В—Л, —Г –Ї–Њ—В–Њ—А—Л—Е –ї–µ—З–µ–±–љ–∞—П —В–∞–Ї—В–Є–Ї–∞ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М —Б —Г—З–µ—В–Њ–Љ –і–∞–љ–љ—Л—Е –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є.
–Т –љ–∞—И–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є—П—Е –њ—А–µ–≤–∞–ї–Є—А–Њ–≤–∞–ї–Є –±–Њ–ї—М–љ—Л–µ —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° – 152 —З–µ–ї–Њ–≤–µ–Ї–∞ (71,0%). –С–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –±—Л–ї–Њ 62 (29,0%).
–Ю–±—Б–ї–µ–і—Г–µ–Љ—Л–µ –±–Њ–ї—М–љ—Л–µ –±—Л–ї–Є –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 21 –і–Њ 90 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 65,1±2,1 –ї–µ—В).
–Я—А–µ–Њ–±–ї–∞–і–∞–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є – 87 –±–Њ–ї—М–љ—Л—Е (40,7%), –Є —Б —П–≤–ї–µ–љ–Є—П–Љ–Є –Њ—Б—В–µ–Њ–Љ–Є–µ–ї–Є—В–∞ –Ї–Њ—Б—В–µ–є —Б—В–Њ–њ—Л – 40 –±–Њ–ї—М–љ—Л—Е (18,7%). –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –∞–љ–∞–ї–Є–Ј–Є—А—Г–µ–Љ—Л—Е –±–Њ–ї—М–љ—Л—Е –Є–Љ–µ–ї–Є II–V —Б—В–∞–і–Є–Є –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ–Њ Wagner F.W.
–С–Њ–ї—М–љ—Л–µ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–∞—Е –±—Л–ї–Є —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ—Л –њ–Њ –≤–Њ–Ј—А–∞—Б—В—Г, —В—П–ґ–µ—Б—В–Є, –≥–ї—Г–±–Є–љ–µ –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Є –њ–Њ —З–∞—Б—В–Њ—В–µ –≤—Л—П–≤–ї–µ–љ–љ–Њ–є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є.
–Ю–±—Й–Є–µ –њ—А–Є–љ—Ж–Є–њ—Л –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –°–Ф–° –≤–Ї–ї—О—З–∞–ї–Є: —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї—Г—О –Њ–±—А–∞–±–Њ—В–Ї—Г –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—З–∞–≥–∞, –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є—О –°–Ф, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Г—О –∞–і–µ–Ї–≤–∞—В–љ—Г—О –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ—Г—О —В–µ—А–∞–њ–Є—О, –Љ–µ—Б—В–љ—Г—О —В–µ—А–∞–њ–Є—О —А–∞–љ—Л —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ–µ—А–µ–≤—П–Ј–Њ—З–љ—Л—Е —Б—А–µ–і—Б—В–≤, –і–≤–Є–≥–∞—В–µ–ї—М–љ—Г—О —А–∞–Ј–≥—А—Г–Ј–Ї—Г —Б—В–Њ–њ—Л, –Ї–Њ–ґ–љ—Г—О –њ–ї–∞—Б—В–Є–Ї—Г –і–µ—Д–µ–Ї—В–Њ–≤ —Б—В–Њ–њ—Л (–њ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ).
–£ –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –°–Ф–° –Њ—Ж–µ–љ–Ї–∞ —В–Њ–ї—М–Ї–Њ –ї–Є—И—М –Љ–∞–Ї—А–Њ–≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –љ–µ –≤—Б–µ–≥–і–∞ –∞–і–µ–Ї–≤–∞—В–љ–Њ –Њ—В—А–∞–ґ–∞–µ—В —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–Є—В–∞–љ–Є—П —В–Ї–∞–љ–µ–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Ю–±—Й–µ–њ—А–Є–љ—П—В–Њ, —З—В–Њ –њ—А–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є–Є –Є –њ—А–Є –љ–∞–ї–Є—З–Є–Є –≥–∞–љ–≥—А–µ–љ–Њ–Ј–љ–Њ––Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–∞ —Б—В–Њ–њ–µ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–Є–±–µ–≥–∞—О—В –Ї –≤—Л—Б–Њ–Ї–Є–Љ –∞–Љ–њ—Г—В–∞—Ж–Є—П–Љ –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є (—З–∞—Й–µ –љ–∞ —Г—А–Њ–≤–љ–µ –±–µ–і—А–∞). –Ф–µ—В–∞–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –±–Њ–ї–µ–µ –∞–і–µ–Ї–≤–∞—В–љ–Њ –Њ—Ж–µ–љ–Є—В—М —А–µ–Ј–µ—А–≤—Л –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є —Б—В—А–Њ–Є—В—М –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ—Г—О —В–∞–Ї—В–Є–Ї—Г —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –≤—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –≤—Л–њ–Њ–ї–љ–µ–љ–Њ —В—А–∞–љ—Б–Ї—Г—В–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–∞–њ—А—П–ґ–µ–љ–Є—П –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –≤ –Њ–±–ї–∞—Б—В–Є —Б—В–Њ–њ—Л –Є –≥–Њ–ї–µ–љ–Є (–Ґ—Б–†–Ю2) –∞–њ–њ–∞—А–∞—В–Њ–Љ –Ґ–°–Ь 400
(RADIOMETR), –ї–∞–Ј–µ—А–љ–∞—П –і–Њ–њ–њ–ї–µ—А–Њ–≤—Б–Ї–∞—П —Д–ї–Њ—Г–Љ–µ—В—А–Є—П (–Ы–Ф–§) –∞–њ–њ–∞—А–∞—В–Њ–Љ BLF–21 (TRANSONIC SYSTEMS), –£–Ч–Ф–У –њ–∞–ї—М—Ж–µ–≤—Л—Е –∞—А—В–µ—А–Є–є —Б—В–Њ–њ –і–∞—В—З–Є–Ї–Њ–Љ 16 –У—Ж –∞–њ–њ–∞—А–∞—В–Њ–Љ ANGIODIN–PC (–С–Ш–Ю–°–°).
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–ї—Б—П –±–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Є –і–Є–љ–∞–Љ–Є–Ї–∞ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –њ—А–Њ–±. –Т –љ–∞—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Љ—Л –њ—А–Є–Љ–µ–љ—П–ї–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї—Г—О –њ—А–Њ–±—Г, –Ї–Њ—В–Њ—А–∞—П –Ј–∞–Ї–ї—О—З–∞–ї–∞—Б—М –≤ –њ–Њ–і–љ—П—В–Є–Є –љ–Є–ґ–љ–µ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –≤ –ї–µ–ґ–∞—З–µ–Љ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –љ–∞ 30–45° –≤ —В–µ—З–µ–љ–Є–µ 3 –Љ–Є–љ. –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Ґ—Б–†–Ю2, –Є –≤ –Њ–њ—Г—Б–Ї–∞–љ–Є–Є –љ–Є–ґ–љ–µ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –≤ —В–µ—З–µ–љ–Є–µ 3 –Љ–Є–љ. –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Ы–Ф–§. –°—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є —В–Њ—З–Ї–∞–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ —П–≤–ї—П–ї–Є—Б—М: —В—Л–ї—М–љ–∞—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М —Б—В–Њ–њ—Л –≤ 1––Љ –Љ–µ–ґ–њ–∞–ї—М—Ж–µ–≤–Њ–Љ –њ—А–Њ–Љ–µ–ґ—Г—В–Ї–µ, –њ–Њ–і–Њ—И–≤–µ–љ–љ–∞—П –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М —Б—В–Њ–њ—Л –≤ –Њ–±–ї–∞—Б—В–Є —Б–≤–Њ–і–∞, –≤–µ—А—Е–љ—П—П —В—А–µ—В—М –≥–Њ–ї–µ–љ–Є –њ–Њ –љ–∞—А—Г–ґ–љ–Њ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —В–Њ—З–Ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Љ–µ–љ—П–ї–Є—Б—М.
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В –Ґ—Б–†–Ю2 –Є –Ы–Ф–§, –≥–і–µ –њ—А–Њ–Є–Ј–≤–Њ–і–Є—В—Б—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –њ—А–Є –£–Ч–Ф–У –њ–∞–ї—М—Ж–µ–≤—Л—Е –∞—А—В–µ—А–Є–є —Б—В–Њ–њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л–µ –њ–∞—А–∞–Љ–µ—В—А—Л –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, —В–∞–Ї–Є–µ –Ї–∞–Ї —Е–∞—А–∞–Ї—В–µ—А –Ј–≤—Г–Ї–Њ–≤–Њ–≥–Њ —Б–Є–≥–љ–∞–ї–∞ –Є —Д–Њ—А–Љ–∞ –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞–Љ–Љ—Л, –њ–Њ—Н—В–Њ–Љ—Г –і–∞–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є.
–Я–Њ –ї–Є—В–µ—А–∞—В—Г—А–љ—Л–Љ –і–∞–љ–љ—Л–Љ [10], –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ–Є –Ј–љ–∞—З–µ–љ–Є—П–Љ–Є –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ —П–≤–ї—П—О—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ґ—Б–†–Ю2>40 –Љ–Љ —А—В.—Б—В., —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±—Л –љ–∞ 10–15 –Љ–Љ —А—В.—Б—В. (—А–Є—Б. 1), –∞ –±–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ы–Ф–§>2,0 –њ—Д.–µ–і. —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –њ–µ—А—Д—Г–Ј–Є–Є –≤ 2–3 —А–∞–Ј–∞ –њ—А–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±–µ.
–Я—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–µ –°–Ф–° –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ–њ–∞¬—В–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –њ–∞—А–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–Љ—Г —А–∞—Б—И–Є—А–µ–љ–Є—О —И—Г–љ—В–Њ–≤ –Љ–µ–ґ–і—Г –∞—А—В–µ—А–Є–Њ–ї–∞–Љ–Є –Є –≤–µ–љ—Г–ї–∞–Љ–Є –Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –њ–Њ–≤—Л—И–µ–љ–Є—О –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –љ–Є—Е, —З—В–Њ —Г–Љ–µ–љ—М—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—Г—Й–µ—Б—В¬–≤—Г—О—Й–µ–є —В–Ї–∞–љ–µ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є. –£ –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° –≤ –Њ—Б–љ–Њ–≤–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –ї–µ–ґ–Є—В –Є—И–µ–Љ–Є—П –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –љ–∞–ї–Є—З–Є—П –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є. –Ю—В–µ–Ї –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ —В–∞–Ї–ґ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ (–Ї–∞–Ї –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є –њ—А–Є –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–µ –°–Ф–°).
–†–µ–Ј—Г–ї—М—В–∞—В—Л
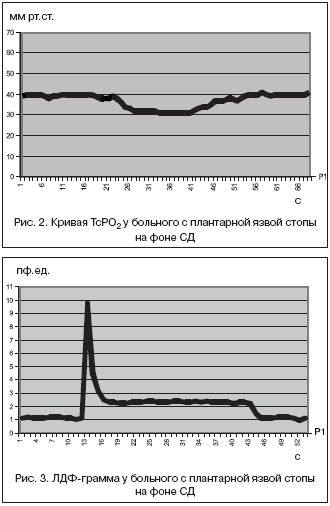
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° –±–µ–Ј –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б—В–Њ–њ—Л (–њ–ї–∞–љ—В–∞—А–љ—Л–µ —П–Ј–≤—Л, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є –Њ—Б—В–µ–Њ–Љ–Є–µ–ї–Є—В –Ї–Њ—Б—В–µ–є —Б—В–Њ–њ—Л –Є –і—А.) –Њ—В–Љ–µ—З–∞–ї—Б—П –±–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ґ—Б–†–Ю2 –Њ—В 30 –і–Њ 48 –Љ–Љ —А—В.—Б—В. (37,2±1,3) —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±—Л –Њ—В 20 –і–Њ 34 –Љ–Љ —А—В.—Б—В. (27,9±1,8) (—А<0,05) (—А–Є—Б. 2), –±–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ы–Ф–§ –±—Л–ї –Њ—В 1,0 –і–Њ 1,5 –њ—Д.–µ–і. (1,2±0,04) —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Ј–љ–∞—З–µ–љ–Є–є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±—Л –Њ—В 2 –і–Њ 3,2 –њ—Д.–µ–і. (2,5±0,12) (—А<0,05) (—А–Є—Б. 3).
–Я—А–Є –љ–∞–ї–Є—З–Є–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –≤ –Ј–Њ–љ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—Д–ї–µ–≥–Љ–Њ–љ–∞ —Б—В–Њ–њ—Л –Є –і—А.) –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –њ–Њ–≤—Л—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ґ—Б–†–Ю2>40 –Љ–Љ —А—В.—Б—В., –∞ –Ы–Ф–§>2,0 –њ—Д.–µ–і. —Б–Њ —Б–≥–ї–∞–ґ–µ–љ–љ–Њ–є —Д–Њ—А–Љ–Њ–є –Ї—А–Є–≤–Њ–є.
–Т –Ј–Њ–љ–µ –Є—И–µ–Љ–Є–Є —В–Ї–∞–љ–µ–є, —А–∞–Ј–≤–Є–≤—И–µ–є—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–Є–Ї—А–Њ—В—А–Њ–Љ–±–Њ–Ј–Њ–≤ –Љ–µ–ї–Ї–Є—Е –∞—А—В–µ—А–Є–є —Б—В–Њ–њ –љ–∞ —Д–Њ–љ–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ґ—Б–†–Ю2 –Є –Ы–Ф–§ –±—Л–ї–Є, –љ–∞–Њ–±–Њ—А–Њ—В, —А–µ–Ј–Ї–Њ —Б–љ–Є–ґ–µ–љ—Л (–Ґ—Б–†–Ю2 0–20 –Љ–Љ —А—В.—Б—В., –Ы–Ф–§<0,3 –њ—Д.–µ–і.).
–Э–∞–ї–Є—З–Є–µ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –∞–і–µ–Ї–≤–∞—В–љ–Њ –Њ—Ж–µ–љ–Є—В—М –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –≤ —Б—В–Њ–њ–µ, –њ–Њ—Н—В–Њ–Љ—Г –њ–Њ—Б–ї–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —П–≤–ї–µ–љ–Є–є –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ —Б –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ –і–∞–ї—М–љ–µ–є—И–µ–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —В–∞–Ї—В–Є–Ї–Є. –Ь–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–µ –°–Ф–° –±—Л—Б—В—А–Њ –Ї—Г–њ–Є—А—Г—О—В—Б—П –њ–Њ—Б–ї–µ –∞–і–µ–Ї–≤–∞—В–љ–Њ–є —Б–∞–љ–∞—Ж–Є–Є –≥–љ–Њ–є–љ–Њ–≥–Њ –Њ—З–∞–≥–∞, –∞–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–Њ–є –Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –њ–Њ—П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М —Б–Њ—Е—А–∞–љ–µ–љ–Є—П —Б—В–Њ–њ—Л –і–∞–ґ–µ –њ—А–Є –±–Њ–ї—М—И–Њ–Љ –Њ–±—К–µ–Љ–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П.
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Њ–њ–Њ—А–љ–∞—П —Д—Г–љ–Ї—Ж–Є—П —Б—В–Њ–њ—Л –±—Л–ї–∞ —Б–Њ—Е—А–∞–љ–µ–љ–∞ —Г –≤—Б–µ—Е 32 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–°, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –Є–Ј 30 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В–Њ–є –ґ–µ —Д–Њ—А–Љ–Њ–є –°–Ф–°, –њ—А–Є –Њ–±—И–Є—А–љ–Њ–Љ –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Г 3 –±–Њ–ї—М–љ—Л—Е (10,0%) –±—Л–ї–∞ –≤—Л–њ–Њ–ї–љ–µ–љ–∞ –∞–Љ–њ—Г—В–∞—Ж–Є—П –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –љ–∞ —Г—А–Њ–≤–љ–µ –≤–µ—А—Е–љ–µ–є —В—А–µ—В–Є –≥–Њ–ї–µ–љ–Є.
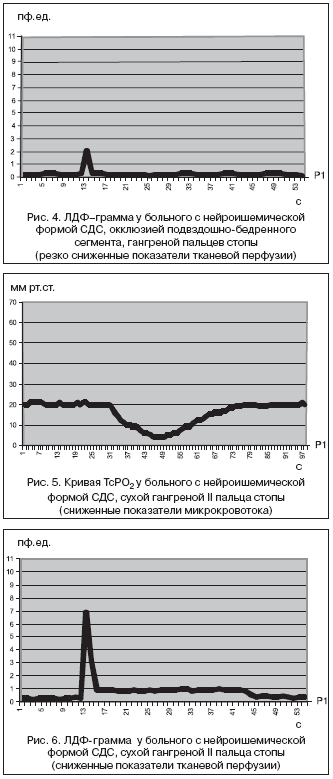
–£ –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—Ж–µ–љ–Є—В—М —Б—В–µ–њ–µ–љ—М –Є—И–µ–Љ–Є–Є, —Г—А–Њ–≤–µ–љ—М –Њ–Ї–Ї–ї—О–Ј–Є–Є –∞—А—В–µ—А–Є–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є, –Њ–±—К–µ–Љ –≥–∞–љ–≥—А–µ–љ–Њ–Ј–љ–Њ––Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –Я—А–Є –Њ–Ї–Ї–ї—О–Ј–Є–Є –∞—А—В–µ—А–Є–є —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –•–Р–Э IV —Б—В. –Є –Њ–±—К–µ–Љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є—П IV–V —Б—В. –њ–Њ F.W. Wagner, —Б–Њ—Е—А–∞–љ–µ–љ–Є–µ —Б—В–Њ–њ—Л –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤ —Б–≤—П–Ј–Є —Б –њ–Њ–ї–љ–Њ–є —Г—В—А–∞—В–Њ–є –µ–µ –љ–∞ —Д–Њ–љ–µ –≥–∞–љ–≥—А–µ–љ–Њ–Ј–љ–Њ––Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–ї–Њ—Б—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞. –£ —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ґ—Б–†–Ю2 –±—Л–ї–Є –Њ—В 1 –і–Њ 15 –Љ–Љ —А—В.—Б—В. (9,2±1,5) (—А<0,05) (—А–Є—Б. 1), –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Ы–Ф–§ –±—Л–ї–Є –Њ—В 0 –і–Њ 0,3 –њ—Д.–µ–і. (0,2±0,04) (—А<0,05) (—А–Є—Б. 4) –њ—А–Є –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±–µ.
–Т –і–∞–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –≤–∞–ґ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –≤–Њ–њ—А–Њ—Б –≤—Л–±–Њ—А–∞ —Г—А–Њ–≤–љ—П –∞–Љ–њ—Г—В–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є. –Ф–ї—П –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ–≥–Њ —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –Ї–Њ–ї–µ–љ–љ–Њ–≥–Њ —Б—Г—Б—В–∞–≤–∞ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –љ–∞ —Г—А–Њ–≤–љ–µ –≤–µ—А—Е–љ–µ–є —В—А–µ—В–Є –≥–Њ–ї–µ–љ–Є. –Ч–љ–∞—З–µ–љ–Є—П –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ґ—Б–†–Ю2>30 –Љ–Љ —А—В.—Б—В., –∞ –Ы–Ф–§>1,0 –њ—Д.–µ–і. —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –∞–Љ–њ—Г—В–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –љ–∞ –і–∞–љ–љ–Њ–Љ —Г—А–Њ–≤–љ–µ, –і–∞–ґ–µ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –Љ–∞–Ї—А–Њ–≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є (–Њ–Ї–Ї–ї—О–Ј–Є–Є –њ–Њ–і–Ї–Њ–ї–µ–љ–љ–Њ–є –∞—А—В–µ—А–Є–Є).
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Є–Ј 77 –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° –≤—Л—Б–Њ–Ї–Є–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л 23 –±–Њ–ї—М–љ—Л–Љ (29,9%), –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —Б–Њ—Е—А–∞–љ–Є—В—М –Ї–Њ–ї–µ–љ–љ—Л–є —Б—Г—Б—В–∞–≤ —Г–і–∞–ї–Њ—Б—М —Г 8 (34,8%) –±–Њ–ї—М–љ—Л—Е, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —Б—А–µ–і–Є 75 –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° —Г 31 (41,3%) –±–Њ–ї—М–љ–Њ–≥–Њ –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л –∞–Љ–њ—Г—В–∞—Ж–Є–Є –љ–∞ —Г—А–Њ–≤–љ–µ –±–µ–і—А–∞.
–Я—А–Є –Љ–µ–љ—М—И–µ–Љ –Њ–±—К–µ–Љ–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П (II–III —Б—В., –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ IV —Б—В. –њ–Њ F.W. Wagner) –Є–Љ–µ–µ—В—Б—П –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–∞ —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –Њ–њ–Њ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Б—В–Њ–њ—Л –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ –і–ї—П –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –љ–∞ —Г—А–Њ–≤–љ–µ —А–µ–Ј–µ—Ж–Є—А—Г–µ–Љ—Л—Е —В–Ї–∞–љ–µ–є.
–Я—А–Є –≤—Л—Б–Њ–Ї–Њ–є –Њ–Ї–Ї–ї—О–Ј–Є–Є —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –њ–∞—А—Ж–Є–∞–ї—М–љ–Њ–є –≥–∞–љ–≥—А–µ–љ—Л —Б—В–Њ–њ—Л –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –љ–Є–ґ–љ–µ–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є —П–≤–ї—П—О—В—Б—П –њ—А–Њ–±–ї–µ–Љ–∞—В–Є—З–љ—Л–Љ–Є –±–µ–Ј —А–µ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є. –£ —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –±–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ґ—Б–†–Ю2 –±—Л–ї –Њ—В 20 –і–Њ 29 –Љ–Љ —А—В.—Б—В. (25,9±0,7) —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±—Л –Њ—В 7 –і–Њ 21 –Љ–Љ —А—В.—Б—В. (14,8±0,9) (—А<0,05) (—А–Є—Б. 5). –С–∞–Ј–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –Ы–Ф–§ –±—Л–ї –Њ—В 0,3 –і–Њ 1,0 –њ—Д.–µ–і. (0,5±0,04) —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Ј–љ–∞—З–µ–љ–Є–є –њ—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –њ—А–Њ–±—Л –Њ—В 0,9 –і–Њ 2,3 –њ—Д.–µ–і. (1,5±0,1) (—А<0,05) (—А–Є—Б. 6).
–Ю–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ –Љ–µ—В–Њ–і–Њ–Љ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Є—И–µ–Љ–Є–Є —П–≤–ї—П–µ—В—Б—П —Б–Њ—Б—Г–і–Є—Б—В–∞—П —А–µ–Ї–Њ–љ—Б—В—А—Г–Ї—Ж–Є—П –∞—А—В–µ—А–Є–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–° —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–∞—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –Є—И–µ–Љ–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М 18 (23,4%) –±–Њ–ї—М–љ—Л–Љ.
–Я—А–Є –і–Є—Б—В–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ–µ –Њ–Ї–Ї–ї—О–Ј–Є–Є –∞—А—В–µ—А–Є–є, –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –±–µ—А—Ж–Њ–≤—Л—Е –Є —Б—В–Њ–њ–љ—Л—Е –∞—А—В–µ—А–Є–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —А–µ–≤–∞—Б–Ї—Г–ї—П—А–Є–Ј–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є —А–µ–Ј–Ї–Њ –Њ–≥—А–∞–љ–Є—З–µ–љ—Л. –Т –і–∞–љ–љ–Њ–є —Б–Є—В—Г–∞—Ж–Є–Є –Њ—Б–љ–Њ–≤–љ–∞—П —А–Њ–ї—М –Њ—В–≤–Њ–і–Є–ї–∞—Б—М –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є—И–µ–Љ–Є–Є. –Ф–ї—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞–Љ–Є –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –њ—А–µ–њ–∞—А–∞—В—Л –Є–Ј –≥—А—Г–њ–њ—Л –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ –Х1 –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б–Њ —Б—В–Є–Љ—Г–ї—П—В–Њ—А–∞–Љ–Є —В–Ї–∞–љ–µ–≤–Њ–є —А–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є (–Р–Ї—В–Њ–≤–µ–≥–Є–љ). –Ь–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Г—О –Ї–Њ—А—А–µ–Ї—Ж–Є—О –Є—И–µ–Љ–Є–Є –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є. –Т–∞–Ј–∞–њ—А–Њ—Б—В–∞–љ –≤–≤–Њ–і–Є–ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –≤ –і–Њ–Ј–µ 30 –Љ–≥ –љ–∞ 200 –Љ–ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 3 —З–∞—Б–Њ–≤. –Т–љ—Г—В—А–Є–≤–µ–љ–љ—Л–µ –Є–љ—Д—Г–Ј–Є–Є 10% —А–∞—Б—В–≤–Њ—А–∞ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤ –Њ–±—К–µ–Љ–µ 250 –Љ–ї –≤ —Б—Г—В–Ї–Є. –Ф–Њ–Ј–Є—А–Њ–≤–Ї–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–∞–≤–Є—Б–µ–ї–∞ –Њ—В –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ—Л –Є –Њ–±—К–µ–Љ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –і–Њ–Ј—Г –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є –і–Њ 500 –Љ–ї –≤ —Б—Г—В–Ї–Є.
–Я—А–Є —А–∞–Ј—А–µ—И–µ–љ–Є–Є –Ї—А–Є—В–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є —Б—В–Њ–њ—Л –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є—А–Њ—Б—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ґ—Б–†–Ю2 –љ–∞ 10 –Є –±–Њ–ї–µ–µ –Љ–Љ —А—В.—Б—В., –∞ –±–∞–Ј–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Ы–Ф–§ –љ–µ –Љ–µ–љ–µ–µ —З–µ–Љ –љ–∞ 0,5 –њ—Д.–µ–і. –Я–Њ—Б–ї–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Є—И–µ–Љ–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –љ–∞–Љ–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л –ї–Њ–Ї–∞–ї—М–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ —Б—В–Њ–њ–µ.
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ—Б–ї–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є—И–µ–Љ–Є–Є –Њ–њ–Њ—А–љ–∞—П —Д—Г–љ–Ї—Ж–Є—П —Б—В–Њ–њ—Л –±—Л–ї–∞ —Б–Њ—Е—А–∞–љ–µ–љ–∞ —Г 49 (94,2%) –±–Њ–ї—М–љ—Л—Е, —Г 3 (5,8%) –±–Њ–ї—М–љ—Л—Е –≤–≤–Є–і—Г –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –≥–∞–љ–≥—А–µ–љ–Њ–Ј–љ–Њ––Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є—И–ї–Њ—Б—М –≤—Л–њ–Њ–ї–љ–Є—В—М –≤—Л—Б–Њ–Ї–Є–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є (–≤ 2 (3,9%) —Б–ї—Г—З–∞—П—Е –љ–∞ —Г—А–Њ–≤–љ–µ –≥–Њ–ї–µ–љ–Є, –≤ 1 (1,9%) —Б–ї—Г—З–∞–µ –љ–∞ —Г—А–Њ–≤–љ–µ –љ–Є–ґ–љ–µ–є —В—А–µ—В–Є –±–µ–і—А–∞). –Т –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –ґ–µ –≥—А—Г–њ–њ–µ —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Є—Б—М —А–∞–Ј–ї–Є—З–љ—Л–µ –≤–Є–і—Л –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є—И–µ–Љ–Є–Є, 7 (13,7%) –±–Њ–ї—М–љ—Л–Љ –њ—А–Є—И–ї–Њ—Б—М –≤—Л–њ–Њ–ї–љ–Є—В—М –≤—Л—Б–Њ–Ї–Є–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є –љ–∞ —Г—А–Њ–≤–љ–µ –±–µ–і—А–∞.
–Ъ–Њ–љ–µ—З–љ—Л–Љ —Н—В–∞–њ–Њ–Љ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Г —А—П–і–∞ –±–Њ–ї—М–љ—Л—Е, –Ї–∞–Ї —Б –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є, —В–∞–Ї –Є —Б –љ–µ–є—А–Њ–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–Њ–є –°–Ф–°, –±—Л–ї–Њ –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ –Ї–Њ–ґ–љ–Њ––њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є –љ–∞ —Б—В–Њ–њ–µ (–∞—Г—В–Њ–і–µ—А–Љ–Њ–њ–ї–∞—Б—В–Є–Ї–∞, –њ–ї–∞—Б—В–Є–Ї–∞ –Љ–µ—Б—В–љ—Л–Љ–Є —В–Ї–∞–љ—П–Љ–Є, –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П –Ї–Њ–ґ–љ–∞—П –њ–ї–∞—Б—В–Є–Ї–∞).
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Ї–Њ–ґ–љ–Њ––њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є–µ –Њ–њ–µ—А–∞—Ж–Є–Є –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л —Г 21 (19,3%) –±–Њ–ї—М–љ–Њ–≥–Њ —Б —А–∞–љ–µ–≤—Л–Љ–Є –Є —П–Ј–≤–µ–љ–љ—Л–Љ–Є –і–µ—Д–µ–Ї—В–∞–Љ–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ–і–Њ–±–љ—Л–µ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞ –±—Л–ї–Є –≤—Л–њ–Њ–ї–љ–µ–љ—Л –ї–Є—И—М —Г 9 (8,6%) –±–Њ–ї—М–љ—Л—Е. –Ф–ї—П —Г–ї—Г—З—И–µ–љ–Є—П —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –Ї–Њ–ґ–љ–Њ–є –њ–ї–∞—Б—В–Є–Ї–Є –±–Њ–ї—М–љ—Л–Љ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –њ—А–Њ–≤–Њ–і–Є–ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л–µ –Є–љ—Д—Г–Ј–Є–Є 10% —А–∞—Б—В–≤–Њ—А–∞ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ –≤ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–µ.
–Ю—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤ –≤–Є–і–µ –љ–µ–Ї—А–Њ–Ј–Њ–≤ –Ї–Њ–ґ–љ—Л—Е –ї–Њ—Б–Ї—Г—В–Њ–≤ –Є –љ–∞–≥–љ–Њ–µ–љ–Є—П –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —А–∞–љ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –≤—Л—П–≤–ї–µ–љ—Л —Г 3 (14,3%) –±–Њ–ї—М–љ—Л—Е, –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ–і–Њ–±–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Є—Б—М 4 (44,5%) –±–Њ–ї—М–љ—Л—Е.
–Я—А–Њ–Є–Ј–≤–µ–і–µ–љ —А–∞—Б—З–µ—В —В–Њ—З–љ–Њ—Б—В–Є, —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В–Є –Ґ—Б–†–Ю2, –Ы–Ф–§ –Є –£–Ч–Ф–У –њ–∞–ї—М—Ж–µ–≤—Л—Е –∞—А—В–µ—А–Є–є —Б—В–Њ–њ—Л –≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –°–Ф–° (—В–∞–±–ї. 1).
–£—З–Є—В—Л–≤–∞—П –і–∞–љ–љ—Л–µ –Њ—Ж–µ–љ–Ї–Є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –°–Ф–° —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ґ—Б–†–Ю2 –Є –Ы–Ф–§, –Љ—Л –≤—Л—П–≤–Є–ї–Є —В—А–Є —В–Є–њ–∞ –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ (—В–∞–±–ї. 2).
–°—А–µ–і–Є –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е —Г 37 —З–µ–ї–Њ–≤–µ–Ї (33,9%) –≤—Л—П–≤–ї–µ–љ –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є —В–Є–њ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –љ–∞ —Б—В–Њ–њ–µ, —Г 52 –±–Њ–ї—М–љ—Л—Е (47,7%) –≤—Л—П–≤–ї–µ–љ —Б—Г–±–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є —В–Є–њ, –∞ —Г –Њ—Б—В–∞–ї—М–љ—Л—Е 20 –±–Њ–ї—М–љ—Л—Е (18,4%) –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є —В–Є–њ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є.
–Я—А–Є –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —В–Є–њ–µ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф–° –њ–µ—А—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –ї–Њ–Ї–∞–ї—М–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ —Б—В–Њ–њ–µ –±–µ–Ј –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є.
–Я—А–Є —Б—Г–±–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —В–Є–њ–µ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –ї–Њ–Ї–∞–ї—М–љ—Л–µ –Њ–њ–µ—А–∞—Ж–Є–Є –љ–∞ —Б—В–Њ–њ–µ –≤—Л–њ–Њ–ї–љ—П–ї–Є—Б—М —В–Њ–ї—М–Ї–Њ –њ–Њ—Б–ї–µ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –ї–Є–±–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є—И–µ–Љ–Є–Є. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Н—Д—Д–µ–Ї—В–∞ –Њ—В –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є—И–µ–Љ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б —Б—Г–±–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–Њ–Љ –љ–∞ —Б—В–Њ–њ–µ —А–µ—И–∞–ї—Б—П –≤–Њ–њ—А–Њ—Б –Њ —А–∞–і–Є–Ї–∞–ї—М–љ–Њ–є –Њ–њ–µ—А–∞—Ж–Є–Є (–≤—Л—Б–Њ–Ї–Њ–є –∞–Љ–њ—Г—В–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є).
–Я—А–Є –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —В–Є–њ–µ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –љ–∞ —Б—В–Њ–њ–µ (–њ—А–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Є—И–µ–Љ–Є–Є) –Љ—Л –≤—Л–њ–Њ–ї–љ—П–ї–Є –њ–µ—А–≤–Є—З–љ—Л–µ –≤—Л—Б–Њ–Ї–Є–µ –∞–Љ–њ—Г—В–∞—Ж–Є–Є –љ–∞ —В–Њ–Љ —Г—А–Њ–≤–љ–µ, –љ–∞ –Ї–Њ—В–Њ—А–Њ–Љ –≤—Л—П–≤–ї—П–ї—Б—П –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞–љ–љ—Л–є –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї.
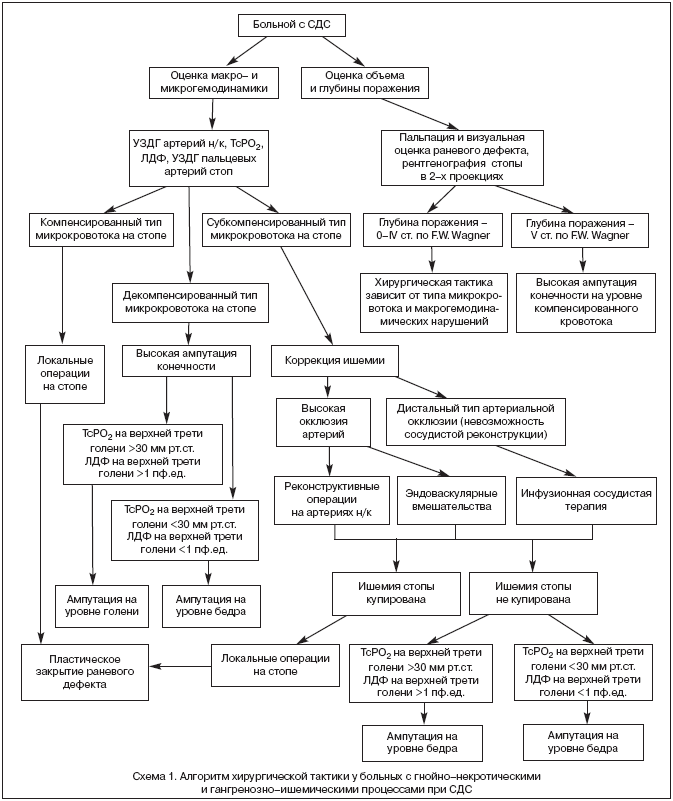
–Р–ї–≥–Њ—А–Є—В–Љ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —В–∞–Ї—В–Є–Ї–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є –њ—А–Є –°–Ф–° —Б —Г—З–µ—В–Њ–Љ –Њ–±—К–µ–Љ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Є –і–∞–љ–љ—Л—Е –Љ–∞–Ї—А–Њ– –Є –Љ–Є–Ї—А–Њ–≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –љ–∞ —Б—Е–µ–Љ–µ 1.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –≤ –≤–Є–і–µ —А–µ–∞–Љ–њ—Г—В–∞—Ж–Є–є, –љ–∞–≥–љ–Њ–µ–љ–Є–є –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —А–∞–љ, –љ–µ–Ї—А–Њ–Ј–Њ–≤ –Ї–Њ–ґ–љ—Л—Е –ї–Њ—Б–Ї—Г—В–Њ–≤ –Є –і—А. –≤—Л—П–≤–ї–µ–љ—Л —Г 14 (12,8%) –±–Њ–ї—М–љ—Л—Е, —З—В–Њ –њ–Њ—З—В–Є –≤ 2 —А–∞–Ј–∞ –Љ–µ–љ—М—И–µ, —З–µ–Љ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ, –≥–і–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –±—Л–ї–Є —Г 26 (24,8%) –±–Њ–ї—М–љ—Л—Е (—А<0,05), —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –і–µ—В–∞–ї—М–љ—Л–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ—Л –Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є (–≤–∞–Ј–∞–њ—А–Њ—Б—В–∞–љ, –Р–Ї—В–Њ–≤–µ–≥–Є–љ) –Ї–Њ—А—А–µ–Ї—Ж–Є–µ–є –Є—И–µ–Љ–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є.
–Ъ–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤—Л—Б–Њ–Ї–Є—Е –∞–Љ–њ—Г—В–∞—Ж–Є–є —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М —Б 32,4 –і–Њ 21,1%, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї–µ–µ —В—Й–∞—В–µ–ї—М–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ —А–µ–Ј–µ—А–≤–Њ–≤ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –≤ –Њ–±–ї–∞—Б—В–Є —Б—В–Њ–њ—Л –Є –≥–Њ–ї–µ–љ–Є, –Є –≤—Л–±–Њ—А–Њ–Љ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –∞–Љ–њ—Г—В–∞—Ж–Є–Є. –Т —Б—В—А—Г–Ї—В—Г—А–µ –≤—Л—Б–Њ–Ї–Є—Е –∞–Љ–њ—Г—В–∞—Ж–Є–є —Б 8,8 –і–Њ 34,8% —Г–≤–µ–ї–Є—З–Є–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –∞–Љ–њ—Г—В–∞—Ж–Є–є –љ–∞ —Г—А–Њ–≤–љ–µ –≥–Њ–ї–µ–љ–Є (–Ї–∞–Ї –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –±–Њ–ї–µ–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е) (—А<0,05).
–£–≤–µ–ї–Є—З–Є–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –≤—Л–њ–Њ–ї–љ—П–µ–Љ—Л—Е –Ї–Њ–ґ–љ–Њ––њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞–љ–µ–≤—Л–Љ–Є –Є —П–Ј–≤–µ–љ–љ—Л–Љ–Є –і–µ—Д–µ–Ї—В–∞–Љ–Є —Б—В–Њ–њ—Л (—Б 8,6 –і–Њ 19,3%), —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї–µ–µ —В—Й–∞—В–µ–ї—М–љ—Л–Љ –Њ—В–±–Њ—А–Њ–Љ –±–Њ–ї—М–љ—Л—Е, –Ї–Њ—В–Њ—А—Л–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –≤—Л–њ–Њ–ї–љ–µ–љ–Є–µ –і–∞–љ–љ—Л—Е –Њ–њ–µ—А–∞—Ж–Є–є —Б –Њ–ґ–Є–і–∞–µ–Љ—Л–Љ —Е–Њ—А–Њ—И–Є–Љ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –ї–µ—З–µ–љ–Є—П (—А<0,05).
–°—А–µ–і–љ–Є–µ —Б—А–Њ–Ї–Є —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —Г–Љ–µ–љ—М—И–Є–ї–Є—Б—М —Б 38,2±2,9 –і–Њ 31,4±2,3 –і–љ–µ–є, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї–µ–µ —В—Й–∞—В–µ–ї—М–љ–Њ–є –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Њ–є –Є —А–∞–љ–љ–Є–Љ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–µ–Љ —В–∞–Ї—В–Є–Ї–Є –і–∞–ї—М–љ–µ–є—И–µ–≥–Њ –ї–µ—З–µ–љ–Є—П (—А<0,05).
–Т—Л–≤–Њ–і—Л
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –Љ–Є–Ї—А–Њ–Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф–° —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–Љ—Г –≤—Л–±–Њ—А—Г —В–∞–Ї—В–Є–Ї–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—О –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Ї–Њ–ґ–љ–Њ––њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є –љ–∞ —Б—В–Њ–њ–µ, –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Є—О –Ї–Њ–љ—В—А–Њ–ї—П –Ј–∞ —В–µ—З–µ–љ–Є–µ–Љ —А–∞–љ–µ–≤–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞, –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—О –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –∞–Љ–њ—Г—В–∞—Ж–Є–Є –Ї–Њ–љ–µ—З–љ–Њ—Б—В–Є, –њ—А–Њ–≥–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —В–µ—А–∞–њ–Є–Є, —З—В–Њ –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ –≤–µ–і–µ—В –Ї –Њ–њ—А–∞–≤–і–∞–љ–љ–Њ–Љ—Г —Б–Њ—Е—А–∞–љ–µ–љ–Є—О —Б—В–Њ–њ—Л –Є –µ–µ –Њ–њ–Њ—А–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є. –Ш—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —В–µ—А–∞–њ–Є–Є 10% —А–∞—Б—В–≤–Њ—А–∞ –Р–Ї—В–Њ–≤–µ–≥–Є–љ–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—О –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е —П–≤–ї–µ–љ–Є–є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф–°, —Б–Ї–Њ—А–µ–є—И–µ–Љ—Г –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—О –Њ—Б—В–∞—В–Њ—З–љ—Л—Е —А–∞–љ–µ–≤—Л—Е –і–µ—Д–µ–Ї—В–Њ–≤ –њ–Њ—Б–ї–µ –≤—Л–њ–Њ–ї–љ—П–µ–Љ—Л—Е –Ї–Њ–ґ–љ–Њ-–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –Њ–њ–µ—А–∞—Ж–Є–є, —З—В–Њ, –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М, –≤–µ–і–µ—В –Ї —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О –Њ–±—Й–Є—Е —Б—А–Њ–Ї–Њ–≤ –ї–µ—З–µ–љ–Є—П –Є —Б–Ї–Њ—А–µ–є—И–µ–є —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є –±–Њ–ї—М–љ–Њ–≥–Њ.



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С—А–µ–≥–Њ–≤—Б–Ї–Є–є –Т.–С., –Ч–∞–є—Ж–µ–≤ –Р.–Р., –Ч–∞–ї–µ–≤—Б–Ї–∞—П –Р.–У., –Ъ–∞—А–њ–Њ–≤ –Ю.–Ш., –Ъ–∞—А–њ–Њ–≤–∞ –Ш.–Р., –¶–≤–µ—В–Ї–Њ–≤–∞ –Ґ.–Ы. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є –њ—А–Є —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ // –Ь. – –°–њ–±. – 2004. – 263 —Б.
2. –С—А–Є—Б–Ї–Є–љ –С.–°., –Я—А–Њ—И–Є–љ –Р.–Т., –Я–Њ–ї—П–љ—Б–Ї–Є–є –Ь.–Т., –Ы–µ–±–µ–і–µ–≤ –Т.–Т., –Я–Є—А–Њ–µ–≤–∞ –Ъ.–≠. –Р–љ—В–Є–±–∞–Ї—В–µ—А–Є–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ —Б–Є–љ–і—А–Њ–Љ–∞ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л // Consilium Medicum. – вДЦ 1. – 2006. – –°. 16–20.
3. –У–Њ—А—О–љ–Њ–≤ –°.–Т., –†–Њ–Љ–∞—И–Њ–≤ –Ф.–Т., –С—Г—В–Є–≤—Й–µ–љ–Ї–Њ –Ш.–Р. «–У–љ–Њ–є–љ–∞—П —Е–Є—А—Г—А–≥–Є—П» –Р—В–ї–∞—Б // –Ь. «–С–Є–љ–Њ–Љ» 2004. – 556 —Б.
4. –Ф–µ–і–Њ–≤ –Ш.–Ш., –£–і–Њ–≤–Є—З–µ–љ–Ї–Њ –Ю.–Т., –У–∞–ї—Б—В—П–љ –У.–†. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П —Б—В–Њ–њ–∞ // –Ь. – 2005. – 175 —Б.
5. –°–≤–µ—В—Г—Е–Є–љ –Р.–Ь., –Ч–µ–Љ–ї—П–љ–Њ–є –Р.–С. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –≥–љ–Њ–є–љ–Њ––љ–µ–Ї—А–Њ—В–Є—З–µ—Б–Ї–Є—Е —Д–Њ—А–Љ –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л.// –Ш–Ј–±—А–∞–љ–љ—Л–є –Ї—Г—А—Б –ї–µ–Ї—Ж–Є–є –њ–Њ –≥–љ–Њ–є–љ–Њ–є —Е–Є—А—Г—А–≥–Є–Є. –Ь. 2007. – –°. 153–171.
6. –°–∞–ї—В—Л–Ї–Њ–≤ –С.–С., –Я–∞—Г–Ї–Њ–≤ –Т.–°. –Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—П // –Ь. – 2002. – 238 —Б.
7. Dinh T.L., Veves A. Treatment of diabetic ulcers // Dermatol. Ther. 2006. – вДЦ6. – —А. 348–355.
8. Loredo R.A., Garcia G., Chhaya S. Medical imaging of the diabetic foot // Clin Podiatr Med Surg. 2007. – вДЦ3. – —А. 397–424.
9. Mandracchia V.J., Robert Y., Donald B. et al. The Diabetic Foot: Treatment Strategies // Hospital Medicine 1999. – вДЦ1. – —А. 27–33.
10. Rooke T. TcPO2 in non–invasive vascular medicine // Blood Gas News. – 1998. – вДЦ7. – —А. 21–23
11. Tooke J.E., London U.K. Diabetic angiopathy // Arnold Publishers. – 1999. – p. 304.












