Интерес к проблеме послеоперационной боли и обезболивания обусловлен в первую очередь пониманием большой роли адекватной анальгезии в реабилитации пациентов после операции, особенно пациентов высоких степеней риска.
Сами по себе болевые ощущения после операции составляют лишь часть проблемы, в то же время являясь первопричиной развития патологического послеоперационного синдромокомплекса, способствуя развитию осложнений. Острая боль повышает ригидность дыхательных мышц грудной клетки и брюшной стенки, что приводит к уменьшению дыхательного объема, жизненной емкости легких, функциональной остаточной емкости и альвеолярной вентиляции. Следствием этого являются коллапс альвеол, гипоксемия и снижение оксигенации крови. Болевой синдром затрудняет откашливание, нарушает эвакуацию бронхиального секрета, что способствует ателектазированию и создает благоприятные условия для развития легочной инфекции.
Боль сопровождается гиперактивностью симпатической нервной системы, что проявляется такими клиническими симптомами, как тахикардия, артериальная гипертензия, повышение сосудистого сопротивления. У лиц без сопутствующей патологии сердечный выброс обычно увеличивается, но при дисфункции левого желудочка может снижаться. Кроме того, симпатическая активация является одним из факторов, вызывающих послеоперационную гиперкоагуляцию за счет повышения адгезивности тромбоцитов и угнетения фибринолиза, и, следовательно, повышает риск тромбообразования. На этом фоне у пациентов с высоким риском кардиальных осложнений высока вероятность развития острого инфаркта миокарда.
Повышение активности симпатической нервной системы на фоне болевого синдрома приводит к увеличению тонуса сфинктеров и снижению перистальтической активности кишечника и моторики мочевыводящих путей, что вызывает соответственно послеоперационный парез и задержку мочи. Гиперсекреция желудочного сока опасна образованием стрессовых язв, а ее сочетание с угнетением моторики предрасполагает к развитию тяжелых послеоперационных пневмоний. Послеоперационный парез кишечника может замедлить выздоровление и продлить сроки госпитализации.
Интенсивная боль является одним из факторов реализации катаболического гормонального ответа на травму: концентрация катехоламинов, кортизола, глюкагона повышается, а инсулина и тестостерона снижается. Развивается отрицательный азотистый баланс, гипергликемия и повышенный липолиз. Повышение концентрации кортизола в сочетании с увеличением уровня ренина, альдостерона, ангиотензина и антидиуретического гормона вызывает задержку натрия, воды и вторичное увеличение объема внеклеточного пространства.
Невозможность ранней мобилизации пациентов на фоне неадекватной анальгезии повышает риск развития венозных тромбозов и тромбоэмболии легочной артерии. Операционный стресс приводит к лейкоцитозу и лимфопении, угнетает ретикулоэндотелиальную систему. Отмечается также существенное ухудшение иммунного статуса и повышение частоты септических осложнений послеоперационного периода при неадекватном купировании болевого синдрома, особенно у пациентов группы повышенного риска.
Ноцицептивная стимуляция модулирующих систем спинного мозга может привести к расширению рецепторных полей и повышению чувствительности боль-воспринимающих нейрональных структур спинного мозга. Результатом является формирование хронических послеоперационных нейропатических болевых синдромов. В частности, от одной до двух третей пациентов, перенесших операции на грудной клетке, в течение длительного периода времени страдают от постторакотомических болей.
Эти и другие данные способствовали появлению в последние годы большого количества исследований, посвященных изучению механизмов послеоперационной боли и сенситизации, разработке новых методик анальгезии, оптимизации организационных подходов к ведению больных в послеоперационном периоде, поиску новых эффективных анальгетиков, изучению влияния адекватности обезболивания на исход. Методы послеоперационного обезболивания представлены в таблице 1.

Шкалы предъявляют пациенту, и он сам отмечает на ней степень своих болевых ощущений (рис. 1). Эти шкалы необходимы для количественной характеристики динамики интенсивности хронического болевого синдрома в процессе лечения.
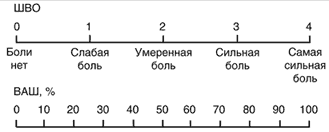
Рис. 1. Шкалы оценки интенсивности боли
Важным считается тестирование пациентов с помощью ВАШ не только в покое, но и при движении и откашливании. Эффективным обезболивание можно считать при наличии оценки по ВАШ при откашливании 3 балла (или %) и ниже. При таких значениях ВАШ пациенты в состоянии двигаться, довольно глубоко дышать и эффективно откашливаться, что снижает риск развития легочных и тромботических осложнений.Для оценки интенсивности болевого синдрома у пациентов ОРИТ, которым проводится искусственная вентиляция легких и седация, предложена поведенческая шкала боли (Behavioral Pain Scale, BPS), оценка по которой может быть произведена в ходе наблюдения за больными. Интенсивность болевого синдрома оценивается по состоянию мимической мускулатуры, движениям верхних конечностей, синхронности с аппаратом ИВЛ. Исследования показали, что, используя BPS, можно достоверно оценить выраженность болевого синдрома.
Лекарственные препараты, наиболее часто используемые для послеоперационной анальгезии:
– нестероидные противовоспалительные препараты (НПВП);
– опиаты и опиоиды (наркотические анальгетики);
– местные анестетики;
– центральные a-адренопозитивные препараты (клонидин и его аналоги);
– ингибиторы протеаз;
– вспомогательные лекарственные средства (бензодиазепины, кофеин, декстроамфетамин, дифенин, карбамазепин, фенотиазины, бутирофеноны).
Опиаты и опиоиды
Морфин применяется обычно в дозе 10 мг в/м, действие его продолжается 3-5 часов. Максимальная доза для взрослых: разовая - 0,02 г, суточная - 0,05 г. Наиболее важные побочные эффекты - угнетение дыхания, тошнота и рвота. Хотя морфин имеет ряд нежелательных побочных эффектов, он является отличным анальгетиком и принят в качестве золотого стандарта, в сравнении с которым оценивается действие всех остальных опиоидов.
Промедол применяется обычно в дозе 20 мг в/м, что вызывает 3-4-х часовую анальгезию. По анальгетической активности он несколько слабее морфина, но значительно менее токсичен, в меньшей степени угнетает дыхательный центр, реже вызывает рвоту.
Омнопон представляет собой смесь гидрохлоридов алкалоидов опия, где на долю морфина приходится около 50%, применяется в дозе 20 мг. Максимальная доза для взрослых: разовая - 0,03 г, суточная - 0,1 г. Обладает меньшей анальгетической активностью, чем морфин и промедол, что обусловливает его меньшую популярность.
Бупренорфина гидрохлорид - относится к частичным агонистам m-опиоидных рецепторов, одновременно являясь антагонистом k-опиоидных рецепторов. Бупренорфин по анальгетической активности превосходит морфин в 30-40 раз, его разовая доза составляет при в/м и в/в введении 0,3 - 0,6 мг, при сублингвальном - 0,2 - 0,4 мг. Важное преимущество препарата - возможность его применения в различных формах - внутримышечное, внутривенное, сублингвальное, а также в форме назального спрея. Длительность действия препарата - 6-8 часов. Отличительная особенность бупренорфина - его высокое сродство к m-опиоидным рецепторам, вследствие чего депрессия дыхания, вызванная бупренорфином, лишь частично устраняется высокими дозами конкурентного антагониста налоксона гидрохлорида.
Трамадола гидрохлорид (Трамал) - анальгетик, опосредующий обезболивающий эффект как через m-опиоидные рецепторы, так и путем ингибирования норадренергического и серотонинергического механизма передачи болевой импульсации. Трамадол характеризуется сравнительно высокой биодоступностью - 60-70 % при разных способах введения, быстрым и длительным болеутоляющим эффектом. Анальгетическая активность составляет 0,05-0,09 активности морфина (по некоторым источникам - в 5 раз ниже, чем у морфина, и в 2 раза выше активности кодеина).
У человека биотрансформация препарата осуществляется в основном печенью через О-диметилирование и конъюгацию продуктов О-диметилирования. Основным путем выведения трамадола и его 11 метаболитов является экскреция почками (90%) и частично через билиарный тракт. Период полувыведения трамадола из организма составляет 5 - 6 часов.
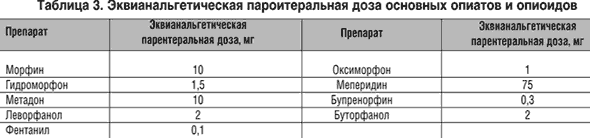
Существенное преимущество трамадола по сравнению с другими опиоидными анальгетиками крайне низкая степень привыкания и минимальный наркогенный потенциал этого препарата. Отдельное удобство представляет наличие большого количества лекарственных форм (табл. 2).

В отличие от других опиоидов, в эквианальгетических дозах трамадол не вызывает запора, не угнетает кровообращения и дыхания. Из возможных побочных эффектов следует отметить развитие тошноты, головокружения, в редких случаях рвоты. Эти реакции обычно преходящие, в большинстве случаев не требуют отмены препарата и могут быть купированы назначением метоклопрамида. В целом, трамадол положительно зарекомендовал себя в клинической практике. По разным данным, эффективность трамадола в травматологии, ортопедии, хирургии и онкологии варьирует от 66 до 94% (M. Cossmann et al., 1987, 1988; A. Anderson, 1994).
Помимо применения трамадола в качестве анальгетика, с 1989 г. он используется (хотя механизм этого действия остается до конца неясным) для купирования мышечного тремора в ближайшем постнаркозном и послеоперационном периодах (Р.Н. Лебедева, 1989).
Буторфанола тартрат - агонист-антагонист - синтетический анальгетик класса налорфин-циклазоцина. Для в/в и в/м введения применяется в дозе 2 мг; продолжительность действия 3-4 часа. Анальгетическая активность препарата в 5-7 раз выше морфина. Анальгетический эффект буторфанола опосредуется путем взаимодействия с k-опиоидными рецепторами, поэтому препарат оказывает определенное депрессивное влияние на функцию дыхания. К положительным сторонам препарата относятся: низкий наркогенный потенциал, отсутствие влияния на моторику ЖКТ и тонус сфинктеров. К отрицательным - неблагоприятное воздействие на гемодинамику и вероятность развития дисфории.
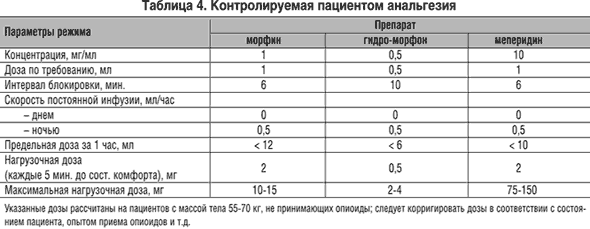
Налбуфина гидрохлорид - агонист-антагонист опиоидных рецепторов. Агонистическая активность препарата опосредуется через k-опиоидные рецепторы. Анальгетическая активность налбуфина по сравнению с морфином, составляет 0,5-1, то есть 10 мг налбуфина эквивалентны такой же дозе морфина. Налбуфин обладает низкой степенью развития привыкания и незначительным влиянием на гемодинамику. Препарат вызывает незначительное угнетение дыхания, не имеющее клинического значения. Для налбуфина характерно наличие эффекта «потолка» в отношении анальгетической активности и влияния на дыхание - повышение дозы налбуфина не усиливает анальгезию и депрессию дыхания («потолок» составляет около 30 мг/70 кг). Эквианальгетические дозы препаратов и контролируемая пациентом анальгезия представлены в таблицах 3 и 4.
К плюсам традиционной анальгезии относятся: легкость применения, дешевизна метода, а также постепенное развитие побочных эффектов, что дает больше возможностей борьбы с ними. Однако эта методика часто приводит к неадекватному обезболиванию (более 60% пациентов отмечают неудовлетворительное качество послеоперационной анальгезии). Причины этого кроются в том, что вводятся фиксированные дозы, без учета фармакологической вариабельности; часто инъекции опиоидов производятся с большими перерывами, то есть тогда, когда уже произошел «прорыв» боли. Немаловажным моментом является также то, что при внутримышечном пути введения начало обезболивания - замедленное.
Внутривенное введение опиоидов: болюс, продолжительная инфузия, контролируемое пациентом обезболивание (КПО). Болюсное введение - наиболее быстрый способ достижения анальгезии. Быстрее действуют те препараты, которые более липофильны. Этот метод применяется для анальгезии пациентов, находящихся на ИВЛ в условиях ОИТ. Угнетение дыхания в такой ситуации является преимуществом.
КПО - метод, использующий быстрый анальгетический эффект болюсного введения. Пациент определяет скорость в/в введения препарата, обеспечивая тем самым контроль с обратной связью. Прибор для КПО включает точный источник инфузии и контролируемое устройство пациент-прибор. Для ограничения устанавливаемой дозы, числа доз, которые могут быть введены, а также интервала между дозами предусмотрено специальное устройство безопасности. Ниже приведены параметры КПО.
При КПО устранение боли обеспечивается лучше, чем при обычном методе периодического внутримышечного введении анальгетика.
Трансдермальное применение - фентанил, будучи высоколипофильным веществом, легко проникает через кожу. Наклейки с фентанилом позволяют поддерживать постоянную концентрацию препарата в крови с помощью системы, которую заменяют каждые 3 сут. Трансдермальная система высвобождает препарат со скоростью 25 мкг/ч. Максимальный болеутоляющий эффект после наложения наклейки развивается в течение 24-72 час. Ввиду широкой фармакологической вариабельности такого пути у разных пациентов, этот метод мало пригоден для контроля острой боли. Метод более применим для устранения хронической боли при злокачественных заболеваниях в терминальной стадии.
Ректальное введение опиоидов - этот путь введения широко не применяется. Из прямой кишки опиоиды быстро всасываются и попадают в систему нижней полой вены, а затем, минуя печень, в системный кровоток. Однако при этом отмечается значительная вариабельность достигаемой плазменной концентрации препарата. Считается, что лучшим показанием к ректальному введению опиоидов служит трудноконтролируемая хроническая боль, сопровождающаяся дисфагией.
Сублингвальное применение бупренорфина позволяет достичь хорошего уровня анальгезии. Сочетание этого метода с введением агонистов опиоидных рецепторов может привести к развитию дисфории и возобновлению болевого синдрома; так что, при выборе этого способа анальгезии, важно использование бупренорфина в качестве единственного опиоида в период подготовки и проведения операции, а также в послеоперационном периоде.
Длительная эпидуральная анальгезия
Длительная эпидуральная анальгезия (ДЭА) является эффективным методом купирования острой боли после операции, с низким риском развития побочных эффектов и высокой степенью удовлетворенности пациентов качеством обезболивания. Эта методика абсолютно показана у пациентов с высоким риском развития сердечно-легочных осложнений после торакальных, ортопедических, абдоминальных операций. В проведении ДЭА нуждаются от 5 до 15% хирургических больных.
С появлением местных анестетиков длительного действия стало возможным проведение продленной эпидуральной инфузии, которая обладает определенными преимуществами перед болюсными введениями.
Однако существуют и недостатки продленной эпидуральной инфузии. Если очаги болевой импульсации значительно удалены друг от друга, невозможно провести полноценное обезболивание. Возможно обеспечение анальгезии на протяжении 5-7 дерматомов, в проекции которых находится кончик эпидурального катетера.
В настоящее время в клинических условиях для эпидурального обезболивания используются следующие группы препаратов:
– местные анестетики (угнетают аксональную и синаптическую возбудимость ноцицептивных нейронов);
– адренергические агонисты (тормозят передачу болевых импульсов за счет воздействия на постсинаптические адренергические нейроны);
– опиоидные агонисты (действуя на пресинаптические опиоидные рецепторы, ингибируют синаптическую передачу (угнетение высвобождения вещества Р из первичных афферентных нейронов), на постсинаптические рецепторы - вызывают гиперполяризацию мембран нейронов задних рогов спинного мозга).
Местные анестетики, такие как лидокаин и бупивакаин, высокоэффективны для достижения и поддержания адекватной анальгезии. Применение лидокаина ограничено коротким периодом действия, высокой вероятностью развития тахифилаксии и появления симптомов общей интоксикации, выраженным моторным блоком. Отличительными особенностями бупивакаина при эпидуральном введении являются большая продолжительность действия и относительно дифференцированное выключение сенсорных волокон при сохранении моторной функции. Бупивакаин является почти идеальным средством для эпидуральной анальгезии в послеоперационном периоде.
По некоторым данным, постоянная инфузия бупивакаина в концентрации 0,25% и выше может вызвать гипотензию, мышечную слабость, сенсорную блокаду, вероятно, связанные с накоплением системного токсического уровня препарата. Отмечено также, что при инфузионном введении бупивакаина возможно развитие тахифилаксии.
Была установлена высокая кардиотоксичность бупивакаина, связанная с его высокой липофильностью и высоким сродством к натриевым каналам миокарда, а также выявлена отрицательная инотропная активность вследствие вмешательства бупивакаина во внутриклеточные токи кальция и негативное действие на синтез АТФ в митохондриях.
Ропивакаина гидрохлорид - обладает меньшей токсичностью и большей продолжительностью действия, чем бупивакаин. При использовании равных концентраций и доз ропивакаин вызывает меньшую моторную блокаду, чем бупивакаин, при одинаковой эффективности анальгезии. Способность ропивакаина вызывать дифференцированный блок определила его клиническое преимущество над бупивакаином для эпидуральной инфузии в послеоперационном периоде.
Согласно исследованиям, ропивакаин в дозе от 675 до 800 мг в течение 72 ч хорошо переносится всеми пациентами без явлений кумуляции и токсических эффектов. При двухкратном превышении судорожных дозировок ропивакаин менее аритмогенен, чем бупивакаин. Кроме того, отмечено, что с ропивакаином связано меньше симптомов со стороны ЦНС, чем с бупивакаином, причем пациенты были устойчивы к дозам ропивакаина на 25% больше, чем бупивакаина. Следует сказать, что пока не зарегистрировано и ни одного случая аллергической реакции на ропивакаин.
Ропивакаин в концентрации 2 мг/мл, вводимый со скоростью 8-12 мл/ч, позволяет обеспечить оптимальный баланс между адекватной анальгезией и минимальным моторным блоком.
С целью улучшения качества послеоперационного обезболивания без увеличения частоты побочных эффектов к местным анестетикам добавляют опиатные и опиоидные анальгетики.
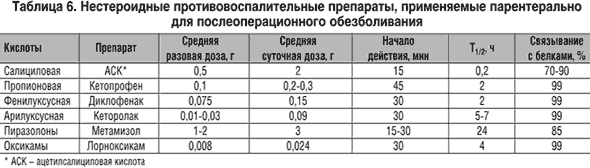
Методики, основанные на введении опиоидов в эпидуральное пространство, широко применяются в США и Австралии и представляют собой либо болюсное введение таких препаратов, как морфин, диаморфин, петидин или продолжающуюся инфузию липофильных опиоидов, таких как фентанил и суфентанил (табл. 5 и 6).
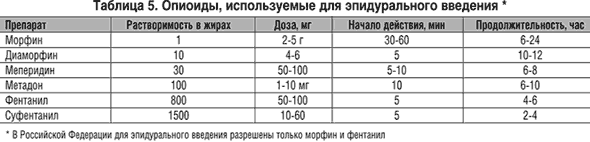

Кроме того, используются различные комбинации вышеуказанных препаратов в малых дозах с целью достижения синергистического анальгетического эффекта. Считается, что малые дозы местных анестетиков облегчают связывание опиоидов с рецепторами, потенцируют действие опиодов на пресинаптические кальциевые каналы за счет снижения проводимости С-волокон задних корешков воротной зоны. Данная комбинация эффективна у пациентов, толерантных к опиоидным анальгетикам. Наиболее часто комбинируют 0,125% бупивакаин или 0,2% ропивакаин с морфином, фентанилом, меперидином. Доказано, что добавление к опиоидам a-адренопозитивных препаратов позволяет уменьшить их дозу. В частности, 150 мкг клонидина при эпидуральном введении удваивают продолжительность анальгетического действия 100 мкг фентанила. Некоторые исследователи сообщают об использовании в качестве адъюванта антагониста NMDA–рецепторов кетамина.
Осложнения ДЭА могут быть связаны с побочными эффектами используемых препаратов. Например, кожный зуд и тошнота при использовании опиоидов или гипотензия при применении местных анестетиков и клонидина, а также моторный блок - при использовании местных анестетиков. Осложнения эпидуральной анальгезии редки, однако могут стать катастрофическими. Крайне редко наблюдаются признаки раздражения мозговых оболочек по типу асептического менингита (0,07%), самостоятельно купирующиеся после удаления эпидурального катетера. Одним из наиболее грозных осложнений ДЭА является образование эпидуральной гематомы с компрессией спинного мозга и развитием параплегии. Факторами, предрасполагающими к развитию данного осложнения, являются: травматичная пункция и катетеризация эпидурального пространства, исходные нарушения гемостаза и антикоагулянтная терапия. Большинство специалистов считает возможным применение эпидуральной анальгезии у пациентов с высоким риском сердечно-легочных осложнений, получающих антикоагулянты. При этом желательно установить катетер до начала антикоагулянтной терапии и не удалять до ее прекращения.
Инфекционные осложнения редки - до 2:13000 пациентов. Случаи развития этих осложнений связаны с более длительным временем стояния эпидурального катетера, чем в среднем в популяции, или с наличием у пациента дисфункции иммунной системы (злокачественные новообразования, диабет, политравма, ХНЗЛ). В литературе нет сообщений о формировании эпидурального абсцесса при длительности стояния эпидурального катетера в течение 2 суток или меньше.
Эпидуральный катетер, как правило, удаляют через 3-7 суток. Эпидуральная анальгезия заменяется пероральным приемом НПВП и других препаратов.
Нестероидные противовоспалительные препараты (НПВП)
Эти препараты следует рассматривать, как одно из наиболее перспективных и действенных патогенетических средств защиты периферических ноцицепторов. Механизм действия этих препаратов связан с ингибированием синтеза простагландинов, сенсибилизирующих периферические болевые рецепторы.
За последние десятилетия были созданы новые препараты для парентерального введения из группы НПВП, выделяющиеся своей анальгетической активностью, которые наравне с опиоидными анальгетиками могут применяться для купирования послеоперационной боли (табл. 6). По сравнению с опиоидами их основные преимущества - минимальное влияние на состояние систем кровообращения и дыхания, моторику желудочно-кишечного тракта, тонус сфинктеров, отсутствие наркогенного потенциала. Кроме того, НПВП свое основное анальгетическое действие оказывают в месте возникновения боли.
Принципиальный механизм противовоспалительного действия НПВП обусловлен подавлением активности циклооксигеназы (ЦОГ) - ключевого фермента синтеза простагландинов.
В настоящее время установлено существование двух изоформ - ЦОГ-1 и ЦОГ-2, обладающих соответственно физиологическим цитопротективным действием и индуцируемым провоспалительным. Изофермент ЦОГ-1 постоянно присутствует во многих тканях, синтезирующих простагландины, регулирует нормальную активность клеток, обеспечивая тем самым цитопротекцию слизистой желудочно-кишечного тракта (ЖКТ), сосудистый гемостаз и функционирование почек. Продукция же изофермента ЦОГ-2 индуцируется только в очаге воспаления, определяя избыточное образование простагландинов провоспалительной активности. Эти данные позволили создать концепцию: эффективность и безопасность НПВП связаны с избирательным подавлением ЦОГ-2. Следовательно, НПВП, сильнее подавляющие активность ЦОГ-1 (например, ацетилсалициловая кислота), чаще вызывают поражение ЖКТ, чем препараты, более подавляющие ЦОГ-2 или обладающие сбалансированным действием в отношении обоих ЦОГ (диклофенак натрия, кетопрофен), либо время-зависимым эффектом в отношении ЦОГ-1 (ибупрофен).
Особенно важно, что изучение механизмов действия НПВП послужило мощным толчком к созданию новых препаратов, в значительной мере лишенных побочных эффектов. Среди них пока наиболее изучены преимущественно селективные ингибиторы ЦОГ-2 (мелоксикам, нимесулид), накапливаются данные и о специфических ингибиторах ЦОГ-2 (целекоксиб).
Среди неселективных НПВП наибольший интерес представляет кетопрофен, привлекающий анестезиолога целым рядом преимуществ. Весьма важно, что кетопрофен выпускается в разнообразных формах (инъекционной, таблетированной, в форме капсул, крема и в виде свечей). Разовая доза составляет 100 мг, суточная доза препарата - 300 мг.
Препарат характеризуется быстрым и мощным анальгетическим эффектом, сравнимым с опиоидным, а потому находит оправданное применение в хирургической практике при подготовке к операции и в послеоперационном периоде. Кетопрофен отличается коротким периодом полувыведения (1,5-2 часа), исключающим кумуляцию. Кетопрофен не оказывает угнетающего воздействия на кроветворение.
Ингибиторы протеаз
Как мы уже упоминали выше, ноцицепция включает в себя ряд физиологических процессов: трансдукцию, трансмиссию, модуляцию и и перцепцию. Трансдукция сопровождается выбросом в кровь большого количества медиаторов боли, среди которых основными являются кинин-калликреиновый и простагландиновый каскады. Ингибиторы протеаз, подавляя избыточную активность этих каскадов, тормозят формирование боли на уровне трансдукции.
Центральные a-адренопозитивные препараты
Трансмиссия и модуляция боли зависят от соотношения синтеза нейротрансмиттеров, облегчающих и тормозящих проведение боли. Среди последних ведущую роль играет норадреналин - нейротрансмиттер собственной антиноцицептивной системы. Клонидин, стимулируя центральные a1- и, в большей степени, a2–адренорецепторы, тормозит проведение боли на сегментарном уровне, воздействуя на процессы трансдукции и модуляции боли.
Вспомогательные лекарственные средства
Бензодиазепины в комбинации с рядом других лекарственных средств способны внести вклад в проблему терапии болевого синдрома, в том числе фантомно-болевого синдрома.
Установлено, что комбинированная терапия на основе применения анаприлина, амитриптилина, феназепама и тизанидина позволяет после операций ампутации конечности полностью купировать каузалгический болевой синдром в 28% случаев и существенно ослабить боль - в 42,8% случаев.
В последнее время большое внимание уделяется так называемой предупреждающей (pre-emptive) анальгезии. Концепция предупреждающей анальгезии основана на том, что обезболивание, предвосхищающее болевое воздействие, предупреждает (частично или полностью) последующую боль. Глубокая соматическая боль способна вызвать длительные изменения возбудимости спинного мозга; в этом случае для обезболивания необходимы большие дозы опиоидов. Изменения в ноцицептивной системе могут быть предупреждены назначением анальгетиков до хирургического вмешательства.
Предупреждающая анальгезия способна предотвратить гипервозбудимость ЦНС, снижая потребность в анальгетиках в послеоперационном периоде. Возможно, такая анальгезия подавляет развитие нейрональной пластичности, которая имеет определенное значение при нейропатической боли.
Для предупреждающей анальгезии используются различные методики, одной из которых является введение нестероидного противовоспалительного препарата еще до основного болевого воздействия, то есть до начала хирургического вмешательства. При проведении регионарной анестезии нестероидный противовоспалительный препарат должен вводиться до начала манипуляций, связанных с проведением этого вида анестезиологического пособия.
Концепция сбалансированной анальгезии аналогична концепции сбалансированной анестезии. Для послеоперационной анальгезии можно использовать комбинацию препаратов, действующих на разные участки передачи боли: на периферии, на соматические и симпатические нервы, на уровне спинного и головного мозга.
Преимущество такого подхода в том, что комбинация препаратов обеспечивает отличную анальгезию, а дозу каждого из них можно уменьшить.
Передача боли может блокироваться на следующих этапах:
1) подавление механизмов периферических ноцицепторов с помощью НПВП;
2) блокада афферентной нейрональной передачи посредством регионарного блока;
3) воздействие как на уровне спинного мозга, так и высших центров системно вводимых опиоидов.
Послеоперационное обезболивание может также поддерживаться комбинированным применением одного из анальгетиков периферического действия (кетопрофена и др.) в сочетании с Трамалом, средняя анальгетическая суточная доза которого колеблется от 345±29 мг в 1–е сутки после операции до 205±16 мг (4–е сутки). При этом достигается хорошая анальгезия при активном состоянии оперированных больных без серьезных побочных симптомов, свойственных морфину и промедолу.
Естественно, что методику сбалансированной анальгезии не требуется применять после небольших операций, когда достаточно проведения предупреждающей анальгезии нестероидным противовоспалительным препаратом и использования того же НПВП в послеоперационном периоде. Она показана при обширных хирургических вмешательствах.
1. Вейн А. М., Авруцкий М. Я. Боль и обезболивание. - Москва, 1997, 279 с.
2. Лебедева Р.Н., Никода В.В. Фармакотерапия острой боли. - М.:» Аир-Арт», 1998, - 184 с.
3. Осипова Н. А., Новиков Г. А., Прохоров Б. М. Хронический болевой синдром в онкологии. Москва, «Медицина», 1998.
4. Wall P. D., Melzack R. (Eds) Textbook of pain, 3rd ed., Churchill Livingstone, Edinburgh, 1994.
5. Ready L.B., Edwards W.T. Management of acute pain: a practical guide. // IASP Publications, Seattle, Ready L.B., Edwards W.T. Management 1992.
6. Rawal N. Postoperative pain and its management, p. 367, In Raj P.P., Practical Management of Pain, 2nd Ed, Mosby-year Book, Malvers, PA, 1992
7. Tucker G.T., Mather L.E. Properties, Absorption, and Disposition of Local Anesthetic Agents. Neural Blockade in Clinical Anesthesia and Management of Pain. // third Edition 1998.
8. Крыжановский Г.Н. Детерминантные структуры в патологии нервной системы. - М.,1980.
9. Яковлева Л.В., Шаповал О.Н., Зупанец И.А. // Современные аспекты рационального обезболивания в медицинской практике. - Киев «Морион», - 2000. - С.6- 12.
10. Ferrante F.M., VadeBoncouer T.R. Postoperative Pain Management / Послеоперационная боль, М.: Медицина, 1998. - 640 c.












