Радикальное хирургическое лечение пролежней IV степени остается очень сложной проблемой, поскольку только 50–75% пролежней после операции заживает первичным натяжением, сохраняется высоким процент послеоперационных осложнений [5, 6].
Поиск препаратов, имплантируемых интраоперационно, полностью биодеградирующих, гипоаллергенных и обладающих выраженным эффектом стимуляции регенерации и репарации, активно осуществляется во всем мире. Биоматериал на основе нативного коллагена Коллост производства ЗАО «БиоФармахолдинг» при поддержке ООО «Ниармедик Плюс» (Россия) идеально соответствует решению этих задач, поэтому был применен в комплексном хирургическом лечении пациентов с пролежнями IV степени [4].
Материалы и методы
В своей работе мы пользовались классификацией трофических дефектов The Agency for Health Care Policy and Research (AHCPR), которая основана [9] на описании внешнего вида пролежня и глубины поражения тканей:
I степень – эритема, не распространяющаяся на здоровые участки кожи, без признаков язвообразования.
II степень – частичное снижение толщины кожи, связанное с повреждением эпидермиса или кожи; поверхностная язва в виде ссадины, пузыря или неглубокого кратера.
III степень – полная потеря толщины кожи, развившаяся вследствие повреждения или некроза тканей, располагающихся под ней, но не глубже фасции.
IV степень – полная потеря толщины кожи с некрозом или разрушением тканей мышц, костей и других опорных структур (сухожилия, связки, капсулы суставов и т. д.).
С применением биопластического материала Коллост пролечено 26 больных с пролежнями IV степени: у 14 – в области крестца, у 6 – в области седалищного бугра, у 6 – в области большого вертела. Эти пациенты составили основную группу (ОГ). Группу сравнения (ГС) составили 27 пациентов с той же патологией и локализацией пролежней (табл. 1).
Обе группы были сопоставимы по возрасту, полу, основному и сопутствующим заболеваниям, а также локализации и длительности существования пролежней. Пациенты обеих групп получали общепринятое общее и местное лечение [2, 6–8].
Хирургический этап в ОГ был, как правило, трехмоментным, а в ГС – двухмоментным. Первой операцией в обеих группах являлась максимально возможная у конкретного пациента радикальная некрэктомия (включая остеонекрэктомию, которую мы предпочитали производить осциллирующей пилой).
На 2-м этапе оперативного лечения (в стадии пролиферации) в ОГ для временного закрытия раневого дефекта применялся Коллост в виде мембран 60х50 мм и толщиной 1,5 мм, геля 7 или 15%, порошка. Количество необходимого для введения или имплантации биоматериала определялось индивидуально и зависело от размеров раневого дефекта. Проводились микроинъекции геля в края и дно раны, затем раневая поверхность импрегнировалась порошком.
Завершающим этапом являлось полное закрытие раневого дефекта мембранами, отмоделированными по размерам раны (при этом края мембраны должны были выступать за края раны на 2–3 мм). Мембраны фиксировались к кожным краям раны одиночными швами по всему периметру, а при необходимости сшивались друг с другом с целью формирования непрерывного покровного «полотна».
В послеоперационном периоде проводились перевязки в среднем 1 раз в 5 дней, при этом наложенные салфетки поддерживались в постоянно увлажненном состоянии с помощью водного раствора антисептика (1% раствора гидроксиметилхиноксилиндиоксида, 0,01% раствора бензилдиметил-миристоиламино-пропиламмония и др.).
Швы, как правило, снимали через 4–6 нед. после максимальной или полной биодеградации мембраны.
Лечение пациентов в ГС после первой операции было консервативным и общепринятым [6].
Окончательное закрытие раневого дефекта в обеих группах осуществлялось либо с помощью наложения вторичных швов, либо путем перемещения полнослойного кожно-мышечного лоскута, либо выполнением аутодермопластики (АДП).
Результаты
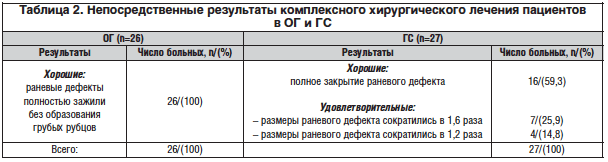
В ОГ непосредственные результаты комплексного стационарного хирургического лечения были хорошими у всех 26 больных (100%) – раневые дефекты полностью зажили без образования грубых рубцов (табл. 2).
В ГС у 16 пациентов раневые дефекты полностью закрылись, у 4 – размеры раневого дефекта сократились в 1,6 раза, у 4 – в 1,2 раза. Наблюдались случаи реинфицирования и суперинфицирования ран после выполненной некрэктомии: непосредственные хорошие результаты составили 55,6%, относительно удовлетворительные – 44,4% (табл. 2).
У пациентов ОГ на фоне биодеградации биоматериала Коллост активизировались процессы образования грануляционной ткани, краевая эпителизация, что позволило достигнуть более ранней, чем в ГС, готовности раны к закрытию с помощью наложения вторичных швов либо путем перемещения полнослойного кожно-мышечного лоскута, либо выполнением АДП.
Суммарная длительность подготовки раны к полному закрытию тем или иным способом (вторичные швы, закрытие перемещенным кожно-мышечным лоскутом, выполнение АДП) составила 35,0±4,8 сут в ОГ и 61,2±9,1 сут в ГС (р<0,01). Все пролеченные больные наблюдались нами в сроки до 2-х лет.
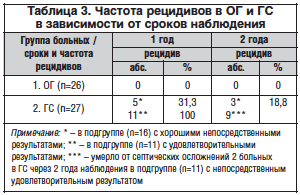
В ОГ у всех 26 пациентов в течение 2-х лет наблюдения не отмечено ни одного рецидива пролежня в области хирургического вмешательства с применением биоматериала Коллост.
В ГС у 5 пациентов из 16 с полным заживлением пролежней в результате комплексного хирургического лечения без применения Коллоста в течение 1-го года наблюдения отмечен рецидив заболевания, что потребовало проведения повторного курса комплексного хирургического лечения. Еще у 3 из 16 больных в ГС, закончивших лечение с хорошими результатами, наступил рецидив в течение 2-го года наблюдения, что также потребовало повторной госпитализации для проведения комплексного стационарного хирургического лечения.
У 11 пациентов из ГС, у которых удалось в результате комплексного хирургического лечения добиться сокращения раневого дефекта в 1,2 и 1,6 раза (4 и 7 пациентов соответственно), в течение первого года наблюдения потребовались повторные госпитализации и проведение в условиях стационара комплексного хирургического лечения с удовлетворительными результатами. К концу 2-го года наблюдения в ГС умерли от септических осложнений 2 пациента из 11, у которых получены удовлетворительные результаты после первого курса комплексного хирургического стационарного лечения без применения Коллоста (табл. 3).
Обсуждение
Эффективность коллагенового биопластического материала Коллост является многофакторной, что согласуется с данными других исследователей [9, 10].
1. Препарат обладает выраженной биосовместимостью, что позволяет использовать его для закрытия покровных дефектов различной локализации и глубины.
2. Сохраненная нативная структура коллагеновых волокон I типа способствует более быстрой инициации биодеградации за счет миграции в препарат макрофагов и фибробластов, регулируемой сложными медиаторными системами репарации и регенерации тканей.
3. Продукты биодеградации материала Коллост как местно, так и на системном уровне инициируют клеточную миграцию, пролиферацию и рост новой полноценной ткани на месте дефекта.
4. Биоматериал Коллост, выступая в роли внеклеточного матрикса, обеспечивает направляемый контакт эпителиальных клеток и фибробластов, обеспечивая их оптимальную миграцию и необходимую пространственную ориентацию.
5. Фибробласты, кровеносные и лимфатические сосуды, нервные волокна из окружающей здоровой ткани, внедряясь в коллагеновую матрицу биопластического материала, распространяются строго по ней (структурированная репарация и регенерация).
6. Благодаря структурированной репарации и регенерации практически исключается беспорядочный рост грануляционной и рубцовой тканей.
7. Плотное прилегание Коллоста препятствует проникновению инфекции из внешней среды в рану, параллельно с этим предотвращает потерю богатого протеином раневого экссудата.
8. Возможна шовная фиксация биоматериала к окружающим тканям благодаря достаточно высокой прочности и пластичности мембран Коллост.
9. Коллост, являясь нативным белком, легко образует комплексы с различными лекарственными агентами, в т. ч. с антибактериальными, противогрибковыми препаратами, антисептиками.
Анализ полученных результатов убедительно доказывает не только высокую эффективность биоматериала Коллост в отношении сокращения сроков заживления раны или ее подготовки к закрытию вторичными швами, перемещенным кожно-мышечным лоскутом, с помощью АДП, но и полноценности новообразованных покровных тканей с преобладанием процессов истинной регенерации, а не репарации (рубцевания). Это заключение тесно перекликается и в основном соответствует данным, полученным другими авторами [1, 4, 9, 10].
Выводы
Применение биоматериала Коллост в комплексном хирургическом лечении пациентов с пролежнями IV степени значительно (в 1,75 раза) позволяет сократить сроки подготовки раны к полному закрытию путем наложения вторичных швов либо перемещения кожно-мышечного лоскута, либо выполнения того или иного вида АДП за счет активизации процессов матрично-направленного образования грануляционной ткани, эпителизации и системных процессов активации регенеративных процессов.
Клинические примеры
Клиническое наблюдение № 1 (рис. 1)
Пациент А., 77 лет, около 15 лет назад перенес геморрагический инсульт с выраженными остаточными неврологическими дефектами: тетраплегия, полное отсутствие речи. Диагностирован пролежень IV степени по классификации AHCPR в области крестца общей площадью 106 см2. Длительность существования пролежня – около 3-х лет (рис. 1 а).
Назначено общее лечение (дезагреганты, нейропротекторы, антигипоксанты, витамины группы В, антибактериальная, противовоспалительная, десенсибилизирующая терапия).
Проводились перевязки с водным 0,01% раствором бензилдиметил-миристоиламино-пропиламмония в сочетании с борной кислотой в виде порошка, ежедневно. По мере отторжения и лизиса некротических тканей во время перевязок острым путем проводились этапные некрэктомии (рис. 1 б).
Пролежень очистился, появились сочные грануляции и краевая эпителизация. В это же время выполнено введение 6 мл 7% геля Коллост путем микроинъеций в края, дно раны, затем раневая поверхность полностью укрыта 4-мя мембранами Коллост 50х60 мм толщиной 1,5 мм, которые были подшиты отдельными узловыми швами к краям раны и сшиты между собой с целью формирования единого пласта для укрытия раны. После введения геля Коллост и укрытия раневой поверхности мембранами Коллост наложена влажная повязка с 0,01% водным раствором бензилдиметил-миристоиламино-пропиламмония, которая постоянно увлажнялась тем же раствором.
Первая перевязка проведена на 7-е сут (рис. 1 в). Отчетливо заметны активная биодеградация имплантированных мембран Коллост, быстрый рост грануляционной ткани от дна раны под мембранами Коллост, отмечаются элементы краевой эпителизации. Динамика заживления пролежня на 30, 48, 55, 90 и 112-е сут отражена на рисунках 1 г–ж.
На рисунке 1 з хорошо видно полное заживление пролежня IV степени на 112-е сут после включения в комплекс лечения биоматериала Коллост в виде геля и мембран.
Клиническое наблюдение № 2 (рис. 2)
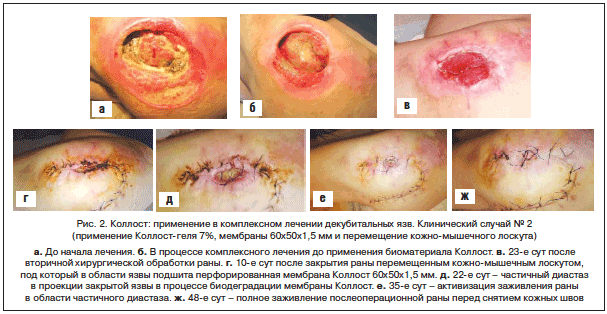
Пациент Б., 54 года, перенес тяжелую спинальную травму с полным перерывом спинного мозга в нижнегрудном отделе. В момент осмотра отмечался тяжелый неврологический дефицит: полная нижняя параплегия, нарушение функции тазовых органов. Диагностирован пролежень IV степени по классификации AHCPR в области большого вертела бедренной кости с контактным остеомиелитом. Длительность существования пролежня – около 1,5 года (рис. 2 а).
На первом этапе лечения (после первого визита врача совместно с участковым фельдшером на дом к пациенту и обучения родственников правилам ухода за раной, правильному выполнению перевязок на дому) назначено общее лечение (дезагреганты, нейропротекторы, антигипоксанты, витамины группы В, антибактериальная, противовоспалительная, десенсибилизирующая терапия).
Ежедневно проводились перевязки с 1% водным раствором повидон-йода, этапные некрэктомии во время перевязок участковым фельдшером под контролем врача с помощью видеосвязи по Интернету и выполнением этапных контрольных фотоснимков во время перевязок. Эти снимки отправлялись в режиме реального времени по электронной почте врачу, который контролировал процесс консервативного лечения пациента на дому, своевременно проводил коррекцию общего и местного лечения. На фоне проведенного на дому комплексного лечения пролежневая рана очистилась, сократилась в размерах, появились грануляции от дна раны и краевая эпителизация (рис. 2 б).
После очищения пролежневой раны, стихания острого воспалительного процесса, хорошего развития грануляционной ткани (этот этап лечения длился около 30 сут) пациент был госпитализирован в отделение гнойной хирургии ГБУ РО ОКБ, где выполнено первое оперативное вмешательство: радикальная некрэктомия пролежня с тангенциальной остеонекрэктомией участка большого вертела бедренной кости, пораженного контактным остеомиелитом. После тщательного гемостаза интраоперационно в края и дно раны проведены микроинъекции 7% геля Коллост в суммарном объеме 6,0 мл.
После операции продолжено общее и местное лечение. Рана значительно сократилась в размерах, полностью заполнилась грануляциями от дна, отмечалась активная краевая эпителизация (рис. 2 в).
Второе хирургическое вмешательство заключалось в выкраивании полнослойного кожно-мышечного лоскута с его перемещением для полного закрытия раны. Перед фиксацией перемещенного кожно-мышечного лоскута рана полностью укрыта мембраной Коллост 60х50 мм толщиной 1,5 мм, которая фиксирована отдельными узловыми швами (викрил, 3/0, атравматика). Таким образом, между поверхностью раны и подшиваемым кожно-мышечным лоскутом была проложена мембрана Коллост. На рисунке 2 г – вид раны после второй операции.
Пациент выписан на амбулаторное лечение на дому на 10–е сут после выполнения второй операции, со швами на операционной ране.
На дому продолжено общее лечение, перевязки со сменой асептической наклейки под контролем оперирующего врача через Интернет (видеосвязь по Skype, этапные фотоснимки послеоперационной раны) и участкового фельдшера, родственников пациента. Этапы заживления послеоперационной раны отражены на рисунках 2 д–е.
На рисунке 2 ж – вид полностью зажившей раны на 48-е сут перед полным снятием швов.
Опыт ведения данных пациентов позволил реализовать принятый и одобренный к широкому применению на конгрессе EWMA (Мадрид, 2015) принцип лечения больных с хроническими ранами, получивший название «Distance care – Home care» и позволяющий оказывать эффективную и результативную специализированную хирургическую помощь этой тяжелой группе больных с рациональной минимизацией материально-технических затрат за счет сокращения этапа стационарного лечения и затрат рабочего времени врачей и среднего медицинского персонала специализированного стационара [11].
Авторы приносят глубокую благодарность всем сотрудникам клиники, участвовавшим в лечении этой группы тяжелых больных