–Я—А–Є —Б–љ–Є–ґ–µ–љ–Є–Є –≤—Б–∞—Б—Л–≤–∞—О—Й–µ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ–Њ–і–≤–Ј–і–Њ—И–љ–Њ–є –Ї–Є—И–Ї–Є –Є–Ј––Ј–∞ –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Ї–Є—И–Ї–Є –Є–ї–Є –њ—А–Є –Њ–±—И–Є—А–љ—Л—Е —А–µ–Ј–µ–Ї—Ж–Є—П—Е –Ї–Є—И–Ї–Є —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В –Є –ґ–Є—А–Њ–≤ [2]. –£ —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤ –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї –љ–∞—А—Г—И–µ–љ–Є—О –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –≤–Є—В–∞–Љ–Є–љ–∞ B12 –Є –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В –Є–Ј––Ј–∞ —Б–љ–Є–ґ–µ–љ–Є—П –≤—Б–∞—Б—Л–≤–∞—О—Й–µ–є –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –Ї–Є—И–Ї–Є, –∞–љ–∞—Н—А–Њ–±–љ–∞—П –Љ–Є–Ї—А–Њ—Д–ї–Њ—А–∞ —В–Њ–ї—Б—В–Њ–є –Ї–Є—И–Ї–Є –≤—Б–ї–µ–і—Б—В–≤–Є–µ –Њ—В—Б—Г—В—Б—В–≤–Є—П –Є–ї–µ–Њ—Ж–µ–Ї–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞–њ–∞–љ–∞ –Љ–Њ–ґ–µ—В –њ–Њ–њ–∞–і–∞—В—М –≤ —В–Њ–љ–Ї—Г—О –Ї–Є—И–Ї—Г [1,2].
–Э–µ–Ї–Њ—В–Њ—А—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ –≤—А–µ–Љ–µ–љ–µ–Љ (–њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞) –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —З–∞—Б—В–Є—З–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –ґ–Є—А–Њ–≤, –∞–Ј–Њ—В–∞, –ґ–µ–ї—З–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –≤–Є—В–∞–Љ–Є–љ–∞ –Т12, –Ї–∞–ї—М—Ж–Є—П –Є —Г–≥–ї–µ–≤–Њ–і–Њ–≤ (–Њ—Б–Њ–±–µ–љ–љ–Њ –≥–ї—О–Ї–Њ–Ј—Л). –≠—В–Њ —Б—В–∞–љ–Њ–≤–Є—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –±–ї–∞–≥–Њ–і–∞—А—П —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н–љ—В–µ—А–Њ—Ж–Є—В–Њ–≤, —Г—З–∞—Б—В–≤—Г—О—Й–Є—Е –≤–Њ –≤—Б–∞—Б—Л–≤–∞–љ–Є–Є. –Ф–ї—П —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –∞–і–∞–њ—В–∞—Ж–Є–Њ–љ–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤ –Њ—Б—В–∞–≤—И–µ–є—Б—П —З–∞—Б—В–Є –Ї–Є—И–Ї–Є –њ—А–Є–Љ–µ–љ—П–ї–Њ—Б—М –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ —Б–њ–Њ—Б–Њ–±–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Њ—Б—В–∞–≤—И–Є–є—Б—П –Њ—В—А–µ–Ј–Њ–Ї –Ї–Є—И–Ї–Є —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ–Є—В–∞—В–µ–ї—М–љ—Л–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є, —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –≤—Л–і–µ–ї–µ–љ–Є—П –ґ–µ–ї—З–Є –Є —Б–Њ–Ї–∞ –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –≥–Њ—А–Љ–Њ–љ–Њ–≤, —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –Ї–Є—И–Ї–Є –њ–Њ–ї–Є–∞–Љ–Є–і–∞–Љ–Є, —Г–ї—Г—З—И–µ–љ–Є–µ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ –Њ—Б—В–∞–≤—И–µ–є—Б—П —З–∞—Б—В–Є –Ї–Є—И–Ї–Є [2–7]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –і–ї—П –ї–µ—З–µ–љ–Є—П «—Б–Є–љ–і—А–Њ–Љ–∞ –Ї–Њ—А–Њ—В–Ї–Њ–є –Ї–Є—И–Ї–Є» —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –ї–Є—И—М –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Ї–Є—И–Ї—Г –њ–Є—В–∞—В–µ–ї—М–љ—Л–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г —В–Њ–ї—М–Ї–Њ –Њ–љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б—В–Є–Љ—Г–ї–Є—А—Г—О—В –∞–і–∞–њ—В–∞—Ж–Є–Њ–љ–љ—Л–µ –њ—А–Њ—Ж–µ—Б—Б—Л [2]. –Я–Њ—Н—В–Њ–Љ—Г —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –љ–∞ –њ–Њ–ї–љ–Њ–Љ –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–Љ –њ–Є—В–∞–љ–Є–Є, –∞–і–∞–њ—В–∞—Ж–Є—П –Њ—Б—В–∞–≤—И–µ–є—Б—П —З–∞—Б—В–Є –Ї–Є—И–Ї–Є –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–∞, —Г –љ–Є—Е —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≥–Є–њ–Њ–њ–ї–∞–Ј–Є—П –Ї–Є—И–µ—З–љ–Њ–≥–Њ —Н–њ–Є—В–µ–ї–Є—П [2,4,5].
–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤–∞–ґ–љ–∞—П —А–Њ–ї—М –Њ—В–≤–Њ–і–Є—В—Б—П —Н–љ—В–µ—А–∞–ї—М–љ–Њ–Љ—Г –њ–Є—В–∞–љ–Є—О –≤ –Њ–±—Й–µ–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –Њ–±—И–Є—А–љ—Л–Љ–Є —А–µ–Ј–µ–Ї—Ж–Є—П–Љ–Є. –¶–µ–ї—М –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е – –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є–µ –і–µ—Д–Є—Ж–Є—В–∞ –≤–µ—Й–µ—Б—В–≤, –≤–Њ–Ј–љ–Є–Ї—И–µ–≥–Њ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –љ–∞—А—Г—И–µ–љ–Є—П –≤—Б–∞—Б—Л–≤–∞–љ–Є—П –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Э–Њ –і–∞–ґ–µ –њ—А–Є —Г—Б–ї–Њ–≤–Є–Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –љ–µ–њ—А–µ—А—Л–≤–љ–Њ—Б—В–Є –њ–Є—Й–µ–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Њ—Б—В–∞–µ—В—Б—П –њ—А–Њ–±–ї–µ–Љ–∞ –љ—Г—В—А–Є—В–Є–≤–љ–Њ–≥–Њ –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –≤ —Б–≤—П–Ј–Є —Б —Г—Б–Ї–Њ—А–µ–љ–Є–µ–Љ –Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–љ–Ј–Є—В–∞ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –≤—Б–∞—Б—Л–≤–∞–љ–Є—П.
–Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ –Є–Ј—Г—З–∞–µ–Љ—Л—Е –≤–Њ–њ—А–Њ—Б–Њ–≤ —П–≤–ї—П–µ—В—Б—П –≤–Њ–њ—А–Њ—Б —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –і–Є–µ—В—Л –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–±—И–Є—А–љ—Л–Љ–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞–Љ–Є [3–7]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –і–Є–µ—В—Л —Б –љ–Є–Ј–Ї–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ –ґ–Є—А–Њ–≤, –≤—Л—Б–Њ–Ї–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ —Г–≥–ї–µ–≤–Њ–і–Њ–≤ –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤ —Б–Њ —Б—А–µ–і–љ–µ–є –і–ї–Є–љ–Њ–є —Ж–µ–њ–Њ—З–Ї–Є –љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П [2]. –Ґ–∞–Ї–Є–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –і–ї—П –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П –±–∞–ї–∞–љ—Б–∞ –њ–Є—В–∞—В–µ–ї—М–љ—Л—Е –≤–µ—Й–µ—Б—В–≤ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Г–њ–Њ—В—А–µ–±–ї—П—В—М –њ–Є—Й—Г —Б —Н–љ–µ—А–≥–Њ–µ–Љ–Ї–Њ—Б—В—М—О, –њ—А–µ–≤—Л—И–∞—О—Й–µ–є –Њ—Б–љ–Њ–≤–љ–Њ–є —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є–є –Њ–±–Љ–µ–љ –≤ 2–3 —А–∞–Ј–∞.
–Э–∞ –љ–∞—З–∞–ї—М–љ—Л—Е —Н—В–∞–њ–∞—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –≠–Я —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–ї—Г—Н–ї–µ–Љ–µ–љ—В–љ—Л—Е —Б–Љ–µ—Б–µ–є (–і–µ—В—П–Љ —А–∞–љ–љ–µ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ – «–Р–ї—М—Д–∞—А–µ», —Б 1––≥–Њ –≥–Њ–і–∞ – «–Я–µ–њ—В–∞–Љ–µ–љ –Ѓ–љ–Є–Њ—А», —Б—В–∞—А—И–µ 3–—Е –ї–µ—В – «–Я–µ–њ—В–∞–Љ–µ–љ» (–Э–µ—Б—В–ї–µ, –®–≤–µ–є—Ж–∞—А–Є—П)), –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–ї—Г—З–µ–љ—Л –Љ–µ—В–Њ–і–Њ–Љ –≥–Є–і—А–Њ–ї–Є–Ј–∞ –њ–Є—Й–µ–≤—Л—Е –±–µ–ї–Ї–Њ–≤ –і–Њ –Њ–ї–Є–≥–Њ–њ–µ–њ—В–Є–і–Њ–≤ –Є –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–≤–Њ–±–Њ–і–љ—Л—Е –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В, —З—В–Њ —Г–ї—Г—З—И–∞–µ—В –Є—Е –њ—А–Є—Б—В–µ–љ–Њ—З–љ–Њ–µ –њ–Є—Й–µ–≤–∞—А–µ–љ–Є–µ –Є –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –≤ –Ї–Є—И–Ї–µ. –°–Љ–µ—Б–Є —Б–Њ–і–µ—А–ґ–∞—В —Б—А–µ–і–љ–µ—Ж–µ–њ–Њ—З–µ—З–љ—Л–µ —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і—Л, –≤—Б–∞—Б—Л–≤–∞–љ–Є–µ –Ї–Њ—В–Њ—А—Л—Е –љ–µ —В—А–µ–±—Г–µ—В –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–∞—В–Є–≤–љ—Л—Е —Г—Б–Є–ї–Є–є, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–є –њ–Њ–Ї–Њ–є –њ–µ—З–µ–љ–Є –Є –њ–Њ–і–ґ–µ–ї—Г–і–Њ—З–љ–Њ–є –ґ–µ–ї–µ–Ј–µ. –£–Ї–∞–Ј–∞–љ–љ—Л–µ —Б–Љ–µ—Б–Є —Б –њ–Њ–Љ–Њ—Й—М—О –њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ–Њ–≥–Њ –љ–∞—Б–Њ—Б–∞ –Є–ї–Є –Ї–∞–њ–µ–ї—М–љ–Є—Ж—Л –≤–≤–Њ–і—П—В —З–µ—А–µ–Ј –Є–љ—Д—Г–Ј–Є–Њ–љ–љ—Л–є –Ї–∞–љ–∞–ї –Ј–Њ–љ–і–∞ —Б–Њ —Б–Ї–Њ—А–Њ—Б—В—М—О 5–10 –Љ–ї/—З. –° –љ–∞—З–∞–ї–∞ –≤–љ—Г—В—А–Є–Ї–Є—И–µ—З–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –Њ–±—К–µ–Љ —А–∞—Б—В–≤–Њ—А–Њ–≤, –≤–≤–Њ–і–Є–Љ—Л—Е –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ, –≤–Ї–ї—О—З–∞—П –њ—А–µ–њ–∞—А–∞—В—Л –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П, —Г–Љ–µ–љ—М—И–∞–ї–Є –љ–∞ 50%, —Б –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–є –Њ—В–Љ–µ–љ–Њ–є –њ–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П –Ї 3–5––Љ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б—Г—В–Ї–∞–Љ. –Я–Њ—Н—В–∞–њ–љ–Њ –њ–µ—А–µ—Е–Њ–і—П—В –љ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –≠–Я –Ї 5–7––Љ—Г –і–љ—О, –њ—А–µ–Ї—А–∞—Й–∞—П –њ–Њ–ї–љ–Њ—Б—В—М—О –Я–Я. –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ, –њ–Њ—Б–ї–µ –њ–µ—А–µ–≤–Њ–і–∞ –≤ –Ї–Њ–µ—З–љ–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ –±–Њ–ї—М–љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ 7–14 –і–љ–µ–є –њ—А–Њ–і–Њ–ї–ґ–∞—О—В –њ—А–Є–µ–Љ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Б–Љ–µ—Б–µ–є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ –≤ –≤–Є–і–µ –љ–∞–њ–Є—В–Ї–∞ –Њ–±—К–µ–Љ–Њ–Љ –і–Њ 1000–1500 –Љ–ї/—Б—Г—В. –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –і–Є–µ—В–Є—З–µ—Б–Ї–Є–Љ –њ–Є—В–∞–љ–Є–µ–Љ.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –њ–µ—А–µ–і —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є –ї–µ—З–µ–±–љ—Л–Љ–Є –і–Є–µ—В–∞–Љ–Є –њ–Њ–ї—Г—З–Є–ї–Є —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л –њ–Є—В–∞–љ–Є—П, –і–Њ—Б—В–Њ–Є–љ—Б—В–≤–∞ –Ї–Њ—В–Њ—А—Л—Е –≤—Л—А–∞–ґ–∞—О—В—Б—П –≤ –њ–Њ–ї–љ–Њ–Љ —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ–Њ–Љ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –њ–Њ—В—А–µ–±–љ–Њ—Б—В—П–Љ–Є –і–µ—В–µ–є, –љ–∞–ї–Є—З–Є–µ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –Є –≤–∞–ґ–љ—Л—Е –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –Є –Љ–Є–Ї—А–Њ—Н–ї–µ–Љ–µ–љ—В–Њ–≤, –љ–∞–ї–Є—З–Є–µ–Љ –≤—Л—Б–Њ–Ї–Њ–Ї–∞—З–µ—Б—В–≤–µ–љ–љ—Л—Е –±–µ–ї–Ї–Њ–≤ –ґ–Є—А–љ—Л—Е –Ї–Є—Б–ї–Њ—В, –∞ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≥–ї—О—В–µ–љ–∞ –Є –ї–∞–Ї—В–Њ–Ј—Л –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –њ—А–Њ–і—Г–Ї—В—Л –њ—А–Є –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞.
–Э–∞ –±–∞–Ј–µ –Њ—В–і–µ–ї–µ–љ–Є—П —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–љ–Є–Љ–∞—Ж–Є–Є –Ф–Ъ–У–С вДЦ 9 –Є–Љ. –У.–Э. –°–њ–µ—А–∞–љ—Б–Ї–Њ–≥–Њ –±—Л–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–∞ –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Б–Љ–µ—Б–µ–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ–Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є —А–∞—Ж–Є–Њ–љ–∞–Љ–Є. –° —Н—В–Њ–є —Ж–µ–ї—М—О —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ–њ–µ—А–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–Њ –њ–Њ–≤–Њ–і—Г –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Ц–Ъ–Ґ, —Б–Њ 2–3–—Е –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ—Л—Е —Б—Г—В–Њ–Ї, –њ–Њ –Љ–µ—А–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –≤—Б–∞—Б—Л–≤–∞—В–µ–ї—М–љ–Њ–є –Є –њ–µ—А–µ–≤–∞—А–Є–≤–∞—О—Й–µ–є —Д—Г–љ–Ї—Ж–Є–є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –љ–∞—З–Є–љ–∞–ї–Њ—Б—М –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –≠–Я –≤ –Њ–±—К–µ–Љ–µ 50% –Њ—В —Б—Г—В–Њ—З–љ–Њ–є —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є. –° —Н—В–Њ–≥–Њ –Љ–Њ–Љ–µ–љ—В–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Є–і–∞ –њ–Є—В–∞–љ–Є—П –≤—Б–µ –і–µ—В–Є –≥—А—Г–њ–њ –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ –і–≤–µ –њ–Њ–і–≥—А—Г–њ–њ—Л.
–Я–µ—А–≤—Г—О –њ–Њ–і–≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є –і–µ—В–Є, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –ї–µ—З–µ–±–љ—Л–Љ–Є —Б–Љ–µ—Б—П–Љ–Є.
–Т—В–Њ—А—Г—О –њ–Њ–і–≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ —В–Њ–ї—М–Ї–Њ –љ–∞—В—Г—А–∞–ї—М–љ—Л–µ –њ—А–Њ–і—Г–Ї—В—Л – —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–є —А–∞—Ж–Є–Њ–љ. –Я—А–Є–Љ–µ—А–љ—Л–є —Б–Њ—Б—В–∞–≤ —Б—Г—В–Њ—З–љ—Л—Е —А–∞—Ж–Є–Њ–љ–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –≤ —В–∞–±–ї–Є—Ж–µ 1.
–°—В–µ–њ–µ–љ—М —А–∞–Ј–≤–µ–і–µ–љ–Є—П —Б–Љ–µ—Б–µ–є –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ј–∞–≤–Є—Б–µ–ї–Є –Њ—В –Њ–±—Й–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П —А–µ–±–µ–љ–Ї–∞, —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞, –Њ–±—К–µ–Љ–∞ –Њ–њ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –≤–Љ–µ—И–∞—В–µ–ї—М—Б—В–≤–∞, —Б—А–Њ–Ї–Њ–≤ –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞.
–Т –њ–µ—А–≤—Л–µ –і–љ–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —Б–Љ–µ—Б–µ–є –љ–µ –њ—А–µ–≤—Л—И–∞–ї–∞ 20%, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—П —Н–љ–µ—А–≥–Њ—Ж–µ–љ–љ–Њ—Б—В—М —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П 800–1000 –Ї–Ї–∞–ї. –Т –і–∞–ї—М–љ–µ–є—И–µ–Љ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Є –Ї–∞–ї–Њ—А–Є–є–љ–Њ—Б—В—М —Б—Г—В–Њ—З–љ–Њ–≥–Њ —А–∞—Ж–Є–Њ–љ–∞ –≤–Њ–Ј—А–∞—Б—В–∞–ї–Є –і–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є (—В–∞–±–ї.1).
–Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–∞–≤–ї—П–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 5 –і–љ–µ–є, –њ–Њ—Б–ї–µ —З–µ–≥–Њ –±–Њ–ї—М–љ—Л–µ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ –њ–µ—А–µ–≤–Њ–і–Є–ї–Є—Б—М –љ–∞ –ї–µ—З–µ–±–љ—Г—О –і–Є–µ—В—Г –Є–Ј –љ–∞—В—Г—А–∞–ї—М–љ—Л—Е –њ—А–Њ–і—Г–Ї—В–Њ–≤.
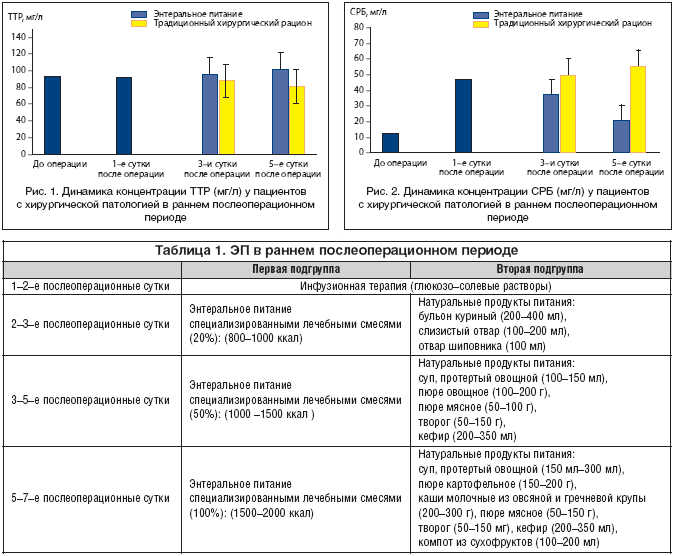
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Н–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б–Љ–µ—Б–µ–є, –Ї 5––Љ —Б—Г—В–Ї–∞–Љ –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ–Њ–≤—Л—И–∞–ї–∞—Б—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —В—А–∞–љ—Б—В–Є—А–µ—В–Є–љ–∞ –Є –∞–ї—М–±—Г–Љ–Є–љ–∞ (—А<0,001), —З—В–Њ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–ї–Њ—Б—М, –Ї–∞–Ї –њ—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–є –Ј–љ–∞–Ї (—А–Є—Б. 1).
–Ъ–∞–Ї –≤–Є–і–љ–Њ –Є–Ј –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л—Е —А–Є—Б—Г–љ–Ї–Њ–≤, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —В—А–∞–і–Є—Ж–Є–Њ–љ–љ—Л–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–є —А–∞—Ж–Є–Њ–љ, –Њ—В–Љ–µ—З–µ–љ–∞ –њ—А—П–Љ–Њ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞: –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —В—А–∞–љ—Б—В–Є—А–µ—В–Є–љ–∞ –Є –∞–ї—М–±—Г–Љ–Є–љ–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–∞—Б—М –≤ 1,2 —А–∞–Ј–∞ (—А<0,001) (—А–Є—Б. 1).
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–і–≥—А—Г–њ–њ—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е —Б—В–∞–љ–і–∞—А—В–љ—Л–є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–є —А–∞—Ж–Є–Њ–љ, –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ –і–∞–ї—М–љ–µ–є—И–µ–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Њ—Б—В—А–Њ—Д–∞–Ј–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞, –≤—Л—А–∞–ґ–∞–≤—И–µ–≥–Њ—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ (—А<0,001) –љ–∞—А–∞—Б—В–∞–љ–Є–µ–Љ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є –°–†–С (—А–Є—Б. 2).
–Э–∞–Ј–љ–∞—З–µ–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П —Н—В–Є–Љ –±–Њ–ї—М–љ—Л–Љ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –њ—А–Є–Њ—Б—В–∞–љ–Њ–≤–Є—В—М –і–∞–ї—М–љ–µ–є—И–µ–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –≥–Є–њ–µ—А–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Є –Ї–∞—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є —А–µ–∞–Ї—Ж–Є–є, –Њ —З–µ–Љ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В —А–µ–≥—А–µ—Б—Б–Є—П –Њ—Б—В—А–Њ—Д–∞–Ј–љ—Л—Е –±–µ–ї–Ї–Њ–≤ (–°–†–С, α1––∞–љ—В–Є—В—А–Є–њ—Б–Є–љ–∞, –Њ—А–Њ–Ј–Њ–Љ—Г–Ї–Њ–Є–і–∞), –∞ —В–∞–Ї–ґ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–є —В—А–∞–љ—Б—В–Є—А–µ—В–Є–љ–∞ –Є –∞–ї—М–±—Г–Љ–Є–љ–∞.
–Ф–µ—В–Є, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –њ–Є—В–∞–љ–Є–µ –ї–µ—З–µ–±–љ—Л–Љ–Є —Б–Љ–µ—Б—П–Љ–Є, –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 4 –і–љ—П —А–∞–љ—М—И–µ –њ–µ—А–µ–≤–Њ–і–Є–ї–Є—Б—М –≤ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –Њ—В–і–µ–ї–µ–љ–Є–µ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ —Н–љ—В–µ—А–∞–ї—М–љ–Њ–≥–Њ –њ–Є—В–∞–љ–Є—П —Б –њ–Њ–Љ–Њ—Й—М—О —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б–Љ–µ—Б–µ–є –≤ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г—Б—В—А–∞–љ–Є—В—М –љ–∞—А—Г—И–µ–љ–Є—П –љ—Г—В—А–Є—В–Є–≤–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞, –Њ–±–µ—Б–њ–µ—З–Є—В—М –±–µ—Б—И–ї–∞–Ї–Њ–≤—Г—О –і–Є–µ—В—Г, –њ–Њ—П–≤–ї–µ–љ–Є–µ –≤ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є–µ —Б—А–Њ–Ї–Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—Г–ї–∞, —З—В–Њ –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ –њ—А–Є–≤–Њ–і–Є—В –Ї –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–Љ—Г —В–µ—З–µ–љ–Є—О –њ–Њ—Б–ї–µ–Њ–њ–µ—А–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –Є —Г–ї—Г—З—И–µ–љ–Є—О —Б–Њ—Б—В–Њ—П–љ–Є—П —А–µ–±–µ–љ–Ї–∞ —Б —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –С–∞—А–∞–љ–Њ–≤—Б–Ї–Є–є –Р.–Ѓ., –®–∞–њ–Є—А–Њ –Ш.–ѓ.. –Ш—Б–Ї—Г—Б—Б—В–≤–µ–љ–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –±–Њ–ї—М–љ—Л—Е. //–°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥, –2000 –≥. –154 —Б.
2. –С–Њ—А–Њ–≤–Є–Ї –Ґ.–≠. –≠–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –і–µ—В–µ–є —Б —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –Ї–Є—И–µ—З–љ–Є–Ї–∞. // –Я–µ–і–Є–∞—В—А–Є—П.–2000. –вДЦ3. –—Б.66–68.
3. Chwals W.J., Lally K.P., Woolley M.M. et all. Measured energy expenditure in critically ill infants and young children. // J.Surg.Res.–1988.–V.44. – –†. 467–472.
4. Colomb V., Goulet O., Ricour C. Home enteral and parenteral nutrition in children. //. J. Clin.Gastroent. –1998. –V.12. – –†. 897–894.
5. Mullen F.L., Dooden M., Frank P. Implications of malnutrition in surgical patients .// Arch. Surg.– 1995.–V.130, вДЦ 2.– p. 148–156.
6. Kudsk K. Early Enteral Nutrition in surgical patients. // Selected Abstracts From the 3rd Congress of the Parenteral and Enteral Nutrition Society of Asia (PENSA), October 29–31,1997, Bangkok, Thailand. Nutr. – 1999. – V.15. –P.V.
7. Lipman T.O. Grains or Veins: Is Enteral Nutrition Really Better Than Parenteral Nutrition? A look at the Evidence. // JPEN. – 1998. – V.22. – вДЦ 3. – P.167–182.












