Введение
За последние годы отмечается значительный рост хирургических вмешательств, проводимых амбулаторно. Болевой синдром – один из важнейших факторов, влияющих на раннюю реабилитацию таких пациентов [1]. Это наиболее часто встречающийся симптом в современной клинической практике. Согласно International Association for the Study of Pain определение боли звучит следующим образом: «неприятное ощущение и эмоциональное переживание, сочетанное с имеющимся или возможным повреждением ткани или же описываемое больным в терминах такого повреждения» [2].Проблема лечения послеоперационного болевого синдрома в амбулаторной хирургии остается актуальной как в России, так и за рубежом. По данным исследований конца прошлого века, от 30 до 70% пациентов страдали от выраженного болевого синдрома после перенесенного оперативного вмешательства [3].
В XXI в. ситуация улучшилась, однако результаты послеоперационного обезболивания все еще не вполне удовлетворительны. По данным одного из наиболее крупных исследований, болевой синдром средней интенсивности после перенесенного хирургического вмешательства выявляется в 26,4–33% случаев, высокой – в 8,4–13,4% случаев [4].
Масштабное эпидемиологическое исследование PATHOS, проведенное в Европе и включавшее данные 746 клиник, выявило низкое качество послеоперационного обезболивания у пациентов [5].
Болевой синдром усиливает нагрузку практически на все жизненно важные системы организма. Со стороны сердечно-сосудистой системы чаще всего отмечаются тахикардия, аритмия, артериальная гипертензия. Со стороны дыхательной системы – снижение дыхательного объема и жизненной емкости легких, что, в свою очередь, приводит к нарушению дренажа мокроты, пневмонии, гипоксемии и формированию ателектазов. Также встречаются нарушения свертывания крови, а именно тромбозы глубоких вен нижних конечностей, тромбоэмболия легочной артерии, гиперкоагуляция. Нагрузка на центральную нервную систему (ЦНС) характеризуется эмоциональным возбуждением с последующим развитием депрессивного состояния, а также формированием хронического послеоперационного болевого синдрома [6].
В 30–40% случаев у выписанных амбулаторных пациентов послеоперационный болевой синдром сохраняется в течение 24–48 часов. Интенсивность болевого синдрома со временем уменьшается, однако затрудняет раннюю реабилитацию пациента и снижает качество жизни [7, 8].
Сохранение болевого синдрома у пациента, находящегося дома, как правило, влечет дополнительные расходы и со стороны самого больного, и со стороны здравоохранения. Пациент позже возвращается к привычному образу жизни и работе. Выраженная боль после перенесенного амбулаторного хирургического вмешательства является также одной из главных причин задержки выписки из стационара, повторного обращения пациента после выписки с возможной незапланированной госпитализацией, что, в свою очередь, повышает расходы на лечение [9].
В амбулаторной практике послеоперационное обезболивание должно быть не только эффективным, но и максимально безопасным и простым для пациента. Все пациенты при выписке должны быть информированы о различных вариантах лечения боли. Необходимо предоставлять информацию не только в письменном виде, но и давать четкие устные инструкции [10].
Наиболее простым способом достижения адекватного обезболивания для пациентов после выписки из стационара является прием таблетированных форм препаратов. Безопасными и с адекватным анальгетическим эффектом являются нестероидные противовоспалительные препараты (НПВП), обладающие, помимо обезболивающего, противовоспалительным и жаропонижающим эффектами. Болеутоляющий эффект НПВП связан с центральным (нарушение проведения болевых импульсов на уровне таламуса) и периферическим (блокирование взаимодействия брадикинина с периферическими ноцицепторами) влиянием. Противовоспалительный эффект ненаркотических анальгетиков реализуется за счет ингибирования синтеза простагландинов и циклооксигеназ, что приводит к снижению проницаемости капилляров и экссудации. Блокирование пирогенного влияния простагландинов на нейроны центра терморегуляции и теплопродукции гипоталамуса и торможение синтеза эндогенных пирогенов обусловливает жаропонижающее действие НПВП [11]. Высокой эффективностью при болевом синдроме различной этиологии и интенсивности, воспалении, лихорадке объясняется широкое применение и популярность НПВП в мире [12].
Частота и выраженность основных побочных эффектов НПВП напрямую зависят от селективности действия на изоферменты циклооксигеназы (ЦОГ) – ЦОГ-1 и ЦОГ-2 [13]. Изофермент ЦОГ-1 является физиологическим ферментом, постоянно присутствующим во многих тканях и обеспечивающим физиологические процессы в организме. Синтез ЦОГ-1 сравнительно мало (в 2–4 раза) увеличивается при воспалении. ЦОГ-2 в здоровом организме содержится в очень малых количествах, его уровень существенно (в 10–80 раз) увеличивается при воспалении, в связи с чем ее считают патологическим ферментом [14]. С ингибированием ЦОГ-1 и ослаблением физиологической роли простагландинов связаны побочные эффекты НПВП, особенно со стороны ЖКТ. Для минимизации указанных нежелательных явлений были разработаны селективные ингибиторы ЦОГ-2, не менее эффективные, чем «стандартные» НПВП, но с менее опасными побочными эффектами.
К преимущественно селективным ингибиторам ЦОГ-2 относятся сульфонанилиды и оксикамы. Нимесулид (Найз®) – единственный представитель класса сульфонанилидов среди НПВП, активность которого в отношении ЦОГ-2 в 5–50 раз превосходит его активность в отношении ЦОГ-1 [15]. В исследованиях in vivo при применении нимесулида в терапевтической дозе (100 мг 2 р./сут) было продемонстрировано значительное снижение концентрации простагландина E2 в плазме крови. Оценка индуцированной активности ЦОГ-1 показала, что нимесулид не оказывает влияния на агрегацию тромбоцитов. Также препарат не оказывает влияния на образование в желудке простагландина E2 и простагландина I2, которое также зависит от ЦОГ-1 [16]. Все это обусловливает высокую клиническую эффективность препарата при ряде состояний [17–21], а также его хороший профиль безопасности [22–28].
C целью сравнения эффективности применения таблетированных форм нимесулида и лорноксикама для обезболивания амбулаторных пациентов в раннем послеоперационном периоде нами было проведено настоящее исследование.
Материал и методы
В рандомизированном проспективном исследовании, продолжавшемся в течение 2016 г., приняли участие пациенты, которым были выполнены малотравматичные оперативные вмешательства: алло- и аутогерниопластика пупочной и паховой грыж малых размеров, иссечение доброкачественных новообразований кожи и подкожной клетчатки, вскрытие и дренирование гнойных полостей малых размеров, косметические операции на коже в условиях поликлиники и дневного стационара кафедры госпитальной хирургии СамГМУ.От каждого пациента было получено информированное согласие на участие в исследовании, которое проводилось в соответствии с утвержденным протоколом, этическими принципами Хельсинкской декларации Всемирной медицинской ассоциации (Сеул, 2008), трехсторонним Соглашением по надлежащей клинической практике (ICH GCP) и действующим законодательством РФ.
Критерии исключения: возраст пациентов меньше 25 лет и старше 65 лет; гастропатии; сопутствующие онкологические заболевания; гормонотерапия и химиотерапия в анамнезе; отягощенный преморбидный фон (патологии сердца, легких, печени, почек, органическая патология ЦНС); наркомания; токсикомания; иммунодепрессивные состояния, в т. ч. ВИЧ-инфекция; наличие декомпенсированного сахарного диабета в анамнезе; септические состояния; пациенты с аллергическими реакциями на НПВП; беременные.
Всего было включено 92 пациента: 52 (56,5%) женщины, и 40 (43,5%) мужчин.
Все пациенты были разделены на 2 группы методом случайной выборки:
в I группу (n=46) были включены пациенты с четными номерами историй болезни, которым в послеоперационном периоде был назначен нимесулид (Найз®) в таблетках по 100 мг 2 р./ день;
во II группу (n=46) были включены пациенты с нечетными номерами историй болезни, которым в послеоперационном периоде был назначен лорноксикам в таблетках по 8 мг 2 р./ день.
Препараты пациенты получали через 2 часа после проведенной операции и далее в течение пяти дней.
Средний возраст пациентов I группы составил 34,5±5,6 года, II группы – 37,2±6,2 года (t=0,3231, р>0,05). В I группе было 29 (63%) женщин и 17 (37%) мужчин, во II группе – 27 (58,7%) женщин и 19 (41,3%) мужчин. Статистически значимых различий между группами пациентов по полу не выявлено (t=0,38; р>0,05).
Все пациенты были обследованы на догоспитальном этапе, что позволило исключить патологии, относящиеся к критериям исключения. Всем пациентам выполнялось запланированное оперативное вмешательство в день поступления. В послеоперационном периоде для купирования болевого синдрома и с целью снижения воспалительной реакции назначались таблетированные формы НПВП соответствующей группы.
Для оценки эффективности купирования болевого синдрома в послеоперационном периоде использовалась визуальная аналоговая шкала (ВАШ) боли (VAS, Huskisson E.C., 1974). Больные отмечали точку на горизонтальной шкале длиной 100 мм, где 0 означал отсутствие боли, а 100 – крайне сильную боль. Пациенты отмечали уровень боли по шкале 3 раза в день в течение 5 сут после проведенного оперативного вмешательства, после чего высчитывали среднее значение шкалы за каждые сутки.
Значимость различий количественных данных оценивали с использованием t-критерия Стьюдента. Критическое значение уровня значимости принималось равным 5% (р≤0,05).
Результаты и обсуждение
В послеоперационном периоде уровень болевых ощущений по ВАШ у пациентов I группы составил 65±5 мм, у пациентов II группы – 63±3 мм (p>0,05). После начала приема НПВП в первые сутки уровень болевых ощущений по ВАШ у пациентов I группы снизился до 38±5 мм, у пациентов II группы – до 55±6 мм (p<0,05); на вторые сутки – до 33±3 мм и 51±4,5 мм (p<0,05) соответственно; на третьи сутки – до 18±3 мм и 28±3,5 мм (p<0,05), на четвертые сутки – до 14±3,5 мм и 20±3,5 мм, на пятые – до 10±2,5 мм и 17±2,5 мм соответственно. На четвертые и пятые сутки наблюдения статистически значимых различий не получено (рис. 1).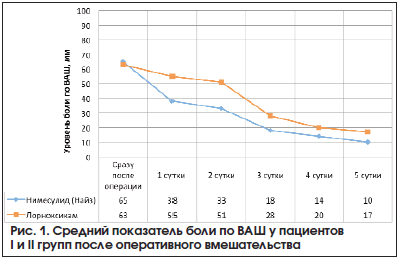
Результаты исследования демонстрируют, что прием нимесулида в дозе 100 мг 2 р./день оказывает более выраженный анальгетический эффект в первые трое суток после проведенной операции по сравнению с лорноксикамом в дозе 8 мг 2 р./день. Интенсивность боли была достоверно ниже у пациентов I группы в сравнении с пациентами II группы в покое и при движении (р=0,02).
На наш взгляд, препарат нимесулид (Найз®) обладает хорошей анальгетической активностью у пациентов с выраженными и умеренными болями в послеоперационном периоде.








.gif)



