–ü–Β―Ä–Β–¥–Α―΅–Α –Η–Ϋ―³–Β–Κ―Ü–Η–Η –Ω―Ä–Η –û–†–£–‰ –Ψ―¹―É―â–Β―¹―²–≤–Μ―è–Β―²―¹―è –≤–Ψ–Ζ–¥―É―à–Ϋ–Ψ––Κ–Α–Ω–Β–Μ―¨–Ϋ―΄–Φ –Ω―É―²–Β–Φ. –ü―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Η–Ϋ–Κ―É–±–Α―Ü–Η–Ψ–Ϋ–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Η–Ψ–¥–Α ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² –Ψ―² 2 –¥–Ψ 5 ―¹―É―². (–≤ ―¹―Ä–Β–¥–Ϋ–Β–Φ 2–3). –£ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –Η–Ϋ―³–Η―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –≤ –Κ–Μ–Β―²–Κ–Α―Ö ―ç–Ω–Η―²–Β–Μ–Η―è ―Ä–Β―¹–Ω–Η―Ä–Α―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Κ―²–Α –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥–Η―² –Α–Κ―²–Η–≤–Ϋ–Ψ–Β ―Ä–Α–Ζ–Φ–Ϋ–Ψ–Ε–Β–Ϋ–Η–Β –≤–Ψ–Ζ–±―É–¥–Η―²–Β–Μ–Β–Ι ―¹ ―Ä–Α–Ζ–≤–Η―²–Η–Β–Φ –Ψ―¹―²―Ä–Ψ–≥–Ψ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è. –ü–Β―Ä–≤–Η―΅–Ϋ–Α―è –≤–Η―Ä―É―¹–Ϋ–Α―è ―Ä–Β–Ω–Μ–Η–Κ–Α―Ü–Η―è –Ζ–Α–Κ–Α–Ϋ―΅–Η–≤–Α–Β―²―¹―è –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η–Β–Φ –Η–Ζ –Η–Ϋ―³–Η―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Κ–Μ–Β―²–Ψ–Κ –¥–Ψ―΅–Β―Ä–Ϋ–Η―Ö –≤–Η―Ä–Η–Ψ–Ϋ–Ψ–≤, ―΅―²–Ψ ―¹–Ψ–Ω―Ä–Ψ–≤–Ψ–Ε–¥–Α–Β―²―¹―è –≤–Η―Ä―É―¹–Β–Φ–Η–Β–Ι. –£–Η―Ä―É―¹–Β–Φ–Η―è, –Κ–Α–Κ –Ω―Ä–Α–≤–Η–Μ–Ψ, –Ϋ–Ψ―¹–Η―² –Κ―Ä–Α―²–Κ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ―΄–Ι ―Ö–Α―Ä–Α–Κ―²–Β―Ä –Η –Ϋ–Β –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –≥–Β–Ϋ–Β―Ä–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Ω―Ä–Ψ―Ü–Β―¹―¹–Α, –Ϋ–Ψ –Ω―Ä–Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ―΄―Ö ―É―¹–Μ–Ψ–≤–Η―è―Ö (–Ϋ–Α–Ω―Ä–Η–Φ–Β―Ä, –Η–Φ–Φ―É–Ϋ–Ψ–¥–Β―³–Η―Ü–Η―²–Β) –Φ–Ψ–Ε–Β―² ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤–Ψ–≤–Α―²―¨ ―²―è–Ε–Β–Μ–Ψ–Φ―É ―²–Β―΅–Β–Ϋ–Η―é –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è –Η ―Ä–Α–Ζ–≤–Η―²–Η―é –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η–Ι [1].
–ö–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Α―è –Κ–Α―Ä―²–Η–Ϋ–Α –û–†–£–‰ ―¹–Κ–Μ–Α–¥―΄–≤–Α–Β―²―¹―è –Η–Ζ –Ψ–±―â–Η―Ö –Η –Φ–Β―¹―²–Ϋ―΄―Ö ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤. –ü―Ä–Η ―ç―²–Ψ–Φ –Μ–Η―Ö–Ψ―Ä–Α–¥–Κ–Α, –Ψ–Ζ–Ϋ–Ψ–±, ―É―Ö―É–¥―à–Β–Ϋ–Η–Β –Α–Ω–Ω–Β―²–Η―²–Α, –Ϋ–Β–¥–Ψ–Φ–Ψ–≥–Α–Ϋ–Η–Β –Η –¥―Ä―É–≥–Η–Β –Ψ–±―â–Η–Β –Ω―Ä–Ψ―è–≤–Μ–Β–Ϋ–Η―è –û–†–£–‰ –≤–Ψ–Ζ–Ϋ–Η–Κ–Α―é―² –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ –Η–Ζ––Ζ–Α –Κ―Ä–Α―²–Κ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ–Ι –≤–Η―Ä―É―¹–Β–Φ–Η–Η, –Ϋ–Ψ –Η –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β ―¹–Η―¹―²–Β–Φ–Ϋ–Ψ–≥–Ψ –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α –Ψ―Ä–≥–Α–Ϋ–Η–Ζ–Φ –Ω―Ä–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄―Ö –Φ–Β–¥–Η–Α―²–Ψ―Ä–Ψ–≤. –€–Β―¹―²–Ϋ―΄–Β ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ –û–†–£–‰ –Ψ―²―Ä–Α–Ε–Α―é―² –Ω―Ä–Ψ―Ü–Β―¹―¹―΄ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è ―¹–Μ–Η–Ζ–Η―¹―²―΄―Ö –Ψ–±–Ψ–Μ–Ψ―΅–Β–Κ ―Ä–Β―¹–Ω–Η―Ä–Α―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Κ―²–Α, ―΅―²–Ψ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η –Ω―Ä–Ψ―è–≤–Μ―è–Β―²―¹―è ―É –¥–Β―²–Β–Ι ―΅–Η―Ö–Α–Ϋ–Η–Β–Φ, –Ζ–Α―²―Ä―É–¥–Ϋ–Β–Ϋ–Ϋ―΄–Φ –Ϋ–Ψ―¹–Ψ–≤―΄–Φ –¥―΄―Ö–Α–Ϋ–Η–Β–Φ, –±–Ψ–Μ―¨―é –≤ –≥–Ψ―Ä–Μ–Β, –Ϋ–Α―¹–Φ–Ψ―Ä–Κ–Ψ–Φ –Η –Κ–Α―à–Μ–Β–Φ [4,8,13].
–û–¥–Ϋ–Η–Φ –Η–Ζ ―΅–Α―¹―²―΄―Ö –Η –Ϋ–Α–Η–±–Ψ–Μ–Β–Β –Φ―É―΅–Η―²–Β–Μ―¨–Ϋ―΄―Ö ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –û–†–£–‰ ―è–≤–Μ―è–Β―²―¹―è –Κ–Α―à–Β–Μ―¨, –Ω―Ä–Β–¥―¹―²–Α–≤–Μ―è―é―â–Η–Ι ―¹–Ψ–±–Ψ–Ι –Ζ–Α―â–Η―²–Ϋ―΄–Ι ―Ä–Β―³–Μ–Β–Κ―¹, –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ―΄–Ι –Ϋ–Α ―¹–Α–Ϋ–Α―Ü–Η―é –¥―΄―Ö–Α―²–Β–Μ―¨–Ϋ―΄―Ö –Ω―É―²–Β–Ι. –ö–Α―à–Β–Μ―¨ – –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―²–Ψ―Ä–Ϋ―΄–Ι –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ, ―Ä–Α–Ζ–≤–Η–≤–Α―é―â–Η–Ι―¹―è –Ω―Ä–Η –Ϋ–Β―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ–Ψ–≥–Ψ –Κ–Μ–Η―Ä–Β–Ϋ―¹–Α. –ü―Ä–Η –≥–Η–Ω–Β―Ä―¹–Β–Κ―Ä–Β―Ü–Η–Η –Κ–Α―à–Β–Μ―¨ –Φ–Ψ–Ε–Β―² –¥–Α–≤–Α―²―¨ –Ψ―΅–Η―â–Β–Ϋ–Η–Β –±–Ψ–Μ–Β–Β ―΅–Β–Φ –Ϋ–Α 50%, –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Η―Ä―É―è ―ç―²–Η–Φ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ―΄–Β –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Ϋ―¹–Ω–Ψ―Ä―²–Α. –ê–Κ―²–Η–≤–Α―Ü–Η―è –Κ–Α―à–Μ–Β–≤–Ψ–≥–Ψ ―Ä–Β―³–Μ–Β–Κ―¹–Α ―¹–≤―è–Ζ–Α–Ϋ–Α ―¹ ―Ä–Α–Ζ–¥―Ä–Α–Ε–Β–Ϋ–Η–Β–Φ –Ψ–Κ–Ψ–Ϋ―΅–Α–Ϋ–Η–Ι ―è–Ζ―΄–Κ–Ψ–≥–Μ–Ψ―²–Ψ―΅–Ϋ–Ψ–≥–Ψ, –±–Μ―É–Ε–¥–Α―é―â–Β–≥–Ψ –Η ―²―Ä–Ψ–Ι–Ϋ–Η―΅–Ϋ–Ψ–≥–Ψ –Ϋ–Β―Ä–≤–Ψ–≤, ―Ä–Α―¹–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Ϋ―΄―Ö –≤ –Ϋ–Ψ―¹–Ψ–≤–Ψ–Ι –Ω–Ψ–Μ–Ψ―¹―²–Η –Η –Ψ–Κ–Ψ–Μ–Ψ–Ϋ–Ψ―¹–Ψ–≤―΄―Ö –Ω–Α–Ζ―É―Ö–Α―Ö, –Ϋ–Α―Ä―É–Ε–Ϋ–Ψ–Φ ―¹–Μ―É―Ö–Ψ–≤–Ψ–Φ –Ω―Ä–Ψ―Ö–Ψ–¥–Β, –Ϋ–Α –Ζ–Α–¥–Ϋ–Β–Ι ―¹―²–Β–Ϋ–Κ–Β –≥–Μ–Ψ―²–Κ–Η, –≤ ―²―Ä–Α―Ö–Β–Β, –±―Ä–Ψ–Ϋ―Ö–Α―Ö, –Ω–Μ–Β–≤―Ä–Β, –¥–Η–Α―³―Ä–Α–≥–Φ–Β –Η –¥―Ä. –ê―³―³–Β―Ä–Β–Ϋ―²–Ϋ–Α―è –Η–Φ–Ω―É–Μ―¨―¹–Α―Ü–Η―è –¥–Ψ―¹―²–Η–≥–Α–Β―² –Κ–Α―à–Μ–Β–≤–Ψ–≥–Ψ ―Ü–Β–Ϋ―²―Ä–Α, ―Ä–Α―¹–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Ϋ–Ψ–≥–Ψ –≤ –Ω―Ä–Ψ–¥–Ψ–Μ–≥–Ψ–≤–Α―²–Ψ–Φ –Φ–Ψ–Ζ–≥–Β. –£ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –Α–Κ―²–Η–≤–Α―Ü–Η–Η –Κ–Α―à–Μ–Β–≤–Ψ–≥–Ψ ―Ü–Β–Ϋ―²―Ä–Α ―³–Ψ―Ä–Φ–Η―Ä―É–Β―²―¹―è ―ç―³―³–Β―Ä–Β–Ϋ―²–Ϋ―΄–Ι –Η–Φ–Ω―É–Μ―¨―¹, –Κ–Ψ―²–Ψ―Ä―΄–Ι –Ω―Ä–Ψ–≤–Ψ–¥–Η―²―¹―è –Κ –Φ―΄―à―Ü–Α–Φ –≥―Ä―É–¥–Ϋ–Ψ–Ι –Κ–Μ–Β―²–Κ–Η, –¥–Η–Α―³―Ä–Α–≥–Φ―΄ –Η –±―Ä―é―à–Ϋ–Ψ–≥–Ψ –Ω―Ä–Β―¹―¹–Α –Ω–Ψ –≤–Ψ–Μ–Ψ–Κ–Ϋ–Α–Φ –±–Μ―É–Ε–¥–Α―é―â–Β–≥–Ψ, –¥–Η–Α―³―Ä–Α–≥–Φ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Η ―¹–Ω–Η–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –Ϋ–Β―Ä–≤–Ψ–≤. –£–Ψ–Ζ–Ϋ–Η–Κ–Α–Β―² –Η–Ϋ―²–Β–Ϋ―¹–Η–≤–Ϋ–Ψ–Β –Κ―Ä–Α―²–Κ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ–Β –Η ―¹–Ψ–¥―Ä―É–Ε–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Β ―¹–Ψ–Κ―Ä–Α―â–Β–Ϋ–Η–Β ―É–Κ–Α–Ζ–Α–Ϋ–Ϋ–Ψ–Ι –Φ―É―¹–Κ―É–Μ–Α―²―É―Ä―΄, ―΅―²–Ψ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η –Ω―Ä–Ψ―è–≤–Μ―è–Β―²―¹―è ―Ä–Α–Ζ–≤–Η―²–Η–Β–Φ –Κ–Α―à–Μ―è.
–†–Α–Ζ–≤–Η–≤–Α―é―â–Β–Β―¹―è –Ω―Ä–Η –û–†–£–‰ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η–Β ―¹–Μ–Η–Ζ–Η―¹―²―΄―Ö ―Ä–Β―¹–Ω–Η―Ä–Α―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Κ―²–Α –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―é –Φ–Β―Ä―Ü–Α―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―é ―¹–Μ–Η–Ζ–Β–Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―è, –Α ―²–Α–Κ–Ε–Β –Κ –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―é –Κ–Α―΅–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ–≥–Ψ ―¹–Ψ―¹―²–Α–≤–Α ―¹–Μ–Η–Ζ–Η. –Γ ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β–Φ –≤―è–Ζ–Κ–Ψ―¹―²–Η ―¹–Μ–Η–Ζ–Η, –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥―è―â–Η–Φ –≤–Ψ –≤―²–Ψ―Ä–Ψ–Ι ―³–Α–Ζ–Β –≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―Ü–Β―¹―¹–Α, ―É–Φ–Β–Ϋ―¨―à–Α–Β―²―¹―è ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Ψ―΅–Η―â–Β–Ϋ–Η―è –Φ–Β―Ä―Ü–Α―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é –Κ–Α―à–Μ―è. –ü―Ä–Η ―ç―²–Ψ–Φ –Ϋ–Α―΅–Α–Μ―¨–Ϋ–Ψ–Β ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β –≤―è–Ζ–Κ–Ψ―¹―²–Η ―¹–Μ–Η–Ζ–Η ―¹―²–Η–Φ―É–Μ–Η―Ä―É–Β―² –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ―΄–Ι –Κ–Μ–Η―Ä–Β–Ϋ―¹, –Ψ–¥–Ϋ–Α–Κ–Ψ –Ζ–Α―²–Β–Φ –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―²–Ψ―Ä–Ϋ―΄–Β –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Η –Ψ―Ä–≥–Α–Ϋ–Η–Ζ–Φ–Α –Η―¹―΅–Β―Ä–Ω―΄–≤–Α―é―²―¹―è –Η ―É–Ε–Β –Ϋ–Η –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ―΄–Ι –Κ–Μ–Η―Ä–Β–Ϋ―¹, –Ϋ–Η –Κ–Α―à–Β–Μ―¨ –Ϋ–Β ―¹–Ω–Ψ―¹–Ψ–±–Ϋ―΄ –Α–¥–Β–Κ–≤–Α―²–Ϋ–Ψ ―ç–Μ–Η–Φ–Η–Ϋ–Η―Ä–Ψ–≤–Α―²―¨ –Η–Ζ–±―΄―²–Ψ–Κ –Ψ–±―Ä–Α–Ζ―É―é―â–Β–≥–Ψ―¹―è –≥―É―¹―²–Ψ–≥–Ψ –Η –≤―è–Ζ–Κ–Ψ–≥–Ψ ―¹–Β–Κ―Ä–Β―²–Α [1,5,7].
–‰–Φ–Β–Ϋ–Ϋ–Ψ –Ω–Ψ―ç―²–Ψ–Φ―É –Α―Ä―¹–Β–Ϋ–Α–Μ –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤ –Ψ―² –Κ–Α―à–Μ―è –≤–Κ–Μ―é―΅–Α–Β―² –Κ–Α–Κ –Ω―Ä–Ψ―²–Η–≤–Ψ–Κ–Α―à–Μ–Β–≤―΄–Β ―¹―Ä–Β–¥―¹―²–≤–Α (―É–≥–Ϋ–Β―²–Α―é―â–Η–Β –Κ–Α―à–Μ–Β–≤–Ψ–Ι ―Ä–Β―³–Μ–Β–Κ―¹), ―²–Α–Κ –Η –Ψ―²―Ö–Α―Ä–Κ–Η–≤–Α―é―â–Η–Β (–Ω–Ψ–¥–¥–Β―Ä–Ε–Η–≤–Α―é―â–Η–Β –Κ–Α―à–Μ–Β–≤–Ψ–Ι ―Ä–Β―³–Μ–Β–Κ―¹ –Η ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É―é―â–Η–Β –Ψ―΅–Η―â–Β–Ϋ–Η―é –¥―΄―Ö–Α―²–Β–Μ―¨–Ϋ―΄―Ö –Ω―É―²–Β–Ι). –ö―Ä–Ψ–Φ–Β ―²–Ψ–≥–Ψ, –≤–Α–Ε–Ϋ–Ψ–Β –Φ–Β―¹―²–Ψ –≤ ―²–Β―Ä–Α–Ω–Η–Η –Κ–Α―à–Μ―è –Ψ―²–≤–Ψ–¥–Η―²―¹―è –Φ―É–Κ–Ψ–Α–Κ―²–Η–≤–Ϋ―΄–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α–Φ, –Ζ–Α–¥–Α―΅–Α–Φ–Η –Κ–Ψ―²–Ψ―Ä―΄―Ö –≤ ―ç―²–Ψ–Φ ―¹–Μ―É―΅–Α–Β ―è–≤–Μ―è―é―²―¹―è [6,9]:
• ―¹―²–Η–Φ―É–Μ―è―Ü–Η―è –≤―΄–≤–Β–¥–Β–Ϋ–Η―è ―¹–Μ–Η–Ζ–Η,
• ―Ä–Α–Ζ–Ε–Η–Ε–Β–Ϋ–Η–Β ―¹–Μ–Η–Ζ–Η,
• ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β –Β–Β –≤–Ϋ―É―²―Ä–Η–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α–Ϋ–Η―è,
• ―Ä–Β–≥–Η–¥―Ä–Α―²–Α―Ü–Η―è.
–£―΄–±–Ψ―Ä –Κ–Ψ–Ϋ–Κ―Ä–Β―²–Ϋ―΄―Ö –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤ –Ψ―² –Κ–Α―à–Μ―è –Ω―Ä–Η –Μ–Β―΅–Β–Ϋ–Η–Η –û–†–£–‰ –Ω―Ä–Ψ–≤–Ψ–¥–Η―²―¹―è –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Β –¥–Β―²–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Η–Ζ–Α –Β–≥–Ψ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ―¹―²–Β–Ι. –ü―Ä–Η ―ç―²–Ψ–Φ –Ψ―Ü–Β–Ϋ–Η–≤–Α―é―² –Β–≥–Ψ ―΅–Α―¹―²–Ψ―²―É, –Η–Ϋ―²–Β–Ϋ―¹–Η–≤–Ϋ–Ψ―¹―²―¨, –±–Ψ–Μ–Β–Ζ–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨, –Ϋ–Α–Μ–Η―΅–Η–Β –Φ–Ψ–Κ―Ä–Ψ―²―΄ –Η –Β–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä. –£ ―²–Β―Ö ―¹–Μ―É―΅–Α―è―Ö, –Κ–Ψ–≥–¥–Α –Κ–Α―à–Β–Μ―¨ ―Ä–Β–¥–Κ–Η–Ι, –Α ―¹–Κ―É–¥–Ϋ–Α―è –Φ–Ψ–Κ―Ä–Ψ―²–Α –Ϋ–Β –Ψ―²–Μ–Η―΅–Α–Β―²―¹―è –≤―΄―¹–Ψ–Κ–Ψ–Ι –≤―è–Ζ–Κ–Ψ―¹―²―¨―é, –Φ–Ψ–≥―É―² –±―΄―²―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ―΄ –Ψ―²―Ö–Α―Ä–Κ–Η–≤–Α―é―â–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄. –ù–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β –Ω―Ä–Ψ―²–Η–≤–Ψ–Κ–Α―à–Μ–Β–≤―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Ω―Ä–Η –û–†–£–‰ –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ ―¹ –Ω–Β―Ä–≤―΄―Ö –¥–Ϋ–Β–Ι –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, –Κ–Ψ–≥–¥–Α –Ψ―²–Φ–Β―΅–Α–Β―²―¹―è ―¹―É―Ö–Ψ–Ι, –Ϋ–Α–≤―è–Ζ―΅–Η–≤―΄–Ι, ―΅–Α―¹―²―΄–Ι –Κ–Α―à–Β–Μ―¨ [1,2].
–ü―Ä–Η –Κ–Α―à–Μ–Β ―¹ –≥―É―¹―²–Ψ–Ι, –≤―è–Ζ–Κ–Ψ–Ι, ―²―Ä―É–¥–Ϋ–Ψ–Ψ―²–¥–Β–Μ―è–Β–Φ–Ψ–Ι –Φ–Ψ–Κ―Ä–Ψ―²–Ψ–Ι, ―΅―²–Ψ ―΅–Α―¹―²–Ψ –Ϋ–Α–±–Μ―é–¥–Α–Β―²―¹―è –≤–Ψ –≤―²–Ψ―Ä―É―é ―³–Α–Ζ―É –≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―Ü–Β―¹―¹–Α –Ω―Ä–Η –û–†–£–‰, –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β –Ψ–¥–Ϋ–Ψ–≥–Ψ –Η–Ζ –Φ―É–Κ–Ψ–Α–Κ―²–Η–≤–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, ―¹―Ä–Β–¥–Η –Κ–Ψ―²–Ψ―Ä―΄―Ö –≤―΄–¥–Β–Μ―è―é―² ―¹―Ä–Β–¥―¹―²–≤–Α ―¹ –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ –Φ―É–Κ–Ψ–Μ–Η―²–Η―΅–Β―¹–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨―é, ―¹–Β–Κ―Ä–Β―²–Ψ–Μ–Η―²–Η–Κ–Η –Η ―¹–Β–Κ―Ä–Β―²–Ψ–Φ–Η–Φ–Β―²–Η–Κ–Η [1,2].
–Γ–Μ–Β–¥―É–Β―² –Ψ―²–Φ–Β―²–Η―²―¨, ―΅―²–Ψ –Φ–Ϋ–Ψ–≥–Η–Β –Η–Ζ ―¹–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ―΄―Ö –Φ―É–Κ–Ψ–Α–Κ―²–Η–≤–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Η–Φ–Β―é―² –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Ψ ―²–Ψ―΅–Β–Κ –Ω―Ä–Η–Μ–Ψ–Ε–Β–Ϋ–Η―è. –£ ―΅–Α―¹―²–Ϋ–Ψ―¹―²–Η, –Φ―É–Κ–Ψ–Μ–Η―²–Η–Κ –Ϋ–Β–Ω―Ä―è–Φ–Ψ–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è –Κ–Α―Ä–±–Ψ―Ü–Η―¹―²–Β–Η–Ϋ–Α –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Ψ–±–Μ–Α–¥–Α–Β―² –Ψ–¥–Ϋ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ –Φ―É–Κ–Ψ―Ä–Β–≥―É–Μ–Η―Ä―É―é―â–Η–Φ –Η –Φ―É–Κ–Ψ–Μ–Η―²–Η―΅–Β―¹–Κ–Η–Φ –Ψ―²―Ö–Α―Ä–Κ–Η–≤–Α―é―â–Η–Φ ―ç―³―³–Β–Κ―²–Α–Φ–Η. –€–Β―Ö–Α–Ϋ–Η–Ζ–Φ –Β–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è ―¹–≤―è–Ζ–Α–Ϋ ―¹ –Α–Κ―²–Η–≤–Α―Ü–Η–Β–Ι ―¹–Η–Α–Μ–Ψ–≤–Ψ–Ι ―²―Ä–Α–Ϋ―¹―³–Β―Ä–Α–Ζ―΄ – ―³–Β―Ä–Φ–Β–Ϋ―²–Α –±–Ψ–Κ–Α–Μ–Ψ–≤–Η–¥–Ϋ―΄―Ö –Κ–Μ–Β―²–Ψ–Κ ―¹–Μ–Η–Ζ–Η―¹―²–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η –±―Ä–Ψ–Ϋ―Ö–Ψ–≤. –ö–Α―Ä–±–Ψ―Ü–Η―¹―²–Β–Η–Ϋ–Α –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Ϋ–Ψ―Ä–Φ–Α–Μ–Η–Ζ―É–Β―² –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Β ―¹–Ψ–Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Β –Κ–Η―¹–Μ―΄―Ö –Η –Ϋ–Β–Ι―²―Ä–Α–Μ―¨–Ϋ―΄―Ö ―¹–Η–Α–Μ–Ψ–Φ―É―Ü–Η–Ϋ–Ψ–≤ –±―Ä–Ψ–Ϋ―Ö–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―¹–Β–Κ―Ä–Β―²–Α (―É–Φ–Β–Ϋ―¨―à–Α–Β―² –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –Ϋ–Β–Ι―²―Ä–Α–Μ―¨–Ϋ―΄―Ö –≥–Μ–Η–Κ–Ψ–Ω–Β–Ω―²–Η–¥–Ψ–≤ –Η ―É–≤–Β–Μ–Η―΅–Η–≤–Α–Β―² –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –≥–Η–¥―Ä–Ψ–Κ―¹–Η―¹–Η–Α–Μ–Ψ–≥–Μ–Η–Κ–Ψ–Ω–Β–Ω―²–Η–¥–Ψ–≤), ―΅―²–Ψ –≤–Ψ―¹―¹―²–Α–Ϋ–Α–≤–Μ–Η–≤–Α–Β―² –≤―è–Ζ–Κ–Ψ―¹―²―¨ –Η ―ç–Μ–Α―¹―²–Η―΅–Ϋ–Ψ―¹―²―¨ ―¹–Μ–Η–Ζ–Η. –ü–Ψ–¥ –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η–Β–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥―è―² ―Ä–Β–≥–Β–Ϋ–Β―Ä–Α―Ü–Η―è ―¹–Μ–Η–Ζ–Η―¹―²–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Η, –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η–Β –Β–Β ―¹―²―Ä―É–Κ―²―É―Ä―΄, ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β (–Ϋ–Ψ―Ä–Φ–Α–Μ–Η–Ζ–Α―Ü–Η―è) –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α –±–Ψ–Κ–Α–Μ–Ψ–≤–Η–¥–Ϋ―΄―Ö –Κ–Μ–Β―²–Ψ–Κ, –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ –≤ ―²–Β―Ä–Φ–Η–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –±―Ä–Ψ–Ϋ―Ö–Η–Ψ–Μ–Α―Ö, –Α –Ζ–Ϋ–Α―΅–Η―², –Η ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α –≤―΄―Ä–Α–±–Α―²―΄–≤–Α–Β–Φ–Ψ–Ι ―¹–Μ–Η–Ζ–Η.
–ü–Ψ–Φ–Η–Φ–Ψ ―ç―²–Ψ–≥–Ψ, –≤–Ψ―¹―¹―²–Α–Ϋ–Α–≤–Μ–Η–≤–Α―é―²―¹―è ―¹–Β–Κ―Ä–Β―Ü–Η―è –Η–Φ–Φ―É–Ϋ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η –Α–Κ―²–Η–≤–Ϋ–Ψ–≥–Ψ IgA (―¹–Ω–Β―Ü–Η―³–Η―΅–Β―¹–Κ–Α―è –Ζ–Α―â–Η―²–Α) –Η ―΅–Η―¹–Μ–Ψ ―¹―É–Μ―¨―³–≥–Η–¥―Ä–Η–Μ―¨–Ϋ―΄―Ö –≥―Ä―É–Ω–Ω (–Ϋ–Β―¹–Ω–Β―Ü–Η―³–Η―΅–Β―¹–Κ–Α―è –Ζ–Α―â–Η―²–Α); ―É–Μ―É―΅―à–Α–Β―²―¹―è –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ―΄–Ι –Κ–Μ–Η―Ä–Β–Ϋ―¹ (–Ω–Ψ―²–Β–Ϋ―Ü–Η―Ä―É–Β―²―¹―è –¥–Β―è―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ ―Ä–Β―¹–Ϋ–Η―²―΅–Α―²―΄―Ö –Κ–Μ–Β―²–Ψ–Κ). –ö–Α―Ä–±–Ψ―Ü–Η―¹―²–Β–Η–Ϋ–Α –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Ψ–¥–Η–Ϋ–Α–Κ–Ψ–≤–Ψ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Α –≤–Ψ –≤―¹–Β―Ö –Ψ–±–Μ–Α―¹―²―è―Ö –¥―΄―Ö–Α―²–Β–Μ―¨–Ϋ―΄―Ö –Ω―É―²–Β–Ι –Η ―¹―Ä–Β–¥–Ϋ–Β–≥–Ψ ―É―Ö–Α, –Η–Φ–Β―é―â–Η―Ö ―¹―Ö–Ψ–¥–Ϋ–Ψ–Β ―¹―²―Ä–Ψ–Β–Ϋ–Η–Β ―ç–Ω–Η―²–Β–Μ–Η―è –Η ―Ä–Β―¹–Ϋ–Η―²―΅–Α―²―΄–Β –Κ–Μ–Β―²–Κ–Η [10,15].
–û–¥–Ϋ–Η–Φ –Η–Ζ –Η–Ζ–≤–Β―¹―²–Ϋ―΄―Ö –Η ―Ö–Ψ―Ä–Ψ―à–Ψ –Ζ–Α―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥–Ψ–≤–Α–Ϋ–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Β –Κ–Α―Ä–±–Ψ―Ü–Η―¹―²–Β–Η–Ϋ–Α –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Ψ–Ι ―¹–Ψ–Μ–Η ―è–≤–Μ―è–Β―²―¹―è –Λ–Μ―É–Η―³–Ψ―Ä―², –Κ–Ψ―²–Ψ―Ä―΄–Ι –≤―΄–Ω―É―¹–Κ–Α–Β―²―¹―è –≤ –≤–Η–¥–Β –≥―Ä–Α–Ϋ―É–Μ –¥–Μ―è –Ω―Ä–Η–≥–Ψ―²–Ψ–≤–Μ–Β–Ϋ–Η―è ―¹―É―¹–Ω–Β–Ϋ–Ζ–Η–Η –¥–Μ―è –Ω―Ä–Η–Β–Φ–Α –≤–Ϋ―É―²―Ä―¨ –Η ―¹–Η―Ä–Ψ–Ω–Α. –Γ–Ψ–Β–¥–Η–Ϋ–Β–Ϋ–Η–Β –Κ–Α―Ä–±–Ψ―Ü–Η―¹―²–Β–Η–Ϋ–Α ―¹ –Μ–Η–Ζ–Η–Ϋ–Ψ–Φ ―É–≤–Β–Μ–Η―΅–Η–≤–Α–Β―² –≤–Ψ–¥–Ψ―Ä–Α―¹―²–≤–Ψ―Ä–Η–Φ–Ψ―¹―²―¨ –Η –Ψ–±–Β―¹–Ω–Β―΅–Η–≤–Α–Β―² –±―΄―¹―²―Ä–Ψ–Β –Η –Ω–Ψ–Μ–Ϋ–Ψ–Β –≤―¹–Α―¹―΄–≤–Α–Ϋ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α, ―²–Α–Κ–Ε–Β ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É–Β―² –Ϋ–Β–Ι―²―Ä–Α–Μ–Η–Ζ–Α―Ü–Η–Η –Β–≥–Ψ –Κ–Η―¹–Μ–Ψ―²–Ϋ–Ψ―¹―²–Η (―¹ ―Ä–ù=3 –¥–Ψ 6,8), ―΅―²–Ψ ―¹―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ ―¹–Ψ–Κ―Ä–Α―â–Α–Β―² ―Ä–Η―¹–Κ –≤–Ψ–Ζ–Ϋ–Η–Κ–Ϋ–Ψ–≤–Β–Ϋ–Η―è –Ω–Ψ–±–Ψ―΅–Ϋ―΄―Ö ―ç―³―³–Β–Κ―²–Ψ–≤ ―¹–Ψ ―¹―²–Ψ―Ä–Ψ–Ϋ―΄ –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ––Κ–Η―à–Β―΅–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Κ―²–Α (–•–ö–Δ). –‰–Φ–Β–Ϋ–Ϋ–Ψ ―ç―²–Η–Φ –Ψ–±―¹―²–Ψ―è―²–Β–Μ―¨―¹―²–≤–Ψ–Φ –Ψ–±―É―¹–Μ–Ψ–≤–Μ–Β–Ϋ–Α –Ψ―²–Μ–Η―΅–Ϋ–Α―è –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²―¨ –Λ–Μ―É–Η―³–Ψ―Ä―²–Α.
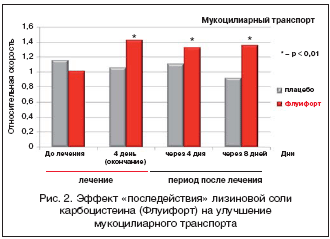
–ö–Α―Ä–±–Ψ―Ü–Η―¹―²–Β–Η–Ϋ–Α –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Ψ–±–Μ–Α–¥–Α–Β―² ―²–Α–Κ –Ϋ–Α–Ζ―΄–≤–Α–Β–Φ―΄–Φ ―ç―³―³–Β–Κ―²–Ψ–Φ «–Ω–Ψ―¹–Μ–Β–¥–Β–Ι―¹―²–≤–Η―è», ―΅―²–Ψ –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α–Β―² –Ϋ–Ψ―Ä–Φ–Α–Μ–Η–Ζ–Α―Ü–Η―è –≤―è–Ζ–Κ–Ψ―¹―²–Η –Η ―ç–Μ–Α―¹―²–Η―΅–Ϋ–Ψ―¹―²–Η ―¹–Β–Κ―Ä–Β―²–Α –Η –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Ϋ―¹–Ω–Ψ―Ä―²–Α –≤ ―²–Β―΅–Β–Ϋ–Η–Β 8–12 ―¹―É―². –Ω–Ψ―¹–Μ–Β –Ψ–Κ–Ψ–Ϋ―΅–Α–Ϋ–Η―è 4–―¹―É―². –Κ―É―Ä―¹–Α –Μ–Β―΅–Β–Ϋ–Η―è –Λ–Μ―É–Η―³–Ψ―Ä―²–Ψ–Φ (―Ä–Η―¹. 1 –Η 2) [16].
–†–Α–Ζ–¥―Ä–Α–Ε–Β–Ϋ–Η–Β –Κ–Α―à–Μ–Β–≤―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Ω―Ä–Η –û–†–£–‰ –≤–Ψ–Ζ–Ϋ–Η–Κ–Α–Β―² –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ –Η–Ζ––Ζ–Α –Η–Ζ–±―΄―²–Ψ―΅–Ϋ–Ψ–≥–Ψ –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Α –≤―è–Ζ–Κ–Ψ–≥–Ψ ―¹–Μ–Η–Ζ–Η―¹―²–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ―è–Β–Φ–Ψ–≥–Ψ, –Ϋ–Ψ –Η –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω―Ä–Ψ―Ü–Β―¹―¹–Α –≤ ―¹–Μ–Η–Ζ–Η―¹―²–Ψ–Ι –Ψ–±–Ψ–Μ–Ψ―΅–Κ–Β ―Ä–Β―¹–Ω–Η―Ä–Α―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ ―ç–Ω–Η―²–Β–Μ–Η―è, ―è–≤–Μ―è―é―â–Β–≥–Ψ―¹―è ―¹–Μ–Β–¥―¹―²–≤–Η–Β–Φ –Κ–Α–Κ –Ω―Ä―è–Φ–Ψ–≥–Ψ –Ω–Ψ–≤―Ä–Β–Ε–¥–Α―é―â–Β–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è –≤–Η―Ä―É―¹–Ψ–≤ –Ϋ–Α –Κ–Μ–Β―²–Κ–Η, ―²–Α–Κ –Η –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α ―¹–Ψ–Β–¥–Η–Ϋ–Η―²–Β–Μ―¨–Ϋ―É―é ―²–Κ–Α–Ϋ―¨, –Φ–Η–Κ―Ä–Ψ―¹–Ψ―¹―É–¥―΄ –Η –Κ―Ä–Ψ–≤―¨ –≤―΄―¹–≤–Ψ–±–Ψ–¥–Η–≤―à–Η―Ö―¹―è –≤–Ϋ–Β–Κ–Μ–Β―²–Ψ―΅–Ϋ–Ψ –Μ–Η–Ζ–Ψ―¹–Ψ–Φ–Α–Μ―¨–Ϋ―΄―Ö ―³–Β―Ä–Φ–Β–Ϋ―²–Ψ–≤ –Η –Α–Κ―²–Η–≤–Ϋ―΄―Ö –Φ–Β―²–Α–±–Ψ–Μ–Η―²–Ψ–≤ –Κ–Η―¹–Μ–Ψ―Ä–Ψ–¥–Α [14]. –£ ―ç―²–Ψ–Ι ―¹–≤―è–Ζ–Η –Ω―Ä–Β–¥―¹―²–Α–≤–Μ―è–Β―²―¹―è –Α–Κ―²―É–Α–Μ―¨–Ϋ―΄–Φ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β –≤ –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –Κ–Α―à–Μ―è –Η –¥―Ä―É–≥–Η―Ö ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –û–†–£–‰ –Ϋ–Β―¹―²–Β―Ä–Ψ–Η–¥–Ϋ―΄―Ö –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ (–ù–ü–£–ü). –Θ―΅–Η―²―΄–≤–Α―è –Η–Ζ–≤–Β―¹―²–Ϋ―΄–Β –Ϋ–Β–¥–Ψ―¹―²–Α―²–Κ–Η ―¹–Η―¹―²–Β–Φ–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –¥–Α–Ϋ–Ϋ–Ψ–Ι –≥―Ä―É–Ω–Ω―΄, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄–Β ―¹ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²―¨―é –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –•–ö–Δ –Η –Ω–Ψ―΅–Β–Κ, –Ϋ–Α–Μ–Η―΅–Η–Β –≤ –Α―Ä―¹–Β–Ϋ–Α–Μ–Β –Ω―Ä–Α–Κ―²–Η–Κ―É―é―â–Β–≥–Ψ –≤―Ä–Α―΅–Α –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ ―¹ –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ―΄–Φ –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Φ –¥–Β–Ι―¹―²–≤–Η–Β–Φ –Η –Ψ–¥–Ϋ–Ψ–≤―Ä–Β–Φ–Β–Ϋ–Ϋ–Ψ ―¹ –≤―΄―¹–Ψ–Κ–Η–Φ –Ω―Ä–Ψ―³–Η–Μ–Β–Φ –±–Β–Ζ–Ψ–Ω–Α―¹–Ϋ–Ψ―¹―²–Η ―¹―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ –Ψ–±–Μ–Β–≥―΅–Α–Β―² –Ω–Ψ–¥–±–Ψ―Ä –Ω–Β―Ä―¹–Ψ–Ϋ–Η―³–Η―Ü–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Ι ―¹―Ö–Β–Φ―΄ –Μ–Β―΅–Β–Ϋ–Η―è –Κ–Α―à–Μ―è –Η –¥―Ä―É–≥–Η―Ö ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è –Ω―Ä–Η –û–†–£–‰.
–û–¥–Ϋ–Η–Φ –Η–Ζ ―²–Α–Κ–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ ―è–≤–Μ―è–Β―²―¹―è –≥―Ä–Α–Ϋ―É–Μ―è―² –û–ö–‰ (–Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Α), –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è –Κ–Ψ―²–Ψ―Ä–Ψ–≥–Ψ ―¹–≤―è–Ζ–Α–Ϋ ―¹ –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Β–Φ ―¹–Η–Ϋ―²–Β–Ζ–Α –Ω―Ä–Ψ―¹―²–Α–Ϋ–Ψ–Η–¥–Ψ–≤ (–Ψ―¹–Ϋ–Ψ–≤–Ϋ―΄―Ö –Φ–Β–¥–Η–Α―²–Ψ―Ä–Ψ–≤ –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è) –Η–Ζ –Α―Ä–Α―Ö–Η–¥–Ψ–Ϋ–Ψ–≤–Ψ–Ι –Κ–Η―¹–Μ–Ψ―²―΄ –Ω―É―²–Β–Φ –±–Μ–Ψ–Κ–Α–¥―΄ ―Ü–Η–Κ–Μ–Ψ–Ψ–Κ―¹–Η–≥–Β–Ϋ–Α–Ζ―΄ I –Η II ―²–Η–Ω–Α. –ö―Ä–Ψ–Φ–Β ―²–Ψ–≥–Ψ, –Ω―Ä–Β–Ω–Α―Ä–Α―² –Ω–Ψ–¥–Α–≤–Μ―è–Β―² –≤―΄―Ä–Α–±–Ψ―²–Κ―É –Μ–Β–Ι–Κ–Ψ―²―Ä–Η–Β–Ϋ–Ψ–≤, –Ψ–±–Μ–Α–¥–Α―é―â–Η―Ö ―Ö–Β–Φ–Ψ―²–Α–Κ―¹–Η―΅–Β―¹–Κ–Η–Φ –¥–Β–Ι―¹―²–≤–Η–Β–Φ, –Ω―Ä–Ψ―è–≤–Μ―è–Β―² –Α–Ϋ―²–Η–±―Ä–Α–¥–Η–Κ–Η–Ϋ–Η–Ϋ–Ψ–≤―É―é –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨, ―¹―²–Α–±–Η–Μ–Η–Ζ–Η―Ä―É–Β―² –Μ–Η–Ζ–Ψ―¹–Ψ–Φ–Α–Μ―¨–Ϋ―΄–Β –Φ–Β–Φ–±―Ä–Α–Ϋ―΄, ―¹–Ϋ–Η–Ε–Α–Β―² –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ ―Ü–Η―²–Ψ–Κ–Η–Ϋ–Ψ–≤ –Η –Ϋ–Β–Ι―²―Ä–Ψ―³–Η–Μ–Ψ–≤, –Η–≥―Ä–Α―é―â–Η―Ö ―Ä–Β―à–Α―é―â―É―é ―Ä–Ψ–Μ―¨ –≤ –≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–Φ –Ω–Ψ–≤―Ä–Β–Ε–¥–Β–Ϋ–Η–Η ―²–Κ–Α–Ϋ–Β–Ι.
–ü–Ψ–Φ–Η–Φ–Ψ –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è –Ω―Ä–Β–Ω–Α―Ä–Α―² –Ψ―²–Μ–Η―΅–Α–Β―²―¹―è –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ―΄–Φ –Ψ–±–Β–Ζ–±–Ψ–Μ–Η–≤–Α―é―â–Η–Φ ―ç―³―³–Β–Κ―²–Ψ–Φ –Ζ–Α ―¹―΅–Β―² –Ω―Ä―è–Φ–Ψ–≥–Ψ –Η –Ϋ–Β–Ω―Ä―è–Φ–Ψ–≥–Ψ –≤–Μ–Η―è–Ϋ–Η―è –Ϋ–Α –±–Ψ–Μ–Β–≤―΄–Β ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Ϋ–Α ―É―Ä–Ψ–≤–Ϋ–Β ―¹–Η–Ϋ–Α–Ω―¹–Ψ–≤ –Η –≤ –Π–ù–Γ [11,12]. –¦–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Α –Ψ–±–Μ–Α–¥–Α–Β―² –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Ψ―¹–Ω–Α–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Φ, –Ψ–±–Β–Ζ–±–Ψ–Μ–Η–≤–Α―é―â–Η–Φ –Η –Ε–Α―Ä–Ψ–Ω–Ψ–Ϋ–Η–Ε–Α―é―â–Η–Φ ―¹–≤–Ψ–Ι―¹―²–≤–Α–Φ–Η, –±―΄―¹―²―Ä―΄–Φ –Ϋ–Α―΅–Α–Μ–Ψ–Φ –¥–Β–Ι―¹―²–≤–Η―è (―É–Ε–Β ―΅–Β―Ä–Β–Ζ 15–20 –Φ–Η–Ϋ.), –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –¥–Β–Ι―¹―²–≤–Η―è –¥–Ψ 8 ―΅ –Η ―Ö–Ψ―Ä–Ψ―à–Β–Ι –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²―¨―é. –ë―΄―¹―²―Ä–Ψ–Β –Ϋ–Α―΅–Α–Μ–Ψ –¥–Β–Ι―¹―²–≤–Η―è –Ψ–±―ä―è―¹–Ϋ―è–Β―²―¹―è –±–Ψ–Μ–Β–Β –≤―΄―¹–Ψ–Κ–Ψ–Ι ―Ä–Α―¹―²–≤–Ψ―Ä–Η–Φ–Ψ―¹―²―¨―é –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Ψ–Ι ―¹–Ψ–Μ–Η –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Α –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Ϋ–Β–Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Ϋ―΄–Φ –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Ψ–Φ. –£―΄―¹–Ψ–Κ–Α―è ―Ä–Α―¹―²–≤–Ψ―Ä–Η–Φ–Ψ―¹―²―¨ ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É–Β―² –±–Ψ–Μ–Β–Β –±―΄―¹―²―Ä–Ψ–Φ―É –Η –Ω–Ψ–Μ–Ϋ–Ψ–Φ―É –≤―¹–Α―¹―΄–≤–Α–Ϋ–Η―é –¥–Β–Ι―¹―²–≤―É―é―â–Β–≥–Ψ –≤–Β―â–Β―¹―²–≤–Α, ―΅―²–Ψ –Ω―Ä–Η–≤–Ψ–¥–Η―² –Κ –¥–Ψ―¹―²–Η–Ε–Β–Ϋ–Η―é –Ω–Η–Κ–Α –Κ–Ψ–Ϋ―Ü–Β–Ϋ―²―Ä–Α―Ü–Η–Η –≤ –Ω–Μ–Α–Ζ–Φ–Β –Κ―Ä–Ψ–≤–Η –Ω―Ä–Η –Ω–Β―Ä–Ψ―Ä–Α–Μ―¨–Ϋ–Ψ–Φ –Ω―Ä–Η–Β–Φ–Β ―É–Ε–Β ―΅–Β―Ä–Β–Ζ 15 –Φ–Η–Ϋ. (―Ä–Η―¹. 3), ―²–Ψ–≥–¥–Α –Κ–Α–Κ –Ψ–±―΄―΅–Ϋ―΄–Ι –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ –¥–Ψ―¹―²–Η–≥–Α–Β―² –Φ–Α–Κ―¹–Η–Φ―É–Φ–Α ―΅–Β―Ä–Β–Ζ 60 –Φ–Η–Ϋ. –Ω–Ψ―¹–Μ–Β –Ω―Ä–Η–Β–Φ–Α [17].
–ü―Ä–Η –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Η ―²–Β―Ä–Α–Ω–Η–Η –ù–ü–£–ü –Ψ―¹–Ψ–±–Ψ–Β –≤–Ϋ–Η–Φ–Α–Ϋ–Η–Β –≤―¹–Β–≥–¥–Α ―É–¥–Β–Μ―è–Β―²―¹―è –Ω–Ψ–±–Ψ―΅–Ϋ―΄–Φ ―ç―³―³–Β–Κ―²–Α–Φ, ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Ϋ―΄–Φ –¥–Μ―è –¥–Α–Ϋ–Ϋ–Ψ–Ι –≥―Ä―É–Ω–Ω―΄ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, –Η –Ω―Ä–Β–Ε–¥–Β –≤―¹–Β–≥–Ψ ―ç―²–Ψ –Κ–Α―¹–Α–Β―²―¹―è –Ε–Β–Μ―É–¥–Ψ―΅–Ϋ–Ψ––Κ–Η―à–Β―΅–Ϋ–Ψ–Ι –Η –Κ―Ä–Ψ–≤–Β―²–≤–Ψ―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ. –ë–Ψ–Μ–Η –≤ –Ε–Η–≤–Ψ―²–Β, –¥–Η–Α―Ä–Β―è, –Ψ–±–Ψ―¹―²―Ä–Β–Ϋ–Η–Β –≥–Α―¹―²―Ä–Η―²–Α –Η–Μ–Η ―è–Ζ–≤–Β–Ϋ–Ϋ–Ψ–Ι –±–Ψ–Μ–Β–Ζ–Ϋ–Η, –Ω–Β―΅–Β–Ϋ–Ψ―΅–Ϋ―΄–Β ―Ä–Β–Α–Κ―Ü–Η–Η – –¥–Α–Μ–Β–Κ–Ψ –Ϋ–Β –Ω–Ψ–Μ–Ϋ―΄–Ι –Ω–Β―Ä–Β―΅–Β–Ϋ―¨ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ―΄―Ö –Ϋ–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η–Ι. –£ –¥–Α–Ϋ–Ϋ–Ψ–Φ –Α―¹–Ω–Β–Κ―²–Β –Μ–Η–Ζ–Η–Ϋ–Ψ–≤–Α―è ―¹–Ψ–Μ―¨ –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Α –Η–Φ–Β–Β―² –Ω―Ä–Β–Η–Φ―É―â–Β―¹―²–≤–Α –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Ψ–Φ, –Ω–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –≥–Ψ―Ä–Α–Ζ–¥–Ψ ―Ä–Β–Ε–Β –≤―΄–Ζ―΄–≤–Α–Β―² –Ω–Ψ–±–Ψ―΅–Ϋ―΄–Β ―ç―³―³–Β–Κ―²―΄. –ë–Μ–Α–≥–Ψ–¥–Α―Ä―è ―¹–≤–Ψ–Β–Φ―É ―Ö–Η–Φ–Η―΅–Β―¹–Κ–Ψ–Φ―É ―¹–Ψ―¹―²–Α–≤―É –û–ö–‰ –±―΄―¹―²―Ä–Ψ ―Ä–Α―¹―²–≤–Ψ―Ä―è–Β―²―¹―è –Η –Ω–Ψ―΅―²–Η –Ϋ–Β ―Ä–Α–Ζ–¥―Ä–Α–Ε–Α–Β―² –•–ö–Δ. –ü–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²―¨ –û–ö–‰ –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Κ–Β―²–Ψ–Ω―Ä–Ψ―³–Β–Ϋ–Ψ–Φ –Μ―É―΅―à–Β –≤ 1,6 ―Ä–Α–Ζ–Α. –ù–Α ―Ä–Η―¹―É–Ϋ–Κ–Β 4 –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ―΄ –Ψ–±―â–Α―è –Η –Φ–Β―¹―²–Ϋ–Α―è –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²―¨ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –û–ö–‰ (–Ω–Ψ –¥–Α–Ϋ–Ϋ―΄–Φ –≥–Α―¹―²―Ä–Ψ―¹–Κ–Ψ–Ω–Η–Η) –Ϋ–Α ―³–Ψ–Ϋ–Β 10––¥–Ϋ–Β–≤–Ϋ–Ψ–≥–Ψ –Ω―Ä–Η–Β–Φ–Α –≤ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ –Ω–Μ–Α―Ü–Β–±–Ψ. –ü–Ψ –Ψ―Ü–Β–Ϋ–Κ–Β –≤―Ä–Α―΅–Β–Ι, –Ψ–±―â–Α―è –Η –Φ–Β―¹―²–Ϋ–Α―è –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²―¨ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α –û–ö–‰ –±―΄–Μ–Η ―¹―Ä–Α–≤–Ϋ–Η–Φ―΄ ―¹ –Ω–Μ–Α―Ü–Β–±–Ψ [18].
–ù–Α –Κ–Α―³–Β–¥―Ä–Β –Ψ―²–Ψ―Ä–Η–Ϋ–Ψ–Μ–Α―Ä–Η–Ϋ–≥–Ψ–Μ–Ψ–≥–Η–Η –Λ–ü–î–û –€–™–€–Γ–Θ –±―΄–Μ–Ψ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β, ―Ü–Β–Μ―¨―é –Κ–Ψ―²–Ψ―Ä–Ψ–≥–Ψ ―è–≤–Η–Μ–Α―¹―¨ –Ψ―Ü–Β–Ϋ–Κ–Α ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Η –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ–Ψ―¹―²–Η –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Λ–Μ―É–Η―³–Ψ―Ä―² –Η –û–ö–‰ –≤ ―¹–Ψ―¹―²–Α–≤–Β –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Κ–Α―à–Μ–Β–Φ –Ϋ–Α ―³–Ψ–Ϋ–Β –û–†–£–‰. –£ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –±―΄–Μ–Η –≤–Κ–Μ―é―΅–Β–Ϋ―΄ 68 –±–Ψ–Μ―¨–Ϋ―΄―Ö (–Φ―É–Ε―΅–Η–Ϋ – 32, –Ε–Β–Ϋ―â–Η–Ϋ – 36, ―¹―Ä–Β–¥–Ϋ–Η–Ι –≤–Ψ–Ζ―Ä–Α―¹―² – 44,72±10,13 –≥–Ψ–¥–Α) ―¹ –¥–Η–Α–≥–Ϋ–Ψ–Ζ–Ψ–Φ –û–†–£–‰, –Κ–Ψ―²–Ψ―Ä―΄–Β –±―΄–Μ–Η –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ―΄ –Κ –Ψ―²–Ψ―Ä–Η–Ϋ–Ψ–Μ–Α―Ä–Η–Ϋ–≥–Ψ–Μ–Ψ–≥―É ―¹–Ω―É―¹―²―è 3–5 ―¹―É―². –Ψ―² –Ϋ–Α―΅–Α–Μ–Α ―²–Β―Ä–Α–Ω–Η–Η –≤ ―¹–≤―è–Ζ–Η ―¹ ―¹–Ψ―Ö―Ä–Α–Ϋ―è―é―â–Η–Φ―¹―è –Κ–Α―à–Μ–Β–Φ. –ö―Ä–Η―²–Β―Ä–Η―è–Φ–Η –≤–Κ–Μ―é―΅–Β–Ϋ–Η―è –≤ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ―è–≤–Η–Μ–Η―¹―¨ –Ϋ–Α–Μ–Η―΅–Η–Β –Ω―Ä–Ψ–¥―É–Κ―²–Η–≤–Ϋ–Ψ–≥–Ψ –Κ–Α―à–Μ―è –Ϋ–Α ―³–Ψ–Ϋ–Β –Κ–Α―²–Α―Ä–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―¹–Η–Ϋ–¥―Ä–Ψ–Φ–Α –≤ –Ω–Ψ–Μ–Ψ―¹―²–Η –Ϋ–Ψ―¹–Α –Η –≥–Μ–Ψ―²–Κ–Β, ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –Ψ–±―â–Β–Ι –Η–Ϋ―²–Ψ–Κ―¹–Η–Κ–Α―Ü–Η–Η, –Ω–Ψ–≤―΄―à–Β–Ϋ–Η–Β ―²–Β–Φ–Ω–Β―Ä–Α―²―É―Ä―΄ ―²–Β–Μ–Α. –ö―Ä–Η―²–Β―Ä–Η–Β–Φ –Η―¹–Κ–Μ―é―΅–Β–Ϋ–Η―è –Η–Ζ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –±―΄–Μ–Ψ ―Ä–Α–Ζ–≤–Η―²–Η–Β –±–Α–Κ―²–Β―Ä–Η–Α–Μ―¨–Ϋ―΄―Ö –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η–Ι –û–†–£–‰ (―¹–Η–Ϋ―É―¹–Η―², ―²–Ψ–Ϋ–Ζ–Η–Μ–Μ–Η―², ―²―Ä–Α―Ö–Β–Η―², –±―Ä–Ψ–Ϋ―Ö–Η―²), ―²―Ä–Β–±―É―é―â–Η―Ö –Ϋ–Α–Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è –Α–Ϋ―²–Η–±–Α–Κ―²–Β―Ä–Η–Α–Μ―¨–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤.
–ü–Α―Ü–Η–Β–Ϋ―²―΄ –±―΄–Μ–Η ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ―΄ –≤ 2 ―Ä–Α–≤–Ϋ–Ψ–Ζ–Ϋ–Α―΅–Ϋ―΄–Β ―¹–Ψ–Ω–Ψ―¹―²–Α–≤–Η–Φ―΄–Β –≥―Ä―É–Ω–Ω―΄. –û―¹–Ϋ–Ψ–≤–Ϋ―É―é –≥―Ä―É–Ω–Ω―É (–û–™) ―¹–Ψ―¹―²–Α–≤–Η–Μ–Η 34 –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω―Ä–Η–Φ–Β–Ϋ―è–Μ–Η ―¹–Η―Ä–Ψ–Ω –Λ–Μ―É–Η―³–Ψ―Ä―² –Ω–Ψ 15 –Φ–Μ (1,35 –≥) 2–3 ―Ä–Α–Ζ–Α/―¹―É―²., –Α ―²–Α–Κ–Ε–Β –≥―Ä–Α–Ϋ―É–Μ―è―² –û–ö–‰ –¥–Μ―è –Ω―Ä–Η–≥–Ψ―²–Ψ–≤–Μ–Β–Ϋ–Η―è ―Ä–Α―¹―²–≤–Ψ―Ä–Α – 1 –¥–≤―É―Ö–Ψ–±―ä–Β–Φ–Ϋ―΄–Ι –Ω–Α–Κ–Β―²–Η–Κ (–Ω–Ψ–Μ–Ϋ–Α―è –¥–Ψ–Ζ–Α) ―Ä–Α―¹―²–≤–Ψ―Ä―è–Μ–Η –≤ 0,5 ―¹―²–Α–Κ–Α–Ϋ–Α –Ω–Η―²―¨–Β–≤–Ψ–Ι –≤–Ψ–¥―΄ –Η –Ω―Ä–Η–Ϋ–Η–Φ–Α–Μ–Η –≤–Ϋ―É―²―Ä―¨ 3 ―Ä–Α–Ζ–Α/―¹―É―². –≤–Ψ –≤―Ä–Β–Φ―è –Β–¥―΄. –ö―É―Ä―¹ –Μ–Β―΅–Β–Ϋ–Η―è –Ψ–±–Ψ–Η–Φ–Η –Ω―Ä–Β–Ω–Α―Ä–Α―²–Α–Φ–Η ―¹–Ψ―¹―²–Α–≤–Η–Μ 7 ―¹―É―². –ü–Ψ–Φ–Η–Φ–Ψ –Ω–Β―Ä–Β―΅–Η―¹–Μ–Β–Ϋ–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤, –≤ ―¹–Ψ―¹―²–Α–≤ –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –≤–Κ–Μ―é―΅–Α–Μ–Η―¹―¨ –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄ –¥–Μ―è –Η―Ä―Ä–Η–≥–Α―Ü–Η–Η –Ω–Ψ–Μ–Ψ―¹―²–Η –Ϋ–Ψ―¹–Α, ―²–Ψ–Ω–Η―΅–Β―¹–Κ–Η–Β –¥–Β–Κ–Ψ–Ϋ–≥–Β―¹―²–Α–Ϋ―²―΄ –Η –Φ–Β―¹―²–Ϋ―΄–Β –Α–Ϋ―²–Η―¹–Β–Ω―²–Η–Κ–Η –¥–Μ―è –Ω–Ψ–Μ–Ψ―¹–Κ–Α–Ϋ–Η―è –≥–Ψ―Ä–Μ–Α.
–£ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨–Ϋ―É―é –≥―Ä―É–Ω–Ω―É (–ö–™) –≤–Ψ―à–Μ–Η 34 –±–Ψ–Μ―¨–Ϋ―΄―Ö, –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω–Ψ–Μ―É―΅–Α–Μ–Η ―²–Ψ–Μ―¨–Κ–Ψ ―¹―Ä–Β–¥―¹―²–≤–Α –¥–Μ―è –Η―Ä―Ä–Η–≥–Α―Ü–Η–Η –Ω–Ψ–Μ–Ψ―¹―²–Η –Ϋ–Ψ―¹–Α, ―²–Ψ–Ω–Η―΅–Β―¹–Κ–Η–Β –¥–Β–Κ–Ψ–Ϋ–≥–Β―¹―²–Α–Ϋ―²―΄ –Η –Φ–Β―¹―²–Ϋ―΄–Β –Α–Ϋ―²–Η―¹–Β–Ω―²–Η–Κ–Η –¥–Μ―è –Ω–Ψ–Μ–Ψ―¹–Κ–Α–Ϋ–Η―è –≥–Ψ―Ä–Μ–Α.
–ü―Ä–Β–¥–≤–Α―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–Β –Ψ–±―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―Ü–Β–Μ―¨―é ―Ä–Β―à–Β–Ϋ–Η―è –≤–Ψ–Ω―Ä–Ψ―¹–Α –Ψ –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ―¹―²–Η –≤–Κ–Μ―é―΅–Β–Ϋ–Η―è –Η―Ö –≤ –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ―É –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –≤–Κ–Μ―é―΅–Α–Μ–Ψ ―¹–±–Ψ―Ä –Ε–Α–Μ–Ψ–± –Η –Α–Ϋ–Α–Φ–Ϋ–Β–Ζ–Α –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, –Ψ―Ü–Β–Ϋ–Κ―É –Μ–Β―΅–Α―â–Η–Φ –≤―Ä–Α―΅–Ψ–Φ ―¹―É–±―ä–Β–Κ―²–Η–≤–Ϋ―΄―Ö –Η –Ψ–±―ä–Β–Κ―²–Η–≤–Ϋ―΄―Ö –¥–Α–Ϋ–Ϋ―΄―Ö –Ψ ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Α (―¹―²–Α–Ϋ–¥–Α―Ä―²–Ϋ―΄–Ι –¦–û–†––Ψ―¹–Φ–Ψ―²―Ä), ―Ä–Β–Ϋ―²–≥–Β–Ϋ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ψ–Κ–Ψ–Μ–Ψ–Ϋ–Ψ―¹–Ψ–≤―΄―Ö –Ω–Α–Ζ―É―Ö –¥–Μ―è –Η―¹–Κ–Μ―é―΅–Β–Ϋ–Η―è –±–Α–Κ―²–Β―Ä–Η–Α–Μ―¨–Ϋ–Ψ–≥–Ψ ―¹–Η–Ϋ―É―¹–Η―²–Α, –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Ϋ―¹–Ω–Ψ―Ä―²–Α –Ω–Ψ―¹―Ä–Β–¥―¹―²–≤–Ψ–Φ ―¹–Α―Ö–Α―Ä–Η–Ϋ–Ψ–≤–Ψ–≥–Ψ ―²–Β―¹―²–Α. –û―Ü–Β–Ϋ–Κ–Α –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Κ–Α―à–Μ―è –Ω―Ä–Ψ–≤–Ψ–¥–Η–Μ–Α―¹―¨ –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Α–Ϋ–Η–Η 10––±–Α–Μ–Μ―¨–Ϋ–Ψ–Ι –≤–Η–Ζ―É–Α–Μ―¨–Ϋ–Ψ–Ι –Α–Ϋ–Α–Μ–Ψ–≥–Ψ–≤–Ψ–Ι ―à–Κ–Α–Μ―΄ (―Ä–Η―¹. 5), –≤ –Κ–Ψ―²–Ψ―Ä–Ψ–Ι –Ψ―²―¹―É―²―¹―²–≤–Η–Β –Κ–Α―à–Μ―è ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Ψ–≤–Α–Μ–Ψ 0 –±–Α–Μ–Μ–Α–Φ, –Α –Ϋ–Α–Μ–Η―΅–Η–Β –Φ―É―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Κ–Α―à–Μ―è – 10 –±–Α–Μ–Μ–Α–Φ.
–ö–Ψ–Ϋ―²―Ä–Ψ–Μ―¨–Ϋ–Α―è –Ψ―Ü–Β–Ϋ–Κ–Α ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η―è –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ω―Ä–Ψ–≤–Ψ–¥–Η–Μ–Α―¹―¨ –≤ 1––Ι –¥–Β–Ϋ―¨ –Ψ―² –Ϋ–Α―΅–Α–Μ–Α ―²–Β―Ä–Α–Ω–Η–Η (1––Ι –≤–Η–Ζ–Η―²), 3––Ι –¥–Β–Ϋ―¨ (2––Ι –≤–Η–Ζ–Η―²), 5––Ι –¥–Β–Ϋ―¨ (3––Ι –≤–Η–Ζ–Η―²) –Η 7––Ι –¥–Β–Ϋ―¨ (4––Ι –≤–Η–Ζ–Η―²). –ö–Ψ–Ϋ―²―Ä–Ψ–Μ―¨–Ϋ–Α―è –Ψ―Ü–Β–Ϋ–Κ–Α –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ–Ψ–≥–Ψ ―²―Ä–Α–Ϋ―¹–Ω–Ψ―Ä―²–Α –Ω―Ä–Ψ–≤–Ψ–¥–Η–Μ–Α―¹―¨ –Ϋ–Α 3––Ι –¥–Β–Ϋ―¨ (2––Ι –≤–Η–Ζ–Η―²) –Η 7––Ι –¥–Β–Ϋ―¨ (4––Ι –≤–Η–Ζ–Η―²).
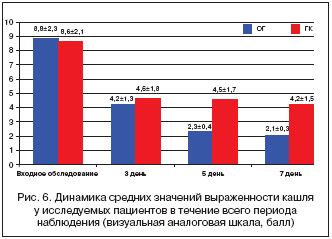
–î–Ψ –Ϋ–Α―΅–Α–Μ–Α ―²–Β―Ä–Α–Ω–Η–Η ―¹―Ä–Β–¥–Ϋ–Η–Β –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Κ–Α―à–Μ―è –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ –Ϋ–Β ―Ä–Α–Ζ–Μ–Η―΅–Α–Μ–Η―¹―¨ –≤ –Ψ–±–Β–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö (p≥0,05). –ù–Α ―³–Ψ–Ϋ–Β –Ω―Ä–Ψ–≤–Ψ–¥–Η–Φ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –Ω–Ψ–Μ–Ψ–Ε–Η―²–Β–Μ―¨–Ϋ–Α―è –¥–Η–Ϋ–Α–Φ–Η–Κ–Α –Ψ―²–Φ–Β―΅–Β–Ϋ–Α –≤ –Ψ–±–Β–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö, –Ψ–¥–Ϋ–Α–Κ–Ψ ―¹―É―â–Β―¹―²–≤–Ψ–≤–Α–Μ–Η –Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ―΄–Β ―Ä–Α–Ζ–Μ–Η―΅–Η―è (―Ä–Η―¹. 6).
–ü―Ä–Η –Α–Ϋ–Α–Μ–Η–Ζ–Β –Ω–Ψ–Μ―É―΅–Β–Ϋ–Ϋ―΄―Ö –¥–Α–Ϋ–Ϋ―΄―Ö –Ψ―²–Φ–Β―΅–Β–Ϋ–Ψ ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ―¹―²–Η –Κ–Α―à–Μ―è –≤ –û–™ –Κ–Ψ 2––Φ―É –≤–Η–Ζ–Η―²―É –Ϋ–Α 52%, –Α –≤ –ö–™ – –Ϋ–Α 47% (p≥0,05). –ö 3––Φ―É –≤–Η–Ζ–Η―²―É –≤ –û–™ ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β ―¹–Ψ―¹―²–Α–≤–Η–Μ–Ψ ―É–Ε–Β 73,9%, –Α –≤ –ö–™ –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η –Ϋ–Β –Η–Ζ–Φ–Β–Ϋ–Η–Μ–Ψ―¹―¨ –Ϋ–Η –Κ 3––Φ―É, –Ϋ–Η –Κ 4––Φ―É –≤–Η–Ζ–Η―²–Α–Φ, ―΅―²–Ψ –Ω–Ψ–Ζ–≤–Ψ–Μ–Η–Μ–Ψ –¥–Ψ―¹―²–Η―΅―¨ ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Ψ–Ι –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ―¹―²–Η ―Ä–Α–Ζ–Μ–Η―΅–Η–Ι –Φ–Β–Ε–¥―É –≥―Ä―É–Ω–Ω–Α–Φ–Η (p<0,05). –Θ–Κ–Α–Ζ–Α–Ϋ–Ϋ–Α―è ―¹–Η―²―É–Α―Ü–Η―è –≤ –û–™ ―¹―²–Ψ–Ι–Κ–Ψ ―¹–Ψ―Ö―Ä–Α–Ϋ―è–Μ–Α―¹―¨ –Κ 4––Φ―É –≤–Η–Ζ–Η―²―É.
–£–Ψ –≤―Ä–Β–Φ―è –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η―è –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Ψ―²–Φ–Β―΅–Α–Μ–Ψ―¹―¨ ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β –≤―Ä–Β–Φ–Β–Ϋ–Η –Φ―É–Κ–Ψ―Ü–Η–Μ–Η–Α―Ä–Ϋ–Ψ–≥–Ψ –Κ–Μ–Η―Ä–Β–Ϋ―¹–Α –≤ –Ψ–±–Β–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö, –Ψ–¥–Ϋ–Α–Κ–Ψ –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ―¹―²―¨ ―É–Κ–Α–Ζ–Α–Ϋ–Ϋ―΄―Ö –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η–Ι –≤ –û–™ –±―΄–Μ–Α ―¹―²–Α―²–Η―¹―²–Η―΅–Β―¹–Κ–Η –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ–Ι –Ω―Ä–Η ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ –Α–Ϋ–Α–Μ–Ψ–≥–Η―΅–Ϋ―΄–Φ–Η –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―è–Φ–Η –≤ –ö–™ –≤–Ψ –≤―¹–Β―Ö ―²–Ψ―΅–Κ–Α―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è (―Ä–Η―¹. 7). –ù–Β–Ε–Β–Μ–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―è–≤–Μ–Β–Ϋ–Η–Ι –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –≤ –Ψ–±–Β–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö –Ϋ–Β –≤―΄―è–≤–Μ–Β–Ϋ–Ψ.
–ü–Ψ–Μ―É―΅–Β–Ϋ–Ϋ―΄–Β ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –¥–Η–Ϋ–Α–Φ–Η–Κ–Η –Κ–Α―à–Μ―è –Ψ―²―Ä–Α–Ζ–Η–Μ–Η―¹―¨ –Ϋ–Α –Η―²–Ψ–≥–Ψ–≤–Ψ–Ι ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Μ–Β―΅–Β–Ϋ–Η―è –û–†–£–‰ –≤ –Ψ–±–Β–Η―Ö –≥―Ä―É–Ω–Ω–Α―Ö (―Ä–Η―¹. 8). –ü―Ä–Η ―ç―²–Ψ–Φ –≤ –û–™ –Ζ–Α―Ä–Β–≥–Η―¹―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ–Ψ –¥–Ψ―¹―²–Ψ–≤–Β―Ä–Ϋ–Ψ –±–Ψ–Μ―¨―à–Β–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ ―¹–Μ―É―΅–Α–Β–≤ –≤―΄–Ζ–¥–Ψ―Ä–Ψ–≤–Μ–Β–Ϋ–Η―è –Κ 7 ―¹―É―². –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –ö–™ (p<0,05), –≤ –Κ–Ψ―²–Ψ―Ä–Ψ–Ι ―É 5 (14,7%) –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Κ –Κ–Ψ–Ϋ―Ü―É –Μ–Β―΅–Β–Ϋ–Η―è ―Ä–Α–Ζ–≤–Η–Μ–Η―¹―¨ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –±–Α–Κ―²–Β―Ä–Η–Α–Μ―¨–Ϋ―΄–Β –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η―è –û–†–£–‰ (―É 2 –±–Ψ–Μ―¨–Ϋ―΄―Ö – –Ψ―¹―²―Ä―΄–Ι –±–Α–Κ―²–Β―Ä–Η–Α–Μ―¨–Ϋ―΄–Ι ―Ä–Η–Ϋ–Ψ―¹–Η–Ϋ―É―¹–Η―², ―É 2 – –Ψ―¹―²―Ä―΄–Ι ―²―Ä–Α―Ö–Β–Η―², ―É 1 – –Ψ―¹―²―Ä―΄–Ι –±―Ä–Ψ–Ϋ―Ö–Η―²).
–Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, –Ζ–Α–¥–Α―΅–Η, ―¹―²–Ψ―è―â–Η–Β –Ω–Β―Ä–Β–¥ –Ω―Ä–Α–Κ―²–Η–Κ―É―é―â–Η–Φ –≤―Ä–Α―΅–Ψ–Φ –Ω―Ä–Η –≤―΄–±–Ψ―Ä–Β –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö ―¹―Ä–Β–¥―¹―²–≤ –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –Κ–Α―à–Μ―è –Ω―Ä–Η –û–†–£–‰, –Ω―Ä–Η –Κ–Α–Ε―É―â–Η―Ö―¹―è –Ω―Ä–Ψ―¹―²–Ψ―²–Β –Η –Μ–Β–≥–Κ–Ψ―¹―²–Η, –Ϋ–Β ―²–Ψ–Μ―¨–Κ–Ψ ―²―Ä–Β–±―É―é―² –≥–Μ―É–±–Ψ–Κ–Η―Ö –Ζ–Ϋ–Α–Ϋ–Η–Ι –Ψ –Ω–Α―²–Ψ–≥–Β–Ϋ–Β–Ζ–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è, –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Α―Ö –¥–Β–Ι―¹―²–≤–Η―è –Η―¹–Ω–Ψ–Μ―¨–Ζ―É–Β–Φ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –Η –Η―Ö –Ω–Ψ–±–Ψ―΅–Ϋ―΄―Ö ―ç―³―³–Β–Κ―²–Α―Ö, –Ϋ–Ψ –Η –Ψ–±―è–Ζ―΄–≤–Α―é―² –≤ –Κ–Α–Ε–¥–Ψ–Φ –Κ–Ψ–Ϋ–Κ―Ä–Β―²–Ϋ–Ψ–Φ ―¹–Μ―É―΅–Α–Β –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ–Η–Ζ–Η―Ä–Ψ–≤–Α―²―¨ –Μ–Β―΅–Β–±–Ϋ―É―é ―²–Α–Κ―²–Η–Κ―É. –£ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –Η–Φ–Β―é―²―¹―è ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―΄–Β –Η –±–Β–Ζ–Ψ–Ω–Α―¹–Ϋ―΄–Β –Μ–Β–Κ–Α―Ä―¹―²–≤–Β–Ϋ–Ϋ―΄–Β ―¹―Ä–Β–¥―¹―²–≤–Α, –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―â–Η–Β ―¹―É―â–Β―¹―²–≤–Β–Ϋ–Ϋ–Ψ ―É–Φ–Β–Ϋ―¨―à–Η―²―¨ ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –Ω―Ä–Ψ―è–≤–Μ–Β–Ϋ–Η―è –û–†–£–‰ –≤ –Κ–Ψ―Ä–Ψ―²–Κ–Η–Β ―¹―Ä–Ψ–Κ–Η –Η –Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―²–Η―²―¨ ―Ä–Α–Ζ–≤–Η―²–Η–Β –±–Α–Κ―²–Β―Ä–Η–Α–Μ―¨–Ϋ―΄―Ö –Ψ―¹–Μ–Ψ–Ε–Ϋ–Β–Ϋ–Η–Ι.






–¦–Η―²–Β―Ä–Α―²―É―Ä–Α
1. –½–Α–Ω–Μ–Α―²–Ϋ–Η–Κ–Ψ–≤ –ê.–¦. –ü―Ä–Η–Ϋ―Ü–Η–Ω―΄ ―Ä–Α―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –Ψ―¹―²―Ä―΄―Ö ―Ä–Β―¹–Ω–Η―Ä–Α―²–Ψ―Ä–Ϋ―΄―Ö –≤–Η―Ä―É―¹–Ϋ―΄―Ö –Η–Ϋ―³–Β–Κ―Ü–Η–Ι ―É –¥–Β―²–Β–Ι ―Ä–Α–Ϋ–Ϋ–Β–≥–Ψ –≤–Ψ–Ζ―Ä–Α―¹―²–Α // –†―É―¹―¹–Κ–Η–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ―¹–Κ–Η–Ι –Ε―É―Ä–Ϋ–Α–Μ. 2004. –Δ. 12. ⳕ 13. –Γ. 790–795.
2. –û–≤―΅–Α―Ä–Β–Ϋ–Κ–Ψ –Γ.–‰. –€―É–Κ–Ψ–Μ–Η―²–Η―΅–Β―¹–Κ–Η–Β (–Φ―É–Κ–Ψ―Ä–Β–≥―É–Μ―è―²–Ψ―Ä–Ϋ―΄–Β) –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄ –≤ –Μ–Β―΅–Β–Ϋ–Η–Η ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Ψ–Ι –Ψ–±―¹―²―Ä―É–Κ―²–Η–≤–Ϋ–Ψ–Ι –±–Ψ–Μ–Β–Ζ–Ϋ–Η –Μ–Β–≥–Κ–Η―Ö // –†―É―¹―¹–Κ–Η–Ι –Φ–Β–¥–Η―Ü–Η–Ϋ―¹–Κ–Η–Ι –Ε―É―Ä–Ϋ–Α–Μ. 2002. –Δ. 10. ⳕ 4. –Γ. 153–157.
3. –û―¹―²―Ä―΄–Β ―Ä–Β―¹–Ω–Η―Ä–Α―²–Ψ―Ä–Ϋ―΄–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è ―É –¥–Β―²–Β–Ι: –Μ–Β―΅–Β–Ϋ–Η–Β –Η –Ω―Ä–Ψ―³–Η–Μ–Α–Κ―²–Η–Κ–Α. –ù–Α―É―΅–Ϋ–Ψ––Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Α―è –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ–Α –Γ–Ψ―é–Ζ–Α –Ω–Β–¥–Η–Α―²―Ä–Ψ–≤ –†–Ψ―¹―¹–Η–Η. –€.: –€–Β–Ε–¥―É–Ϋ–Α―Ä–Ψ–¥–Ϋ―΄–Ι ―³–Ψ–Ϋ–¥ –Ψ―Ö―Ä–Α–Ϋ―΄ –Ζ–¥–Ψ―Ä–Ψ–≤―¨―è –Φ–Α―²–Β―Ä–Η –Η ―Ä–Β–±–Β–Ϋ–Κ–Α, 2002. 69 ―¹.
4. –ü–Ψ–Κ―Ä–Ψ–≤―¹–Κ–Η–Ι –£.–‰. –‰–Ϋ―³–Β–Κ―Ü–Η–Ψ–Ϋ–Ϋ–Α―è –Ω–Α―²–Ψ–Μ–Ψ–≥–Η―è: –≤―΅–Β―Ä–Α, ―¹–Β–≥–Ψ–¥–Ϋ―è, –Ζ–Α–≤―²―Ä–Α. –ü―Ä–Ψ―³–Η–Μ–Α–Κ―²–Η–Κ–Α, –¥–Η–Α–≥–Ϋ–Ψ―¹―²–Η–Κ–Α –Η ―³–Α―Ä–Φ–Α–Κ–Ψ―²–Β―Ä–Α–Ω–Η―è –Ϋ–Β–Κ–Ψ―²–Ψ―Ä―΄―Ö –Η–Ϋ―³–Β–Κ―Ü–Η–Ψ–Ϋ–Ϋ―΄―Ö –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Ι. –€., 2002. –Γ. 7–17.
5. –ü–Ψ–Μ–Β–≤―â–Η–Κ–Ψ–≤ –ê.–£. –†–Η–Ϋ–Ψ―¹–Η–Ϋ―É―¹–Η―²―΄: –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ―΄ ―Ä–Α–Ζ–≤–Η―²–Η―è –≤–Ψ―¹–Ω–Α–Μ–Β–Ϋ–Η―è ―¹–Μ–Η–Ζ–Η―¹―²―΄―Ö –Ψ–±–Ψ–Μ–Ψ―΅–Β–Κ –Η –Ω―É―²–Η –≤–Ψ–Ζ–¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α –Ϋ–Β–≥–Ψ: –€–Α―²–Β―Ä–Η–Α–Μ―΄ XVI ―¹―ä–Β–Ζ–¥–Α –Ψ―²–Ψ―Ä–Η–Ϋ–Ψ–Μ–Α―Ä–Η–Ϋ–≥–Ψ–Μ–Ψ–≥–Ψ–≤ –†–Λ. –Γ–ü–±., 2001. –Γ. 7.
6. –†―è–Ζ–Α–Ϋ―Ü–Β–≤ –Γ.–£. –†–Ψ–Μ―¨ –Φ―É–Κ–Ψ–Μ–Η―²–Η―΅–Β―¹–Κ–Η―Ö, ―¹–Β–Κ―Ä–Β―²–Ψ–Μ–Η―²–Η―΅–Β―¹–Κ–Η―Ö –Η ―¹–Β–Κ―Ä–Β―²–Ψ–Φ–Ψ―²–Ψ―Ä–Ϋ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –Ψ―¹―²―Ä―΄―Ö –Η ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η―Ö ―¹–Η–Ϋ―É―¹–Η―²–Ψ–≤ ―É –¥–Β―²–Β–Ι // –ù–Ψ–≤–Ψ―¹―²–Η –Ψ―²–Ψ―Ä–Η–Ϋ–Ψ–Μ–Α―Ä. –Η –Μ–Ψ–≥–Ψ–Ω–Α―²–Ψ–Μ. 2002. ⳕ 1 (29). –Γ. 129–132.
7. –Γ–Η–Ϋ–Ψ–Ω–Α–Μ―¨–Ϋ–Η–Κ–Ψ–≤ –ê.–‰., –ö–Μ―è―΅–Κ–Η–Ϋ–Α –‰.–¦. –€–Β―¹―²–Ψ –Φ―É–Κ–Ψ–Μ–Η―²–Η―΅–Β―¹–Κ–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ –≤ –Κ–Ψ–Φ–Ω–Μ–Β–Κ―¹–Ϋ–Ψ–Ι ―²–Β―Ä–Α–Ω–Η–Η –±–Ψ–Μ–Β–Ζ–Ϋ–Β–Ι –Ψ―Ä–≥–Α–Ϋ–Ψ–≤ –¥―΄―Ö–Α–Ϋ–Η―è // –†–Ψ―¹. –Φ–Β–¥. –≤–Β―¹―²–Η. 1997. –Δ. 2. ⳕ 4. –Γ. 9–18.
8. –Θ―΅–Α–Ι–Κ–Η–Ϋ –£.–Λ. –†―É–Κ–Ψ–≤–Ψ–¥―¹―²–≤–Ψ –Ω–Ψ –Η–Ϋ―³–Β–Κ―Ü–Η–Ψ–Ϋ–Ϋ―΄–Φ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è–Φ ―É –¥–Β―²–Β–Ι. –€.: –™―ç–Ψ―²–Α―Ä––€–Β–¥–Η―Ü–Η–Ϋ–Α, 1998. 700 ―¹.
9. Chalumeau M., Cheron G., Assathiany R., et al. Mucolitic agents for acute respiratory tract infections in infants: a pharmaco–epiderniologic problem? // Arch Pediatr. 2002. Vol. 9. P. 1128–1136.
10. Ishibashi Y., Takayama G., Inouye Y. et al. Carbocisteine normalizes the viscous property of mucus through regulation of fucosylated and sialylated sugar chain on airway mucins // Eur J Pharmacol. 2010. Vol. 641 (2–3). P. 226–228.
11. Lemke T.L., Williams D.A., Roche V.F. et al. Foyes Principles of Medical Chemistry. 6th ed. Philadelphia: Lippincott Williams and Wilkins, 2008. 673 p.
12. Mazieres B., Rouanet S., Guillon Y. et al. Topical ketoprofen patch in the treatment of tendinitis: a randomized, double blind, placebo controlled study // The Journal of rheumatology. 2005. Vol. 32 (8). P. 1563–1570.
13. Red Book: 2000. Report of the Committee on Infection Diseases. 25rd: American Academy of Pediatrics, 2000. 855 p.
14. Xiao H., Li D.X., Liu M. Knowledge translation: airway epithelial cell migration and respiratory diseases // Cell Mol Life Sci. 2012. In print.
15. Yasuo M., Fujimoto K., Imamura H., Ushiki A. et al. L–carbocisteine reduces neutrophil elastase–induced mucin production // RespirPhysiol Neurobiol. 2009. Vol. 167 (2). P. 214–216.
16. Braga P.C. et al. Long–lasting effects on rheology and clearance of bronchial mucus after short–term administration of high doses of carbocysteine–lysine to patients with chronic bronchitis // Respiration. 1990. Vol. 57. –†. 353–358.
17. Fatti F. Summary of product characteristics. Data on file, 1991.
18. Fatti F. et al. // Minerva Med. 1994. Vol. 85. –†. 531–535.












