–Я—А–Њ—Ж–µ—Б—Б –∞–Ї—В–Є–≤–∞—Ж–Є–Є –≤—Л–Ј—Л–≤–∞–µ—В—Б—П —В–∞–Ї–Є–Љ–Є –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, –Ї–∞–Ї —Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–≥–Њ –≤—Л–±—А–Њ—Б–∞, –Є—И–µ–Љ–Є—П –ґ–Є–Ј–љ–µ–љ–љ–Њ –≤–∞–ґ–љ–Њ–≥–Њ –Њ—А–≥–∞–љ–∞, –њ–Њ—В–µ—А—П –љ–∞—В—А–Є—П –Є –≤–Њ–і—Л, –Ј–љ–∞—З–Є–Љ–Њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —АH –Є –і—А. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ – –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II, –Ї–Њ—В–Њ—А—Л–є —П–≤–ї—П–µ—В—Б—П –Љ–Њ—Й–љ—Л–Љ –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–Њ–Љ, —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–Љ –≤—Л–±—А–Њ—Б –∞–ї—М–і–Њ—Б—В–µ—А–Њ–љ–∞, –∞ —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±–µ–љ –њ–Њ–≤—Л—И–∞—В—М –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –°–Р–° – –≤—Л–±—А–Њ—Б –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞. –Э–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ –≤ —Б–≤–Њ—О –Њ—З–µ—А–µ–і—М –Љ–Њ–ґ–µ—В –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞—В—М –†–Р–Р–° – —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —Б–Є–љ—В–µ–Ј —А–µ–љ–Є–љ–∞. –Т –Є—В–Њ–≥–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Є—Е –і–≤—Г—Е —Б–Є—Б—В–µ–Љ, –≤—Л–Ј—Л–≤–∞—П –Љ–Њ—Й–љ—Г—О –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є—О, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –І–°–°, —Б–µ—А–і–µ—З–љ–Њ–≥–Њ –≤—Л–±—А–Њ—Б–∞, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞–µ—В —Д—Г–љ–Ї—Ж–Є—О –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –љ–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–Љ —Г—А–Њ–≤–љ–µ, —Б–Њ—Е—А–∞–љ—П–µ—В –≥–Њ–Љ–µ–Њ—Б—В–∞–Ј –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Т –љ–Њ—А–Љ–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ—А–µ—Б—Б–Њ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ (–†–Р–Р–° –Є –°–Р–°) –њ—А–Њ—В–Є–≤–Њ—Б—В–Њ–Є—В –і–µ–є—Б—В–≤–Є–µ –і–µ–њ—А–µ—Б—Б–Њ—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л – –Ї–∞–ї–ї–Є–Ї—А–µ–Є–љ––Ї–Є–љ–Є–љ–Њ–≤–Њ–є (–Ї–ї—О—З–µ–≤–Њ–µ –Ј–≤–µ–љ–Њ – –±—А–∞–і–Є–Ї–Є–љ–Є–љ), –≤—Л–Ј—Л–≤–∞—О—Й–µ–µ —Б–Є—Б—В–µ–Љ–љ—Г—О –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—О. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ –і–µ–є—Б—В–≤–Є–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤, –Њ–њ–Є—Б–∞–љ–љ—Л—Е –≤—Л—И–µ, –љ–Њ—А–Љ–∞–ї—М–љ–∞—П —А–µ–≥—Г–ї—П—Ж–Є—П –љ–∞—А—Г—И–∞–µ—В—Б—П, –Є –њ—А–µ–Њ–±–ї–∞–і–∞—О—В —Н—Д—Д–µ–Ї—В—Л –њ—А–µ—Б—Б–Њ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ. –Ш–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§ —В–Њ—А–Љ–Њ–Ј—П—В —Н—Д—Д–µ–Ї—В—Л –њ—А–µ—Б—Б–Њ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ –Є –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —П–≤–ї—П—О—В—Б—П –∞–Ї—В–Є–≤–∞—В–Њ—А–∞–Љ–Є –і–µ–њ—А–µ—Б—Б–Њ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ.
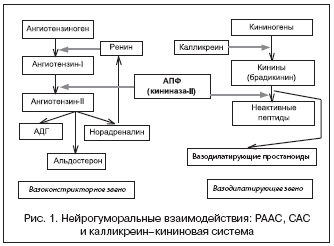
–Ю—Б–љ–Њ–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–Р–Я–§ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –±–ї–Њ–Ї–∞–і–Њ–є –Р–Я–§ (—А–Є—Б. 1): —Г—Б—В—А–∞–љ–µ–љ–Є–µ–Љ –≤–∞–Ј–Њ–њ—А–µ—Б—Б–Њ—А–љ–Њ–≥–Њ, –∞–љ—В–Є–і–Є—Г—А–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –∞–љ—В–Є–љ–∞—В—А–Є–є—Г—А–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II, —Г—Б–Є–ї–µ–љ–Є–µ–Љ —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–µ–≥–Њ, –і–Є—Г—А–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –љ–∞—В—А–Є–є—Г—А–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ –Є –і—А—Г–≥–Є—Е —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–Њ–≤ (–њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤ J2 –Є E2, –љ–∞—В—А–Є–є—Г—А–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–µ–њ—В–Є–і–∞, —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–≥–Њ —Д–∞–Ї—В–Њ—А–∞ —А–µ–ї–∞–Ї—Б–∞—Ж–Є–Є), –∞ —В–∞–Ї–ґ–µ –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–є –±–ї–Њ–Ї–∞–і–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –°–Р–° –њ—Г—В–µ–Љ —В–Њ—А–Љ–Њ–ґ–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞.
–Т —Б–µ—А–µ–і–Є–љ–µ 1980–—Е –≥–≥. –≤—Л—П–≤–ї–µ–љ—Л –ї–Њ–Ї–∞–ї—М–љ—Л–µ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ —Б–Є—Б—В–µ–Љ—Л (–њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –†–Р–Р–°) –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—А–≥–∞–љ–∞—Е –Є —В–Ї–∞–љ—П—Е –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Р–Ї—В–Є–≤–∞—Ж–Є—П —В–Ї–∞–љ–µ–≤—Л—Е –†–Р–Р–° –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ –њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–є (—Ж–Є—А–Ї—Г–ї–Є—А—Г—О—Й–µ–є), –љ–Њ –і–µ–є—Б—В–≤–Є–µ —Н—В–Є—Е —Б–Є—Б—В–µ–Љ —А–∞–Ј–ї–Є—З–∞–µ—В—Б—П. –Я–ї–∞–Ј–Љ–µ–љ–љ–∞—П –†–Р–Р–° –∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П –±—Л—Б—В—А–Њ, –љ–Њ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л. –Р–Ї—В–Є–≤–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–≤—Л—Е –†–Р–Р–° –љ–∞—А–∞—Б—В–∞–µ—В –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ, –Њ–і–љ–∞–Ї–Њ —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ. –°–Є–љ—В–µ–Ј–Є—А—Г—О—Й–Є–є—Б—П –≤ –Љ–Є–Њ–Ї–∞—А–і–µ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II –∞–Ї—В–Є–≤–Є—А—Г–µ—В –њ—А–Њ—В–Њ–Њ–љ–Ї–Њ–≥–µ–љ—Л –Є —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В –≥–Є–њ–µ—А—В—А–Њ—Д–Є—О –Є —Д–Є–±—А–Њ–Ј –Љ—Л—И–µ—З–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–љ –∞–Ї—В–Є–≤–Є—А—Г–µ—В –ї–Њ–Ї–∞–ї—М–љ—Л–є —Б–Є–љ—В–µ–Ј –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–∞–±–ї—О–і–∞—О—В—Б—П –≤ –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А–µ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ –Є –њ—А–Є–≤–Њ–і—П—В –Ї –µ–µ –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є.
V. Dzau [1] –≤—Л–і–µ–ї—П–µ—В —Б–ї–µ–і—Г—О—Й–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л–µ —Н—Д—Д–µ–Ї—В—Л –Є–Р–Я–§:
• —Б–Є—Б—В–µ–Љ–љ–∞—П –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П (—Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ—Б—В–љ–∞–≥—А—Г–Ј–Ї–Є –љ–∞ –ї–µ–≤—Л–є –ґ–µ–ї—Г–і–Њ—З–µ–Ї) –±–µ–Ј —А–∞–Ј–≤–Є—В–Є—П —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є —В–∞—Е–Є–Ї–∞—А–і–Є–Є;
• –≤–µ–љ–Њ–Ј–љ–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П (—Г–≤–µ–ї–Є—З–µ–љ–Є–µ –µ–Љ–Ї–Њ—Б—В–Є –≤–µ–љ–Њ–Ј–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–µ–і–љ–∞–≥—А—Г–Ј–Ї–Є);
• –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ –і–Є–ї–∞—В–∞—Ж–Є–Є –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤ (–Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П);
• –Њ–±—А–∞—В–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤ (–Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П) –Є —Б—В–µ–љ–Ї–Є –∞—А—В–µ—А–Є–є –Є –∞—А—В–µ—А–Є–Њ–ї;
• –Ї–Њ—А–Њ–љ–∞—А–љ–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П;
• –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ —А–µ–њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ—Л—Е –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Л—Е –∞—А–Є—В–Љ–Є–є (–Ї–∞—А–і–Є–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П);
• –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є–µ —А–∞–Ј–≤–Є—В–Є—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї –љ–Є—В—А–∞—В–∞–Љ –Є –њ–Њ—В–µ–љ—Ж–Є—А–Њ–≤–∞–љ–Є–µ –≤–∞–Ј–Њ–і–Є–ї–∞—В–Є—А—Г—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–Є—В—А–∞—В–Њ–≤;
• —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Ј–∞–і–µ—А–ґ–Ї–Є –љ–∞—В—А–Є—П –Є –≤–Њ–і—Л, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Ї–∞–ї–Є—П.
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Є–Р–Я–§ –Њ—Б–љ–Њ–≤–∞–љ–∞ –љ–∞ —Е–Є–Љ–Є—З–µ—Б–Ї–Њ–є —Б—В—А—Г–Ї—В—Г—А–µ —З–∞—Б—В–Є –Љ–Њ–ї–µ–Ї—Г–ї—Л, —Б–≤—П–Ј—Л–≤–∞—О—Й–µ–є—Б—П —Б –Р–Я–§. –Я—А–µ–њ–∞—А–∞—В—Л –њ–Њ–і—А–∞–Ј–і–µ–ї—П—О—В –љ–∞ 3 –≥—А—Г–њ–њ—Л – –Є–Р–Я–§, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–і–µ—А–ґ–∞—В:
• —Б—Г–ї—М—Д–≥–Є–і—А–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (–Ї–∞–њ—В–Њ–њ—А–Є–ї);
• –Ї–∞—А–±–Њ–Ї—Б–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г –Є–ї–Є –Ї–∞—А–±–Њ–Ї—Б–Є–∞–ї–Ї–Є–ї–і–Є–њ–µ–њ—В–Є–і—Л (—Н–љ–∞–ї–∞–њ—А–Є–ї, –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї, —А–∞–Љ–Є–њ—А–Є–ї, –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї, —Ж–Є–ї–∞–Ј–∞–њ—А–Є–ї, –±–µ–љ–∞–Ј–µ–њ—А–Є–ї, –Ї–≤–Є–љ–∞–њ—А–Є–ї, —В—А–∞–љ–і–Њ–ї–∞–њ—А–Є–ї, —Б–њ–Є—А–∞–њ—А–Є–ї);
• —Д–Њ—Б—Д–Њ—А–Є–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (—Д–Њ–Ј–Є–љ–Њ–њ—А–Є–ї).
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –љ–µ–Ї–Њ—В–Њ—А—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —Д–∞—А–Љ–∞–Ї–Њ–Ї–Є–љ–µ—В–Є–Ї–Є –Є–Р–Я–§: –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М, –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є—П (–і–µ–є—Б—В–≤—Г–µ—В –њ—А–µ–њ–∞—А–∞—В —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ, —В.–µ. —П–≤–ї—П–µ—В—Б—П –ї–Є –Њ–љ –∞–Ї—В–Є–≤–љ—Л–Љ –≤–µ—Й–µ—Б—В–≤–Њ–Љ –Є–ї–Є –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–Њ–Љ, –Ї–Њ—В–Њ—А–Њ–µ –њ—А–µ–≤—А–∞—Й–∞–µ—В—Б—П –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –≤ –∞–Ї—В–Є–≤–љ—Л–µ –Љ–µ—В–∞–±–Њ–ї–Є—В—Л), –њ—Г—В–Є —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М —В–Њ—А–Љ–Њ–ґ–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–Я–§.
–Т—Б–µ –Ї–∞—А–±–Њ–Ї—Б–Є–∞–ї–Ї–Є–ї–і–Є–њ–µ–њ—В–Є–і—Л –њ—А–µ–≤–Њ—Б—Е–Њ–і—П—В –Ї–∞–њ—В–Њ–њ—А–Є–ї –њ–Њ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –і–µ–є—Б—В–≤–Є—П, —В–∞–Ї –Ї–∞–Ї –Є–Љ–µ—О—В –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–є –њ–µ—А–Є–Њ–і –њ–Њ–ї—Г–≤—Л–≤–µ–і–µ–љ–Є—П –Є –њ–Њ—Н—В–Њ–Љ—Г –њ—А–Є–Љ–µ–љ—П—О—В—Б—П 1–2 —А–∞–Ј–∞/—Б—Г—В. –Ю–љ–Є –Љ–µ–љ—М—И–µ —Б–≤—П–Ј—Л–≤–∞—О—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є –≤ –њ—А–Њ–і—Г–Ї—В–∞—Е –њ–Є—В–∞–љ–Є—П, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Є—Е –Љ–Њ–ґ–љ–Њ –њ—А–Є–љ–Є–Љ–∞—В—М –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –њ—А–Є–µ–Љ–∞ –њ–Є—Й–Є. –Т—Б–µ –Ї–∞—А–±–Њ–Ї—Б–Є–∞–ї–Ї–Є–ї–і–Є–њ–µ–њ—В–Є–і—Л, –Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ –ї–Є–Ј–Є–љ–Њ–њ—А–Є–ї–∞, —П–≤–ї—П—О—В—Б—П –њ—А–Њ–ї–µ–Ї–∞—А—Б—В–≤–∞–Љ–Є, —В.–µ. –і–ї—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –∞–Ї—В–Є–≤–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ —В—А–µ–±—Г–µ—В—Б—П –±–Є–Њ—В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є—П —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ –њ–µ—З–µ–љ–Є. –Ш–Ј —Н—В–Њ–≥–Њ —Б–ї–µ–і—Г–µ—В, —З—В–Њ –і–∞–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —Б –Њ—Б—В–Њ—А–Њ–ґ–љ–Њ—Б—В—М—О –њ—А–Є–Љ–µ–љ—П—В—М —Г –ї–Є—Ж —Б –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О, –∞ —В–∞–Ї–ґ–µ —В–Њ, —З—В–Њ –Њ–љ–Є –љ–µ –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤ —Б–Ї–Њ—А–Њ–є –њ–Њ–Љ–Њ—Й–Є.
–†–∞–Љ–Є–њ—А–Є–ї (–Ф–Є–ї–∞–њ—А–µ–ї®) – –њ—А–µ–њ–∞—А–∞—В –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –Њ–±–ї–∞–і–∞—О—Й–Є–є –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —Б—А–Њ–і—Б—В–≤–Њ–Љ –Ї —В–Ї–∞–љ–µ–≤–Њ–Љ—Г –Р–Я–§ –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, –Њ—А–≥–∞–љ–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Я—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б –њ—А–Є–µ–Љ–Њ–Љ –њ–Є—Й–Є –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –µ–≥–Њ –∞–±—Б–Њ—А–±—Ж–Є—О. –Т –њ–µ—З–µ–љ–Є –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ—А–µ–≤—А–∞—Й–µ–љ–Є–µ –≤ —А–∞–Љ–Є–њ—А–Є–ї–∞—В, –Ї–Њ—В–Њ—А—Л–є —П–≤–ї—П–µ—В—Б—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ—Л–Љ –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–Љ (–≤ 6 —А–∞–Ј –∞–Ї—В–Є–≤–љ–µ–µ –Є–љ–≥–Є–±–Є—А—Г–µ—В –Р–Я–§, —З–µ–Љ —А–∞–Љ–Є–њ—А–Є–ї). –Т—Л–≤–Њ–і–Є—В—Б—П –≥–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ –њ–Њ—З–Ї–∞–Љ–Є (60%). –І–∞—Б—В–Є—З–љ–Њ (40%) —Н–Ї—Б–Ї—А–µ—В–Є—А—Г–µ—В—Б—П —З–µ—А–µ–Ј –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л–є —В—А–∞–Ї—В [2]. –†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ–Љ—Л–µ –і–Њ–Ј—Л —А–∞–Љ–Є–њ—А–Є–ї–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 1. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 60 –ї–µ—В —Б—В–∞—А—В–Њ–≤–∞—П –і–Њ–Ј–∞ –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –Є–Ј —Г–Ї–∞–Ј–∞–љ–љ—Л—Е.
–Є–Р–Я–§ –Њ–±–ї–∞–і–∞—О—В –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –љ–µ–±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ъ –Њ—Б–љ–Њ–≤–љ—Л–Љ –Є–Ј –љ–Є—Е –Њ—В–љ–Њ—Б—П—В—Б—П: –≥–Є–њ–Њ—В–µ–љ–Ј–Є—П, –≥–Є–њ–µ—А–Ї–∞–ї–Є–µ–Љ–Є—П, –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Ї—А–µ–∞—В–Є–љ–Є–љ–∞, —Б—Г—Е–Њ–є –Ї–∞—И–µ–ї—М, –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–µ —А–µ–∞–Ї—Ж–Є–Є. –У–Є–њ–Њ—В–µ–љ–Ј–Є—П –љ–µ—А–µ–і–Ї–Њ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –љ–∞ —Д–Њ–љ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, –±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Љ–µ–і–ї–µ–љ–љ—Л—Е –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ –Є —В.–і. –Є–ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е –Р–Ф –љ–µ –±–Њ–ї–µ–µ 110/70 –Љ–Љ —А—В.—Б—В., –Є –Њ–±—Л—З–љ–Њ –љ–Њ—Б–Є—В –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –У–Є–њ–µ—А–Ї–∞–ї–Є–µ–Љ–Є—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –≤—Б—В—А–µ—З–∞–µ—В—Б—П –љ–∞ —Д–Њ–љ–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Ї–∞–ї–Є–є—Б–±–µ—А–µ–≥–∞—О—Й–Є—Е –і–Є—Г—А–µ—В–Є–Ї–Њ–≤, –∞ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Б –≤–љ–µ–њ–Њ—З–µ—З–љ—Л–Љ –њ—Г—В–µ–Љ –≤—Л–≤–µ–і–µ–љ–Є—П —Б–љ–Є–ґ–∞–µ—В –Њ–≥—А–∞–љ–Є—З–µ–љ–Є—П –љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є–Р–Я–§ —Г –±–Њ–ї—М–љ—Л—Е —Б –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О. –°—Г—Е–Њ–є –Ї–∞—И–µ–ї—М –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е. –°—З–Є—В–∞–µ—В—Б—П, —З—В–Њ –Њ–љ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –≤ –Њ—В–≤–µ—В –љ–∞ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –±—А–∞–і–Є–Ї–Є–љ–Є–љ–∞ –≤ —Б–ї–Є–Ј–Є—Б—В–Њ–є –і—Л—Е–∞—В–µ–ї—М–љ—Л—Е –њ—Г—В–µ–є.
–Я—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Є–Р–Я–§:
• –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–µ —Б—В–µ–љ–Њ–Ј—Л –њ–Њ—З–µ—З–љ—Л—Е –∞—А—В–µ—А–Є–є –Є–ї–Є —Б—В–µ–љ–Њ–Ј –∞—А—В–µ—А–Є–Є –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–є –њ–Њ—З–Ї–Є;
• —В—П–ґ–µ–ї—Л–є –∞–Њ—А—В–∞–ї—М–љ—Л–є –Є–ї–Є –Љ–Є—В—А–∞–ї—М–љ—Л–є —Б—В–µ–љ–Њ–Ј, –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–∞—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є—П;
• –Є—Б—Е–Њ–і–љ–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є—П (–Р–Ф –Љ–µ–љ–µ–µ 100/60 –Љ–Љ —А—В.—Б—В.);
• –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В—М, –ї–∞–Ї—В–∞—Ж–Є—П.
–Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –Р–У
—Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞–Љ–Є–њ—А–Є–ї–∞
–Э–∞–Ј–љ–∞—З–µ–љ–Є–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ –ї–Є—Ж–∞–Љ —Б –≤—Л—Б–Њ–Ї–Є–Љ –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –Р–Ф –њ—А–Є–≤–Њ–і–Є—В –Ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Р–У. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ PHARAO [3] –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 1008 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 50, –љ–Њ –Љ–Њ–ї–Њ–ґ–µ 85 –ї–µ—В —Б –њ—А–µ–і–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є (–≤—Л—Б–Њ–Ї–Є–Љ –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ –Р–Ф). –Ш–Ј –љ–Є—Е 505 —З–µ–ї–Њ–≤–µ–Ї –њ–Њ–ї—Г—З–∞–ї–Є —В–µ—А–∞–њ–Є—О —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ –≤ –і–Њ–Ј–µ 5 –Љ–≥ 1 —А–∞–Ј/—Б—Г—В. —Г—В—А–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 3 –ї–µ—В, –∞ 503 –њ–∞—Ж–Є–µ–љ—В–∞ –і–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –љ–µ –њ—А–Є–љ–Є–Љ–∞–ї–Є. –Т –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ –Р–У —А–∞–Ј–≤–Є–ї–∞—Б—М —Г 155 (30,7%) —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Б–Њ—Б—В–∞–≤–Є–ї 42,9% (–Р–У —А–∞–Ј–≤–Є–ї–∞—Б—М —Г 216 —З–µ–ї–Њ–≤–µ–Ї).
–Ю–њ—Л—В –ї–µ—З–µ–љ–Є—П –Р–У —Б –њ–Њ–Љ–Њ—Й—М—О —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–Р–Я–§ –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г 50–75% –±–Њ–ї—М–љ—Л—Е —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є –Р–У. –Ъ–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–Њ–≤—Л—И–∞–µ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–Р–Я–§ –і–Њ 75–90%. –У–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є–Р–Я–§ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–µ–є, –Њ–і–љ–∞–Ї–Њ —А–∞–Ј–≤–Є—В–Є—П —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є —В–∞—Е–Є–Ї–∞—А–і–Є–Є –љ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П, —В–∞–Ї –Ї–∞–Ї –±–ї–Њ–Ї–Є—А—Г–µ—В—Б—П –≤—Л–±—А–Њ—Б –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–Њ–≤. –І–°–°, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Њ—Б—В–∞–µ—В—Б—П –љ–µ–Є–Ј–Љ–µ–љ–љ–Њ–є.
–Т –Њ—В–ї–Є—З–Є–µ –Њ—В –і–Є—Г—А–µ—В–Є–Ї–Њ–≤ –Є b––∞–і—А–µ–љ–Њ–±–ї–Њ–Ї–∞—В–Њ—А–Њ–≤ –Є–Р–Я–§, –Ї–∞–Ї –Є –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Ї–∞–ї—М—Ж–Є—П, –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —Г–≥–ї–µ–≤–Њ–і–љ—Л–є –Њ–±–Љ–µ–љ, –ї–Є–њ–Є–і–љ—Л–є —Б–Њ—Б—В–∞–≤ –Ї—А–Њ–≤–Є –Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Љ–Њ—З–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, —В.–µ. –љ–µ –∞–Ї—В–Є–≤–Є—А—Г—О—В —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –°–°–Ч, –њ–Њ—Н—В–Њ–Љ—Г –µ—Б—В—М –Њ—Б–љ–Њ–≤–∞–љ–Є—П –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–Р–Я–§. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Р–Я–§, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л–µ –≤ —В–µ—З–µ–љ–Є–µ –і–Њ–ї–≥–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є, –Ј–∞–Љ–µ–і–ї—П—О—В —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –Ї–ї—Г–±–Њ—З–Ї–Њ–≤–Њ–є —Д–Є–ї—М—В—А–∞—Ж–Є–Є (–°–Ъ–§) —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є –Є –і—А—Г–≥–Є–Љ–Є –і–Є—Д—Д—Г–Ј–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–Њ—З–µ–Ї, –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—П —А–∞–Ј–≤–Є—В–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–•–Я–Э). –Є–Р–Я–§ —Б —Г—Б–њ–µ—Е–Њ–Љ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П –њ—А–Є –ї–µ—З–µ–љ–Є–Є —А–µ–љ–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –Р–У, –Њ–і–љ–∞–Ї–Њ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ—Л –њ—А–Є –љ–∞–ї–Є—З–Є–Є –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є—Е —Б—В–µ–љ–Њ–Ј–Њ–≤ –њ–Њ—З–µ—З–љ—Л—Е –∞—А—В–µ—А–Є–є –Є–ї–Є —Б—В–µ–љ–Њ–Ј–∞ –∞—А—В–µ—А–Є–Є –µ–і–Є–љ—Б—В–≤–µ–љ–љ–Њ–є –њ–Њ—З–Ї–Є –Є–Ј––Ј–∞ –Њ–њ–∞—Б–љ–Њ—Б—В–Є —Б–љ–Є–ґ–µ–љ–Є—П —Б—Г–Љ–Љ–∞—А–љ–Њ–є –°–Ъ–§ –Є —А–∞–Ј–≤–Є—В–Є—П –∞–Ј–Њ—В–µ–Љ–Є–Є.
–Т –њ–Њ—Б—В—А–µ–≥–Є—Б—В—А–∞—Ж–Є–Њ–љ–љ–Њ–Љ –Њ—В–Ї—А—Л—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CARE [4] –Є–Ј—Г—З–∞–ї–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —А–∞–Љ–Є–њ—А–Є–ї–∞ –≤ –Њ–±—Л—З–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. –Т 8––љ–µ–і–µ–ї—М–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 11 000 –±–Њ–ї—М–љ—Л—Е —Б –Р–У 1–2 —Б—В–µ–њ–µ–љ–Є –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 18 –і–Њ 75 –ї–µ—В. –†–∞–Љ–Є–њ—А–Є–ї –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –≤ —Б—В–∞—А—В–Њ–≤–Њ–є –і–Њ–Ј–µ 2,5 –Љ–≥ 1 —А–∞–Ј/—Б—Г—В. —Б —В–Є—В—А–Њ–≤–∞–љ–Є–µ–Љ –і–Њ–Ј—Л —Б —Ж–µ–ї—М—О –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Ж–µ–ї–µ–≤–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф –і–Њ 10 –Љ–≥/—Б—Г—В. (4 –љ–µ–і.), –Ј–∞—В–µ–Љ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П —В–µ—А–∞–њ–Є—П (4 –љ–µ–і.). –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Њ—Ж–µ–љ–Є–≤–∞–ї–Є —Г 8261 –њ–∞—Ж–Є–µ–љ—В–∞. –†–∞–Љ–Є–њ—А–Є–ї —Б–љ–Є–ґ–∞–ї —Б–Є—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф (–°–Р–Ф) –Є –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–µ –Р–Ф (–Ф–Р–Ф) –љ–∞ 13%. –Э–∞ –ї–µ—З–µ–љ–Є–µ –Њ—В–≤–µ—В–Є–ї–Є 86% –±–Њ–ї—М–љ—Л—Е —Б–Є—Б—В–Њ–ї–Њ––і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є. –І–∞—Б—В–Њ—В–∞ –Њ—В–≤–µ—В–∞ –±—Л–ї–∞ —Б–∞–Љ–Њ–є –≤—Л—Б–Њ–Ї–Њ–є —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є (87,2%), —Б–∞–Љ–Њ–є –љ–Є–Ј–Ї–Њ–є – —Г –∞—Д—А–Њ–∞–Љ–µ—А–Є–Ї–∞–љ—Ж–µ–≤ (81,2%). –Э–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —П–≤–ї–µ–љ–Є—П –±—Л–ї–Є –ї–µ–≥–Ї–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є, —З–∞—Б—В–Њ—В–∞ –Ї–∞—И–ї—П –љ–µ –њ—А–µ–≤—Л—Б–Є–ї–∞ 3%.
–≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Р–У –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ –≥–Є–њ–µ—А—В—А–Њ—Д–Є—П –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–У–Ы–Ц) —П–≤–ї—П–µ—В—Б—П —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–°–°–Ю). –Ґ–∞–Ї, —Г –ї–Є—Ж —Б –Р–У –њ—А–Є –љ–∞–ї–Є—З–Є–Є –У–Ы–Ц —З–∞—Б—В–Њ—В–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь) —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≤ 3 —А–∞–Ј–∞, –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–Љ–µ—А—В–Є – –≤ 3–5 —А–∞–Ј, —Б–ї–Њ–ґ–љ—Л—Е –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤—Л—Е –∞—А–Є—В–Љ–Є–є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–•–°–Э) – –≤ 5 —А–∞–Ј. –Ю—В–Љ–µ—З–∞–µ—В—Б—П –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –≤—Б–ї–µ–і—Б—В–≤–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–Є—Ж–∞–Љ–Є, –Є–Љ–µ—О—Й–Є–Љ–Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –Р–Ф –±–µ–Ј –У–Ы–Ц. –Ш–Љ–µ–љ–љ–Њ –њ–Њ—Н—В–Њ–Љ—Г —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є–Р–Я–§, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —А–∞–Љ–Є–њ—А–Є–ї–∞, –≤—Л–Ј—Л–≤–∞—В—М —А–µ–≥—А–µ—Б—Б –У–Ы–Ц —П–≤–ї—П–µ—В—Б—П –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–Љ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П HYCAR, RACE) [5,6].
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Р–Я–§ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є (–≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤ –њ–Њ—Б—В–Є–љ—Д–∞—А–Ї—В–љ–Њ–Љ –њ–µ—А–Є–Њ–і–µ)
–Ю–±–Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–Р–Я–§ –і–ї—П –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О —П–≤–Є–ї–Њ—Б—М –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–Є—Е –њ—А–Є –•–°–Э, —Б–≤—П–Ј–∞–љ–љ–Њ–µ —Б –≤–µ–і—Г—Й–µ–є —А–Њ–ї—М—О –∞–Ї—В–Є–≤–∞—Ж–Є–Є –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ—Л—Е —Б–Є—Б—В–µ–Љ (–†–Р–Р–°, –°–Р–°). –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї—А—Г–њ–љ—Л—Е –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ї–∞–Ј–∞–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–∞–Ї —Б —В—П–ґ–µ–ї–Њ–є –•–°–Э, —В–∞–Ї –Є —Б —Г–Љ–µ—А–µ–љ–љ–Њ–є, –ї–µ–≥–Ї–Њ–є –Є –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є. –®–Є—А–Њ–Ї–Њ–Љ–∞—Б—И—В–∞–±–љ—Л–µ –Є—Б–њ—Л—В–∞–љ–Є—П, –Њ—Е–≤–∞—В—Л–≤–∞–≤—И–Є–µ —В—Л—Б—П—З–Є –±–Њ–ї—М–љ—Л—Е, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ —А–∞–Ј–ї–Є—З–Є—П –≤ –њ—А–Њ—В–Њ–Ї–Њ–ї–∞—Е, –Ї—А–Є—В–µ—А–Є—П—Е –≤–Ї–ї—О—З–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В–µ–њ–µ–љ—П—Е –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є, –і–Њ–Ј–∞—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞–Ј–љ—Л—Е –Є–Р–Я–§, –њ–Њ–Ї–∞–Ј–∞–ї–Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –≤—Б–µ–≥–Њ —Н—В–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–µ —В–Њ–ї—М–Ї–Њ —Г–ї—Г—З—И–∞—В—М —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є–µ, –љ–Њ –Є –њ–Њ–≤—Л—И–∞—В—М –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э. –Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П SAVE [7] –Є SOLVD prevention [8] –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Є–Р–Я–§ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –•–°–Э (—Г –±–Њ–ї—М–љ—Л—Е —Б –ї–µ–≤–Њ–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є, —Б–љ–Є–ґ–µ–љ–љ–Њ–є —Д—А–∞–Ї—Ж–Є–µ–є –≤—Л–±—А–Њ—Б–∞ (–§–Т), –љ–Њ –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞—Б—В–Њ–є–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є) –Ї–∞–њ—В–Њ–њ—А–Є–ї –Є —Н–љ–∞–ї–∞–њ—А–Є–ї –Ј–∞–Љ–µ–і–ї—П—О—В –љ–∞ 37% –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є.
–Я—А–Є –Ш–Ь –њ—А–Њ–Є—Б—Е–Њ–і—П—В –Ї–∞–Ї –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ (–≥–µ–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Є–µ –Є —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ), —В–∞–Ї –Є –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П, –њ—А–Є–≤–Њ–і—П—Й–Є–µ –Ї —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—О —Б–µ—А–і—Ж–∞. –Э–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Ш–Ь –њ—А–Є–≤–Њ–і—П—В –Ї –њ–Њ–≤—Л—И–µ–љ–Є—О –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –°–Р–° –Є –†–Р–Р–°, –њ—А–Є —Н—В–Њ–Љ –≤ –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П –Љ–Є–Њ–Ї–∞—А–і–Є–∞–ї—М–љ–∞—П –†–Р–Р–°. –£–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II –њ—А–Є–≤–Њ–і–Є—В –Ї –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є, –њ–Њ–≤—Л—И–µ–љ–Є—О –њ–Њ—Б—В–љ–∞–≥—А—Г–Ј–Ї–Є, —З—В–Њ —Б–Њ–Ј–і–∞–µ—В —Г—Б–ї–Њ–≤–Є—П –і–ї—П —А–∞—Б—И–Є—А–µ–љ–Є—П –Ј–Њ–љ—Л –љ–µ–Ї—А–Њ–Ј–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –≤ –Ї–Є—Б–ї–Њ—А–Њ–і–µ, —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–≤—В–Њ—А–љ—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є, —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Є –∞—А–Є—В–Љ–Є–є. –Я—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–∞ II –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Є —Д–Є–±—А–Њ–Ј—Г –Љ–Є–Њ–Ї–∞—А–і–∞. –Ґ–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є–µ –Њ—Б–љ–Њ–≤–∞–љ–Є—П –і–ї—П –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–Р–Я–§ —Б —Ж–µ–ї—М—О –њ—А–µ–і–Њ—В–≤—А–∞—Й–µ–љ–Є—П –њ–Њ—Б—В–Є–љ—Д–∞—А–Ї—В–љ–Њ–≥–Њ —А–µ–Љ–Њ–і–µ–ї–Є—А–Њ–≤–∞–љ–Є—П –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ (–Ы–Ц) –Є, –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ —Б—З–µ—В–µ, —Г–ї—Г—З—И–µ–љ–Є—П –њ—А–Њ–≥–љ–Њ–Ј–∞ –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є—Б–њ—Л—В–∞–љ–Є—П–Љ–Є.
–Я–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ AIRE [9] –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Є–Р–Я–§ –±–Њ–ї—М–љ—Л–Љ —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –•–°–Э II–III –§–Ъ –њ–Њ—Б–ї–µ –Њ—Б—В—А–Њ–≥–Њ –Ш–Ь (–Ю–Ш–Ь). –°—А–∞–≤–љ–Є–≤–∞–ї—Б—П —Н—Д—Д–µ–Ї—В —А–∞–Љ–Є–њ—А–Є–ї–∞ (5–10 –Љ–≥/—Б—Г—В., 1006 –±–Њ–ї—М–љ—Л—Е) –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ (1000 –±–Њ–ї—М–љ—Л—Е) –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є —Б 3–10 –і–љ—П –Њ—В –љ–∞—З–∞–ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ –Ї —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ю–Ш–Ь. –Я–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П –≤ —Б—А–µ–і–љ–µ–Љ —Б–Њ—Б—В–∞–≤–Є–ї 15 –Љ–µ—Б. –Т –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ —А–Є—Б–Ї –Њ–±—Й–µ–є —Б–Љ–µ—А—В–Є —Б–љ–Є–Ј–Є–ї—Б—П –љ–∞ 27%, –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П —В—П–ґ–µ–ї–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –љ–Њ —А–Є—Б–Ї –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –Ш–Ь –љ–µ —Г–Љ–µ–љ—М—И–∞–ї—Б—П. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ —Б–Љ–µ—А—В–Є (–љ–∞ 29%) –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–ґ–µ –њ–Њ—Б–ї–µ 30 –і–љ–µ–є –ї–µ—З–µ–љ–Є—П —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ.
–Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –Є–Р–Я–§ –њ—А–Є –Ш–С–°
–Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Є–Р–Я–§ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–∞—Б—И–Є—А–µ–љ—Л. –Т—Л—П–≤–ї–µ–љ—Л –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –Є–Р–Я–§. –Я—А–µ–њ–∞—А–∞—В—Л —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ш–С–°. –Ґ–µ–Њ—А–µ—В–Є—З–µ—Б–Ї–Є —Б—Г—Й–µ—Б—В–≤—Г—О—В 2 –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Є–Р–Я–§:
1. –Я—А—П–Љ–∞—П –Ї–Њ—А–Њ–љ–∞—А–Њ–і–Є–ї–∞—В–∞—Ж–Є—П –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–Њ–≤ (–±—А–∞–і–Є–Ї–Є–љ–Є–љ, —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ—Л–є —Д–∞–Ї—В–Њ—А —А–µ–ї–∞–Ї—Б–∞—Ж–Є–Є –Є –і—А.) –Є —Г–Љ–µ–љ—М—И–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–Њ–≤ (–∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ II, –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ—Л –Є –і—А.) –≤ —Б—В–µ–љ–Ї–µ –Ї–Њ—А–Њ–љ–∞—А–љ—Л—Е –∞—А—В–µ—А–Є–є, –њ—А–Є–≤–Њ–і—П—Й–∞—П –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –і–Њ—Б—В–∞–≤–Ї–Є –Ї–Є—Б–ї–Њ—А–Њ–і–∞ –Є –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –Ї –Љ–Є–Њ–Ї–∞—А–і—Г.
2. –°–Є—Б—В–µ–Љ–љ–∞—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П (—Б–љ–Є–ґ–µ–љ–Є–µ –њ—А–µ–і– –Є –њ–Њ—Б—В–љ–∞–≥—А—Г–Ј–Ї–Є) –±–µ–Ј —А–∞–Ј–≤–Є—В–Є—П —А–µ—Д–ї–µ–Ї—В–Њ—А–љ–Њ–є —В–∞—Е–Є–Ї–∞—А–і–Є–Є, –≤—Л–Ј—Л–≤–∞—О—Й–∞—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ–Њ—В—А–µ–±–љ–Њ—Б—В–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –≤ –Ї–Є—Б–ї–Њ—А–Њ–і–µ –Є –Љ–µ—В–∞–±–Њ–ї–Є—В–∞—Е.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –љ–∞–±–ї—О–і–µ–љ–Є–є –љ–µ–Њ–і–љ–Њ–Ј–љ–∞—З–љ—Л. –Ь–Њ–љ–Њ—В–µ—А–∞–њ–Є—П –Є–Р–Я–§, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–і–µ–Ї–≤–∞—В–љ–Њ–≥–Њ –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –С–Њ–ї–µ–µ –Њ–њ—В–Є–Љ–Є—Б—В–Є—З–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –њ–Њ—Б–ї–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є–Р–Я–§ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–Р–Я–§ –њ–Њ—В–µ–љ—Ж–Є—А—Г–µ—В –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л –Є–Ј–Њ—Б–Њ—А–±–Є–і–∞ –і–Є–љ–Є—В—А–∞—В–∞ –Є –љ–Є—Д–µ–і–Є–њ–Є–љ–∞. –Р–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є–Р–Я–§ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≤ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є —З–Є—Б–ї–∞ –њ—А–Є—Б—В—Г–њ–Њ–≤ —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –≤ —Б—Г—В–Ї–Є, —З–Є—Б–ї–∞ —Н–њ–Є–Ј–Њ–і–Њ–≤ –±–Њ–ї–µ–≤–Њ–є –Є –±–µ–Ј–±–Њ–ї–µ–≤–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –≤ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–Љ —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Є–Ј–Њ–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —Г –ї–Є—Ж —Б—В–∞—А—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ.
–Х—Й–µ –≤ –њ—А–Њ—И–ї–Њ–Љ –≤–µ–Ї–µ –љ–∞–Љ–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ [10], —З—В–Њ –Є–Р–Я–§ (—Н–љ–∞–ї–∞–њ—А–Є–ї –≤ –і–Њ–Ј–µ 5–10 –Љ–≥/c—Г—В. –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –≥–Є–і—А–Њ—Е–ї–Њ—А–Њ—В–Є–∞–Ј–Є–і–Њ–Љ 3,125–6,25 –Љ–≥/c—Г—В., –Ї–≤–Є–љ–∞–њ—А–Є–ї–Њ–Љ 5–10 –Љ–≥/c—Г—В., —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ 2,5–5 –Љ–≥/c—Г—В.) —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –±–Њ–ї—М–љ—Л—Е –Ш–С–° —Б–Њ —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П II–III –§–Ъ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –љ–∞–ї–Є—З–Є—П –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є—П –Р–У, –±–µ–Ј–±–Њ–ї–µ–≤–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П. –Ф–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є–Р–Я–§ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–∞—В—М –≤ —Б–ї–µ–і—Г—О—Й–Є—Е —А–∞–Ј–Њ–≤—Л—Е –і–Њ–Ј–∞—Е: 2,5 –Љ–≥ –њ–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ –і–ї—П —Н–љ–∞–ї–∞–њ—А–Є–ї–∞ –Є –Ї–≤–Є–љ–∞–њ—А–Є–ї–∞ –Є 1,25 –Љ–≥ – –і–ї—П —А–∞–Љ–Є–њ—А–Є–ї–∞ (–њ—А–Є —Г—Б–ї–Њ–≤–Є–Є —Б–љ–Є–ґ–µ–љ–Є—П –°–Р–Ф –±–Њ–ї–µ–µ —З–µ–Љ –љ–∞ 10 –Љ–Љ —А—В.—Б—В.) 2 —А–∞–Ј–∞/—Б—Г—В. —З–µ—А–µ–Ј 12 —З. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –і–Є–љ–∞–Љ–Є–Ї–Є –Р–Ф –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞–і–Њ —Г–≤–µ–ї–Є—З–Є—В—М –≤ 2 —А–∞–Ј–∞.
–Т—Л—Б–Ї–∞–Ј—Л–≤–∞–ї–Є—Б—М –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є—П, —З—В–Њ –Є–Р–Я–§ —Б –≤—Л—Б–Њ–Ї–Њ–є —Б–њ–µ—Ж–Є—Д–Є—З–љ–Њ—Б—В—М—О –Ї —В–Ї–∞–љ–µ–≤—Л–Љ –Р–Я–§, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –Є —А–∞–Љ–Є–њ—А–Є–ї, —Б–њ–Њ—Б–Њ–±–љ—Л —Г–ї—Г—З—И–Є—В—М —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ —Н–љ–і–Њ—В–µ–ї–Є—П, –Ј–∞–Љ–µ–і–ї–Є—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є HOPE [11] –±—Л–ї–∞ –і–Њ–Ї–∞–Ј–∞–љ–∞ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–∞—П –њ–Њ–ї—М–Ј–∞ —А–∞–Љ–Є–њ—А–Є–ї–∞ —Г –ї–Є—Ж —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –°–°–Ю. –Я–∞—Ж–Є–µ–љ—В—Л 55 –ї–µ—В –Є —Б—В–∞—А—И–µ (n=9297) —Б –°–°–Ч –Є–ї–Є —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ (–°–Ф) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Њ–і–љ–Є–Љ –і—А—Г–≥–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞, –љ–Њ –±–µ–Ј –•–°–Э –Є —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–µ–є –Ы–Ц –±—Л–ї–Є —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ—Л –ї–Є–±–Њ –≤ –≥—А—Г–њ–њ—Г –њ—А–Є–µ–Љ–∞ —А–∞–Љ–Є–њ—А–Є–ї–∞ 10 –Љ–≥/—Б—Г—В., –ї–Є–±–Њ –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г (–њ—А–Є–µ–Љ –њ–ї–∞—Ж–µ–±–Њ). –Я–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П –Є –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї –Њ–Ї–Њ–ї–Њ 5 –ї–µ—В. –†–∞–Љ–Є–њ—А–Є–ї —Б–љ–Є–Ј–Є–ї –љ–∞ 22% –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–є —А–Є—Б–Ї –Ш–Ь, –Є–љ—Б—Г–ї—М—В–∞ –Є —Б–Љ–µ—А—В–Є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ. –Ю–±—А–∞—Й–∞–µ—В –љ–∞ —Б–µ–±—П –≤–љ–Є–Љ–∞–љ–Є–µ –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ф —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–°–Р–Ф —Б–љ–Є–Ј–Є–ї–Њ—Б—М –љ–∞ 2 –Љ–Љ —А—В.—Б—В., –∞ –Ф–Р–Ф – –љ–∞ 3 –Љ–Љ —А—В.—Б—В.). –Я–Њ—Н—В–Њ–Љ—Г —Б—В–Њ–ї—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В –ї–µ—З–µ–љ–Є—П —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —А–Є—Б–Ї—Г –°–°–Ю –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—К—П—Б–љ–µ–љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ – –љ–∞–Є–±–Њ–ї–µ–µ –≤–µ—А–Њ—П—В–љ–Њ, —З—В–Њ –Њ–љ —Б–≤—П–Ј–∞–љ —Б –њ—А—П–Љ—Л–Љ —В–Ї–∞–љ–µ–≤—Л–Љ –≤–ї–Є—П–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є SECURE [12], –њ—А–Њ–≤–Њ–і–Є–≤—И–µ–Љ—Б—П –≤ —А–∞–Љ–Ї–∞—Е HOPE, —Г 732 –±–Њ–ї—М–љ—Л—Е –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –≤–ї–Є—П–љ–Є–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ –љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –Ї–∞—А–Њ—В–Є–і–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞. –Я—А–Є–µ–Љ —А–∞–Љ–Є–њ—А–Є–ї–∞ –≤ –і–Њ–Ј–µ 10 –Љ–≥/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 4 –ї–µ—В —В–Њ—А–Љ–Њ–Ј–Є–ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –≤ —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є—П—Е –њ–Њ –і–∞–љ–љ—Л–Љ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–є –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є. –Ґ–Њ–ї—Й–Є–љ–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Є–љ—В–Є–Љ–∞––Љ–µ–і–Є–∞ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –љ–∞ 37% –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ. –Ф–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –њ–ї–∞—Ж–µ–±–Њ –Є —А–∞–Љ–Є–њ—А–Є–ї–∞ –≤ –і–Њ–Ј–µ 2,5 –Љ–≥/—Б—Г—В. –љ–µ –±—Л–ї–Њ. –Т HOPE –±—Л–ї–Є –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ—Л –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л —А–∞–Љ–Є–њ—А–Є–ї–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ, –∞–љ—В–Є–∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–µ –Є –∞–љ—В–Є–∞—А–Є—В–Љ–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞. –°–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ, —Б —Ж–µ–ї—М—О –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Љ–Є–њ—А–Є–ї —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–∞—В—М –±–Њ–ї—М–љ—Л–Љ —Б—В–∞—А—И–µ 55 –ї–µ—В —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –°–°–Ю –љ–∞ —Д–Њ–љ–µ –°–°–Ч –Є–ї–Є –°–Ф.
–≠—Д—Д–µ–Ї—В—Л —А–∞–Љ–Є–њ—А–Є–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є
–Ч–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –Є–љ—В–µ—А–µ—Б –≤—Л–Ј—Л–≤–∞—О—В —А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–µ–є—Б—В–≤–Є—П —А–∞–Љ–Є–њ—А–Є–ї–∞ –њ—А–Є –њ–Њ—А–∞–ґ–µ–љ–Є–Є –њ–Њ—З–µ–Ї —А–∞–Ј–ї–Є—З–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є MICRO–HOPE (–≤ —А–∞–Љ–Ї–∞—Е HOPE) [13] –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є –≤–ї–Є—П–љ–Є–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ –љ–∞ –Љ–∞–Ї—А–Њ– –Є –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –°–Ф –±–µ–Ј –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є (n=3577). –Ш—Б—Е–Њ–і–љ–Њ –Љ–Є–Ї—А–Њ–∞–ї—М–±—Г–Љ–Є–љ—Г—А–Є—П –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —Г 1140 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –Ј–∞–≤–µ—А—И–µ–љ–Њ –љ–∞ 6 –Љ–µ—Б. —А–∞–љ—М—И–µ –љ–∞–Љ–µ—З–µ–љ–љ–Њ–≥–Њ —Б—А–Њ–Ї–∞ (—З–µ—А–µ–Ј 4,5 –≥–Њ–і–∞) –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Ї–Њ–Љ–Є—В–µ—В–Њ–Љ –њ–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—О –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є, —Г—З–Є—В—Л–≤–∞—П —П–≤–љ–Њ–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ —А–∞–Љ–Є–њ—А–Є–ї–∞ –њ–µ—А–µ–і –њ–ї–∞—Ж–µ–±–Њ. –Ы–µ—З–µ–љ–Є–µ –Є–Р–Я–§ –њ—А–Є–≤–µ–ї–Њ –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–є –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є –љ–∞ 25% –Є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є – –љ–∞ 24%. –Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —Б—Г–Љ–Љ–∞—А–љ–Њ–є —З–∞—Б—В–Њ—В—Л –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (—П–≤–љ–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є, –і–Є–∞–ї–Є–Ј–∞ –Є –ї–∞–Ј–µ—А–љ–Њ–є —В–µ—А–∞–њ–Є–Є) –Њ—В–Љ–µ—З–µ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—Б–Ї–∞ –љ–∞ 16% –≤ –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞.
–Т –і—А—Г–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б–њ—Л—В–∞–љ–Є—П—Е –Є–Ј—Г—З–∞–ї–Є—Б—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —А–∞–Љ–Є–њ—А–Є–ї–∞ –њ—А–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –њ–Њ—З–µ–Ї, –љ–µ —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –°–Ф. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —А–∞–Љ–Є–њ—А–Є–ї–∞ –≤ –і–Њ–Ј–µ 1,25–5 –Љ–≥/—Б—Г—В. —Г 352 –±–Њ–ї—М–љ—Л—Е —Б –Р–У –Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–µ–є (–Ї–ї–Є—А–µ–љ—Б –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ 20–70 –Љ–ї/–Љ–Є–љ., –њ—А–Њ—В–µ–Є–љ—Г—А–Є—П –±–Њ–ї–µ–µ 1 –≥/—Б—Г—В.) –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –≤ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є REIN [14] –≤ —В–µ—З–µ–љ–Є–µ 27 –Љ–µ—Б. –Є –≤ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 36 –Љ–µ—Б. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л: 1–—О —Б–Њ—Б—В–∞–≤–Є–ї–Є –±–Њ–ї—М–љ—Л–µ —Б –њ—А–Њ—В–µ–Є–љ—Г—А–Є–µ–є –Њ—В 1 –і–Њ 2,9 –≥/—Б—Г—В., 2–—О – —Б –њ—А–Њ—В–µ–Є–љ—Г—А–Є–µ–є –±–Њ–ї–µ–µ 3 –≥/—Б—Г—В. –Э–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Є–Р–Я–§ —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ 2––є –≥—А—Г–њ–њ—Л –°–Ъ–§ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞–ї–∞—Б—М –Љ–µ–і–ї–µ–љ–љ–µ–µ –њ—А–Є —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –њ–ї–∞—Ж–µ–±–Њ (–љ–∞ 0,53 –њ—А–Њ—В–Є–≤ 0,88 –Љ–ї/–Љ–Є–љ/–Љ–µ—Б.). –Т —В–µ—З–µ–љ–Є–µ 1 –Љ–µ—Б. –њ—А–Є–µ–Љ–∞ —А–∞–Љ–Є–њ—А–Є–ї–∞ –њ—А–Њ—В–µ–Є–љ—Г—А–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –Є—Б—Е–Њ–і–љ—Л—Е –і–∞–љ–љ—Л—Е –Є –Њ—Б—В–∞–≤–∞–ї–∞—Б—М —Б—В–∞–±–Є–ї—М–љ–Њ–є –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –≤—Б–µ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –њ–ї–∞—Ж–µ–±–Њ, —Б—Г—В–Њ—З–љ–∞—П –њ—А–Њ—В–µ–Є–љ—Г—А–Є—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–µ –Є–Ј–Љ–µ–љ—П–ї–∞—Б—М. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –≤ –њ–Њ—З–µ—З–љ–Њ–є —В—А–∞–љ—Б–њ–ї–∞–љ—В–∞—Ж–Є–Є, –≥–µ–Љ–Њ–і–Є–∞–ї–Є–Ј–µ –Є —Г–і–≤–Њ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —Б—Л–≤–Њ—А–Њ—В–Њ—З–љ–Њ–≥–Њ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ –≤ –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —А–µ–ґ–µ.
–Я–Њ—Б–ї–µ –Ј–∞–≤–µ—А—И–µ–љ–Є—П REIN –њ–∞—Ж–Є–µ–љ—В—Л —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –њ—А–Њ—В–µ–Є–љ—Г—А–Є–µ–є –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –µ—Й–µ 3 –≥–Њ–і–∞, –≤—Б–µ –њ–Њ–ї—Г—З–∞–ї–Є —А–∞–Љ–Є–њ—А–Є–ї. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –њ–Њ—З–µ–Ї –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–ї–Њ –і–Њ —Б—В–∞–і–Є–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –•–Я–Э —Г 30% –±–Њ–ї—М–љ—Л—Е –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ, –∞ –≤ –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞ –љ–Њ–≤—Л—Е —Б–ї—Г—З–∞–µ–≤ –љ–µ –±—Л–ї–Њ. –°–Ъ–§ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Б–љ–Є–ґ–∞–ї–∞—Б—М –Є –≤ –≥—А—Г–њ–њ–µ —А–∞–Љ–Є–њ—А–Є–ї–∞, –Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ. –Я—А–Њ—В–µ–Є–љ—Г—А–Є—П —Г–≤–µ–ї–Є—З–Є–ї–∞—Б—М –љ–∞ 15% –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ –Є —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –љ–∞ 13% –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П —А–∞–Љ–Є–њ—А–Є–ї–Њ–Љ. –Э–∞—А–∞—Б—В–∞–љ–Є–µ –њ—А–Њ—В–µ–Є–љ—Г—А–Є–Є –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –љ–µ—Д—А–Њ–њ–∞—В–Є–Є –і–Њ —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –•–Я–Э –≤ –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —З–∞—Й–µ, —З–µ–Љ –≤ –≥—А—Г–њ–њ–µ –ї–µ—З–µ–љ–Є—П. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –і–Њ–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞–ї–Є—З–Є–µ –љ–µ—Д—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ —А–∞–Љ–Є–њ—А–Є–ї–∞ (—Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ—В–µ–Є–љ—Г—А–Є—О, –Ј–∞–Љ–µ–і–ї—П–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є –і–Њ —Б—В–∞–і–Є–Є —В–µ—А–Љ–Є–љ–∞–ї—М–љ–Њ–є –•–Я–Э).
–Ъ –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є —А–∞–Љ–Є–њ—А–Є–ї —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Є–Ј—Г—З–µ–љ–љ—Л—Е –Є–Р–Я–§. –Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –і–Њ–Ї–∞–Ј–∞–љ—Л –µ–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –≤ –ї–µ—З–µ–љ–Є–Є –Р–У, —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є, –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –°–°–Ю —Г –±–Њ–ї—М–љ—Л—Е –≥—А—Г–њ–њ—Л –≤—Л—Б–Њ–Ї–Њ–≥–Њ —А–Є—Б–Ї–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф, –∞ —В–∞–Ї–ґ–µ –≤ –Ј–∞–Љ–µ–і–ї–µ–љ–Є–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Є –љ–µ–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—Д—А–Њ–њ–∞—В–Є–Є.
–Э–µ–і–∞–≤–љ–Њ –≤ –†–§ –њ–Њ—П–≤–Є–ї—Б—П –љ–Њ–≤—Л–є –і–ґ–µ–љ–µ—А–Є–Ї –Њ—А–Є–≥–Є–љ–∞–ї—М–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —А–∞–Љ–Є–њ—А–Є–ї–∞ – –Ф–Є–ї–∞–њ—А–µ–ї® (–Ч–Р–Ю «–Т–µ—А—В–µ–Ї—Б», –°–∞–љ–Ї—В––Я–µ—В–µ—А–±—Г—А–≥, –†–Њ—Б—Б–Є—П). –≠—В–Њ –≤—Б–µ–ї—П–µ—В –љ–∞–і–µ–ґ–і—Г –љ–∞ –±–Њ–ї–µ–µ —И–Є—А–Њ–Ї–Њ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є–Р–Я–§ —А–∞–Љ–Є–њ—А–Є–ї–∞ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –°–°–Ч.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. Dzau V.J. Clinical implications for therapy: possible cardioprotective effects of ACE inhibition // Brit J Clin Pharmacol.1989. Vol. 28. –†. 183–187.
2. Opie L. Angiotensin Converting Enzyme Inhibitors. Authors’ Publishing House. 3rd Ed. 1999.
3. Luders S., Schrader J., Berger J. et al. The PHARAO study: prevention of hypertention with the angiotensin–converting enzyme inhibitor ramipril in patients with high–normal blood pressure: a prospective, randomized, controlled prevention trial of the German Hypertension League // J Hypertens. 2008. Vol. 26 (7). –†. 1487–1496.
4. Kaplan N.M. The CARE Study: a postmarketing evaluation of ramipril in 11,100 patients. The Clinical Altace Real–World Efficacy (CARE) Investigators. Clin Ther. 1996. Vol. 18 (4). –†. 658–670.
5. Livre M., Guret P., Gayet C. et al. Remissiom of left ventricular hypertrophy with ramipril independently of blood pressure changes: the HYCAR study (cardiac hypertrophy and ramipril) // Arch Mal Couer Vaiss. 1995 Feb. Vol. 88. Spec No. 2. –†. 35–42.
6. Agabiti–Rosei E., Ambrosioni E., Dal Palu C. et al. ACE inhibitor ramipril is more effective than the beta–blocker atenolol in reducing left ventricular mass in hypertension. Results of the RACE (RAmipril Cardioprotective Evaluation) study // J Hypertens. 1995. Vol. 13. –†. 1325–1334.
7. Pfeffer M.A., Braunwald E., Moye L.A., et al., on behalf of the SAVE Investigators. Effect of captopril on mortality and morbidity in patients with left ventricular dysfunction after myocardial infarction: results of the Survival and Ventricular Enlargement Trial // N Engl J Med. 1992. Vol. 327. –†. 669–677.
8. The SOLVD Investigators. Effect of enalapril on mortality and the development of heart failure in asymptomatic patients with reduced left ventricular ejection fractions // N Engl J Med. 1992. Vol. 327. –†. 685–691.
9. The Acute Infarction Ramipril Efficacy (AIRE) Investigators. Effects of ramipril on mortality and morbidity or survivors of acute myocardial infarction with clinical evidence of heart failure // Lancet. 1993. Vol. 342. –†. 821–828.
10. –Ы–∞–Ј–µ–±–љ–Є–Ї –Ы.–С., –Ф—А–Њ–Ј–і–Њ–≤–∞ –°.–Ы., –Т—С—А—В–Ї–Є–љ –Р.–Ы., –Ъ–Њ–љ–µ–≤ –Ѓ.–Т., –У–Њ–љ—З–∞—А–Њ–≤ –Ы.–§. –Р–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ–њ—А–µ–≤—А–∞—Й–∞—О—Й–µ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ // –Ґ–µ—А –∞—А—Е–Є–≤. 1996. вДЦ 4.
11. Yusuf S., Sleight P., Pogue J. et al. Effects of an angiotensin–converting–enzyme inhibitor, ramipril, on cardiovascular events in high–risk patients // N Engl J Med. 2000. Vol. 342 (3). –†. 145–153.
12. Lonn E., Yusuf S., Dzavik V. et al. Effects of ramipril and vitamin E on atherosclerosis: the study to evaluate carotid ultrasound changes in patients treated with ramipril and vitamin E (SECURE) // Circulation. 2001. Vol. 103 (7). –†. 919–925.
13. –Э–µ–∞rt Outcomes Prevention Evaluation (HOPE) Study Investigators. Effects of ramipril on cardiovascular and microvascular outcomes in people with diabetes mellitus: results of the HOPE study and MICRO–HOPE substudy // Lancet. 2000. Vol. 355. –†. 253–259.
14. The GISEN Group. Randomised placebo–controlled trial of effect of ramipril on decline in glomerular filtration rate and risk of terminal renal failure in proteinuric, non–diabetic nephropathy // Lancet. 1997. Vol. 349. –†. 1857–1863.












