Гипертоническая болезнь (ГБ) является одной из важнейших медико–социальных проблем. Повышенный уровень артериального давления (АД) вызывает поражение органов–мишеней и приводит к развитию сердечно–сосудистых осложнений (сердечной недостаточности, инфаркта миокарда, мозгового инсульта, почечной недостаточности). Артериальная гипертензия (АГ) остается причиной инвалидизации и преждевременной смертности до 30% населения развитых стран [2,3,6].
Арсенал современных антигипертензивных лекарственных средств велик. Ключевые позиции в их ряду в настоящее время занимают и блокаторы кальциевых каналов (БКК). История БКК началась в 1961 г., когда был создан верапамил – родоначальник новой группы вазоактивных препаратов. В 1969 г. был синтезирован нифедипин, давший начало самой многочисленной подгруппы БКК – производных дигидропиридина. В 80–х гг. появились пролонгированные формы верапамила и нифедипина, а в 1988 г. в рекомендациях JNC IV БКК впервые появились в ряду препаратов первого выбора для лечения АГ [5]. Пережив волну отката, в 90–е гг. БКК вновь заняли заслуженное место в качестве антигипертензивных препаратов [5,10].
Амлодипин представляет собой единственный БКК III поколения по классификации Toyo–oka T. et al. [11]. Особенности фармакокинетики амлодипина являются следствием отличий в химической структуре от его предшественника, нифедипина, и включают медленное начало действия, продолжительный эффект, высокую биодоступность и относительно малую разницу между выраженностью снижения АД на пике и в конце действия [1,7].
Целью настоящего исследования являлась оценка антигипертензивной эффективности и переносимости Веро–амлодипина в условиях суточного мониторирования АД (СМАД), исследования центральной и периферической гемодинамики под контролем ряда параметров биохимического спектра крови.
Материалы и методы
В исследование были включены 30 пациентов (11 мужчин и 19 женщин) с ГБ I и II стадии (по классификации ВОЗ), мягкого и умеренного течения. Средний возраст группы составил 46,1±10,4 (36–68) лет, продолжительность заболевания – 7,4±6,11 (3–15) лет. У 8 пациентов имелась мягкая и у 12 – умеренная АГ. Из исследования исключались пациенты с симптоматической АГ, перенесенным инфарктом миокарда либо острым нарушением мозгового кровообращения в последние 6 месяцев, клапанными пороками сердца, патологией печени и почек.
До включения в исследование в течение 7–10 дней («отмывочный» период) пациенты не получали антигипертензивной терапии. После этого назначался Веро–амлодипин (производство ЗАО «Верофарм», Россия) в суточной дозе 5 мг. Больные получали препарат с учетом индивидуальных особенностей суточного ритма АД (по данным суточного мониторирования) за 3 ч до максимального его подъема. Исходно, а также через 8 недель лечения проводилось суточное мониторирование АД (СМАД), исследование параметров центральной и периферической гемодинамики и уровень липидов крови.
СМАД проводили с помощью портативного регистратора Cardiotens (Meditech, Венгрия), осуществляющего регистрацию АД и ЧСС осциллометрическим методом. Исследование начинали в 9:00–11:00 ч. Измерения осуществлялись каждые 20 минут в дневное время (6:00–22:00) и 30 минут – в ночное время (22:00–6:00). По данным СМАД анализировали усредненные показатели систолического АД (САД), диастолического АД (ДАД), ЧСС в периоды бодрствования, сна и за сутки в целом, вариабельность АД (стандартное отклонение САД и ДАД), степень ночного снижения АД (процент снижения АД в ночные часы), гипертоническую нагрузку (доля измерений АД, превышающих верхнюю границу нормы в общем числе регистраций). Нормальными значениями считали АД ниже 130/80 мм рт.ст. за сутки, ниже 140/90 мм рт.ст. днем и ниже 120/70 мм рт.ст. ночью.
Центральная гемодинамика изучалась на аппарате Acuson «Sequoia» (США). Периферическая гемодинамика оценивалась с помощью метода лазерной допплеровской флоуметрии на аппарате ЛАКК–01 (НПП «Лазма», Россия). Показания регистрировались в области наружной поверхности предплечья левой руки на уровне 4 см выше линии, соединяющей основания шиловидных отростков локтевой и лучевой костей (4).
Статистическая обработка результатов проводилась с помощью программного пакета SPSS–10.0. Данные представлены в виде средних величин ± стандартное отклонение. Для выявления достоверности различий до и после лечения применялся t–тест Стьюдента. Различия между группами, касающиеся распространенности, оценивались с помощью теста c2. Различия считались достоверными при р<0,05.
Результаты и обсуждение
Исходно пациенты предъявляли жалобы на головные боли (80%), головокружение (56,7%), боли в области сердца нестенокардитического характера (70%), нарушение сна (43,3%), слабость и утомляемость (66,7%), периферические отеки (6,7%). У 5 (16,7%) пациентов жалобы отсутствовали. По данным СМАД отмечалось повышение средних дневных, средних ночных и среднесуточных значений САД и ДАД при нормальных показателях ЧСС (табл. 1). Были увеличены вариабельность АД и доля измерений, превышающих норму (ДИПН), так называемая нагрузка давлением. Степень ночного снижения (СНС) в среднем для группы составила для САД 10,8±5,6%, для ДАД – 10,9±4,8%. У 21 (70%) пациента СНС соответствовала группе «dipper», у 8 (26,7%) пациентов – «non–dipper», чрезмерное снижение АД («overdipper») в ночное время выявлено у 1 пациента.
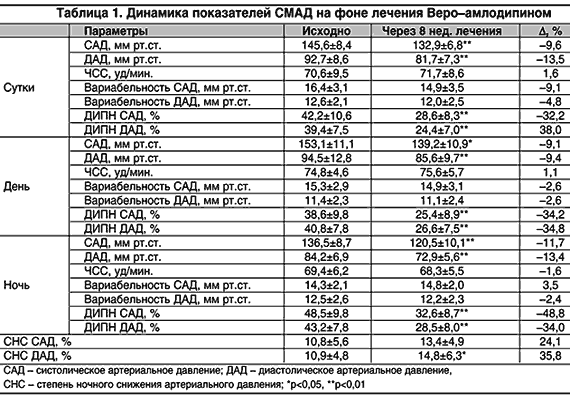
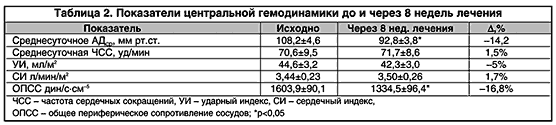
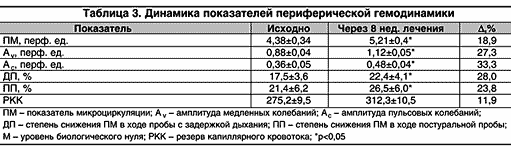
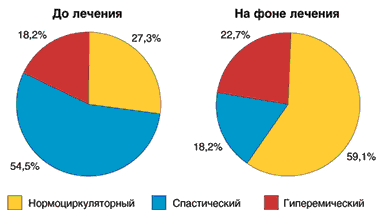
Рис. 1. Типы периферической гемодинамики до и на фоне лечения
Через 8 недель терапии в клиническом состоянии больных отмечена явная положительная динамика: улучшилось общее самочувствие, уменьшились или исчезли головные боли (у 66,7%), головокружение (у 76,5%), кардиалгии (у 42,9%), нарушение сна (у 30,5%), слабость и утомляемость (у 90%).По данным СМАД выявлено статистически достоверное уменьшение САД и ДАД за сутки, день и ночь (табл. 1). Увеличение ЧСС было статистически недостоверным, что, вероятно, может быть объяснено отсутствием влияния Веро–амлодипина на активность симпатической нервной системы [6,8]. Лечение Веро–амлодипином оказалось эффективным (среднесуточное АД менее 130/80 мм рт.ст.) у 66,7% пациентов, что соответствует современным данным об эффективности монотерапии [1]. Отмечено достоверное уменьшение ДИПН. В меньшей степени изменилась вариабельность АД. СНС увеличилась для САД до 13,4±4,9% (недостоверно), для ДАД – до 14,8±6,3%. Доля пациентов с нормальным суточным ритмом АД (dipper) достигла 76,7%. Данные факты свидетельствуют о том, что Веро–амлодипин в дозе 5 мг 1 раз в сутки позволяет контролировать уровень АД в течение 24 часов, не влияя на циркадный ритм АД.
Анализ центральной гемодинамики на фоне терапии Веро–амлодипином выявил достоверное снижение среднего АД за сутки на 14,2% (р<0,05) и ОПСС на 16,8% (р<0,05). Ударный и сердечный индексы изменились недостоверно (табл. 2). Таким образом, снижение АД произошло преимущественно за счет уменьшения периферического сосудистого сопротивления. В этой связи интересны результаты исследования состояния микроциркуляции, существенно влияющей на ОПСС. По данным лазерной допплеровской флоуметрии число пациентов с нормоциркуляторным типом микроциркуляции увеличилось с 7 до 13 (59,1%). При этом доля больных со спастическим типом периферической гемодинамики уменьшилась до 18,2%. Таким образом, можно сделать вывод о том, что с патогенетической точки зрения Веро–амлодипин наиболее оправдан именно при спастическом типе микроциркуляции. У одного пациента на фоне лечения произошла трансформация типа микроциркуляции с нормоциркуляторного на гиперемический. Примечательно, что именно у этого больного отмечены побочные реакции в виде чувства жара и периферических отеков, заставившие его прекратить лечение. В целом, отмечено улучшение показателя микроциркуляции, амплитуды медленных и пульсовых колебаний (табл. 3). В положительную сторону изменились и параметры микроциркуляции при проведении функциональных проб, что может косвенно свидетельствовать о восстановлении сократительной активности прекапиллярных сфинктеров, т.е. благоприятном влиянии Веро–амлодипина на состояние эндотелиальной функции.
При биохимическом анализе крови достоверной динамики содержания холестерина и триглицеридов не отмечено, что позволяет сделать вывод о метаболической инертности Веро–амлодипина.
Побочные реакции отмечены у 5 больных: периферические отеки – у 4, чувство жара («приливы») – у 2, ощущение учащенного сердцебиения – у 3, головная боль – у 2 пациентов. Их выраженность в большинстве случаев была незначительной и не потребовала отмены препарата. Лечение прекратил лишь один пациент (из–за периферических отеков и чувства жара через 1,5–2 часа после приема препарата).
Выводы
1. Веро–амлодипин является эффективным и безопасным препаратом для монотерапии мягкой и умеренной артериальной гипертензии.
2. Антигипертензивный эффект препарата обусловлен его преимущественным влиянием на уровень ОПСС.
3. Исследование микроциркуляции у пациентов дает возможность дифференцированного подхода к назначению терапии: Веро–амлодипин наиболее оправдан при спастическом типе периферической гемодинамики и нежелателен – при гиперемическом.
4. При 8–недельном курсе лечения Веро–амлодипином не отмечено изменений показателей липидного обмена.
1. Белоусов Ю.Б., Грацианская А.Н. Клиническая фармакология амлодипина (норваска). – М.; 1998.
2. Гогин Е.Е. Гипертоническая болезнь. – М.; 1997.
3. Маколкин В.И., Подзолков В.И. Гипертоническая болезнь. – М.; 2000.
4. Маколкин В.И., Бранько В.В., Богданова Э.А. и соавт. Метод лазерной допплеровской флуометрии в кардиологии. М., 1999 г.
5. 1999 World Health Organization – International Society of Hypertension Guidelines for the Management of Hypertension. J. Hypertens. 1999; 17(2): 151–183.
6. Campbell D.B., Moore R. // Am. J. Hypertens. 1981; 57: 7–17.
7. Epstein M. (ed.). Calcium antagonists in clinical medicine, 2–nd ed.. Philadelphia, 1997.
8. Joint National Commitee on Detection, Evaluation, and Treatment of High Blood Pressure. The 1988 Report. Arch Intern. Med. 1988; 148:1023–1038
9. Oparil S., Weber M.A. (eds.). Hypertension: a companion to Brenner and Rector’s the Kidney. Philadelphia, 2000.
10. Siegel D., Lopez J. Trends in drug use in the United States. JAMA. 1997; 278:1747–1748.
11. Toyo–oka T., Naylor W.G. Third generation calcium entry blockers. Blood Pressure. 1996; 5:206–208.












