–Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –°–Ф 2-–≥–Њ —В–Є–њ–∞ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В –Ї–∞–Ї —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В –њ—А–Є—Б—Г—В—Б—В–≤–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–∞ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (–°–°–Ч), —З—В–Њ –≥–Њ–≤–Њ—А–Є—В –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є —Г–і–µ–ї—П—В—М —Н—В–Њ–є –њ—А–Њ–±–ї–µ–Љ–µ –Њ—Б–Њ–±–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ. –Я—А–Є –і–Є–∞–±–µ—В–µ –°–°–Ч –≤—Б—В—А–µ—З–∞—О—В—Б—П –≤ 2–5 —А–∞–Ј —З–∞—Й–µ, —З–µ–Љ —Г –ї–Є—Ж –±–µ–Ј –і–∞–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Я—А–Є —Н—В–Њ–Љ –≤—Л—Б–Њ–Ї —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —В–∞–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є, –Ї–∞–Ї –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М —Б–µ—А–і—Ж–∞ (–Ш–С–°), –Є–љ—Д–∞—А–Ї—В –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь), –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П (–Р–У), –Њ—Б—В—А–Њ–µ –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П (–Ю–Э–Ь–Ъ). –Ґ–∞–Ї, 69% –±–Њ–ї—М–љ—Л—Е –°–Ф –Є–Љ–µ—О—В –і–Є—Б–ї–Є–њ–Є–і–µ–Љ–Є—О, 80% — –Р–У, 50–75% — –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї—Г—О –і–Є—Б—Д—Г–љ–Ї—Ж–Є—О, 12–22% — —Е—А–Њ–љ–Є—З–µ—Б–Ї—Г—О —Б–µ—А–і–µ—З–љ—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М (–•–°–Э). –°–Љ–µ—А—В–љ–Њ—Б—В—М –Њ—В –Ш–Ь —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е —Б –°–Ф –≤ 1,5–2 —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ —Б—А–µ–і–Є –ї—О–і–µ–є, –љ–µ —Б—В—А–∞–і–∞—О—Й–Є—Е —Н—В–Є–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ, –Ї–∞–Ї –≤ –Њ—Б—В—А–Њ–є —Б—В–∞–і–Є–Є –Ш–Ь, —В–∞–Ї –Є –њ—А–Є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ–Љ –љ–∞–±–ї—О–і–µ–љ–Є–Є [2]. –Т–љ–µ–Ј–∞–њ–љ–∞—П —Б–µ—А–і–µ—З–љ–∞—П —Б–Љ–µ—А—В–љ–Њ—Б—В—М —Б—А–µ–і–Є –≤—Б–µ–є –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В 50%. –¶–µ–љ—В—А–∞–ї—М–љ–Њ–µ –Љ–µ—Б—В–Њ –≤ —Н—В–Њ–Љ –Ј–∞–љ–Є–Љ–∞–µ—В –∞—А–Є—В–Љ–Њ–≥–µ–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –°–Ф [3]. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М —Б–Є–љ—Г—Б–Њ–≤–Њ–є —В–∞—Е–Є–Ї–∞—А–і–Є–Є –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 43,1% (–±–µ–Ј —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–≥–Њ –°–Ф — 27,3%), –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л—Е —Д–Њ—А–Љ —Д–Є–±—А–Є–ї–ї—П—Ж–Є–Є –њ—А–µ–іc–µ—А–і–Є–є, —Г–≤–µ–ї–Є—З–Є–≤–∞—О—Й–Є—Е —А–Є—Б–Ї —Б–Љ–µ—А—В–Є –≤ 1,8–2 —А–∞–Ј–∞, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф — 2–8,6% (–њ—А–Њ—В–Є–≤ –µ–і–Є–љ–Є—З–љ—Л—Е) [5, 6], —Б—Г–њ—А–∞–≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–Њ–є —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї–Є–Є — 15,5% (–њ—А–Њ—В–Є–≤ 9,1%) [3, 4]. –І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П —Б—В—А—Г–Ї—В—Г—А—Л –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ–±—Б—Г–ґ–і–∞–µ–Љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ, —В–Њ –Њ–љ–∞ –≤—Л–≥–ї—П–і–Є—В —Б–ї–µ–і—Г—О—Й–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ: 90–97% — —Б—Г–њ—А–∞–≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ–∞—П —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї–Є—П, 60–68% — –ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–∞—П —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї–Є—П, 12–30% — –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ–∞—П —В–∞—Е–Є–Ї–∞—А–і–Є—П [7].
–Ф–ї—П –≤—Л—П–≤–ї–µ–љ–Є—П –ї–Є—Ж —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –°–Ф –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –Є—Е –љ–∞ —В—А–Є –Ї–∞—В–µ–≥–Њ—А–Є–Є:
- –Њ–±—Й–∞—П –њ–Њ–њ—Г–ї—П—Ж–Є—П;
- –ї–Є—Ж–∞ —Б –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є (–Њ–ґ–Є—А–µ–љ–Є–µ, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П (–Р–У) –Є–ї–Є –°–Ф –≤ —Б–µ–Љ–µ–є–љ–Њ–Љ –∞–љ–∞–Љ–љ–µ–Ј–µ);
- –њ–∞—Ж–Є–µ–љ—В—Л —Б —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є –°–°–Ч.

–° –≤—Л—Б–Њ–Ї–Є–Љ —Г—А–Њ–≤–љ–µ–Љ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Є –Њ–≥—А–Њ–Љ–љ—Л–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–≥–Њ –Њ–±—Й–µ—Б—В–≤–∞ –Ї–∞—А–і–Є–Њ–ї–Њ–≥–Њ–≤ –Є –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –°–Ф (European Society of Cardiology — EASC and the European Association for the study of diabetes — EASD) [8] –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л —Б–ї–µ–і—Г—О—Й–Є–µ —Д–∞–Ї—В—Л:
–Я—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–µ–є –Є –°–°–Ч. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DECODE –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є –±–Њ–ї–µ–µ 8 –Љ–Љ–Њ–ї—М/–ї —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –≤ 2 —А–∞–Ј–∞. –Я—А–Є —Н—В–Њ–Љ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –±—Л–ї –Њ—В–Љ–µ—З–µ–љ –≤ –≥—А—Г–њ–њ–µ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї—А–Њ–≤–Є —З–µ—А–µ–Ј 2 —З –њ–Њ—Б–ї–µ –µ–і—Л (>11,1 –Љ–Љ–Њ–ї—М/–ї). –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Б–љ–Є–ґ–µ–љ–Є–µ —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –≤—Б–µ–≥–Њ –ї–Є—И—М –љ–∞ 2 –Љ–Љ–Њ–ї—М/–ї —Г–Љ–µ–љ—М—И–∞–ї–Њ —А–Є—Б–Ї —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –њ—А–Є –°–Ф –љ–∞ 20–30%. –Р–љ–∞–ї–Њ–≥–Є—З–љ–Њ–µ 12-–ї–µ—В–љ–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞–≤—И–µ–µ 95 783 —З–µ–ї–Њ–≤–µ–Ї–∞, –≤—Л—П–≤–Є–ї–Њ, —З—В–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є –і–Њ 7,8% —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —А–Њ—Б—В–Њ–Љ —А–Є—Б–Ї–∞ –°–°–Ч –≤ 1,58 —А–∞–Ј–∞ [21].
–°–Њ–≥–ї–∞—Б–љ–Њ –Х–≤—А–Њ–њ–µ–є—Б–Ї–Њ–Љ—Г –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–Љ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О EPIC-Norfolk, –њ–Њ–≤—Л—И–µ–љ–Є–µ –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ –љ–∞ 1% —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї –°–°–Ч –≤ 1,31 —А–∞–Ј–∞ (p<0,001). –Я–Њ–і–Њ–±–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е ARIC –Є UKPDS: —Б–љ–Є–ґ–µ–љ–Є–µ HbA1c –љ–∞ 1% —Г–Љ–µ–љ—М—И–∞–ї–Њ —А–Є—Б–Ї –Ш–Ь –љ–∞ 14%, –Є–љ—Б—Г–ї—М—В–∞ — –љ–∞ 12% [9]. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є ADVANCE (Action in Diabetes and Vascular Disease: Preterax and Diamicron Modified Release Controlled Evaluation) [9] —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞ –љ–∞ 1% (–љ–∞—З–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М HbA1c –Њ—В 6,5%) –њ–Њ—З—В–Є –≤ 2 —А–∞–Ј–∞ –њ–Њ–≤—Л—И–∞–ї–Њ —А–Є—Б–Ї –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –∞ –њ—А–Є –Є—Б—Е–Њ–і–љ–Њ–Љ —Г—А–Њ–≤–љ–µ HbA1c –Њ—В 7% —Г–ґ–µ –≤–Њ–Ј—А–∞—Б—В–∞–ї —А–Є—Б–Ї –Є –Љ–∞–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–∞ 38% [10]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б–љ–Є–ґ–µ–љ–Є–µ —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –љ–∞ 1% –љ–Є–≤–µ–ї–Є—А–Њ–≤–∞–ї–Њ —А–Є—Б–Ї –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є –љ–∞ 26% [11], –∞ –Љ–∞–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е — –љ–∞ 22%, –∞ —В–∞–Ї–ґ–µ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Є –Њ–±—Й–µ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –љ–∞ 25% –Є 22% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ [12, 13].
–Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, —Б–≤—П–Ј—М –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є —Б –°–°–Ч –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ UKPDS (UK Prospective Diabetes Study — –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –°–Ф –≤ –Р–љ–≥–ї–Є–Є). –†–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –•–°–Э –њ—А–Є –°–Ф —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ–Ї–Њ–ї–Њ 3% –≤ –≥–Њ–і –Є –њ—А—П–Љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї–µ–љ —Г—А–Њ–≤–љ—О HbA1c [14]. –Х–≥–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –љ–∞ 1% —Г–Љ–µ–љ—М—И–∞–µ—В —А–Є—Б–Ї —Б–Љ–µ—А—В–Є –љ–∞ 21%, –Ю–Ш–Ь — –љ–∞ 14%, –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є — –љ–∞ 14% –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤ — –љ–∞ 43%. –Ш—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є –і–Њ–Ї–∞–Ј–∞–ї–Є —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є —Б–љ–Є–ґ–∞–ї —А–Є—Б–Ї –ї—О–±–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –љ–∞ 12%, –∞ –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є — –љ–∞ 25%. –Р –µ—Б–ї–Є –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї—Б—П –Є –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–µ–Љ –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Р–Ф, —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –ї—О–±–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П —Г–Љ–µ–љ—М—И–∞–ї—Б—П –љ–∞ 24%, —Б–Љ–µ—А—В–Є –Њ—В –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –°–Ф — –љ–∞ 37%, –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ–Њ—Б–ї–µ–і—Б—В–≤–Є–є — –љ–∞ 37%, –Ю–Э–Ь–Ъ — –љ–∞ 44%.
- –І–∞—Б—В–Њ—В–∞ –°–°–Ч —Г –Љ—Г–ґ—З–Є–љ —Б –°–Ф –≤ 2–3 —А–∞–Ј–∞, –∞ —Г –ґ–µ–љ—Й–Є–љ –≤ 3–5 —А–∞–Ј –≤—Л—И–µ, —З–µ–Љ —Г –ї–Є—Ж –±–µ–Ј –°–Ф.
- –Я–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П — –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є, –љ–µ–ґ–µ–ї–Є —Г—А–Њ–≤–µ–љ—М –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї. –Я–Њ—Н—В–Њ–Љ—Г –ї–Њ–≥–Є—З–љ–Њ, —З—В–Њ –њ–Њ—Б—В–њ—А–∞–љ–і–Є–∞–ї—М–љ–∞—П –≥–ї–Є–Ї–µ–Љ–Є—П –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –°–°–Ч —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ–Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –љ–∞—В–Њ—Й–∞–Ї.
- –°–Ф –Є –°–°–Ч –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В —Б–Њ–±–Њ–є –≤–Ј–∞–Є–Љ–Њ–Њ—В—П–≥–Њ—Й–∞—О—Й–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Т–Њ–Њ–±—Й–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –љ–∞ —Д–Њ–љ–µ –°–Ф –Љ–Њ–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ –њ—А–Є—З–Є–љ –Ї—А–Њ–Љ–µ –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є: –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П, –ї–∞–±–Є–ї—М–љ–Њ—Б—В—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≥–ї–Є–Ї–µ–Љ–Є–Є, –і–µ–Ј–Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є—П –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —Б–Њ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –њ–∞—А–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В—Л, —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Є–Њ–Ї–∞—А–і–∞ (–≥–Є–њ–µ—А—В—А–Њ—Д–Є—П –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В–Њ–≤, –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ –≥–ї–Є–Ї–Њ–≥–µ–љ–∞, –Њ–≥—А–Њ–Љ–љ–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –љ–µ–Ј—А–µ–ї—Л—Е —Н–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –і–Є—Д—Д—Г–Ј–љ—Л–є —Б–Ї–ї–µ—А–Њ–Ј –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–є —В–Ї–∞–љ–Є, –ї–Є–њ–Є–і–љ–∞—П –Є–љ—Д–Є–ї—М—В—А–∞—Ж–Є—П –Ї–ї–µ—В–Њ–Ї –Љ–Є–Њ–Ї–∞—А–і–∞, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —А–∞—Б—И–Є—А–µ–љ–Є–µ —Б–∞—А–Ї–Њ–њ–ї–∞–Ј–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —А–µ—В–Є–Ї—Г–ї—Г–Љ–∞, –Љ–Є–Ї—А–Њ–Љ–Є—В–Њ—Е–Њ–љ–і—А–Є–Њ–Ј, –≥–Є–њ–µ—А–њ–ї–∞–Ј–Є—П –∞–њ–њ–∞—А–∞—В–∞ –У–Њ–ї—М–і–ґ–Є, –ї–Њ–Ї–∞–ї—М–љ—Л–є –Љ–Є–Њ—Ж–Є—В–Њ–ї–Є–Ј –Є —В. –і.) [15]. –Э–µ–ї—М–Ј—П –љ–µ –Ј–∞–Њ—Б—В—А–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —А–∞–љ–љ–µ–Љ —А–∞–Ј–≤–Є—В–Є–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Њ—З–∞–≥–Њ–≤—Л—Е –Ј–Њ–љ —Д–Є–±—А–Њ–Ј–∞ [16, 17]. –°–∞–Љ –њ–Њ —Б–µ–±–µ –°–Ф 2-–≥–Њ —В–Є–њ–∞ —Г—Б–Ї–Њ—А—П–µ—В –Є —Г—Б—Г–≥—Г–±–ї—П–µ—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –Ї–Њ—В–Њ—А—Л–є –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –і–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –°–Ф –Є –њ–Њ—П–≤–ї–µ–љ–Є—П –љ–∞—З–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є–Ї–Є. –Т —Б—В—А—Г–Ї—В—Г—А–µ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ –њ—А–Є–Љ–µ—А–љ–Њ 60–75% –Ј–∞–љ–Є–Љ–∞–µ—В —Б–Љ–µ—А—В—М –Њ—В –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Є 10–25% — –Њ—В —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ [18,19].
–Т —З–∞—Б—В–љ–Њ—Б—В–Є, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј –њ—А–Є –°–Ф –Є–Љ–µ–µ—В –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є: –љ–∞—З–∞–ї–Њ –µ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П — –љ–∞ 8–10 –ї–µ—В —А–∞–љ—М—И–µ –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б —В–µ–Љ–Є –ї—О–і—М–Љ–Є, —Г –Ї–Њ—В–Њ—А—Л—Е –і–Є–∞–±–µ—В –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В, –Є –Љ–Њ–ґ–µ—В –±—Л—В—М –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ –µ—Й–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Б—В–∞–і–Є–Є –љ–∞—А—Г—И–µ–љ–Є—П —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В–Є –Ї –≥–ї—О–Ї–Њ–Ј–µ. –Р—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ — —Н—В–Њ –і–≤—Г—Б—В–Њ—А–Њ–љ–љ–Є–є –њ—А–Њ—Ж–µ—Б—Б, —З–∞—Й–µ –≤—Б–µ–≥–Њ –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–є –≤ —Б–Њ—Б—Г–і–∞—Е —Б—А–µ–і–љ–µ–≥–Њ –і–Є–∞–Љ–µ—В—А–∞. –Ю–љ–Њ –±—Л—Б—В—А–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г–µ—В –Є –њ—А–Њ—В–µ–Ї–∞–µ—В —Г –ї–Є—Ж —Б –°–Ф –≤ –±–Њ–ї–µ–µ —В—П–ґ–µ–ї–Њ–є —Д–Њ—А–Љ–µ.
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ш–С–° —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ –≤—Л—И–µ –≤ 2–4 —А–∞–Ј–∞, –Р–У — –≤ 3 —А–∞–Ј–∞, –Ю–Ш–Ь — –≤ 4–7 —А–∞–Ј –≤—Л—И–µ, —З–µ–Љ —Б—А–µ–і–Є –ї–Є—Ж –±–µ–Ј —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т –Ї—А—Г–њ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —А–∞–Ј–љ–Є—Ж–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є –±–µ–Ј –°–Ф 2-–≥–Њ —В–Є–њ–∞ (n=2332, –Є–Ј –љ–Є—Е —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ — 1059). –Ч–∞ 7 –ї–µ—В –љ–∞–±–ї—О–і–µ–љ–Є—П —Г –ї–Є—Ж –±–µ–Ј —Н—В–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ —А–Є—Б–Ї –Ш–Ь —Б–Њ—Б—В–∞–≤–Є–ї 3,5%, —Г –±–Њ–ї—М–љ—Л—Е —Б –°–Ф –±–µ–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ш–С–° — 20,2%, –∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Ш–Ь, — 45%. –Ф–µ–ї–∞—П –≤—Л–≤–Њ–і, –Љ–Њ–ґ–љ–Њ —Б–Ї–∞–Ј–∞—В—М, —З—В–Њ —А–Є—Б–Ї –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ —Г –ї–Є—Ж —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ —В–∞–Ї –ґ–µ –≤—Л—Б–Њ–Ї, –Ї–∞–Ї –Є —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° —Б –њ–Њ—Б—В–Є–љ—Д–∞—А–Ї—В–љ—Л–Љ –Ї–∞—А–і–Є–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ [20].
–°—В–Њ–Є—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є–µ –Ш–С–° –њ—А–Є –°–Ф –Є–Љ–µ—О—В —А—П–і –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–µ–є [37]. –Т–Њ-–њ–µ—А–≤—Л—Е, –Њ–і–Є–љ–∞–Ї–Њ–≤–∞—П —З–∞—Б—В–Њ—В–∞ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –Љ—Г–ґ—З–Є–љ –Є –ґ–µ–љ—Й–Є–љ, —В–Њ–≥–і–∞ –Ї–∞–Ї —Г –ї–Є—Ж, –љ–µ –Є–Љ–µ—О—Й–Є—Е –°–Ф, –Ш–С–° —З–∞—Й–µ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г –Љ—Г–ґ—З–Є–љ [38]. –Т–Њ-–≤—В–Њ—А—Л—Е, —Г –±–Њ–ї—М–љ—Л—Е –°–Ф —З–∞—Й–µ –Є–Љ–µ—О—В –Љ–µ—Б—В–Њ –±–µ–Ј–±–Њ–ї–µ–≤—Л–µ («–љ–µ–Љ—Л–µ») —Д–Њ—А–Љ—Л –Ш–С–°, –≤–њ–ї–Њ—В—М –і–Њ –±–µ–Ј–±–Њ–ї–µ–≤–Њ–≥–Њ –Ш–Ь, —З—В–Њ –Њ–±—К—П—Б–љ—П–µ—В—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є, –Є–Ј —З–µ–≥–Њ –≤—Л—В–µ–Ї–∞–µ—В –њ–Њ–Ј–і–љ—П—П –њ–Њ—Б—В–∞–љ–Њ–≤–Ї–∞ –і–Є–∞–≥–љ–Њ–Ј–∞, –љ–µ—Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –ї–µ—З–µ–љ–Є—П –Є, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–∞—П —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є [39]. –Ґ–µ—З–µ–љ–Є–µ –Ш–С–° —З–∞—Б—В–Њ –Ј–∞–Ї–∞–љ—З–Є–≤–∞–µ—В—Б—П –≤–љ–µ–Ј–∞–њ–љ–Њ–є –∞—А–Є—В–Љ–Є—З–µ—Б–Ї–Њ–є —Б–Љ–µ—А—В—М—О, –∞ —Б—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е –°–Ф —А–Є—Б–Ї —В–∞–Ї–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –≤ 2 —А–∞–Ј–∞.
–Р—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П. –Т –њ–Њ–њ—Г–ї—П—Ж–Є–Є –ї–Є—И—М —В—А–µ—В—М –±–Њ–ї—М–љ—Л—Е –Р–У –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—В –Р–Ф –љ–Є–ґ–µ 140/90 –Љ–Љ —А—В. —Б—В., –∞ —З–µ–ї–Њ–≤–µ–Ї, —Б—В—А–∞–і–∞—О—Й–Є–є –°–Ф, –Є–Љ–µ–µ—В –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —А–Є—Б–Ї —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Я–Њ—Н—В–Њ–Љ—Г —Н—В–∞ –њ—А–Њ–±–ї–µ–Љ–∞ –≤–µ—Б—М–Љ–∞ –∞–Ї—В—Г–∞–ї—М–љ–∞, –≤–µ–і—М —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є–∞–±–µ—В–Њ–Љ 70–80% –Є–Љ–µ—О—В —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й—Г—О –Р–У. –Ю–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –њ–Њ–і–Њ–±–љ–∞—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є–µ–Љ —Б—Е–Њ–і–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Ю–±–∞ —Н—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П — –Љ–Њ—Й–љ—Л–µ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –±—Л—Б—В—А–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П –±–Њ–ї—М—И–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Б–ї—Г—З–∞–µ–≤ –Ї–∞—А–і–Є–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞, –њ–Њ—А–∞–ґ–µ–љ–Є–є —Б–Њ—Б—Г–і–Њ–≤ –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞, –њ–Њ—З–µ–Ї –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Њ–≤. –°–Њ—З–µ—В–∞–љ–Є–µ –Њ–±—Б—Г–ґ–і–∞–µ–Љ–Њ–≥–Њ «–і—Г—Н—В–∞» —А–µ–Ј–Ї–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П —В–µ—А–Љ–Є–љ–∞–ї—М–љ—Л—Е —Б—В–∞–і–Є–є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є — –•–Я–Э, —Б–ї–µ–њ–Њ—В—Л, –∞–Љ–њ—Г—В–∞—Ж–Є–Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є. –Ґ–∞–Ї, –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞ –±–µ–Ј –Р–У —А–Є—Б–Ї –Ш–С–° –Є –Є–љ—Б—Г–ї—М—В–∞ –≤ 2–3 —А–∞–Ј–∞ –≤—Л—И–µ, —З–µ–Љ —Г –ї–Є—Ж –±–µ–Ј –°–Ф, —А–Є—Б–Ї –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є — –≤ 15–20 —А–∞–Ј –≤—Л—И–µ, —Б–ї–µ–њ–Њ—В—Л — –≤ 10–20 —А–∞–Ј, –≥–∞–љ–≥—А–µ–љ—Л — –≤ 20 —А–∞–Ј. –Ю–і–љ–∞–Ї–Њ –њ—А–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–µ–є –Р–У —А–Є—Б–Ї –≤—Б–µ—Е –≤—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –µ—Й–µ –≤ 2–3 —А–∞–Ј–∞.

–Х—Й–µ –Њ–і–љ–Є–Љ –Њ—Б–љ–Њ–≤–Њ–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –Є —Г—Б–Ї–Њ—А–µ–љ–љ–Њ–≥–Њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –°–°–Ч –њ—А–Є –°–Ф —Б–ї—Г–ґ–Є—В –Є–љ—Б—Г–ї–Є–љ–Њ—А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М (–Ш–†) [18, 22, 23]. –Ш–† –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –і—А—Г–≥–Є—Е –Ј–љ–∞—З–Є–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –Ї–∞—А–і–Є–∞–ї—М–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –°–°–Ч [19, 24, 25].
–Т–Є—Б—Ж–µ—А–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ — —Н—В–Њ –љ–µ —В–Њ–ї—М–Ї–Њ –Љ–Њ—Й–љ—Л–є –Ї–Њ—А—А–Є–≥–Є—А—Г–µ–Љ—Л–є —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ –°–Ф 2-–≥–Њ —В–Є–њ–∞, –љ–Њ –Є –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–µ–і–Є–Ї—В–Њ—А —Б–Њ–њ—А—П–ґ–µ–љ–љ—Л—Е —Б –Њ–ґ–Є—А–µ–љ–Є–µ–Љ –Љ–љ–Њ–ґ–µ—Б—В–≤–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –≠—В–Њ –Љ–∞—А–Ї–µ—А –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞, –Ї–Њ—В–Њ—А—Л–є —Б–Њ–≤–Љ–µ—Й–∞–µ—В –≤ —Б–µ–±–µ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ—Л–µ –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П, –Њ–±—К–µ–і–Є–љ–µ–љ–љ—Л–µ –Њ–±—Й–Є–Љ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –њ—А–Њ—Ж–µ—Б—Б–Њ–Љ, –Ш–† [26].
–С–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–Њ–Ї–∞–Ј–∞–ї–Њ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е —В–Ї–∞–љ–µ–є –Ї –Є–љ—Б—Г–ї–Є–љ—Г [27]. –Ш–† — —Д–∞–Ї—В–Њ—А —А–∞–Ј–≤–Є—В–Є—П –Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Р–У, –Ш–С–°, –Ш–Ь, –∞, –њ–Њ–Љ–Є–Љ–Њ –њ—А–Њ—З–µ–≥–Њ, –Є —А–∞–Ї–∞ —И–µ–є–Ї–Є –Љ–∞—В–Ї–Є, —В–Њ–ї—Б—В–Њ–є –Є –њ—А—П–Љ–Њ–є –Ї–Є—И–Ї–Є, —П–Є—З–љ–Є–Ї–Њ–≤, –Љ–Њ–ї–Њ—З–љ—Л—Е –ґ–µ–ї–µ–Ј –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Њ–њ–Њ—А–љ–Њ-–і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞. –Ґ–∞–Ї–ґ–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –µ—Б—В—М –і–∞–љ–љ—Л–µ –Њ –њ—А–Є—З–∞—Б—В–љ–Њ—Б—В–Є –Ш–† –Ї —А–∞–Ј–≤–Є—В–Є—О —Б—В—А—Г–Ї—В—Г—А–љ—Л—Е –Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Љ–Є–Њ–Ї–∞—А–і–∞. –Я—А–Њ–≤–µ–і–µ–љ—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –і–Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Ш–† –Є –≥–Є–њ–µ—А—В—А–Њ—Д–Є–Є –Ы–Ц –Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є—П –µ–≥–Њ –Љ–∞—Б—Б—Л —Г –ї–Є—Ж –±–µ–Ј –°–Ф [28, 29]. –Т –Њ–і–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 140 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф —Г—А–Њ–≤–µ–љ—М —В–Њ—Й–∞–Ї–Њ–≤–Њ–≥–Њ –њ–ї–∞–Ј–Љ–µ–љ–љ–Њ–≥–Њ –Є–љ—Б—Г–ї–Є–љ–∞ –Њ–Ї–∞–Ј–∞–ї—Б—П —Б–∞–Љ—Л–Љ —Б–Є–ї—М–љ—Л–Љ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –Љ–∞—Б—Б—Л –Ы–Ц —Г –≤—Б–µ—Е –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –ї–Є—Ж. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–∞ –Ї—А—Л—Б–∞—Е –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ, —З—В–Њ –Ш–† –≤–ї–Є—П–µ—В –љ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ [30]. –Т –±–Њ–ї–µ–µ –Ї—А—Г–њ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є (—З–Є—Б–ї–Њ —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ — 2623) –Ш–† –±—Л–ї–∞ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–∞ —В–Њ–ї—М–Ї–Њ —Б —Г–≤–µ–ї–Є—З–µ–љ–љ–Њ–є –Љ–∞—Б—Б–Њ–є –Ы–Ц, –Є —Н—В–∞ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Њ–±—К—П—Б–љ—П–ї–∞—Б—М –Њ–ґ–Є—А–µ–љ–Є–µ–Љ [31].

–Ґ–∞–Ї–ґ–µ –љ–µ–ї—М–Ј—П –љ–µ –Ј–∞—В—А–Њ–љ—Г—В—М —В–µ–Љ—Г –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є. –Х–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ–Њ–ї–љ–Њ—Ж–µ–љ–љ–Њ –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Њ –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤. –Т–Њ-–њ–µ—А–≤—Л—Е, –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –Є–Ј–Љ–µ–љ–µ–љ–Є–µ —А–µ–Њ–ї–Њ–≥–Є–Є — —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–∞–≥—Г–ї—П—Ж–Є–Є –Ї—А–Њ–≤–Є –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤, –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≤—П–Ј–Ї–Њ—Б—В–Є –Ї—А–Њ–≤–Є. –Т–Њ-–≤—В–Њ—А—Л—Е, –њ–Њ–≤—Л—И–∞–µ—В—Б—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П —Н–љ–і–Њ—В–µ–ї–Є–љ–∞ –Є –°-—А–µ–∞—В–Є–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞, –∞–Ї—В–Є–≤–Є—А—Г–µ—В—Б—П —Б–Є–Љ–њ–∞—В–Њ–∞–і—А–µ–љ–∞–ї–Њ–≤–∞—П —Б–Є—Б—В–µ–Љ–∞ (—Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В—Б—П –І–°–° –Є –Р–Ф), —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—Ж–Є—П –Є —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є—П (–≥–Є–њ–Њ–Ї—Б–Є—П, –љ–∞—А—Г—И–µ–љ–Є–µ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –Љ–Є–Њ–Ї–∞—А–і–∞, –∞—А–Є—В–Љ–Є–Є) [32]. –Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –љ–µ–і–Њ—Б—В–∞—В–Ї–∞ –≥–ї—О–Ї–Њ–Ј—Л –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Б–љ–Є–ґ–µ–љ–Є–µ –Р–Ґ–§, –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—Й–µ–µ –≥–Є–њ–Њ–Ї—Б–Є—О –Є —Б–љ–Є–ґ–µ–љ–Є–µ —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞ —Б —Г–і–ї–Є–љ–µ–љ–Є–µ–Љ –Є–љ—В–µ—А–≤–∞–ї–∞ QT [33, 34]. –Э—Г –Є, –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–∞—П –≥–ї–Є–Ї–µ–Љ–Є—П —Б–љ–Є–ґ–∞–µ—В –∞–і–∞–њ—В–∞—Ж–Є—О –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –Ї —Б—В—А–µ—Б—Б—Г.

–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Bode 101 –њ–∞—Ж–Є–µ–љ—В—Г –њ—А–Њ–≤–Њ–і–Є–ї–Є —Б—Г—В–Њ—З–љ–Њ–µ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –≥–ї—О–Ї–Њ–Ј—Л –≤ —В–µ—З–µ–љ–Є–µ 12 –і–љ–µ–є. –С–Њ–ї—М–љ—Л–µ, –≤–Ї–ї—О—З–µ–љ–љ—Л–µ –≤ —Н—В–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –љ–µ –±—Л–ї–Є –Њ—Б–≤–µ–і–Њ–Љ–ї–µ–љ—Л –Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞—Е –Є–Ј–Љ–µ—А–µ–љ–Є–є –≥–ї—О–Ї–Њ–Ј—Л, –∞ –≤–µ–і—М –Њ–љ–Є —Б—В–∞–ї–Є —Г–љ–Є–Ї–∞–ї—М–љ—Л–Љ–Є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –±—Л–ї–Њ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б 9-–Ї—А–∞—В–љ—Л–Љ –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї –њ–Њ –≥–ї—О–Ї–Њ–Љ–µ—В—А—Г –њ—А–µ–±—Л–≤–∞–ї–Є –≤ —Н—Г–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–Љ –і–Є–∞–њ–∞–Ј–Њ–љ–µ –≤—Б–µ–≥–Њ 65% –≤—А–µ–Љ–µ–љ–Є. –Я–Њ—З—В–Є —В—А–µ—В—М –≤—А–µ–Љ–µ–љ–Є –±–Њ–ї—М–љ—Л–µ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М –≤ –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–Љ —Б–Њ—Б—В–Њ—П–љ–Є–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –і–∞–љ–љ—Л–µ –Њ–± —Н–њ–Є–Ј–Њ–і–∞—Е –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є, –љ–∞ –і–Њ–ї—О –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є—Е–Њ–і–Є–ї–Њ—Б—М –Њ–Ї–Њ–ї–Њ 8% –≤—А–µ–Љ–µ–љ–Є. –Ч–љ–∞—З–Є–Љ—Л–Љ —Б–ї—Г–ґ–Є—В —В–Њ, —З—В–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–љ—Л–µ —Б–ї—Г—З–∞–Є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є —З–∞—Й–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Є –≤ –љ–Њ—З–љ—Л–µ —З–∞—Б—Л, —З—В–Њ, –њ–Њ –і–∞–љ–љ—Л–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –ї–Є—В–µ—А–∞—В—Г—А—Л, –Њ—З–µ–љ—М –Њ–њ–∞—Б–љ–Њ –≤ –њ–ї–∞–љ–µ —А–∞–Ј–≤–Є—В–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ї–∞—В–∞—Б—В—А–Њ—Д. –Т –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ –њ—А–Є–≤–µ—Б—В–Є –њ—А–Є–Љ–µ—А —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞ 70 –ї–µ—В —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ –њ–Њ—Б–ї–µ –њ–µ—А–µ–љ–µ—Б–µ–љ–љ–Њ–≥–Њ –Ш–Ь. –Я–∞—Ж–Є–µ–љ—В –љ–∞—Е–Њ–і–Є–ї—Б—П –љ–∞ –±–∞–Ј–Є—Б–љ–Њ-–±–Њ–ї—О—Б–љ–Њ–є –Є–љ—Б—Г–ї–Є–љ–Њ—В–µ—А–∞–њ–Є–Є. –£ —Н—В–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї—О–Ї–Њ–Ј—Л –≤ –Ї—А–Њ–≤–Є –≤ —Г—В—А–µ–љ–љ–µ–µ –≤—А–µ–Љ—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –±–µ—Б—Б–Є–Љ–њ—В–Њ–Љ–љ—Л—Е –і–ї–Є—В–µ–ї—М–љ—Л—Е –љ–Њ—З–љ—Л—Е –≥–ї–Є–Ї–µ–Љ–Є–є, –љ–µ –±–µ–Ј –≤–ї–Є—П–љ–Є–є –Ї–Њ—В–Њ—А—Л—Е —З–µ—А–µ–Ј 2 –і–љ—П –њ–Њ—Б–ї–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г –љ–µ–≥–Њ —А–∞–Ј–≤–Є–ї—Б—П –њ–Њ–≤—В–Њ—А–љ—Л–є –Ш–Ь.
–Т 2009 –≥. –≤ –Ы–Є–≤–µ—А–њ—Г–ї—М—Б–Ї–Њ–Љ —Г–љ–Є–≤–µ—А—Б–Є—В–µ—В–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ –≤–ї–Є—П–љ–Є—О –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞ –і–Є–љ–∞–Љ–Є–Ї—Г –≠–Ъ–У. 25 –њ–∞—Ж–Є–µ–љ—В–∞–Љ –Њ–і–љ–Њ–Љ–Њ–Љ–µ–љ—В–љ–Њ –њ—А–Њ–≤–Њ–і–Є–ї–Є –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–µ –≠–Ъ–У –Є –≥–ї–Є–Ї–µ–Љ–Є–Є. –Я–Њ–ї—Г—З–µ–љ–Њ, —З—В–Њ 13 —Н–њ–Є–Ј–Њ–і–Њ–≤ –љ–Њ—З–љ–Њ–є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Є—Б—М —Г–і–ї–Є–љ–µ–љ–Є–µ–Љ –Є–љ—В–µ—А–≤–∞–ї–∞ QT –і–Њ 445±23 –Љ—Б, —В–Њ–≥–і–∞ –Ї–∞–Ї –њ—А–Є –љ–Њ—А–Љ–Њ–≥–ї–Є–Ї–µ–Љ–Є–Є –Њ–љ –Њ—Б—В–∞–≤–∞–ї—Б—П –љ–Њ—А–Љ–∞–ї—М–љ—Л–Љ. –°—Е–Њ–і–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –µ—Й–µ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е, –≥–і–µ –±—Л–ї–Њ –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–Њ, —З—В–Њ –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —Г–і–ї–Є–љ–µ–љ–Є–µ–Љ –Є–љ—В–µ—А–≤–∞–ї–∞ QT –Є –і–µ–њ—А–µ—Б—Б–Є–µ–є —Б–µ–≥–Љ–µ–љ—В–∞ ST.
–Э–∞—А—Г—И–µ–љ–Є—П –≥–ї–Є–Ї–µ–Љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –љ–µ –Њ–≥—А–∞–љ–Є—З–µ–љ—Л —В–Њ–ї—М–Ї–Њ –≥–Є–њ–µ—А- –Є–ї–Є –≥–Є–њ–Њ–≥–ї–Є–Ї–µ–Љ–Є—П–Љ–Є, –Њ–љ–Є –≤–Ї–ї—О—З–∞—О—В —В–∞–Ї–ґ–µ –Є –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –≥–ї—О–Ї–Њ–Ј—Л –Ї—А–Њ–≤–Є. –Ь–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –ї–∞–±–Є–ї—М–љ–Њ—Б—В—М —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є — —Н—В–Њ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–є —Д–∞–Ї—В–Њ—А —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Б–Љ–µ—А—В–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т –љ–µ–і–∞–≤–љ–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є Krinsley –≥–Њ–≤–Њ—А–Є–ї–Њ—Б—М –Њ —Б–≤—П–Ј–Є –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –Є —Б–Љ–µ—А—В–µ–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤. –Ы–µ—В–∞–ї—М–љ–Њ—Б—В—М –њ—А–Є –љ–Є–Ј–Ї–Њ–є –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 12,1% –Є —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞—Б—М –і–Њ 19,9%, 27,7% –Є 37,8% –≤–Њ –≤—В–Њ—А–Њ–Љ, —В—А–µ—В—М–µ–Љ –Є —З–µ—В–≤–µ—А—В–Њ–Љ –Ї–≤–∞—А—В–Є–ї—П—Е [42]. –Т 2008 –≥. Ceriello –Є —Б–Њ–∞–≤—В. –≤—Л—П–≤–Є–ї–Є, —З—В–Њ –њ–Є–Ї–Є –≥–ї–Є–Ї–µ–Љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ –њ—А–Є–≤–Њ–і—П—В –Ї –±–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є—О 3-–љ–Є—В—А–Њ–Ј–Є–љ–∞-–Љ–∞—А–Ї–µ—А–∞ –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞ –Є 8-–Є–Ј–Њ–њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–∞ F2a (–Љ–∞—А–Ї–µ—А–∞ –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞), —З–µ–Љ –њ—А–Є —Б—В–∞–±–Є–ї—М–љ–Њ –≤—Л—Б–Њ–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ –≥–ї–Є–Ї–µ–Љ–Є–Є. –°–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Н—В–Њ –њ–Њ–≤—Л—И–∞–ї–Њ —А–Є—Б–Ї –°–°–Ч –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–µ–є [43].
–Ъ—Б—В–∞—В–Є, –Ј–∞—В—А–Њ–љ—Г–≤ —В–µ–Љ—Г –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ —Б—В—А–µ—Б—Б–∞, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—Б–≤–µ—В–Є—В—М –Є –µ–≥–Њ –≤–Ї–ї–∞–і –≤ —А–∞–Ј–≤–Є—В–Є–µ –°–°–Ч. –Ь–љ–Њ–ґ–µ—Б—В–≤–Њ —А–∞–±–Њ—В –њ–Њ—Б–ї–µ–і–љ–Є—Е –ї–µ—В —Г–Ї–∞–Ј—Л–≤–∞—О—В –љ–∞ —Б–≤—П–Ј—М —В–∞–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –Ї–∞–Ї –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј, –Ш–С–°, –Р–У, –°–Ф 2-–≥–Њ —В–Є–њ–∞, —Б —Г—Е—Г–і—И–µ–љ–Є–µ–Љ —Н–љ–і–Њ—В–µ–ї–Є–є–Ј–∞–≤–Є—Б–Є–Љ–Њ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—Ж–Є–Є, –Њ–њ–Њ—Б—А–µ–і–Њ–≤–∞–љ–љ–Њ–є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є –њ—А–Њ–і—Г–Ї—Ж–Є–Є –Є–ї–Є –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є –Њ–Ї—Б–Є–і–∞ –∞–Ј–Њ—В–∞ (NO). –Я—А–Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–Љ —Б—В—А–µ—Б—Б–µ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –њ–Њ–≤—Л—И–µ–љ–љ–Њ–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ (—А–µ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е –Ї–Є—Б–ї–Њ—А–Њ–і–∞) –Є/–Є–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З—В–Њ –љ–∞—А—Г—И–∞–µ—В –±–∞–ї–∞–љ—Б –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ-–≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є –Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–µ—А—М–µ–Ј–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –Ї–ї–µ—В–Њ—З–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ —Б—В—А—Г–Ї—В—Г—А—Л –Ї–ї–µ—В–Њ–Ї. –Я—А–Є —Г—З–∞—Б—В–Є–Є —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤ —В–∞–Ї–ґ–µ —Г—Б–Є–ї–Є–≤–∞–µ—В—Б—П –њ–µ—А–µ–Ї–Є—Б–љ–Њ–µ –Њ–Ї–Є—Б–ї–µ–љ–Є–µ –ї–Є–њ–Є–і–Њ–≤, –≤—Б–ї–µ–і—Б—В–≤–Є–µ —З–µ–≥–Њ –љ–∞—Б—В—Г–њ–∞–µ—В –і–Є—Б–±–∞–ї–∞–љ—Б –Љ–µ–ґ–і—Г –њ—А–Њ–і—Г–Ї—Ж–Є–µ–є –≤–∞–Ј–Њ–і–Є–ї–∞—В–Є—А—Г—О—Й–Є—Е, –∞–љ–≥–Є–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л—Е, –∞–љ—В–Є–њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, –Є –≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–љ—Л—Е, –њ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є—Е, –њ—А–Њ–ї–Є—Д–µ—А–∞—В–Є–≤–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤, —Б –і—А—Г–≥–Њ–є. –Р —Н—В–Њ –≤—Б–µ –Љ–Њ–ґ–µ—В –Є–≥—А–∞—В—М –≤–∞–ґ–љ—Г—О —А–Њ–ї—М –≤ —Б–љ–Є–ґ–µ–љ–Є–Є –Ї–Њ—А–Њ–љ–∞—А–љ–Њ–≥–Њ —А–µ–Ј–µ—А–≤–∞ —Г –±–Њ–ї—М–љ—Л—Е –Р–У —Б –∞–љ–≥–Є–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є –љ–µ–њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л–Љ–Є –Ї–Њ—А–Њ–љ–∞—А–љ—Л–Љ–Є –∞—А—В–µ—А–Є—П–Љ–Є.
–Ъ—А–Њ–Љ–µ —Н—В–Њ–≥–Њ, –°–Ф — —Н—В–Њ –њ—А–Є—З–Є–љ–∞ –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –Љ—Л—И—Ж—Л (–і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ–њ–∞—В–Є–Є), –њ—А–Є–≤–Њ–і—П—Й–µ–є –Ї —А–∞–Ј–≤–Є—В–Є—О –•–°–Э –Є –љ–∞—А—Г—И–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Є –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞. –Я–Њ–Љ–Є–Љ–Њ —Г–њ–Њ–Љ–Є–љ–∞–≤—И–µ–≥–Њ—Б—П —А–∞–љ–µ–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Љ–Є–Њ–Ї–∞—А–і–∞ –≤—Л–Ј—Л–≤–∞—О—В —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П: –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ—В–Є–Є –Є –љ–µ–є—А–Њ–њ–∞—В–Є–Є. –•–°–Э –Є –°–Ф 2-–≥–Њ —В–Є–њ–∞ –њ—А–Є—Б—Г—В—Б—В–≤—Г—О—В —Г —В—А–µ—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –•–°–Э –≤ 2–3 —А–∞–Ј–∞ —З–∞—Й–µ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г –ї–Є—Ж —Б –°–Ф, –љ–µ–ґ–µ–ї–Є –±–µ–Ј –љ–µ–≥–Њ. –Т —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≠–Я–Ю–•–Р –Ј–≤—Г—З–∞–ї–Њ —Б–ї–µ–і—Г—О—Й–µ–µ: –љ–∞–ї–Є—З–Є–µ —Б–µ—А–і–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є — –њ—А–µ–і–Є–Ї—В–Њ—А —А–∞–Ј–≤–Є—В–Є—П –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –°–Ф. –°—А–µ–і–Є –±–Њ–ї—М–љ—Л—Е –•–°–Э III–IV —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –Ї–ї–∞—Б—Б–∞ — 15,8% –ї–Є—Ж —Б –°–Ф.
–Я–Њ –і–∞–љ–љ—Л–Љ –§—А–µ–Љ–Є–љ–≥–µ–Љ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –°–Э –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ 4 —А–∞–Ј–∞ —З–∞—Й–µ —Г –Љ—Г–ґ—З–Є–љ –Є –≤ 8 —А–∞–Ј —З–∞—Й–µ —Г –ґ–µ–љ—Й–Є–љ —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –і–Њ 65 –ї–µ—В, —З–µ–Љ –≤ –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–Є [35]. –Х–ґ–µ–≥–Њ–і–љ–Њ –°–Э —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П —Г 3,3% –±–Њ–ї—М–љ—Л—Е –°–Ф 2-–≥–Њ —В–Є–њ–∞, –љ–µ –Є–Љ–µ–≤—И–Є—Е —А–∞–љ–µ–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –°–Э [36]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е SOLVD (Studies of Left Ventricular Dysfunction) –Є RESOLVD (Randomized Evaluation for Strategies of Left Ventricular Dysfunction) –°–Ф –±—Л–ї –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є. –Т DIGAMI –°–Э —Б—В–∞–ї–∞ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є –ї–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф 2-–≥–Њ —В–Є–њ–∞ –Є –Ш–Ь –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ –Є –Њ–±—Г—Б–ї–Њ–≤–Є–ї–∞ 66% —Б–Љ–µ—А—В–µ–ї—М–љ—Л—Е —Б–ї—Г—З–∞–µ–≤ –≤ –≥–Њ–і.
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –њ—А–Є–Ј–љ–∞–µ—В—Б—П, —З—В–Њ –њ–µ—А–≤—Л–Љ –і–Њ–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞ —Б–ї—Г–ґ–Є—В –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ [40, 41]. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –≤ –†–Њ—Б—Б–Є–Є –њ–Њ–і —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ–Љ –Р. –Ь. –Ь–Ї—А—В—Г–Љ—П–љ–∞, –°. –Т. –Я–Њ–і–∞—З–Є–љ–Њ–є –Є –Ь. –Р. –°–≤–Є—А–Є–і–Њ–≤–Њ–є, –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Њ—В –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –°–Ф. –†–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М —Н—В–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –±—Л–ї–∞ –љ–∞–Љ–љ–Њ–≥–Њ –≤—Л—И–µ –њ—А–Є —Б—В–∞–ґ–µ –°–Ф –±–Њ–ї–µ–µ 5 –ї–µ—В — 50% –Є 75% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Т —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Г –ї–Є—Ж, —Б—В—А–∞–і–∞—О—Й–Є—Е –°–Ф –Љ–µ–љ–µ–µ 5 –ї–µ—В, —З–∞—Б—В–Њ—В–∞ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 37%, –∞ —Н–љ–і–Њ—В–µ–ї–Є–∞–ї—М–љ–Њ–є — 50%.
–Я–Њ–Љ–Є–Љ–Њ —Б–≤—П–Ј–Є —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П —Б –°–°–Ч —Б—Г—Й–µ—Б—В–≤—Г—О—В –Є –і—А—Г–≥–Є–µ –њ—А–µ–і–Є–Ї—В–Њ—А—Л. –Ш—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—О—В —А–Њ–ї—М –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є (–Ф–Р–Э) –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ—В—П–≥–Њ—Й–∞—О—Й–µ–≥–Њ —Д–∞–Ї—В–Њ—А–∞. –Ф–Р–Э —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–∞ —А–Є—Б–Ї –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–µ—А–і–µ—З–љ–Њ–є —Б–Љ–µ—А—В–Є, —З—В–Њ –±—Л–ї–Њ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е UK-HEART, ATRAMI –Є –≤ –і—А.
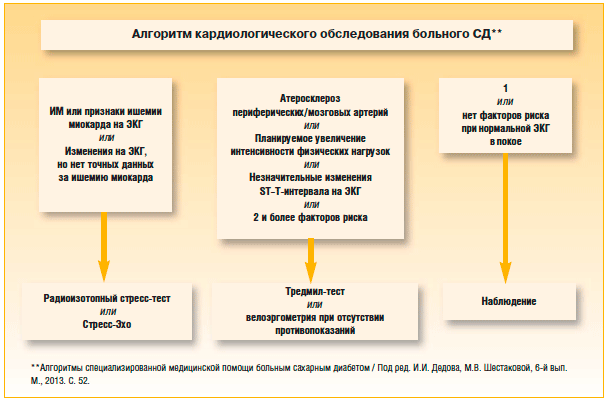
–°–ї–µ–і—Б—В–≤–Є—П –≤–ї–Є—П–љ–Є—П –Ф–Р–Э:
- –†–∞–Ј–≤–Є—В–Є–µ –±–µ–Ј–±–Њ–ї–µ–≤–Њ–є –Є—И–µ–Љ–Є–Є –Ј–∞ —Б—З–µ—В –њ–Њ—А–∞–ґ–µ–љ–Є—П –∞—Д—Д–µ—А–µ–љ—В–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –Я–Њ –і–∞–љ–љ—Л–Љ P. Kempler, –њ—А–Є —Е–Њ–ї—В–µ—А–Њ–≤—Б–Ї–Њ–Љ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є–Є –≤—Л—П–≤–ї–µ–љ–Њ 64,7% «–љ–µ–Љ–Њ–є» –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –Ф–Р–Э, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –њ—А–Є –µ–µ –Њ—В—Б—Г—В—Б—В–≤–Є–Є — 4,1%.
- –Я–Њ–≤—Л—И–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –∞—А–Є—В–Љ–Є–Є –Ј–∞ —Б—З–µ—В —Б–љ–Є–ґ–µ–љ–Є—П –њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ–∞—А–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л [44].
- –Э–∞—А—Г—И–µ–љ–Є–µ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї—П –Р–Ф –≤ –≤–Є–і–µ –µ–≥–Њ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –≤ –љ–Њ—З–љ—Л–µ —З–∞—Б—Л, —З—В–Њ —П–≤–ї—П–µ—В—Б—П —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ—А–≥–∞–љ–Њ–≤-–Љ–Є—И–µ–љ–µ–є –Є –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–Љ–µ—А—В–Є. –Ю—В–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –°–Ф 1-–≥–Њ –Є –°–Ф 2-–≥–Њ —В–Є–њ–∞ —Б–≤—П–Ј–∞–љ—Л —Б —А–∞–Ј–ї–Є—З–Є—П–Љ–Є –≤ —В–µ—З–µ–љ–Є–Є –Ф–Р–Э: –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞ —Б–Є–Љ–њ—В–Њ–Љ—Л –њ–Њ—П–≤–ї—П—О—В—Б—П, –њ—А–µ–і—И–µ—Б—В–≤—Г—П –Љ–Њ–Љ–µ–љ—В—Г –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Т–µ—А–Њ—П—В–љ–µ–є –≤—Б–µ–≥–Њ, —Н—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞. –†–∞–љ–љ—П—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ф–Р–Э –њ–Њ–Ј–≤–Њ–ї–Є—В –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –±–µ–Ј–±–Њ–ї–µ–≤–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –≤–љ–µ–Ј–∞–њ–љ–Њ–є —Б–Љ–µ—А—В–Є.
–Т –Ј–∞–Ї–ї—О—З–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –°–Ф –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Ї–Њ–ї–Њ—Б—Б–∞–ї—М–љ—Г—О –њ—А–Њ–±–ї–µ–Љ—Г –і–ї—П –Ј–і–Њ—А–Њ–≤—М—П –љ–∞—Б–µ–ї–µ–љ–Є—П –≤—Б–µ—Е —Б—В—А–∞–љ –Љ–Є—А–∞, –≤–µ–і—М —А–Њ—Б—В –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –њ–Њ–Ј–≤–Њ–ї–Є–ї –≥–Њ–≤–Њ—А–Є—В—М –Њ –≥–ї–Њ–±–∞–ї—М–љ–Њ–є —Н–њ–Є–і–µ–Љ–Є–Є. –Т–µ–і–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –°–Ф –Є –°–°–Ч –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –±–Њ–ї—М—И—Г—О —Б–ї–Њ–ґ–љ–Њ—Б—В—М –Ї–∞–Ї –і–ї—П –Ї–∞—А–і–Є–Њ–ї–Њ–≥–∞ –Є —В–µ—А–∞–њ–µ–≤—В–∞, —В–∞–Ї –Є —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–∞. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Ї—А–∞–є–љ–µ –∞–Ї—В—Г–∞–ї—М–љ–Њ —Б–Њ–Ј–і–∞–љ–Є–µ —Б–Њ–≤–Љ–µ—Б—В–љ—Л–Љ–Є —Г—Б–Є–ї–Є—П–Љ–Є —З–µ—В–Ї–Є—Е –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л—Е –∞–ї–≥–Њ—А–Є—В–Љ–Њ–≤ –≤–µ–і–µ–љ–Є—П –њ–Њ–і–Њ–±–љ—Л—Е –±–Њ–ї—М–љ—Л—Е. –Ш –њ—А–Є —Н—В–Њ–Љ –≤–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –њ–Њ–і—Е–Њ–і –Ї –Ї–∞–ґ–і–Њ–Љ—Г —З–µ–ї–Њ–≤–µ–Ї—Г –і–Њ–ї–ґ–µ–љ –±—Л—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Л–Љ. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤—А–∞—З—Г –ї—О–±–Њ–є —Б–њ–µ—Ж–Є–∞–ї—М–љ–Њ—Б—В–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Ј–љ–∞—В—М –≤—Б–µ —В–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є —В–µ—З–µ–љ–Є—П –°–Ф, –Њ –Ї–Њ—В–Њ—А—Л—Е –≥–Њ–≤–Њ—А–Є–ї–Њ—Б—М —А–∞–љ–µ–µ.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
- Morris N.J., Wang S.L., Stevens L.K. et al. Mortality and causes of death in the WHO Multinational Study of Vascular Disease in Diabetes // Diabetol. 2001. Vol. 44 (Suppl. 2). S. 1 4–21.
- Herlitz J., Maimberg K., Karlson B.W. et al. Mortability and morbidity during a five-year follow-up of diabetics with myocardial infarction // Acta Med. Scand. 1988. Vol. 224 (1). P. 31–38.
- –Ь–∞—Б–ї—П–µ–≤–∞ –Ы.–Т., –°—В–∞—А—З–µ–љ–Ї–Њ –Ґ. –У. –Э–∞—А—Г—И–µ–љ–Є–µ —А–Є—В–Љ–∞ –Є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є —Б–µ—А–і—Ж–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞ // –Ь–∞—В–µ—А–Є–∞–ї—Л –њ–µ—А–≤–Њ–≥–Њ –≤—Б–µ—А–Њ—Б—Б–Є–є—Б–Ї–Њ–≥–Њ —Б—К–µ–Ј–і–∞ –∞—А–Є—В–Љ–Њ–ї–Њ–≥–Њ–≤. –Ь., 2005. –°. 72–74.
- Osgren C.J. et al. Atrial fibrillation and its association with type 2 diabetes and hypertension in a Swedish community // Obes. Metab. 2004.Vol. 6. P. 367–374.
- Rywic S.L. et al. Heart failure in patients seeking medical help in outpatients clinics. Pt I. General characteristics // Eur. J. Heart Fail. 2000. Vol. 2, № 4. P. 413–421.
- –Э–µ—Б—В–µ—А–Њ–≤–∞ –Ш.–Т. –Є –і—А. –Р—А–Є—В–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞ –±–Њ–ї—М–љ—Л—Е —Б –•–°–Э –њ—А–Є —Б–Њ—Е—А–∞–љ–µ–љ–љ–Њ–Љ —Б–Є–љ—Г—Б–Њ–≤–Њ–Љ —А–Є—В–Љ–µ –Є –њ–Њ–і—Е–Њ–і –Ї –µ–µ —Г–ї—Г—З—И–µ–љ–Є—О // –Т–µ—Б—В–љ–Є–Ї –∞—А–Є—В–Љ–Њ–ї–Њ–≥–Є–Є. 2–3. № 31. –°. 20–25.
- –Ш–Ј–Љ–∞–є–ї–Њ–≤ –Р.–Ф., –Ъ–Њ–ї–Њ–Љ–Є–љ –Х.–Ѓ., –Ъ–∞—А–њ–Њ–≤ –†. –°. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ —Н–њ–Є–Ј–Њ–і–Њ–≤ –Є—И–µ–Љ–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Є –љ–∞—А—Г—И–µ–љ–Є—П —А–Є—В–Љ–∞ —Б–µ—А–і—Ж–∞ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ —Б—Г—В–Њ—З–љ–Њ–≥–Њ –Љ–Њ–љ–Є—В–Њ—А–Є—А–Њ–≤–∞–љ–Є—П –≠–Ъ–У —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б –Є–љ—Б—Г–ї–Є–љ–љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ // –Т–µ—Б—В–љ–Є–Ї –∞—А–Є—В–Љ–Њ–ї–Њ–≥–Є–Є. 2000. № 3. –°. 21–25.
- Ryden L., Standl E., Bartnic M. et al. Task Force on Diabetes and Cardiovascular Diseases of the European Society of Cardiology; Eiropean Association for the Study of Diabetes. Guidelines on diabetes, pre-diabetes, and cardiovascular diseases: executive summary // Eur. Heart J. 2007. Vol. 28 (1). P. 88–136.
- Woodward M., Patel A., Zoungas S. et al. Does glycemic control offer similar benefits among patients with diabetes in different regions of the world? Results from the ADVANCE trial // Diabetes Care. 2011. Vol. 34 (12). P. 2491–2495.
- Low fasting plasma glucose levels as a predictor of cardiovascular disease and all-cause mortality // Circulation. 2000. Vol. 101. P. 2047–2052.
- Drzewoski J., Zurawska-Klis M. Effect of gliclazide modified release on adiponectin, interleukin-6. And tumor necrosis factor-alpha plasma levels in individuals with type 2 diabetes mellitus // Curr. Med. Res. Opin. 2006. Vol. 22(10). P. 1921.
- Papanas N., Tziakas D., Chalikias G. et. al. Gliclazide treatment lowers serum ICAM-1 levels in poorly controlled type 2 diabetic patients // Diabetes Metab. 2006. Vol. 32 (4). P. 344, 671–674.
- Patel A., MacMahon S., Chalmers. J. et al., ADVANCE Collaborative Group 2008. Intensive blood glucose control and vascular outcomes in patients with type 2 diabetes // N. Engl. J. Med. 2008. Vol. 358. P. 2560–2572.
- Intensive blood-glucose control with sulphonilureas or insulin compared with conventional treatment and risk of complications in patiemts with type 2 diabetes (UKPDS 33). UK Prospective Diabetes Study Group // Lancet. 1998. Vol. 352. № 9131. –†. 837–853.
- –Ф–∞–≤—Л–і–Њ–≤ –Р.–Ы., –С–∞—А–∞–љ–Њ–≤–∞ –Ы. –Ѓ. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –≥–Є—Б—В–Њ- –Є —Г–ї—М—В—А–∞—Б—В—А—Г–Ї—В—Г—А–љ–Њ–є –Њ—А–≥–∞–љ–Є–Ј–∞—Ж–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –Є —Б—В–µ–љ–Ї–Є —Б–Њ—Б—Г–і–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ —В–Є–њ–∞ 2 // –Я—А–Њ–±–ї–µ–Љ—Л —Н–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є–Є. 2005. № 3. –°. 21–25.
- –Э–Є–Ї–Њ–ї–∞–µ–≤ –Э.–Р. –Є –і—А. –Т–љ–µ–Ј–∞–њ–љ–∞—П –Ї–Њ—А–Њ–љ–∞—А–љ–∞—П —Б–Љ–µ—А—В—М // –°–µ—А–і—Ж–µ. 2006. –Ґ. 5–± № 5. –°. 265–267.
- Risk factors in coronary atherosclerosis athero-inflammation // Thromb. J. 2003. Vol.1, № 1. –†.4.
- Mazzone T., Chait A., Plutsky J. Cardiovascular disease risk in type 2 diabetes mellitus: Insights from mechanistic studies // Lancet. 2008. Vol. 371. P. 1800–1809.
- Meier M., Hummel M. Cardiovascular disease and intensive glucose control in type 2 diabetes mellitus: moving practice toward evidence-based strategies // Vasc. Health Risk. Manag. 2009. Vol. 5. P. 859–871.
- Haffner S. M., Lehto S., Ronnemaa T. et al. Mortality from coronary heart disease in subjects with type 2 diabetes and in nondiabetes subjects with and without prior myocardial infarction // N. Engl. J. Med. 1998. Vol. 339. P. 229–234.
- Coutinho M., Genstein H. C. The relationship between glucose and incident cardiovascular events; met regression analysis of published data 20 studies of 95783 individuals followed for 12?4 years // Diabetes Care. 1999. P. 223–240.
- Ajjan R.A., Grant P. J. Cardiovascular disease prevention in patients with type 2 diabetes: The role of oral anti-diabetic agents // Diab. Vasc. Dis. Res. 2006. Vol. 3(3). P. 147–158.
- Hemmingsen B., Lund S., Wetterslev J., Vaag A. Oral hypogkycaemic agents, insulin resistence and cardiovascular disease in patients with type 2 diabetes // Eur. J. Endocrinol. 2009. Vol. 161. P. 1–9.
- –Р—А—Г—В—О–љ–Њ–≤ –У. –Я. –°–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В –Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј. –Ъ–∞–Ї–Њ–≤–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ–∞—П —Б—В—А–∞—В–µ–≥–Є—П —Б–і–µ—А–ґ–Є–≤–∞–љ–Є—П –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞? // –°–µ—А–і—Ж–µ. 2004. № 1 (13). –°. 36–40.
- Johnson J.A., Simpson S.H., Majumdar S.R., Toth E. L. Decreased mortality associated with the use of metformin compared with sulfonylurea monotherapy in type 2 diabetes // Diabetes Care. 2002. Vol. 25. P. 2244–2248.
- –°—В–∞—А–Њ—Б—В–Є–љ–∞ –Х. –У. –Ф—А–µ–≤–∞–ї—М –Р. –Т. –С–Є–≥—Г–∞–љ–Є–і—Л –≤ –ї–µ—З–µ–љ–Є–Є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞. –Ь.: –Ь–µ–і–њ—А–∞–Ї—В–Є–Ї–∞, 2000. 104 —Б.
- –Ф–µ–і–Њ–≤ –Ш.–Ш., –Ь–µ–ї—М–љ–Є—З–µ–љ–Ї–Њ –У.–Р., –§–∞–і–µ–µ–≤ –Т. –§. –≠–љ–і–Њ–Ї—А–Є–љ–Њ–ї–Њ–≥–Є—П: —Г—З–µ–±–љ–Є–Ї –і–ї—П –≤—Г–Ј–Њ–≤. –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2007. 432 —Б.
- Paternostro G., Pagano D., Gnecchi-Ruscone T. et al. Insulin resistance in patients with cardiac hypertrophy // Cardiovasc. Res. 1999. Vol. 42. P. 246–253.
- Davis C.L., Kapuku G., Snieder H. et al. Insulin resistance syndrome and left ventricular mass in healthy young people /// Am J. Med. Sci. 2002. Vol. 324. P. 72–75.
- De Kreutzenberg S.v. , Avogaro A., Tiengo A. et al. Left ventricular mass in type 2 diabetes mellitus. A study employing a simple ECG index: the Cornell voltage // J. Endocrinol. Invest. 2000. Vol. 23. P. 139–144.
- Hintz K.K., Ren J. Prediabetic insulin resistance is not permissive to the development of cardiac resistance to insulin-like growth factor I in ventricular myocytes // Diabet. Res. Clin. Pract. 2002. Vol. 55. P. 89–98.
- Investigating the dual nature of endothelin-1: ischemia or direct arrhethmogenic effect / T.Szabo, B. Merkely // Life Sci. 2000. Vol.66, № 26. P. 2527–2541.
- Dead in bed syndrome — a hypothesis // Diabetes Obes. Metab. 2006. Vol. 8. P. 261–263.
- Lee S.P. et. al. Influence of autonomic neuropathy on QT interval lengthening during hypoglycemia in type 1 diabetes // Diabetes. 2004. Vol. 53. P. 1535–1542.
- Kannel W.B., McGee D.L., Diabetes and cardiovascular disease: the Framingham study // JAMA. 1979. Vol. 241. P. 2035–2038.
- Nichols G.A., Hillier T.A., Erbey J.R. et al. Congestive heart failure in type 2 diabetes: prevalence, incidence, and risk factors // Diabetes Care. 2001. Vol. 24. P. 1614–1619.
- –Р–±–і–∞–ї–Ї–Є–љ–∞ –Х. –Э. –°–Њ—Б—В–Њ—П–љ–Є–µ –і–Є–∞—Б—В–Њ–ї–Є—З–µ—Б–Ї–Њ–є —Д—Г–љ–Ї—Ж–Є–Є –Љ–Є–Њ–Ї–∞—А–і–∞ –ї–µ–≤–Њ–≥–Њ –ґ–µ–ї—Г–і–Њ—З–Ї–∞ —Г –±–Њ–ї—М–љ—Л—Е –Ш–С–° —Б –љ–∞—А—Г—И–µ–љ–љ–Њ–є —В–Њ–ї–µ—А–∞–љ—В–љ–Њ—Б—В—М—О –Ї –≥–ї—О–Ї–Њ–Ј–µ // –Ґ—А–µ—В–Є–є –†–Њ—Б—Б–Є–є—Б–Ї–Є–є –і–Є–∞–±–µ—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –Ї–Њ–љ–≥—А–µ—Б—Б. –Ґ–µ–Ј. –і–Њ–Ї–ї. –Ь., 2004. –°. 17–218.
- –Ф–µ–і–Њ–≤ –Ш.–Ш., –Р–ї–µ–Ї—Б–∞–љ–і—А–Њ–≤ –Р.–Р, —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –Ш–С–° —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞: —А–Њ–ї—М –≥–Є–њ–µ—А—Б–Є–Љ–њ–∞—В–Є–Ї–Њ—В–Њ–љ–Є–Є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –µ–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є // –Ъ–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є. –Ь–µ–і–Є—Ж–Є–љ–∞. 2003. № 2. 34 —Б.
- Juutilainen A. Gender difference in the impact of type 2 diabetes on coronary heart disease risk // Diabet. Care. 2004. Vol. 27. P. 2898–2904.
- Schannwelll C.M., Schneppengeim M., Perings S. et al. Left ventricular diastolic dysfunction as an early manifestation of diabetic cardiomyopathy // Cardiol. 2002. Vol. 98. № 1–2. P. 33–39.
- Cabou C., Campistron G., Marsollier N. et al. Brain glucagonlike peptide-1 regulates arterial blood flow, heart rate, and insulin sensitivity // Diabetes. 2008. Vol. 57 № 10. P. 2577–2787.
- Krinsley J. S. Glycemic variability: a strong independent predictor of mortality in critically ill patients // Crit. Care Med. 2008. Vol. 36. P. 3008–3013.
- Ceriello A. et al. Oscillating glucose is more deleterious to endothelial function and oxidative stress than mean glucose in normal and type 2 diabetic parients // Diabetes. 2008. Vol. 57, № 5. P. 1349–1354.
- Palatini P., Julius P., Julius S. The role of cardiac autonomic function in hypertension and cardiovascular disease // Curr. Hypertens. Rep. 2009. Vol. 11, № 3. P. 199–205.
- Ihnat M.A., Kaltreider R.C., Thorpe J. E. Attenuated speroxide dismutase induction in retinal cells in response to intermittent high versus continuous high glucose // Am. J. Biochem. Biotech. 2007. Vol. 3. P. 16–23.

















