|
Н |
аличие тяжелого ожирения связано с повышенным артериальным давлением (АД) [1], высоким почечным плазмотоком [2–4], повышенной скоростью клубочковой фильтрации (СКФ) [2,5] и усиленной экскрецией альбумина с мочой [6,7]. Ранее мы изучали клубочковую гемодинамику у пациентов с тяжелым ожирением путем измерения фракционного клиренса декстранов [8]. Анализ прохождения декстранов с использованием теоретической модели транспорта макромолекул через гетеропорную мембрану показал, что клубочковое капиллярное ложе подвергалось повышенному транскапиллярному гидростатическому градиенту давления, что привело к гиперфильтрации. Кроме данных физиологических аномалий многие авторы связывают ожирение с развитием нефротического синдрома и почечной недостаточностью [9–19]. Связанная с ожирение гломерулопатия не так давно была определена морфологически как гломеруломегалия с или без фокального сегментарного гломерулосклероза [20]. Ожирение также может ускорять течение идиопатической гломерулярной болезни, такой как IgA–гломерулопатии [21]. Распространенность связанной с ожирением гломерулопатии, которая может привести к терминальной почечной недостаточности, в течение последних 15 лет увеличилась в 10 раз вследствие «эпидемии» ожирения [22]. Хотя до конца не доказана причинно–следственная связь между клубочковой гиперфункцией при ожирении и развитием нефротического синдрома с почечной недостаточностью, экспериментальные и клинические данные показывают, что гиперфильтрация и гломеруломегалия могут привести к поражению клубочков. Поэтому снижение клубочковой гиперфильтрации может быть эффективным путем профилактики или отсрочки развития почечной патологии при ожирении.
Целью настоящего исследования явилась оценка влияния снижения массы тела на обратимость гломерулярной дисфункции у больных ожирением без развившейся патологии почек.
Материалы и методы
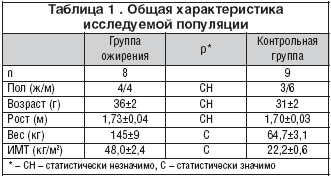
Исследуемая популяция
В данном исследовании приняли участие 17 волонтеров (10 женщин и 7 мужчин) в возрасте от 23 до 46 лет. 8 человек страдали тяжелым ожирением (ИМТ>38 кг/м2) и 9 были здоровы и служили контрольной группой. Участники не страдали какой–либо почечной патологией. Никто не получал лечение по поводу гипертензии, сахарного диабета или других хронических заболеваний. У всех выявлен нормальный уровень сывороточного креатинина и отрицательный результат по тест–полоскам для измерения уровня экскреции белка с мочой. Характеристика обеих групп представлена в таблице 1. Распределение по возрасту и полу было сходно в обеих группах. Вес группы больных ожирением в 2 раза превышал вес контрольной группы. ИМТ группы ожирения варьировал между 8,1 и 61,3 кг/м2 у всех кроме одного пациента, который страдал морбидным ожирением, определяемым как ИМТ более 40. Систолическое и диастолическое АД больных с ожирением составило 143±6 (от 122 до 173) и 80±3 (от 66 до 92) мм рт.ст. соответственно. Один пациент страдал АГ 2–й степени (систолодиастолической) и 4 больных – 1–й степени (систолической). Никто не получал лечение по поводу АГ. 3 пациента не страдали АГ. Систолическое и диастолическое АД контрольной группы составило 120±2 мм рт.ст. (от 108 до 129) и 70±3 мм рт.ст. (от 56 до 82) соответственно.
Протокол исследования
Пациентам проводился пероральный глюкозо–толерантный тест (ПГТТ) и функциональные почечные тесты. ПГТТ выполнялся с 8 утра после 10 ч голодания. Пациенты получали 75 г глюкозы, разведенной в воде. Образцы крови забирались через венозный катетер за 10 и 1 мин до и через 60 и 120 мин после введения глюкозы для измерения уровня глюкозы плазмы крови и инсулина. Образцы мочи, полученные за 1 нед. до выполнения почечных функциональных проб, оценивались на уровень мочевины, креатинина и содержания натрия. Функциональные почечные пробы выполнялись на 4–5 дней позже у всех пациентов. Обследование пациентов проводилось в 8 утра после легкого завтрака с низким содержанием белка. Пациенты находились в положении лежа, им устанавливались катетеры в обе руки для инфузии маркеров клиренса и забора крови. Начальная доза инулина составила 50 мг/кг, р–аминогиппуриновой кислоты (РАГ) – 8 мг/кг и декстрана 40–130 мг/кг. Инулин, РАГ и декстран 40 затем вводились медленно капельно. Водная нагрузка (15 мл/кг) давалась в течение первых 60 мин. Четыре определенных по времени сбора мочи производились при самостоятельном мочеиспускании. Периферическая венозная кровь забиралась в рамках каждого сбора мочи. АД измерялось во время каждого сбора мочи.
Пациентам с ожирением проводилась гастропластика с 1–й по 3–ю нед. после выполнения функциональных почечных проб. Почечные функциональные пробы и ПГТТ повторялись не менее чем через 12 мес. после хирургического вмешательства по такому же протоколу.
Девять пациентов контрольной группы и 6 из 8 пациентов с ожирением были частью большой группы, включенной в исследование клубочковой гемодинамики при ожирении [8]. Раствор декстрана 40 вводился для измерения коэффициента прохождения макромолекул у всех участников – пациентов с ожирением, до и после снижения веса, и в контрольной группе. Анализ коэффициента прохождения декстрана в контрольной группе и у лиц с ожирением до хирургического лечения было предметом нашего начального сообщения [8]. Сывороточная и концентрация в моче декстрана не измерялись после снижения веса. Однако раствор декстрана вводился для достижения стандартных условий во время исследования до и после снижения веса.
Лабораторные процедуры
Концентрация инулина и РАГ в моче и плазме определялась колориметрическими методами [23,24]. Уровень глюкозы плазмы, альбумина сыворотки крови, пре–альбумина, сывороточного трансферрина, общее число лимфоцитов и мочевины мочи, креатинин и натрий измерялись с помощью стандартной лабораторной методики. Инулин сыворотки крови измерялся с помощью RIA (Sorin biomedica, Италия). Альбумин мочи измерялся нефелометрическими методами (Beckman, Ирландия).
Расчеты
СКФ определялась по среднему клиренсу инулина. Почечный плазмоток вычислялся путем деления среднего РАГ клиренса на установленное отношение почечного выведения РАГ, умноженное на 0,9. Отношение мочевина/креатинин мочи (мг/мг) и натрий/креатинин (мЕД/мг) использовались для оценки изменения потребления белка и натрия после снижения веса. Среднее АД вычислялось как ДАД +1/3 пульсового давления. Изменения СКФ (ΔСКФ), ИМТ (ΔИМТ), площади под кривой глюкозы и инсулина (ΔAUCглюк и ΔAUCинс) и САД (ΔСАД) после снижения веса выражались в % от начальных значений.
Результаты
Пациенты с ожирением потеряли 48 кг веса в течение от 12 до 17 мес., с 145±9 до 97±7 кг (р<0,0005), и ИМТ снизился на 16 единиц, с 48±2,4 до 32,1±1,5 кг/м2 (p<0,0001). Несмотря на такое снижение ИМТ остался повышенным в сравнении с контролем – 22,2±1,7, р<0,0001.
ПГТТ
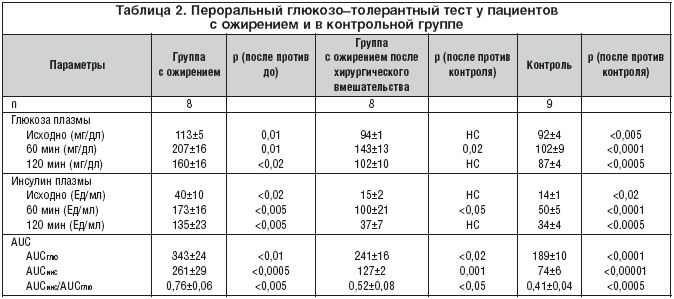
В таблице 2 суммированы результаты ПГГТ. Уровень глюкозы в крови натощак был выше в группе ожирения в сравнении с контролем, все значения были ниже 140. Уровень инсулина натощак был повышен почти в 3 раза в группе ожирения. Площадь под кривой (AUCглю) глюкозы и инсулина в группе ожирения были повышены на
80 и 250% соответственно, в сравнении с контролем. Отношение площадей под кривой «инсулин к глюкозе» в группе ожирения было повышено на 85%, что указывает на инсулинорезистентность.
После хирургического вмешательства уровень глюкозы натощак и инсулина значительно снизился. Отношение площадей под кривой «инсулин к глюкозе» снизилось на 32%, достигая значния 27% сверх нормального. Эти результаты указывают на улучшение инсулинорезистентности.
Нутриционные параметры
Отношение мочевина/креатинин мочи снизилось с 17,1±1,9 до 11,8±1,3 (р<0,05) после снижения веса. Отношение натрий/креатинин мочи снизилось с 0,16 ±0,01 до 0,12±0,02 (р<0,05). Альбумин сыворотки крови составил 4,2±0,1 до хирургического вмешательства и 4,3±0,1 мг/дл после снижения веса (СН). Преальбумин сыворотки крови составил 27,3±3,1 до и 25,3±1,0 мг/дл после снижения веса (СН). Трансферрин сыворотки крови был 312±13 до и 314±21 мг/дл после снижения веса (СН). Общее число лимфоцитов составило 1946±186 до и 1728±146/мм3 после снижения веса (СН).
Динамика фильтрации
Динамика фильтрации и артериального давления (АД) показаны в таблице 3. В группе больных с ожирением, САД было в пределах нормальных значений. Диастолическое и среднее АД были нормальными. Однако эти значения были выше чем в контрольной группе.
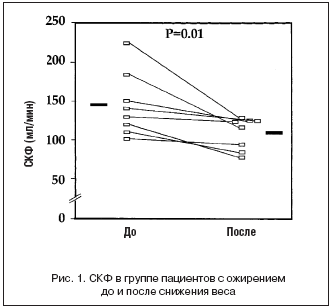
СКФ была на 61% выше в группе ожирения, чем в контроле. Она была повышена у 6 из 8 пациентов. Повышение почечного плазмотока было пропорционально меньше, в среднем на 32%. Повышение СКФ было, таким образом, связано с повышением фильтрационной фракции. После снижения веса СКФ и ПП снизились на 24 и 13% соответственно (рис. 1 и 2). САД снизилось на 10 мм рт.ст. ДАД осталось на таком же уровне, и среднее АД снизилось незначительно.
Экскреция альбумина с мочой
После снижения веса, уровень экскреции альбумина с мочой снизился с 16 μг/мин (4 до 152 μг/мин) до 5 г/мин (от 3 до 37 μг/мин), р<0,01 и фракционный клиренс альбумина снизился с 3,2х10–6 (1,1 до 23х10–6) до 1,2х10–6 (0,5 до 6,8х10–6), р<0,02.
Предикторы изменения СКФ
По унивариантному анализу ΔСКФ коррелировала с ΔAUCглю (r=0,76, р<0,03). Корреляция между ΔСКФ и ΔИМТ достигла статистической значимости (r=0,69, р=0,059). ΔAUCинс (r=0,33, р=СН) и ΔСАД (r=0,37, р=СН) не были предикторами ΔСКФ. При мультивариантном анализе следование ΔСАД за ΔAUCглю привело к увеличению корреляции с ΔСКФ, r=0,95, р=0,01.
Обсуждение
Данное исследование показало, что такие нарушения почечной гемодинамики, как, например повышенные СКФ, ПП, альбуминурия, связаны с тяжелым ожирением и значительно улучшаются после снижения веса. Ранее было показано [2–4,8], что вызванная ожирением гиперфильтрация связана с повышением ПП, что дает основание думать о состоянии почечной вазодилатации, в особенности афферентной артериолы. Группа больных ожирением имела более высокое САД и АДср, чем контроль. Мы ранее анализировали АД по прохождению макромолекул в клубочке при помощи гетеропорной модели, имитирующей селективность клубочка [8], в группе из 12 больных, страдающих ожирением крайней степени выраженности (в группу вошли 6 из 8 пациентов, участвующих в настоящем исследовании). Данный анализ показал, что повышенный транскапиллярный градиент давления играет роль в повышении СКФ, повышенное клубочковое давление возникает за счет трансмиссии повышенного аритериолярного давления через дилатированную клубочковую афферентную артериолу.
После снижения веса СКФ, ПП и ФФ значимо снизились. ПП нормализировался, в то время как СКФ осталась немного повышенной. Данное улучшение было связано со снижением альбуминурии. Это уменьшение альбуминурии было вызвано снижением не СКФ, а фракционного клиренса альбумина.
Настоящее исследование – первое, которое показывает, что СКФ, ПП и МАУ снижаются после снижения веса у пациентов, страдающих ожирением. Лишь в 1 работе ранее опубликованы данные по влиянию снижения веса на почечную функцию [5], которое показало, что СКФ снижается после интестинального хирургического вмешательства с наложением обходного пути у пациентов с ожирением. Однако в том исследовании не было данных по ПП, АЛ и альбуминурии. Кроме того, состояние мальабсорбции, ассоциированное с наложением обходного пути, зачастую ведет к значимой мальнутриции. В настоящем исследовании пациентам выполнялась гастропластика и не выявлено биохимических маркеров мальнутриции после снижения веса.
Мы хотим подчеркнуть, что СКФ в настоящем исследовании не была скорректирована по площади поверхности тела. Число нефронов не увеличивается с увеличением жировой ткани, следовательно, ожирение должно приводить к увеличению СКФ отдельных нефронов. Абсолютная СКФ отражает данный феномен, в то время как скорректированная СКФ скрывает это. Мы проанализировали данную информацию путем использования данной нескорректированной, абсолютной СКФ.
Каковы отдаленные последствия улучшения гемодинамических возможностей клубочка?
Вызванная ожирением патология почек была впервые выявлена почти 3 декады назад [9]. За прошедшее время опубликовано множество статей [10–20]. Эта гломерулопатия часто дебютирует в виде нефротического синдрома, с или без почечной недостаточности. Распространенность клубочковой патологии среди больных ожирением неизвестна. В недавней публикации было сообщено, что распространенность вызванной ожирением гломерулопатии, морфологически определенной как гломеруломегалия с или без фокального гломерулосклероза, выросла в 10 раз за последние 15 лет [20]. Патогенез заболевания неизвестен. Однако, учитывая, что клубочки пациентов с тяжелым ожирением подвергаются повышенному транскапиллярному фильтрационному градиенту давления и повышенному уровню фильтрации [8], интересно предположение о том, что эти физиологические аномалии лежат в основе повреждения клубочков. Brenner и соавт. [25,26] 2 десятилетия назад предположили, что адаптивные изменения клубочка происходят после снижения функциональной массы почки, и эти изменения лежат в основе начала и прогрессирования гломерулосклероза. Клубочковая гипертензия, гиперфильтрация и АГ ведут к истончению капиллярной стенки клубочка, поражению клеток эндотелия и эпителия и транссудации макромолекул в мезангиум [27]. Это приводит к мезангиальной перегрузке и дисфункции [28,29] и со временем к разрастанию мезангия и склерозу [30]. Данный механизм, подтвержденный экспериментальными данными, предположительно вносит вклад в прогрессирование диабетической нефропатии в диабетической почке с гиперфильтрацией [31,32]. Клубочковая гиперфильтрация и гипертензия связаны с гипертрофией клубочоков в оставшейся части модели почки и модели диабетической почки. Предполагается, что гипертрофия клубочка также приводит к развитию гломерулосклероза [33] путем повышения напряжения стенки клубочка [34] и натяжения и поражения эпителиальных клеток клубочка [35].
Как было показано в настоящем исследовании и ранее проведенных работах [2,5,8], почка пациента с ожирением разделяет функциональные патологии, такие как почечная вазодилатация и гиперфильтрация, с диабетической почкой, делая ее восприимчивой к поражению. Важно, что снижение площади под кривой глюкозы после снижения веса было предиктором изменения СКФ. Однако данная находка не обязательно является причиной и влияет на взаимоотношение между нарушенной толерантностью к глюкозе и гиперфильтрацией и может отражать тот факт, что оба фактора независимо улучшают последующее снижение веса.
В настоящем исследовании повышенный ПП и СКФ снижались после уменьшения веса. Опираясь на факт, что число клубочков остается неизменным в течение исследования, данное изменение отражает снижение плазмотока отдельного нефрона и СКФ отдельного нефрона. Снижение ПП говорит о том, что афферентная артериола клубочка стала менее дилатированной, таким образом передавая меньшее давление на капиллярное ложе клубочка. Снижение капиллярного гидростатического давления (КГД) даже более заметно, поскольку системное АД также снижается. Таким образом, капиллярное гидростатическое давление снизилось с помощью 2 механизмов: снижения системного АД и повышения резистивности афферентной артериолы. Кроме того, снижение ПП может повлиять на СКФ независимо от изменений гидростатического давления: это снижение предположительно вызывает повышение интралюминальной концентрации макромолекул, поскольку кровяные потоки максимальны вдоль капилляров клубочка [36]. Это приводит к повышению интракапиллярного онкотического давления клубочка, таким образом уменьшаются силы, способствующие клубочковой ультрафильтрации. Важно, что СКФ снизилась у всех пациентов в настоящем исследовании, ПП не снизился у 2 из этих пациентов. Причина дисбаланса между изменениями СКФ у всех пациентов и недостаточным снижением ПП неизвестен. У одного пациента из двоих ПП был в пределах нормальных значений до снижения веса – факт, который может объяснить недостаточное изменение после снижения веса. Однако данная находка противоречит данным, что СКФ может изменяться вне зависимости от изменения ПП.
В итоге фракционная экскреция альбумина снизилась вслед за снижением веса. Механизмы, связывающие нарушения клубочковой гемодинамики и фракционный клиренс альбумина, непонятны. Повышенный фракционный клиренс альбумина может быть теоретически связан с нарушением селективности клубочковой мембраны по размеру или по заряду или со снижением тубулярного катаболизма альбумина. Исследование коэффициента прохождения молекул фракционированного декстрана показало, что МАУ не связана с нарушением селективности по размеру [37]. Таким образом, повышенная экскреция альбумина может возникать вследствие нарушения селективности клубочка по заряду или снижения тубулярного катаболизма. Результаты недавних исследований позволяют выдвинуть версию, что повышенное клубочковое давление может повышать экскрецию альбумина путем влияния на метаболизм клеток клубочка:β, который может повреждать лизосомальные ферменты активности в клетках канальцев [41,42]. Это ведет к повышенной экскреции альбуминов с мочой независимо от нарушенной клубочковой селективности, как показано на модели вызванной гипертензией альбуминурии [42]. Далее повышенная экскреция альбумина у пациентов без сахарного диабета может привести к системной эндотелиальной дисфункции, независимо от местных гемодинамических нарушений клубочка. Ожирение связно с эндотельной дисфункцией [43–47], которая является одним из факторов, учитывающихся при повышенной сердечно–сосудистой заболеваемости среди лиц с ожирением [48,49]. Таким образом, возможно, что снижение альбуминурии после уменьшения веса отражает положительное влияние похудения на интегральный показатель системной капиллярной сети. Несмотря на патогенез альбуминурии пациентов с ожирением пониженная фракционная экскреция альбумина после снижения веса отражает улучшенную клубочковую и/или системную капиллярную функцию.
Улучшение клубочковой гемодинамики после снижения веса, показанное в настоящем исследовании, было связано со снижением АД, которое коррелирует при мультивариантном анализе с изменениями СКФ. Reisin и соавт. [50] показали, что снижение веса у пациентов с АГ и избыточным весом приводит к снижению АД и что это снижение не зависит от снижения потребления соли. Hall и соавт. [51] на экспериментальной модели доказали, что ожирение связано со значимой задержкой натрия. Hall [52] предположил, что повышенная канальцевая реабсорбция натрия приводит к сниженной доставке соли к maculа densa, что ведет к вазодилатации артериол клубочка и повышению ПП и СКФ. Эта гипотеза связывает вызванную ожирением гипертензию и гиперфильтрацию. Снижение СКФ и АД после снижения веса совместимо с этой гипотезой, однако ее еще надо доказать.
Данное исследование поведено среди пациентов, не страдающих почечной патологией. Гиперфильтрация может играть роль не только в патогенезе гломерулопатии при ожирении, но и в прогрессировании других гломерулопатий. Недавнее исследование показало, что IgA–нефропатия прогрессирует быстрее у пациентов с ожирением, чем у пациентов с нормальным весом [21]. Эта находка и результаты настоящего исследования говорят о том, что снижение веса может положительно влиять на течение хронической почечной недостаточности путем снижения клубочковой гиперфильтрации при ожирении. Таким образом, в связи с увеличивающейся распространенностью ожирения [22] и патологии почек при ожирении [20,21] эти результаты имеют важную теоретическую и практическую ценность.
in Patients with Severe Obesity»,
J Am Soc Nephrol 2003; 14: 1480–1486.


Литература
1. Must A, Spadano J, Coakley FH, Field AE, Colditz G, Dietz WH: The disease burden associated with overweight and obesity. JAMA 282: 1523–9, 1999
2. Ribstein J, du Cailar G, Mimran A: Combined renal effects of overweight and hypertension. Hypertension 26: 610–615, 1995
3. Reisin E, Messerli FG, Ventura HO, Frohlich ED: Renal haemodynamic studies in obesity hypertension. J Hypertens 5: 397–400, 1987
4. Porter LE, Hollenberg NK: Obesity, salt intake and renal perfusion in healthy humans. Hypertension 32:144–148, 1998
5. Brochner–Mortensen J, Rickers H, Balslev I: Renal function and body composition before and after intestinal bypass operation in obese patients. Scand J Clin Lab Invest 40: 695–702, 1980
6. Metcalf P, Baker J, Scott A, Wild C, Scragg R, Dryson E: Albuminuria in people at least 40 years old: Effect of obesity, hypertension, and hyperlipidemia. Clin Chem 38: 1802–1808, 1992
7. Valensi P, Assayag M, Busby M, Paries J, Lormeau B, Attali JR: Microalbuminuria in obese patients with or without hypertension. Int J Obes Relat Metab Disord 20: 574–579, 1996
8. Chagnac A, Weinstein T, Korzets A, Ramadan E, Hirsch J, Gafter U: Glomerular hemodynamics in severe obesity. Am J Physiol Renal Physiol 278: F817–F822, 2000
9. Weisinger JR, Kempson RL, Eldridge FL, Swensen RS: The nephrotic syndrome: A complication of massive obesity. Ann Intern Med 81: 440–447, 1974
10. Kasiske BL, Crosson JT: Renal disease in patients with massive obesity. Arch Intern Med 146: 1105–1109, 1986
11. Warnke RA, Kempson RL: The nephrotic syndrome in massive obesity: A study by light, immunofluorescence and electron microscopy. Arch Pathol Lab Med 102: 431–438, 1978
12. Wesson DE, Kurtzman NA, Frommer JP: Massive obesity and nephrotic proteinuria with a normal renal biopsy. Nephron 40:235–237, 1985
13. Jennette JC, Charles L, Grubb W: Glomerulomegaly and focal segmental glomerulosclerosis associated with obesity and sleep apnea syndrome. Am J Kidney Dis 10: 470–472, 1987
14. Lamas S, Sanz A, Ruiz A, Alvarez J, Mejia F, Rodriguez–Puyol D: Weight reduction in massive obesity associated with focal segmental glomerulosclerosis: Another evidence for hyperfiltration? Nephron 56: 225–226, 1990
15. Bailey RR, Lynn KL, Burry AF, Drennan C: Proteinuria, glomerulomegaly and focal glomerulosclerosis in a grossly obese man with obstructive sleep apnea syndrome. Aust N Z J Med 19:473–474, 1989
16. Shimomura Y, Murakami M, Shimizu H, Uehara Y, Takahasi M, Inukai T, Kobayashi I, Kobayashi S: Improvement of nephrotic syndrome in a massively obese patient after weight loss and treatment with an anti allergic drug. J Med 21: 337–347, 1990
17. Praga M, Hernandez E, Adres A, Leon M, Ruilope LM, Rodicio JL: Effects of body–weight loss and captopril treatment on proteinuria associated with obesity. Nephron 70: 35–41, 1995
18. Praga M, Morales E, Herrero JC, Perez–Campos A, Dominguez–Gil B, Alegre R, Vara J, Martinez MA: Absence of hypoalbuminemia despite massive proteinuria in focal segmental glomerulosclerosis secondary to hyperfiltration. Am J Kidney Dis 33:52–58, 1999
19. Adelman RD, Restaino IG, Alon US, Blowey DL: Proteinuria and focal segmental glomerulosclerosis in severely obese adolescents. J Pediatr 138: 481–485, 2001
20. Kambham N, Markowitz S, Valeri AM, Lin J, D’Agati VD: Obesity–related glomerulonephropathy: an emerging epidemic. Kidney Int 59: 1498–1509, 2001
21. Bonnet E, Deprele C, Sassolas A, Moulin P, Alamartine E, Berthezene F, Bertoux F: Excessive body weight as a new independent risk factor for clinical and pathological progression in primary IgA nephritis. Am J Kidney Dis 37: 720–727, 2001
22. Mokdad AH, Serdula MK, Dietz WH, Bowman BA, Marks JS, Koplan JP: The spread of the obesity epidemic in the United States, 1991–1998. JAMA 282: 1519–1522, 1999
23. Schreiner GE: Determination of inulin by means of resorcinol. Proc Soc Exp Biol Med 74: 117–120, 1950
24. Brun C: A rapid method for determination of paraaminohippuric acid in kidney function tests. J Lab Clin Med 37: 955–958, 1951
25. Brenner BM: Hemodynamically mediated glomerular injury and the progressive nature of kidney disease. Kidney Int 23: 647, 1983
26. Brenner BM, Meyer TW, Hostetter TH: Dietary protein intake and the progressive nature of kidney disease. New Eng J Med 307: 652–660, 1982
27. Olson JL, de Urdaneta AG, Heptinstall RH: Glomerulohyalinosis and its relation to hyperfiltration. Lab Invest 52: 387–398, 1985
28. Grond J, Elema JD: Glomerular mesangium. Analysis of the increased activity observed in experimental acute aminonucleoside nephrosis in the rat. Lab Invest 45: 400–409, 1981
29. Grond J, Schilthius M, Koudstaal J, Elema JD: Mesangial function and glomerular sclerosis in rats after unilateral nephrectomy. Kidney Int 22: 338–343, 1982
30. Rennke HG: Structural alterations associated with glomerular hyperfiltration. Contemp Issues Nephrol 14: 111–131, 1986
31. Hostetter TH, Troy JL, Brenner BM: Glomerular haemodynamics in experimental dialbetes mellitus. Kidney Int 19: 410–413, 1981
32. Rudberg S, Persson B, Dahlquist G: Increased glomerular filtration rate as a predictor of diabetic nephropathy –results from an 8–year prospective study. Kidney Int 41: 822–828, 1992
33. Yoshida Y, Fogo A, Ichikawa I: Glomerular hemodynamic changes vs. hypertrophy in experimental glomerular sclerosis. Kidney Int 35: 654–660, 1989
34. Daniel BS, Hostetter TH: Adverse effects of growth in the glomerular microcirculation. Am J Physiol 258: F1409–F1416, 1990
35. Fries JW, Sandstrom DJ, Meyer TW, Rennke HG: Glomerular hypertrophy and epithelial cell injury modulate progressive glomerulosclerosis in the rat. Lab Invest 60: 205–218, 1989
36. Deen WM, Robertson CR, and Brenner BM: A model of glomerular ultrafiltration in the rat. Am J Physiol 223: 1178–1183, 1972
37. Lemley KV, Blouch K, Abdullah I, Boothroyd DB, Bennett PH, Myers BD, Nelson RG: Glomerular permselectivity at the onset of nephropathy in type 2 diabetes mellitus. J Am Soc Nephrol 11:2095–2105, 2000
38. Hirakata M, Kaname S, Chung UG, Joki N, Hori Y, Noda M, Takuwa Y, Okazaki T, Fujita T, Katoh T, Kurokawa K: Tyrosine kinase dependent expression of TGF–beta induced by stretch on mesangial cells. Kidney Int 51: 1028–1036, 1997
39. Riser BL, Cortes P, Heilig C, Gordin J, Ladson–Wofford S, Patterson D, Narins RG: Cyclic stretching forces selectively upregulates TGF–beta isoforms in culltured rat mesangial cells. Am J Pathol 148: 1915–1923, 1996
40. Li Q, Muragaki Y, Hatamura I, Ueno H, Ooshima A: Stretchinduced collagen synthesis in cultured smooth muscle cells from rabbic aortic media and a possible involvement of angiotensin II and TGF–beta. J Vasc Res 35: 93–103, 1998
41. Scheng O, Ling H, Sebekova K, Vamvakas S, Heidland A: High glucose media enhance the responsiveness of tubular cells to growth promoters: Effect on lysosomial cathepsins and protein degradation. Mineral Electrolyte Metab 24: 254–260, 1998
42. Russo LM, Osicka TM, Bonnet F, Jerums G, Comper WD: Albuminuria in hypertension is linked to altered lysosomal activity and TGF–beta1 expression. Hypertension 39: 281–286, 2002
43. Steinberg HO, Chaker H, Leaming R, Johnson A, Brechtel J, Baron AD: Obesity/insulin resistance is associated with endothelial dysfunction: Implications for the syndrome of insulin resistance. J Clin Invest 97: 2601–2610, 1996
44. Arcaro G, Zamboni M, Rossi L, Turcato E, Covi G, Armellini F, Bosello O, Lechi A: Body fat distribution predicts the degree of endothelial cell dysfunction in uncomplicated obesity. Int J Obes 23: 936–942, 1999
45. Perticone F, Ceravolo R, Candigliota M, Ventura G, Iacopino S, Sinopoli F, Mattioli PL: Obesity and body fat distribution induce endothelial dysfunction by oxidative stress. Diabetes 50: 159–165, 2001
46. Suwaidi JA, Higano ST, Holmes DR, Lennon R, Lerman A: Obesity is independently associated with coronary endothelial dysfunction in patients with normal or mildly diseased coronary arteries. J Am Coll Cardiol 37: 1523–1528, 2001
47. Brook RD, Bard RL, Rubenfire M, Ridker P, Rajagopalan S: Usefulness of visceral obesity (waist/hip ratio) in predicting vascular endothelial function in healthy overweight adults. Am J Cardiol 88: 1264–1269, 2001
48. Suwaidi J, Hamasaki S, Higano ST, Nishimura RA, Holmes DR, Lerman A: Long–term follow–up of patients with mild coronary artery disease and endothelial dysfunction. Circulation 101:948–954, 2000
49. Schachinger V, Britten MB, Zeiher AM: Prognostic impact of coronary vasodilator dysfunction on adverse long–term outcome of coronary heart disease. Circulation 101: 1899–1906, 2000
50. Reisin E, Abel R, Modan M, Silverberg DS, Eliahou HE, Modan B: Effect of weight loss without salt restriction on the reduction of blood pressure in overweight hypertensive patients. N Engl J Med 298: 1–6, 1978
51. Hall, JE MW Brands, WN Dixon, and M.J: Smith Jr: Obesity induced hypertension. Renal function and systemic hemodynamics. Hypertension 22: 292–299, 1993
52. Hall JE: Renal and cardiovascular mechanisms of hypertension in obesity. Hypertension 23: 381–394, 1994












