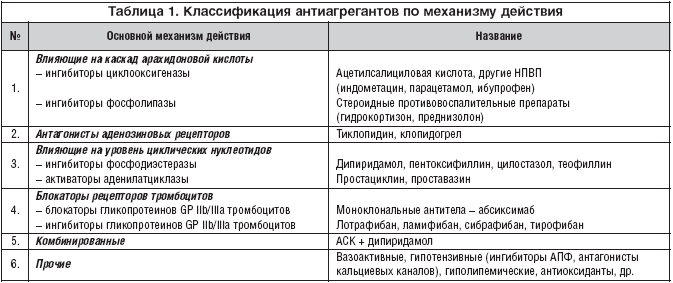
–Я—А–µ–і—Б—В–∞–≤–ї–µ–љ–љ—Л–µ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л —Б–Є–ї—М–љ–Њ —А–∞–Ј–ї–Є—З–∞—О—В—Б—П –њ–Њ —Б–≤–Њ–Є–Љ –Њ—Б–љ–Њ–≤–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ, –љ–Њ –≤—Б–µ —П–≤–ї—П—О—В—Б—П –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є –∞–≥—А–µ–≥–∞—Ж–Є–Є –Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —В–Њ—З–Ї–∞—Е –њ—А–Є–ї–Њ–ґ–µ–љ–Є—П (—В–∞–±–ї. 1).
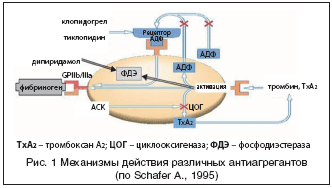
–Ш—Б—В–Њ—А–Є—З–µ—Б–Ї–Є –њ–Њ–ї—М–Ј—Г—О—Й–∞—П—Б—П –љ–∞–Є–±–Њ–ї—М—И–µ–є –њ–Њ–њ—Г–ї—П—А–љ–Њ—Б—В—М—О, –≤ —В–Њ–Љ —З–Є—Б–ї–µ –≤ —Б–Є–ї—Г –µ–µ —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї, –∞—Ж–µ—В–Є–ї—Б–∞–ї–Є—Ж–Є–ї–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ (–Р–°–Ъ) –±—Л–ї–∞ –≤–њ–µ—А–≤—Л–µ –њ–Њ–ї—Г—З–µ–љ–∞ –≤ 1899 –≥–Њ–і—Г —Д–∞—А–Љ–∞—Ж–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ–Љ–њ–∞–љ–Є–µ–є «Bayer». –Т–µ–і—Г—Й–Є–Љ –≤ –Љ–µ—Е–∞–љ–Є–Ј–Љ–µ –і–µ–є—Б—В–≤–Є—П –Р–°–Ъ —П–≤–ї—П–µ—В—Б—П –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–∞—Б–Ї–∞–і –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –њ—Г—В–µ–Љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є—П —Д–µ—А–Љ–µ–љ—В–∞ —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Л–1 (–¶–Ю–У–1) —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г—О—Й–µ–є –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤—Г—О –Ї–Є—Б–ї–Њ—В—Г –і–Њ —Н–љ–і–Њ–њ–µ—А–µ–Ї–Є—Б–µ–є. –Р–°–Ъ –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ –∞—Ж–µ—В–Є–ї–Є—А—Г–µ—В —Ж–Є–Ї–ї–Њ–Њ–Ї—Б–Є–≥–µ–љ–∞–Ј—Г–1 (–њ–Њ –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В–љ–Њ–Љ—Г –Њ—Б—В–∞—В–Ї—Г —Б–µ—А–Є–љ–∞ –≤ –њ–Њ–ї–Њ–ґ–µ–љ–Є–Є 529) –≤–±–ї–Є–Ј–Є –µ–µ –Ї–∞—В–∞–ї–Є—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Ж–µ–љ—В—А–∞, –њ—А–µ–њ—П—В—Б—В–≤—Г—П —В–µ–Љ —Б–∞–Љ—Л–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –Љ–µ—В–∞–±–Њ–ї–Є—В–Њ–≤ –∞—А–∞—Е–Є–і–Њ–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –Є –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ —В–∞–Ї–Њ–≥–Њ –Љ–Њ—Й–љ–Њ–≥–Њ –∞–Ї—В–Є–≤–∞—В–Њ—А–∞ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –Ї–∞–Ї —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ –Р2 (—А–Є—Б. 1) [Catella–Lawson F. et al., 2001; Topol E.J., 2004].
–Т–њ–µ—А–≤—Л–µ —Б–Њ–Њ–±—Й–µ–љ–Є—П –Њ –≤—Л—Б–Њ–Ї–Њ–є –Ї–Њ—А—А–µ–ї—П—Ж–Є–Є –Љ–µ–ґ–і—Г –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Р–°–Ъ –Є —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —З–∞—Б—В–Њ—В—Л –Ґ–Ш–Р –њ–Њ—П–≤–Є–ї–Є—Б—М –≤ –љ–∞—З–∞–ї–µ 70–—Е –≥–Њ–і–Њ–≤ –њ—А–Њ—И–ї–Њ–≥–Њ —Б—В–Њ–ї–µ—В–Є—П, –∞ –њ–µ—А–≤—Л–Љ —Г–њ–Њ–Љ–Є–љ–∞–љ–Є–µ–Љ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–≥–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –Р–°–Ъ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–Є—Б–Ї–Њ–Љ –Є–љ—Б—Г–ї—М—В–∞ —П–≤–Є–ї—Б—П –Њ—В—З–µ—В Canadian Cooperative Study Group (The Canadian Cooperative Study Group, 1978). –Т–њ–Њ—Б–ї–µ–і—Б—В–≤–Є–Є –±—Л–ї –њ—А–Њ–≤–µ–і–µ–љ —Ж–µ–ї—Л–є —А—П–і –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —Б—В—А–∞–љ–∞—Е –Х–≤—А–Њ–њ—Л –Є –°–µ–≤–µ—А–љ–Њ–є –Р–Љ–µ—А–Є–Ї–Є, –і–Њ–Ї–∞–Ј–∞–≤—И–Є–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї—Г—О –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–°–Ъ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–µ–≥–Њ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–°–Ъ –њ—А–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ
–Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П
–£—З–Є—В—Л–≤–∞—П –љ–∞–Є–±–Њ–ї—М—И—Г—О —Б—В–µ–њ–µ–љ—М –∞–Ї—В–Є–≤–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ —Б –∞–Ї—В–Є–≤–љ—Л–Љ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ–Љ –љ–µ–є—А–Њ—В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є—Е –Є —В—А–Њ–Љ–±–Њ–≥–µ–љ–љ—Л—Е —Н–є–Ї–Њ–Ј–∞–љ–Њ–Є–і–Њ–≤ –≤ –Њ—Б—В—А–Њ–є —Б—В–∞–і–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П (–Э–Ь–Ъ), –љ–∞–Є–±–Њ–ї–µ–µ –ї–Њ–≥–Є—З–љ—Л–Љ –Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–°–Ъ –Є–Љ–µ–љ–љ–Њ –≤ —Н—В–Њ—В –њ–µ—А–Є–Њ–і.
–Р–°–Ъ —П–≤–ї—П–µ—В—Б—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ –Њ—Б—В—А—Л–є –њ–µ—А–Є–Њ–і –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ (–Ш–Ш) –њ–Њ–і–Ї—А–µ–њ–ї–µ–љ–∞ –і–∞–љ–љ—Л–Љ–Є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л.
–Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Р–°–Ъ –њ—А–Є –µ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 6 —З–∞—Б–Њ–≤ –Ш–Ш –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є MAST–I (Multicentre Acute Stroke Trial–Italy, 1995): –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ї–∞–Ї –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 10 –і–љ–µ–є, —В–∞–Ї –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –њ–Њ—Б–ї–µ –Ш–Ш, –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є.
–Ю—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –Р–°–Ъ –њ—А–Є –µ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 48 —З–∞—Б–Њ–≤ –Ш–Ш –њ–Њ—Б–≤—П—Й–µ–љ—Л –і–≤–∞ –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: IST (International Stroke Trial, 1997) –Є CAST (Chinese Acute Stroke Trial, 1997).
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є IST —Б —Г—З–∞—Б—В–Є–µ–Љ 19 435 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –ї–µ—В–∞–ї—М–љ–Њ—Б—В–Є (11,3 –Є 12,4% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –і–ї—П –ї–µ—З–µ–љ–љ—Л—Е –Є –љ–µ–ї–µ—З–µ–љ–љ—Л—Е) –Є —З–∞—Б—В–Њ—В—Л –њ–Њ–≤—В–Њ—А–љ—Л—Е –Ш–Ш (2,8 –Є 3,9% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –і–ї—П –ї–µ—З–µ–љ–љ—Л—Е –Є –љ–µ–ї–µ—З–µ–љ–љ—Л—Е) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–°–Ъ (–≤ –і–Њ–Ј–µ 300 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –≤ —В–µ—З–µ–љ–Є–µ 14 —Б—Г—В–Њ–Ї, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є–Љ–Є –Р–°–Ъ (International Stroke Trial Collaborative Group, 1997).
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є CAST —Б —Г—З–∞—Б—В–Є–µ–Љ 21 106 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–°–Ъ –≤ –і–Њ–Ј–µ 160 –Љ–≥ –≤ —Б—Г—В–Ї–Є –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Ш–Ш —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–Љ–µ—А–µ–љ–љ–Њ–Љ—Г, –љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ—Г (–Њ–Ї–Њ–ї–Њ 11 —Б–ї—Г—З–∞–µ–≤ –љ–∞ –Ї–∞–ґ–і—Л–µ 1000 –ї–µ—З–µ–љ–љ—Л—Е –±–Њ–ї—М–љ—Л—Е) —Б–љ–Є–ґ–µ–љ–Є—О —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Є–ї–Є —З–∞—Б—В–Њ—В—Л –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –≤ –њ–µ—А–≤—Л–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–µ–і–µ–ї—М –њ–Њ—Б–ї–µ –Ш–Ш (Chinese Acute Stroke Trial Collaborative Group, 1997).
–°–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ —Н—В–Є—Е –і–≤—Г—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ –±–Њ–ї–µ–µ —А–∞–љ–љ–µ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–°–Ъ –њ—А–Є –Ш–Ш (AHA–ASA, 2007; ESO, 2008). –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –Є–Љ–µ—В—М –≤ –≤–Є–і—Г, —З—В–Њ –њ—А–Є –њ—А–Њ—З–Є—Е —А–∞–≤–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–°–Ъ –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Ш–Ш –љ–µ —П–≤–ї—П–µ—В—Б—П –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є —В—А–Њ–Љ–±–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є (AHA–ASA, 2007). –Ґ–∞–Ї–ґ–µ –љ–µ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Р–°–Ъ –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 24 —З–∞—Б–Њ–≤ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П —В—А–Њ–Љ–±–Њ–ї–Є–Ј–Є—Б–∞ (AHA–ASA, 2007; ESO, 2008).
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б –њ–Њ–Љ–Њ—Й—М—О –Р–°–Ъ –±—Л–ї–Њ –њ–Њ—Б–≤—П—Й–µ–љ–Њ 6 –Ї—А—Г–њ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є.
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PHS (Physicians' Health Study, 1989), –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ –°–®–Р, –Ј–і–Њ—А–Њ–≤—Л–Љ –Љ—Г–ґ—З–Є–љ–∞–Љ –љ–∞–Ј–љ–∞—З–∞–ї–∞—Б—М –Р–°–Ъ –≤ –і–Њ–Ј–µ 325 –Љ–≥ —З–µ—А–µ–Ј —Б—Г—В–Ї–Є. –Я–Њ–Ї–∞–Ј–∞–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–Ь —Г –Љ—Г–ґ—З–Є–љ —Б—В–∞—А—И–µ 50 –ї–µ—В, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ —З–∞—Б—В–Њ—В—Г —А–∞–Ј–≤–Є—В–Є—П –Ш–Ш –Р–°–Ъ –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї–∞ (Steering Committee of the Physicians' Health Study Research Group, 1989).
–Т —Б—Е–Њ–і–љ–Њ–Љ –њ–Њ –і–Є–Ј–∞–є–љ—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є BDS (Britain Doctors Study, 1988), –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –≤ –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є–Є, –Ј–і–Њ—А–Њ–≤—Л–Љ –Љ—Г–ґ—З–Є–љ–∞–Љ –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Р–°–Ъ (–≤ –і–Њ–Ј–µ 500 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є –љ–µ –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–°–Ъ, —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞ –Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–Є –±—Л–ї –Њ–і–Є–љ–∞–Ї–Њ–≤ [Peto R. et al., 1988].
–Ґ–∞–Ї–ґ–µ –≤ –Т–µ–ї–Є–Ї–Њ–±—А–Є—В–∞–љ–Є–Є –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ TPT (Thrombosis Prevention Trial, 1998), –≤ –Ї–Њ—В–Њ—А–Њ–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ –Ш–С–° (—Г—З–Є—В—Л–≤–∞—П —Б–µ–Љ–µ–є–љ—Л–є –∞–љ–∞–Љ–љ–µ–Ј, –Є–љ–і–µ–Ї—Б –Љ–∞—Б—Б—Л —В–µ–ї–∞, —Г—А–Њ–≤–µ–љ—М —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, —Д–Є–±—А–Є–љ–Њ–≥–µ–љ–∞ –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є, –љ–∞–ї–Є—З–Є–µ –Є–ї–Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є, —В–∞–±–∞–Ї–Њ–Ї—Г—А–µ–љ–Є—П) –љ–∞–Ј–љ–∞—З–∞–ї–∞—Б—М –Р–°–Ъ (–≤ –і–Њ–Ј–µ 75 –Љ–≥ –≤ —Б—Г—В–Ї–Є), –≤–∞—А—Д–∞—А–Є–љ (—Ж–µ–ї–µ–≤–Њ–є —Г—А–Њ–≤–µ–љ—М –Ь–Э–Ю – 1,5) –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ–Њ–є –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –≤—Л—Б–Њ–Ї–Є–Љ —А–Є—Б–Ї–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –њ—А–Є–µ–Љ –Р–°–Ъ –≤–µ–і–µ—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О —А–Є—Б–Ї–∞ –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ (–Ш–Ь) (Thrombosis prevention trial., 1998).
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є HOT (The Hypertension Optimal Treatment, 1998) –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–µ–є –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Р–°–Ъ (–≤ –і–Њ–Ј–µ 75 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –Я–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –Р–°–Ъ, –Є–Љ–µ–ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –Љ–µ–љ—М—И–Є–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ш–Ь. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В –ї—О–±–Њ–є –њ—А–Є—З–Є–љ—Л, —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –∞ —В–∞–Ї–ґ–µ –Ш–Ш –≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е –њ–Њ–ї—Г—З–µ–љ–Њ –љ–µ –±—Л–ї–Њ [Hansson L. et al., 1998].
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є PPP (Primary Prevention Project, 2001) –њ–∞—Ж–Є–µ–љ—В–∞–Љ (–Љ—Г–ґ—З–Є–љ–∞–Љ –Є –ґ–µ–љ—Й–Є–љ–∞–Љ), –Є–Љ–µ—О—Й–Є–Љ –Њ–і–Є–љ –Є –±–Њ–ї–µ–µ —Д–∞–Ї—В–Њ—А —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –љ–∞–Ј–љ–∞—З–∞–ї–Є—Б—М –Р–°–Ъ (–≤ –і–Њ–Ј–µ 100 –Љ–≥ –≤ —Б—Г—В–Ї–Є), –≤–Є—В–∞–Љ–Є–љ –Х (–≤ –і–Њ–Ј–µ 300 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –Є–ї–Є –њ–ї–∞—Ж–µ–±–Њ. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –і–Њ—Б—А–Њ—З–љ–Њ –њ—А–µ–Ї—А–∞—Й–µ–љ–Њ –Є–Ј––Ј–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Ї–∞–Ї —А–Є—Б–Ї–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є (–љ–∞ 23%), —В–∞–Ї –Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Љ–µ—А—В–Є (–љ–∞ 44%) –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Р–°–Ъ (Collaborative Group of the Primary Prevention Project, 2001).
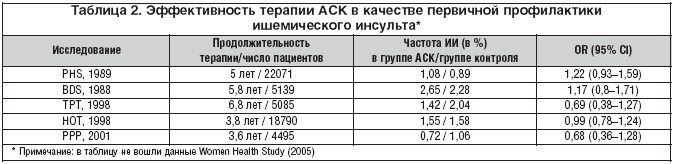
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —Г—Б–њ–µ—Е–Є –≤ –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ш–Ь, –≤ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ —Б –њ–Њ–Љ–Њ—Й—М—О –Р–°–Ъ –Ї–∞–Ї —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж, —В–∞–Ї –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Є–Љ–µ—О—Й–Є—Е —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–Ш (—В–∞–±–ї. 2).
–Х–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ–Љ, –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–≤—И–Є–Љ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–°–Ъ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є, —Б—В–∞–ї–Њ –Ј–∞–Ї–Њ–љ—З–Є–≤—И–µ–µ—Б—П –≤ 2005 –≥–Њ–і—Г Women Health Study, –≤ –Ї–Њ—В–Њ—А–Њ–Љ —Г—З–∞—Б—В–≤–Њ–≤–∞–ї–Є 39 876 –Ј–і–Њ—А–Њ–≤—Л—Е –ґ–µ–љ—Й–Є–љ —Б—В–∞—А—И–µ 45 –ї–µ—В. –£—З–∞—Б—В–љ–Є–Ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –≤ 2 –≥—А—Г–њ–њ—Л: –Р–°–Ъ (100 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –Є –њ–ї–∞—Ж–µ–±–Њ. –Я—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 10 –ї–µ—В. –Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ, —З—В–Њ –≤ WHS –љ–µ –±—Л–ї–Њ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–Є (—Г–Љ–µ–љ—М—И–µ–љ–Є—П —Б—Г–Љ–Љ–∞—А–љ–Њ–є —З–∞—Б—В–Њ—В—Л –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Ш–Ь, –љ–µ—Д–∞—В–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –Є —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є), –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –љ–∞ 17% —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–Ї —Б—В–∞—А—И–µ 45 –ї–µ—В (RR 0,83; 95% CI 0,69–0,99; p=0,04); –њ—А–Є —Н—В–Њ–Љ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ш–Ш —Г–Љ–µ–љ—М—И–Є–ї—Б—П –љ–∞ 24% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ (RR 0,76; 95% CI 0,63–0,93; p=0,009) [Ridker P.M. et al., 2005].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Є–Љ–µ—О—Й–Є–µ—Б—П –љ–∞ —Б–µ–≥–Њ–і–љ—П –і–∞–љ–љ—Л–µ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ш–Ш –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–∞–ї—Л—Е (100 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –і–Њ–Ј –Р–°–Ъ –ґ–µ–љ—Й–Є–љ–∞–Љ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 45 –ї–µ—В –Є —Б—В–∞—А—И–µ, –љ–µ –Є–Љ–µ—О—Й–Є—Е —А–Є—Б–Ї–∞ –≤–љ—Г—В—А–Є—З–µ—А–µ–њ–љ—Л—Е –Ї—А–Њ–≤–Њ–Є–Ј–ї–Є—П–љ–Є–є –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ (–Ї–ї–∞—Б—Б I, —Г—А–Њ–≤–µ–љ—М –Р) (ESO, 2008). –†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —В–∞–Ї–ґ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–∞–ї—Л—Е –і–Њ–Ј –Р–°–Ъ –Љ—Г–ґ—З–Є–љ–∞–Љ –і–ї—П –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞, –Њ–і–љ–∞–Ї–Њ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ —Г –љ–Є—Е –љ–µ —Б–љ–Є–ґ–∞–µ—В—Б—П (–Ї–ї–∞—Б—Б I, —Г—А–Њ–≤–µ–љ—М –Р) (ESO, 2008).
Cote R. et al. (1995) –Њ—В–Љ–µ—В–Є–ї–Є, —З—В–Њ –Р–°–Ъ –≤ –і–Њ–Ј–µ 325 –Љ–≥ –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —Г –ї–Є—Ж —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –∞—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ –Ї–∞—А–Њ—В–Є–і–љ—Л–Љ —Б—В–µ–љ–Њ–Ј–Њ–Љ (≥ 50%). –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ –Є–Љ–µ—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ —В–Њ–Љ, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—З–∞–ї—М–љ—Л–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –Љ–Њ–Ј–≥–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ –Ј–і–Њ—А–Њ–≤—Л–Љ–Є –ї—О–і—М–Љ–Є –Є–Љ–µ–µ—В –Љ–µ—Б—В–Њ –і–Є—Б–±–∞–ї–∞–љ—Б –≤ —Б–Є—Б—В–µ–Љ–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤: —Б–љ–Є–ґ–µ–љ–Є–µ —Б—Г–Љ–Љ–∞—А–љ–Њ–≥–Њ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–љ—Л—Е –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є —В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–∞ – —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2 [–°—Г—Б–ї–Є–љ–∞ –Ч.–Р., 1990]. –≠—В–Њ –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М –Њ–і–љ–Є–Љ –Є–Ј –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–Є–є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Р–°–Ъ —В–∞–Ї–Є–Љ –±–Њ–ї—М–љ—Л–Љ.
–Т –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–µ Antithrombotic Trialists’ Collaboration (2002) –±—Л–ї —Б–і–µ–ї–∞–љ –≤—Л–≤–Њ–і –Њ —В–Њ–Љ, —З—В–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –Р–°–Ъ –і–Њ–ї–ґ–љ—Л –±—Л—В—М —А–∞—Б—И–Є—А–µ–љ—Л –Ј–∞ —Б—З–µ—В –≤–Ї–ї—О—З–µ–љ–Є—П –ї–Є—Ж, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Б–Њ —Б—В–µ–љ–Њ–Ј–Њ–Љ —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –∞—А—В–µ—А–Є–є, —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ, —В–Њ –µ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є—Е –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ (Antithrombotic Trialists’ Collaboration, 2002). –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л —Б –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –∞—А—В–µ—А–Є–є –Є–Љ–µ—О—В –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —А–Є—Б–Ї –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞, –Є–љ—Б—Г–ї—М—В–∞ –Є —Б–Љ–µ—А—В–Є –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ. –Р–°–Ъ —Б–љ–Є–ґ–∞–µ—В —З–∞—Б—В–Њ—В—Г –Ш–Ь —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ —Б–Њ–љ–љ—Л—Е –∞—А—В–µ—А–Є–є [Hobson R. et al., 1993] –Є —З–∞—Б—В–Њ—В—Г –Є–љ—Б—Г–ї—М—В–∞ –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є –Ї–∞—А–Њ—В–Є–і–љ–Њ–є —Н–љ–і–∞—А—В–µ—А—Н–Ї—В–Њ–Љ–Є–Є [Engelter S., Lyrer P., 2003]. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –Р–°–Ъ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –Ї –њ—А–Є–µ–Љ—Г –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –∞—Б–Є–Љ–њ—В–Њ–Љ–љ—Л–Љ —Б—В–µ–љ–Њ–Ј–Њ–Љ –≤–љ—Г—В—А–µ–љ–љ–µ–є —Б–Њ–љ–љ–Њ–є –∞—А—В–µ—А–Є–Є (–Т–°–Р) >50% –і–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —А–Є—Б–Ї–∞ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Б–Њ–±—Л—В–Є–є (–Ї–ї–∞—Б—Б II, —Г—А–Њ–≤–µ–љ—М –Т) (ESO, 2008).
–®–Є—А–Њ–Ї–∞—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–є –∞—А–Є—В–Љ–Є–Є –Є –≤—Л—Б–Њ–Ї–Є–є —А–Є—Б–Ї —Б–Є—Б—В–µ–Љ–љ–Њ–є —Н–Љ–±–Њ–ї–Є–Є –Є –Ї–∞—А–і–Є–Њ—Н–Љ–±–Њ–ї–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Ю–і–љ–∞–Ї–Њ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –њ—А–Є –µ–µ –±–µ–Ј—Г—Б–њ–µ—И–љ–Њ—Б—В–Є –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є —Г —Н—В–Њ–≥–Њ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–∞ –±–Њ–ї—М–љ—Л—Е. –Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П SPAF (1991) –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ш–Ш —Г –±–Њ–ї—М–љ—Л—Е —Б –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ–Њ–є –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Д–Њ—А–Љ–∞–Љ–Є —Д–Є–±—А–Є–ї–ї—П—Ж–Є–Є –њ—А–µ–і—Б–µ—А–і–Є–є, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Р–°–Ъ –≤ –і–Њ–Ј–µ 325 –Љ–≥/—Б—Г—В, —Б–љ–Є–ґ–∞–µ—В—Б—П –љ–∞ 42% –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–љ–Є–Љ–∞–≤—И–Є–Љ–Є –њ–ї–∞—Ж–µ–±–Њ. –Ю–і–љ–∞–Ї–Њ —А—П–і–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є (AFASAK 1989; SPAF 1991; EAFT 1993 –Є –і—А.) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ј–∞—Й–Є—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ —Г –Р–°–Ъ –љ–Є–ґ–µ, —З–µ–Љ —Г –Њ—А–∞–ї—М–љ—Л—Е –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–Њ–≤, –Є, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ –Ї–Њ–љ—В–Є–љ–≥–µ–љ—В–Њ–Љ –Љ–Њ–ї–Њ–і—Л—Е –±–Њ–ї—М–љ—Л—Е —Б –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Д–Є–±—А–Є–ї–ї—П—Ж–Є–µ–є –њ—А–µ–і—Б–µ—А–і–Є–є –±–µ–Ј –њ–Њ—А–∞–ґ–µ–љ–Є—П –Ї–ї–∞–њ–∞–љ–Њ–≤ –Є –њ–Њ–≤—Л—И–µ–љ–љ–Њ–є —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М—О –Ї —А–∞–Ј–≤–Є—В–Є—О —В—А–Њ–Љ–±–Њ–≤ —Б –±–Њ–ї—М—И–Є–Љ —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ–Љ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤.
–Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, —Г—З–Є—В—Л–≤–∞—П –≤ —Ж–µ–ї–Њ–Љ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–Ш –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–°–Ъ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–Њ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –љ–µ–Ї–ї–∞–њ–∞–љ–љ–Њ–є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–є –∞—А–Є—В–Љ–Є–µ–є –Љ–Њ–ї–Њ–ґ–µ 65 –ї–µ—В, –љ–µ –Є–Љ–µ—О—Й–Є–Љ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ (–Ї–ї–∞—Б—Б I, —Г—А–Њ–≤–µ–љ—М –Р). –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –љ–µ–Ї–ї–∞–њ–∞–љ–љ–Њ–є –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–є –∞—А–Є—В–Љ–Є–µ–є –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 65 –і–Њ 75 –ї–µ—В, –љ–µ –Є–Љ–µ—О—Й–Є–Љ —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Р–°–Ъ –Є–ї–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–≥–Њ –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В–∞ (–Ї–ї–∞—Б—Б I, —Г—А–Њ–≤–µ–љ—М –Р), –∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –Љ–µ—А—Ж–∞—В–µ–ї—М–љ–Њ–є –∞—А–Є—В–Љ–Є–µ–є, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ —В–µ–Љ –Є–ї–Є –Є–љ—Л–Љ –њ—А–Є—З–Є–љ–∞–Љ –љ–µ –Љ–Њ–≥—Г—В –њ—А–Є–љ–Є–Љ–∞—В—М –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –∞–љ—В–Є–Ї–Њ–∞–≥—Г–ї—П–љ—В, —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–Є—В—М –Р–°–Ъ (–Ї–ї–∞—Б—Б I, —Г—А–Њ–≤–µ–љ—М –Р) (ESO, 2008).
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Р–°–Ъ –і–ї—П –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤–њ–µ—А–≤—Л–µ –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –±–Њ–ї–µ–µ 30 –ї–µ—В –љ–∞–Ј–∞–і [Fields W.S. et al., 1977].
–Я–Њ–≤—В–Њ—А–љ—Л–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –Є–љ—Б—Г–ї—М—В—Л, —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ—В–Њ—А—Л—Е —Б–Њ—Б—В–∞–≤–ї—П–µ—В –Њ—В 16 –і–Њ 42% –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤—Л—Е 5 –ї–µ—В – –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–∞—П –њ—А–Є—З–Є–љ–∞ –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е. –Ю–±—Й–µ–Є–Ј–≤–µ—Б—В–љ–∞ –±–Њ–ї—М—И–∞—П –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–≤—В–Њ—А–љ—Л—Е –Э–Ь–Ъ –≤ –±–ї–Є–ґ–∞–є—И–Є–µ –Љ–µ—Б—П—Ж—Л –Є –≥–Њ–і—Л –њ–Њ—Б–ї–µ –њ–µ—А–≤–Њ–≥–Њ —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–≥–Њ —Н–њ–Є–Ј–Њ–і–∞ [–Т–µ—А–µ—Й–∞–≥–Є–љ –Э.–Т. —Б —Б–Њ–∞–≤—В., 2002].
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–°–Ъ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ –і–ї—П –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ш–Ш –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М —Б —Г—З–∞—Б—В–Є–µ–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Љ–∞–ї—Л–є –Є–љ—Б—Г–ї—М—В –Є–ї–Є –Ґ–Ш–Р. –Я—А–Є—З–Є–љ–Њ–є –Ґ–Ш–Р –Љ–Њ–ґ–µ—В —Б–ї—Г–ґ–Є—В—М —А–µ—Ж–Є–і–Є–≤–Є—А—Г—О—Й–∞—П –Љ–Є–Ї—А–Њ—Н–Љ–±–Њ–ї–Є—П —Б –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –±–ї—П—И–µ–Ї, –њ–Њ–ї–Њ—Б—В–µ–є —Б–µ—А–і—Ж–∞, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л–Љ–Є –∞–≥—А–µ–≥–∞—В–∞–Љ–Є. –Р–°–Ъ –≤ –і–Њ–Ј–∞—Е –Њ—В 100 –і–Њ 300 –Љ–≥ –≤ —Б—Г—В–Ї–Є —В–Њ—А–Љ–Њ–Ј–Є—В —Н—В–Є –њ—А–Њ—Ж–µ—Б—Б—Л, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞—П —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, —Г—А–Њ–≤–µ–љ—М —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2 –Є –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ—Л—Е –∞–≥—А–µ–≥–∞—В–Њ–≤ [Lee T.K. et al., 1988].
–Т 1972 –≥–Њ–і—Г –≤ –°–®–Р –±—Л–ї–Њ –≤–њ–µ—А–≤—Л–µ –њ—А–Њ–≤–µ–і–µ–љ–Њ –±–Њ–ї—М—И–Њ–µ –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–°–Ъ —Г 303 –±–Њ–ї—М–љ—Л—Е —Б –Ґ–Ш–Р – AITIA (Aspirin in Transient Ischemic Attacks, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–Њ –≤ 1977). –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –і–ї–Є—В–µ–ї—М–љ—Л–є (–±–Њ–ї–µ–µ 1 –≥–Њ–і–∞) –њ—А–Є–µ–Љ –Р–°–Ъ –≤ –і–Њ–Ј–µ 1300 –Љ–≥ (–њ–Њ 650 –Љ–≥ –і–≤–∞ —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є) —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —Б–Љ–µ—А—В–µ–ї—М–љ–Њ–≥–Њ –Є—Б—Е–Њ–і–∞ –Њ—В –Є–љ—Б—Г–ї—М—В–∞ –љ–∞ 30% [Fields W.S. et al., 1977].
–Ь–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–µ –∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є–љ—Б—Г–ї—М—В–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Д–Є–±—А–Є–ї–ї—П—Ж–Є–µ–є –њ—А–µ–і—Б–µ—А–і–Є–є –±–µ–Ј –њ–Њ—А–Њ–Ї–∞ –Ї–ї–∞–њ–∞–љ–Њ–≤, –љ–µ–і–∞–≤–љ–Њ –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Ґ–Ш–Р – SPAF (Stroke Prevention in Atrial Fibrillation, 1991) –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –њ—А–Є –µ–ґ–µ–і–љ–µ–≤–љ–Њ–Љ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–Љ –њ—А–Є–µ–Љ–µ 325 –Љ–≥ –Р–°–Ъ –≤ —В–µ—З–µ–љ–Є–µ 16 –Љ–µ—Б—П—Ж–µ–≤ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –љ–µ—Д–∞—В–∞–ї—М–љ—Л—Е –Є–љ—Б—Г–ї—М—В–Њ–≤ —Б–љ–Є–ґ–∞–µ—В—Б—П –љ–∞ 54%, —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є – –љ–∞ 36%, –∞ —Б–Љ–µ—А—В–µ–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ – –љ–∞ 27%.
–Т –±—А–Є—В–∞–љ—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є UK–TIA (United Kingdom Transient Ischaemic Attack Aspirin Trial, 1991), –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ –љ–∞ 2435 –±–Њ–ї—М–љ—Л—Е —Б –њ–µ—А–µ–љ–µ—Б–µ–љ–љ—Л–Љ –±–Њ–ї–µ–µ 3 –Љ–µ—Б—П—Ж–µ–≤ –і–Њ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ґ–Ш–Р –Є–ї–Є –Љ–∞–ї—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ, –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 3 –≥—А—Г–њ–њ—Л, –њ–µ—А–≤–∞—П –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –њ–Њ–ї—Г—З–∞–ї–∞ –Р–°–Ъ –≤ –і–Њ–Ј–µ 600 –Љ–≥ 2 —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є, –≤—В–Њ—А–∞—П – –Р–°–Ъ 300 –Љ–≥ –Њ–і–Є–љ —А–∞–Ј –≤ —Б—Г—В–Ї–Є, —В—А–µ—В—М—П – –њ–ї–∞—Ж–µ–±–Њ –≤ —В–µ—З–µ–љ–Є–µ 50 –Љ–µ—Б—П—Ж–µ–≤. –Я–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ —Б—Г–Љ–Љ–∞—А–љ–∞—П —З–∞—Б—В–Њ—В–∞ –љ–µ—Д–∞—В–∞–ї—М–љ—Л—Е –Є–љ—Б—Г–ї—М—В–Њ–≤ –Є —Б–Љ–µ—А—В–µ–ї—М–љ—Л—Е –Є—Б—Е–Њ–і–Њ–≤ –Њ—В —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ—А–Є—З–Є–љ —Б–љ–Є–ґ–∞–ї–∞—Б—М –≤ –≥—А—Г–њ–њ–∞—Е, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Р–°–Ъ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 18%, –њ—А–Є—З–µ–Љ –Њ–±–µ –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –њ—А–µ–њ–∞—А–∞—В–∞ –±—Л–ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л [Farrell B. et al., 1991].
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є
–і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Р–°–Ъ
–°—А–∞–≤–љ–µ–љ–Є—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–∞–Ј–ї–Є—З–љ—Л—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–∞ —В–∞–Ї–ґ–µ –њ–Њ—Б–≤—П—Й–µ–љ —А—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є [The Dutch TIA Trial Study Group, 1991; Farrell B. et al., 1991; Lindblad B. —Б —Б–Њ–∞–≤—В., 1993; Algra –Р., van Gijn J., 1996].
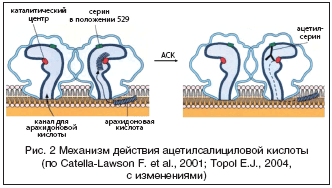
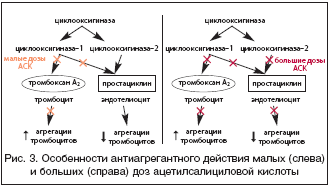
–Т—Л–±–Њ—А –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј–Є—А–Њ–≤–Ї–Є –Р–°–Ъ –±–∞–Ј–Є—А—Г–µ—В—Б—П –љ–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є—П—Е –Њ —В–Њ–Љ, —З—В–Њ –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞, –Ї–∞–Ї –±—Л–ї–Њ —Б–Ї–∞–Ј–∞–љ–Њ –≤—Л—И–µ, —Б–≤—П–Ј–∞–љ —Б –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ–є –±–ї–Њ–Ї–∞–і–Њ–є —Д–µ—А–Љ–µ–љ—В–∞ –¶–Ю–У–1 —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є –њ–Њ—З—В–Є –њ–Њ–ї–љ–Њ–≥–Њ –њ–Њ–і–∞–≤–ї–µ–љ–Є—П –њ—А–Њ–і—Г–Ї—Ж–Є–Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2. –Ю—Б–Њ–±–µ–љ–љ–Њ—Б—В—М—О –і–∞–љ–љ–Њ–≥–Њ —Д–µ—А–Љ–µ–љ—В–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —З—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤—Л—Б–Њ–Ї–∞—П —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М –Ї –і–µ–є—Б—В–≤–Є—О –Р–°–Ъ, –Ї–Њ—В–Њ—А–∞—П –≤ –і–µ—Б—П—В–Ї–Є —А–∞–Ј –њ—А–µ–≤—Л—И–∞–µ—В —В–∞–Ї–Њ–≤—Г—О –¶–Ю–У–2, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ–є –Ј–∞ –њ—А–Њ–і—Г–Ї—Ж–Є—О –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –≤ —Н–љ–і–Њ—В–µ–ї–Є–Є —Б–Њ—Б—Г–і–Њ–≤. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –≤ –Љ–∞–ї—Л—Е –і–Њ–Ј–∞—Е –Р–°–Ъ, –±–ї–Њ–Ї–Є—А—Г—П —В–Њ–ї—М–Ї–Њ –¶–Ю–У–1 –Є –Њ—Б—В–∞–≤–ї—П—П –Є–љ—В–∞–Ї—В–љ—Л–Љ –і—А—Г–≥–Њ–є —Д–µ—А–Љ–µ–љ—В, –≤—Л–Ј—Л–≤–∞–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –њ—А–Њ–і—Г–Ї—Ж–Є–Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї —Г—А–Њ–≤–µ–љ—М –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞, –Љ–Њ—Й–љ–Њ–≥–Њ –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А–∞ –Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–∞, —Б–Њ—Е—А–∞–љ—П–µ—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–Є–Љ [–°—Г—Б–ї–Є–љ–∞ –Ч.–Р., –Ш–Њ–љ–Њ–≤–∞ –Т.–У., 1988]. –Т –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е –Р–°–Ъ –≤—Л–Ј—Л–≤–∞–µ—В –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –Њ–±–Њ–Є—Е –Є–Ј–Њ—Д–µ—А–Љ–µ–љ—В–Њ–≤, —З—В–Њ, –µ—Б—В–µ—Б—В–≤–µ–љ–љ–Њ, –њ—А–Є–≤–Њ–і–Є—В –Ї –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О –њ—А–Њ–і—Г–Ї—Ж–Є–Є –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –Є —Г—Б—В—А–∞–љ–µ–љ–Є—О –µ–≥–Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –љ–∞ –Ї—А–Њ–≤—П–љ—Л–µ –њ–ї–∞—Б—В–Є–љ–Ї–Є –Є —Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б—В–µ–љ–Ї—Г (—А–Є—Б. 2).
–Я–µ—А–≤—Л–є –≤ –Љ–Є—А–Њ–≤–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Њ–њ—Л—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Љ–∞–ї—Л—Е –і–Њ–Ј –Р–°–Ъ (1 –Љ–≥ –љ–∞ 1 –Ї–≥ –≤–µ—Б–∞ –≤ —Б—Г—В–Ї–Є) —Г –±–Њ–ї—М–љ—Л—Е —Б —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –љ–∞ —Д–Њ–љ–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–Њ–љ–Є–Є, –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–љ—Л–є –≤ –Э–Ш–Ш –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –†–Р–Ь–Э, –њ–Њ–Ї–∞–Ј–∞–ї –±—Л—Б—В—А–Њ–µ –Є —Б—В–Њ–є–Ї–Њ–µ —Г—Б—В—А–∞–љ–µ–љ–Є–µ –≥–Є–њ–µ—А–∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ–Њ—З—В–Є 3––Ї—А–∞—В–љ–Њ–≥–Њ —Б–љ–Є–ґ–µ–љ–Є—П –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2 –≤ –Ї—А–Њ–≤–Є –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –њ–Њ–ї–∞ –±–Њ–ї—М–љ—Л—Е –Є –≤–Є–і–∞ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Э–Ь–Ъ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л –њ–∞—Ж–Є–µ–љ—В—Л —Б –Ґ–Ш–Р –Є –њ–µ—А–µ–љ–µ—Б—И–Є–µ –Ш–Ш [–°—Г—Б–ї–Є–љ–∞ –Ч.–Р., –Т—Л—Б–Њ—Ж-
–Ї–∞—П –Т.–У., 1983].
–£ –±–Њ–ї—М–љ—Л—Е —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –њ–Њ—А–∞–ґ–µ–љ–Є—П–Љ–Є —Б–Є–љ—В–µ–Ј –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –љ–∞—А—Г—И–µ–љ –Є–Ј––Ј–∞ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є —Н–љ–і–Њ—В–µ–ї–Є—П —Б–Њ—Б—Г–і–Њ–≤, –Є, –Ї—А–Њ–Љ–µ —В–Њ–≥–Њ, –Р–°–Ъ –Є–љ–≥–Є–±–Є—А—Г–µ—В —Н—В–Њ—В –њ—А–Њ—Ж–µ—Б—Б —Г –љ–Є—Е –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї—О–і–µ–є. –Т 1988 –≥–Њ–і—Г Lee T.K. et al. –њ—А–Є —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–Є–Є –і–µ–є—Б—В–≤–Є—П –Р–°–Ъ –≤ –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е 40 –Љ–≥, 75 –Љ–≥, 300 –Љ–≥ –Є 600 –Љ–≥ –≤ —Б—Г—В–Ї–Є –љ–∞ –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ —Н–љ–і–Њ–≥–µ–љ–љ—Л—Е –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ш–Ш –Њ–±–љ–∞—А—Г–ґ–Є–ї–Є, —З—В–Њ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј–Њ–є, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–µ–є –Є–љ–≥–Є–±–Є—В–Њ—А–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л –Є —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р2, —П–≤–ї—П–µ—В—Б—П 75 –Љ–≥ –Р–°–Ъ –≤ —Б—Г—В–Ї–Є, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –±–Њ–ї—М—И–Є–µ –і–Њ–Ј—Л –њ—А–Є–≤–Њ–і—П—В –Ї –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ—Г –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ—Г —Б–љ–Є–ґ–µ–љ–Є—О —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞, –∞ –Љ–µ–љ—М—И–Є–µ –љ–µ –Њ–±–ї–∞–і–∞—О—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ (—А–Є—Б. 3). –Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–є (81 –Љ–≥ –Є 325 –Љ–≥) –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Р–°–Ъ, –Ї–∞–Ї –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–≥–Њ –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–∞, –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –і–Њ–Ј—Л 81 –Љ–≥ –≤ —Б—Г—В–Ї–Є –љ–∞ –∞–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –∞–і—А–µ–љ–∞–ї–Є–љ–∞ –Є –Р–Ф–§, –Њ–і–љ–∞–Ї–Њ –Ї–Њ–ї–ї–∞–≥–µ–љ––Є–љ–і—Г—Ж–Є—А—Г–µ–Љ–∞—П –∞–≥—А–µ–≥–∞—Ж–Є—П —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Б–љ–Є–ґ–∞–ї–∞—Б—М —В–Њ–ї—М–Ї–Њ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є 325 –Љ–≥ –Р–°–Ъ –≤ —Б—Г—В–Ї–Є, —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М —Г—З–µ—В–∞ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е –Є–Ј—К—П–Ј–≤–ї–µ–љ–Є–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Њ–є –±–ї—П—И–Ї–Є –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–µ –≤—Л—Б–≤–Њ–±–Њ–ґ–і–µ–љ–Є–µ –Ї–Њ–ї–ї–∞–≥–µ–љ–∞ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–є –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ [Feng D. et al., 1997].
–У–Њ–ї–ї–∞–љ–і—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–µ—Е–Њ–і—П—Й–Є—Е –Э–Ь–Ъ (Dutch TIA Study, 1991) –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–Є–Ј–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ —Г 3131 –±–Њ–ї—М–љ–Њ–≥–Њ —Б –Ґ–Ш–Р, –њ–Њ–Ї–∞–Ј–∞–≤, —З—В–Њ –њ—А–Є –њ—А–Є–µ–Љ–µ –Р–°–Ъ –Ї–∞–Ї –≤ –і–Њ–Ј–µ 30 –Љ–≥ –≤ —Б—Г—В–Ї–Є, —В–∞–Ї –Є 283 –Љ–≥ –≤ —Б—Г—В–Ї–Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –љ–µ—Д–∞—В–∞–ї—М–љ—Л—Е –Є–љ—Б—Г–ї—М—В–Њ–≤ –±—Л–ї–Њ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –Њ–і–Є–љ–∞–Ї–Њ–≤—Л–Љ (30 –Љ–≥ – 14,7%; 283 –Љ–≥ – 15,2%), –∞ –њ—А–µ–њ–∞—А–∞—В –≤ –і–Њ–Ј–µ 30 –Љ–≥ —Б–љ–Є–ґ–∞–ї —Г—А–Њ–≤–µ–љ—М —А–µ—Ж–Є–і–Є–≤–Њ–≤ –Ґ–Ш–Р –љ–∞ 20–25%. –†–µ–Ј—Г–ї—М—В–∞—В—Л —Н—В–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —В–∞–Ї–ґ–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Є, —З—В–Њ —З–∞—Б—В–Њ—В–∞ –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –±—Л–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Љ–µ–љ—М—И–µ–є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Љ–∞–ї—Л—Е –і–Њ–Ј –Р–°–Ъ (The Dutch TIA Trial Study Group, 1991).
–Р–љ–∞–ї–Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–Є–Ј–Ї–Є—Е (–Љ–µ–љ–µ–µ 100 –Љ–≥ –≤ —Б—Г—В–Ї–Є), —Б—А–µ–і–љ–Є—Е (300–325 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –Є –≤—Л—Б–Њ–Ї–Є—Е (–±–Њ–ї–µ–µ 900 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –і–Њ–Ј –Р–°–Ъ (–њ–Њ –і–∞–љ–љ—Л–Љ 10 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є) –љ–µ –Њ–±–љ–∞—А—Г–ґ–Є–ї –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –≤ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є —А–Є—Б–Ї–∞ –њ–Њ–≤—В–Њ—А–љ–Њ–≥–Њ –Ш–Ш. –≠—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –Р–°–Ъ –≤ –ї—О–±–Њ–є –і–Њ–Ј–µ –≤—Л—И–µ 30 –Љ–≥ –≤ —Б—Г—В–Ї–Є –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞–µ—В —А–∞–Ј–≤–Є—В–Є–µ –≤ —Б—А–µ–і–љ–µ–Љ 13% –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Э–Ь–Ъ [Algra –Р., van Gijn J., 1996]. –Т —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —В–Њ–ї—М–Ї–Њ –Љ–∞–ї—Л—Е –і–Њ–Ј –Р–°–Ъ (50–300 –Љ–≥ –≤ —Б—Г—В–Ї–Є) SALT (Swedish aspirin low Dose Trial, 1991), —Е–Њ—В—П –Є —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–≤—В–Њ—А–љ—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –љ–∞ 18%, –Њ–і–љ–∞–Ї–Њ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –ї–µ—В–∞–ї—М–љ–Њ—Б—В—М –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М (The SALT Collaborative Group, 1991).
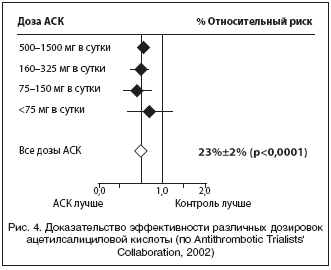
–Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞ 11 —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ–ї–∞—Ж–µ–±–Њ––Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –Р–°–Ъ —Г–Љ–µ–љ—М—И–∞–µ—В —А–Є—Б–Ї –Є–љ—Б—Г–ї—М—В–∞ –≤ –Є–љ—В–µ—А–≤–∞–ї–µ –і–Њ–Ј –Њ—В 50 –і–Њ 1500 –Љ–≥ –≤ —Б—Г—В–Ї–Є, –њ—А–Є—З–µ–Љ –љ–Є–Ј—И–Є–є –њ–Њ—А–Њ–≥ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –і–Њ–Ј—Л –љ–µ –Њ–њ—А–µ–і–µ–ї–µ–љ, –љ–Њ, –њ–Њ –Љ–љ–µ–љ–Є—О –њ—А–Њ–≤–Њ–і–Є–≤—И–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –∞–≤—В–Њ—А–Њ–≤ [Johnson E.S. et al., 1999], –Њ–љ –Љ–Њ–ґ–µ—В –±—Л—В—М –љ–Є–ґ–µ 50 –Љ–≥ –≤ —Б—Г—В–Ї–Є. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ–Њ—Б–≤—П—Й–µ–љ–љ—Л—Е –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –љ–µ –≤—Л—П–≤–Є–ї –і–Њ–Ј–Њ–Ј–∞–≤–Є—Б–Є–Љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Р–°–Ъ [Albers G. et al., 1999]. –°–Њ–≥–ї–∞—Б–љ–Њ –њ–Њ—Б–ї–µ–і–љ–µ–Љ—Г –Ј–∞–Ї–ї—О—З–µ–љ–Є—О —Н–Ї—Б–њ–µ—А—В–Њ–≤ –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –Љ–µ—В–∞––∞–љ–∞–ї–Є–Ј–∞ 287 –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ –њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Р–°–Ъ –≤ –ї—О–±–Њ–є –і–Њ–Ј–µ —Б —Б—Г–Љ–Љ–∞—А–љ–Њ–є —А–µ–і—Г–Ї—Ж–Є–µ–є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –≤ —Б—А–µ–і–љ–µ–Љ –љ–∞ 23% (—А<0,0001). –Я—А–Є —Н—В–Њ–Љ –љ–∞–Є–±–Њ–ї–µ–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ–Њ–є –њ—А–Є–Ј–љ–∞–µ—В—Б—П –і–Њ–Ј–∞ 75–150 –Љ–≥ –≤ —Б—Г—В–Ї–Є, –Њ–і–љ–∞–Ї–Њ –≤ —Б–ї—Г—З–∞—П—Е —Б –Њ—Б—В—А—Л–Љ–Є —Н–њ–Є–Ј–Њ–і–∞–Љ–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ –љ–∞—З–∞–ї—М–љ–∞—П –љ–∞–≥—А—Г–Ј–Њ—З–љ–∞—П –њ—А–Њ–±–∞ –≤ 150 –Љ–≥ (Antithrombotic Trialists’ Collaboration, 2002) (—А–Є—Б. 4). –†–µ–Ј—Г–ї—М—В–∞—В—Л –і–∞–љ–љ–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –ї–µ–≥–ї–Є –≤ –Њ—Б–љ–Њ–≤—Г —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –µ–≤—А–Њ–њ–µ–є—Б–Ї–Є—Е (ESO, 2008) –Є —Б–µ–≤–µ—А–Њ–∞–Љ–µ—А–Є–Ї–∞–љ—Б–Ї–Є—Е (AHA–ASA, 2011) —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–є –њ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—О –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤–Њ –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ш–Ш.
–Я–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –Р–°–Ъ
–Є –њ—Г—В–Є –Є—Е —Г—Б—В—А–∞–љ–µ–љ–Є—П
–Т –≤–Њ–њ—А–Њ—Б–∞—Е –≤—Л–±–Њ—А–∞ –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л—Е —Б—Г—В–Њ—З–љ—Л—Е –і–Њ–Ј–Є—А–Њ–≤–Њ–Ї –Р–°–Ъ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –Ш–Ш –љ–µ–Љ–∞–ї–Њ–≤–∞–ґ–љ—Г—О —А–Њ–ї—М –Є–≥—А–∞—О—В –µ–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л. –Ъ–∞–Ї –Є –і—А—Г–≥–Є–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –Р–°–Ъ –Љ–Њ–ґ–µ—В –Њ–Ї–∞–Ј—Л–≤–∞—В—М –Ї–∞–Ї –Љ–µ—Б—В–љ–Њ–µ (–Ј–∞ —Б—З–µ—В —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П —Б–ї–Є–Ј–Є—Б—В–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є), —В–∞–Ї –Є —Б–Є—Б—В–µ–Љ–љ–Њ–µ (–Ј–∞ —Б—З–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–≤) –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –њ—А–Є –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –µ–≥–Њ –њ—А–Є–µ–Љ–µ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ —Б –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ–Љ —Н—А–Њ–Ј–Є–є –Є —П–Ј–≤, –∞ —В–∞–Ї–ґ–µ —А–∞–Ј–≤–Є—В–Є–µ–Љ –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є. –І–∞—Б—В–Њ—В–∞ —Н—В–Њ–≥–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П –љ–∞–њ—А—П–Љ—Г—О –Ј–∞–≤–Є—Б–Є—В –Њ—В —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј—Л. –Ґ–∞–Ї, –њ–Њ–±–Њ—З–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Р–°–Ъ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ —Б–љ–Є–ґ–∞–ї–Њ—Б—М –њ—А–Є –њ—А–Є–µ–Љ–µ 300 –Љ–≥ –≤ —Б—Г—В–Ї–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є—Е (1200 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –і–Њ–Ј –Р–°–Ъ –Є —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 31 –Є 41% –і–ї—П –Њ—Й—Г—Й–µ–љ–Є—П –і–Є—Б–Ї–Њ–Љ—Д–Њ—А—В–∞ –≤ –Њ–±–ї–∞—Б—В–Є –ґ–Є–≤–Њ—В–∞ –Є 3,1 –Є 4,8% –і–ї—П –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ—Л—Е –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є (UK–TIA Study Group, 1991). –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є European Stroke Prevention Study 2 (ESPS 2) –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Є –љ–Є–Ј–Ї–Є–µ –і–Њ–Ј—Л –Р–°–Ъ –љ–µ —Г—Б—В—А–∞–љ—П—О—В –њ–Њ–ї–љ–Њ—Б—В—М—О –µ–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–Є—О –Ї—А–Њ–≤–Њ—В–µ—З–µ–љ–Є–є.
–Ф–ї—П —Г—Б—В—А–∞–љ–µ–љ–Є—П –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Р–°–Ъ –љ–∞ —Б–ї–Є–Ј–Є—Б—В—Г—О –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –њ—А–µ–і–ї–Њ–ґ–µ–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–µ —Д–Њ—А–Љ—Л —Б –Ї–Є—И–µ—З–љ–Њ–—А–∞—Б—В–≤–Њ—А–Є–Љ–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Њ–є. –Я—А–Є–Љ–µ–љ—П–µ—В—Б—П —В–∞–Ї–ґ–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –Р–°–Ъ (–≤ –і–Њ–Ј–µ 75 –Є–ї–Є 150 –Љ–≥) –Є –∞–љ—В–∞—Ж–Є–і–∞ – –≥–Є–і—А–Њ–Ї—Б–Є–і–∞ –Љ–∞–≥–љ–Є—П (—Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ 15,2 –Є 30,39 –Љ–≥) – –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Ъ–∞—А–і–Є–Њ–Љ–∞–≥–љ–Є–ї. –Ь–∞–≥–љ–Є—П –≥–Є–і—А–Њ–Ї—Б–Є–і, –≤—Е–Њ–і—П—Й–Є–є –≤ —Б–Њ—Б—В–∞–≤ –Ъ–∞—А–і–Є–Њ–Љ–∞–≥–љ–Є–ї–∞, –Ј–∞—Й–Є—Й–∞–µ—В —Б–ї–Є–Ј–Є—Б—В—Г—О –Њ–±–Њ–ї–Њ—З–Ї—Г –ґ–µ–ї—Г–і–Њ—З–љ–Њ––Ї–Є—И–µ—З–љ–Њ–≥–Њ —В—А–∞–Ї—В–∞ –Њ—В –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Р–°–Ъ, –љ–Є–≤–µ–ї–Є—А—Г—П –µ–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Љ–∞–≥–љ–Є—П –≥–Є–і—А–Њ–Ї—Б–Є–і –љ–µ –≤–ї–Є—П–µ—В –љ–∞ –±–Є–Њ–і–Њ—Б—В—Г–њ–љ–Њ—Б—В—М –Р–°–Ъ. –Я—А–µ–њ–∞—А–∞—В –њ—А–Є–Љ–µ–љ—П—О—В –њ–Њ 1 —В–∞–±–ї–µ—В–Ї–µ 1 —А–∞–Ј –≤ —Б—Г—В–Ї–Є.
–°–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –Њ—Б–Њ–±–Њ–µ –≤–љ–Є–Љ–∞–љ–Є–µ —В–∞–Ї–ґ–µ –љ–∞ —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ—А–Є –µ–ґ–µ–і–љ–µ–≤–љ–Њ–Љ –њ—А–Є–µ–Љ–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –Р–°–Ъ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ –Р–Ф –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ–ї–љ–Њ–≥–Њ –њ–Њ–і–∞–≤–ї–µ–љ–Є—П —Б–Є–љ—В–µ–Ј–∞ –і–µ–њ—А–µ—Б—Б–Њ—А–љ—Л—Е –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤, –∞ —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є—Е –Є–љ—Б—Г–ї—М—В–Њ–≤. –Я—А–Є —Н—В–Њ–Љ –Љ–∞–ї—Л–µ –і–Њ–Ј—Л —Г–Љ–µ–љ—М—И–∞—О—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є: —В–∞–Ї, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є SAPAT [Juul–Moller S. et al., 1992] —З–∞—Б—В–Њ—В–∞ —А–∞–Ј–≤–Є—В–Є—П –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ —Г –ї–µ—З–µ–љ–љ—Л—Е (75 –Љ–≥ –≤ —Б—Г—В–Ї–Є) –Є –љ–µ–ї–µ—З–µ–љ–љ—Л—Е –Р–°–Ъ –±–Њ–ї—М–љ—Л—Е –±—Л–ї–∞ –њ–Њ—З—В–Є –Њ–і–Є–љ–∞–Ї–Њ–≤–∞.
–Я–Њ–Љ–Є–Љ–Њ —Н—В–Њ–≥–Њ, –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –Р–°–Ъ –Љ–Њ–≥—Г—В –≤—Л–Ј—Л–≤–∞—В—М –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї (–љ–∞–њ—А–Є–Љ–µ—А, —А–∞–Ј–≤–Є—В–Є–µ –Є–љ—В–µ—А—Б—В–Є—Ж–Є–∞–ї—М–љ–Њ–≥–Њ –љ–µ—Д—А–Є—В–∞), –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П (–Ї–∞–Ї –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П, —В–∞–Ї –Є –њ–Њ—Б–ї–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞), –≤ —А–µ–і–Ї–Є—Е —Б–ї—Г—З–∞—П—Е —Г –Њ—В–і–µ–ї—М–љ—Л—Е –±–Њ–ї—М–љ—Л—Е – —Г–≥–љ–µ—В–µ–љ–Є–µ –ї–µ–є–Ї–Њ–њ–Њ—Н–Ј–∞. –Т —Н—В–Њ–є —Б–≤—П–Ј–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –∞–Ї—В—Г–∞–ї—М–љ–Њ –Ј–≤—Г—З–Є—В –≤–Њ–њ—А–Њ—Б –Њ –њ–Њ–Є—Б–Ї–∞—Е –њ—Г—В–µ–є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Р–°–Ъ —Н—Д—Д–µ–Ї—В–Є–≤–љ–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ –∞–љ—В–Є—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Ш–Ш, –≤ –њ–µ—А–≤–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ —Г –Њ—В–і–µ–ї—М–љ—Л—Е –≥—А—Г–њ–њ –±–Њ–ї—М–љ—Л—Е, –∞ —В–∞–Ї–ґ–µ –≤–Њ –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ш–Ш. –Т–Љ–µ—Б—В–µ —Б —В–µ–Љ, –љ–µ—Б–Љ–Њ—В—А—П –љ–∞ –µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї—Г—О –њ—А–Є–≤–ї–µ–Ї–∞—В–µ–ї—М–љ–Њ—Б—В—М, –њ—А–Є—Е–Њ–і–Є—В—Б—П —Б—З–Є—В–∞—В—М—Б—П –Є —Б –љ–µ–і–Њ—Б—В–∞—В–Ї–∞–Љ–Є –Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є —В–µ—А–∞–њ–Є–Є –Р–°–Ъ, –∞ —В–∞–Ї–ґ–µ —Б —А–µ–Ј–Є—Б—В–µ–љ—В–љ–Њ—Б—В—М—О –Ї —В–µ—А–∞–њ–Є–Є –Р–°–Ъ.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ш–љ—Б—Г–ї—М—В. –Я—А–Є–љ—Ж–Є–њ—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є, –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є / –Ъ—А–∞—В–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. –Я–Њ–і —А–µ–і–∞–Ї—Ж–Є–µ–є –Э.–Т. –Т–µ—А–µ—Й–∞–≥–Є–љ–∞, –Ь.–Р. –Я–Є—А–∞–і–Њ–≤–∞, –Ч.–Р. –°—Г—Б–ї–Є–љ–Њ–є. –Ь., 2002
2. –°—Г—Б–ї–Є–љ–∞ –Ч.–Р. –Ш—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є —Б–Є—Б—В–µ–Љ–∞ –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ (–Ї–ї–Є–љ–Є–Ї–Њ––±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ). –Ф–Є—Б—Б. –і–Њ–Ї—В. –Љ–µ–і. –Э–∞—Г–Ї. –Ь., 1990
3. –°—Г—Б–ї–Є–љ–∞ –Ч.–Р., –Т—Л—Б–Њ—Ж–Ї–∞—П –Т.–У. –Р–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Љ–∞–ї—Л—Е –і–Њ–Ј –∞—Б–њ–Є—А–Є–љ–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–Њ–ї—М–љ—Л—Е —Б —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –љ–∞ —Д–Њ–љ–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –Љ–µ–і–Є—Ж–Є–љ–∞, 1983; 9: 51–59.
4. –°—Г—Б–ї–Є–љ–∞ –Ч.–Р., –Ш–Њ–љ–Њ–≤–∞ –Т.–У. –Т–ї–Є—П–љ–Є–µ –Љ–∞–ї—Л—Е –і–Њ–Ј –∞—Б–њ–Є—А–Є–љ–∞ –љ–∞ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Г—О —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї—Г –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ –Є –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е —Б —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є / –Т –Ї–љ. –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—П –Є –љ–∞—Г—З–љ–Њ–—В–µ—Е–љ–Є—З–µ—Б–Ї–Є–є –њ—А–Њ–≥—А–µ—Б—Б. –Ґ–∞—И–Ї–µ–љ—В, 1988
5. A comparison of two doses of aspirin (30 mg vs. 283 mg a day) in patients after a transient ischemic attack or minor ischemic stroke. The Dutch TIA Trial Study Group. N Engl J Med. 1991 Oct 31;325(18):1261–1266
6. A randomized trial of aspirin and sulfinpyrazone in threatened stroke: the Canadian Cooperative Study Group. N Engl J Med. 1978; 299:53–59
7. Adams H. et al. Guidelines for the management of adults with ischemic stroke. Stroke 2007; 38; 1655–1711
8. Albers G.W. AHA Scientific Statement. Supplement to the guedelines for the management of transient ischemic attacks: A statement from the Ad Hoc Committee on guedelines for the management of transient ischemic attacks, Stroke Council, AHA. Stroke 1999, 30: 2502–2511
9. Algra A.,Van Gijn J. Aspirin at any dose above 30 mg offers only modest protection after cerebral ischemia. J Neurol Neurosurg Psychiatry, 1996; 60: 197–199.
10. Antithrombotic Trialists’ Collaboration. Collaborative meta–analysis of randomised trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ. 2002; 324: 71–86
11. Atlas of Atherothrombosis / Edit.–in–Chief Topol E.J. Science Press, UK, 2004
12. CAST (Chinese Acute Stroke Trial) Collaborative Group. CAST: randomised placebo–controlled trial of early aspirin use in 20,000 patients with acute ischaemic stroke. Lancet. 1997;349:1641–1649
13. Catella–Lawson F. et al. Cyclooxygenase inhibitors and the antiplatelet effects of aspirin. N Engl J Med 2001; 345: 1809–1817
14. Cote R. et al. Lack of effect of aspirin in asymptomatic patients with carotid bruits and substantial carotid narrowing. Ann Intern Med, 1995; 123: 649–655.
15. Diener H.C. et al., for the European Stroke Prevention Study 2. Cardiac safety in the European Stroke Prevention Study 2 (ESPS2). Int J Clin Pract. 2001; 55: 162–163
16. Engelter S., Lyrer P. Antiplatelet therapy for preventing stroke and other vascular events after carotid endarterectomy. Cochrane Database Syst Rev 2003:CD001458
17. Farrell B. et al. The United Kingdom transient ischaemic attack (UK–TIA) aspirin trial: final results J Neurol Neurosurg Psychiatry. 1991 Dec;54(12):1044–1054
18. Feng D. et al. Effect of aspirin dosage and enteric coating on platelet reactivity. Am J Cardiol, 1997; 80: 189–193
19. Fields W.S. et al. Controlled trial of aspirin in cerebral ischemia. Stroke, 1977; 8, 301–314
20. Guidelines for Management of Ischaemic Stroke of the European Stroke Organisation, 2008 http://www.eso–stroke.org/recommendations
21. Hansson L. et al. Effects of intensive blood–pressure lowering and low–dose aspirin in patients with hypertension: principal results of the Hypertension Optimal Treatment (HOT) randomised trial. Lancet 1998;351(9118):1755–62
22. Hobson R. et al. Influence of aspirin in the management of asymptomatic carotid artery stenosis. Va cooperative study group on asymptomatic carotid stenosis. J Vasc Surg 1993;17:257–263
23. International Stroke Trial Collaborative Group. The International Stroke Trial (IST): a randomised trial of aspirin, subcutaneous heparin, both, or neither among 19435 patients with acute ischaemic stroke. Lancet. 1997;349:1569 –1581
24. Johnson E.S. et al. A metaregression analysis of the dose–response effect of aspirin on stroke. Arch Intern Med., 1999;159: 1248–1253
25. Juul–Moller S. et al. Double–blind trial of aspirin in primary prevention of myocardial infarction in patients with stable chronic angina pectoris. The Swedish Angina Pectoris Aspirin Trial (SAPAT) Group. Lancet. 1992;340(8833):1421–1425
26. Lee T.K. et al. Inhibitory effect of acetylsalicylic acid on platelet function in patients with completed stroke or reversible ischemic neurologic deficit. Stroke, 1988; 19: 566–570
27. Lindblad B. et al. Does low–dose acetylsalicylic acid prevent stroke after carotid surgery? A double–blind, placebo–controlled randomized trial. Stroke 1993, 24: 1125–1128
28. Peto R. et al. Randomized trial of prophylactic daily aspirin in British male doctors. Br Med J (Clin Res) 1988; 296 (6618):313–316
29. Ridker P.M. et al. A randomized trial of low–dose aspirin in the primary prevention of cardiovascular disease in women. N Engl J Med 2005;352:1293–1304
30. Steering Committee of the Physicians' Health Study Research Group. Final report on the aspirin component of the ongoing Physicians' Health Study. N Engl J Med 1989; 321(3):129–35
31. Stroke Prevention in Atrial Fibrillation Study. Final results. Circulation. 1991; 84(2):527–539
32. Swedish Aspirin Low–Dose Trial (SALT) of 75 mg aspirin as secondary prophylaxis after cerebrovascular ischaemic events. The SALT Collaborative Group. Lancet. 1991 Nov 30;338(8779):1345–1349
33. The Multicentre Acute Stroke Trial–Italy (MAST–I) Study Group. Randomised controlled trial of Streptokinase, aspirin, and combination of both in treatment of acute ischemic stroke. Lancet. 1995; 346:1509–1514
34. Thrombosis prevention trial: randomized trial of low–intensity oral anticoagulation with warfarin and low–dose aspirin in the primary prevention of ischaemic heart disease in men at increased risk: the Medical Research Council's general practice research framework. Lancet 1998;351(9098):233–41












