


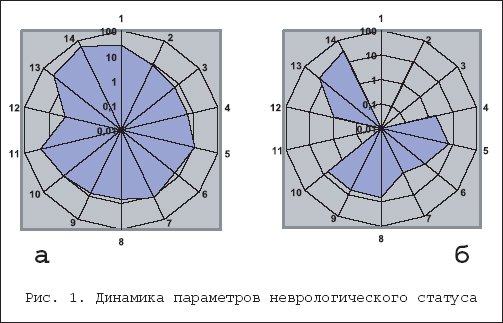
Современной неврологией и реаниматологией сформулированы положения о ведущей роли гипоксии и эндогенной интоксикации в возникновении любого критического состояния, а также в дезинтеграции регуляторно–трофической деятельности центральной нервной системы. Эта дезинтеграция обусловливает прогрессирование расстройств систем гомеостаза, снижение неспецифической резистентности организма, развитие и прогрессирование очаговой и диффузной неврологической патологии, значительно усугубляющей тяжесть фонового заболевания. Помимо пациентов с патологией нервной системы экстрацеребрального генеза, в последние годы в отделениях интенсивной терапии и реанимации многопрофильных больниц более чем в 3 раза увеличилось число больных с интрацеребральной патологией, прежде всего с нарушениями мозгового кровообращения. В конце XX и начале XXI века проблема инсульта приобрела не только медицинское, но и медико – социальное значение . Это связано с колоссальным ростом численности больных с острой церебральной сосудистой патологией, ростом летальности и инвалидизации. По материалам ВОЗ, частота инсульта в течение года колеблется от 1,5 до 7,4 на 1000 населения . Имеется прямая корреляция между заболеваемостью инсультом и возрастом пациентов. Наиболее высока заболеваемость инсультом в возрасте от 60 до 75 лет. Так, в возрасте 50–59 лет она составляет 7,4 на 1000, а в возрасте 70–75 лет – 20 на 1000 населения. В 52–70% случаев пациенты, перенесшие инсульт, остаются инвалидами, нуждающимися в постороннем уходе. Процент заболеваемости в нашей стране точно неизвестен из–за отсутствия общегосударственного регистра инсульта, но в реальности он выше данных ВОЗ. В РФ в течение последнего десятилетия отмечается прогрессирующий рост заболеваемости инсультом и постинсультной инвалидизации. Так, в Москве количество острых инсультов составляет от 100 до 120 случаев в сутки, что за год составляет от 36 до 44 тысяч. Колоссальные затраты на лечение пациентов с последствиями острых нарушений мозгового кровообращения могут быть сокращены не только правильной профилактикой этого тяжелейшего заболевания, но и рациональной и патогенетическиобусловленной терапией мозгового инсульта, особенно в ранние его сроки. Возможность воздействия различными фармакологическими препаратами при локальной ишемии мозга ограничена нескольники составляющими: – временными рамками (период от 2 до 6 часов), когда еще имеется возможность влияния на зоны отека и пограничные с необратимо пострадавшими; – правильным подбором средств нейрофармакологической коррекции; – адекватными способами доставки этих средств в точку действия; – целесообразностью комплексного воздействия на нейрональном, органном и организменном уровнях. Проблема эффективной терапии больных с критическими состояниями экстрацеребрального и интрацеребрального генеза представляется весьма сложной и далеко еще не решенной, несмотря на значительный накопленный опыт. Тем не менее в терапии таких больных есть несколько бесспорных и важнейших общих положений, применение которых позволяет в ряде случаев добиваться успеха. К общим принципам лечения таких больных относятся прежде всего восстановление перфузии тканей, коррекция нарушений дыхания и устранение гипоксии , так как гипоксия является ведущим повреждающим фактором при любых критических состояниях. Гипоксия – это нарушение кислородного баланса, при котором обеспечение организма кислородом неадекватно потребности в нем. От длительности периода гипоксии и степени ее выраженности во многом зависит вероятность развития посткритических осложнений и исход заболевания. Известна роль гипоксии для продукции и освобождения вазоактивных метаболитов и других токсических соединений. Эти метаболиты, воздействуя на сосудистое русло и миокард, вызывают депрессию его сократительной способности, создавая условия для прогрессирования расстройств макро– и микроциркуляции. На фоне расстройств микроциркуляции и подавления иммунитета у больных с критическими состояниями возрастает роль бактериальной эндотоксемии, как пускового механизма формирования многих патологических процессов, прежде всего – полиорганной недостаточности. Факторы и механизмы формирования полиорганной недостаточности (ПОН) достаточно подробно изучены и складываются из нескольких составляющих, таких как: механические факторы, вызывающие нарушения микроциркуляции и гипоксические повреждения; неуправляемый выброс цитотоксических медиаторов, повреждающих мембраны и клетки; специфические дефекты в клеточных и митохондриальных окислительных процессах вследствие прямого угнетающего действия эндотоксинов. Несмотря на существенные различия в подходах к оценке значения тех или иных факторов в патогенезе постгипоксического повреждения тканей, следует признать, что ведущая роль принадлежит нарушениям метаболизма, утилизации и расходования энергии в клетках. Тканевая гипоксия может развиваться даже при достаточно высоком сердечном выбросе, давлении и оксигенации крови вследствие нарушения микроциркуляции и расстройств метаболизма. Повреждающее действие эндотоксикоза проявляется главным образом в двух направлениях: путем прямого воздействия на капилляры, приводящего к увеличению их проницаемости, и непрямым эффектом, в результате которого освобождающиеся из надпочечников и постганглионарных симпатических нервных окончаний вазоактивные вещества воздействуют на сосудистую стенку. Необходимо отметить, что именно системная и церебральная гипоксия определяют особенности клиники, течение и прогноз критического состояния. Различная глубина повреждения вещества головного мозга (от нарушений корково–подкорковых взаимоотношений до мезенцефально–диенцефальных и стволовых расстройств) является результатом этого гипоксическо–токсического воздействия. Восстановление адекватного кислородного обеспечения органов и тканей создает предпосылки для их нормальной жизнедеятельности. Ведущим этиопатогенетическим фактором постгипоксической энцефалопатии (диффузной или очаговой) всегда является энергетичесикй дисбаланс, обусловленный системной, циркуляторной и нейрональной ишемией и гипоксией – результатом расстройств циклов аэробного и анаэробного окисления, утилизации кислорода и глюкозы. Таким образом, ведущим фактором сохранения нейроглиальных структур в условиях ишемии и гипоксии является поддержание стабильного церебрального кровотока, оксигенации и создание условий активации утилизации кислорода и глюкозы с целью обеспечения функционирования цикла Кребса. Практически все больные, перенесшие гипоксию, имеют различные формы поражений центральной нервной системы: от функциональных, проявляющихся астено–невротическим синдромом до глубоких нейроморфологических расстройств, ведущих к длительным депрессиям сознания, персистирующему вегетативному состоянию. При прогрессировании гипоксии при церебральном инсульте у больных возникают вторичные диффузные очаговые поражения, определяющие высокий процент летальности и постинсультной инвалидизации. Основной задачей и итогом деятельности реаниматологии как нейронауки, является не только поддержание основных жизненных функций, но и сохранение человека как социальной личности, а не вегетативной субстанции. Ни одно отделение реанимации не обладает возможностями эффективно лечить пациентов с уже развившимся персистирующим вегетативным состоянием. Эти пациенты тяжким и беспросветным грузом ложатся на руки персонала неврологических или нейрореанимационных отделений. Упущенные на ранних этапах терапии мгновения некорригированной гипоксии оборачиваются месяцами и годами бесперспективного лечения. Возможности коррекции как диффузных, так и очаговых расстройств при ишемических и гипоксических повреждениях мозга зависят от двух ведущих составляющих: 1) от глубины воздействия патогенетических факторов; 2) от возможности восстановления обратимо поврежденной мозговой ткани за счет активации и поддержания механизмов функционирования церебральных структур и гомеостаза организма. Реституционные (восстановительные) процессы могут происходить в нервных клетках, волокнах, синаптическом аппарате и в структурных элементах нейродистрофически измененных органов и тканей и осуществляться благодаря восстановлению проницаемости и возбудимости мембран, нормализации внутриклеточных окислительно–восстановительных процессов и активации ферментных систем, следствием чего является нормализация биоэнергетической и белоксинтезирующих функций нейронов. Возможности фармакологических вмешательств и коррекции этих процессов на современном этапе достаточно широки, но не всегда эффективны, поскольку при большом количестве препаратов с нейротропным действием, при крайне тяжелых расстройствах нейрометаболизма они зачастую бывают малоэффективны. Совершенно обособленно в ряду антигипоксических препаратов, влияющих на содержание циклических нуклеотидов (АТФ) в клетке, т.е. на поддержание адекватного церебрального метаболизма и интегративной деятельности нервной системы, стоит препарат Актовегин. На протяжении последних 20 лет препарат стал уже не средством выбора, а неотъемлемой частью фармакологического арсенала многих отделений реанимации и интенсивной терапии и неврологических отделений. Актовегин – высокоактивный стимулятор синтеза и утилизации кислорода и глюкозы в условиях ишемии и гипоксии. Препарат, являющийся гемодиализатом, помимо неорганических электролитов и других микроэлементов, содержит 30% органических веществ, таких как пептиды, аминокислоты, нуклеозиды, промежуточные продукты углеводного и животного обмена, липиды и олигосахариды. Молекулярный вес его органических соединений составляет менее 5000 дальтон. Клетки различных клеточных и тканевых культур, а также органов людей и животных под воздействием Актовегина увеличивают потребление кислорода и глюкозы. Этот эффект, независимый от самого органа, ведет к увеличению энергетического статуса клетки, что, в свою очередь, оказывает влияние на ее функциональный метаболизм. С помощью различных хроматографических методов было доказано, что выделенная из Актовегина активная фракция оказывает инсулиноподобное действие на биосинтез липидов , который может вырасти в зависимости от дозы в 5 раз, с торможением внутриклеточного образования Ц–АМФ. Применение активной фракции препарата вызывает зависящую от концентрации стимуляцию активности пируватдегидрогеназы (ПДГ). Актовегин не только улучшает транспорт глюкозы и поглощение кислорода, но и стимулирует их утилизацию, что улучшает кислородный метаболизм. Этот механизм обеспечивает клиническую эффективность в условиях временно индуцированного стресса и гипоксии тканей. Влияние препарата на утилизацию глюкозы особенно велико, так как при артериальной недостаточности любого генеза глюкоза является единственным и самым важным субстратом для производства энергии. Более того, последние исследования показали, что у пациентов с артериальной недостаточностью наблюдается резистентность к инсулину и карбогидратный метаболизм может быть устранен инсулиноподобным действием Актовегина. Используя биохимические методы, Ноуег и соавт. показали, что Актовегин оказывает положительное действие на нарушенный церебральный метаболизм при ишемии , наблюдая заметные изменения в накоплении глюкозы, АТФ и лактата под действием основных субстратов Актовегина, представленных в таблице 1. Кроме общей церебральной ишемии, гемодиализат с успехом применялся для улучшения энергетического статуса клеток, при поражениях гиппокампа. Структурный анализа раствора Актовегина выявил в нем присутствие 6 основных микроэлементов (натрия, калия, кальция, фосфора, магния). Магний входит в Актовегин на правах компонента нейропептидных фрагментов и ферментов в качестве каталитического центра. При этом необходимо отметить, что по данным современной нейробиохимии именно магний является каталитическим центром всех известных на сегодняшний день нейропептидов головного мозга и имеет статус нейроседативного иона. Актовегин обладает как центральным действием, стимулируя процессы церебрального метаболизма, так и достаточно выраженным действием при периферических артериальных нарушениях. Этот механизм обеспечивает стабилизацию функционального метаболизма тканей в условиях временно индуцированного стресса и гипоксии припериферических артериальных расстройствах, часто сопровождающих тяжелое течение нарушений мозгового кровообращения. Речь идет о стимуляции под действием Актовегина периферического кровотока , улучшении периферической трофики и профилактики пролежней. Применение Актовегина целесообразно в различных областях медицины для коррекции состояния органов и тканей при патологических состояниях, и в том числе – с особенной эффективностью при критических состояниях связанных с ишемией и гипоксией. Основные механизмы действия Актовегина как стабилизатора энергетического гомеостаза в условиях критических состояний представлены в таблице 2. Использование Актовегина у больных с церебральными инсультами показано при депрессии фоновой функциональной активности ЭЭГ, выявленной при мониторировании спектра ЭЭГ или при исследовании нативной ЭЭГ. Целесообразность такого использования объективизирована большим количеством исследований в ведущих лечебных учреждениях, где препарат активно и с успехом используется уже в течение многих лет и имеет под собой биохимическое обоснование, базирующееся на рецепторнотропных и нейрорегуляторных механизмах действия препарата, представленных в таблице 3. В нашей клинике на протяжении многих лет проводились исследования эффективности использования Актовегина у больных с критическими состояниями различного генеза, прежде всего – с постгипоксической энцефалопатией и церебральными инсультами ишемического характера. Клинические исследования при применении Актовегина с оценкой особенностей соматического и неврологического статуса, комплекса биохимических показателей, данных кислотно–щелочного состояния крови, балльной оценки состояния сознания и параметров иммунологического статуса объективизировались также изучением состояния электрогенеза мозга по данным компрессированного спектрального анализа электроэнцефалограммы (КСА ЭЭГ) с длительным мониторингом. Применение КСА ЭЭГ расценивается как высокоинформативный тест, позволяющий не только оценить сравнительную эффективность нейропротекторов, но и выработать критерии их назначения с учетом индивидуальной чувствительности. При использовании Актовегина положительная динамика прослеживалась у больных с острой постгипоксической энцефалопатией с фоновыми расстройствами сознания различной степени . Так, при депрессии сознания до уровня сопора и комы 1–2 она заключалась в активации состояния сознания до более высоких уровней значимо быстрее по сравнению со стандартной терапией, а при отсутствии фоново глубоких расстройств сознания (сонливость, оглушение) – в уменьшении явлений астено–невротического синдрома, головокружений, слабости, координаторных расстройств. У 62% больных положительная динамика после применения Актовегина коррелировала с активацией ? –ритма по данным КСА ЭЭГ, с билатеральным нарастанием суммарной мощности спектра, а при очаговых поражениях – в наиболее пострадавшем полушарии. Повышение энергетического уровня спектра в среднем составляло до 26% от исходного, характерен был также сдвиг в сторону быстрых волн, что у коматозных больных считается благоприятным прогностическим признаком. Подобная динамика спектра ЭЭГ отмечалась только у больных с фоново низким уровнем энергетического метаболизма, когда под воздействием нейрометаболитов удавалось нивелировать депрессию функциональной активности мозга с преобладанием низкоамплитудной медленноволновой части спектра. При исходно высоком уровне спектра КСА ЭЭГ, свидетельствовавшем о компенсаторном гиперметаболизме, положительных клинических и электрофизиологических феноменов отмечено не было. Эти особеннности клинико–электрофизиологических реакций на применение Актовегина дали основания предложить некоторые практические рекомендации по применению Актовегина у больных с критическими состояниями . Так, у больных с тяжелыми формами постгипоксической энцефалопатии (при расстройствах сознания до уровня комы 2–3) применение Актовегина считаем целесообразным на 3–4 сутки заболевания (после прекращения проведения нейровегетативной блокады) или при сочетании медикаментозной седации во второй половине дня и нейростимуляции в первой половине. Использование Актовегина целесообразно при депрессии фоновой функциональной активности ЭЭГ, выявленной при мониторировании спектра ЭЭГ. С целью изучения влияния инфузионно–корригирующих программ с использованием нейрометаболической терапии Актовегином на состояние гомеостаза, степень неврологического дефицита и уровень летальности больных с церебральными инсультами было проведено сравнительное комплексное клиническое соматоневрологическое и биохимическое исследование больных с церебральным инсультом, проходивших курс лечения в условиях нейроблока отделения реанимации (1 группа) и больных со сходной степенью тяжести и сроками развития инсульта, проходивших курс лечения в отделении неврологии (2 группа). У всех больных 1 группы был диагностирован ишемический инсульт в 70% случаев в системе каротидных церебральных сосудов, в 30% случаяев – в вертебрально–базиллярной системе. У 10% больных срок госпитализации от момента развития заболевания был от 2 до 6 часов, у 15% – до 24 часов, у остальных пациентов – более 24 часов. У всех больных отмечалась тяжелое течение инсульта с расстройствами сознания от сопора до комы, грубо выраженными очаговыми пирамидными или стволовыми симптомами, формирующимися расстройствами дыхания в виде тахи– или брадипное. У всех больных при сроках поступления более 24 часов были отмечены клинические и лабораторные расстройства состояния гемо– и гомеостаза, характеризовавшиеся явлениями дегидратации, сухостью кожных покровов и языка, тахикардией, снижением диуреза, отрицательными показателями центрального венозного давления, резким нарастанием гемоглобина (до 165–180 г/л), гематокрита (до 49–60%), выраженными явлениями гиперкоагуляции, нарастанием пула средних молекул, явлениями гипоксемии и ацидоза, с уменьшением артериовенозной разницы по кислороду. При сроках поступления в стационар в период от 6 до 24 часов все указанные расстройства гомеостаза также имели место, но были выражены в меньшей степени, что было связано с ранними сроками заболевания. Фоновая тяжесть инсульта, соматических расстройств и уровень лабораторных отклоненийу больных 2 группы были практически идентичными. Все пациенты 1 группы с момента поступления в нейроблок отделения реанимации получали инфузионно–корригирующую терапию в объеме 50 мл/кг в сутки с учетом возраста больных, сопутствующей кардиальной патологии, в сочетании с нейрометаболитом Актовегином в дозировке 1000 мг в сутки в растворе для инфузий (250 мл в 10% р–ре глюкозы). Инфузионно–корригирующая терапия проводилась круглосуточно после постановки больным центральной вены стандартным подключичным доступом, что облегчало уход за пациентами, давало возможность контроля центрального венозного давления. Инфузия Актовегина проводилась в первой половине суток. Сочетание программированной гемодилюции с использованием электролитно сбалансированного нейрометаболита Актовегина в дозировке 1000 мг в сутки с 1 суток развития инсульта позволяло добиться оптимизации реологических свойств крови за счет снижения ее вязкости, уменьшения явлений циркуляторной гипоксии на фоне нарастания ОЦК, а также улучшения показателей неврологического статуса, урежения развития пролежней по сравнению с контрольной группой. На фоне указанной терапии было отмечено улучшение клинического состояния больных , активизация состояния сознания, стабилизация показателей неврологического статуса (рис. 1), купирование дыхательных расстройств без применения ИВЛ. По лабораторным показателям было отмечено снижение уровня гемоглобина и гематокрита, пула средних молекул, улучшение агрегационных свойств крови, стабилизация показателей КЩС. На рисунке 1б представлена положительная динамика параметров неврологического статуса (уменьшение площади диаграммы) по сравнению с фоновым состоянием больных (1а) на 5–е сутки лечения Актовегином. По данным мониторирования ЭЭГ на фоне применения Актовегина отмечалось нарастание спектра мощности ЭЭГ в диапазоне быстрых волн ( ? и ? ) до 20% от фонового и в диапазоне медленных волн до 15%. Положительная динамика спектра ЭЭГ опережала по времени активацию состояния сознания у пациентов в среднем на 12–24 часа, что позволяет использовать длительный электроэнцефалографическиймониторинг для выявления эффективности нейрофармакологического воздействия на состояние электрогенеза мозга и в качестве прогностическго критерия клинической динамики у больных с фоновыми депрессиями сознания и энергетического метаболизма головного мозга. Летальность в 1 группе больных составила: при поступлении в период до 6 часов 7% даже при фоновых расстройствах сознания до глубокого сопора; при поступлении в стационар в период до 24 часов – 10%; более 24 часов –14%. Во второй группе больных объем инфузионной терапии не превышал 400–600 мл в сутки, нейропротективная терапии антигипоксантом Актовегином не проводилась. Динамики лабораторных показателей в первые трое суток не отмечалось, гемоглобин и гематокрит оставались высокими, уровень диуреза низким, что усугубляло нарастающую тяжесть течения инсульта и прогрессирование дыхательных расстройств. Летальность в указанной группе составила 20%. Таким образом, актуальной для интенсивной терапии тяжелых форм острых нарушений мозгового кровообращения является инфузионная коррекция в сочетании с применением нейрометаболита Актовегина . Данная терапия за счет гемодилюции улучшает реологические свойства крови, а метаболотропное действие Актовегина позволяет стабилизировать оксигенацию за счет мобилизации респираторных единиц, снизить содержание продуктов нарушенного метаболизма, активировать утилизацию глюкозы и кислорода в условиях ишемии и гипоксии. Применение ориентированных на клинико–лабораторные показатели инфузионных программ с включением нейропротектора Актовегина в ранние сроки критических состояний экстра– и интрацеребрального генеза позволяет снизить летальность и добиться более выраженного регресса посткритического неврологического дефицита.




Данный информационный сайт предназначен исключительно для медицинских, фармацевтических и иных работников системы здравоохранения.
Вся информация сайта www.rmj.ru (далее — Информация) может быть доступна исключительно для специалистов системы здравоохранения. В связи с этим для доступа к такой Информации от Вас требуется подтверждение Вашего статуса и факта наличия у Вас профессионального медицинского образования, а также того, что Вы являетесь действующим медицинским, фармацевтическим работником или иным соответствующим профессионалом, обладающим соответствующими знаниями и навыками в области медицины, фармацевтики, диагностики и здравоохранения РФ. Информация, содержащаяся на настоящем сайте, предназначена исключительно для ознакомления, носит научно-информационный характер и не должна расцениваться в качестве Информации рекламного характера для широкого круга лиц.
Информация не должна быть использована для замены непосредственной консультации с врачом и для принятия решения о применении продукции самостоятельно.
На основании вышесказанного, пожалуйста, подтвердите, что Вы являетесь действующим медицинским или фармацевтическим работником, либо иным работником системы здравоохранения.