Согласно современным представлениям хроническая гипергликемия при СД приводит к развитию патологии микроциркуляторного русла в сетчатке, почках и периферических нервах. Исследования DCCT и UKPDS показали, что имеется четкая корреляция между гипергликемией и диабетическими осложнениями при СД 1 и 2 типа. Большинство известных метаболических и сосудистых механизмов развития патологии при поздних осложнениях СД объединены их зависимостью от включения в патологический процесс гиперпродукции супероксида в митохондриях [17]. Таким образом, основной причиной формирования поздних осложнений СД является оксидантный стресс – нарушение равновесия между продукцией свободных радикалов и активностью антиоксидантных ферментов, которая при СД снижена [9]. Недостаточная активность антиоксидантных ферментов при СД определяется генетическими факторами, что подтверждается изучением полиморфизма генов ферментов антиоксидантной системы организма [2,22]. Возможность коррекции оксидантного стресса с уменьшением проявлений поздних осложнений СД была показана в клинических исследованиях с применением естественного антиоксиданта – a–липоевой кислоты (АЛК) [26]. Вместе с тем применение АЛК имеет свои ограничения – ее не следует применять у больных в возрасте старше 70 лет, у больных с наличием в анамнезе или на момент лечения нарушений сердечного ритма, при наличии свежих геморрагий на глазном дне. Начинать лечение АЛК следует с внутривенного ее введения, что также ограничивает круг больных, у которых ее можно использовать. Одним из препаратов, который может быть альтернативой АЛК, является признанный антиоксидант – Танакан [EGB 761], который показал свою эффективность в клинических исследованиях при заболеваниях, в патогенезе которых феномен окcидантного стресса играет важную роль [4].
Танакан – фармакологический препарат из натурального сырья, содержит стандартизированную смесь из фармакологически активных компонентов: 24% флавоноидных гликозидов и 6% терпеновых лактонов (гинкголиды, билобалиды). Он был впервые зарегистрирован во Франции фирмой «IPSEN Laboratories» в 1974 г. и представлен на рынке лекарственных препаратов в более чем 30 странах. Важным достоинством пероральных форм EGb 761 (таблетки, раствор) является их высокая биодоступность [24]. В экспериментальной работе методом спектрометрии электронного парамагнитного резонанса (ЭПР) исследована активность EGb 761, как ловушки основных видов свободных радикалов – супероксида и гидроксила, и показано, что он очищает исследованный раствор от обоих видов свободных радикалов [25].
Танакан предупреждает хроническое оксидативное поражение, улучшает кровоток в микроциркуляторном русле, уменьшает апоптоз нервных клеток и предотвращает окислительное поражение митохондрий, что предполагает его эффективность при поражениях нервной системы у больных СД.
Клинические работы по использованию Танакана при сосудистых нарушениях, в основном цереброваскулярной патологии, проведены в Германии и Франции и показали его эффективность в дозе от 120 до 360 мг в день. Отечественные исследования подтвердили, что Танакан оказывает несомненный эффект при сосудистых поражениях головного мозга, уменьшая выраженность когнитивных нарушений [4]. Цель настоящего исследования заключалась в оценке эффективности и переносимости препарата Танакан у больных СД 2 типа с дистальной симметричной сенсорно–моторной полиневропатией и диабетической ретинопатией.
Пациенты и методы исследования. В рамках открытого многоцентрового исследования проведено обследование 58 больных СД 2 типа (13 мужчин и 45 женщин) в возрасте от 39 до 75 лет (средний возраст 61,1±9,0 лет), длительностью СД от 1 года до 24 лет (в среднем 14,7±7,8 лет), длительностью ДПН от 1 года до 15 лет (5,0±3,1 лет) и ДР от 1 года до 14 лет (4,3±3,2 лет). Индекс массы тела в группе составил 24,4±4,3 кг/см2, уровень гликогемоглобина (HbA1с) – 8,56±0,18% (меньше 10% индивидуально). 32 больных получали таблетированные формы сахароснижающих препаратов (гликлазид, глибенкламид, гликуидон) и 26 больных – комбинированную терапию (инсулин и пероральные сахароснижающие препараты). В процессе лечения Танаканом сахароснижающую терапию у больных не изменяли. Пациенты получали Танакан в дозе 120 мг в сутки (40 мг 3 раза в день) в течение 2 мес. Обследование больных проводилось до начала, на 21–й и 60–й день лечения Танаканом.
У всех больных определяли уровень гликозилированного гемоглобина, интенсивность перекисного окисления липидов (ПОЛ) в сыворотке крови и мембранах эритроцитов. Для оценки выраженности ДПН анализировали жалобы пациентов (шкала TSS) и неврологическую симптоматику (шкала NISLL). Электромиографическое исследование (ЭМГ) проводили до начала лечения и на 60–й день при кожной температуре не ниже 30°С. Анализировали скорость распространения возбуждения (СРВ), резидуальную латенцию (РЛ) и амплитуду М–ответа при стимуляции моторных волокон срединного и малоберцового нервов, амплитуду потенциала, СРВ при стимуляции сенсорных волокон срединного и икроножного нервов. Состояние микроциркуляции ногтевого ложа безымянного пальца исследовали с помощью компьютерного капилляроскопа «Капилляр» (Россия) в положении сидя, с руками, расположенными на уровне сердца, при комнатной температуре 21–23°С. До обследования больные находились в покое около 20 минут и в день обследования не курили, не пили кофе и не применяли препаратов, влияющих на артериальное давление. Определение скорости капиллярного кровотока проводилось не менее чем в 6 различных капиллярах, в течение 10 с. Обследование пациентов на выраженность ДР включало определение остроты зрения, биомикроскопию, офтальмоскопию. Для фоторегистрации картины глазного дна использовался ретинофот «CR–45 ММ» фирмы «Canon»; исследование полей зрения проводилось на отечественном компьютере «Периком». В группу сравнения вошли 50 больных СД, которые получали только сахароснижающую терапию.
Статистическая обработка материала проводилась методами вариационной статистики с использованием критерия достоверности Стьюдента, для малых выборок – непараметрическими методами.
Результаты и обсуждение. Лечение Танаканом не вызвало существенного изменения показателей углеводного обмена. До лечения уровень HBA1c составлял 8,56±0,18%, а после лечения – 8,34±0,19%. Достоверно снижались уровни холестерина (5,61±0,10 до и 4,89±0,07 ммоль/л после лечения, p<0,01) и b–липопротеидов (5,65±0,16 до и 5,35±0,10 ммоль/л после лечения, p<0,05). Уровень триглицеридов на фоне лечения не изменился (2,24±0,10 до и 2,00±0,05 ммоль/л после лечения). Танакан не оказал влияния на углеводный обмен, хотя в условиях эксперимента другой антиоксидант – АЛК – обладает способностью уменьшать инсулинорезистентность. С другой стороны, при клинических исследованиях значимый гипогликемический эффект тиоктовой кислоты подтверждался не всегда. Неожиданным оказался эффект Танакана на липидный обмен, что ранее не описывалось в литературе при обследовании больных с СД, хотя показано улучшение показателей липидного обмена при лечении Танаканом пациентов с облитерирующим эндартериитом [6]. Улучшение биохимических показателей липидного обмена в нашем исследовании сочеталось с уменьшением числа липидных включений в капиллярном кровотоке. Здесь следует отметить, что некоторые антиоксиданты (например, a–токоферол) уменьшают уровень атерогенных липопротеинов.
Уровень МДА в плазме до лечения составлял 1,25±0,03 нмоль/мл, 0,98±0,01 – на 21 день и 0,71±0,02 на 60 день лечения (р<0,01). В мембранах эритроцитов уровень МДА до лечения составлял 2,15±0,02 нмоль/мл, на 21 день – 1,78±0,02 и на 60 день лечения – 1,20±0,02 (p<0,01). В контрольной группе из 10 здоровых добровольцев, сопоставимых по возрасту, уровень МДА в плазме составлял 0,30±0,05, а в мембранах эритроцитов – 0,95±0,12 нмоль/мл. При CД одним из основных механизмов действия оксидантного стресса на нервные ткани является образование продуктов перекисного окисления липидов. У обследованной группы больных выявлено исходное увеличение ПОЛ в сыворотке и мембранах эритроцитов. Назначение Танакана привело к достоверному уменьшению содержания МДА как в сыворотке, так и мембранах эритроцитов, что подтвердило значительный антиоксидантный эффект Танакана. Дозозависимое угнетение EGb 761 перекисного окисления липидов показано и в экспериментальных работах на тканях головного мозга и тканях печени [19,21]. Ранее уменьшение выраженности ПОЛ при лечении Танаканом было показано у больных с сахарным диабетом 1 типа [8].
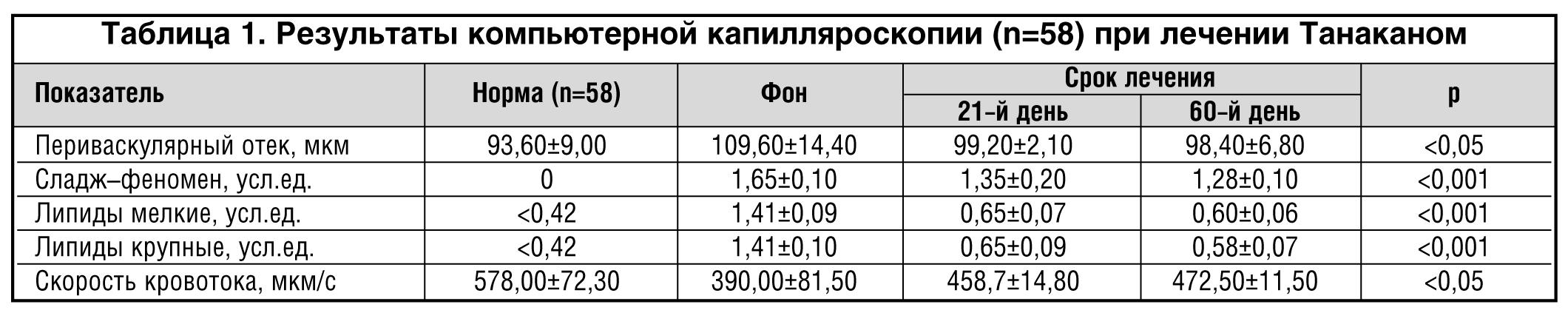
Компьютерная капилляроскопия ногтевого ложа показала, что исходно у больных СД 2 типа имеются выраженные нарушения микроциркуляции в виде извитости капилляров, укорочения капиллярных петель, обедненности капиллярного рисунка, замедленности кровотока, увеличения зоны перикапиллярного отека, наличия сладж–феноменов, увеличения числа липидных включений.
Исследование состояния микроциркуляции ногтевого ложа при лечении Танаканом (табл. 1) выявило значительное улучшение практически всех показателей состояния микроциркуляторного русла: уменьшение периваскулярного отека, сладж–феномена и количества липидных включений, увеличение скорости кровотока. Исследование микроциркуляции у человека в динамике под действием различных лекарственных веществ возможно при морфологических исследованиях биоптатов кожи, при помощи лазерной допплеровской анемометрии и компьютерной капилляроскопии [7,11]. Компьютерная капилляроскопия относится к неинвазивным методам в отличие от морфологических методик и в отличие от допплеровской анемометрии позволяет позволяет оценить весь спектр параметров микроциркуляции (не только скорость кровотока, но и периваскулярный отек, выраженность сладж–феномена, количество липидных включений в капиллярной крови), что делает ее особо привлекательной при обследовании больных с СД. Основной вопрос, который возникает при трактовке полученных результатов, заключается в том, можно ли переносить результаты, полученные при исследовании капилляров ногтевого ложа, на эндоневральный кровоток. Рассматривая микроциркуляцию в различных органах и тканях как единую систему, реагирующую на патогенные воздействия одинаково качественно, хотя и различно – количественно, можно считать, что изучение состояния микроциркуляции в конкретной области дает представление о ее состоянии в целом [3]. В определенной мере это подтверждается в нашем исследовании улучшением состояния капилляров сетчатки с увеличением объема зрения. Нарушение микроциркуляции во многом связано с действием фактора активации тромбоцитов (ФАТ). ФАТ вызывает агрегацию тромбоцитов, формирование тромбов и стимулирует образование свободных радикалов. Показано, что EGb 761 угнетает эти действия ФАТ, ингибируя агрегацию тромбоцитов и блокируя связь ФАТ с тромбоцитами [12]. В эксперименте показано, что EGb 761 стимулирует продукцию простациклина и эндотелий–зависимого релаксирующего фактора, угнетает агрегацию тромбоцитов и эритроцитов, улучшает эластичность мембран эритроцитов, повышая их способность к деформации, уменьшает проницаемость сосудистой стенки [13].
Субъективные неприятные ощущения больных, обусловленные ДПН (боль, жжение, парестезии, онемение), по шкале TSS (значение до начала лечения – 5,89±0,84 баллов) достоверно уменьшались уже к 21 дню лечения (3,78±1,03 баллов) и еще больше – к 60 дню (1,64±0,29 баллов, р<0,01). Динамика объективных симптомов по шкале NISLL в виде уменьшения нарушений чувствительности и оживления или появления сухожильных рефлексов была достоверной к 60 дню лечения (в начале лечения – 7,76±2,16 баллов, на 21 день – 6,79±1,98 баллов, на 60 день – 5,68±1,51 баллов, р<0,05). Таким образом, на фоне лечения Танаканом отмечено как уменьшение субъективных проявлений ДПН, так и улучшение неврологической симптоматики. Последнее является крайне важным, так как, например, основным возражением против результатов исследования ALADIN [26] было применение только шкалы TSS, оценивающей субъективные ощущения больных. Вместе с тем известно, что большинство ощущений при ДПН плацебозависимо, поэтому необходимо для подтверждения эффекта препарата получить улучшение по плацебонезависимой шкале NISLL.
ЭМГ показатели при подсчетах в общей группе достоверно не изменялись, кроме резидуальной латенции n. medianus (2,95±0,18 мс до лечения и 2,71±0,14 мс – после него, р<0,01). При специальном подсчете динамики только в группах больных, имевших исходное патологическое уменьшение (амплитуда М–ответа и ПД, СРВ) или увеличение (РЛ) ЭМГ–показателей функции нерва, был выявлен достоверный положительный эффект лечения Танаканом в отношении как двигательных, так и чувствительных нервов (табл. 2).
Отмечено улучшение всех показателей – амплитуды М–ответа и потенциала действия чувствительного нерва, резидуальной латенции и СРВ. Исследование функционального состояния периферических нервов при испытании препаратов, предназначенных для лечения ДПН, является обязательным атрибутом современных исследований [26]. Крайне важно, что отмечено не только улучшение СРВ, что может отражать не процесс ремиелинизации, а улучшение функции К–Nа–АТФазы, но также увеличение амплитуды, что свидетельствует о воздействии на активность новых мышечных волокон в результате процессов реиннервации [1].
При исследовании состояния глазного дна отсутствие ДР выявлено у 14 больных, непролиферативная ДР (ДР1) – у 17, препролиферативная ДР (ДР2) – у 24 и пролиферативная ДР – у 3 больных. Офтальмоскопическая картина глазного дна была представлена расширенностью и извитостью вен (ДР1), наличием интраретинальных геморрагий и эксудатов (ДР2), новообразованных сосудов, пролиферативной тканью в случаях пролиферативной ДР. К концу лечения отмечалось частичное рассасывание интраретинальных кровоизлияний (51,16% больных), исчезновение мелких экссудатов (37,5%), уменьшение отека сетчатки (23,8%). Всего у 66,7% больных наблюдалась положительная динамика. Ни у одного больного не произошло ухудшения состояния глазного дна. При осмотре через 6 месяцев у всех больных сохранялись отмеченные при приеме Танакана положительные сдвиги. В группе сравнения картина глазного дна была нестабильной, ретинопатия прогрессировала: у 26,9% больных увеличился отек сетчатки и количество интраретинальных геморрагий, у 7,3% больных с ДР1 появилась неоваскуляризация диска зрительного нерва, у 25,4% больных с ДР2 потребовалась лазерная коагуляция сетчатки (рис. 1). Острота зрения увеличилась на 0,1–0,2 только у 5 (8,6%) больных, а у остальных осталась без изменений. Вместе с тем компьютерная периметрия показала, что на фоне лечения произошло расширения поля зрения (правый глаз до лечения – 74,9±2,43%, после – 82,2±1,88%; р<0,05; левый глаз до лечения – 75,12±2,56%, после – 81,90±1,87%; p<0,05) за счет уменьшения относительных и абсолютных скотом (правый глаз до лечения 5,94±1,48%, после – 4,10±0,69%; левый глаз 4,32±1,00% до лечения, 3,89±0,79% – после, p<0,05). При проведении общей и локальной электроретинографии (ЭРГ) на фоне лечения выявлена тенденция к нормализации всех показателей, но достоверным было только увеличение волны А (3,69±0,2 – до лечения, 6,02±0,81 – после лечения, n=48) при локальной ЭРГ. Танакан оказал несомненный эффект на состояние глазного дна, что привело к увеличению объема зрения и уменьшению числа относительных и абсолютных скотом. Известно, что EGb 761 уменьшает содержание свободных радикалов в сетчатке, что было показано методом ЭПР после ишемии–реперфузии [23]. Дозозависимое действие EGb 761 на содержание свободных радикалов в сетчатке может быть обусловлено как эффектом ловушки, так и угнетением продукции свободных радикалов [16]. При ретинопатии показан патологический эффект свободных радикалов на сетчатку, связь свободных радикалов с пролиферативными процессами, обусловленными воспалением в сетчатке, и протекторное действие EGb 761 [10]. Сетчатка особенно богата полиненасыщенными жирными кислотами, поэтому она высокочувствительна к липидной пероксидации. EGb 761 предохраняет сетчатку от функционального и морфологического поражения, вызванного перекисным окислением липидов [20]. При исследовании электрофизиологической активности изолированной сетчатки крыс было показано, что применение препарата может предотвращать нарушения функции клеточных мембран сетчатки, которые наблюдаются при СД [14,15]. Клинические результаты нескольких двойных спепых плацебо–контролируемых исследований при диабетической ретинопатии также подтвердили фармакологический эффект EGb 761 в виде улучшения состояния сетчатки и увеличения остроты зрения [14]. Следует обратить внимание, что в этих исследованиях влияния Танакана на состояние сетчатки и остроту зрения курс лечения был длительный – до 6 месяцев. Возможно, что использованный нами курс лечения был недостаточным по продолжительности для получения «драматического» улучшения состояния зрительной функции и глазного дна.
Прием Танакана не вызвал отрицательных побочных эффектов ни у одного больного, за исключением пациентки с хроническим колитом в анамнезе, у которой в начале лечения участился стул, но в дальнейшем в процессе лечения нормализовался. Известно, что побочными эффектами при приеме Танакана могут быть диспептические явления, головная боль, головокружения, аллергические реакции, которые наблюдаются менее чем у 1% больных, и отмена препарата всегда приводит к их исчезновению [4].
Проведенное исследование показало, что Танакан, уменьшая выраженность оксидантного стресса, улучшает микроциркуляцию, функцию периферических нервов и сетчатки, приводя к значительному клиническому улучшению. Учитывая практическое отсутствие побочных эффектов, не вызывает сомнения, что Танакан является препаратом выбора для лечения пожилых больных с СД 2 типа с поздними осложнениями, особенно имеющих изменения в деятельности сердечно–сосудистой системы и когнитивные нарушения.
Литература:
1. Гехт Б.М., Коломенская Е.А., Строков И.А. Электромиографические характеристики нервно–мышечной передачи у человека. М.: Наука, 1974.
2. Дедов И.И. Сахарный диабет в Российской Федерации: проблемы и пути решения. // Сахарный диабет – 1998 – №1 – С.7–18.
3. Ефимов А.С. Диабетические ангиопатии. М., 1989.
4. Захаров В.В., Яхно Н.Н. Применение танакана при нарушениях мозгового и периферического кровообращения // Русск. мед. журн. – 2001 – Т.9,№5 – С.3–9.
5. Кацнельсон Л.А., Форофонова Т.И., Бунин А.Я. Сосудистые заболевания глаз. М., Медицина, 1990.
6. Наумов С.С. Результаты применения Танакана у больных хронической артериальной недостаточностью сосудов нижних конечностей в условиях поликлиники // В сб. «Танакан: опыт применения в медицинской практике в странах СНГ – М. – 2001 – С.73–74.
7. Салтыков Б.Б., Пауков В.С. Диабетическая микроангиопатия. М., Медицина, 2002.
8. Строков И.А., Смирнова В.Ю., Мясоедов С.П. Роль окислительного стресса в развитии поражения периферического нерва при сахарном диабете // Актуальные вопросы железнодорожной медицины – 1997 – М. – С. 404–406.
9. Baynes J.W., Thorpe S.R. Oxidative stress in diabetes // Antioxidants in diabetes management // Ed.: L.Packer, N.Y. M.Dekker Inc, 2000 – P. 77–92.
10. Baudouin C., Pisella P.J., Ettaiche M. et al. Effects of Egb 761 and superoxide dismutase in an experimental model of retinopathy generated by intravitreal production of superoxide anion radical // Graefes Arch. Clin. Exp. Ophthalmol – 1999 – Vol. 237 – P. 58–66.
11. Bollinger A., Fagrell B. Clinical capillaroscopy. Hogrefe & Huber Publishers, 1990.
12. Braquet P., Hosford D. Ethnopharmacology and the development of natural PAF antagonists as therapeutic agents // J. Ethnopharmacol. – 1991 – Vol. 32 – P. 135–139.
13. Delaflotte S., Auguet M., Defeudis F.V. et al. Endothelium–dependant relaxations of rabbit isolated aorta produced by carbochol and by Ginkgo biloba extract // Biomed.Boichim.Acta – 1984 – Vol. 43 – P. 8–9.
14. Doly M., Bonhomme B., Cluzel J. et al. Enhancement of retinal tolerance to glucose by adminisrtation of Ginkgo biloba extract (EGb 761) // Invest Ophthalmol Vis Sci – 1994 – –Vol. 35 – P.1587
15. Droy–Lefaix M.T., Bonhomme B., Doly M. Protective effect of Ginkgo biloba extract (EGB 761) on free radical–induced changes in the electroretinogram of isolated rat retina // Drugs Exp Clin Res – 1991 – Vol.17 – №12 – P.571–575
16. Droy–Lefaixt L.M.,Cluzel J., Menerath J.M. et al. Antioxidant effect of a Ginkgo biloba extract (EGb 761) on the retina // Int. J. Tissue React – 1995 – Vol. 17 – P. 93–100.
17. Du X.L. et al. Hyperglycemia–induced mitochondrial superoxide overproduction activates the hexosamine pathway and induces plasminogen activator inhibitor–1 expression by increasing Sp1 glycosylation // Proc Natl Acad Sci USA 97 – 2000 – P.12222–12226.
18. Giannini C., Dyck P.J. Pathologic alterations in human diabetic polyneuropathy // In: Diabetic neuropathy. Eds: Dyck P.J., Thomas P.K., 2–nd ed.: Phyladelphia: Saunders W.B., 1999 – P. 279–295.
19. Miyajima M., Yoshikawa T., Ichikawa H. et al. Anti–oxidative properties of Gingko biloba extract (GBE) // In: Frontiers of reactuve oxigen spacies in biology and medicine. Eds. Asada Kand Yoshikawa. Science B.V., Amsterdam: Elsevier Science B.V., 1994 – P.341–342.
20. Murata T., Nishida T., Eto S et al. Lipid peroxidation in diabetic rat retina // Metab Pediat Ophphalmol – 1981 – №5 – P.83–87
21. Seif E. L., Nasr M., El F. Lipid peroxide, phospholipids, biloba extract // Pharmacol. Res. – 1995 – Vol. 32 – P. 273–278.
22. Strokov I.A., Bursa T.R., Drepa O.I. et al. Predisposing genetic factors for diabetic polyneuropathy in patients with type 1 diabetes: a population–based case control study // Acta diabetologica – 2003 – Vol.40 – P.375–379.
23. Szabo M.E., Droy–Lefaix M.T., Doly M. EGb 761 and the recovery of ion imbalance in ischemic reperfused diabetic rat retina // Ophphalmic Res – 1995 – Vol 27 – №2 – P.102–109.
24. Wojcicki J., Gawronska S.B., Bieganowski W. et al. Comparative pharmacokinetics and bioavailability of flavonoid glycosides of Ginkgo biloba after a single oral administration of three formulations to healthy volunteers // Mater. Med.Pol. – 1995 – Vol. 27 – P. 141–146.
25. Yoshikawa T. Ginkgo biloba leaf extract: review of biological actions and clinical applications // Antioxidants & Redox Signaling – 1999 – Vol. 1, N 4 – P. 469–480.
26. Ziegler D., Reljanovic M., Mehnert H. et al. ?–Lipoic acid in the treatment of diabetic polyneuropathy in Germany: Current evidence from clinical trials // Exp.Clin. Endocrinol Diabetes – 1999 – Vol. 107 – P. 421