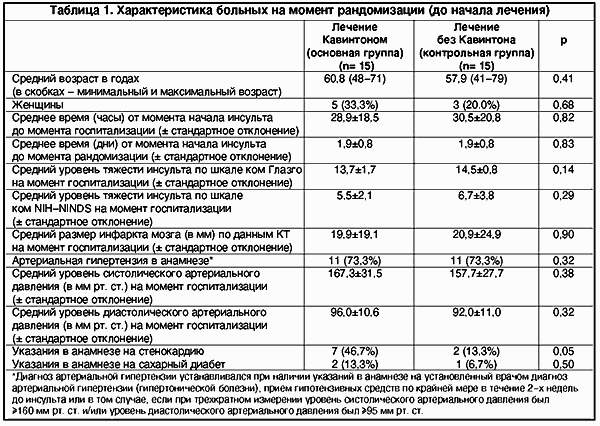
В данном рандомизированном клиническом исследовании была изучена безопасность и эффективность лечебного воздействия раннего применения препарата Кавинтон на функциональный исход и инвалидизацию больных с КТ-верифицированным диагнозом острого ишемического инсульта. Тридцать больных, отвечающих критериям включения и не имеющих критериев исключения из исследования, были рандомизированы с формированием двух группы, в одной из которых (основная группа, в количестве 15 больных, средний возраст 60,8 ±6,6 лет) лечение Кавинтоном проводилось в сочетании с препаратом Реополиглюкин, а в другой (контрольная группа, в количестве 15 больных, средний возраст 57,9 ±11,6 лет) лечение Реополиглюкином проводилось без сопутствующего лечения Кавинтоном. Обе группы были хорошо сопоставимы по основным прогностическим факторам. Неблагоприятным исходом считалась смерть больного или выраженная степень инвалидизации (уровень инвалидизации по индексу Бартела <70 или 3й-5й уровень инвалидизации по шкале Рэнкина).
Результаты настоящего исследования позволяют заключить, что:
1. Лечение препаратом Кавинтон улучшает восстановление неврологических функций и уменьшает степень инвалидизации больных с острым ишемическим инсультом.
2. Как показывают расчеты, для того, чтобы предупредить неблагоприятный исход заболевания (смертельный исход или выраженную инвалидизацию у 1 больного), нужно пролечить препаратом Кавинтон всего только 5 больных с острым ишемическим инсультом.
3. Тенденция к улучшению исходов инсульта по выраженности пропорциональна времени проведения лечения Кавинтоном. Наибольшие результаты достигаются к концу 3-го месяца заболевания.
4. Лечение препаратом Кавинтон не сопровождается выраженными побочными эффектами, препарат хорошо переносится больными.
Введение
Кавинтон (международное непатентованное название – винпоцетин, этиловый эфир аповинкаминовой кислоты) – производное алкалоида девинкана из растений рода Барвинок. Фармакологическими свойствами Кавинтона являются усиление мозгового кровотока в очаге ишемии [1], уменьшение агрегационной способности тромбоцитов [2] и увеличение деформируемости эритроцитов у больных с острыми цереброваскулярными заболеваниями [3]. Результаты исследований также указывают на то, что Кавинтон обладает нейропротективными свойствами [4-8] и предохраняет ткани мозга от ишемии [9]. Использование данного препарата в лабораторно-экспериментальных условиях сопровождалось уменьшением зоны инфаркта мозга [9, 10]. Результаты двух ранее проведенных двойных слепых плацебо контролируемых рандомизированных клинических исследований у больных с хронической цереброваскулярной недостаточностью и дегенеративными заболеваниями головного мозга указывают на способность Кавинтона существенно улучшать когнитивные функции у больных с данной патологией [11, 12]. Несмотря на большое количество проведенных в России исследований по изучению Кавинтона при острых цереброваскулярных заболеваниях, ни одно из ранее проведенных у нас в стране исследований не было основано на компьютерно-томографически (КТ) или магнитнорезонансно-томографически (МРТ) верифицированных случаях острого ишемического инсульта. Вместе с тем, общепризнанно, что для проведения патогенетической терапии острого ишемического инсульта обязательным является подтверждение характера инсульта методом КТ или МРТ головного мозга [13, 14].
В 1986 году в Венгрии было проведено двойное слепое рандомированное клиническое исследование эффективности Кавинтона у больных инсультом [15]. Однако КТ или МРТ головного мозга в данном исследовании не проводились. По данным недавно опубликованного мета-анализа [16], к 1998 году в мире не было проведено ни одного рандомизированного исследования по изучению эффективности применения Кавинтона у больных с КТ/МРТ с достоверным диагнозом острого ишемического инсульта.
Целью настоящего слепого рандомизированного клинического исследования являлось изучение безопасности и эффективности раннего применения препарата Кавинтон: 10 мг в/в капельно один раз в день на протяжении 5-7 дней с последующим пероральным приемом в дозе 10 мг 3 раза в день в течение 30 дней, на функциональный исход и инвалидизацию больных с КТ-верифицированным диагнозом острого ишемического инсульта.
Материал и методы
Отбор больных
В исследование были включены все госпитализированные в пределах 72 часов с момента начала ишемического инсульта больные, отвечающие критериям включения и не имеющие критериев для исключения из исследования. Диагноз ишемического инсульта устанавливался в том случае, если у больного имело место острое (минуты или часы) развитие очагового дефекта неврологических функций цереброваскулярного происхождения длительностью не менее 24 часов, при котором КТ головного мозга, проведенная в первые 72 часа заболевания, не обнаруживала никаких признаков кровоизлияния (данные КТ головного мозга могли указывать или не указывать на очаговую ишемию мозга, соответствующую зоне инфаркта мозга). КТ головного мозга была проведена у всех включенных в данное исследование больных до начала процедуры рандомизации.
Из исследования были исключены больные c любым из нижеперечисленных патологических состояний: повторный инсульт, коматозное состояние, неконтролируемый сахарный диабет, системное инфекционное заболевание, почечная или печеночная недостаточность, рак любой локализации, интракраниальное кровоизлияние (включая КТ признаки геморрагической трансформации зоны инфаркта мозга), предполагаемое использование антикоагулянтов, тяжелая форма ишемической болезни сердца (включая данные, указывающие на перенесенный инфаркт миокарда, сердечную недостаточность или выраженную аритмию сердца), установленный кардиогенный источник эмболии (включая мерцание предсердий и заболевание клапанного аппарата сердца), выраженная (систолическое давление – 220 мм рт. ст. и/или диастолическое давление – 140 мм рт. ст.) артериальная гипертензия, не корригируемая терапией на момент рандомизации, беременность, указание в анамнезе на плохую переносимость Кавинтона. Больные, отвечающие критериям включения и не имеющие критериев исключения из исследования, были рандомизированы методом последовательно пронумерованных непрозрачных конвертов. Рандомизационный код был генерирован компьютером на основе метода случайных чисел.
Порядок лечения
Дифференцированное лечение больных проводилось либо с использованием только препарата реополиглюкин (3 гр в 250 мл физиологического раствора в/в капельно - контрольная группа больных), либо реополиглюкином в сочетании с препаратом Кавинтон (в/в капельно в дозе 10 мг один раз в день в течение 5-7 дней с последующим переходом на пероральное применение в дозе 10 мг 3 раза в день в течение 30 дней - основная группа больных). Данное лечение начиналось сразу после рандомизации больного (в первые 3 дня после начала инсульта). Выбор сопутствующего лечения (включая назначение 20% раствора маннитола в дозе 0,25 мг/кг в 500 мл физиологического раствора в/в капельно, ноотропных, сердечно-сосудистых препаратов, ЛФК, массажа) определялся лечащим невропатологом в соответствии с медицинскими показаниями (все назначаемые больным препараты регистрировались с целью их последующего сопоставления в основной и контрольной группе ).
Оценка исходов
Степень тяжести инсульта определялась при госпитализации больных в соответствии со шкалой ком. Глазго [17] и шкалой инсульта Институтов здоровья (NIHNINDS) США [18]. Кроме того, шкала инсульта Институтов здоровья США была также использована для оценки динамики изменения степени тяжести инсульта через 1 месяц и через 3 месяца после его начала. Степень инвалидизации по индексу Бартела [19] и по шкале Рэнкина [20] определялась у всех рандомизированных больных через 1 месяц и через 3 месяца после начала инсульта. Для обеспечения сопоставимости результатов клинической оценки степени тяжести и уровня инвалидизации больных в течение всего периода катамнестического наблюдения перед началом исследования было проведено несколько учебных занятий для участвующих в исследовании невропатологов. Основными конечными точками, используемыми для оценки эффективности лечения, являлись дискретные исходы инсульта (благоприятный исход или неблагоприятный исход) к концу 3-го месяца заболевания, определяемые по модифицированным шкалам Бартела и Рэнкина (в случае смерти больного ему устанавливался наихудший показатель исхода). Неблагоприятным исходом считалась смерть больного или выраженная степень инвалидизации (уровень инвалидизации по индексу Бартела <70 или 3-5 уровень инвалидизации по шкале Рэнкина). Благоприятным исходом считался исход, при котором больной оставался жив и его уровень инвалидизации по индексу Бартела был і71 или 1-2 по шкале Рэнкина. Вторичными конечными точками, используемыми для оценки эффективности лечения, были показатели шкалы тяжести инсульта Институтов здоровья США (средние величины), определяемые к концу 1-го и 3-го месяца после инсульта, а также уровень инвалидизации по шкале Бартела и Рэнкина к концу 1-го месяца после инсульта. Хотя отнесение больных острым ишемическим инсультом к тому или иному тестируемому методу лечения было проведено открытым способом, больные не были информированы о том, получают ли они или не получают лечение Кавинтоном. Все возможные побочные эффекты лечения фиксировались у всех рандомизированных больных в течение первых 3-х месяцев после начала лечения.
Статистический анализ
Анализ данных проведен на основе принципа «intention-to-treat», то есть исходы заболевания и побочные эффекты лечения были проанализированы у всех первоначально рандомизированных больных. Сравнение частоты побочных эффектов лечения и дискретных исходов заболевания между основной и контрольной группами больных проведено на основе точного теста Фишера. Сопоставление продолженных показателей (показатели, для характеристики которых использовались их средние величины) между основной и контрольной группой больных проведено на основе метода ANOVA. Был также рассчитан относительный риск (ОР) неблагоприятного исхода ишемического инсульта и соответствующий ему 95% доверительный интервал (ДИ) [21]. Различия сравниваемых показателей признавались статистически значимыми при величине р <0,05. Статистическая обработка материала проведена на основе программы SPSS (версия 7.5.1) [22] и EPI INFO (версия 6.0) [23].
Результаты
За период с сентября 1998 г. по март 1999 г. было рандомизировано 30 больных острым ишемическим инсультом, госпитализированных в неврологическое отделение Муниципальной городской клинической больницы №1 г. Новосибирска. Катамнестические данные за 3-месячный период наблюдения получены у всех первоначально рандомизированных больных. Как видно из таблицы 1, распределение прогностически значимых факторов между больными основной и контрольной групп до начала лечения (до момента рандомизации) существенно не отличалось. В целом, стационарное лечение было начато через 29,9 часов после начала ишемического инсульта (стандартное отклонение ±19,3), и у 19 из 30 больных (63%) при поступлении в стационар на КТ головного мозга обнаружены признаки инфаркта мозга (табл. 1), что соответствует данным литературы. Клиническое состояние большинства больных при поступлении было средней или легкой степени тяжести (средний бал по шкале ком Глазго равен 14,1; стандартное отклонение ±1,4). Характер и объем сопутствующего лечения в основной и контрольной группах больных (дегидротационная и сердечно-сосудистая терапия, приём ноотропных препаратов, ЛФК, массаж, т.д.) достоверно не отличался. Побочных эффектов действия Кавинтона не обнаружено.
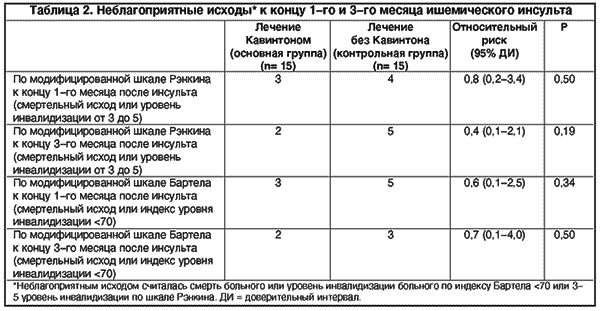
За период лечения 1 больной контрольной группы (реополиглюкин без Кавинтона) умер от инфаркта миокарда. На момент выписки из стационара уровень артериального давления в основной и контрольной группах больных статистически достоверно не различался: средний уровень систолического артериального давления в основной группе был 143 мм рт. ст. (стандартное отклонение ±13,7), в контрольной группе - 135,9 мм рт. ст. (стандартное отклонение ±18,7) (р= 0,26); среднее диастолическое артериальное давление в основной и котрольной группах было соответственно 88,3 мм рт. ст. (стандартное отклонение ±3,9) и 84,8 мм рт. ст. (стандартное отклонение ±8,4) (р= 0,19). Случаи неблагоприятных исходов к концу 1-го и 3-го месяца после ишемического инсульта отражены в таблице 2.
Обсуждение
Результаты данного рандомизированного исследования свидетельствуют о том, что при раннем применении препарата Кавинтон у больных острым ишемическим инсультом имеется отчетливая тенденция к улучшению неврологических функций и уменьшение инвалидизации больных (особенно к концу 3-го месяца заболевания). Наши данные показывают, что для того, чтобы предупредить неблагоприятный исход заболевания (смертельный исход или выраженную инвалидизацию) у 1 больного, нужно пролечить препаратом Кавинтон всего только 5 больных с острым ишемическим инсультом. Степень нарушения неврологических функций, определяемая по Американской шкале степени тяжести инсульта (NIH-NINDS), к концу 3-го месяца заболевания в группе больных, получающих лечение препаратом Кавинтон, была ниже, чем в контрольной группе больных (p = 0,05). Лечение препаратом Кавинтон сопровождалось снижением ОР неблагоприятного исхода к концу 3-го месяца инсульта на 30% (ОР = 0,7; 95% ДИ = 0,1-3,4) по модифицированной шкале индекса Бартела и на 60% по модифицированной шкале Рэнкина (ОР = 0,4; 95% ДИ = 0,1-1,7). Важно подчеркнуть, что лечение Кавинтоном хорошо переносилось больными и не сопровождалось никакими серьезными побочными эффектами, такими как значительное снижение систолического или диастолического артериального давления.
В нашем исследовании диагноз острого ишемического инсульта был подтвержден данными КТ головного мозга у всех больных до проведения процедуры рандомизации. Использование нами общепризнанных и валидных критериев для оценки этих исходов за достаточно длительный катамнестический период наблюдения (3 месяца) позволили минимизировать вероятность системной ошибки при оценке исходов заболевания. Проведенный нами статистический анализ данных на основе «intention-to-treat» принципа позволяет судить не только о действенности, но и об эффективности использования препарата Кавинтон в повседневной практике. Хотя клиническая интерпретация результатов любого исследования может быть затруднена при использовании усредненных показателей (например, средняя величина баллов) как конечных точек исходов заболевания [27] ограниченность размера нашего исследования 30 больными и связанная с этим меньшая вероятность обнаружения статистически достоверных различий между группами сравнения при использовании дискретных показателей эффективности лечения обосновывала целесообразность использования бальной оценки функциональных исходов инсульта по Американской шкале тяжести инсульта (NIH-NINDS). Однонаправленность и близость величины различий по всем использованным в данном исследовании шкалам инсульта (Американская шкала тяжести инсульта, индекс Бартела и шкала Рэнкина) между основной и контрольной группами больных делают более убедительными полученные выводы. Учитывая нейропротективный и вазоактивный механизм действия препарата Кавинтон и результаты настоящего исследования по его применению в среднем через 30 часов с начала заболевания, можно ожидать, что при его более раннем применении у больных острым ишемическим инсультом (например, в первые 6 часов заболевания) терапевтический эффект данного препарата будет еще более выражен. Использование препарата Реополиглюкин у всех рандомизированных больных было обосновано существующими в нашем городе требованиями к правилам ведения больных острым ишемическим инсультом. При этом нужно заметить, что частота использования не только данного препарата, но всех других сопутствующих средств и методов лечения в основной и контрольной группах больных существенно не отличалась. Отсутствие информированности больных о проводимом им лечении препаратом Кавинтон устраняло возможность системной ошибки, связанной с искаженной интерпретацией больными своего состояния. Возможность системной ошибки в оценке функциональных исходов инсульта была также минимизирована предшествующей специальной учебной подготовкой невропатологов, принимавших участие в исследовании. Кроме того, рентгенологи, оценивающие результаты КТ головного мозга, не были осведомлены о предполагаемом лечении, что исключало возможность системной ошибки в интерпретации КТ-данных.
Заключение
Данное исследование является первым российским рандомизированным клиническим исследованием по оценке эффективности применения препарата Кавинтон у больных с КТ-верифицированным диагнозом острого ишемического инсульта. Результаты исследования позволяют заключить, что лечение препаратом Кавинтон улучшает восстановление неврологических функций и уменьшает степень инвалидизации больных с острым ишемическим инсультом к концу 3-го месяца заболевания. Препарат хорошо переносится больными и не обладает побочными эффектами.
Список литературы Вы можете найти на сайте http://www.rmj.ru
Винпоцетин –
Кавинтон (торговое название)
(Gedeon Richter)
Литература
1. Tamaki N, Kusunoki T, Matsumoto S: The effect of vinpocetine on cerebral blood flow in patients with cerebrovascular disorders. Therapia Hungarica 1985;33:13-21.
2. Itoh T: Effect of vinpocetine on platelet aggregation in patients with cerebrovascular diseases. Jap Pharmacol Ther 1982;10:1481-1485.
3. Hayakawa M: Effect of vinpocetine on red blood cell deformability in stroke patients. Arzneim-Forsch/Drug Res 1992;42:425-427.
4. Erdo SL, Ning-Sheng C, Wolff JR, Kiss B: Vinpocetine protects against excitotoxic cell death in primary cultures of rat cerebral cortex. European Journal of Pharmacology 1990;187:551-553.
5. Kiss B, Ning-Sheng C, Erdo SL: Vinpocetine preferentially antagonizes quisqualate/AMPA receptor responses: evidence from release and ligand binding studies. European Journal of Pharmacology 1991;209:109-112.
6. Erdo SL: Vinpocetine is as potent as phenytoin to block voltage-gated Na channels in rat cortical neurons. European Journal of Pharmacology 1995;273:303-306.
7. Krieglstein J, Rischke R: Vinpocetine increases the neuroprotective effect of adenosine in vitro. European Journal of Pharmacology 1991;205:7-10.
8. Sauer D, Rischke R, Beck T, Rossberg C, Mennel HD, Bielenberg GW, Krieglstein J: Vinpocetine prevents ischemic cell damage in rat hippocampus. Life Sciences 1988;43:1733-1739.
9. Rischke R, Krieglstein J: Effects of vinpocetine on local cerebral blood flow and glucose utilization seven days after forebrain ischemia in the rat. Pharmacology 1990;41:153-160.
10. Backhauss C, Karkoutly C, Welsch M, Krieglstein J: A mouse model of focal cerebral ischemia for screening neuroprotective drug effects. Journal of Pharmacological & Toxicological Methods 1992;27:27-32.
11. Balestrini R, Fontana L, Astengo F: A double-blind placebo controlled evaluation of the safety and efficacy of vinpocetine in the treatment of patients with chronic vascular senile cerebral dysfunction. Journal of American Geriatric Society 1987;35:425-430.
12. Manconi E, Binaghi F, Pitzus F: A double blind clinical trial of vinpocetine in the treatment of cerebral insufficiency of vascular and degenerative origin. Current Therapeutic Research , Clinical & Experimental 1986;40:702-709.
13. Aboderin I, Venables G: Stroke management in Europe. Pan European Consensus Meeting on Stroke Management. Journal of Internal Medicine 1996;240:173-180.
14. Adams HPJ, Brott TG, Crowell RM, Furlan AJ, Gomez CR, Grotta J, Helgason CM, Marler JR, Woolson RF, Zivin JA: Guidelines for the management of patients with acute ischemic stroke. A statement for healthcare professionals from a special writing group of the Stroke Council, American Heart Association. Stroke 1994;25:1901-1914.
15. Werner J, Apececha M, Schaltenbrand R, Fenzl E: Clinical study to evaluate the efficacy and tolerance of vinpocetine i.v. added to standard therapy in patients suffering from an acute apoplectic insult. Bes A, et al.: 636-641. 1986. John Libbey Eurotext. Senile Dementias: Early Detection.
16. Bereczki D, Fekete I: Vinpocetine in acute ischaemic stroke (Cochrane Review). The Cochrane Library, Issue 2. 1998. Oxford, Update Software.
17. Teasdale G, Jennett B: Assessment of coma and impaired consciousness: a practical scale. Lancet 1974;2:81-84.
18. Goldstein LB, Bertels C, Davis JN: Interrater reliability of the NIH stroke scale. Archives of Neurology 1989;46:660-662.
19. Mahoney FI, Barthel DW: Functional evaluation: the Barthel Index. Md Med J 1965;14:61-65.
20. Rankin J: Cerebral vascular accidents in patients over the age of 60: II. Prognosis. Scottish Medical Journal 1957;2:200-213.
21. Altman DG. Practical statistics for medical research. 5 ed. London: Chapman & Hall; 1995:1-611.
22. AnonymousSPSS for Windows, Version 7.5.1. SPSS, Inc., 1996.
23. Dean A.G., Dean JA, Coulombier D, et al. Epi Info Version 6.0: a word processing, database, and statistics program for epidemiology on microcomputers. Centers for disease Control and Prevention, Atlanta, Georgia: USA and World Health Organization, Geneva, Switzerland, 1998.
24. Chamorro A, Vila N, Ascaso C, Saiz A, Montalvo J, Alonso P, Tolosa E: Early prediction of stroke severity. Role of the erythrocyte sedimentation rate. Stroke 1995;26:573-576.
25. Marks MP, Holmgren EB, Fox AJ, Patel S, von Kummer R, Froehlich J: Evaluation of early computed tomographic findings in acute ischemic stroke. Stroke 1999;30:389-392.
26. Tatemichi TK, Mohr JP, Rubinstein LV, Kase CS, Nichols FT, Price TR, Wolf PA: CT findings and clinical course in acute stroke: the NINCDS Pilot Stroke Data Bank. Stroke 1985;16:138-138.
27. Roberts L, Counsell C: Assessment of clinical outcomes in acute stroke trials. Stroke 1998;29:986-991.
| Приложения к статье |