–Т –Ї–ї–Є–љ–Є–Ї–µ –±–Њ–ї—М —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –Ї–∞–Ї –љ–µ–њ—А–Є—П—В–љ–Њ–µ —З—Г–≤—Б—В–≤–Њ, –њ—А–Є—З–Є–љ—П—О—Й–µ–µ –±–Њ–ї—М–љ–Њ–Љ—Г —Б—В—А–∞–і–∞–љ–Є–µ —А–∞–Ј–ї–Є—З–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є. –§–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М вАУ –≤–∞–ґ–љ–µ–є—И–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–∞ –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–Є–µ —Д–∞–Ї—В–Њ—А—Л, –Њ–љ–∞ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –ґ–Є–≤–Њ–≥–Њ –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ –Њ–Ї—А—Г–ґ–∞—О—Й–µ–є —Б—А–µ–і–µ. –І—Г–≤—Б—В–≤–Њ –±–Њ–ї–Є —П–≤–ї—П–µ—В—Б—П —Б–Є–≥–љ–∞–ї–Њ–Љ –Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є —А–∞–Ј—А—Г—И–µ–љ–Є—П, –≤—Л–Ј—Л–≤–∞–µ—В —Ж–µ–њ—М —А–µ—Д–ї–µ–Ї—В–Њ—А–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ —Г—Б—В—А–∞–љ–µ–љ–Є–µ –Њ–њ–∞—Б–љ–Њ—Б—В–Є. –С–Њ–ї—М –Љ–Њ–±–Є–ї–Є–Ј—Г–µ—В —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Њ–≤ –Є –Є—Е –Ј–∞—Й–Є—В–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –Њ–Ї–∞–Ј—Л–≤–∞—П —Б—В–Є–Љ—Г–ї–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В –љ–∞ –≥—Г–Љ–Њ—А–∞–ї—М–љ—Л–µ –Є –Ї–ї–µ—В–Њ—З–љ—Л–µ –Ј–≤–µ–љ—М—П –Є–Љ–Љ—Г–љ–Є—В–µ—В–∞, —Г—Б–Є–ї–Є–≤–∞—П –∞–љ—В–Є—В–µ–ї–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ, –Љ–Є–≥—А–∞—Ж–Є–Њ–љ–љ—Г—О —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –ї–µ–є–Ї–Њ—Ж–Є—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ –±–Њ–ї—М –Є–≥—А–∞–µ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О —А–Њ–ї—М —В–Њ–ї—М–Ї–Њ –і–Њ —В–Њ–≥–Њ –Љ–Њ–Љ–µ–љ—В–∞, –њ–Њ–Ї–∞ –Њ–љ–∞ –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞–µ—В –Њ –љ–∞—А—Г—И–µ–љ–Є–Є —Ж–µ–ї–Њ—Б—В–љ–Њ—Б—В–Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞.
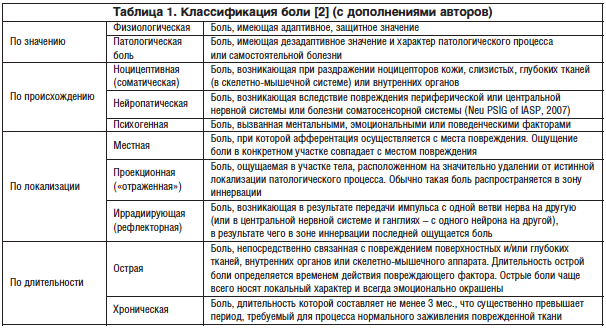
–Я–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М (—В–µ—А–Љ–Є–љ, –њ—А–µ–і–ї–Њ–ґ–µ–љ–љ—Л–є —А–Њ—Б—Б–Є–є—Б–Ї–Є–Љ —Г—З–µ–љ—Л–Љ-–њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Њ–Љ –У.–Э. –Ъ—А—Л–ґ–∞–љ–Њ–≤—Б–Ї–Є–Љ –≤ 1975 –≥.) —Г—В—А–∞—З–Є–≤–∞–µ—В –∞–і–∞–њ—В–Є–≤–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є —П–≤–ї—П–µ—В—Б—П –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ. –Я–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М —З–∞—Б—В–Њ –њ—А–Є–Њ–±—А–µ—В–∞–µ—В –Ј–љ–∞—З–µ–љ–Є–µ –њ–Њ–і–ї–Є–љ–љ–Њ–є –±–Њ–ї–µ–Ј–љ–Є. –Ю–љ–∞ –Љ–Њ–ґ–µ—В –≤–Њ–Ј–љ–Є–Ї–∞—В—М –њ—А–Є —А–∞–Ј–ї–Є—З–љ–Њ–є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –њ–∞—В–Њ–ї–Њ–≥–Є–Є —Б–∞–Љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ю—Б–љ–Њ–≤–Њ–є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є —П–≤–ї—П–µ—В—Б—П –і–Є—Б–±–∞–ї–∞–љ—Б –љ–Њ—Ж–Є- –Є –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ. –Т –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П —Б–Ї–Њ–њ–ї–µ–љ–Є—П –≥–Є–њ–µ—А–∞–Ї—В–Є–≤–љ—Л—Е –љ–µ–є—А–Њ–љ–Њ–≤, —П–≤–ї—П—О—Й–Є—Е—Б—П –≥–µ–љ–µ—А–∞—В–Њ—А–∞–Љ–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є —Г—Б–Є–ї–µ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–±—Г–ґ–і–µ–љ–Є—П [1]. –†–∞–Ј–ї–Є—З–∞—О—В —Б–ї–µ–і—Г—О—Й–Є–µ –≤–∞—А–Є–∞–љ—В—Л –±–Њ–ї–Є (—В–∞–±–ї. 1).
–Э–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–µ –±–Њ–ї–µ–≤—Л–µ —Б–Є–љ–і—А–Њ–Љ—Л –≤–Њ–Ј–љ–Є–Ї–∞—О—В –≤—Б–ї–µ–і—Б—В–≤–Є–µ –∞–Ї—В–Є–≤–∞—Ж–Є–Є –љ–Њ—Ж–Є—Ж–µ–њ—В–Њ—А–Њ–≤ –њ—А–Є —В—А–∞–≤–Љ–µ, –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є, –Є—И–µ–Љ–Є–Є, –Њ—В–µ–Ї–µ —В–Ї–∞–љ–µ–є. –Т–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–µ –њ—А–Є —Н—В–Њ–Љ –Є–Љ–њ—Г–ї—М—Б—Л, —Б–ї–µ–і—Г—П –њ–Њ –≤–Њ—Б—Е–Њ–і—П—Й–Є–Љ –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–Љ –њ—Г—В—П–Љ, –і–Њ—Б—В–Є–≥–∞—О—В –≤—Л—Б—И–Є—Е –Њ—В–і–µ–ї–Њ–≤ –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –Є –Њ—В–Њ–±—А–∞–ґ–∞—О—В—Б—П —Б–Њ–Ј–љ–∞–љ–Є–µ–Љ, –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ, —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –Њ—Й—Г—Й–µ–љ–Є–µ –±–Њ–ї–Є.
–Я–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ—Б–љ–Њ–≤–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П –љ–∞—А—Г—И–µ–љ–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –≥–µ–љ–µ—А–∞—Ж–Є–Є –Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–≥–Њ —Б–Є–≥–љ–∞–ї–∞ –≤ –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–љ–∞—Е –Є –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—П –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В–Є –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л—Е –љ–µ–є—А–Њ–љ–Њ–≤ –≤ —Б—В—А—Г–Ї—В—Г—А–∞—Е —Б–њ–Є–љ–љ–Њ–≥–Њ –Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Я–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –љ–µ—А–≤–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—В—А—Г–Ї—В—Г—А–љ–Њ-—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ –њ—А–µ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П–Љ –≤ –љ–µ—А–≤–љ–Њ–Љ –≤–Њ–ї–Њ–Ї–љ–µ, –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —З–µ–≥–Њ —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–∞—П —А–µ–∞–Ї—Ж–Є—П –љ–µ—А–≤–љ–Њ–≥–Њ –≤–Њ–ї–Њ–Ї–љ–∞ –љ–∞ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ; –њ–∞—В—В–µ—А–љ –њ–µ—А–µ–і–∞–≤–∞–µ–Љ–Њ–≥–Њ —Б–Є–≥–љ–∞–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Љ–µ–љ—П–µ—В—Б—П. –£—Б–Є–ї–µ–љ–љ–∞—П –Є–Љ–њ—Г–ї—М—Б–∞—Ж–Є—П —Б –њ–µ—А–Є—Д–µ—А–Є–Є –і–µ–Ј–Њ—А–≥–∞–љ–Є–Ј—Г–µ—В –Є —А–∞–±–Њ—В—Г —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А. –Т —Б–Њ–Ј–і–∞–≤—И–Є—Е—Б—П —Г—Б–ї–Њ–≤–Є—П—Е –њ—А–Њ–Є—Б—Е–Њ–і–Є—В —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞, –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ—П–≤–ї—П—О—Й–µ–≥–Њ—Б—П –≤ –≤–Є–і–µ —Б–љ–Є–ґ–µ–љ–Є—П –Є/–Є–ї–Є –њ–Њ—В–µ—А–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞–ї–ї–Њ–і–Є–љ–Є–µ–є, –≥–Є–њ–µ—А–∞–ї–≥–µ–Ј–Є–µ–є, –і–Є–Ј–µ—Б—В–µ–Ј–Є–µ–є, –≥–Є–њ–µ—А–њ–∞—В–Є–µ–є.
–Я—Б–Є—Е–Њ–≥–µ–љ–љ–∞—П –±–Њ–ї—М –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤–љ–µ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е, –≤–Є—Б—Ж–µ—А–∞–ї—М–љ—Л—Е –Є–ї–Є –љ–µ–є—А–Њ–љ–∞–ї—М–љ—Л—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–є –Є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є —Б–Њ—Ж–Є–∞–ї—М–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є.
–Т—Л–і–µ–ї—П—О—В —В–∞–Ї–ґ–µ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є —В–Є–њ –±–Њ–ї–Є, –≤–µ–і—Г—Й—Г—О —А–Њ–ї—М –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–Є –Ї–Њ—В–Њ—А–Њ–Љ –Є–Љ–µ—О—В —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л (–і–µ–Ј–Є–љ–≥–Є–±–Є—Ж–Є—П –Є —Ж–µ–љ—В—А–∞–ї—М–љ–∞—П —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є—П вАУ –њ–Њ–≤—Л—И–µ–љ–Є–µ –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В–Є –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л—Е –љ–µ–є—А–Њ–љ–Њ–≤ –Ј–∞–і–љ–Є—Е —А–Њ–≥–Њ–≤ —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞) –њ—А–Є –љ–∞–ї–Є—З–Є–Є –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–≥–Њ –Є–ї–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ [3].
–Т –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞—О—В—Б—П —Б–Њ—З–µ—В–∞–љ–љ—Л–µ —Д–Њ—А–Љ—Л –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–ґ–љ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –њ–Њ –≤—А–µ–Љ–µ–љ–љ—Л–Љ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–∞–Љ. –Ю—Б—В—А–∞—П –±–Њ–ї—М, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–є –∞—Д—Д–µ—А–µ–љ—В–∞—Ж–Є–µ–є –Є –≥–Њ—А–∞–Ј–і–Њ —А–µ–ґ–µ –Є–Љ–µ–µ—В –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї—Г—О –њ—А–Є—А–Њ–і—Г. –Я—А–Є—З–Є–љ–∞–Љ–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –Љ–Њ–≥—Г—В –±—Л—В—М –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–µ –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –Є–ї–Є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –•–С вАУ —Н—В–Њ –±–Њ–ї—М, –њ—А–Њ–і–Њ–ї–ґ–∞—О—Й–∞—П—Б—П —Б–≤–µ—А—Е –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –њ–µ—А–Є–Њ–і–∞ –Ј–∞–ґ–Є–≤–ї–µ–љ–Є—П –Є –і–ї—П—Й–∞—П—Б—П –≤ —В–µ—З–µ–љ–Є–µ 3 –Љ–µ—Б. –Є –±–Њ–ї–µ–µ.
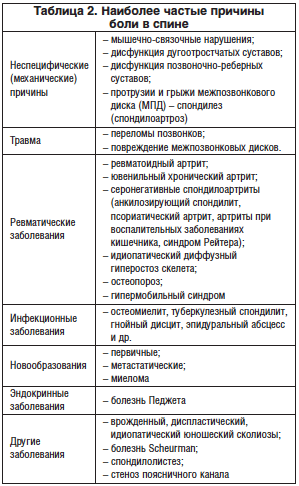
–Я—А–Є–Љ–µ—А–Њ–Љ —Б–Њ—З–µ—В–∞–љ–љ–Њ–є —Д–Њ—А–Љ—Л –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —П–≤–ї—П–µ—В—Б—П –±–Њ–ї—М –≤ —Б–њ–Є–љ–µ (–С–°). –Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —Б–њ–Є–љ–∞ вАУ –Љ–љ–Њ–≥–Њ–Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ–∞—П –∞–љ–∞—В–Њ–Љ–Є—З–µ—Б–Ї–∞—П —Б—В—А—Г–Ї—В—Г—А–∞ –Є –ї—О–±–Њ–є –µ–µ —Н–ї–µ–Љ–µ–љ—В –Љ–Њ–ґ–µ—В –≤—Л—Б—В—Г–њ–∞—В—М –Є—Б—В–Њ—З–љ–Є–Ї–Њ–Љ –±–Њ–ї–Є. –Ю—Б–љ–Њ–≤–љ—Л–µ –њ—А–Є—З–Є–љ—Л –С–° –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2.
–•–Њ—В—П –≤ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –≤ —Б–њ–Є–љ–µ –љ–Њ—Б–Є—В –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А –Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –Љ—Л—И–µ—З–љ–Њ-—Б–Ї–µ–ї–µ—В–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, —Б—Г—Й–µ—Б—В–≤—Г–µ—В —А—П–і –њ—А–Є—З–Є–љ (–і–Є—Б–Ї–Њ–≥–µ–љ–љ—Л–µ –±–Њ–ї–µ–≤—Л–µ —Б–Є–љ–і—А–Њ–Љ—Л, —Б–њ–Њ–љ–і–Є–ї–µ–Ј –Є –∞—А—В—А–Њ–Ј —Д–∞—Б–µ—В–Њ—З–љ—Л—Е —Б—Г—Б—В–∞–≤–Њ–≤, —В—А–∞–≤–Љ—Л –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ (–≤ —В. —З. –њ—А–Є –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј–µ), —Б—В–µ–љ–Њ–Ј –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –Є —В. –і.), –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞—О—Й–Є—Е –њ—А–Є—Б–Њ–µ–і–Є–љ–µ–љ–Є–µ –Є –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –±–Њ–ї–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Є–Ј—Г—З–∞–µ—В—Б—П —А–Њ–ї—М —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є —Б–µ–љ—Б–Є—В–Є–Ј–∞—Ж–Є–Є –≤ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є–Є –Є –њ–Њ–і–і–µ—А–ґ–∞–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –С–°. –†—П–і –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–∞–ї–Є—З–Є–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–≥–Њ, –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–ї–Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –≤–∞—А–Є–∞–љ—В–∞ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –С–°, —З—В–Њ –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ –Љ–Њ–ґ–µ—В –≤–ї–Є—П—В—М –љ–∞ –≤—Л–±–Њ—А –ї–µ—З–µ–±–љ–Њ–є —В–∞–Ї—В–Є–Ї–Є [4].
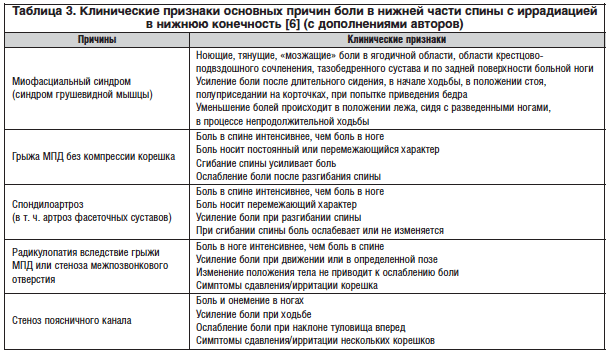
–°—А–µ–і–Є –≤—Б–µ—Е –њ—А–Є—З–Є–љ —А–∞–Ј–≤–Є—В–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –С–° –≤–µ–і—Г—Й–µ–µ –Љ–µ—Б—В–Њ –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–Љ—Г –њ–Њ—А–∞–ґ–µ–љ–Є—О –Ь–Я–Ф. –Я—А–Є –і–Њ—А—Б–∞–ї—М–љ–Њ–Љ –≤—Л–њ—П—З–Є–≤–∞–љ–Є–Є –Ь–Я–Ф –±–Њ–ї—М –≤–љ–∞—З–∞–ї–µ –њ–Њ—П–≤–ї—П–µ—В—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –±–Њ–ї–µ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –љ–∞—А—Г–ґ–љ—Л—Е —Б–ї–Њ–µ–≤ —Д–Є–±—А–Њ–Ј–љ–Њ–≥–Њ –Ї–Њ–ї—М—Ж–∞ –Є –Ј–∞–і–љ–µ–є –њ—А–Њ–і–Њ–ї—М–љ–Њ–є —Б–≤—П–Ј–Ї–Є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–µ–≥–Њ—Б—П —Б–њ–∞–Ј–Љ–Њ–Љ —Б–µ–≥–Љ–µ–љ—В–∞—А–љ—Л—Е –Љ—Л—И—Ж (—А–µ—Д–ї–µ–Ї—В–Њ—А–љ–∞—П –ї—О–Љ–±–Њ–Є—И–Є–∞–ї–≥–Є—П). –°–Љ–µ—Й–∞—П—Б—М –≤ —Б—В–Њ—А–Њ–љ—Г –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Ї–∞–љ–∞–ї–∞ –Є–ї–Є –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П, –≥—А—Л–ґ–∞ –Ь–Я–Ф –Љ–Њ–ґ–µ—В –Ї–Њ–Љ–њ—А–Є–Љ–Є—А–Њ–≤–∞—В—М —Б–њ–Є–љ–љ–Њ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –Ї–Њ—А–µ—И–Њ–Ї, —З—В–Њ –≤–µ–і–µ—В –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Ї–Њ—А–µ—И–Ї–Њ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (—А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є). –†–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П –Ї–∞–Ї –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–µ –≥—А—Л–ґ–µ–≤–Њ–≥–Њ –≤—Л–њ—П—З–Є–≤–∞–љ–Є—П –і–Є—Б–Ї–∞ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ 5вАУ7% —Б–ї—Г—З–∞–µ–≤ [5]. –Ф—А—Г–≥–Є–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є–Є –Љ–Њ–≥—Г—В –≤—Л—Б—В—Г–њ–∞—В—М –Њ—Б—В–µ–Њ—Д–Є—В, —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л–є –љ–∞ —Д–Њ–љ–µ —Б–њ–Њ–љ–і–Є–ї–µ–Ј–∞ (—Б–њ–Њ–љ–і–Є–ї–Њ–∞—А—В—А–Њ–Ј–∞), –≥–Є–њ–µ—А—В—А–Њ—Д–Є—П –ґ–µ–ї—В–Њ–є —Б–≤—П–Ј–Ї–Є –Є —Б—В–µ–љ–Њ–Ј –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤–Њ–≥–Њ –Њ—В–≤–µ—А—Б—В–Є—П. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Є—З–Є–љ –±–Њ–ї–Є –≤ –љ–Є–ґ–љ–µ–є —З–∞—Б—В–Є —Б–њ–Є–љ—Л —Б –Є—А—А–∞–і–Є–∞—Ж–Є–µ–є –≤ –љ–Є–ґ–љ—О—О –Ї–Њ–љ–µ—З–љ–Њ—Б—В—М –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 3.
–С–°, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ–∞—П —Б –≥—А—Л–ґ–µ–є –Ь–Я–Ф, –Ї–Њ–Љ–њ—А–Є–Љ–Є—А—Г—О—Й–µ–є –љ–µ—А–≤–љ—Л–є –Ї–Њ—А–µ—И–Њ–Ї, –љ–Њ—Б–Є—В —Б–Љ–µ—И–∞–љ–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, –Є–Љ–µ–µ—В –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–є –Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л. –Э–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ —Б–≤—П–Ј–∞–љ —Б —А–∞–Ј–і—А–∞–ґ–µ–љ–Є–µ–Љ –±–Њ–ї–µ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –≤ –љ–∞—А—Г–ґ–љ—Л—Е —Б–ї–Њ—П—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ–Њ–≥–Њ –і–Є—Б–Ї–∞ –Є –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е –µ–≥–Њ —В–Ї–∞–љ—П—Е, –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є вАУ —Б –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ –≤–Њ–ї–Њ–Ї–Њ–љ –Ї–Њ—А–µ—И–Ї–∞, –Є–љ—В–µ—А–љ–µ–≤—А–∞–ї—М–љ—Л–Љ –Њ—В–µ–Ї–Њ–Љ, –Є—И–µ–Љ–Є–µ–є –Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ–Љ, –њ—А–Є–≤–Њ–і—П—Й–Є–Љ–Є –љ–∞ –љ–∞—З–∞–ї—М–љ—Л—Е —Н—В–∞–њ–∞—Е –Ї —Д–Њ–Ї–∞–ї—М–љ–Њ–є –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є, –∞ –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ вАУ –Є –Ї –∞–Ї—Б–Њ–љ–∞–ї—М–љ–Њ–є –і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є. –Т—Л—Б–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ, —З—В–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –С–° –њ—А–Є–≤–Њ–і–Є—В –Ї —А–∞–љ–љ–Є–Љ —Б—В—А—Г–Ї—В—Г—А–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ. –Т —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –Є –і–ї–Є—В–µ–ї—М–љ–Њ–є –±–Њ–ї–µ–≤–Њ–є –Є–Љ–њ—Г–ї—М—Б–∞—Ж–Є–Є –≥–Є–±–љ—Г—В —Б–њ–Є–љ–∞–ї—М–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А–љ—Л–µ –≤—Б—В–∞–≤–Њ—З–љ—Л–µ –љ–µ–є—А–Њ–љ—Л, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л–µ –Ј–∞ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–є –∞—Д—Д–µ—А–µ–љ—В–∞—Ж–Є–Є. –Я–Њ—Н—В–Њ–Љ—Г —А–∞–љ–љ–µ–µ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –±–Њ–ї–Є –Є –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П –Љ–Њ–≥—Г—В –њ—А–µ–і—Г–њ—А–µ–ґ–і–∞—В—М —А–∞–Ј–≤–Є—В–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –С–° [7].
–Я–Њ–і—Е–Њ–і –Ї –ї–µ—З–µ–љ–Є—О –С–° —Д–Њ—А–Љ–Є—А—Г–µ—В—Б—П –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є –Њ–± —Н—В–Є–Њ–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞—Е –µ–µ —А–∞–Ј–≤–Є—В–Є—П, –∞ —В–∞–Ї–ґ–µ —Б —Г—З–µ—В–Њ–Љ –≤–∞—А–Є–∞–љ—В–∞ —В–µ—З–µ–љ–Є—П –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞.
–Я—А–Є –Њ—Б—В—А–Њ–Љ –±–Њ–ї–µ–≤–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ —Б–ї–µ–і—Г–µ—В –Њ–ґ–Є–і–∞—В—М —Г–Љ–µ–љ—М—И–µ–љ–Є—П –±–Њ–ї–Є –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і. –Т —А—П–і–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–Њ—Б—В–µ–ї—М–љ—Л–є —А–µ–ґ–Є–Љ –љ–µ —В–Њ–ї—М–Ї–Њ –љ–µ —Г—Б–Ї–Њ—А—П–µ—В –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ, –љ–Њ, –љ–∞–Њ–±–Њ—А–Њ—В, –Љ–Њ–ґ–µ—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞—В—М —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –Њ—Б—В—А–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –≤ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–є. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –±–Њ–ї–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –≤ –њ–Њ—Б—В–µ–ї—М–љ–Њ–Љ —А–µ–ґ–Є–Љ–µ –љ–µ—В, –∞ –њ—А–Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –±–Њ–ї–Є –µ–≥–Њ —Б–ї–µ–і—Г–µ—В –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ –Њ–≥—А–∞–љ–Є—З–Є—В—М (–і–Њ 1вАУ3 –і–љ–µ–є). –Ю–і–љ–∞–Ї–Њ —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –љ–µ –њ–Њ–Ї–∞–Ј–∞–љ—Л (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р).
–£—З–Є—В—Л–≤–∞—П, —З—В–Њ –њ—А–Є –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –≤ —Б—В—А—Г–Ї—В—Г—А–∞—Е –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є–µ, –≤ –њ—А–Њ–≥—А–∞–Љ–Љ—Г –ї–µ—З–µ–љ–Є—П –і–Њ–ї–ґ–љ—Л –≤–Ї–ї—О—З–∞—В—М—Б—П –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–Э–Я–Т–Я) –≤ –њ–µ—А–≤—Л–µ 24вАУ48 —З –Њ—В –љ–∞—З–∞–ї–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р). –Я–Њ–Ї–∞–Ј–∞–љ–Њ –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Э–Я–Т–Я –≤ —В–µ—З–µ–љ–Є–µ 2вАУ3 –і–љ–µ–є —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –њ–µ—А–µ—Е–Њ–і–Њ–Љ –љ–∞ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ (10вАУ14 –і–љ–µ–є). –Т–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ –Љ—Л—И–µ—З–љ—Л–є –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤, —Г—Б—В—А–∞–љ—П—О—Й–Є—Е –Љ—Л—И–µ—З–љ—Л–є —Б–њ–∞–Ј–Љ, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ—В–Њ—А—Л—Е —Б–Њ—Б—В–∞–≤–ї—П–µ—В –љ–µ –±–Њ–ї–µ–µ 2 –љ–µ–і. (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р). –Т–∞–ґ–љ–Њ–є —Б–Њ—Б—В–∞–≤–ї—П—О—Й–µ–є —П–≤–ї—П–µ—В—Б—П –ї–Њ–Ї–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Э–Я–Т–Я-—Б–Њ–і–µ—А–ґ–∞—Й–Є—Е –≥–µ–ї–µ–є –Є –Љ–∞–Ј–µ–є (–љ–µ–њ—А–µ—А—Л–≤–љ—Л–Љ –Ї—Г—А—Б–Њ–Љ вАУ –љ–µ –±–Њ–ї–µ–µ 2 –љ–µ–і.).
–Ь–∞–љ—Г–∞–ї—М–љ–∞—П —В–µ—А–∞–њ–Є—П –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–Љ—Г —Г–ї—Г—З—И–µ–љ–Є—О, –Њ–і–љ–∞–Ї–Њ –љ–µ —П–≤–ї—П–µ—В—Б—П –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–Њ–є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–Љ—Г –ї–µ—З–µ–љ–Є—О (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Т). –°—Д–Њ—А–Љ—Г–ї–Є—А–Њ–≤–∞–љ—Л –∞–±—Б–Њ–ї—О—В–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П –Ї –њ—А–Њ–≤–µ–і–µ–љ–Є—О –Љ–∞–љ—Г–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є: –Њ–њ—Г—Е–Њ–ї–Є –Є –Љ–µ—В–∞—Б—В–∞—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, —Б–њ–Њ–љ–і–Є–ї–Є—В, –Њ—Б—В–µ–Њ–њ–Њ—А–Њ–Ј. –Ю—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л–Љ–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є —П–≤–ї—П—О—В—Б—П –≥—А—Л–ґ–∞ –Ь–Я–Ф, –≥–Є–њ–µ—А–ї–Њ—А–і–Њ–Ј –њ–Њ—П—Б–љ–Є—З–љ–Њ–≥–Њ –Є —И–µ–є–љ–Њ–≥–Њ –Њ—В–і–µ–ї–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞, –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Ї–Є—Д–Њ–Ј–∞ –≤ –≥—А—Г–і–љ–Њ–Љ –Њ—В–і–µ–ї–µ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ (¬Ђ–њ–ї–Њ—Б–Ї–∞—П¬ї —Б–њ–Є–љ–∞), –≤—А–Њ–ґ–і–µ–љ–љ–∞—П –і–Є—Б–њ–ї–∞–Ј–Є—П –Ї–Њ—Б—В–љ–Њ-—Е—А—П—Й–µ–≤–Њ–є —З–∞—Б—В–Є –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ–Є–Ї–∞ –Є —Б–≤—П–Ј–Њ—З–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞. –Я—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є —Н—Д—Д–µ–Ї—В–∞ –Њ—В —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 6 –љ–µ–і. (—Б–Њ—Е—А–∞–љ–µ–љ–Є–µ —Б—В–Њ–є–Ї–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –Є/–Є–ї–Є –љ–∞—А–∞—Б—В–∞–љ–Є–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞) –њ–Њ–Ї–∞–Ј–∞–љ–∞ –Ї–Њ–љ—Б—Г–ї—М—В–∞—Ж–Є—П –љ–µ–є—А–Њ—Е–Є—А—Г—А–≥–∞.
–°—Е–µ–Љ—Г –ї–µ—З–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (–љ–∞—А—П–і—Г —Б –Э–Я–Т–Я –Є –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–∞–Љ–Є –њ—А–Є –Њ–±–Њ—Б—В—А–µ–љ–Є–Є) –і–Њ–њ–Њ–ї–љ—П—О—В –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р), —Б–ї–∞–±—Л—Е –Њ–њ–Є–Њ–Є–і–Њ–≤ (—В—А–∞–Љ–∞–і–Њ–ї) (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р), –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Ї–∞–њ—Б–∞–Є—Ж–Є–љ–∞ (–ї–Њ–Ї–∞–ї—М–љ–Њ вАУ 3 –љ–µ–і.) (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р). –Ш–Ј —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П –∞–Ї—В–Є–≤–љ–Њ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П —З—А–µ—Б–Ї–Њ–ґ–љ–∞—П —Н–ї–µ–Ї—В—А–Њ–љ–µ–є—А–Њ—Б—В–Є–Љ—Г–ї—П—Ж–Є—П (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Т) –Є –љ–µ–є—А–Њ—А–µ—Д–ї–µ–Ї—Б–Њ—В–µ—А–∞–њ–Є—П (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р). –Ю—Б–Њ–±–Њ–µ –Љ–µ—Б—В–Њ –Ј–∞–љ–Є–Љ–∞–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Њ–±—Г—З–∞—О—Й–Є—Е –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е –њ—А–Њ–≥—А–∞–Љ–Љ (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р) –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –њ—Б–Є—Е–Њ—Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –Ї–Њ—А—А–µ–Ї¬≠—Ж–Є–µ–є (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Р), –Ї–Њ–Љ–њ–ї–µ–Ї—Б —Б–њ–µ—Ж–Є–∞–ї—М–љ—Л—Е —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Г–њ—А–∞–ґ–љ–µ–љ–Є–є (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –Т). –•–Є—А—Г—А–≥–Є—З–µ—Б–Ї–∞—П –Ї–Њ—А—А–µ–Ї—Ж–Є—П –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –±–Њ–ї–µ–≤–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –љ–µ —А–∞–љ–µ–µ —З–µ–Љ —З–µ—А–µ–Ј 2 –≥–Њ–і–∞ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є (–Ј–∞ –Є—Б–Ї–ї—О—З–µ–љ–Є–µ–Љ —Б–ї—Г—З–∞–µ–≤ –њ–Њ—П–≤–ї–µ–љ–Є—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞) (—Г—А–Њ–≤–µ–љ—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ—Б—В–Є –°) [8].
–Ю—Б–љ–Њ–≤—Г –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є —А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П—Е —Б–Њ—Б—В–∞–≤–ї—П—О—В –≤–Є—В–∞–Љ–Є–љ—Л –≥—А—Г–њ–њ—Л –Т. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤–Є—В–∞–Љ–Є–љ—Л –≥—А—Г–њ–њ—Л –Т (—В–Є–∞–Љ–Є–љ (–Т1), –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ (–Т6), —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ (–Т12)) –Њ–±–ї–∞–і–∞—О—В –љ–µ–є—А–Њ—В—А–Њ–њ–љ—Л–Љ–Є —А–µ–≥–µ–љ–µ—А–∞—В–Њ—А–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є. –Т–Є—В–∞–Љ–Є–љ B1 —Г—З–∞—Б—В–≤—Г–µ—В –≤ –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –љ–µ—А–≤–љ—Л—Е –Є–Љ–њ—Г–ї—М—Б–Њ–≤, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –∞–Ї—Б–Њ–љ–∞–ї—М–љ—Л–є —В—А–∞–љ—Б–њ–Њ—А—В, –Њ–њ—А–µ–і–µ–ї—П–µ—В —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О –љ–µ—А–≤–љ–Њ–є —В–Ї–∞–љ–Є. –Я–Є—А–Є–і–Њ–Ї—Б–Є–љ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –±–µ–ї–Ї–Њ–≤–Њ–≥–Њ –Њ–±–Љ–µ–љ–∞, —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В –Ј–∞–њ–∞—Б—Л –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ –Љ–∞–≥–љ–Є—П, —Г—З–∞—Б—В–≤—Г—О—Й–µ–≥–Њ –≤ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–∞—Е –Є –љ–µ—А–≤–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є. –¶–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ (–Љ–µ—В–Є–ї–Ї–Њ–±–∞–ї–∞–Љ–Є–љ вАУ –∞–Ї—В–Є–≤–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є—В –≤–Є—В–∞–Љ–Є–љ–∞ –Т12) –њ—А–Є–љ–Є–Љ–∞–µ—В —Г—З–∞—Б—В–Є–µ –≤ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —Б—В—А—Г–Ї—В—Г—А—Л –Љ–Є–µ–ї–Є–љ–Њ–≤–Њ–є –Њ–±–Њ–ї–Њ—З–Ї–Є. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–є –Љ–Њ–і–µ–ї–Є –∞–Ї—А–Є–ї–∞–Љ–Є–і-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є —Г –ґ–Є–≤–Њ—В–љ—Л—Е –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ —Б–≤–µ—А—Е–≤—Л—Б–Њ–Ї–∞—П –і–Њ–Ј–∞ –Љ–µ—В–Є–ї–Ї–Њ–±–∞–ї–∞–Љ–Є–љ–∞ —Б—В–Є–Љ—Г–ї–Є—А—Г–µ—В —А–µ–≥–µ–љ–µ—А–∞—Ж–Є—О –љ–µ—А–≤–∞ –њ—Г—В–µ–Љ –њ–Њ–≤—Л—И–µ–љ–Є—П —В—А–∞–љ—Б–Ї—А–Є–њ—Ж–Є–Є –≥–µ–љ–∞ [9].
–Э–∞—А—П–і—Г —Б –Њ–њ–Є—Б–∞–љ–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є —В–Є–∞–Љ–Є–љ—Г, –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ—Г –Є —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ—Г —Б–≤–Њ–є—Б—В–≤–µ–љ–љ–Њ –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ–Є –Љ–Є—И–µ–љ—П–Љ–Є –≤—Л—Б—В—Г–њ–∞—О—В –±–Њ–ї–µ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л –Є –љ–∞—В—А–Є–µ–≤—Л–µ –Ї–∞–љ–∞–ї—Л –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ. –£—З–Є—В—Л–≤–∞—П –љ–∞–ї–Є—З–Є–µ –∞—Б–µ–њ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П –њ—А–Є –С–°, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –≤ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –Э–Я–Т–Я –Љ–Њ–ґ–љ–Њ —Б—З–Є—В–∞—В—М –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ. –Р–љ–∞–ї—М–≥–µ—В–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤–Є—В–∞–Љ–Є–љ–∞ –Т6 –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–Њ –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ –Њ–±–Љ–µ–љ –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ–Њ–≤ [10]. –Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –і–Њ–Ї–∞–Ј–∞–љ–Њ –њ–Њ–і–∞–≤–ї–µ–љ–Є–µ –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –љ–µ–є—А–Њ–љ–Њ–≤ –Ј–∞–і–љ–µ–≥–Њ —А–Њ–≥–∞ —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –љ–µ–є—А–Њ–љ–Њ–≤ –≤ —В–∞–ї–∞–Љ—Г—Б–µ –≤–Є—В–∞–Љ–Є–љ–∞–Љ–Є –≥—А—Г–њ–њ—Л –Т. –Э–∞ —Б–∞–Љ—Ж–∞—Е –Ї—А—Л—Б –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ —Б–Љ–µ—Б–Є –≤–Є—В–∞–Љ–Є–љ–Њ–≤ вАУ –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞, —В–Є–∞–Љ–Є–љ–∞ –Є —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ–∞ вАУ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –±–Њ–ї–Є, –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –љ–∞–≥—А–µ–≤–Њ–Љ, —Б–і–∞–≤–ї–µ–љ–Є–µ–Љ –Є —Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –∞–≥–µ–љ—В–∞–Љ–Є. –Ґ–Є–∞–Љ–Є–љ –њ—А–Њ—П–≤–ї—П–ї –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є –∞–і—К—О–≤–∞–љ—В-–Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –∞—А—В—А–Є—В–µ, —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ вАУ –њ—А–Є –≤–Њ—Б–њ–∞–ї–µ–љ–Є–Є, –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ –Ї–∞—А—А–∞–≥–µ–љ–Є–љ–∞; –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ –і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –∞–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤ –Љ–Њ–і–µ–ї—П—Е —В–µ–њ–ї–Њ–≤–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –Є –њ–Њ–і–∞–≤–ї—П–ї –љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –љ–µ–є—А–Њ–љ–Њ–≤ —В–∞–ї–∞–Љ—Г—Б–∞ [11].
–Э–∞–Є–±–Њ–ї–µ–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т, —В. –Ї. –њ—А–Є —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–Љ –Є—Е –≤–≤–µ–і–µ–љ–Є–Є –≤–Њ–Ј–љ–Є–Ї–∞–µ—В —Н—Д—Д–µ–Ї—В —Б–Є–љ–µ—А–≥–Є–Ј–Љ–∞, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—Й–Є–є —Г—Б–Є–ї–µ–љ–Є–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —В–Є–∞–Љ–Є–љ–∞, –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞ –Є —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ–∞. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Њ–њ—Л—В –і–µ–Љ–Њ–љ—Б—В—А–Є—А—Г–µ—В –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—П—Е, –љ–µ–≤—А–∞–ї–≥–Є—П—Е, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –С–°, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є –Ї–∞–Ї –Љ—Л—И–µ—З–љ–Њ-—Б–≤—П–Ј–Њ—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–µ–є, —В–∞–Ї –Є –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ. R. Marcolongo –Є A. Fioravante –љ–∞–±–ї—О–і–∞–ї–Є –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–Є –Є –њ–Њ–≤—Л—И–µ–љ–Є–µ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –ї—О–Љ–±–Њ–Є—И–Є–∞–ї–≥–Є–µ–є, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т [12]. –Я–Њ –і–∞–љ–љ—Л–Љ Destito et al. (1987), —З–µ—А–µ–Ј 10 –і–љ–µ–є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –±–Њ–ї–Є –Є —Г–ї—Г—З—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Б—В—А–∞–і–∞—О—Й–Є—Е –С–°, –њ—А–Є—З–µ–Љ –њ–µ—А–≤—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є —Г–ї—Г—З—И–µ–љ–Є—П –љ–∞–±–ї—О–і–∞–ї–Є—Б—М —Г–ґ–µ —З–µ—А–µ–Ј 3 –і–љ—П –Њ—В –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П [13].
–Т –Ї–∞—З–µ—Б—В–≤–µ –њ—А–Є–Љ–µ—А–∞ –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –љ–µ–є—А–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Љ–Њ–ґ–љ–Њ –њ—А–Є–≤–µ—Б—В–Є –Э–µ–є—А–Њ–±–Є–Њ–љ, –Ї–Њ—В–Њ—А—Л–є —Б–Њ–і–µ—А–ґ–Є—В —Б–±–∞–ї–∞–љ—Б–Є—А–Њ–≤–∞–љ–љ—Г—О –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—О –љ–µ–є—А–Њ—В—А–Њ–њ–љ—Л—Е –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≤ –∞–і–µ–Ї–≤–∞—В–љ–Њ –≤—Л—Б–Њ–Ї–Є—Е –ї–µ—З–µ–±–љ—Л—Е –і–Њ–Ј–∞—Е. –Я–∞—А–µ–љ—В–µ—А–∞–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞, –≤ –Ї–Њ—В–Њ—А—Л–є –≤—Е–Њ–і—П—В —В–Є–∞–Љ–Є–љ, –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ –Є —Ж–Є–∞–љ–Њ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –Ї—Г–њ–Є—А—Г–µ—В –±–Њ–ї–µ–≤—Л–µ –Њ—Й—Г—Й–µ–љ–Є—П, –љ–Њ—А–Љ–∞–ї–Є–Ј—Г–µ—В —А–µ—Д–ї–µ–Ї—В–Њ—А–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В –љ–∞—А—Г—И–µ–љ–љ—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М. –Т —Б–ї—Г—З–∞—П—Е –≤—Л—А–∞–ґ–µ–љ–љ–Њ–≥–Њ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –ї–µ—З–µ–љ–Є–µ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –љ–∞—З–Є–љ–∞—В—М —Б –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П (–≥–ї—Г–±–Њ–Ї–Є–µ –Є–љ—К–µ–Ї—Ж–Є–Є –≤ —П–≥–Њ–і–Є—З–љ—Г—О –Љ—Л—И—Ж—Г) –њ–Њ 3 –Љ–ї (1 –∞–Љ–њ—Г–ї–∞) 1 —А./—Б—Г—В –µ–ґ–µ–і–љ–µ–≤–љ–Њ. –Я–Њ—Б–ї–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Є–ї–Є –≤ —Б–ї—Г—З–∞–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ —Г–Љ–µ—А–µ–љ–љ–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і—П—В –њ–Њ 3 –Љ–ї 2вАУ3 —А–∞–Ј–∞ –≤ –љ–µ–і–µ–ї—О –≤ —В–µ—З–µ–љ–Є–µ 2вАУ3 –љ–µ–і. –Т –Ї–∞—З–µ—Б—В–≤–µ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –Є –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–µ—Ж–Є–і–Є–≤–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ—А–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –Э–µ–є—А–Њ–±–Є–Њ–љ –≤ —Д–Њ—А–Љ–µ —В–∞–±–ї–µ—В–Њ–Ї.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –±–Њ–ї—М, —П–≤–ї—П—П—Б—М —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞, –њ—А–Є–Њ–±—А–µ—В–∞–µ—В —А–∞–Ј–ї–Є—З–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л –Є –≤–∞—А–Є–∞–љ—В—Л —В–µ—З–µ–љ–Є—П, —В—А–µ–±—Г—О—Й–Є–µ –Љ–љ–Њ–≥–Њ–Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–љ–Њ–≥–Њ –Є –њ–Њ—Н—В–∞–њ–љ–Њ–≥–Њ –њ–Њ–і—Е–Њ–і–∞ –Ї –ї–µ—З–µ–љ–Є—О.
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –®–Њ—Б—В–∞–Ї –Э.–Р. –Р–ї–≥–Њ–ї–Њ–≥–Є—П –Ї–∞–Ї –Љ–µ–ґ–і–Є—Б—Ж–Є–њ–ї–Є–љ–∞—А–љ–∞—П –њ—А–Њ–±–ї–µ–Љ–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Љ–µ–і–Є—Ж–Є–љ—Л // –Ъ–ї–Є–љ–Є—Ж–Є—Б—В. 2008. вДЦ 1. –°. 4вАУ9.
2. Allan I. Basbaum, Bushnell M.C. // Science of Pain. 2008. 1120 —А.
3. Woolf C.J. Pain: moving from symptom control toward mechanism specific pharmacologic management // Ann. Intern. Med. 2004. Vol. 140. P. 441вАУ451.
4. Nijs J., Apeldoorn A., Hallegraeff H., Clark J. et al. Low back pain: guidelines for the clinical classification of predominant neuropathic, nociceptive, or central sensitization pain // Pain Physician. 2015. Vol.18(3). P.E333вАУ346.
5. Waddell G. The back pain revolution. London: Churchill Livingstone, 2004. 475 p.
6. –Ы–µ–≤–Є–љ –Ю.–°. –°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Є –ї–µ—З–µ–љ–Є—О –±–Њ–ї–µ–є –≤ —Б–њ–Є–љ–µ. –Ь., 2006. 62 —Б.
7. –Т–µ—А—И–Є–љ–Є–љ–∞ –°.–Т. –†–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П –Ї–∞–Ї —Д–∞–Ї—В–Њ—А —Е—А–Њ–љ–Є–Ј–∞—Ж–Є–Є –±–Њ–ї–Є –≤ —Б–њ–Є–љ–µ // –Ь–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –≤–µ—Б—В–љ–Є–Ї. –®–Ї–Њ–ї–∞ –Ї–ї–Є–љ–Є—Ж–Є—Б—В–∞. 2009. вДЦ 31 (500). –°. 11.
8. –†–µ–≤–Љ–∞—В–Њ–ї–Њ–≥–Є—П: —Г—З–µ–±–љ–Њ–µ –њ–Њ—Б–Њ–±–Є–µ / –Я–Њ–і —А–µ–і. –Э.–Р. –®–Њ—Б—В–∞–Ї. –Ь.: –У–≠–Ю–Ґ–Р–†-–Ь–µ–і–Є–∞, 2012. 448 —Б.
9. Kathleen A. Head. –Я–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П: –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Є –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–µ –≤–Є–і—Л —В–µ—А–∞–њ–Є–Є.
10. Abbas Z.G., Swai A.B. Evaluation of the efficacy of thiamine and pyridoxine in the treatment of symptomatic diabetic peripheral neuropathy // East. Afr. Med. J. 1997. Vol. 74, вДЦ 12. –†. 803вАУ808.
11. Bartoszyk G.D., Wild A. –Р–љ—В–Є–љ–Њ—Ж–Є—Ж–µ–њ—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞, —В–Є–∞–Љ–Є–љ–∞ –Є —Ж–Є–∞–љ–Ї–Њ–±–∞–ї–∞–Љ–Є–љ–∞ —Г –Ї—А—Л—Б.
12. Marcolongo R., Fioravanti A. Vitamins B1, B6 and B12 for lumboischialgia. Bvitamins in Pain: Associated Symposium to the 5th World Congress on Pain, Hamburg, Germany, August 2, 1987. eds HU Gerbershagen, M. Zimmermann.
13. Destito D., Canonico N., Tentori-Monalto T. Analgesic activitiy of vitamins B1, B6 and B12 in the painful vertebral syndrome. Associated Symposium to the 5th World Congress on Pain, Hamburg, Germany, August 2, 1987. eds HU Gerbershagen, M. Zimmermann.












