–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–Є–µ –Ф–≠ —Г—Б–ї–Њ–≤–љ–Њ —Б–≤–Њ–і–Є—В—Б—П –Ї —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ––≤–Њ–ї–µ–≤–Њ–Љ—Г, –Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Њ–Љ—Г, –њ–Є—А–∞–Љ–Є–і–љ–Њ–Љ—Г, —Б—В–≤–Њ–ї–Њ–≤–Њ––Љ–Њ–Ј–ґ–µ—З–Ї–Њ–≤–Њ–Љ—Г, –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ—Г –Є –і—А—Г–≥–Є–Љ —Б–Є–љ–і—А–Њ–Љ–∞–Љ [–®–Љ–Є–і—В –Х.–Т., 1985, –С—Г—А—Ж–µ–≤ –Х.–Ь. 1998, –ѓ—Е–љ–Њ –Э.–Э., 2000].
–Т–µ–і—Г—Й—Г—О —А–Њ–ї—М –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –Ф–≠ –Є–≥—А–∞–µ—В —А–∞–Ј–Њ–±—Й–µ–љ–Є–µ –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є –Є –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤—Л—Е –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –≤—В–Њ—А–Є—З–љ–Њ–є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –°–Њ–≥–ї–∞—Б–љ–Њ —В–µ–Њ—А–Є–Є –Р.–†. –Ы—Г—А–Є—П, –ї–Њ–±–љ—Л–µ –і–Њ–ї–Є –Њ—В–≤–µ—З–∞—О—В –Ј–∞ —А–µ–≥—Г–ї—П—Ж–Є—О –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є: —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Љ–Њ—В–Є–≤–∞—Ж–Є–Є, –≤—Л–±–Њ—А —Ж–µ–ї–Є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, –њ–Њ—Б—В—А–Њ–µ–љ–Є–µ –њ—А–Њ–≥—А–∞–Љ–Љ—Л –Є –Ї–Њ–љ—В—А–Њ–ї—М –Ј–∞ –µ–µ –і–Њ—Б—В–Є–ґ–µ–љ–Є–µ–Љ [5]. –Я—А–Є —Н—В–Њ–Љ –і–Њ—А–Ј–Њ–ї–∞—В–µ—А–∞–ї—М–љ–∞—П –ї–Њ–±–љ–∞—П –і–Њ–ї—П –Ї–Њ—А—Л –Є –µ–µ —Б–≤—П–Ј–Є —Б–Њ —Б—В—А–Є–∞—А–љ—Л–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–Њ–Љ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—О—В –њ–µ—А–µ–Ї–ї—О—З–∞–µ–Љ–Њ—Б—В—М –≤–љ–Є–Љ–∞–љ–Є—П, —З—В–Њ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–ї—П —Б–Љ–µ–љ—Л –∞–ї–≥–Њ—А–Є—В–Љ–∞ –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є. –Ю—А–±–Є—В–Њ—Д—А–Њ–љ—В–∞–ї—М–љ—Л–µ –Њ—В–і–µ–ї—Л —Г—З–∞—Б—В–≤—Г—О—В –≤ –њ–Њ–і–∞–≤–ї–µ–љ–Є–Є –љ–µ—А–µ–ї–µ–≤–∞–љ—В–љ—Л—Е —Ж–µ–ї–Є –њ–Њ–±—Г–ґ–і–µ–љ–Є–є, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—П —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –≤–љ–Є–Љ–∞–љ–Є—П –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ—Б—В—М –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ—А–±–Є—В–Њ—Д—А–Њ–љ—В–∞–ї—М–љ–∞—П –ї–Њ–±–љ–∞—П –Ї–Њ—А–∞ –љ–∞—Е–Њ–і–Є—В—Б—П –≤ —В–µ—Б–љ–Њ–є –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є —Б –≥–Є–њ–њ–Њ–Ї–∞–Љ–њ–Њ–Љ, –Њ–±–µ—Б–њ–µ—З–Є–≤–∞—П —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –≤–љ–Є–Љ–∞–љ–Є—П –≤ –Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є [7,9].
–Я–Њ—Н—В–Њ–Љ—Г –ї–µ—З–µ–љ–Є–µ –Ф–≠ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –љ–∞ –Њ—Б–љ–Њ–≤–љ–Њ–µ —Б–Њ—Б—Г–і–Є—Б—В–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ (—Н—В–Є–Њ—В—А–Њ–њ–љ–∞—П —В–µ—А–∞–њ–Є—П), –Њ—Б–љ–Њ–≤–љ—Л–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї—Г, –Ї–Њ—В–Њ—А–∞—П –њ—А–Є–≤–Њ–і–Є—В –Ї —Г—Е—Г–і—И–µ–љ–Є—О –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –Є—Е –±–ї–Є–ґ–∞–є—И–Є—Е —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤.
–° –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –Њ–њ—А–∞–≤–і–∞–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Г–ї—Г—З—И–∞—О—Й–Є—Е —Ж–µ—А–µ–±—А–∞–ї—М–љ—Г—О –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О, –љ–Њ –љ–µ –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е —Н—Д—Д–µ–Ї—В «–Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—П». –° —Н—В–Њ–є —Ж–µ–ї—М—О –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —И–Є—А–Њ–Ї–Њ –њ—А–Є–Љ–µ–љ—П—О—В—Б—П —В–∞–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –≥—А—Г–њ–њ, –Ї–∞–Ї –Є–љ–≥–Є–±–Є—В–Њ—А—Л —Д–Њ—Б—Д–Њ–і–Є—Н—Б—В–µ—А–∞–Ј—Л (—Н–Ї—Б—В—А–∞–Ї—В –≥–Є–љ–Ї–≥–Њ –±–Є–ї–Њ–±–∞, –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ), –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤ (—Ж–Є–љ–љ–∞—А–Є–Ј–Є–љ, –љ–Є–Љ–Њ–і–Є–њ–Є–љ), –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є—Е α––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–љ–Є—Ж–µ—А–≥–Њ–ї–Є–љ, –њ–Є—А–Є–±–µ–і–Є–ї). –Ф–ї—П –Њ–±–µ—Б–њ–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є –Ј–∞—Й–Є—В—Л –љ–µ–є—А–Њ–љ–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –њ—А–µ–њ–∞—А–∞—В—Л, –њ–Њ–≤—Л—И–∞—О—Й–Є–µ –≤—Л–ґ–Є–≤–∞–µ–Љ–Њ—Б—В—М –љ–µ–є—А–Њ–љ–Њ–≤ –≤ —Г—Б–ї–Њ–≤–Є—П—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–Њ–Ї—Б–Є–Є.
–Э–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ –Є —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, —Г–ї—Г—З—И–∞—О—Й–Є–Љ –њ–∞–Љ—П—В—М, –≤–љ–Є–Љ–∞–љ–Є–µ, —Г–Љ—Б—В–≤–µ–љ–љ—Г—О –і–µ—П—В–µ–ї—М–љ–Њ—Б—В—М, –∞ —В–∞–Ї–ґ–µ –њ–Њ–≤—Л—И–∞—О—Й–Є–Љ —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Љ–Њ–Ј–≥–∞ –Ї –≥–Є–њ–Њ–Ї—Б–Є–Є, —П–≤–ї—П–µ—В—Б—П –њ–Є—А–∞—Ж–µ—В–∞–Љ, –Ї–Њ—В–Њ—А—Л–є —Г–ґ–µ —Е–Њ—А–Њ—И–Њ –Є–Ј–≤–µ—Б—В–µ–љ —И–Є—А–Њ–Ї–Њ–Љ—Г –Ї—А—Г–≥—Г –Ї–ї–Є–љ–Є—Ж–Є—Б—В–Њ–≤. –Ю–і–љ–∞–Ї–Њ –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –Є–љ—В–µ—А–µ—Б –Ї –њ–Є—А–∞—Ж–µ—В–∞–Љ—Г –≤—Л—А–Њ—Б –±–ї–∞–≥–Њ–і–∞—А—П –њ–Њ—П–≤–ї–µ–љ–Є—О –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–∞–њ—А–Є–Љ–µ—А –Ю–Љ–∞—А–Њ–љ—Г, –Њ–і–љ–∞ —В–∞–±–ї–µ—В–Ї–∞ –Ї–Њ—В–Њ—А–Њ–≥–Њ —Б–Њ–і–µ—А–ґ–Є—В –њ–Є—А–∞—Ж–µ—В–∞–Љ (0,4 –≥) –Є —Ж–Є–љ–љ–∞—А–Є–Ј–Є–љ (0,025 –≥). –Ф–∞–љ–љ–∞—П –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Ї —Б–≤–Њ–є—Б—В–≤–∞–Љ «–Є–і–µ–∞–ї—М–љ–Њ–≥–Њ» –љ–Њ–Њ—В—А–Њ–њ–∞ –і–Њ–±–∞–≤–Є—В—М —Б–≤–Њ–є—Б—В–≤–∞ —Ж–Є–љ–љ–∞—А–Є–Ј–Є–љ–∞, –Њ–±–ї–∞–і–∞—О—Й–µ–≥–Њ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ —Б–Њ—Б—Г–і—Л –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞.
–Ю–Љ–∞—А–Њ–љ – –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–µ —Б—А–µ–і—Б—В–≤–Њ —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –∞–љ—В–Є–≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ, –љ–Њ–Њ—В—А–Њ–њ–љ—Л–Љ –Є —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ [6].
–Я–Є—А–∞—Ж–µ—В–∞–Љ —Г–Љ–µ–љ—М—И–∞–µ—В –њ–Њ—В—А–µ–±–љ–Њ—Б—В—М —В–Ї–∞–љ–µ–є –≤ –Ї–Є—Б–ї–Њ—А–Њ–і–µ –Є –њ–Њ–≤—Л—И–∞–µ—В —Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ —Г—Б–ї–Њ–≤–Є—П—Е –≥–Є–њ–Њ–Ї—Б–Є–Є, —З—В–Њ –і–µ–ї–∞–µ—В –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ I –Є II —Б—В–∞–і–Є–є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –Њ–±–Њ—Б–љ–Њ–≤–∞–љ–љ—Л–Љ.
–¶–Є–љ–љ–∞—А–Є–Ј–Є–љ – —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –±–ї–Њ–Ї–∞—В–Њ—А –Љ–µ–і–ї–µ–љ–љ—Л—Е –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е –Ї–∞–љ–∞–ї–Њ–≤, –Є–љ–≥–Є–±–Є—А—Г–µ—В –њ–Њ—Б—В—Г–њ–ї–µ–љ–Є–µ –≤ –Ї–ї–µ—В–Ї–Є –Є–Њ–љ–Њ–≤ –Ї–∞–ї—М—Ж–Є—П –Є —Г–Љ–µ–љ—М—И–∞–µ—В –Є—Е —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –≤ –і–µ–њ–Њ –њ–ї–∞–Ј–Љ–Њ–ї–µ–Љ–Љ—Л, —Б–љ–Є–ґ–∞–µ—В —В–Њ–љ—Г—Б –≥–ї–∞–і–Ї–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –∞—А—В–µ—А–Є–Њ–ї, —Г–Љ–µ–љ—М—И–∞–µ—В –Є—Е —А–µ–∞–Ї—Ж–Є—О –љ–∞ –±–Є–Њ–≥–µ–љ–љ—Л–µ —Б–Њ—Б—Г–і–Њ—Б—Г–ґ–Є–≤–∞—О—Й–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ (—Н–њ–Є–љ–µ—Д—А–Є–љ, –љ–Њ—А—Н–њ–Є–љ–µ—Д—А–Є–љ, –і–Њ—Д–∞–Љ–Є–љ, –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ, –≤–∞–Ј–Њ–њ—А–µ—Б—Б–Є–љ). –Ю–±–ї–∞–і–∞–µ—В —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ (–Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Б–Њ—Б—Г–і–Њ–≤ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —Г—Б–Є–ї–Є–≤–∞—П –∞–љ—В–Є–≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ–Є—А–∞—Ж–µ—В–∞–Љ–∞), –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ. –Я—А–Њ—П–≤–ї—П–µ—В —Г–Љ–µ—А–µ–љ–љ—Г—О –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М, —Г–Љ–µ–љ—М—И–∞–µ—В –≤–Њ–Ј–±—Г–і–Є–Љ–Њ—Б—В—М –≤–µ—Б—В–Є–±—Г–ї—П—А–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞, –њ–Њ–љ–Є–ґ–∞–µ—В —В–Њ–љ—Г—Б —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я–Њ–≤—Л—И–∞–µ—В —Н–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М –Љ–µ–Љ–±—А–∞–љ —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤, –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї –і–µ—Д–Њ—А–Љ–∞—Ж–Є–Є, —Б–љ–Є–ґ–∞–µ—В –≤—П–Ј–Ї–Њ—Б—В—М –Ї—А–Њ–≤–Є.
–Ю–±–∞ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞ –Ю–Љ–∞—А–Њ–љ–∞ —Г—Б–Є–ї–Є–≤–∞—О—В –і–µ–є—Б—В–≤–Є–µ –і—А—Г–≥ –і—А—Г–≥–∞, –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Г–Љ–µ–љ—М—И–∞—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤.
–Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Ю–Љ–∞—А–Њ–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠. –¶–µ–ї—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П – –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ю–Љ–∞—А–Њ–љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠.
–Ь–∞—В–µ—А–Є–∞–ї—Л –Є –Љ–µ—В–Њ–і—Л
–Т –Њ—В–Ї—А—Л—В–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –≤–Ї–ї—О—З–µ–љ–Њ 203 –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В 40 –і–Њ 75 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 61,7 –≥–Њ–і–∞) –Њ–±–Њ–Є—Е –њ–Њ–ї–Њ–≤ —Б –і–Њ–Ї—Г–Љ–µ–љ—В–Є—А–Њ–≤–∞–љ–љ—Л–Љ –і–Є–∞–≥–љ–Њ–Ј–Њ–Љ «–Ф–≠ II —Б—В–∞–і–Є–Є». –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ–Њ–і–њ–Є—Б—Л–≤–∞–ї–Є –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М—О –љ–∞—Е–Њ–і–Є—В—М—Б—П –њ–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ 45 –і–љ–µ–є. –Ф–Є–∞–≥–љ–Њ–Ј –Ф–≠, —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–ї—Б—П –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є [4] –Є –њ—А–Њ—П–≤–ї—П–ї—Б—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –Њ–±—Л—З–љ–Њ –і–Њ—Б—В–Є–≥–∞—О—Й–Є–Љ–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є.
–°–Є–љ–і—А–Њ–Љ–∞–ї—М–љ–∞—П –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є Touchon J., Petersen R. 2004 [8]: –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ–Њ —Б–ї–Њ–≤–∞–Љ –њ–∞—Ж–Є–µ–љ—В–∞ –Є–ї–Є —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤; –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є; —Г—Е—Г–і—И–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–µ–є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –љ–µ–і–∞–≤–љ–Є–Љ –њ—А–Њ—И–ї—Л–Љ; –Њ—В—Б—Г—В—Б—В–≤–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є; –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–µ–Љ–µ–љ—Ж–Є–Є.
–Ъ—А–Є—В–µ—А–Є–Є –Є—Б–Ї–ї—О—З–µ–љ–Є—П –Є–Ј –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П: –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ, –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –≤—Л–њ–Њ–ї–љ–Є—В—М –њ—А–µ–і–ї–∞–≥–∞–µ–Љ—Л–µ —В–µ—Б—В—Л, —Г—А–Њ–≤–µ–љ—М –і–µ–њ—А–µ—Б—Б–Є–Є –±–Њ–ї—М—И–µ 17 –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ –С–µ–Ї–∞, –≤–Њ–Ј—А–∞—Б—В —Б—В–∞—А—И–µ 75 –ї–µ—В.
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л, –≤–Ї–ї—О—З–µ–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –Љ–µ—В–Њ–і–Њ–Љ –њ—А–Њ—Б—В–Њ–є —А–∞–љ–і–Њ–Љ–Є–Ј–∞—Ж–Є–Є –±—Л–ї–Є —А–∞–Ј–±–Є—В—Л –љ–∞ –Њ—Б–љ–Њ–≤–љ—Г—О –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Л. –Ь–µ–ґ–і—Г –≥—А—Г–њ–њ–∞–Љ–Є –љ–µ –±—Л–ї–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –њ–Њ –њ–Њ–ї—Г, –≤–Њ–Ј—А–∞—Б—В—Г –Є –љ–∞–ї–Є—З–Є—О —Д–Њ–љ–Њ–≤–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є. –Я–∞—Ж–Є–µ–љ—В—Л –Њ–±–µ–Є—Е –≥—А—Г–њ–њ –њ–Њ–ї—Г—З–∞–ї–Є —Б–Њ–Љ–∞—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–µ, –≤–∞–Ј–Њ–і–Є–ї–∞—В–∞—В–Њ—А—Л –Є —В.–і.), –Ї–Њ—В–Њ—А—Л–µ –љ–µ –Є–Љ–µ–ї–Є –љ–Њ–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –Є —Б–µ–і–∞—В–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Є –љ–µ –Њ–±–ї–∞–і–∞–ї–Є –њ—А—П–Љ—Л–Љ —Б–Є–љ–µ—А–≥–Є–Ј–Љ–Њ–Љ —Б –Ю–Љ–∞—А–Њ–љ–Њ–Љ. –Ґ–µ—А–∞–њ–Є—П –Ю–Љ–∞—А–Њ–љ–Њ–Љ –њ–Њ 2 –Ї–∞–њ—Б—Г–ї—Л 3 —А–∞–Ј–∞/—Б—Г—В. –≤ —В–µ—З–µ–љ–Є–µ 45 –і–љ–µ–є –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Г 117 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, 86 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї–Є –Ї–Њ–љ—В—А–Њ–ї—М–љ—Г—О –≥—А—Г–њ–њ—Г. –Ю–±–µ –≥—А—Г–њ–њ—Л –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ –њ–Њ–і–≥—А—Г–њ–њ—Л: 55 –ї–µ—В –Є –Љ–Њ–ї–Њ–ґ–µ, –≤—В–Њ—А–∞—П – —Б—В–∞—А—И–µ 55 –ї–µ—В.
–Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є –і–≤–∞–ґ–і—Л –Њ—Б–Љ–Њ—В—А–µ–љ—Л –љ–µ–≤—А–Њ–ї–Њ–≥–Њ–Љ –Є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Њ–Љ – –≤ 1––є –і–µ–љ—М –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –љ–∞ 45––є –і–µ–љ—М. –Я—А–Є –Ї–∞–ґ–і–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ –њ–∞—Ж–Є–µ–љ—В—Л –њ—А–Њ—Е–Њ–і–Є–ї–Є –њ–Њ–ї–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ, –љ–µ–є—А–Њ–Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ (–Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П, –Њ—Б–Љ–Њ—В—А –≥–ї–∞–Ј–љ–Њ–≥–Њ –і–љ–∞, –Є–Ј–Љ–µ—А–µ–љ–Є–µ –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –Љ–µ—В–Њ–і–Є–Ї–µ), –Є–Ј–Љ–µ—А—П–ї–Њ—Б—М —Б—А–µ–і–љ–µ—Б—Г—В–Њ—З–љ–Њ–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–µ –і–∞–≤–ї–µ–љ–Є–µ, –њ—Г–ї—М—Б, –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞, –њ–Њ–±–Њ—З–љ—Л–µ –і–µ–є—Б—В–≤–Є—П, –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї—Б—П —Г—А–Њ–≤–µ–љ—М —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є. –Ґ–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Њ—Ж–µ–љ–Є–≤–∞–ї–Њ—Б—М –Ї–∞—З–µ—Б—В–≤–Њ —Б–љ–∞, –ї–Є—З–љ–Њ—Б—В–љ–∞—П –Є —Б–Є—В—Г–∞—Ж–Є–Њ–љ–љ–∞—П —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В—М.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Њ –≤ —Б–µ–±—П –Њ—Ж–µ–љ–Ї—Г —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –ґ–∞–ї–Њ–± –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Њ—Ж–µ–љ–Ї—Г –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞, –Є–Ј–Љ–µ—А–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Є –њ—Г–ї—М—Б–∞ —Б —Ж–µ–ї—М—О —Г—Б—В–∞–љ–Њ–≤–Є—В—М, –≤–ї–Є—П–µ—В –ї–Є –Ю–Љ–∞—А–Њ–љ –љ–∞ –Њ—Б–љ–Њ–≤–љ—Л–µ –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –Є —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є—П. –§–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М –њ–Њ 5––±–∞–ї–ї—М–љ—Л–Љ —А–µ–є—В–Є–љ–≥–Њ–≤—Л–Љ —И–Ї–∞–ї–∞–Љ —Б–Њ —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Њ—Ж–µ–љ–Ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–∞–ґ–і–Њ–≥–Њ —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞ (–Њ—В 0 – –љ–µ—В –љ–∞—А—Г—И–µ–љ–Є–є –і–Њ 4 – –≥—А—Г–±—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П, –∞–љ–∞–ї–Њ–≥–Є—З–љ–Њ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ). –Ю—Ж–µ–љ–Є–≤–∞–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л: –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ, —И—Г–Љ –≤ –≥–Њ–ї–Њ–≤–µ, –љ–∞—А—Г—И–µ–љ–Є–µ –њ–∞–Љ—П—В–Є –Є —Б–љ–∞, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М, –Ј–∞—В—А—Г–і–љ–µ–љ–Є–µ –њ—А–Є —Е–Њ–і—М–±–µ, —Б–љ–Є–ґ–µ–љ–Є–µ –Ј—А–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є–µ —А–µ—З–Є, –љ–µ–і–µ—А–ґ–∞–љ–Є–µ –Љ–Њ—З–Є, —З—Г–≤—Б—В–≤–Њ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –љ–∞–њ—А—П–ґ–µ–љ–Є—П, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, —Б—В—А–∞—Е–Є, –Њ–љ–µ–Љ–µ–љ–Є–µ –≤ –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е. –Э–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ї–ї—О—З–∞–ї–Њ –≤ —Б–µ–±—П: –Љ–Є–љ–Є—В–µ—Б—В –Њ—Ж–µ–љ–Ї–Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П (Mini–mental scale examination – MMSE); –і–ї—П –Њ—Ж–µ–љ–Ї–Є –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –Ј—А–Є—В–µ–ї—М–љ–Њ–є –њ–∞–Љ—П—В–Є –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–µ–і—К—П–≤–ї—П–ї–Є—Б—М 16 –Ї–∞—А—В–Є–љ–Њ–Ї —Б —Н–Ї—Б–њ–Њ–Ј–Є—Ж–Є–µ–є 30–60 —Б (—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ј–∞–њ–Њ–Љ–љ–Є–≤—И–Є—Е—Б—П –Ї–∞—А—В–Є–љ–Њ–Ї); –і–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є —Б–ї—Г—Е–Њ–≤–Њ–є –њ–∞–Љ—П—В–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Њ—Б—М 10 —Б–ї–Њ–≤ (—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Њ—Б—М –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Ј–∞–њ–Њ–Љ–љ–Є–≤—И–Є—Е—Б—П —Б–ї–Њ–≤ –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–≥–Њ –њ–Њ–≤—В–Њ—А–µ–љ–Є—П) [3]. –Ф–ї—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Г—А–Њ–≤–љ—П –≤–љ–Є–Љ–∞–љ–Є—П –±—Л–ї–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л —З–µ—А–љ–Њ––±–µ–ї—Л–µ —В–∞–±–ї–Є—Ж—Л –®—Г–ї—М—В–µ (—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Њ—Б—М –≤—А–µ–Љ—П, –Ј–∞ –Ї–Њ—В–Њ—А–Њ–µ –њ–∞—Ж–Є–µ–љ—В –љ–∞—Е–Њ–і–Є–ї —Ж–Є—Д—А—Л –Њ—В 1 –і–Њ 25 –≤ –Ї–≤–∞–і—А–∞—В–∞—Е). –Т –Ї–Њ—А—А–µ–Ї—В—Г—А–љ–Њ–є –њ—А–Њ–±–µ –С—Г—А–і–Њ–љ–∞ —А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Њ—Б—М –≤—А–µ–Љ—П –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –њ–µ—А–≤–Њ–є –Є –≤—В–Њ—А–Њ–є –њ–Њ–ї–Њ–≤–Є–љ—Л —В–∞–±–ї–Є—Ж—Л, –њ—А–Њ–і—Г–Ї—В–Є–≤–љ–Њ—Б—В—М –≤–љ–Є–Љ–∞–љ–Є—П – –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–Њ—Б–Љ–Њ—В—А–µ–љ–љ—Л—Е –Ј–љ–∞–Ї–Њ–≤ –Ј–∞ 5 –Љ–Є–љ., —В–Њ—З–љ–Њ—Б—В—М –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П – –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–∞–≤–Є–ї—М–љ–Њ –Є –Њ—И–Є–±–Њ—З–љ–Њ –≤—Л—З–µ—А–Ї–љ—Г—В—Л—Е —Ж–Є—Д—А –Ј–∞ 5 –Љ–Є–љ.). –Я–Њ—Б–ї–µ–і–љ–Є–µ –і–≤–∞ –Љ–µ—В–Њ–і–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ј–≤–Њ–ї—П—О—В –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞—В—М –љ–µ —В–Њ–ї—М–Ї–Њ —Г—А–Њ–≤–µ–љ—М –≤–љ–Є–Љ–∞–љ–Є—П, –љ–Њ –Є –Є—Б—В–Њ—Й–∞–µ–Љ–Њ—Б—В—М –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —А–∞–±–Њ—В—Л.
–Ф–ї—П —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –њ–µ—А–≤—Л–є —А–∞–Ј–і–µ–ї (General Health (GH) – –Њ–±—Й–µ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ј–і–Њ—А–Њ–≤—М—П) –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є «SF–36 HEALTH STATUS SURVEY» – –Њ—Ж–µ–љ–Ї–∞ –±–Њ–ї—М–љ—Л–Љ —Б–≤–Њ–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Ј–і–Њ—А–Њ–≤—М—П –≤ –љ–∞—Б—В–Њ—П—Й–Є–є –Љ–Њ–Љ–µ–љ—В –Є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤ –ї–µ—З–µ–љ–Є—П (–≤—Л—Б–Њ–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –ї—Г—З—И–µ–µ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є) [10].
–Ф–ї—П —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –Ї–∞—З–µ—Б—В–≤–∞ –љ–Њ—З–љ–Њ–≥–Њ —Б–љ–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М 5––±–∞–ї–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ —Б–ї–µ–і—Г—О—Й–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Б–љ–∞: —Б–Ї–Њ—А–Њ—Б—В—М –Ј–∞—Б—Л–њ–∞–љ–Є—П, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –Є –≥–ї—Г–±–Є–љ–∞ —Б–љ–∞, —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є–µ –њ–Њ—Б–ї–µ –њ—А–Њ–±—Г–ґ–і–µ–љ–Є—П, –≥–і–µ 1 –±–∞–ї–ї – –њ–ї–Њ—Е–Њ, –∞ 5 –±–∞–ї–ї–Њ–≤ – –Њ—В–ї–Є—З–љ–Њ. –Т—Б–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —Б—Г–Љ–Љ–Є—А–Њ–≤–∞–ї–Є—Б—М –≤ –Њ–±—Й—Г—О –Њ—Ж–µ–љ–Ї—Г —Б–љ–∞. –£—А–Њ–≤–µ–љ—М –ї–Є—З–љ–Њ—Б—В–љ–Њ–є –Є —А–µ–∞–Ї—В–Є–≤–љ–Њ–є —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В–Є –Њ—Ж–µ–љ–Є–≤–∞–ї—Б—П –њ–Њ —И–Ї–∞–ї–µ –°–њ–Є–ї–±–µ—А–≥–µ—А–∞ [3].
–Т—А–∞—З–Њ–Љ –Є –±–Њ–ї—М–љ—Л–Љ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞ –≤—Л—Б—В–∞–≤–ї—П–ї–∞—Б—М –Њ–±—Й–∞—П –Њ—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–∞ –Є –њ–Њ–±–Њ—З–љ—Л—Е –і–µ–є—Б—В–≤–Є–є –ї–µ—З–µ–љ–Є—П, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М —И–Ї–∞–ї–∞ –Њ–±—Й–µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–њ–µ—З–∞—В–ї–µ–љ–Є—П (Clinical Global Impression’Scale — CGI), –∞ –Є–Љ–µ–љ–љ–Њ —Б—Г–±—И–Ї–∞–ї–∞ –Є–љ–і–µ–Ї—Б–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є, –Ї–Њ—В–Њ—А—Л–є —А–∞—Б—Б—З–Є—В—Л–≤–∞–µ—В—Б—П –њ–Њ —Б–Њ–≤–Њ–Ї—Г–њ–љ–Њ—Б—В–Є –Њ–і–љ–Њ–є –Є–Ј —З–µ—В—Л—А–µ—Е —Б—В–µ–њ–µ–љ–µ–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ (–Ј–∞–Љ–µ—В–љ—Л–є, —Г–Љ–µ—А–µ–љ–љ—Л–є, –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–є, –±–µ–Ј –Є–Ј–Љ–µ–љ–µ–љ–Є–є) –Є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –њ–Њ–±–Њ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А–µ–њ–∞—А–∞—В–∞ (–Њ—В—Б—Г—В—Б—В–≤—Г–µ—В, –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є, –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є, –љ–Є–≤–µ–ї–Є—А—Г—О—Й–Є–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В).
–Я—А–Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Д–Є–Ї—Б–Є—А–Њ–≤–∞–ї–Є—Б—М –Њ—Б—В—А–Њ—В–∞ –Ј—А–µ–љ–Є—П, —Б–Њ—Б—В–Њ—П–љ–Є–µ —Б–Њ—Б—Г–і–Њ–≤ —Б–µ—В—З–∞—В–Ї–Є, –Ј–љ–∞—З–µ–љ–Є—П –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П –љ–∞ –Њ–±–∞ –≥–ї–∞–Ј–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –°—Г–Љ–Љ–∞ –≤—Б–µ—Е –Љ–µ—А–Є–і–Є–∞–љ–Њ–≤ –≤ –љ–Њ—А–Љ–µ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 535 –≥—А–∞–і—Г—Б–Њ–≤, —З—В–Њ –±—Л–ї–Њ –љ–∞–Љ–Є –њ—А–Є–љ—П—В–Њ –Ј–∞ 100%. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–∞ –њ–µ—А–Є–Љ–µ—В—А–µ –§–µ—А—Б—В–µ—А–∞, –±–µ–ї–∞—П –Љ–µ—В–Ї–∞ 2 –Љ–Љ. –Я—А–Є –Њ–≥—А–∞–љ–Є—З–µ–љ–Є–Є –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П, –Ј–∞—Д–Є–Ї—Б–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –њ–Њ –Њ—В–і–µ–ї—М–љ—Л–Љ –Љ–µ—А–Є–і–Є–∞–љ–∞–Љ, —Б—Г–Љ–Љ–∞ –≤—Б–µ—Е –Љ–µ—А–Є–і–Є–∞–љ–Њ–≤ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П, —З—В–Њ —Д–Є–Ї—Б–Є—А–Њ–≤–∞–ї–Њ—Б—М –Њ—Д—В–∞–ї—М–Љ–Њ–ї–Њ–≥–Њ–Љ.
–Ф–ї—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ –∞–љ–∞–ї–Є–Ј–∞ –њ–Њ–і—Б—З–Є—В—Л–≤–∞–ї–Є—Б—М —Б—А–µ–і–љ–Є–µ –Ј–љ–∞—З–µ–љ–Є—П –Є —Б—В–∞–љ–і–∞—А—В–љ–Њ–µ –Њ—В–Ї–ї–Њ–љ–µ–љ–Є–µ. –°—А–∞–≤–љ–µ–љ–Є–µ –њ—А–Њ–≤–Њ–і–Є–ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ t––Ї—А–Є—В–µ—А–Є—П –°—В—М—О–і–µ–љ—В–∞ –Є –љ–µ–њ–∞—А–∞–Љ–µ—В—А–Є—З–µ—Б–Ї–Њ–≥–Њ U––Ї—А–Є—В–µ—А–Є—П –Ь–∞–љ–љ–∞ – –£–Є—В–љ–Є, –њ—А–Є –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Ї—А–Є—В–µ—А–Є–є –£–Є–ї–Ї–Њ–Ї—Б–Њ–љ–∞. –†–∞–Ј–ї–Є—З–Є—П —Б—З–Є—В–∞–ї–Є—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ–Є –њ—А–Є p<0,05. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П –Њ–±—А–∞–±–Њ—В–Ї–∞ –Љ–∞—В–µ—А–Є–∞–ї–∞ –њ—А–Њ–≤–Њ–і–Є–ї–∞—Б—М —Б –њ–Њ–Љ–Њ—Й—М—О –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ—Л Statistica 6.0.
–†–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –њ—А–Є—З–Є–љ–∞–Љ–Є —А–∞–Ј–≤–Є—В–Є—П –Ф–≠ —Г –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е 203 –±–Њ–ї—М–љ—Л—Е —П–≤–Є–ї–∞—Б—М –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М – —Г 185 (91,1%) —З–µ–ї–Њ–≤–µ–Ї, –љ–∞—А—Г—И–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–≥–Њ —А–Є—В–Љ–∞ – —Г 51 (25,1%), —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В – —Г 43 (22,6%), –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є—П – 25 (12,3%). –Ґ—А–∞–љ–Ј–Є—В–Њ—А–љ—Л–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –∞—В–∞–Ї–Є –Є–Љ–µ–ї–Є 11 (5,4%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤.
–£ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≤—Л—П–≤–ї—П–ї–Є—Б—М —Б–ї–µ–і—Г—О—Й–Є–µ –ґ–∞–ї–Њ–±—Л: –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М —Г 64 (31,5%) —З–µ–ї–Њ–≤–µ–Ї, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ – —Г 46 (22,6%), –љ–∞—А—Г—И–µ–љ–Є–µ –њ–∞–Љ—П—В–Є – —Г 50 (24,6%), —И—Г–Љ –≤ –≥–Њ–ї–Њ–≤–µ – 85 (41,8%), –љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞ – —Г 144 (70,9)%, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М 164 (80,8%), –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М – —Г 91 (44,8%), –Ј–∞—В—А—Г–і–љ–µ–љ–Є–µ –њ—А–Є —Е–Њ–і—М–±–µ – —Г 34 (16,7%), —Б–љ–Є–ґ–µ–љ–Є–µ –Ј—А–µ–љ–Є—П – —Г 103 (50,7%), –љ–∞—А—Г—И–µ–љ–Є–µ —А–µ—З–Є – —Г 6 (3%), –љ–µ–і–µ—А–ґ–∞–љ–Є–µ –Љ–Њ—З–Є – —Г 1 (0,5%), —З—Г–≤—Б—В–≤–Њ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –љ–∞–њ—А—П–ґ–µ–љ–Є—П 28(13,8%), —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М – —Г 10 (4,9%), —Б—В—А–∞—Е–Є – —Г 4 (2%), –Њ–љ–µ–Љ–µ–љ–Є–µ –Є —Б–ї–∞–±–Њ—Б—В—М –≤ –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е —Г 24 (11,8%).
–Я—А–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ –≤—Л—П–≤–ї—П–ї–Є—Б—М —В–∞–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л, –Ї–∞–Ї –ї–µ–≥–Ї–∞—П –њ–Є—А–∞–Љ–Є–і–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –≤ –≤–Є–і–µ –њ–Њ–≤—Л—И–µ–љ–Є—П —Б—Г—Е–Њ–ґ–Є–ї—М–љ—Л—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤ –Є–ї–Є –∞–љ–Є–Ј–Њ—А–µ—Д–ї–µ–Ї—Б–Є–Є 105 (51,7%), —А–µ—Д–ї–µ–Ї—Б—Л –Њ—А–∞–ї—М–љ–Њ–≥–Њ –∞–≤—В–Њ–Љ–∞—В–Є–Ј–Љ–∞ —Г 34 (16,7%), –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–∞—П –∞—В–∞–Ї—Б–Є—П –≤ –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е —Г 45 (22,1%), —Ж–µ—А–µ–±—А–Њ–∞—Б—В–µ–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П – 78 (38,4%), –і–Є–Ј–∞—А—В—А–Є—П —Г 11 (5,4%), –і–Є—Б—Д–Њ–љ–Є—П – 9 (4,4%), —А–∞—Б—Б–µ—П–љ–љ–∞—П –Љ–Є–Ї—А–Њ–Њ—З–∞–≥–Њ–≤–∞—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ —Г 53 (26,1%). –Ъ–∞–Ї –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є, —В–∞–Ї –Є –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ —Б—В–∞—В—Г—Б–µ –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М.
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –Ї—А–∞—В–Ї–Њ–є —И–Ї–∞–ї—Л –Њ—Ж–µ–љ–Ї–Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ (MMSE) –Њ—Ж–µ–љ–Ї–∞ –Ї–Њ–ї–µ–±–∞–ї–∞—Б—М –Њ—В 16 –і–Њ 30 –±–∞–ї–ї–Њ–≤, —Б—А–µ–і–љ–Є–є –±–∞–ї–ї 25, –љ–∞ 45––є –і–µ–љ—М –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –љ–µ –±—Л–ї–Њ –Ј–љ–∞—З–Є–Љ–Њ–є —А–∞–Ј–љ–Є—Ж—Л. –Ф–Є–љ–∞–Љ–Є–Ї–∞ —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –ґ–∞–ї–Њ–± –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–µ–љ–∞ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.
–Я—А–Є —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞–±–Њ—В–Ї–µ –і–∞–љ–љ—Л—Е –њ–Њ–ї—Г—З–µ–љ—Л —А–∞–Ј–ї–Є—З–Є—П –Љ–µ–ґ–і—Г –Њ—Б–љ–Њ–≤–љ–Њ–є –Є –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–∞–Љ–Є –љ–∞ 45––є –і–µ–љ—М –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—А–Є—Б. 1): —Г–ї—Г—З—И–µ–љ–Є—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ—Л –њ–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ –њ—А–Є–Ј–љ–∞–Ї–∞–Љ: –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М (—А<0,01), –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ (—А<0,01), –љ–∞—А—Г—И–µ–љ–Є–µ –њ–∞–Љ—П—В–Є (—А<0,05), —Б–љ–Є–ґ–µ–љ–Є–µ –Ј—А–µ–љ–Є—П (—А<0,01), –Њ–љ–µ–Љ–µ–љ–Є–µ –Є —Б–ї–∞–±–Њ—Б—В—М –≤ –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е (—А<0,05).
–Т –њ–µ—А–≤—Л–є –і–µ–љ—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –њ—А–∞–≤–Є–ї—М–љ–Њ –љ–∞–Ј–≤–∞–љ–љ—Л—Е –Ї–∞—А—В–Є–љ–Њ–Ї –±—Л–ї–Њ –Њ–±—А–∞—В–љ–Њ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –≤–Њ–Ј—А–∞—Б—В—Г –њ–∞—Ж–Є–µ–љ—В–∞. –Т –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Њ–±—К–µ–Љ –Ј—А–Є—В–µ–ї—М–љ–Њ–є –њ–∞–Љ—П—В–Є –њ–Њ—Б–ї–µ 45––і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ (—А<0,01) –≤–Њ–Ј—А–Њ—Б –≤ –Њ–±–µ–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е (–Љ–ї–∞–і—И–∞—П, —Б—В–∞—А—И–∞—П) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б 10,3 (–Ї–∞—А—В–Є–љ–Њ–Ї) –і–Њ 12,0 –Є —Б 8,1 –і–Њ 9,8 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –∞ —В–∞–Ї–ґ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є, –≤ –Ї–Њ—В–Њ—А–Њ–є –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–ї—Г—З—И–µ–љ–Є–µ –Ј—А–Є—В–µ–ї—М–љ–Њ–є –њ–∞–Љ—П—В–Є –ї–Є—И—М —Б 9,1 –і–Њ 10,4 –Є —Б 8,7 –і–Њ 9,1.
–°–Њ—Б—В–Њ—П–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–є –≤–µ—А–±–∞–ї—М–љ–Њ–є –њ–∞–Љ—П—В–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–Њ –љ–∞—З–∞–ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ –њ–Њ –≤—Б–µ–Љ –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ—Л–Љ –њ–∞—А–∞–Љ–µ—В—А–∞–Љ –љ–Є–ґ–љ–Є–Љ –≥—А–∞–љ–Є—Ж–∞–Љ –љ–Њ—А–Љ—Л. –Т —Е–Њ–і–µ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –Њ—В—З–µ—В–ї–Є–≤—Л–µ –њ–Њ–Ј–Є—В–Є–≤–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ –≤—Б–µ–Љ –Њ—Ж–µ–љ–Є–≤–∞–µ–Љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П–Љ. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е —А–∞–Ј–ї–Є—З–Є–є –Љ–µ–ґ–і—Г –≤–Њ–Ј—А–∞—Б—В–љ—Л–Љ–Є –њ–Њ–і–≥—А—Г–њ–њ–∞–Љ–Є –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М. –Ъ 45––Љ—Г –і–љ—О –њ—А–Є–µ–Љ–∞ –Ю–Љ–∞—А–Њ–љ–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –њ–∞–Љ—П—В–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–Є–љ–∞–Љ–Є–Ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –£–≤–µ–ї–Є—З–µ–љ–Є–µ –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–є —Б–ї—Г—Е–Њ–≤–Њ–є –њ–∞–Љ—П—В–Є –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –ї–µ—З–µ–љ–Є—П –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Њ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 2.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –≤—Л—П–≤–Є–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –Є—Е —Г–ї—Г—З—И–µ–љ–Є–µ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ: —Г–ї—Г—З—И–Є–ї–Є—Б—М —В–∞–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є, –Ї–∞–Ї –Њ–±—К–µ–Љ—Л –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П, —Д—Г–љ–Ї—Ж–Є–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –Є –њ–µ—А–µ–Ї–ї—О—З–µ–љ–Є—П. –Ю–њ—В–Є–Љ–Є–Ј–∞—Ж–Є—П —Д—Г–љ–Ї—Ж–Є–є –≤–љ–Є–Љ–∞–љ–Є—П –≤—Л—А–∞–ґ–∞–ї–∞—Б—М –≤ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –≤—А–µ–Љ–µ–љ–Є –њ—А–Њ—Б–Љ–Њ—В—А–∞ —В–∞–±–ї–Є—Ж, –≤–Њ–Ј—А–Њ—Б —В–∞–Ї–ґ–µ –Њ–±—Й–Є–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —А–∞–±–Њ—В—Л.
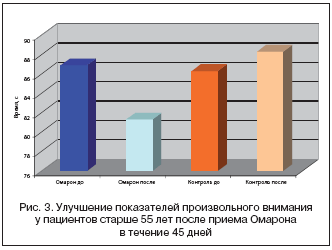
–£–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –≤—Л—А–∞–Ј–Є–ї–Њ—Б—М –≤ —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –≤—А–µ–Љ–µ–љ–Є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ –і–ї—П –љ–∞—Е–Њ–ґ–і–µ–љ–Є—П —Ж–Є—Д—А –њ–Њ —В–∞–±–ї–Є—Ж–∞–Љ –®—Г–ї—М—В–µ (—А–Є—Б. 3). –°—А–µ–і–љ–µ–µ –≤—А–µ–Љ—П –Њ–±—А–∞–±–Њ—В–Ї–Є –≤—Б–µ—Е –Ї–≤–∞–і—А–∞—В–Њ–≤ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Њ—Б—М –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є: —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —А–∞–Ј–ї–Є—З–Є—П (—А=0,01) –њ–Њ–ї—Г—З–µ–љ—Л –њ–Њ –њ–µ—А–≤–Њ–є, –≤—В–Њ—А–Њ–є —В–∞–±–ї–Є—Ж–µ –Є —Б—А–µ–і–љ–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –≤—Б–µ—Е —В–∞–±–ї–Є—Ж. –≠—Д—Д–µ–Ї—В «–≤—А–∞–±–∞—В—Л–≤–∞–µ–Љ–Њ—Б—В–Є» –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П –≤—А–µ–Љ–µ–љ–Є —А–∞–±–Њ—В—Л —Б –њ—П—В—Л–Љ –Ї–≤–∞–і—А–∞—В–Њ–Љ –њ—А–Є—Б—Г—В—Б—В–≤—Г–µ—В –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ. –Ґ.–µ. –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П –љ–∞—А–∞—Б—В–∞–љ–Є–µ –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–≥–Њ —В–µ–Љ–њ–∞ –Є —Б–Ї–Њ—А–Њ—Б—В–Є –Њ—А–Є–µ–љ—В–Є—А–Њ–≤–Њ—З–љ–Њ––њ–Њ–Є—Б–Ї–Њ–≤—Л—Е –і–≤–Є–ґ–µ–љ–Є–є –≤–Ј–Њ—А–∞ –њ—А–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є–Є –Ј–∞–і–∞–љ–Є—П. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –і–Њ—Б—В–Є–≥–љ—Г—В–Њ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ —В–Њ–ї—М–Ї–Њ –Ј–∞ —Б—З–µ—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –њ–Њ–і–≥—А—Г–њ–њ—Л, –≤ –Љ–Њ–ї–Њ–і–Њ–є –њ–Њ–і–≥—А—Г–њ–њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–є –љ–µ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М, —В.–Ї. –≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≤ –љ–µ–є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –љ–Њ—А–Љ–µ 48 –Є 50 —Б.
–Р–љ–∞–ї–Є–Ј —Г—А–Њ–≤–љ—П —Г–Љ—Б—В–≤–µ–љ–љ–Њ–є —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –≤ —Е–Њ–і–µ —В–µ—А–∞–њ–Є–Є –Ю–Љ–∞—А–Њ–љ–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –µ–≥–Њ –њ—А–Є–µ–Љ–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є—Б—М –Њ–±—К–µ–Љ—Л –Њ–±—А–∞–±–Њ—В–∞–љ–љ–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –Є –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ —Г–ї—Г—З—И–∞–ї–Њ—Б—М –Ї–∞—З–µ—Б—В–≤–Њ —Г–Љ—Б—В–≤–µ–љ–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —З–Є—Б–ї–∞ –Њ—И–Є–±–Њ–Ї.
–Ф–Є–љ–∞–Љ–Є–Ї–∞ —Г–Љ—Б—В–≤–µ–љ–љ–Њ–є —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, —В–Њ—З–љ–Њ—Б—В–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Ј–∞–і–∞–љ–Є–є –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –≤ –Ї–Њ—А—А–µ–Ї—В—Г—А–љ–Њ–є –њ—А–Њ–±–µ –С—Г—А–і–Њ–љ–∞ (—В–∞–±–ї. 1). –Ю—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –Ю–Љ–∞—А–Њ–љ, –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –њ–Њ–Ї–∞–Ј—Л–≤–∞–ї–Є –љ–µ—Б—А–∞–≤–љ–Є–Љ–Њ –ї—Г—З—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ —Б–Ї–Њ—А–Њ—Б—В–Є –Є —В–Њ—З–љ–Њ—Б—В–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П —В–µ—Б—В–∞. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї–µ–Љ –њ–Њ–ї—Г—З–µ–љ—Л –њ–Њ –Њ–±—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –≤—Л–њ–Њ–ї–љ–µ–љ–Є—П –Ј–∞–і–∞–љ–Є—П (—А<0,01) –Є –њ–µ—А–≤–Њ–є –њ–Њ–ї–Њ–≤–Є–љ—Л –Ј–∞–і–∞–љ–Є—П (—А<0,01), –Ї–Њ–ї–Є—З–µ—Б—В–≤—Г –њ—А–Њ—Б–Љ–Њ—В—А–µ–љ–љ—Л—Е –Ј–љ–∞–Ї–Њ–≤ (—А<0,05) –Є –њ—А–∞–≤–Є–ї—М–љ–Њ –≤—Л—З–µ—А–Ї–љ—Г—В—Л—Е –Ј–љ–∞–Ї–Њ–≤ (—А<0,05), –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Њ—И–Є–±–Њ–Ї —Г–Љ–µ–љ—М—И–Є–ї–Њ—Б—М —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–Ј–љ–∞—З–Є–Љ–Њ. –Ю—И–Є–±–Ї–Є —З–∞—Й–µ —Б–Њ–≤–µ—А—И–∞–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л –Љ–Њ–ї–Њ–ґ–µ 55 –ї–µ—В.
–Я—А–Є –њ—А–µ–і—К—П–≤–ї–µ–љ–Є–Є –њ–µ—А–≤–Њ–≥–Њ —А–∞–Ј–і–µ–ї–∞ (General Health (GH) – –Њ–±—Й–µ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ –Ј–і–Њ—А–Њ–≤—М—П) –Њ–њ—А–Њ—Б–љ–Є–Ї–∞ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є «SF–36 HEALTH STATUS SURVEY» –њ–∞—Ж–Є–µ–љ—В—Л –≤—Б–µ—Е –≤–Њ–Ј—А–∞—Б—В–Њ–≤ –Є –≥—А—Г–њ–њ –і–∞–≤–∞–ї–Є —Е–Њ—А–Њ—И—Г—О –Њ—Ж–µ–љ–Ї—Г —Б–≤–Њ–µ–Љ—Г –Ј–і–Њ—А–Њ–≤—М—О –Є –љ–µ –Њ—В–Љ–µ—З–∞–ї–Є —Г—Е—Г–і—И–µ–љ–Є—П –≤ –љ–µ–Љ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ. –¶–Є—Д—А—Л –≤—Б–µ—Е –Њ—Ж–µ–љ–Њ–Ї –Ї–Њ–ї–µ–±–∞–ї–Є—Б—М –≤ —Б–ї–µ–і—Г—О—Й–Є—Е –њ—А–µ–і–µ–ї–∞—Е: 3,4–3,7.
–С—Л–ї–∞ –Њ—Ж–µ–љ–µ–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П –≤—А–∞—З–Њ–Љ –Є –±–Њ–ї—М–љ—Л–Љ, –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞, –њ–Њ —И–Ї–∞–ї–µ –Њ–±—Й–µ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –≤–њ–µ—З–∞—В–ї–µ–љ–Є—П (–Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ – 3). –Я–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞–≤—И–Є–µ –Ю–Љ–∞—А–Њ–љ, –і–∞–ї–Є —Б–ї–µ–і—Г—О—Й–Є–µ –Њ—Ж–µ–љ–Ї–Є: –Љ–Њ–ї–Њ–ґ–µ 55 –ї–µ—В – 2,5, —Б—В–∞—А—И–∞—П –≥—А—Г–њ–њ–∞ –Њ—Ж–µ–љ–Є–ї–∞ –ї–µ—З–µ–љ–Є–µ –≤ 1,6 –±–∞–ї–ї–∞. –Я—А–Є —Н—В–Њ–Љ –Њ–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є—П—Е –њ—А–Њ–Є–Ј–Њ—И–ї–Њ –±–Њ–ї—М—И–µ —Г —Б—В–∞—А—И–µ–є –≥—А—Г–њ–њ—Л –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Т—А–∞—З–Є –і–∞–ї–Є –Њ—Ж–µ–љ–Ї–Є 2,4 –Є 2,2 —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ –Љ–ї–∞–і—И–µ–є –Є —Б—В–∞—А—И–µ–є –њ–Њ–і–≥—А—Г–њ–њ–∞–Љ.
–Ф–Є–љ–∞–Љ–Є–Ї–∞ —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–∞ –≤ —В–∞–±–ї–Є—Ж–µ 2. –Ы–Є—З–љ–Њ—Б—В–љ–∞—П —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В—М –љ–µ –њ—А–µ—В–µ—А–њ–µ–ї–∞ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е: –і–ї—П –ї–Є—Ж –Љ–Њ–ї–Њ–ґ–µ 55 –ї–µ—В –Ј–љ–∞—З–µ–љ–Є–µ —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В–Є –±—Л–ї–Њ —Г–Љ–µ—А–µ–љ–љ—Л–Љ: 43,1–45,3, —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –≥—А—Г–њ–њ—Л –ї–Є—З–љ–Њ—Б—В–љ–∞—П —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В—М –±—Л–ї–∞ –≤—Л—И–µ: 47,6–50,1. –Я—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Њ–њ—А–Њ—Б–µ –≤—Л—П–≤–ї–µ–љ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —А–µ–∞–Ї—В–Є–≤–љ–Њ–є —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В–Є –≤ —Б—В–∞—А—И–Є—Е –њ–Њ–і–≥—А—Г–њ–њ–∞—Е, –њ—А–Є—З–µ–Љ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –ї–µ—З–µ–љ–Є—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–Ј–Є–ї—Б—П –і–Њ —Г–Љ–µ—А–µ–љ–љ–Њ–≥–Њ (—А<0,01), –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –Њ–љ –і–∞–ґ–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Г–≤–µ–ї–Є—З–Є–ї—Б—П. –Т –Љ–ї–∞–і—И–Є—Е –≤–Њ–Ј—А–∞—Б—В–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –љ–µ –њ—А–Њ–Є–Ј–Њ—И–ї–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є.
–£—З–Є—В—Л–≤–∞—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –Њ–±—А–∞–±–Њ—В–Ї–Є –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –њ—А–Є –Њ–њ—А–Њ—Б–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–∞–љ–љ—Л—Е –Њ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ —Г–ї—Г—З—И–µ–љ–Є–Є –Ј—А–µ–љ–Є—П –њ—А–Є –њ—А–Є–µ–Љ–µ –Ю–Љ–∞—А–Њ–љ–∞, –љ–∞–Љ–Є –±—Л–ї–∞ –њ—А–µ–і–њ—А–Є–љ—П—В–∞ –њ–Њ–њ—Л—В–Ї–∞ –Њ–±—К–µ–Ї—В–Є–≤–Є–Ј–Є—А–Њ–≤–∞—В—М —Н—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –Ј—А–Є—В–µ–ї—М–љ–Њ–Љ –∞–љ–∞–ї–Є–Ј–∞—В–Њ—А–µ.
–Ґ–∞–Ї–ґ–µ –±—Л–ї–∞ –њ—А–Њ–≤–µ–і–µ–љ–∞ —Б—В–∞–љ–і–∞—А—В–љ–∞—П –Љ–µ—В–Њ–і–Є–Ї–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П —Г 203 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (406 –≥–ї–∞–Ј). –Я—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —А–µ–Ј—Г–ї—М—В–∞—В—Л (–≤ % –Њ—В –љ–Њ—А–Љ—Л): –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Њ—В 79 –і–Њ 97% —Г –Љ–ї–∞–і—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –њ–Њ–і–≥—А—Г–њ–њ—Л –Є –Њ—В 45 –і–Њ 90% –≤ —Б—В–∞—А—И–µ–є. –Р–±—Б–Њ–ї—О—В–љ—Л–є –њ—А–Є—А–Њ—Б—В –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П —З–µ—А–µ–Ј 45 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –Ю–Љ–∞—А–Њ–љ–∞ —Б–Њ—Б—В–∞–≤–Є–ї –Њ—В 0 –і–Њ 11% –≤ –Љ–ї–∞–і—И–µ–є –≤–Њ–Ј—А–∞—Б—В–љ–Њ–є –њ–Њ–і–≥—А—Г–њ–њ–µ –Є –Њ—В 0 –і–Њ 28% –≤ —Б—В–∞—А—И–µ–є –њ–Њ–і–≥—А—Г–њ–њ–µ. –Я–Њ–ї—П –Ј—А–µ–љ–Є—П –≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–µ –љ–µ –Є–Ј–Љ–µ–љ–Є–ї–Є—Б—М —З–µ—А–µ–Ј 45 –і–љ–µ–є. –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ (—А<0,01) –Њ–Ї–∞–Ј–∞–ї–Њ—Б—М —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б—В–∞—А—И–µ 55 –ї–µ—В, –њ—А–Є–љ–Є–Љ–∞–≤—И–Є—Е –Ю–Љ–∞—А–Њ–љ – –њ—А–Є—А–Њ—Б—В –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П —Г –љ–Є—Е —Б–Њ—Б—В–∞–≤–Є–ї –≤ —Б—А–µ–і–љ–µ–Љ 10,3% (—А–Є—Б. 4).
–Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л, –≤–Ї–ї—О—З–µ–љ–љ—Л–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –њ–Њ–ї—Г—З–Є–ї–Є –њ–Њ–ї–љ—Л–є –Ї—Г—А—Б –ї–µ—З–µ–љ–Є—П. –Я–Њ–±–Њ—З–љ—Л–µ —П–≤–ї–µ–љ–Є—П –њ—А–Є –њ—А–Є–µ–Љ–µ –Ю–Љ–∞—А–Њ–љ–∞ –Њ—В–Љ–µ—З–∞–ї–∞ –Њ–і–љ–∞ –њ–∞—Ж–Є–µ–љ—В–Ї–∞ –≤ –≤–Є–і–µ –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, –њ—А–Є –і–Њ–Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –љ–µ–µ –≤—Л—П–≤–ї–µ–љ—Л –њ–Њ–і—К–µ–Љ—Л –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П, –њ—А–Є –µ–≥–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –≥–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є –Є—Б—З–µ–Ј–ї–Є.
–Т—Л–≤–Њ–і—Л
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ю–Љ–∞—А–Њ–љ–∞ – –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Б –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –∞–љ—В–Є–≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–Љ, –љ–Њ–Њ—В—А–Њ–њ–љ—Л–Љ –Є —Б–Њ—Б—Г–і–Њ—А–∞—Б—И–Є—А—П—О—Й–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 6 —В–∞–±–ї–µ—В–Њ–Ї – –±–µ–Ј–Њ–њ–∞—Б–љ–Њ –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –Ф–≠.
–Ю—Б–љ–Њ–≤–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ю–Љ–∞—А–Њ–љ–∞ –≤—Л—А–∞–ґ–∞—О—В—Б—П –≤ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ —Г–ї—Г—З—И–µ–љ–Є–Є –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є –њ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≥–Њ–ї–Њ–≤–љ–Њ–є –±–Њ–ї–Є, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є–є –њ–∞–Љ—П—В–Є, —Б–љ–Є–ґ–µ–љ–Є—П –Ј—А–µ–љ–Є—П, –Њ–љ–µ–Љ–µ–љ–Є—П –Є —Б–ї–∞–±–Њ—Б—В–Є –≤ –≤–µ—А—Е–љ–Є—Е –Є –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е.
–Ъ 45––Љ—Г –і–љ—О –њ—А–Є–µ–Љ–∞ –Ю–Љ–∞—А–Њ–љ–∞ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Њ–±—К–µ–Љ–∞ –і–Њ–ї–≥–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –њ–∞–Љ—П—В–Є –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ –Є –Њ—В—Б—Г—В—Б—В–≤–Є–µ –і–Є–љ–∞–Љ–Є–Ї–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л. –Ю—Ж–µ–љ–Ї–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П –≤—Л—П–≤–Є–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ –Є—Е —Г–ї—Г—З—И–µ–љ–Є–µ –≤ –Њ—Б–љ–Њ–≤–љ–Њ–є –≥—А—Г–њ–њ–µ: —Г–ї—Г—З—И–Є–ї–Є—Б—М —В–∞–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є, –Ї–∞–Ї –Њ–±—К–µ–Љ—Л –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–≥–Њ –≤–љ–Є–Љ–∞–љ–Є—П, —Д—Г–љ–Ї—Ж–Є–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є, —А–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є—П –Є –њ–µ—А–µ–Ї–ї—О—З–µ–љ–Є—П. –Р–љ–∞–ї–Є–Ј —Г—А–Њ–≤–љ—П —Г–Љ—Б—В–≤–µ–љ–љ–Њ–є —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –≤ —Е–Њ–і–µ —В–µ—А–∞–њ–Є–Є –Ю–Љ–∞—А–Њ–љ–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –µ–≥–Њ –њ—А–Є–µ–Љ–∞ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї–Є—Б—М –Њ–±—К–µ–Љ—Л –Њ–±—А–∞–±–Њ—В–∞–љ–љ–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –Є –њ–∞—А–∞–ї–ї–µ–ї—М–љ–Њ —Г–ї—Г—З—И–∞–ї–Њ—Б—М –Ї–∞—З–µ—Б—В–≤–Њ —Г–Љ—Б—В–≤–µ–љ–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –≤ –≤–Є–і–µ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —З–Є—Б–ї–∞ –Њ—И–Є–±–Њ–Ї.
–Ф–Њ–Ї–∞–Ј–∞–љ–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ–Њ–ї–µ–є –Ј—А–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠ —Б—В–∞—А—И–µ 55 –ї–µ—В —Б –Є—Б—Е–Њ–і–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ю–Љ–∞—А–Њ–љ–∞ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Г–ї—Г—З—И–∞—В—М —Б–Њ—Б—В–Њ—П–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠, —Г–Љ–µ–љ—М—И–∞—П –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –Њ—Б–љ–Њ–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –∞ —В–∞–Ї–ґ–µ —Г–ї—Г—З—И–∞—П –Њ—Б–љ–Њ–≤–љ—Л–µ –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ–Њ––Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є. –Ы–µ—З–µ–љ–Є–µ —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В —Б–µ—А—М–µ–Ј–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є.





–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –С–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –Є —Б–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–Љ–µ–љ—Ж–Є—П / –Я–Њ–і —А–µ–і. –Э.–Э. –ѓ—Е–љ–Њ. –Ь., 2002. 85 —Б.
2. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т., –Я–∞—А—Д–µ–љ–Њ–≤ –Т.–Р., –°–Ї–Њ—А–Њ–Љ–µ—Ж –Р.–Р., –ѓ—Е–љ–Њ –Э.–Э. –Э–∞—А—Г—И–µ–љ–Є—П –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Є —Б–њ–Є–љ–љ–Њ–Љ –Љ–Њ–Ј–≥–µ // –С–Њ–ї–µ–Ј–љ–Є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є / –Я–Њ–і —А–µ–і. –Э.–Э. –ѓ—Е–љ–Њ, –Ф.–†. –®—В—Г–ї—М–Љ–∞–љ. –Ь., 2003. –°. 231–302.
3. –С–µ–ї–Њ–≤–∞ –Р.–Э. –®–Ї–∞–ї—Л –Є –Њ–њ—А–Њ—Б–љ–Є–Ї–Є –≤ –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –љ–µ–є—А–Њ—Е–Є—А—Г—А–≥–Є–Є. –Ь., 2004.
4. –Ч–∞—Е–∞—А–Њ–≤ –Т .–Т. –Ъ–ї–Є–љ–Є–Ї–∞, –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є // –†—Г—Б—Б–Ї–Є–є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. 2009. –Ґ. 17. вДЦ 2. –°. 140–144
5. –Ы—Г—А–Є—П –Р.–†. –Т—Л—Б—И–Є–µ –Ї–Њ—А–Ї–Њ–≤—Л–µ —Д—Г–љ–Ї—Ж–Є–Є —З–µ–ї–Њ–≤–µ–Ї–∞. –Ь.: –Ш–Ј–і––≤–Њ –Ь–У–£, 1969.
6. –Я–∞—А—Д–µ–љ–Њ–≤ –Т.–Р., –С–µ–ї–∞–љ–Є–љ–∞ –У.–†., –Т–∞—Е–љ–Є–љ–∞ –Э.–Т. –Є –і—А. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ю–Љ–∞—А–Њ–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Г–Љ–µ—А–µ–љ–љ—Л–Љ–Є –њ–Њ—Б—В–Є–љ—Б—Г–ї—М—В–љ—Л–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є // –Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2009. вДЦ 6. –°. 47–51.
7. –Я–Є–ї–Є–њ–Њ–љ–Є—З –Р.–Р., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –Ы–Њ–±–љ–∞—П –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –њ—А–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є // –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –≥–µ—А–Њ–љ—В–Њ–ї–Њ–≥–Є—П. 2001. –Ґ. 5. вДЦ 6. –°. 35–41.
8. Petersen R.S., Touchon J. Consensus on mild cognitive impairment. Research and practice in Alzheimer’s disease. // EADS–ADCS jont meeting. 2005. вДЦ 10. P. 24–32
9. Roman G.V. Vascular dementia: NINDS AIREN diagnostic criteria // New concepts in vascular dementia / A. Culebras, J. Matias Guiu, G. Roman (eds). Barcelona: Prous Science Publishers, 1993. P.19.
10. Ware J.E., Snow K.K., Kosinski M. Et al. SF–36 Health Survey. Manuel and Interpretation Guide. Lincoln, RI: Quality Metric Inc. 2000. 150 —А.












