• Дебют депрессии в позднем возрасте
• Превалирование когнитивных нарушений над другими проявлениями депрессии (редукция понимания, частично исполнительная дисфункция)
• Апатия и психомоторная заторможенность
• Наличие доказательного ишемического поражения мозга, особенно белого вещества субкортикальных зон.
Эпидемиологические исследования демонстрируют наличие общих факторов риска между цереброваскулярной болезнью и депрессией. Так многочисленные исследования, в том числе выполненные на российской популяции больных, показывают чрезвычайно устойчивую ассоциацию между артериальной гипертензией и депрессией [3]. Последнее время доказана связь между депрессией и рядом васкулярных факторов риска, включая курение, чрезмерное употребление алкоголя в среднем возрасте [4], уровень липидов [5]. Обсуждается общая клиническая предиспозиция цереброваскулярной болезни и депрессии, в частности полиморфизм гена, кодирующего ангиотензин конвертирующий фермент, ассоциирован с кардиоваскулярным заболеванием и является наиболее вероятным геном ответственным за нарушение настроение, поскольку показано его влияние на активность гипоталамо–гипофизарной надпочечниковой оси [6]. Также получены первые результаты, доказывающие участие полиморфизма генов, ответственных за транспорт серотонина, в нарушении настроения и дисфункции тромбоцитов [7]. Известно, что депрессия крайне часто встречается у пожилых лиц, страдающих деменцией. Однако коморбидность с депрессией гораздо чаще выявляется у пациентов с васкулярной деменцией по сравнению с болезнью Альцгеймера [8]. Причем когнитивные и эмоциональные нарушения зависят от комбинации трех факторов: фокального ишемического поражения мозга, диффузной нейрональной дисфункции и индивидуального статуса больного, в частности, от таких характеристик как возраст, пол и наличия соматического заболевания (сахарный диабет, кардиальные заболевания и др.) [9].
Не только цереброваскулярное заболевание пораждает депрессию, но и депрессия негативно влияет на течение цереброваскулярного заболевания. Связь между цереброваскулярным заболеванием и депрессией двусторонняя, формирующая порочный круг. Депрессия повышает риск развития когнитивных сосудистых нарушений, повторного инсульта, даже после контроля других факторов риска (гипертонической болезни, диабета, гиперлипидемии, ИБС, курения) [10]. Депрессия может способствовать развитию цереброваскулярного заболевания через следующие механизмы:
• Активацию гипоталамо–гипофизарно–надпочечниковой оси
• Гиперактивацию симпато–адреналовой системы
• Облегчение гиперкоагуляционных процессов.
Следствием активации гипоталамо–гипофизарно–надпочечниковой оси при депрессии является повышение кортизола плазмы крови, которое способствует развитию атеросклероза. Избыточная концентрация кортизола ведет к активации симпато–адреналовой системы. Повышенная секреция катехоламинов в свою очередь приводит к вазоконстрикции, активации тромбоцитов и учащению работы сердца. Дисбаланс между симпатической и парасимпатической отделами вегетативной нервной системы у пациентов с депрессией способствует развитию сердечных аритмий и может быть причиной внезапной смерти. При депрессии повышен уровень катехоламинов, препятствующих гипогликемическому действию инсулина, что в свою очередь может приводить к инсулинорезистентности. Депрессия рассматривается как независимый фактор риска развития диабета второго типа. Известно, что гиперактивность гипоталамо–гипофизарно–надпочечниковой оси и симпато–адреналовой системы стимулирует процесс гиперкоагуляции. К тому же показано нарушение функции тромбоцитов у пациентов с нелеченной депрессией. Реактивность тромбоцитов на 40% выше у больных, страдающих депрессией, по сравнению со здоровыми лицами. Нарушение функции тромбоцитов ассоциировано с дисфункцией серотониновых рецепторов, в то время как селективные ингибиторы обратного захвата серотонина (СИОЗС) нормализуют активность тромбоцитов.
Депрессию коморбидную цереброваскулярным заболеваниям часто описывают как трудно диагностируемую и трудно поддающуюся лечению. В тоже время отдельные исследования демонстрируют позитивный опыт лечения васкулярной депрессии антидепрессантами, в частности СИОЗС. Кроме того, накапливаются факты благотворного влияния СИОЗС на биологические последствия депрессии. При общей полезности антидепрессивной терапии эта категория пациентов с большим трудом соглашается на терапию психотропными препаратами. К сожалению, использование антидепрессивной терапии среди пациентов общесоматического звена при наличии у них депрессии в нашей стране крайне низка и колеблется около 10% [3]. Для сравнения в Швеции как минимум каждый 1 из 7 пациентов, перенесших инсульт, прибегает к антидепрессантам. В сравнении с общей популяцией пациенты, перенесшие инсульт, в два раза чаще используют антидепрессанты. Но даже при такой высокой востребованности антидепрессантов в Европе эксперты считают, что пропорциональное отношение васкулярной депрессии и использования антидепрессантов свидетельствует о недостаточном использовании последних [11]. Поэтому крайне востребован любой опыт использования антидепрессивной терапии у больных с цереброваскулярной недостаточностью.
Нами проведено открытое исследование эффективности антидепрессанта сертралина «Асентра» производства компании Крка (Словения) в лечении депрессии у больных, страдающих цереброваскулярной недостаточностью. Выбор сертралина обусловлен тем, что СИОЗС благодаря хорошей переносимости рассматриваются как препараты первой очереди выбора для лечения депрессии у пожилых людей. Механизм действия сертралина складывается из основного – блокирование обратного захвата серотонина и двух дополнительных: блокирование обратного захвата дофамина; мягкое антагонистическое воздействие на сигма–рецепторы. Благодаря дополнительным механизмам сертралин обладает определенными преимуществами, особенно полезными для пациентов с васкулярной депрессией. Сертралин воздействует на астенические симптомы депрессии, и теоретически за счет влияния на дофаминовую систему может улучшать когнитивные функции. Мягкое блокирование сигма–рецепторов потенцирует противотревожное действие сертралина. Подтвержденная доказательными исследованиями кардиоваскулярная безопасность сертралина также не маловажна для лиц, имеющих цереброваскулярное заболевание [12].
В исследование были включены 24 пациента (в возрасте от 56 до 72 лет), страдающих цереброваскулярным заболеванием (дисциркуляторная энцефалопатия) с умеренной или мягкой степени выраженной депрессией, которые получали стандартную терапию для профилактики церебральной ишемии и Асентру в дозе 50 мг/сут. в течение восьми недель. Ноотропных и вазотропных средств за неделю до и во время исследования пациенты не принимали. Все пациенты имели сосудистые факторы риска: гипертоническая болезнь 1–2 стадии (92%), ИБС (75%), сахарный диабет второго типа (42%), гиперхолестеринемия (75%), признаки системного атеросклероза (42%), курение (33%). Всем пациентам было проведено МРТ исследование головного мозга. У 75% пациентов были выявлены сосудистые очаги и диффузное ишемическое поражение белого вещества (лейкариозис) головного мозга. У 4,1% пациентов были выявлены только сосудистые очаги и у 20,8 пациентов только лейкариозис. Все пациенты отрицали семейный анамнез депрессии. Также критерием исключения было наличие эпизодов пониженного настроения или опыта использования антидепрессантов в анамнезе.
Все пациенты были обследованы с помощью следующих методов:
1. клиническое неврологическое исследование
2. оценка состояния эмоционально–мотивационной сферы (геронтологическая шкала депрессии, шкала тревоги Спилбергера)
3. исследование когнитивной сферы (краткое исследование психического состояния (тест MMSE); кратковременной слуховой и зрительной памяти, а также внимания по таблицам Шульте); для исследования кратковременной слуховой памяти использовались 10 слов (слова назывались после двукратного повторения, регистрировалось количество запомнившихся слов); для исследования кратковременной зрительной памяти пациентам предъявлялись 16 картинок с экспозицией 30–60 с (регистрировалось количество запомнившихся картинок); по таблицам Шульте (5 таблиц) регистрировалось время, в течение которого пациент по порядку находил цифры от 0 до 25, указанные в таблицах
4. нарушение сна было оценено с помощью анкеты субъективного качества сна
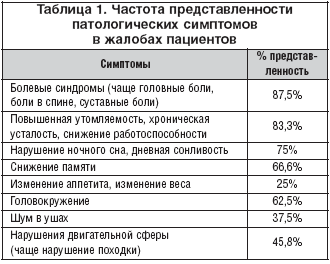
Пациенты обследовались дважды до и после 8–ми недельного курса лечения. При оценке эффективности лечения учитывалось субъективное мнение пациента о влиянии препарата на заболевание с применением следующих градаций: отличное, хорошее, удовлетворительное, плохое. Также эффективность оценивалась врачом с учетом клинических характеристик заболевания, а также общего самочувствия. Частотный спектр жалоб пациентов, послуживших поводом обращения к врачу, представлен в таблице 1.
По крайней мере, шесть первых симптомов могут быть обусловлены, как основным заболеванием, так и депрессией. При расспросе пациентов отчетливые симптомы депрессивного круга (чувство собственного бессилия, необоснованное чувство вины, намеренное ограничение круга общения, чувство тоски, раздражительность, мысли о смерти и другие) были выявлены у 70,8%. Все пациенты сообщали о подавленном или пониженном настроении, но интерпретировали этот симптом как последствие обострения основного заболевания. По данным психометрического тестирования (геронтологическая шкала депрессии – ГШД) у всех пациентов, включенных в исследование, выявлялась отчетливая депрессия. Средний по группе балл депрессии по ГШД составил 21,2±1,8 балла, реактивной тревоги – 51,0+1,6 балла, личностной тревоги – 59,3±1,6 балла. Нарушение сна было оценено с помощью анкеты субъективного качества сна, в среднем по группе качество сна составило 15,95 баллов (более 20 баллов соответствует нормальному качеству сна).
Более половины пациентов (66,6%) предъявляли жалобу на нарушение памяти, однако снижение памяти было выражено умеренно и не вызывало социальной дезадаптации больных. Дисмнестические симптомы при коррекции их простейшими приемами, облегчающими припоминание необходимого, не затрагивали нормальную повседневную активность пациентов. Краткое исследование психического состояния (тест MMSE) показало отсутствие когнитивных нарушений у 37,5% пациентов (свыше 27 балов по тесту MMSE), умеренные когнитивные нарушения у 62,5% пациентов (27–24 балла по тесту MMSE). Дальнейшее исследование когнитивного статуса пациентов показало относительно умеренные нарушения внимания, кратковременной слуховой и зрительной памяти (уровень внимания по таблицам Шульте – 53,4±3,4 с; количество запомнившихся картинок из 16 возможных составило 7,65±0,73 картинок и количество запомнившихся слов из 10 возможных – 5,65±0,33 слов).
Все пациенты, включенные в исследование, полностью завершили исследование. Положительную субъективную оценку результатам лечения (очень хорошую или хорошую) дали 54,2% пациентов. В 29,2% случаев эффект лечения пациенты оценили как незначительный, а в 16,6% отметили отсутствие эффекта.
После проведенного лечения произошли существенные изменения в психическом статусе пациентов, уровень депрессии снизился до 15,6 баллов (рис. 1). Данные настоящего исследования опровергают устоявшееся впечатление о низком эффекте антидепрессантов при депрессии у пациентов с цереброваскулярным заболеванием.
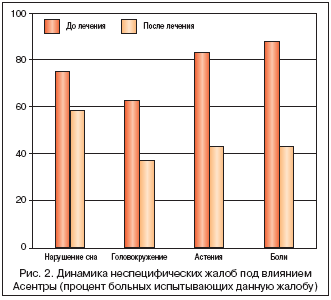
Установлена различная терапевтическая эффективность Асентры в отношении актуальных неспецифических жалоб (рис. 2). Наиболее заметный эффект Асентры отмечен в отношении болевых проявлений, астении, в меньшей степени в отношении головокружения и нарушений сна (р<0,05). Отчетливая динамика этих жалоб под влиянием антидепрессивной терапии позволяет предполагать, что в их генезе основную роль играло депрессивное расстройство. Другие анализируемые жалобы существенных изменений не претерпели. Какой–либо динамики симптомов органического поражения мозга мы не наблюдали. Некоторые пациенты отмечали увеличение общей двигательной активности, при том что объективно степень неврологического дефицита не изменялась.
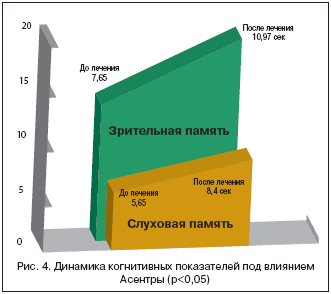
После курса лечения пациенты продолжали субъективно отмечать нарушение памяти, хотя некоторые пациенты (25%) отчитывались об определенном улучшении мнестических возможностей. Мы наблюдали несоответствие между субъективной оценкой памяти и объективными показателями когнитивного статуса, которые значимо улучшились после курса антидепрессивной терапии. Выросла пропорция пациентов с нормальными показателями теста MMSE с 37,5% до 62,5%. Дальнейшее исследование когнитивного статуса показало в первую очередь улучшение функции внимания (рис. 3), а также мнестических возможностей (рис. 4), что позволяет рассматривать определенный вклад депрессии в когнитивный статус больных с цереброваскулярной недостаточностью.
Большинство пациентов, получавших терапию Асентрой, не отметили в ходе лечения никаких побочных эффектов. 12,5% жаловались на сонливость, усиление заторможенности в течение первых 2–х недель терапии Асентрой, которые затем регрессировали. За время наблюдения ни одному из пациентов не потребовалась коррекции базисной терапии цереброваскулярного заболевания.
Представленный материал убедительно демонстрирует трудности диагностики депрессии у пожилых пациентов с цереброваскулярной недостаточностью. В первую очередь это связано с наличием общих симптомов цереброваскулярной недостаточности и депрессии, наиболее часто из них встречаются: жалобы на боли, астению, нарушение сна, головокружение, нарушения памяти. Как показало настоящее исследование, наиболее жестко с депрессией связано болевое расстройство. Клиницисту необходимо подвергать болевой синдром анализу, для исключения его депрессивной этиологии, поскольку болевое расстройство, связанное с депрессией хорошо поддается лечению.
Соматические симптомы депрессии более выражены и значимы для пациента, чем психические симптомы. Как правило, основной симптом депрессии – угнетенное настроение – не являет актуальным для пациента, а рассматривается им как второстепенный симптом, связанный с соматическим недугом. Когнитивные симптомы депрессии также превалируют над аффективными симптомами депрессии. Выраженность когнитивной дисфункции как особенность депрессии пожилых широко обсуждается в литературе. Диагностике депрессии может помочь активное выявление у пациента симптомов депрессивного круга, анализ анамнестических факторов, в частности, связь обострений заболеваний с психогенными событиями и психометрическое тестирование. Использование специальных геронтологических самооценочных шкал для выявления депрессии повышает диагностическую информативность психометрического тестирования у пациентов с цереброваскулярной недостаточностью.
Проведенное лечение свидетельствует о том, что на фоне приема антидепрессантов (Асентра) у больных с хронической цереброваскулярной недостаточностью улучшаются симптомы депрессии и даже частично улучшаются когнитивные функции. Настоящее исследование в определенной мере противоречит убеждению, что депрессия у этой категории больных плохо поддается лечению. Вероятно, современные антидепрессанты (Асентра), обладающие благоприятным спектром переносимости, позволяют проводить более адекватное лечение этой категории пациентов и существенно улучшают прогноз заболевания.
Асентра может быть рекомендована как эффективный и безопасный препарат для лечения депрессии у пациентов с цереброваскулярной недостаточностью.


Литература
1. Alexopoulos GS, Meyers BS, Young RC, et al. Vascular depression hypothesis. // Arch Gen Psychiatry 1997; 54:915–922
2. Baldwin RC. Is vascular depression a distinct sub–type of depressive disorder? A review of causal evidence. // Int J Geriatr Psychiatry 2005;20:1–11
3. Воробьева О.В. Клинические особенности депрессии в общемедицинской практике (по результатам программы «Компас»). // Консилиум 2004; том 6, №2:154–158
4. Hamalainen J, Kaprio J, Isometsa E et al. Cigarette smoking, alcohol intoxication and major depressive episode in a representative population sample. // Journal of Epidemiology and Community Health 2001;55:573–6
5. Shibata H, Kumagai S, Watanabe S, Suzuki T. Relationship of serum cholesterols and vitamin E to depressive states in the elderly. // Journal of Epidemiology 1999;9:261–7
6. Baghai TC, Binder EB, Schule C et al. Polymorphisms in the angiotensin converting enzyme gene are associated with unipolar depression, ACE activity and hypercortisolism. // Mol. Psychiatry 2006;11:1003–1015
7. Ramasubbu R. Serotonin transporter gene functional polymorphism: a plausible candidate gene for increased vascular risk in depression. // Med Hypotheses 2003;61:36–44
8. Allen NHP, Burns A. The non–cognitive features of dementia. // Reviews in Clinical Gerontology 1995;5:57–75
9. de Haan et al. Cognitive functioning following stroke and vascular cognitive impairments. // Curr Opin Neuro 2006;19:559–564
10. Larson SL, Owens PL, Ford D, Eaton W. Depressive disorder, dysthymia, and risk of stroke. Thirteen–year follow–up from the Baltimore Epidemiological Catchment Area Study. // Stroke 2001;32:1979–1983
11. Eriksson M, Asplund K, Glander EL et al. Self–reported depression and use of antidepressants after stroke a national survey. // Stroke 2004;35(4):936–41.
12. Khouzam HR, Emes R, Gill T, Raroque R. The antidepressant sertraline: a review of its uses in a range of psychiatric and medical conditions. // Compr Ther 2003;29:47–53












