Среди мужчин головокружение встречается реже (17,2%), чем у женщин (44,6% случаев).
В клинической практике различают два типа головокружения – «системное» (периферическое или «вестибулогенное») и «несистемное» (центральное, характерное для патологии ЦНС). Несистемное головокружение редко сопровождается тугоухостью, а само головокружение продолжительное, тогда как системное головокружение, как правило, сопровождается тугоухостью, а длительность головокружения обычно не превышает 1–6 ч и редко – более одних суток [1].
Головокружение может привести к значительному ухудшению качества жизни больного, лишая его возможности вести привычный образ жизни и качественно выполнять профессиональные обязанности, нередко делая его зависимым от посторонней помощи в обиходе, может вызвать стойкую утрату трудоспособности либо стать причиной инвалидности. В связи с этим проблема лечения больных, страдающих головокружением, становится все более актуальной не только в медицинском, но и в социальном аспекте.
Среди причин возникновения системного головокружения можно выделить:
1. Поражение вестибулярного анализатора периферического уровня: лабиринтиты различной этиологии – вирусные и бактериальные (гнойные и серозные), вызванные ототоксическими антибиотиками, солями тяжелых металлов, различными отравлениями, термические, травматические; тромбоз или кровоизлияние в области кровоснабжения лабиринтной артерией, при остром и хроническом среднем отите, при разрушении костной стенки горизонтального полукружного канала холестеатомой в полости среднего уха (реже и вертикального канала), травма круглого или овального окна. Особое место занимает болезнь Меньера, при которой возникают вестибулярные головокружения, изнуряющие своим течением; вестибулярный нейронит, купулолитиазис, травма височной кости с переломами пирамиды; заболевания крови, профессиональные заболевания. Нередко вестибулогенное головокружение возникает на фоне шейного остеохондроза с вертебробазилярной недостаточностью (ВБН) или при вегето–сосудистой дистонии, атеросклерозе, гипертонии с локальным сосудистым поражением в лабиринте, заболевании щитовидной железы и сахарном диабете, невриноме статоакустического нерва и арахноидите мостомозжечкового угла. Следует иметь в виду, что поражение лабиринта может быть и при сифилисе, ВИЧ–инфекции, при патологии желудочно–кишечного тракта, при нарушении обмена веществ, высокой температуре, болезни Педжета, при аутоиммунной, аллергической, наследственной патологии лабиринта и других синдромах.
2. Поражение вестибулярного анализатора центрального уровня. Причины такого поражения не менее многолики. Они могут возникать при повреждении связи с вестибулярными ядрами в стволе мозга, нарушении связей с мозжечком, медиальным продольным пучком, с глазодвигательными ядрами и их собственными связями, нарушении вестибулоспинальных и вестибулоретикулярных связей (тракта), а также нарушении связей с корой головного мозга. Эти нарушения могут быть при остром и хроническом арахноидите, стволовых энцефалитах, жидких кистах мозжечка, при опухолях мозжечка, ствола мозга, при выраженной внутричерепной гипертензии, ишемии и кровоизлиянии в области ствола мозга, в результате шейного остеохондроза с ВБН, при дегенеративных заболеваниях ЦНС, височной эпилепсии и др. Дисфункция генерации, интеграции и модуляции по этим путям может привести к головокружению как периферического, так и центрального типа [2].
В прошлом, когда не были достаточно известны физиологические и патологические механизмы, для лечения этой в значительной мере неясной патологии применяли самые разнообразные медикаменты: блокаторы карбоангидразы, адренолитики, трициклические антидепрессанты, бензодиазепины, антихолинергические и антигистаминные средства, антагонисты ионов кальция, антагонисты дофаминовых рецепторов (D2), вазодилататоры (гидергин), β–адреноблокаторы, ингибиторы ангиотензинпревращающего фермента (АПФ) и бетагистин (Бетасерк®) – соединение, различным образом взаимодействующее с гистаминергической системой.
Лечение системного головокружения чаще носит симптоматический характер. Этиологическая терапия возможна лишь при ограниченном круге заболеваний (бактериальный лабиринтит, стволовый инсульт, височная эпилепсия, базилярная мигрень, холестеатома и другие опухоли, вовлекающие вестибулярный анализатор).
Для купирования головокружения используются вестибулолитические средства, действующие на уровне вестибулярных рецепторов или центральных вестибулярных структур, в основном вестибулярных ядер ствола.
Важную роль в функционировании вестибулярных структур играет гистаминергическая система. Передача импульсации от вестибулярных ядер обеспечивается преимущественно гистаминергическими нейронами. Гистаминергическая система также обеспечивает передачу возбуждения между вестибулярными ядрами и рвотным центром. Поэтому для лечения системного головокружения используют антигистаминные препараты (меклозин, прометазин). В последние годы для купирования головокружения, а также в целях профилактики приступов успешно применяется бетагистина гидрохлорид, имеющий структурное сходство с гистамином, аффинитет к блокированию H3– и стимуляции H1–рецепторов.
Впервые препарат был применен в 1962 г. для лечения кластерной головной боли, а в 1965 г. отмечен его положительный эффект при болезни Меньера. В последние 20 лет было проведено большое число работ по оценке эффективности препарата, в том числе ряд двойных слепых исследований. Полученные данные свидетельствуют о высокой эффективности Бетасерка при болезни Меньера и других состояниях, сопровождающихся системным головокружением. Препарат снижал частоту и выраженность приступов системного головокружения, а также уменьшал нарушение равновесия.
Действие препарата Бетасерк®, являющегося структурным аналогом гистамина, реализуется через гистаминовые рецепторы. В настоящее время известны 3 типа гистаминовых рецепторов – Н1, Н2, и Н3. Рецепторы Н1 и Н2 являются постсинаптическими, Н3 – пресинаптическими. Активация рецепторов H1 и Н2 стимулирует синтез циклического аденозинмонофосфата и через систему вторичных мессенджеров увеличивает концентрацию кальция внутри клетки; активация гистаминового рецептора Н3 блокирует выделение гистамина по механизму отрицательной обратной связи.
Наряду с воздействием на гистаминовые рецепторы периферических и центральных вестибулярных структур Бетасерк® оказывает вазоактивное влияние. Препарат вызывает расширение артериол и капилляров внутреннего уха, что приводит к избирательному увеличению кровотока. Кроме того, на фоне приема препарата Бетасерк® отмечается некоторое усиление мозгового кровотока как в вертебральнобазилярном, так и в каротидном бассейне, что приводит к улучшению когнитивных функций у больных с хронической цереброваскулярной недостаточностью. Вазоактивный эффект препарата предположительно обусловлен действием на гистаминовые рецепторы и, возможно, воздействием на пресинаптические адренорецепторы. В связи с этим следует отметить, что наибольшая концентрация гистаминовых рецепторов отмечается в мелких артериях внутреннего уха.
Назначение Бетасерка уменьшает частоту, выраженность и продолжительность приступов системного головокружения. Наряду с положительным влиянием на вестибулярную функцию на фоне лечения также отмечается улучшение слуха, что, по–видимому, связано с вазоактивным действием препарата.
Бетасерк® эффективен как при болезни Меньера, так и при других вестибулярных расстройствах. Бетасерк® – препарат выбора для профилактики приступов головокружения. Его назначают в дозе 48 мг/сут, при этом продолжительность приема должна составлять не менее 2–3 мес. Более выраженный и длительный эффект отмечен при использовании более высоких доз препарата – до 24–72 мг 3 раза в сутки. Необходимо отметить, что фармакологической активностью обладает также один из метаболитов препарата Бетасерк 2,2–аминоэтилпиридин, что, вероятно, является одной из причин длительного положительного эффекта препарата.
Бетасерк не вызывает выраженных побочных эффектов, в редких случаях возникают легкие диспептические явления, кожные аллергические реакции и головная боль. В отличие от других вестибулолитических средств препарат не замедляет психомоторные реакции и может назначаться пациентам, деятельность которых связана с повышенным вниманием, в частности, с управлением транспортными средствами [3].
Учитывая тот факт, что в настоящее время имеется достаточно широкий спектр лекарственных препаратов, применяющихся в лечении головокружения, сравнение их фармакоэкономического аспекта применения явля-ется одной из важнейших и актуальных задач.
По данным доступной литературы, на сегодняшний день оценка фармакоэкономической приемлемости использования Бетасерка по сравнению с наиболее часто применяемыми препаратами в лечении головокружения (винпоцетин, ноотропы) у стационарных больных не проводились. Поэтому результаты данного клинического исследования имеют большое значение в выборе наиболее затратно–эффективной фармакотерапии головокружения в условиях стационара.
Целью данного исследования явилось установление затратной эффективности применения бетагистина (Бетасерка) при лечении системного головокружения в условиях стационара в сравнении с рутинной терапией.
Исходя из поставленной цели, для ее достижения нами были определены следующие задачи исследования:
1. Установление эффективности применения препарата Бетасерк® с использованием следующих параметров: выраженность вертиго (по результатам опросника DHI), частота приступов головокружения в сутки, длительность пребывания в стационаре (количество проведенных к/дней).
2. Оценка сравнительной эффективности препарата Бетасерк® по отношению к рутинной терапии системного головокружения в условиях стационара.
3. Оценка профиля безопасности препарата Бетасерк® при лечении системного головокружения в условиях стационара.
4. Установление фармакоэкономической приемлемости применения препарата Бетасерк в сравнении со стандартной терапией.
Исследование проведено на базе неврологических и терапевтических отделений ГКБ № 6 г. Москвы в течение марта–октября 2009 г.
Для стандартизации получаемой информации была разработана индивидуальная регистрационная карта.
В соответствии с дизайном исследования пациенты получали бетагистин (Бетасерк®) или винпоцетин в течение всего периода госпитализации по основному заболеванию (в среднем 14 дней).
39 пациентов получали бетагистин (Бетасерк®) перорально в таблетках, 60 пациентов – винпоцетин (в виде внутривенных инфузий или в таблетированной форме). Распределение на группы проводилось в зависимости от текущего применения бетагистина (Бета-серка) или винпоцетина.
Оценка эффективности терапии производилась на основании анализа жалоб пациентов (ежедневная оценка частоты приступов головокружения в течение суток), анкетирования пациентов для оценки головокружения и мнестических функций по шкале DHI на 1–й и 7–й день нахождения в стационаре и в день выписки пациента (10–14–е сутки). Также в день выписки пациента оценивались длительность пребывания в стационаре (количество к/дней), количество проведенных лабораторный и инструментальных обследований за время нахождения пациента в стационаре (ОАК, ОАМ, б/х анализ крови, ЭКГ, РЭГ, ЭЭГ, рентгенологические исследования, УЗДГ, АД–мониторирование, КТ).
Параллельно с оценкой эффективности бетагистина (Бетасерка) и винпоцетина проводилась сравнительная оценка их безопасности.
На протяжении всего периода наблюдения за пациентами проводилось активное выявление и регистрация нежелательных побочных реакций.
Оценка безопасности использования медикаментозной терапии боли оценивалась по частоте возникновения НПР и степени их выраженности.
Критерии включения в исследование:
• Наличие головокружения
• Возраст > 18 лет
• Полученное письменное информированное согласие.
Основные критерии исключения
Критерии, связанные с методологией исследования
1. Поражение вестибулярного анализатора центрального уровня следующего генеза:
– острый и хронический арахноидит,
– стволовой энцефалит,
– жидкие кисты мозжечка,
– опухоли мозжечка и ствола мозга,
– дегенеративные заболевания ЦНС,
– височная эпилепсия,
– ОНМК острый период.
2. Беременность
3. Кормление грудью
Критерии, связанные с Бетасерком (бетагистином):
1. Повышенная чувствительность к какому–либо из компонентов препарата.
2. Феохромоцитома.
3. Язвенная болезнь желудка и 12–перстной кишки в фазе обострения.
4. Бронхиальная астма.
Критерии, связанные с винпоцетином:
1. Гиперчувствительность.
2. Тяжелые формы ИБС и аритмии.
Бетасерк® (бетагистин) назначался по 24 мг 2 раза в сутки. Доза и длительность приема подбирались индивидуально в соответствии с реакцией на лечение.
Винпоцетин применялся внутрь по 5 мг 2–3 раза в сутки либо вводился внутривенно капельно 1 раз в сутки в дозе 10–25 мг.
Для оценки фармакоэкономической приемлемости применения препарата Бетасерк® использовался анализ «затраты–эффективность» – тип клинико–экономического анализа, при котором проводят сравнительную оценку результатов и затрат при двух и более вмешательствах, эффективность которых различна, а результаты измеряются в одних и тех же единицах (миллиметры ртутного столба, концентрация гемоглобина, число предотвращенных осложнений, годы сохраненной жизни и т.п.).
В качестве критерия эффективности была выбрана частота головокружений в сутки, а также оценка по шкале DHI. Расчет осуществляли на основании цен, взятых из прайс–листа ЗАО ЦВ Протек по состоянию на 01.11.2009 г. При проведении расчетов учитывались только прямые медицинские затраты.
При проведении расчетов показатель соотношения «затраты–эффективность» оценивался по формуле:
CER = DC,
Ef
где CER – соотношение «затраты–эффективность»,
DC – прямые затраты,
Ef – эффективность применения лекарственного средства.
Вся информация, внесенная в ИРК, вводилась в электронную базу данных и обрабатывалась с помощью компьютерной программы Microsoft Excel. Для кодирования ЛС использовалась рекомендуемая ВОЗ АТC (Anatomical Therapeutic Chemical) – классификация, согласно которой каждому препарату в соответствии с его химической структурой, принадлежностью к определенной терапевтической группе и показаниями к применению присваивался соответствующий АТС–код.
Полученные результаты обрабатывались с расчетом абсолютных и относительных величин с использованием пакета статистических программ «Statistica» фирмы «Statsoft», 1999. Кроме того, рассчитывались средние величины, ошибки средних величин и ошибки относительных величин. Использовались методы параметрической статистики (при нормальном распределении признаков) и непараметрической статистики (при ненормальном распределении признаков). Нормальность распределения признаков проверялась по тесту Колмогорова–Смирнова. При анализе межгрупповых различий в распределении качественных признаков использовался χχ2–критерий Пирсона.
При анализе межгрупповых различий в параметрических данных использовался критерий t или дисперсионный анализ (one–way ANOVA) с расчетом поправки Бонферрони для избежания ошибки первого типа, связанной с множественностью сравнений при дальнейшем погрупповом сравнении.
Все статистические тесты выполнялись для уровня статистической значимости р<0,05.
В исследование всего было включено 99 пациентов с головокружением, проходивших стационарное лечение в терапевтических и неврологических отделениях ГКБ №6 ДЗ г. Москвы. Больные были распределены случайным образом на 2 группы: 1) пациенты, получающие рутинную терапию по поводу головокружения (винпоцетин + ноотропы); 2) больные, получающие бетагистин (Бетасерк®, Эбботт Продактс).
В группу больных, получавших рутинную терапию, было включено 60 больных, из них 53 женщины и 7 мужчин (средний возраст – 60,0±5,7 лет). В 65% случаев основной причиной госпитализации была цереброваскулярная болезнь с системной гипертензией (ЦВБ с АГ, МКБ–10), 25% случаев – ТИА, 10% случаев – нарушения кровообращения в вертебробазилярном бассейне, связанные с патологией позвоночника (дорсопатии).
В группу больных, получавших терапию Бетасерком, было включено 39 человек, из них 30 женщин и 9 мужчин, средний возраст в группе 58,2±7,1 лет. В 76,4% случаев основной причиной госпитализации явилась ЦВБ с АГ, в 18,0% случаев – ТИА, в 5,1% случаев – нарушения кровообращения в вертебробазилярном бассейне, связанные с патологией позвоночника (дорсопатии) (табл. 1).
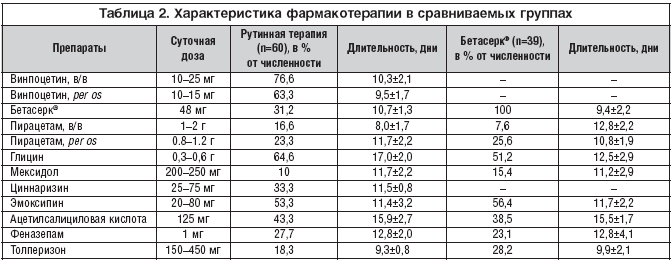
Комплекс фармакотерапии, использовавшейся у пациентов, был представлен, как показано в таблице 2.
Винпоцетин внутривенно капельно в суточной дозе 10–25 мг получали 38 пациентов, per os – 30 пациентов в суточной дозе 10–15 мг, 8 пациентов получали внутривенную инфузию и терапию per os. Средняя длительность лечения внутривенными инфузиями винпоцетина составила 10,3±2,1 дня, per os – 9,5±1,7 дня. 16,6% пациентов был дополнительно назначен пирацетам в виде внутривенных болюсных введений в течение в среднем 8,0±1,7 дня, 23,3% пациентов получали пирацетам per os в суточной дозе 800–1200 мг в течение в среднем 11,7±2,2 дней, 64,6% пациентов – глицин в суточной дозе 0,3–0,6 г в течение 17,0±2,0 дней, 10% пациентов – мексидол внутривенно болюсно в дозе 200–250 мг в среднем 11,7±2,2 дня, 33% пациентов – циннаризин в суточной дозе 25–75 мг в среднем 11,5±0,8 дня, 43,3% пациентов – ацетилсалициловую кислоту в дезагрегационной дозе 125 мг/сут. в среднем 15,9±2,7 дня, 53,3% пациентов – эмоксипин в дозе 20–80 мг/сут. внутривенно инфузионно в среднем 11,4±3,2 дня. Амитриптиллин был назначен 10% пациентов в суточной дозе 25–50 мг/сут. в среднем в течение 10,5±1,9 дня, феназепам – 27,7% пациентов в суточной дозе 1 мг в течение 12,8±2,0 дней. Миорелаксант толперизон использовался в фармакотерапии 18,3% пациентов в суточной дозе 150–450 мг в среднем в течение 9,3±0,8 дней. Кроме того, пациенты по показаниям получали гипотензивную терапию, витаминотерапию.
Пациентам, распределенным в группу лечения бетагистином, был назначен Бетасерк® в суточной дозе 48 мг в среднем в течение 9,4±2,2 дня (табл. 2). Кроме терапии Бетасерком, пациентам по показаниям была назначена следующая сопутствующая терапия: 7,6% пациентов – пирацетам в виде внутривенных болюсных введений в течение в среднем 12,8±2,2 дня, 25,6% пациентов – пирацетам per os в суточной дозе 800–1200 мг в течение в среднем 10,8±1,9 дня, 51,2% пациентов – глицин в суточной дозе 0,3–0,6 г в течение 12,5±2,9 дня, 15,4% пациентов – мексидол внутривенно болюсно в дозе 200–250 мг в среднем 11,2±2,9 дня, 38,5% пациентов – ацетилсалициловая кислота в дезагрегационной дозе 125 мг/сут в среднем 15,5±1,7 дня, 56,4% пациентов – эмоксипин в дозе 20–80 мг/сут внутривенно инфузионно в среднем 11,7±2,2 дня. Амитриптиллин был назначен 12,8% пациентов в суточной дозе 25–50 мг/сут в среднем в течение 12,8±3,9 дня, феназепам – 23,1% пациентов в суточной дозе 1 мг в течение 12,8±4,2 дня. Миорелаксант толперизон использовался в фармакотерапии 28,2% пациентов в суточной дозе 150–450 мг в среднем в течение 9,9±2,1 дней. Кроме того, пациенты по показаниям получали гипотензивную терапию, витаминотерапию.
Проведенный комплекс клинико–лабораторного, инструментального обследования и диагностических манипуляций в сравниваемых подгруппах достоверно не различался.
Фармакотерапия Бетасерком была эффективна у всех пациентов, что выразилось в снижении частоты приступов головокружения в день и выраженности вертиго, оцененного по опроснику DHI, достигавшего статистической достоверности к 7–му дню терапии. Таким образом, клиническая эффективность фармакотерапии в группе пациентов, получавших Бетасерк®, составила 100%.
Обращает на себя внимание тот факт, что в связи с неэффективностью проводимой терапии головокружения в группе рутинной терапии в виде отсутствия динамики объективной симптоматики 19 пациентам (31,2% больных) к проводимому комплексу рутинной терапии в среднем через 5,2±1,2 дня был добавлен Бетасерк® в дозе 48 мг/сут. Таким образом, клиническая эффективность рутинной терапии составила 68,8%.
Средняя длительность пребывания в стационаре в группе рутинной терапии составила 17,3±4,1 дня, в группе Бетасерка – 17,3±3,8 дня, в связи с этим стоимость т.н. «гостиничных услуг» при расчете фармакоэкономических показателей в сравниваемых группах не учитывалась.
Среднее количество эпизодов головокружения в группе, получавшей рутинную терапию, составила в начале лечения 6,9±1,9 эпизода, через 7 дней терапии – 3,4±0,8 эпизода, при выписке – 1,9±1,2 эпизода.
Вновь необходимо подчеркнуть, что у 19 пациентов частота эпизодов головокружения в связи с проводимой терапией не снижалась, в связи с чем в среднем через 5,2±1,2 дня этим пациентам был назначен Бетасерк® в дозе 48 мг в сутки.
В результате оценки состояния пациентов по шкале DHI было установлено следующее. Исходная оценка по шкале DHI в данной группе составила 59,7±8,2 балла, через 7 дней – 44,7±5,8 балла, при выписке 39,4±3,2 балла. Нежелательных явлений в группе не отмечалось (рис. 1 и 2).
Среднее количество эпизодов головокружения в группе, получавшей Бетасерк®, составило в начале лечения 8,6±2,2 эпизода, через 7 дней терапии – 3,8±0,9 эпизода, при выписке – 1,9±0,8 эпизода.
В результате оценки состояния пациентов по шкале DHI было установлено следующее. Исходная оценка по шкале DHI в данной группе составила 59,9±9,2 балла, через 7 дней – 45,4±5,8 балла, при выписке 36,4±7,8 балла. Нежелательных явлений в группе не отмечалось (рис. 1 и 2).
Таким образом, на момент выписки из стационара клиническая эффективность и безопасность проведенной фармакотерапии в сравниваемых группах пациентов статистически достоверно не различались. При этом необходимо вновь подчеркнуть, что сравнимость эффектов была достигнута только после дополнительного назначения части пациентов (31,2% больных), получавших рутинную терапию, Бетасерка в дозе 48 мг/сут.
Однако при оценке прямых затрат, включавших затраты на лекарственную терапию, инфузионные растворы, шприцы, системы для инфузий, установлено, что средние затраты на 1 пациента в группе больных, получавших рутинную терапию, составили 959,3±81,3 рубля, а в группе больных, получавших Бетасерк®, 957,9±75,8 рубля. Достаточно значимую часть в структуре затрат (до 15%) составляют затраты на инфузионные растворы, системы для инфузий, шприцы. Таким образом, изначально более дорогостоящая лекарственная технология (Бетасерк®, по стоимости за упаковку) при совокупной оценке всех затрат оказалась равной по связанным с ее применением затратам по отношению к изначально более дешевой терапии. Более того, учет суммарных затрат в среднем на 1 пациента в случае, если предположить, что при внутривенном введении использовался раствор винпоцетина (рутинная терапия 2), составят 1115,7±82,9 рубля. Таким образом, затраты при лечении Бетасерком статистически достоверно меньше, чем при использовании рутинной фармакотерапии, в которой назначаются в комплексе генерический винпоцетин внутрь и винпоцетин в виде внутривенных инфузий (р<0,05).
На основании полученных результатов были рассчитаны коэффициенты затраты–эффективность для сравниваемых лекарственных технологий:
CER рутинная терапия 1= 959,3/68,8%=13,94 руб./%
CER рутинная терапия 2= 1115,7/68,8%=16,22 руб./%
CER Бетасерк®= 957,9/100%=9,57 руб./%
Следовательно, при лечении головокружения в условиях стационара наиболее предпочтительной с точки зрения клинической эффективности и фармакоэкономической приемлемости является фармакотерапия Бетасерком.
Выводы
Использование Бетасерка в суточной дозе 48 мг в комплексе фармакотерапии головокружения в условиях стационара клинически эффективно и безопасно.
Клинически значимое уменьшение частоты приступов головокружения и статистически значимое снижение оценки по шкале DHI отмечается в 100% случаев при использовании Бетасерка в дозе 48 мг и в 68,8% случаев при назначении т.н. «рутинной» терапии головокружения.
Использование Бетасерка в терапии системного головокружения в условиях стационара более затратно–эффективно по сравнению с использованием рутинной фармакотерапии, в том числе той, при проведении которой назначаются в комплексе генерический винпоцетин внутрь и винпоцетин в виде внутривенных инфузий.



Литература
1. Oosterveld W.J. Current diagnostic techniques in vestibular disorders// Acta Otolaryngol (Stockh).–1991.– Vol. 479 (Suppl.).– P. 29–34
2. Вейс Г. Головокружение / В кн.: «Неврология». Под ред. М. Самуэльса. М.: Практика, 1997.– С. 94–120
3. Лавров А.Ю. Применение бетасерка в неврологической практике // Неврол. журн.– 2001.– Т. 6.– №2
4. Воробьев П.А., Авксентьева М.В., Юрьев А.С., Сура М.В. Клинико–экономический анализ. // Ньюдиамед, М. – 2004












