Боль при диабетической полиневропатии (ДПН) – самый распространенный вариант нейропатического типа боли, который имеет свои клинические отличия и подходы к терапии [1–4]. У больных ДПН она встречается в 25–45% случаев. Причиной боли является поражение тонких сенсорных волокон, ответственных за болевую чувствительность. Важными механизмами в развитии этого типа боли являются периферическая и центральная сенситизация, генерация импульсов из эктопических очагов пораженных нервов, избыточная экспрессия потенциал–зависимых натриевых каналов периферических нейронов и др. [5–7]. Нейропатическая боль при ДПН характеризуется сочетанием позитивных и негативных сенсорных феноменов. Типичными жалобами являются покалывание и онемение в стопах и голенях, усиливающихся в ночное время. В то же время у больных могут возникать резкие, стреляющие, ланцинирующие, пульсирующие и жгучие боли. У части пациентов отмечаются аллодиния и гиперестезия.
Терапия боли, обусловленной диабетическим поражением периферической нервной системы, является трудной задачей. Прогрессирование ДПН во многом зависит от тяжести диабета. Поэтому очень важно строго контролировать уровень гликемии и проводить комплексное лечение ДПН (a–липоевая кислота, бенфотиамин, сосудистая терапия и др.). В лечении боли применяют различные нелекарственные методы лечения (хирургическая декомпрессия малоберцового нерва, лазерная терапия, акупунктура, магнитотерапия, биологическая обратная связь, чрескожная электронейростимуляция, массаж и др.), эффективность которых остается недоказанной. В настоящее время в лечении нейропатической боли наиболее эффективной является лекарственная терапия [7–9]. Следует сразу подчеркнуть, что простые анальгетики и нестероидные противовоспалительные препараты в лечении болей при ДПН не рекомендуются из–за их неэффективности. К сожалению, в мире более 60% больных с нейропатической болью по–прежнему получают эти препараты, что недопустимо и чрезвычайно опасно при длительном применении (осложнения со стороны ЖКТ, печени и крови).
Основными группами препаратов для лечения нейропатической боли при ДПН являются: антидепрессанты, антиконвульсанты и опиоидные анальгетики [7–9]. Контроль боли с помощью средств, активирующих нисходящие антиноцицептивные системы (опиоидной, серотонинергической, норадренергической), является одним из мощных направлений в фармакотерапии нейропатической боли. Среди них особое место занимают опиоидные анальгетики. Однако опасения, связанные с развитием зависимости, и ряд побочных явлений ограничивали применение этой группы лекарственных средств в широкой амбулаторной практике. С появлением трамадола ситуация существенно изменилась. Он показал свою эффективность и безопасность в лечении самых разнообразных болевых синдромов. Однако в последние годы еще более привлекательным стал комбинированный анальгетик, содержащий трамадол и парацетамол, обеспечивающий более высокую степень обезболивания.
В настоящей работе приведено исследование эффективности и безопасности препарата Залдиар в лечении нейропатической боли у больных с ДПН. Залдиар – это комбинированный таблетированный препарат, содержащий в одной таблетке трамадол 37,5 мг и парацетамол 325 мг. Трамадол – синтетический анальгетик, представляющий собой смесь двух изомеров, обладающих взаимодополняющими механизмами действия. Один изомер взаимодействует с опиоидными m–, d– и k–рецепторами, с большей тропностью к m–рецепторам. Другой – ингибирует обратный захват норадреналина и серотонина, активируя нисходящие антиноцицептивные влияния. Синергизм двух механизмов действия трамадола обусловливает его высокую эффективность. Парацетамол обладает обезболивающим и жаропонижающим действием. Считается, что он блокирует циклооксигеназу в центральной нервной системе. Однако в последних работах показано, что парацетамол обладает особым действием на канабиноидные рецепторы, что по–новому объясняет его анальгетическую эффективность [10]. При применении Залдиара благодаря парацетамолу наступает быстрое обезболивание, в то время как трамадол обеспечивает пролонгированный эффект. Синергизм анальгетического действия двух активных веществ увеличивает обезболивающий эффект и снижает риск возникновения побочных эффектов.
Материал и методы исследования
В исследование были включены 30 больных сахарным диабетом 2 типа, имеющих нейропатическую боль. Критериями включения были: мужчины и женщины в возрасте от 35 до 75 лет, наличие диабетической полиневропатии, подтверждение нейропатического типа боли по опроснику DN4, интенсивность боли не менее 5 баллов по визуальной аналоговой шкале (ВАШ), продолжительность болевого синдрома не менее 3 мес. Критерии исключения: декомпенсированный сахарный диабет, тяжелые сопутствующие заболевания сердца, печени и почек, повышенная чувствительность к Залдиару, наличие зависимостей или склонности к ним.
Методы исследования включали: клинический неврологический анализ, оценку интенсивности боли по ВАШ, оценку нейропатического болевого синдрома по анкете DN4, субъективную оценку сна, анализ эффективности лечения по субъективному отчету больных.
Терапия назначалась методом подбора от 1 до 4 таблеток в сутки в течение 10 дней. Через 10 дней после отмены препарата также анализировали интенсивность боли по ВАШ. На протяжении всех дней приема препарата проводился анализ интенсивности болевого синдрома по ВАШ. Все пациенты находились на монотерапии Залдиаром и не получали других препаратов, используемых для лечения боли. Анкетирование с помощью опросника DN4 проводилось до и после лечения. Основная оценка эффективности лечения проводилась по ВАШ на момент последнего визита и через 10 дней после отмены препарата.
Результаты исследования
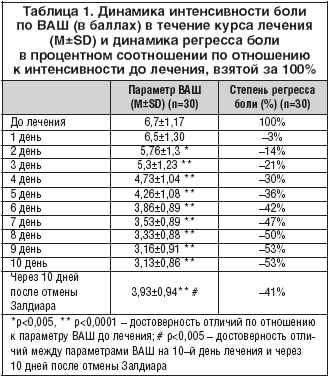
Средний возраст исследуемых пациентов был 66,5±11,2 лет, из них 67% женщин, 33% мужчин. Длительность сахарного диабета была в среднем 8,06±5,8 лет. Длительность ДПН – 15,9±11,6 месяцев. На инсулинотерапии находились 60% больных, 40% принимали пероральные сахароснижающие препараты. По опроснику нейропатической боли DN4 суммарный балл до лечения составил 6,03±1,15. Интенсивность боли по ВАШ до лечения была 6,7±1,17 баллов.
В таблице 1 представлены значения интенсивности боли по ВАШ до лечения, на протяжении 10 дней приема Залдиара и через 10 дней после отмены препарата. Достоверное снижение боли отмечено на второй день терапии и в дальнейшем на протяжении всего курса лечения. Для оценки динамики редукции болевого синдрома был проведен анализ сдвигов по ВАШ в процентах по отношению к интенсивности боли до лечения, взятого за 100% (табл. 1). К четвертому дню лечения было достигнуто клинически значимое для пациентов уменьшение боли (на 30%). Редукция болевого синдрома на 50% отмечена на 8–й день терапии. Следует отметить, что интенсивность боли через 10 дней после отмены Залдиара увеличилась по отношению к значению ВАШ на 10–й день терапии, но была достоверно ниже по сравнению с интенсивностью боли до лечения.
В результате терапии уменьшение боли на 50% и более отмечено у 23 больных, у остальных зафиксировано снижение боли не менее чем на 30%.
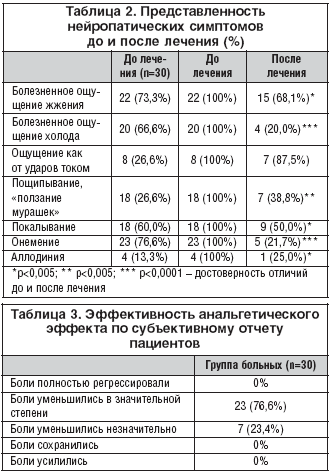
Суммарный бал по опроснику DN4 к концу терапии составил 3,93±0,94, что достоверно ниже, чем до начала лечения 6,04±1,15 (p<0,0001). В таблице 2 приведен анализ нейропатических симптомов до и после лечения. Можно отметить достоверное снижение представленности большинства проявлений нейропатической боли.
Больным также предлагалось самостоятельно оценить обезболивающий эффект препарата по шкале субъективных впечатлений (табл. 3). В целом, по итогам 10 дней лечения 76,6% пациентов отметили значительное уменьшение боли. О том, что боли уменьшились незначительно, сообщили 23,4% больных. Ни у одного больного не было отмечено усиления боли.
Положительный эффект отмечался у больных на разных дозах препарата. На одной таблетке в сутки положительный эффект отмечался у 16,6% больных, на двух таблетках – у 44,3%, на трех таблетках в сутки – у 26,6%, на 4 таблетках – у 10% больных. В большинстве случаев (73%) положительный эффект наблюдался на приеме 2–3 таблеток в сутки и отмечался на 2–4 день терапии. В дальнейшем этим больным не приходилось увеличивать дозу Залдиара.
В процессе терапии не было отмечено серьезных побочных явлений. У 30% пациентов отмечалась некоторая сонливость, что рассматривалось положительно самими больными, так как у них боли чаще отмечались ночью. Практически все пациенты (90%) на фоне проводимой терапии отмечали улучшение сна: быстрее засыпали, реже пробуждались, были удовлетворены сном.
Обсуждение
В развитии периферической нейропатической боли при ДПН участвуют разные периферические механизмы: периферическая сенситизация, эктопическая активность, экспрессия потенциал–зависимых натриевых каналов. Однако, как при любой хронической боли, существенную роль играют и центральные нарушения: центральная сенситизация, феномен «взвинчивания», изменение нисходящих, модулирующих боль влияний и др. Поэтому в лечении нейропатической боли все чаще обсуждается комбинированное применение препаратов, способных повлиять на разные уровни и механизмы формирования боли (антидепрессанты, антиконвульсанты, опиоидные анальгетики, местные анестетики) [7–9]. К сожалению, практически у всех этих средств есть те или иные побочные реакции. Наиболее трудным в этой ситуации является выбор средств, позволяющих достичь наилучшего обезболивающего эффекта при минимальном риске побочных эффектов.
Опиоиды издавна применяются для лечения умеренной или сильной боли. Они ценятся за их болеутоляющие свойства, но препараты этого класса вызывают в организме и другие эффекты. Опиоиды действуют на систему дыхания, сердечную деятельность, желудочно–кишечный тракт и мочевыводящую систему, вызывая потенциально опасные побочные явления. Обезболивание с помощью опиоидов также связано с проблемами толерантности к лекарственным препаратам и развития физической зависимости, а также с психологическими побочными эффектами. Именно поэтому классические наркотические анальгетики не нашли широкого применения в лечении болевой формы ДПН. Кроме того, некоторое время тому назад были высказаны предположения о неэффективности опиоидных анальгетиков при нейропатических болях. Однако в последующих работах эти гипотезы были обоснованно опровергнуты. За последние годы отношение к применению этой группы средств существенно изменилось. Это связано с разработкой опиоидных анальгетиков, не имеющих опасных побочных реакций и не вызывающих зависимость. Таким препаратом является трамадол, который хорошо зарекомендовал себя в лечении боли при ДПН [11–13]. Однако появление комбинированного препарата, содержащего в одной таблетке трамадол и парацетамол (Залдиар), оказалось еще более привлекательным для лечения по нескольким причинам. Во–первых, эффект наступает быстрее (за счет парацетамола) и держится дольше (за счет трамадола). Во–вторых, доза трамадола при курсовом лечении может быть снижена, при повышении обезболивающего эффекта вследствие потенцирующего действия двух лекарственных компонентов. В–третьих, как известно, у парацетамола, наряду с известными свойствами, выявлены новые механизмы действия (опосредованное влияние на канабиноидные рецепторы), играющие существенную роль в контроле боли [10,14,15].
В проведенных ранее клинических исследованиях было показано, что сочетание трамадола и парацетамола дает достоверно больший эффект при лечении боли, чем эти компоненты в отдельности, и что трамадол/парацетамол сокращают время наступления анальгезии и улучшают переносимость по сравнению с трамадолом в отдельности. Мета–анализ семи двойных слепых плацебо–контролируемых исследований по применению указанного комбинированного анальгетика установил, что показатель NNT (number–needed–to–treat), т.е. количество пациентов, которых нужно пролечить, чтобы у одного из них боль уменьшилась не менее чем на 50%, составил 2,6 для комбинированного препарата и 9,9 для монотерапии трамадолом больных с зубной болью [16]. У пациентов с постоперационной болью NNT составил соответственно 2,8 (для трамадола/парацетамола) и 4,4 (для трамадола) [17]. Дополнительные клинические исследования показали эффективность и безопасность совокупной дозы трамадола/парацетамола для лечения хронической скелетно–мышечной боли, включающей боль в спине, боль при остеоартритах и фибромиалгии [18–20]. Недавно опубликованы результаты двойного плацебо–контролируемого исследования, в котором была продемонстрирована высокая эффективность комбинированного анальгетика трамадол/парацетамол в лечении боли при ДПН на протяжении 66 дней терапии [21].
Проведенное нами исследование показало высокую эффективность короткого курса лечения боли при ДПН препаратом Залдиар. Было установлено, что комбинация «трамадол 37,5 мг/парацетамол 325 мг» является эффективной и имеет предпочтительный профиль безопасности для лечения нейропатической боли при ДПН. Особо следует подчеркнуть, что положительные сдвиги отмечались уже со второго и третьего дней терапии. В большинстве случаев суточная доза составляла 2–3 таблетки в сутки, на фоне которых отмечалось существенное уменьшение проявлений нейропатического болевого синдрома. Таким образом, у большинства пациентов положительные результаты были получены при суточной дозе трамадола 75–112,5 мг и парацетамола 650–975 мг. Следует отметить хорошую переносимость Залдиара и отсутствие побочных явлений, что опровергает миф о неблагоприятном профиле безопасности трамадола. Важно подчеркнуть, что после отмены препарата не наблюдалось синдрома отмены. Интенсивность боли через 10 дней после отмены препарата увеличилась по сравнению со значением ВАШ на 10–й день терапии, однако оставалась существенно более низкой по отношению к параметру ВАШ до лечения.
Таким образом, полученные в нашей работе данные позволяют рассматривать Залдиар как безопасное и эффективное обезболивающее средство и рекомендовать его в качестве препарата выбора для лечения нейропатического болевого синдрома при ДПН. Вероятно, сроки терапии больных с нейропатической болью при ДПН не должны ограничиваться 10 днями. Но в этом исследовании нам удалось показать, что даже короткий курс лечения Залдиаром способен быстро и существенным образом снизить интенсивность проявлений нейропатического болевого синдрома, что чрезвычайно важно для этой категории больных, страдающих на протяжении многих месяцев и лет. Следует особо подчеркнуть, что для достижения положительного результата не пришлось использовать высокие дозы препарата: большинство больных были удовлетворены эффектом на фоне 2–3 таблеток в сутки. Таким образом, быстрота наступления эффекта обезболивания, хорошая переносимость и отсутствие побочных явлений делает Залдиар весьма привлекательным для лечения этой труднокурабельной формы патологии.
Литература
1. Данилов А.Б., Давыдов О.С. Нейропатическая боль. Москва: Боргес, 2007. 190 с.
2. Анисимова Е.И., Данилов А.Б. Нейропатический болевой синдром: клинико–нейрофизиологический анализ. Журн. Неврол. Психиатр. Им. С.С.Корсакова, 2003, 103(10):15–20.
3. Строков И. А., Баринов А. Н. Клиника, патогенез и лечение болевого синдрома при диабетической полиневропатии // Неврол. журн – 2001. – № 6. – С. 47–55.
4. Dyck PJ, Kratz KM, Karnes JL, et al. The prevalence by staged severity of various types of diabetic neuropathy,retinopathy, and nephropathy in a population–based cohort: the Rochester Diabetic Neuropathy Study. Neurology 1993;43:817–24.
5. Partanen J, Niskanen L, Lehtinen J, et al. Natural history of peripheral neuropathy in patients with non–insulin–dependent diabetes mellitus. N Engl J Med 1995;333:89–94.
6. Craner MJ, Klein JP, Renganathan M, et al. Changes of sodium channel expression in experimental painful diabetic neuropathy. Ann Neurol 2002;52:786–92.
7. Dworkin RH. An overview of neuropathic pain: syndromes, symptoms, signs, and several mechanisms. Clin J Pain 2002;18:343–9.
8. Dworkin RH, Backonja M, Rowbotham MC, et al. Advances in neuropathic pain: diagnosis, mechanisms, and treatment recommendations. Arch Neurol 2003;60:1524–34.
9. Jensen TS. Anticonvulsants in neuropathic pain: rationale and clinical evidence. Eur J Pain 2002;6(Suppl A):61–8.
10. Bertolini A, Ferrari A, Ottani A, et al. Paracetamol: new vistas of an old dru. CNS Drug Rev. 2006 Fall–Winter;12(3–4):250–75.
11. Harati Y, Gooch C, Swenson M, et al. Double–blind randomized trial of tramadol for the treatment of the pain of diabetic neuropathy. Neurology 1998;50:1842–6.
12. Harati Y, Gooch C, Swenson M, et al. Maintenance of the long–term effectiveness of tramadol in treatment of the pain of diabetic neuropathy. J Diabetes Complications 2000;14:65–70.
13. Sindrup SH, Andersen G, Madsen C, et al. Tramadol relieves pain and allodynia in polyneuropathy: a randomised, doubleblind, controlled trial. Pain 1999;83:85–90.
14. Warner TD, Vojnovic I, Giuliano F, et al. Cyclooxygenases 1, 2, and 3 and the production of prostaglandin I2: investigating the activities of acetaminophen and cyclooxygenase?2–selective inhibitors in rat tissues. J Pharmacol Exp Ther 2004;310:642–7.
15. Raffa RB, Walker EA, Sterious SN. Opioid receptors and acetaminophen (paracetamol). Eur J Pharmacol 2004;503:209–10.
16. Fricke JR, Jr., Hewitt DJ, Jordan DM, et al. A double–blind placebo–controlled comparison of tramadol/acetaminophen and tramadol in patients with postoperative dental pain. Pain 2004;109:250–7.
17. Edwards JE, McQuay HJ, Moore RA. Combination analgesic efficacy: individual patient data meta–analysis of single–dose oral tramadol plus acetaminophen in acute postoperative pain. J Pain Symptom Manage 2002;23:121–30.
18. Mullican WS, Lacy JR. Tramadol/acetaminophen combination tablets and codeine/acetaminophen combination capsules for the management of chronic pain: a comparative trial. Clin Ther 2001;23:1429–45.
19. Ruoff GE, Rosenthal N, Jordan D, et al. Tramadol/acetaminophen combination tablets for the treatment of chronic lower back pain: a multicenter, randomized, double–blind, placebo–controlled outpatient study. Clin Ther 2003;25:1123–41.
20. Peloso PM, Fortin L, Beaulieu A, et al. Analgesic efficacy and safety of tramadol/ acetaminophen combination tablets (Ultracet) in treatment of chronic low back pain: a multicenter, outpatient, randomized, double blind, placebo controlled trial. J Rheumatol 2004;31:2454–63.
21. Freeman R, Raskin P, Hewitt DJ, et al. Randomized study of tramadol/acetaminophen versus placebo in painful diabetic peripheral neuropathy. Current Medical Research and Opinion Vol. 23, No.1, 2007, 147–161.












