–Я—А–Є—З–Є–љ—Л –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤
–Я—А–Є—З–Є–љ–∞–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Љ–Њ–≥—Г—В –±—Л—В—М –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–µ –Є —Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Є–µ –Є –і–Є—Б–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, –љ–µ–є—А–Њ–Є–љ—Д–µ–Ї—Ж–Є–Є –Є –і—А—Г–≥–Є–µ –њ–∞—В–Њ–ї–Њ–≥–Є–Є (—В–∞–±–ї. 1). –Т–Њ –Љ–љ–Њ–≥–Є—Е —Б–ї—Г—З–∞—П—Е –≤ –Њ—Б–љ–Њ–≤–µ –і–µ–Љ–µ–љ—Ж–Є–Є –ї–µ–ґ–∞—В –і–≤–∞ –Є –±–Њ–ї–µ–µ —Б–Њ—Б—В–Њ—П–љ–Є—П, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ – —Б–Њ—З–µ—В–∞–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ (–С–Р) —Б –і—А—Г–≥–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [2].
–Э–∞–±–ї—О–і–∞—О—Й–Є–є—Б—П –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –і–µ—Б—П—В–Є–ї–µ—В–Є—П —А–Њ—Б—В —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ–Њ—Б—В–∞—А–µ–љ–Є–µ–Љ –љ–∞—Б–µ–ї–µ–љ–Є—П [1, 4]. –Э–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —В–Є–њ–Њ–Љ –і–µ–Љ–µ–љ—Ж–Є–Є —Г –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є —П–≤–ї—П–µ—В—Б—П –С–Р, –і–∞–ї–µ–µ —Б–ї–µ–і—Г–µ—В –і–µ–Љ–µ–љ—Ж–Є—П —Б —В–µ–ї—М—Ж–∞–Љ–Є –Ы–µ–≤–Є [5, 6]. «–І–Є—Б—В–∞—П» —Б–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–Љ–µ–љ—Ж–Є—П –≤—Б—В—А–µ—З–∞–µ—В—Б—П —А–µ–і–Ї–Њ, –Њ–і–љ–∞–Ї–Њ —Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –≤–Ї–ї—О—З–∞—П —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ—А–∞–ґ–µ–љ–Є—П, «–љ–µ–Љ–Њ–є» –Є–љ—Д–∞—А–Ї—В –Љ–Њ–Ј–≥–∞ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є —П–≤–љ—Л–є –Є–љ—Б—Г–ї—М—В, —П–≤–ї—П—О—В—Б—П –≤–∞–ґ–љ—Л–Љ–Є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є, –≤–љ–Њ—Б—П—Й–Є–Љ–Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–є –≤–Ї–ї–∞–і –≤ —Г—Е—Г–і—И–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є —Д—Г–љ–Ї—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і—А—Г–≥–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є [2].
–†–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –њ–Њ–≤—Л—И–∞–µ—В—Б—П –њ—А–Є —А—П–і–µ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –њ–∞—В–Њ–ї–Њ–≥–Є–є, –≤ —В. —З. —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е, —Б–∞—Е–∞—А–љ–Њ–Љ –і–Є–∞–±–µ—В–µ –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–Љ —Б–Є–љ–і—А–Њ–Љ–µ, –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П—Е —Й–Є—В–Њ–≤–Є–і–љ–Њ–є –ґ–µ–ї–µ–Ј—Л, –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї, –≥–Є–њ–µ—А—Е–Њ–ї–µ—Б—В–µ—А–Є–љ–µ–Љ–Є–Є –Є –≥–Є–њ–µ—А–≥–Њ–Љ–Њ—Ж–Є—Б—В–µ–Є–љ–µ–Љ–Є–Є, –і–µ—Д–Є—Ж–Є—В–µ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т, —Б–Є–љ–і—А–Њ–Љ–µ –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–≥–Њ –∞–њ–љ–Њ—Н —Б–љ–∞, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–Љ –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є –ї–µ–≥–Ї–Є—Е, –∞–љ–µ–Љ–Є–Є –Є —А—П–і–µ –і—А—Г–≥–Є—Е [5].
–Ы–µ—З–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤
–Ы–µ—З–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –≤ —В–µ—Е —Б–ї—Г—З–∞—П—Е, –Ї–Њ–≥–і–∞ —Н—В–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –љ–∞ —Г—Б—В—А–∞–љ–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ—Л. –Э–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –љ–µ–є—А–Њ–Є–љ—Д–µ–Ї—Ж–Є—П—Е –≥–ї–∞–≤–љ–∞—П —А–Њ–ї—М –њ—А–Є–љ–∞–і–ї–µ–ґ–Є—В —Н—В–Є–Њ—В—А–Њ–њ–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–є –љ–∞ —Н—А–∞–і–Є–Ї–∞—Ж–Є—О –≤–Њ–Ј–±—Г–і–Є—В–µ–ї—П, –њ—А–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є – –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є – –њ—А–µ–њ–∞—А–∞—В–∞–Љ, —Г–ї—Г—З—И–∞—О—Й–Є–Љ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О, –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ – –љ–Є–Ј–Ї–Є–Љ (–і–Њ 500 –Љ–≥) –і–Њ–Ј–∞–Љ –ї–µ–≤–Њ–і–Њ–њ—Л –Є —В. –і. [2, 3]. –Я—А–Є –љ–∞–ї–Є—З–Є–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ–∞—В–Њ–ї–Њ–≥–Є–є –ї–µ—З–µ–љ–Є–µ –і–Њ–ї–ґ–љ–Њ –±—Л—В—М –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞–њ—А–∞–≤–ї–µ–љ–Њ –љ–∞ —Г—Б—В—А–∞–љ–µ–љ–Є–µ —Д–∞–Ї—В–Њ—А–Њ–≤, –≤–љ–Њ—Б—П—Й–Є—Е –љ–∞–Є–±–Њ–ї—М—И–Є–є –≤–Ї–ї–∞–і –≤ —А–∞–Ј–≤–Є—В–Є–µ –і–µ–Љ–µ–љ—Ж–Є–Є [2]. –С–Њ–ї–µ–Ј–љ—М-–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ—А–Є –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В, –њ–Њ—Н—В–Њ–Љ—Г –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –њ—А–Њ–≤–Њ–і–Є—В—Б—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–µ –Є –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–µ–µ –ї–µ—З–µ–љ–Є–µ. –°—А–µ–і–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞–Є–±–Њ–ї–µ–µ —Е–Њ—А–Њ—И–Њ –Є–Ј—Г—З–µ–љ—Л –Є–љ–≥–Є–±–Є—В–Њ—А—Л —Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј—Л (–Є–•–≠) (–∞–љ—В–Є—Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞) –Є –Љ–µ–Љ–∞–љ—В–Є–љ.
–Ш–љ–≥–Є–±–Є—В–Њ—А—Л —Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј—Л
–Ю—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є–•–≠ –њ–Њ—Б–ї—Г–ґ–Є–ї–∞ «—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–Њ—В–µ–Ј–∞», —Б–Њ–≥–ї–∞—Б–љ–Њ –Ї–Њ—В–Њ—А–Њ–є –≤–∞–ґ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–Є–Љ —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –Є –њ—А–Є –С–Р, —П–≤–ї—П–µ—В—Б—П –і–µ—Д–Є—Ж–Є—В –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞ –≤ –¶–Э–°, –∞ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ –µ–≥–Њ –Ј–∞–њ–∞—Б–Њ–≤ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є [7]. –≠—В–∞ –≥–Є–њ–Њ—В–µ–Ј–∞ –њ–Њ–ї—Г—З–Є–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –≤ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.
–Є–•–≠ —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –С–Р –ї–µ–≥–Ї–Њ–є/—Г–Љ–µ—А–µ–љ–љ–Њ–є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є. –Ю–і–љ–∞–Ї–Њ –њ—А–Є –ї–µ–≥–Ї–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–•–≠, –њ–Њ –і–∞–љ–љ—Л–Љ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–∞, –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –њ–Њ–ї—М–Ј–Њ–є, –Ї–Њ—В–Њ—А—Г—О —Б–ї–µ–і—Г–µ—В —Б–Њ–њ–Њ—Б—В–∞–≤–ї—П—В—М —Б —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л—Е [8]. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б—В—А–∞–љ–∞—Е –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —В–∞–Ї–ґ–µ –Њ–і–Њ–±—А–µ–љ–Њ –њ—А–Є —В—П–ґ–µ–ї–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –Њ–і–љ–∞–Ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–•–≠ —Г —Н—В–Є—Е –±–Њ–ї—М–љ—Л—Е –њ–Њ–і–≤–µ—А–≥–∞–µ—В—Б—П —Б–Њ–Љ–љ–µ–љ–Є—О [5].
–Я—А–µ–њ–∞—А–∞—В—Л –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л —В–∞–Ї–ґ–µ —Г–ї—Г—З—И–∞—О—В –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–Ј–љ—М—О –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ –Є –і–µ–Љ–µ–љ—Ж–Є–µ–є —Б —В–µ–ї—М—Ж–∞–Љ–Є –Ы–µ–≤–Є, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –љ–µ–і–∞–≤–љ–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–≥–Њ –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–∞ 10 –†–Ъ–Ш [9]. –Я—А–Є –і–µ–Љ–µ–љ—Ж–Є–Є —Б —В–µ–ї—М—Ж–∞–Љ–Є –Ы–µ–≤–Є –Њ–љ–Є —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—В —Г–ї—Г—З—И–µ–љ–Є—О –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ [10].
–Ф–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ–± —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–•–≠ –њ—А–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л –Є –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л [11, 12]. –Т –њ–Њ—Б–ї–µ–і–љ–Є—Е –Ї–∞–љ–∞–і—Б–Ї–Є—Е —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є—П—Е, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л—Е –≤ 2014 –≥., –њ—А–µ–њ–∞—А–∞—В—Л —Н—В–Њ–є –≥—А—Г–њ–њ—Л —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –і–µ–Љ–µ–љ—Ж–Є–Є —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–Њ–Љ (–љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —В–Є–њ–Њ–Љ –і–µ–Љ–µ–љ—Ж–Є–Є —Б–Љ–µ—И–∞–љ–љ–Њ–≥–Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞), –љ–Њ –љ–µ «—З–Є—Б—В–Њ–є» —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є [2]. –£–±–µ–і–Є—В–µ–ї—М–љ—Л—Е –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–•–≠ –њ—А–Є –Ы–Т–Ф –љ–µ –њ–Њ–ї—Г—З–µ–љ–Њ, –±–Њ–ї–µ–µ —В–Њ–≥–Њ, –µ—Б—В—М –і–∞–љ–љ—Л–µ, —З—В–Њ –Њ–љ–Є –Љ–Њ–≥—Г—В —Г—Е—Г–і—И–∞—В—М —Г —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л [13]. –Ґ–∞–Ї–ґ–µ –љ–µ—В –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–•–≠ –њ—А–Є –і—А—Г–≥–Є—Е –љ–µ–є—А–Њ–Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е.
–Ф–∞–љ–љ—Л–µ –Њ –≤–ї–Є—П–љ–Є–Є –Є–•–≠ –љ–∞ –Њ—В–і–∞–ї–µ–љ–љ—Л–µ –Є—Б—Е–Њ–і—Л, —В–∞–Ї–Є–µ –Ї–∞–Ї –Ј–∞–Љ–µ–і–ї–µ–љ–Є–µ –љ–∞—А—Г—И–µ–љ–Є–є –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–≥–Њ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є—П –Є —Г–і–ї–Є–љ–µ–љ–Є–µ —Б—А–Њ–Ї–∞ –і–Њ –њ–Њ–Љ–µ—Й–µ–љ–Є—П –≤ —Б–њ–µ—Ж–Є–∞–ї–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–µ —Г—З—А–µ–ґ–і–µ–љ–Є—П –њ–Њ —Г—Е–Њ–і—Г, –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л [14].
–Є–•–≠ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —З–∞—Б—В–Њ –≤—Л–Ј—Л–≤–∞—О—В –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л —Б–Њ —Б—В–Њ—А–Њ–љ—Л –Ц–Ъ–Ґ (—В–Њ—И–љ–Њ—В–∞, —А–≤–Њ—В–∞, –і–Є–∞—А–µ—П, –њ–Њ—В–µ—А—П –∞–њ–њ–µ—В–Є—В–∞, —Б–љ–Є–ґ–µ–љ–Є–µ –≤–µ—Б–∞) –љ–∞–±–ї—О–і–∞—О—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ —Г 10–15% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [3]. –°–µ—А—М–µ–Ј–љ—Л–µ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є, –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ —Б–Њ —Б—В–Њ—А–Њ–љ—Л –¶–Э–° –Є –Ц–Ъ–Ґ, –∞ —В–∞–Ї–ґ–µ —Б–µ—А–і–µ—З–љ—Л–µ –∞—А–Є—В–Љ–Є–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П —Г –±–Њ–ї—М–љ—Л—Е —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞, –∞ —В–∞–Ї–ґ–µ –њ–Њ–ї—Г—З–∞—О—Й–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й—Г—О —В–µ—А–∞–њ–Є—О –∞–љ—В–Є–њ—Б–Є—Е–Њ—В–Є–Ї–∞–Љ–Є –њ–µ—А–≤–Њ–≥–Њ –Є –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П, –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є –Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –≤–ї–Є—П—О—Й–Є–Љ–Є –љ–∞ –Ц–Ъ–Ґ –Є –Њ–±–Љ–µ–љ –≤–µ—Й–µ—Б—В–≤ [15]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Є–•–≠ –Њ–≥—А–∞–љ–Є—З–Є–≤–∞–µ—В —А—П–і –∞–±—Б–Њ–ї—О—В–љ—Л—Е –Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є, –≤ –Є—Е —З–Є—Б–ї–µ —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М –ґ–µ–ї—Г–і–Ї–∞ –Є –і–≤–µ–љ–∞–і—Ж–∞—В–Є–њ–µ—А—Б—В–љ–Њ–є –Ї–Є—И–Ї–Є, –њ–Њ—З–µ—З–љ–∞—П –Є –њ–µ—З–µ–љ–Њ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, —Б–Є–љ–і—А–Њ–Љ —Б–ї–∞–±–Њ—Б—В–Є —Б–Є–љ—Г—Б–Њ–≤–Њ–≥–Њ —Г–Ј–ї–∞, –±—А–∞–і–Є–Ї–∞—А–і–Є—П, –±—А–Њ–љ—Е–Є–∞–ї—М–љ–∞—П –∞—Б—В–Љ–∞ –Є —Н–њ–Є–ї–µ–њ—Б–Є—П [3].
–Ь–µ–Љ–∞–љ—В–Є–љ
–Ь–µ–Љ–∞–љ—В–Є–љ —П–≤–ї—П–µ—В—Б—П –љ–µ–Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ—Л–Љ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–Љ –≥–ї—Г—В–∞–Љ–∞—В–љ—Л—Е NMDA(N-–Љ–µ—В–Є–ї-D-–∞—Б–њ–∞—А—В–∞—В)-—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Я—А–µ–і–њ–Њ–ї–∞–≥–∞—О—В, —З—В–Њ –Њ–љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —Н–Ї—Б–∞–є—В–Њ—В–Њ–Ї—Б–Є—З–љ–Њ—Б—В–Є –≤ –Ї–Њ—А–µ –±–Њ–ї—М—И–Є—Е –њ–Њ–ї—Г—И–∞—А–Є–є –Є –≥–Є–њ–њ–Њ–Ї–∞–Љ–њ–µ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ–Њ–є –Є–Ј–±—Л—В–Њ—З–љ—Л–Љ –≤—Л–±—А–Њ—Б–Њ–Љ –≥–ї—Г—В–∞–Љ–∞—В–∞ –≤ —Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї—Г—О —Й–µ–ї—М [16].
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ–Љ–∞–љ—В–Є–љ–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ —Б—А–µ–і–љ–µ—В—П–ґ–µ–ї–Њ–є –Є —В—П–ґ–µ–ї–Њ–є –С–Р, –љ–Њ –љ–µ –њ—А–Є –і—А—Г–≥–Є—Е —Д–Њ—А–Љ–∞—Е –і–µ–Љ–µ–љ—Ж–Є–Є [17]. –Я–Њ–Љ–Є–Љ–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є –Љ–µ–Љ–∞–љ—В–Є–љ –≤—Л–Ј—Л–≤–∞–µ—В –љ–µ–±–Њ–ї—М—И–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –∞–ґ–Є—В–∞—Ж–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є [18].
–£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є —Б —В–µ–ї—М—Ж–∞–Љ–Є –Ы–µ–≤–Є –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є —Б –±–Њ–ї–µ–Ј–љ—М—О –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞, –Љ–µ–Љ–∞–љ—В–Є–љ –≤—Л–Ј—Л–≤–∞–ї –љ–µ–±–Њ–ї—М—И–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Њ–±—Й–µ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П (–њ–Њ —И–Ї–∞–ї–µ CGI), –љ–Њ –љ–µ –≤–ї–Є—П–ї –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є [9]. –Х—Б—В—М —Б–Њ–Њ–±—Й–µ–љ–Є—П –Њ–± —Г—Е—Г–і—И–µ–љ–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –±—А–µ–і–∞ –Є –≥–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–µ–Љ–∞–љ—В–Є–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є —Б —В–µ–ї—М—Ж–∞–Љ–Є –Ы–µ–≤–Є [5].
–Я—А–Є –ї–µ–≥–Ї–Њ–є –Є —Г–Љ–µ—А–µ–љ–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є –Њ–љ –Њ–Ї–∞–Ј—Л–≤–∞–ї –љ–µ–±–Њ–ї—М—И–Њ–є –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –љ–µ –Ј–љ–∞—З–Є–Љ—Л–є —Н—Д—Д–µ–Ї—В [18]. –Ф–∞–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Љ–µ–Љ–∞–љ—В–Є–љ–∞ –њ—А–Є –Ы–Т–Ф –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л [19].
–Ф–Њ—Б—В–Њ–Є–љ—Б—В–≤–Њ–Љ –Љ–µ–Љ–∞–љ—В–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М [5].
–Ф—А—Г–≥–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л
–Т —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Њ–±–Ј–Њ—А–∞—Е –Є –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–∞—Е –љ–µ —Г–і–∞–ї–Њ—Б—М –њ–Њ–ї—Г—З–Є—В—М –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є –Ї–∞–Ї–Є—Е-–ї–Є–±–Њ –і–µ–Љ–µ–љ—Ж–Є—П—Е –њ–Є—А–∞—Ж–µ—В–∞–Љ–∞ [20], –Љ–µ–ї–∞—В–Њ–љ–Є–љ–∞ [21] –Є –≤–Є—В–∞–Љ–Є–љ–Њ–≤ [22–24]. –Ґ–∞–Ї–ґ–µ –љ–µ –і–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М —Б—В–∞—В–Є–љ–Њ–≤, –Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Є –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (–Э–Я–Т–Я) –њ—А–µ–і–Њ—В–≤—А–∞—Й–∞—В—М —Г—Е—Г–і—И–µ–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є [25]. –С–Њ–ї–µ–µ —В–Њ–≥–Њ, –≤ 2012 –≥. –љ–∞ –Њ—Б–љ–Њ–≤–∞–љ–Є–Є —Б–њ–Њ–љ—В–∞–љ–љ—Л—Е —Б–Њ–Њ–±—Й–µ–љ–Є–є –Њ –њ–Њ–±–Њ—З–љ—Л—Е —А–µ–∞–Ї—Ж–Є—П—Е FDA (–°–®–Р) –≤–љ–µ—Б–ї–Њ –≤ –Є–љ—Б—В—А—Г–Ї—Ж–Є–Є –њ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Б—В–∞—В–Є–љ–Њ–≤ –њ—А–µ–і–Њ—Б—В–µ—А–µ–ґ–µ–љ–Є–µ –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ –љ–∞—А—Г—И–µ–љ–Є–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –њ—А–Є –Є—Е –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є [26]. –Т —Ж–µ–ї–µ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ–Љ —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–Љ –Њ–±–Ј–Њ—А–µ –љ–µ —Г–і–∞–ї–Њ—Б—М –љ–Є –њ–Њ–і—В–≤–µ—А–і–Є—В—М, –љ–Є –Њ–њ—А–Њ–≤–µ—А–≥–љ—Г—В—М —Н—В–Њ –њ—А–µ–і–Њ—Б—В–µ—А–µ–ґ–µ–љ–Є–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –њ—А–µ–њ–∞—А–∞—В–Њ–≤ [27]. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –і–∞–љ–љ—Л–µ –Є–Љ–µ—О—В—Б—П –і–ї—П –Э–Я–Т–Я (—А–Њ—Д–µ–Ї–Њ–Ї—Б–Є–±–∞, —Ж–µ–ї–µ–Ї–Њ–Ї—Б–Є–±–∞ –Є –љ–∞–њ—А–Њ–Ї—Б–µ–љ–∞) –Є —Н–Ї–≤–Є–љ-—Н—Б—В—А–Њ–≥–µ–љ–∞ [25].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л–±–Њ—А –њ—А–µ–њ–∞—А–∞—В–Њ–≤, —Г–ї—Г—З—И–∞—О—Й–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є, –Њ—Б—В–∞–µ—В—Б—П –Ї—А–∞–є–љ–µ –Њ–≥—А–∞–љ–Є—З–µ–љ–љ—Л–Љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є–•–≠ –Є –Љ–µ–Љ–∞–љ—В–Є–љ–∞ —Г–Љ–µ—А–µ–љ–љ–∞—П, –Є –Њ–љ–Є –њ–Њ–Ј–≤–Њ–ї—П—О—В –Ј–∞–і–µ—А–ґ–Є–≤–∞—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ —Б—А–µ–і–љ–µ–Љ –ї–Є—И—М –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –Љ–µ—Б—П—Ж–µ–≤. –Я—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є —З–∞—Б—В–Њ —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞—В—М –Є–•–≠ –Є –Љ–µ–Љ–∞–љ—В–Є–љ. –≠—В–∞ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П –±–µ–Ј–Њ–њ–∞—Б–љ–Њ–є –Є —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є, –њ–Њ—Б–Ї–Њ–ї—М–Ї—Г –µ–µ –Є–љ–≥—А–µ–і–Є–µ–љ—В—Л –Є–Љ–µ—О—В —А–∞–Ј–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –і–µ–є—Б—В–≤–Є—П, –Њ–і–љ–∞–Ї–Њ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ—Л—Е –і–∞–љ–љ—Л—Е –і–ї—П —В–Њ–≥–Њ, —З—В–Њ–±—Л –њ–Њ–і–і–µ—А–ґ–∞—В—М –Є–ї–Є –Њ—В–≤–µ—А–≥–љ—Г—В—М –µ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ, –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ [2].
–Я–Њ–Є—Б–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –њ—А–Њ–і–Њ–ї–ґ–∞–µ—В—Б—П, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ—Е–Њ–і—П—В 70 –љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –њ—А–µ–і–љ–∞–Ј–љ–∞—З–µ–љ–љ—Л—Е –і–ї—П –ї–µ—З–µ–љ–Є—П –С–Р [28]. –Т–љ–Є–Љ–∞–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–є –њ—А–Є–≤–ї–µ–Ї–∞—О—В –Є «—Б—В–∞—А—Л–µ» —Б—А–µ–і—Б—В–≤–∞, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є–µ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є. –Ъ –Є—Е —З–Є—Б–ї—Г –Њ—В–љ–Њ—Б–Є—В—Б—П —Е–Њ–ї–Є–љ–∞ –∞–ї—М—Д–Њ—Б—Ж–µ—А–∞—В (–•–Р–§) [29, 30].
–•–Њ–ї–Є–љ–∞ –∞–ї—М—Д–Њ—Б—Ж–µ—А–∞—В –Є –µ–≥–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є
–•–Р–§ —П–≤–ї—П–µ—В—Б—П –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї–Њ–Љ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞. –Ю–љ –ї–µ–≥–Ї–Њ –њ—А–Њ—Е–Њ–і–Є—В —З–µ—А–µ–Ј –≥–µ–Љ–∞—В–Њ—Н–љ—Ж–µ—Д–∞–ї–Є—З–µ—Б–Ї–Є–є –±–∞—А—М–µ—А –Є –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ —А–∞—Б—Й–µ–њ–ї—П–µ—В—Б—П –љ–∞ —Е–Њ–ї–Є–љ –Є –≥–ї–Є—Ж–µ—А–Њ—Д–Њ—Б—Д–∞—В [30]. –•–Њ–ї–Є–љ —П–≤–ї—П–µ—В—Б—П —Б—Г–±—Б—В—А–∞—В–Њ–Љ –і–ї—П —Б–Є–љ—В–µ–Ј–∞ –љ–µ–є—А–Њ–Љ–µ–і–Є–∞—В–Њ—А–∞ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞, –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–Є–≥–љ–∞–ї—М–љ—Л—Е –Љ–Њ–ї–µ–Ї—Г–ї –Є –ї–Є–њ–Є–і–Њ–≤, –≤–Ї–ї—О—З–∞—П –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л–µ –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В—Л –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ (—Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ, –ї–Є–Ј–Њ—Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ, —Б—Д–Є–љ–≥–Њ–Љ–Є–µ–ї–Є–љ), –∞ —В–∞–Ї–ґ–µ –і–Њ–љ–∞—В–Њ—А–Њ–Љ –Љ–µ—В–Є–ї—М–љ—Л—Е –≥—А—Г–њ–њ, –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л—Е –і–ї—П –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –Љ–µ—В–Є–ї–Є—А–Њ–≤–∞–љ–Є—П –Ф–Э–Ъ –Є —А–µ—Б–Є–љ—В–µ–Ј–∞ –Љ–µ—В–Є–Њ–љ–Є–љ–∞ [31]. –У–ї–Є—Ж–µ—А–Њ—Д–Њ—Б—Д–∞—В – –њ—А–µ–і—И–µ—Б—В–≤–µ–љ–љ–Є–Ї —Д–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ–∞ – –Њ–і–љ–Њ–≥–Њ –Є–Ј –≥–ї–∞–≤–љ—Л—Е —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–Њ–≤ –Ї–ї–µ—В–Њ—З–љ—Л—Е –Љ–µ–Љ–±—А–∞–љ, –њ—А–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–Є –Ї–Њ—В–Њ—А—Л—Е –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ –Њ–±—А–∞–Ј—Г—О—В—Б—П –≤—Л—Б–Њ–Ї–Њ—В–Њ–Ї—Б–Є—З–љ—Л–µ —Б–≤–Њ–±–Њ–і–љ—Л–µ —А–∞–і–Є–Ї–∞–ї—Л. –§–Њ—Б—Д–∞—В–Є–і–Є–ї—Е–Њ–ї–Є–љ –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В —Д–Њ—Б—Д–Њ–ї–Є–њ–Є–і–љ—Л–є —Б–Њ—Б—В–∞–≤ –Љ–µ–Љ–±—А–∞–љ –љ–µ–є—А–Њ–љ–Њ–≤ –Є —Г–ї—Г—З—И–∞–µ—В –Є—Е –њ–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М.
–Т —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞—Е –љ–∞ –ґ–Є–≤–Њ—В–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –•–Р–§ —Г—Б–Є–ї–Є–≤–∞–µ—В –≤—Л–і–µ–ї–µ–љ–Є–µ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞ –≤ –≥–Є–њ–њ–Њ–Ї–∞–Љ–њ–µ, —Г–ї—Г—З—И–∞–µ—В –њ–∞–Љ—П—В—М –Є –Њ–±—Г—З–µ–љ–Є–µ, –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Љ–Є–Ї—А–Њ–∞–љ–∞—В–Њ–Љ–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –њ—А–Є —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ–Њ–є –Љ–Њ–і–µ–ї–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, —Б–љ–Є–ґ–∞–µ—В —Б—В—А—Г–Ї—В—Г—А–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ —Б—В–∞—А–µ–љ–Є–µ–Љ, –≤ —В. —З. –Њ—В–≤–µ—З–∞—О—Й–Є–µ –Ј–∞ –њ–∞–Љ—П—В—М –Є –Њ–±—Г—З–µ–љ–Є–µ [30–32].
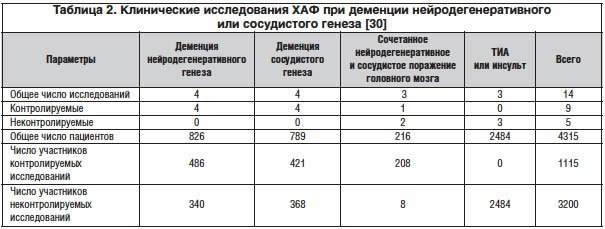
–•–Р–§ –Є–Ј—Г—З–∞–ї—Б—П –≤ 14 –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —Б —Г—З–∞—Б—В–Є–µ–Љ 4054 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –і–µ–Љ–µ–љ—Ж–Є–Є –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ (—В–∞–±–ї. 2) –Є –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –Њ—А–Є–µ–љ—В–∞—Ж–Є—О, –≤–љ–Є–Љ–∞–љ–Є–µ, –њ–∞–Љ—П—В—М, —А–µ—З—М –Є –љ–∞—Б—В—А–Њ–µ–љ–Є–µ [32]. –Т —В—А–µ—Е –Є–Ј –љ–Є—Е (n=2484) –њ–Њ–Ї–∞–Ј–∞–љ–∞ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –•–Р–§ —Г–ї—Г—З—И–∞—В—М —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Є–љ—Б—Г–ї—М—В –Є–ї–Є —В—А–∞–љ–Ј–Є—В–Њ—А–љ—Г—О –Є—И–µ–Љ–Є—З–µ—Б–Ї—Г—О –∞—В–∞–Ї—Г (–Ґ–Ш–Р)[32].
–Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–ї—Г—З–µ–љ—Л –≤ –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Њ—В–Ї—А—Л—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ –Ш—В–∞–ї–Є–Є, –≤ –Ї–Њ—В–Њ—А–Њ–Љ 2044 –њ–∞—Ж–Є–µ–љ—В–∞, –љ–µ–і–∞–≤–љ–Њ –њ–µ—А–µ–љ–µ—Б—И–Є—Е –Є–љ—Б—Г–ї—М—В –Є–ї–Є –Ґ–Ш–Р, –њ–Њ–ї—Г—З–∞–ї–Є –≤ —В–µ—З–µ–љ–Є–µ –њ–µ—А–≤–Њ–≥–Њ –Љ–µ—Б—П—Ж–∞ –Є–љ—К–µ–Ї—Ж–Є–Є –•–Р–§, –∞ –і–∞–ї–µ–µ –≤ —В–µ—З–µ–љ–Є–µ 5 –Љ–µ—Б. – –њ—А–µ–њ–∞—А–∞—В –≤–љ—Г—В—А—М [33]. –Ъ –Ї–Њ–љ—Ж—Г –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –Њ—Ж–µ–љ–Ї–Њ–є –њ–Њ —И–Ї–∞–ї–µ Global Deterioration Scale (–®–Ї–∞–ї–∞ –Њ–±—Й–µ–≥–Њ —Г—Е—Г–і—И–µ–љ–Є—П —Б–Њ—Б—В–Њ—П–љ–Є—П) 71% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Є –Ї—А–Є—В–µ—А–Є—П–Љ «–Њ—В—Б—Г—В—Б—В–≤–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–≥–Њ —Г—Е—Г–і—И–µ–љ–Є—П». –°—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ –Є –њ—А–Є –Њ—Ж–µ–љ–Ї–µ –њ–Њ –≤—Б–µ–Љ –і—А—Г–≥–Є–Љ —В–µ—Б—В–∞–Љ. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —В–∞–Ї–ґ–µ –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –њ—А–µ–Ї—А–∞—Б–љ–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞.
–°—Е–Њ–і–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –Є –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л—Е —Г—З–µ–љ—Л—Е —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –¶–µ—А–µ—В–Њ–љ (–•–Р–§) [34–37]. –Т –Њ–і–љ–Њ–Љ –Є–Ј –љ–Є—Е —Б —Г—З–∞—Б—В–Є–µ–Љ 95 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Ї–∞—А–Њ—В–Є–і–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–∞—П, –љ–Њ –Є –Ј–∞—В—А–∞—В–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –¶–µ—А–µ—В–Њ–љ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є [37].
–Я—А–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е, –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–љ—Л—Е —Б –±–Њ–ї–µ–Ј–љ—М—О –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞, –¶–µ—А–µ—В–Њ–љ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є–ї –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ–Є—А–∞—Ж–µ—В–∞–Љ [38]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–Є—А–∞—Ж–µ—В–∞–Љ–∞, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ—В–Њ—А–Њ–≥–Њ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б —В–µ–љ–і–µ–љ—Ж–Є–µ–є –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –њ—Б–Є—Е–Њ—В–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, –≤–≤–µ–і–µ–љ–Є–µ –•–Р–§ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–Њ—Б—М —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –∞–њ–∞—В–Є–Є, –∞ —В–∞–Ї–ґ–µ —Б –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ —Г–ї—Г—З—И–µ–љ–Є–µ–Љ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –±–Њ–ї—М–љ—Л—Е. –£–ї—Г—З—И–µ–љ–Є–µ –љ–∞—Б—В—А–Њ–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є —Г—Б—В—А–∞–љ–µ–љ–Є–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –ї–∞–±–Є–ї—М–љ–Њ—Б—В–Є, –љ–∞—А—П–і—Г —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П, –њ–Њ–і –≤–ї–Є—П–љ–Є–µ–Љ –•–Р–§ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ–Њ –Є –≤ –і—А—Г–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е [29, 30].
–Т–Ї–ї—О—З–µ–љ–Є–µ –•–Р–§ –љ–∞ —А–∞–љ–љ–Є—Е —Н—В–∞–њ–∞—Е –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г–ї—Г—З—И–µ–љ–Є—О –Є—Б—Е–Њ–і–Њ–≤ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (n=23) —Б —З–µ—А–µ–њ–љ–Њ-–Љ–Њ–Ј–≥–Њ–≤–Њ–є —В—А–∞–≤–Љ–Њ–є [39].
–Я—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ–Љ –•–Р–§ –њ–µ—А–µ–і –Є–•–≠ —П–≤–ї—П–µ—В—Б—П –µ–≥–Њ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М, –≤ —В. —З. –±–Њ–ї—М–љ—Л–Љ–Є —Б –±—А–∞–і–Є–Ї–∞—А–і–Є–µ–є, –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є –∞—Б—В–Љ–Њ–є –Є –і—А—Г–≥–Є–Љ–Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —П–≤–ї—П—О—Й–Є–Љ–Є—Б—П –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –Є–•–≠ [30, 40]. –•–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –Є –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –њ–Њ–Ј–≤–Њ–ї–Є–ї–Є —Н–Ї—Б–њ–µ—А—В–∞–Љ —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –•–Р–§ –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Л–±–Њ—А–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞ –Є —Б—В–µ–њ–µ–љ–Є —В—П–ґ–µ—Б—В–Є —Б—В–∞—А—И–µ 85 –ї–µ—В. –Я—А–µ–њ–∞—А–∞—В –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї–Њ—А—А–µ–Ї—Ж–Є—О –ї–µ–≥–Ї–Є—Е –Є —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –≤ —В. —З. –њ—А–Є –љ–∞–ї–Є—З–Є–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В–Є –Є –і—А—Г–≥–Є—Е —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е [30, 32].
–Ф–ї—П –њ–Њ–≤—Л—И–µ–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –•–Р–§ –Љ–Њ–ґ–љ–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞—В—М —Б –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –і—А—Г–≥–Є—Е –≥—А—Г–њ–њ. –Т –Љ–љ–Њ–≥–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –і–≤–Њ–є–љ–Њ–Љ —Б–ї–µ–њ–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –†–Ъ–Ш ASCOMALVA (Effect of association between a cholinesterase inhibitor and GPC on cognitive deficitsin Alzheimer’s disease associated with cerebrovascular injury), —Г—З–∞—Б—В–љ–Є–Ї–∞–Љ–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ –±—Л–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л —Б –С–Р –Є —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤, –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П –•–Р–§ —Б –Є–•–≠ –і–Њ–љ–µ–њ–µ–Ј–Є–ї–Њ–Љ –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є—В –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є—О –і–Њ–љ–µ–њ–µ–Ј–Є–ї–Њ–Љ –њ–Њ –±–Њ–ї—М—И–Є–љ—Б—В–≤—Г —В–µ—Б—В–Њ–≤ –Є —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –±–Њ–ї—М–љ—Л–Љ–Є [41]. –Т –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —А–Њ—Б—Б–Є–є—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л —Е–Њ—А–Њ—И–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –•–Р–§ —Б —Н—В–Є–ї–Љ–µ—В–Є–ї–≥–Є–і—А–Њ–Ї—Б–Є–њ–Є—А–Є–і–Є–љ–∞ —Б—Г–Ї—Ж–Є–љ–∞—В–Њ–Љ (–≠–Ь–У–Я–°) —Г –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П [42–47].
–≠–Ь–У–Я–° – –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Є–Ј –≥—А—Г–њ–њ—Л –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л—Е 3-–Њ–Ї—Б–Є–њ–Є—А–Є–і–Є–љ–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є–є –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ—Л–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –і–µ–є—Б—В–≤–Є—П, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є–Љ –µ–Љ—Г —А–µ–∞–ї–Є–Ј–Њ–≤—Л–≤–∞—В—М —Б–≤–Њ–Є —Н—Д—Д–µ–Ї—В—Л –љ–∞ —В—А–µ—Е —Г—А–Њ–≤–љ—П—Е – –љ–µ–є—А–Њ–љ–∞–ї—М–љ–Њ–Љ, —Б–Њ—Б—Г–і–Є—Б—В–Њ–Љ –Є –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–Љ, –Є –Њ–Ї–∞–Ј—Л–≤–∞—В—М –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ –љ–∞ –¶–Э–°, –љ–Њ –Є –љ–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –Њ—А–≥–∞–љ—Л –Є —В–Ї–∞–љ–Є [45]. –Я—А–µ–њ–∞—А–∞—В —Б–њ–Њ—Б–Њ–±–µ–љ –Є–љ–≥–Є–±–Є—А–Њ–≤–∞—В—М –њ—А–Њ—Ж–µ—Б—Б—Л —Б–≤–Њ–±–Њ–і–љ–Њ-—А–∞–і–Є–Ї–∞–ї—М–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –Є –њ–Њ–і–∞–≤–ї—П—В—М –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–є —Б—В—А–µ—Б—Б, –Ї–Њ—В–Њ—А—Л–є —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞–µ—В—Б—П –≤ –Ї–∞—З–µ—Б—В–≤–µ –Њ–і–љ–Њ–≥–Њ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, –≤ —В. —З. –С–Р –Є –і—А—Г–≥–Є—Е –≤–Є–і–Њ–≤ –і–µ–Љ–µ–љ—Ж–Є–Є, –±–Њ–ї–µ–Ј–љ–Є –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞, —Н–њ–Є–ї–µ–њ—Б–Є–Є, —А–∞—Б—Б–µ—П–љ–љ–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞, –±–Њ–Ї–Њ–≤–Њ–≥–Њ –∞–Љ–Є–Њ—В—А–Њ—Д–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞. –≠–Ь–У–Я–° –Ї–Њ—А—А–Є–≥–Є—А—Г–µ—В –љ–∞—А—Г—И–µ–љ–љ—Л–µ –њ—А–Є —Б—В–∞—А–µ–љ–Є–Є –њ—А–Њ—Ж–µ—Б—Б—Л –Њ–±—Г—З–µ–љ–Є—П –Є –њ–∞–Љ—П—В–Є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–ї—Г—З—И–µ–љ–Є—О –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ —Б–Њ—Е—А–∞–љ–µ–љ–Є—П –Є –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є, —Б–љ–Є–ґ–∞–µ—В —Г—А–Њ–≤–љ–Є –Љ–∞—А–Ї–µ—А–Њ–≤ —Б—В–∞—А–µ–љ–Є—П (–ї–Є–њ–Њ—Д—Г—Б—Ж–Є–љ–∞, –Љ–∞–ї–Њ–љ–Њ–≤–Њ–≥–Њ –∞–ї—М–і–µ–≥–Є–і–∞, —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞) –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ –Є –Ї—А–Њ–≤–Є, —Г–Љ–µ–љ—М—И–∞–µ—В –њ—А–Њ—П–≤–ї–µ–љ–Є—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞ –Є –≤–Њ—Б—Б—В–∞–љ–∞–≤–ї–Є–≤–∞–µ—В —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–є –Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–є —Б—В–∞—В—Г—Б –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ [46].
–Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ–љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –љ–∞ —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Г—О –Є —Б–≤–µ—А—В—Л–≤–∞—О—Й—Г—О —Б–Є—Б—В–µ–Љ—Г –Ї—А–Њ–≤–Є: –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤, —Б–љ–Є–ґ–∞–µ—В –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є—О –Є —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –∞—В–µ—А–Њ–≥–µ–љ–љ—Л—Е –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤, –њ–Њ–≤—Л—И–∞–µ—В —Г—А–Њ–≤–µ–љ—М –ї–Є–њ–Њ–њ—А–Њ—В–µ–Є–і–Њ–≤ –≤—Л—Б–Њ–Ї–Њ–є –њ–ї–Њ—В–љ–Њ—Б—В–Є –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є, —В–Њ—А–Љ–Њ–Ј–Є—В –ї–Њ–Ї–∞–ї—М–љ—Л–µ —Б–Њ—Б—Г–і–Є—Б—В—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –∞—В–µ—А–Њ–≥–µ–љ–µ–Ј–∞ –Є —Г–Љ–µ–љ—М—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–µ. –Ю–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –≠–Ь–У–Я–° —Г–ї—Г—З—И–∞–µ—В –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –Є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є –њ—Г—В–µ–Љ —Г–≥–љ–µ—В–µ–љ–Є—П –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Р –Є —Г—Б–Є–ї–µ–љ–Є—П –њ—А–Њ–і—Г–Ї—Ж–Є–Є –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ [46].
–Т—Л—И–µ–њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ —Б–≤–Њ–є—Б—В–≤–∞ –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –≠–Ь–У–Я–° –≤ –Ї–∞—З–µ—Б—В–≤–µ –њ—А–µ–њ–∞—А–∞—В–∞ –і–ї—П –±–∞–Ј–Њ–≤–Њ–є —В–µ—А–∞–њ–Є–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Х–≥–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –≤ –Ї–∞—З–µ—Б—В–≤–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—А–µ–і—Б—В–≤–∞ –њ—А–Є –Њ—Б—В—А—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є, –≤–µ–≥–µ—В–Њ—Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–Є—Б—В–Њ–љ–Є–Є, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е —Д—Г–љ–Ї—Ж–Є–є –Љ–Њ–Ј–≥–∞ –Є –њ—А–Є –і—А—Г–≥–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П—Е, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є—Е—Б—П –≥–Є–њ–Њ–Ї—Б–Є–µ–є —В–Ї–∞–љ–µ–є [47].
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л –і–µ–є—Б—В–≤–Є—П –Є —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –•–Р–§ –Є –≠–Ь–У–Я–° –і–Њ–њ–Њ–ї–љ—П—О—В –і—А—Г–≥ –і—А—Г–≥–∞ —Б —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –≤–ї–Є—П–љ–Є—П –Ї–∞–Ї –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є, —В–∞–Ї –Є –љ–∞ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л. –Ъ–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –•–Р–§ –Є –≠–Ь–У–Я–° –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ–±–µ—Б–њ–µ—З–Є—В—М –њ—А–Њ—Ж–µ—Б—Б—Л –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—Ж–Є–Є –Є –љ–µ–є—А–Њ–њ–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –Ї–ї–µ—В–Њ–Ї –Љ–Њ–Ј–≥–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–є —Н–љ–µ—А–≥–Є–µ–є, –∞ —Б–Є–љ–µ—А–≥–Є–Ј–Љ –Љ–µ–ґ–і—Г –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є –Є—Е –і–µ–є—Б—В–≤–Є–µ–Љ –љ–∞ —А–∞–Ј–љ—Л–µ —Н—В–∞–њ—Л –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г—Б–Є–ї–µ–љ–Є—О —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Є —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В—Б—П —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –і–∞–љ–љ–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є.
–Ґ–∞–Ї, —Б–Є–љ–µ—А–≥–Є–і–љ—Л–є —Н—Д—Д–µ–Ї—В –Љ–µ–ґ–і—Г –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –±—Л–ї –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –¶–µ—А–µ—В–Њ–љ–∞ (–•–Р–§) –Є –Э–µ–є—А–Њ–Ї—Б–∞ (–≠–Ь–У–Я–°) –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 49 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 60 –і–Њ 85 –ї–µ—В —Б –≤–њ–µ—А–≤—Л–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –Є –њ–Њ–≤—В–Њ—А–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —Б—В—А–∞–і–∞–ї–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є, —Б–µ—А–і–µ—З–љ—Л–Љ–Є –∞—А–Є—В–Љ–Є—П–Љ–Є –Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Њ–±–Љ–µ–љ–∞ –≥–ї—О–Ї–Њ–Ј—Л [42]. –¶–µ—А–µ—В–Њ–љ –≤–≤–Њ–і–Є–ї–Є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –≤ —Б—Г—В–Њ—З–љ–Њ–є –і–Њ–Ј–µ 1000 –Љ–≥; –Э–µ–є—А–Њ–Ї—Б – –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –Ї–∞–њ–µ–ї—М–љ–Њ (250 –Љ–≥/5,0 –Љ–ї –≤ 250 –Љ–ї —Д–Є–Ј—А–∞—Б—В–≤–Њ—А–∞). –Ф–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї–∞ 14 –і–љ–µ–є, –њ–µ—А–Є–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є—П – 30 –і–љ–µ–є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Њ–є –≤ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–Є —Б–Њ–Ј–љ–∞–љ–Є—П –Є —А–µ–≥—А–µ—Б—Б–µ –Њ—З–∞–≥–Њ–≤—Л—Е –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤. –Э–∞—А—П–і—Г —Б –≤—Л—Б–Њ–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О –Њ—В–Љ–µ—З–µ–љ–∞ –µ–µ —Е–Њ—А–Њ—И–∞—П –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л–Љ–Є –њ–Њ–ґ–Є–ї–Њ–≥–Њ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –•–Р–§ –Є –≠–Ь–У–Я–° –≤ –і—А—Г–≥–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В—П–ґ–µ–ї—Л–Љ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ [43]. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н—В–Њ–є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –Є –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–є —В–µ—А–∞–њ–Є–Є –і—А—Г–≥–Є—Е —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є [44–47].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –•–Р–§ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ—А–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е —А–∞–Ј–ї–Є—З–љ–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞, –∞ –µ–≥–Њ –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П —Б –≠–Ь–У–Я–° —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г—Б–Є–ї–µ–љ–Є—О —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Є —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є.

–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т. –Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Є –ї–µ—З–µ–љ–Є–µ —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—П, –љ–µ–є—А–Њ–њ—Б–Є—Е–Є–∞—В—А–Є—П, –њ—Б–Є—Е–Њ—Б–Њ–Љ–∞—В–Є–Ї–∞. 2009. –Т—Л–њ. вДЦ 2. –°. 14–19.
2. Moore A., Patterson C., Lee L. et al. Fourth Canadian Consensus Conference on the Diagnosis and Treatment of Dementia: recommendations for family physicians // Can. Fam. Physician. 2014. Vol. 60. вДЦ 5. P. 433–438.
3. –Ф–µ–Љ–µ–љ—Ж–Є–Є: —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є / –Э.–Э. –ѓ—Е–љ–Њ –Є –і—А. –Ь–Х–Ф–њ—А–µ—Б—Б-–Є–љ—Д–Њ—А–Љ, 2010. 264 —Б.
4. Lobo A., Launer L.J., Fratiglioni L., et al. Prevalence of dementia and major subtypes in Europe: A collaborative study of population-based cohorts. Neurologic Diseases in the Elderly Research Group // Neurol. 2000. Vol. 54. вДЦ 11 (Suppl. 5). S4–9.
5. Hugo J., Ganguli M. Dementia and Cognitive Impairment: Epidemiology, Diagnosis, and Treatment // Clin. Geriatr. Med. 2014.Vol. 30. вДЦ 3. P. 421–442.
6. Mayo M.C., Bordelon Y. Dementia with lewy bodies // Semin. Neurol. 2014. Vol. 34. вДЦ 2. P. 182–188.
7. Ramanan V.K., Saykin A.J. Pathways to neurodegeneration: mechanistic insights from GWAS in Alzheimer's disease, Parkinson's disease, and related disorders // Am. J. Neurodegener. Dis. 2013. Vol. 2. вДЦ 3. P. 145–175.
8. Russ T.C., Morling J.R. Cholinesterase inhibitors for mild cognitive impairment // Cochrane Database Syst. Rev. 2012. Vol. 9. CD009132.
9. Wang H.F., Yu J.T., Tang S.W. et al. Efficacy and safety of cholinesterase inhibitors and memantine in cognitive impairment in Parkinson's disease, Parkinson's disease dementia, and dementia with Lewy bodies: systematic review with meta-analysis and trial sequential analysis // J. Neurol. Neurosurg. Psychiatry. 2014. May 14.
10. McKeith I., Mintzer J., Aarsland D. et al. Dementia with Lewy bodies // Lancet Neurol. 2004. Vol. 3. вДЦ 1. P. 19–28.
11. Craig D., Birks J. Galantamine for vascular cognitive impairment // Cochrane Database Syst. Rev. 2006. CD004746.
12. Craig D., Birks J. Rivastigmine for vascular cognitive impairment // Cochrane Database Syst. Rev. 2005. CD004744.
13. Hugo, Mendez M.F., Shapira J.S., McMurtray A. et al. Preliminary findings: behavioral worsening on donepezil in patients with frontotemporal dementia // Am. J. Geriatr. Psychiatry. 2007. Vol. 15. вДЦ 1. P. 84–87.
14. Press D., Alexander M. Cholinesterase inhibitors in the treatment of dementia. In: Basow DS, editor. UpToDate. Waltham (MA): UpToDate. Available at: http://www. uptodate.com/contents/cholinesterase-inhibitors-in-the-treatment-of-dementi.2013
15. Pariente A., Sanctussy D.J., Miremont-Salame G. et al. //Factors associated with serious adverse reactions to cholinesterase inhibitors: a study of spontaneous reporting // CNS Drugs. 2010. Vol. 24. вДЦ 1. P. 55–63.
16. Robinson D., Keating G. Memantine: a review of its use in Alzheimer's disease // Drugs. 2006. Vol. 66. вДЦ 11. P. 1515–1534.
17. McKeage K. Memantine: a review of its use in moderate to severe Alzheimer’s disease // CNS Drugs. 2009. Vol. 23. P. 881–897.
18. McShane R., Areosa S.A., Minakaran N. Memantine for dementia // Cochrane Database Syst. Rev. 2006. CD003154.
19. Huey E.D., Putnam K.T., Grafman J. A systematic review of neurotransmitter deficits and treatments in frontotemporal dementia // Neurol. 2006. Vol. 66. вДЦ 1. P. 17–22.
20. Flicker L., Grimley E.J. Piracetam for dementia or cognitive impairment // Cochrane Database Syst. Rev. 2004. CD001011.
21. Jansen S.L., Forbes D., Duncan V. et al. Melatonin for the treatment of dementia // Cochrane Database Syst. Rev. 2006.CD003802.
22. Malouf R., Grimley E.J. Vitamin B6 for cognition // Cochrane Database Syst. Rev. 2003. CD004393.
23. Malouf R., Areosa S.A. Vitamin B12 for cognition // Cochrane Database Syst. Rev. 2003. CD004394.
24. Malouf R., Grimley E.J. Folic acid with or without vitamin B12 for the prevention and treatment of healthy elderly and demented people // Cochrane Database Syst. Rev. 2008. CD004514.
25. Preventing Alzheimer’s Disease and Cognitive Decline. NIH State-of-the-Science Conference April 26–28, 2010. Bethesda, Maryland Final Panel Statement.
26. FDA Drug Safety Communication: Important safety label changes to cholesterol-lowering statin drugs http://www.fda.gov/Drugs/DrugSafety/ucm293101.htm
27. Richardson K., Schoen M., French B. et al. Statins and cognitive function: a systematic review //Ann. Intern. Med. 2013. Vol. 159. вДЦ 10. P. 688–697.
28. Alzheimer?s Association. Alzheimer’s Association Trial Match . http://www.alz.org/research/clinical_trials/find_clinical_trials_trialmatch.asp.
29. Traini E., Bramanti V., Amenta F. Choline alphoscerate (alpha-glyceryl-phosphoryl-choline) an old choline-containing phospholipid with a still interesting profile as cognition enhancing agent // Curr. Alzheimer Res. 2013.Vol. 10. вДЦ 10. P.1070–1079.
30. Scapicchio P.L. Revisiting choline alphoscerate profile: a new, perspective, role in dementia? // Int. J. Neurosci. 2013. Vol.123. вДЦ 7. P. 444–449.
31. Tayebati S.K., Amenta F. Choline-containing phospholipids: relevance to brain functional pathways // Clin. Chem. Lab. Med. 2013. Vol. 51. вДЦ 3. P. 513–521.
32. Parnetti L., Mignini F., Tomassoni D. et al. Cholinergic precursors in the treatment of cognitive impairment of vascular origin: ineffective approaches or need for re-evaluation? // J. Neurol. Sci. 2007. Vol. 257. P. 264–269.
33. Barbagallo Sangiorgi G., Barbagallo M., Giordano M. et al. Alpha-glycerophosphocholine in the mental recovery of cerebral ischemic attacks. An Italian multicenter clinical trial // Ann. NY Acad Sci. 1994. Vol. 717. P. 253–269.
34. –°—В—Г–ї–Є–љ –Ш.–Ф., –Ь—Г—Б–Є–љ –†.–°., –°–Њ–ї–Њ–љ—Б–Ї–Є–є –Ф.–°. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Е–Њ–ї–Є–љ–∞ –∞–ї—М—Д–Њ—Б—Ж–µ—А–∞—В–∞ (—Ж–µ—А–µ—В–Њ–љ) —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–µ–є –Љ–Њ–Ј–≥–∞ // –Ц—Г—А–љ. –љ–µ–≤—А–Њ–ї –Є –њ—Б–Є—Е–Є–∞—В—А. –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2009. вДЦ 7. –°. 87–89.
35. –Ш—Б–Љ–∞–≥–Є–ї–Њ–≤ –Ь.–§., –Т–∞—Б–Є–ї–µ–≤—Б–Ї–∞—П –Ю.–Т., –У–∞–є—Д—Г—В–і–Є–љ–Њ–≤ –†.–Ґ. –Є –і—А. –Ю—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–µ—А–µ—В–Њ–љ–∞ –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ // –Ц—Г—А–љ. –љ–µ–≤—А–Њ–ї. –Є –њ—Б–Є—Е–Є–∞—В—А. –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2009. вДЦ 3. –°. 35–36.
36. –С—Г–є–ї–Њ–≤–∞ –Ґ.–Т., –У–ї–Њ—В–Њ–≤–∞ –Ь.–Х., –•–∞–ї–∞–Ї –Ь.–Х., –Т–∞—И–Ї–µ–≤–Є—З –Т.–Т. –Ю–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –¶–µ—А–µ—В–Њ–љ–∞ –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е —Б –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ // –Ц—Г—А–љ. –љ–µ–≤—А–Њ–ї. –Є –њ—Б–Є—Е–Є–∞—В—А. –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2009. вДЦ 5. –Т—Л–њ. 2. –°. 58–62.
37. –Ъ–∞–Љ—З–∞—В–љ–Њ–≤ –Я.–†., –Р–±—Г—Б—Г–µ–≤–∞ –С.–Р., –Х–≤–Ј–µ–ї—М–Љ–∞–љ –Ь.–Р.–Є –і—А. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Ж–µ—А–µ—В–Њ–љ–∞ –њ—А–Є –Њ—Б—В—А–Њ–Љ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–Љ –Є–љ—Б—Г–ї—М—В–µ (—А–µ–Ј—Г–ї—М—В–∞—В—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –°–Ю–Ы–Э–¶–Х) // –Ц—Г—А–љ. –љ–µ–≤—А–Њ–ї. –Є –њ—Б–Є—Е–Є–∞—В—А. –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2012. вДЦ 3. –Т—Л–њ. 2. –°. 10–14.
38. –Ы–µ–≤–Є–љ –Ю.–°., –С–∞—В—Г–Ї–∞–µ–≤–∞ –Ы.–Р., –Р–љ–Є–Ї–Є–љ–∞ –Ь.–Р., –Ѓ–љ–Є—Й–µ–љ–Ї–Њ –Э.–Р. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —Е–Њ–ї–Є–љ–∞ –∞–ї—М—Д–Њ—Б—Ж–µ—А–∞—В–∞ (—Ж–µ—А–µ—В–Њ–љ–∞) —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–Ј–љ—М—О –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є // –Ц—Г—А–љ. –љ–µ–≤—А–Њ–ї. –Є –њ—Б–Є—Е–Є–∞—В—А. –Є–Љ. –°. –°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. 2009. –Ґ. 109. вДЦ 11. –°. 42–46.
39. Mandat T., Wilk A., Manowiec R. et al. Preliminary evaluation of risk and effectiveness of early choline alphoscerate treatment in craniocerebral injury // Neurol. Neurochir. Pol. 2003. Vol. 37. вДЦ 6. P. 1231–1238.
40. Parnetti L., Abate G., Bartorelli L. et al. Multicentre study of l-alpha-glyceryl-phosphorylcholine vs. ST200 among patients with probable senile dementia of Alzheimer’s type // Drugs Aging. 1993. Vol. 3. –†.159–164.
41. Amenta F., Carotenuto A., Fasanaro A.M. et al. The ASCOMALVA trial: association between the cholinesterase inhibitor donepezil and the cholinergic precursor choline alphoscerate in Alzheimer’s disease with cerebrovascular injury: interim results // J. Neurol. Sci. 2012. Vol. 322. P. 96–101.
42. –®–Љ—Л—А–µ–≤ –Т.–Ш., –Ъ—А—Л–ґ–∞–љ–Њ–≤—Б–Ї–Є–є –°.–Ь. –Ъ–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ —Е–Њ–ї–Є–љ–∞ –∞–ї—М—Д–Њ—Б—Ж–µ—А–∞—В–Њ–Љ –Є —Н—В–Є–ї–Љ–µ—В–Є–ї–≥–Є–і—А–Њ–Ї—Б–Є–њ–Є—А–Є–і–Є–љ–∞ —Б—Г–Ї—Ж–Є–љ–∞—В–Њ–Љ // –§–∞—А–Љ–∞—В–µ–Ї–∞. 2013. вДЦ 9. –°. 79–83.
43. –°–µ—А–µ–≥–Є–љ –Т.–Ш. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≥–ї–Є–∞—В–Є–ї–Є–љ–∞ –Є –Љ–µ–Ї—Б–Є–і–Њ–ї–∞ –≤ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є —В—П–ґ–µ–ї–Њ–≥–Њ –Њ—Б—В—А–Њ–≥–Њ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ // –§–∞—А–Љ–∞—В–µ–Ї–∞. 2006. вДЦ 5.
44. –Ь–µ–љ—М—Й–Є–Ї–Њ–≤–∞ –Х.–С. –Є –і—А. –Ю–Ї–Є—Б–ї–Є—В–µ–ї—М–љ—Л–є —Б—В—А–µ—Б—Б: –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Э–Њ–≤–Њ—Б–Є–±–Є—А—Б–Ї: –Ш–Ј–і-–≤–Њ –Р–†–Ґ–Р, 2008.
45. –С–∞–і–∞–ї—П–љ –Ю.–Ы., –°–∞–≤–µ–љ–Ї–Њ–≤ –Р.–Р., –Ґ–∞–љ—И–µ–≤–∞ –Ъ.–•., –Ґ–µ—А—В—Л—И–љ–Є–Ї –Ю.–Ѓ. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–µ–є—А–Њ–Ї—Б–∞ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Њ–Ј–≥–∞ // –†–Ь–Ц. 2010. –Ґ. 18. вДЦ 8. –°. 455–459.
46. –С–∞–і–∞–ї—П–љ –Ю.–Ы., –Я–Њ–≥–Њ—Б—П–љ –Р.–°., –°–∞–≤–µ–љ–Ї–Њ–≤ –Р.–Р. –Є –і—А. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Э–µ–є—А–Њ–Ї—Б –Є –¶–µ—А–µ—В–Њ–љ –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–Љ –ї–µ—З–µ–љ–Є–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є // –†–Ь–Ц. 2011. вДЦ 12. –°. 764–767.
47. –Э–Є–Ї–Є—Д–Њ—А–Њ–≤ –Р.–°. –Є –і—А. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—П. –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2002. 704 —Б.












