- Артропатии (М00-М25).
- Системные поражения соединительной ткани (М30-М36).
- Дорсопатии (М40-М54).
- Болезни мягких тканей (М60-М79).
- Остеопатии и хондропатии (М80-М94).
- Другие нарушения мышечной системы и соединительной ткани (М95-М99).
Под термином «дорсопатия» чаще всего подразумеваются болевые синдромы в области туловища и конечностей невисцеральной этиологии и связанные с дегенеративными заболеваниями позвоночника. Термин «дорсопатия» в соответствии с МКБ-10 должен заменить термин «остеохондроз позвоночника» [2].
В популяционных исследованиях, проводимых во многих странах мира, отмечается увеличение числа пациентов, обращающихся в лечебные учреждения с жалобами на возникновение болевых синдромов, связанных с патологией позвоночника. В настоящее время распространенность вертеброгенных болевых синдромов в США и странах Европы варьирует от 14 до 42%. Боль в пояснично-крестцовой области остается одним из самых распространенных хронических болевых синдромов. Боль в нижней части спины встречается у 7–9 из 10 членов взрослой популяции, представляя собой наряду с острыми респираторными заболеваниями основную причину временной утраты трудоспособности. Болевой синдром в суставах, позвоночнике и околосуставных мягких тканях встречается более чем у 30% населения земного шара и классифицируется как «ревматические болезни» [3]. В клинической практике жалобы на боли в суставах и околосуставных структурах по частоте встречаемости занимают 2-е место после обращений по поводу артериальной гипертензии [4]. Поражение околосуставных мягких тканей является поводом для первичного обращения к ревматологу в 25% случаев. В структуре хронических заболеваний, регистрируемых среди жителей России, болезни костно-мышечной системы составляют 14–16%, причем их количество имеет тенденцию к росту.
Большая группа ревматических синдромов представлена заболеваниями мягких околосуставных тканей (периартриты), при которых патологический процесс локализован в сухожилиях, сухожильных оболочках, фасциях, мышечно-сухожильных соединениях, суставных связках, энтезисах, суставных сумках, сопровождается хронической локальной болью в области одного сустава, усиливающейся при определенных движениях, связанных с нагрузкой на пораженную структуру [3]. Они могут быть локализованы в области любых суставов скелета, как правило, крупных, несущих большую двигательную и весовую нагрузку. Возрастная дегидратация и физические нагрузки на фоне нарушенной биомеханики обусловливают нарушение сети коллагеновых волокон, утрату амортизационных свойств гиалинового хряща и его постепенную фрагментацию. Нарушается метаболическая функция хондроцитов (синтез протеогликанов, коллагена, эластина), повышается активность протеолитических ферментов этих клеток, что приводит к усилению деструктивных процессов в матриксе (межклеточном веществе хряща).
Большинство современных методов лечения дегенеративно-дистрофических заболеваний воздействуют на их патогенетические и симптоматические механизмы, устраняя болезненные явления, но не влияя на причину заболевания. С разработкой хондропротекторов, содержащих глюкозамин и хондроитин сульфат (ХС), появилась возможность воздействовать на этиологические механизмы дегенеративно-дистрофических заболеваний по принципу заместительной терапии. ХС относится к фармакологической группе корректоров метаболизма костной и хрящевой ткани [5]. ХС — вещество, которое в норме входит в состав суставного хряща и играет важную роль в поддержании необходимого осмотического давления, благодаря чему матрикс и нити коллагена растягиваются, и оказывает хондропротективное, хондростимулирующее фармакологическое действие, стимулирующее регенерацию. Препараты, содержащие ХС, обладают противовоспалительной активностью, воздействуя в основном на клеточный компонент воспаления, стимулируют синтез гиалуроновой кислоты (ГК) и протеогликанов. ГК — полисахарид из семейства гликозаминогликанов, состоящий из повторяющихся дисахаридных звеньев N-ацетил-D-глюкозамина и глюкуроновой кислоты [6]. В организме человека ГК встречается повсеместно, являясь одним из основных компонентов межклеточного вещества, естественным метаболитом соединительной ткани, угнетает действие протеолитических ферментов, за счет чего и реализуется основная противовоспалительная активность, действующая на клеточный компонент воспаления.
Исследователями были получены результаты тестирования фракционного состава 5 коммерческих образцов ГК от различных производителей. Установлено, что все образцы характеризуются широким молекулярно-массовым распределением (ММР). Для таких полимолекулярных систем с достаточно широким ММР параметр средней молекулярной массы не может служить адекватной характеристикой биологических свойств полисахарида. Авторы сделали вывод, что для производства изделий медицинского назначения на основе ГК необходимо использовать однородные по молекулярным массам узкие фракции биополимера [7, 8].
Твердотельный метод сшивания и модифицирования (стабилизации) ГК в 2007 г. был разработан в Институте синтетических полимерных материалов им. Н. С. Ениколопова РАН В. Н. Хабаровым, М. А. Селяниным, В. П. Волковым, А. Н. Зеленецким и соавт. [6]. Метод твердофазной модификации (ТФМ) ГК основан на технологии получения твердых дисперсий посредством механической обработки смесей твердых веществ на специальном оборудовании: смесь порошков подвергают сдавливанию в прессе и вращению на площадке. Данный способ модификации ГК позволяет получать стабильные препараты на основе механополимеров благодаря высокой селективности реакции, равномерной плотности сшивания, чего не удается достичь при проведении жидкофазной стабилизации (химической полимеризации) ГК [9].
Дальнейшие исследования ТФМ ГК различными биоактивными веществами (витаминами, аминокислотами, олигопептидами) привели к созданию принципиально новых медицинских изделий, не имеющих аналогов в мировой практике [10]. В результате использования технологии ТФМ ГК были созданы препараты линии Гиалрипайер, которые включают в себя 10 различных биоактивных композиций [11]. Выполнены токсикологические исследования, показавшие отсутствие изменений гематологических, биохимических и иных жизненно важных показателей у лабораторных животных при контакте с материалом. По результатам этих исследований материал оценен как безопасный, возможно его участие в дальнейших испытаниях [12–14].
При внутритканевом введении препарата ГК, модифицированной твердофазным способом, создается его активное депо в месте инъекции, т. е. происходит избирательное концентрирование, следовательно, отпадает необходимость в высоких концентрациях активных веществ, биогенные метаболиты высвобождаются постепенно, по мере разрушения ГК, улучшается их фармакологический профиль, таким образом, предупреждается развитие возможных побочных реакций [9]. Биоактивные компоненты, находясь в химически связанном состоянии с макромолекулой ГК, приобретают устойчивость при хранении, что особенно важно для таких неустойчивых соединений, как витамин С и аминокислоты, легко окисляемые при обычном хранении и стерилизации [11].
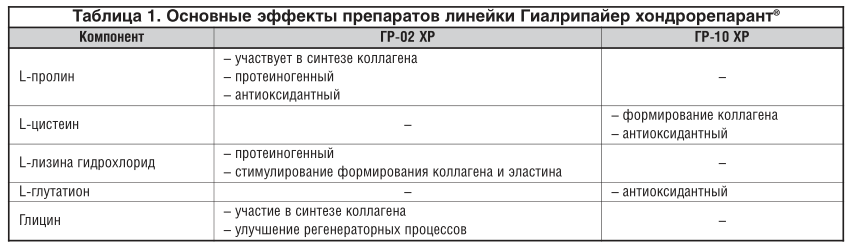
Среди препаратов, обладающих хондропротективным действием, появился новый, разработанный компанией ООО «Лаборатория ТОСКАНИ» препарат Гиалрипайер-02/10 хондрорепарант® (ГР-02/10 ХР) [15], созданный на основе модифицированной ГК (МГК), протеиногенных и антиоксидантных аминокислот (табл. 1). Форма выпуска: в шприцах 2,0 мл, концентрация МГК 1,5%; во флаконах 5,0 мл, концентрация МГК 0,8% [16–19].
Показания [15] к применению препаратов
ГР-02/10 ХР:
- внутрисуставному (в шприцах): дегенеративно-дистрофические поражения суставов I–III степени вне обострения; посттравматические поражения суставов; состояния после оперативных вмешательств на суставах; экстремальные физические нагрузки;
- внесуставному (во флаконах): дегенеративно-дистрофические заболевания мягких тканей и опорно-двигательного аппарата вне обострения; дорсопатии; последствия травматических повреждений тканей.
Противопоказания к внутрисуставному применению ГР ХР: остеоартрит в стадии обострения; синовит; к внесуставному применению: радикулопатия в стадии обострения. Общие противопоказания для всех форм введения: гнойное воспаление поверхностных тканей в зоне введения; гиперчувствительность к компонентам препарата (ГК, аскорбилфосфат); аутоиммунные заболевания соединительной ткани; коагулопатии или прием противосвертывающих препаратов; болезни отложения кристаллов.
За последние годы был проведен ряд доклинических испытаний (НИИ молекулярной медицины Первого МГМУ им. И. М. Сеченова, ФГБУН «НИИ общей патологии и патофизиологии им. А. Д. Сперанского» РАМН, Уральский ветеринарный НИИ РАСХН, ФГБУ «ВНИИИМТ» Росздравнадзора) и клинических исследований (ФГБУЗ «Центр лечебной физкультуры и спортивной медицины» ФМБА России, РАСМИРБИ, ФГУ «ЦИТО им. Н. Н. Приорова» Минздрава России, ГП «Медицинский центр — МТЗ», Республика Беларусь) по оценке эффективности и безопасности линейки Гиалрипайер хондрорепарант®.
Н. П. Михайловой и А. Б. Шехтером (лаборатория экспериментальной морфологии НИИ молекулярной медицины Первого МГМУ им. И. М. Сеченова) в 2011 г. проведен тест in vivo. Результаты экспериментального имплантационного теста при подкожном введении препаратов нативной ГК в сравнении с ГР-02 ХР на биологических моделях подтвердили способность последнего в большей степени активизировать пролиферацию фибробластов кожи и неоангиогенез [20]. Н. П. Михайловой и А. Б. Шехтером был также проведен тест на клеточных линиях «оценка морфологии фибробластов человека», в ходе которого не выявлены эффекты цитодеструкции при всех испытанных дозах препарата ГР-02 ХР, обнаружены выраженный цитопролиферативный эффект и увеличение митотической активности клеток при инкубации фибробластов [20].
В 2012 г. в отделе клеточной патологии и патофизиологии ФГБУН «НИИ общей патологии и патофизиологии им. А. Д. Сперанского» РАН Н. П. Михайловой, А. А. Московцевым и А. А. Соколовской проведены доклинические исследования in vitro по оценке влияния препарата ГР-02 ХР на метаболическую активность, выживаемость и фазы клеточного цикла эндотелиоцитарной линии и фибробластов [20]. Исследования выполнены на клеточных линиях человека — эндотелиоцитарной линии EA.hy926 со свойствами, присущими клеткам эндотелия сосудов, и фибробластоподобной линии FRSN (мезенхимные стволовые клетки из крайней плоти) со свойствами фибробластоподобного клеточного ростка. Инкубация клеток 24 и 48 ч происходила в присутствии тестовых растворов: ГР-02 ХР и нативной ГК в разведениях 0,125–2,0 мг/мл. Использованы методы оценки: 1) динамика клеточного цикла: проточная цитофлуориметрия после окраски ядерной ДНК клеточного супернатанта; 2) цитотоксичность (метаболическая активность клеток): оценка оптической плотности при МТТ-тесте. В ходе исследования было получено: 1) при обработке культур ГР-02 в сравнении с ГК происходит возрастание числа клеток в фазе синтеза, что доказывает стимулирующий эффект ГР-02 на репликацию ДНК, подготавливающий клетку к делению; 2) метаболическая активность эндотелиоцитов и фибробластов при различном времени инкубации была выше в присутствии ГР-02, чем ГК, что также может свидетельствовать о более высокой жизнеспособности клеток в присутствии ГР-02 [20].
В другом доклиническом исследовании in vivo (2012–2013) [21] на экспериментальных моделях (крысы-самцы линии Вистар) И. М. Козловым и Н. М. Перовой, сотрудниками испытательной лаборатории по токсикологическим испытаниям медицинских изделий ФГБУ «Всероссийский научно-исследовательский и испытательный институт медицинской техники» Росздравнадзора, была воссоздана предложенная ранее другими авторами модель неадъювантного артрита, а также разработана оригинальная модель остеоартрита посттравматической этиологии, дана оценка влияния препаратов ГР-02/10 ХР на регенеративные процессы в суставном хряще после внутрисуставного введения. Процесс моделирования патологических состояний у животных (полнослойная травма гиалинового хряща сустава, неадъювантный артрит) длился 5 сут. Методы оценки: гистологическое исследование образцов тканей, рутинные окраски, микроскопия. Схема лечения моделей включала введение препаратов ГР-02/10 ХР на 5-е сут с момента создания модели двукратно в полость сустава с интервалом в 3 дня, выведение из опыта на 7-е сут после курса инъекций. В ходе исследования доказаны выраженное репаративное воздействие на ткани препаратов ГР-02 и ГР-10 ХР при травме и воспалении, а также выраженное противовоспалительное действие на ткани препарата ГР-10 ХР при травме и воспалении [21]. Таким образом, на этих моделях было показано, что препараты ГР-02 ХР и ГР-10 ХР обладают более выраженным стимулирующим репаративным эффектом по сравнению с нативной ГК в той же концентрации. При этом оба состава демонстрируют репаративный потенциал, ускоряя восстановление хрящевой ткани из полнослойного дефекта. ГР-10 ХР показал даже более значимый эффект репарации, что может быть объяснено его антиоксидантными свойствами — патогенез окислительного стресса завязан на деструкции тканей и уменьшении их репаративного потенциала [21].
Описаны результаты масштабных клинических испытаний биоактивных композиций Гиалрипайер для дерматокосметологии на основе солей ГК, содержащих аскорбилфосфаты (химическая форма витамина С) и аминокислоты. Работа завершена в 2013 г. на базе отделения дерматоонкологии и лазерной хирургии ЦКБ РАН с участием 90 женщин в возрасте 35–62 лет с жалобами на снижение тургора и эластичности кожи с проявлениями фото- и хроностарения кожи различной степени тяжести [20, 22]. На основании предварительно полученных экспериментальных результатов ожидаемым эффектом введения ГР-02 ХР считали не только длительную гидратацию дермы, но и формирование физиологически благоприятной среды для восстановления поврежденного межклеточного матрикса соединительнотканного слоя кожи (дермы) и повышения адаптационного ресурса. Проводили 3 процедуры инъекций препарата ГР-02 ХР с интервалом 3 нед. Оценка клинического эффекта и инструментальные исследования (корнеометрия, рН кожи, себуметрия, эластометрия, ультразвуковое дермасканирование, конфокальная лазерная сканирующая микроскопия, визиосканирование) проводили до лечения и через 3–4 нед. после завершения курса. В ходе проведенного исследования отмечались уменьшение или исчезновение проявлений ксероза; перестройка и упорядочивание архитектоники дермальных волокон, снижение количества и плотности участков мономорфной структуры. По результатам исследования сделаны выводы: в областях, окружающих введенный материал, наблюдаются позитивные изменения морфотипа фибробластов, повышение пролиферативной активности клеток, признаки синтеза коллагена [20].
Б. А. Поляевым, С. А. Парастаевым, С. В. Капышевым, В. В. Кармазиным и М. А. Погодиной описан клинический опыт применения ГР-02 ХР (в шприцах) у спортсменов с посттравматическим гонартрозом [23, 24]. Исследование проводилось на базе кафедры реабилитации и спортивной медицины РНИМУ им. Н. И. Пирогова, РАСМИРБИ, Центра спортивной медицины ФМБА в течение 7 мес. В исследовании приняли участие 10 борцов самбо/дзюдо высокой квалификации (мастера спорта, призеры чемпионатов мира) в возрасте 18–35 лет, со спортивным стажем более 10 лет. Оценивали клиническую эффективность и безопасность препарата, изучали его влияние на симптомы и течение гонартроза, в т. ч. на сроки реабилитационного периода после консервативного или оперативного лечения травмы.
Критерии включения в исследование: вторичный посттравматический гонартроз, клинически и рентгенологически верифицированный; реабилитационный период после травм или оперативных вмешательств на коленном суставе. ГР-02 ХР вводили внутрисуставно по схеме: доза 2,0 мл, 3 инъекции на курс с интервалом в 2 нед. Методы оценки: 1) субъективная оценка болевого синдрома по модифицированной визуально-аналоговой шкале для спортсменов (разработка кафедры РНИМУ); 2) оценка постуральной устойчивости с использованием аппаратно-программного стабилометрического комплекса; 3) динамическая подометрия на барометрической платформе; 4) биомеханическое исследование коленных суставов с помощью инерционных датчиков движения. Обследование испытуемых проводилось до лечения, на 30-й день (перед 3-й инъекцией), 120-й день (3 мес. после курса) и 210-й день (6 мес. после курса = 7 мес. наблюдения). До начала исследования 80% спортсменов щадили конечность на стороне поражения коленного сустава в опоре при стоянии и ходьбе; у 90% испытуемых отмечалось функциональное снижение силы ягодичной группы мышц на стороне поражения; у всех пациентов выявлены нарушения проприоцепции. Уже после 2-х инъекций препарата и спустя 3 мес. по окончании курса отмечены нарастание опорной функции поврежденной конечности и прогрессирующее улучшение ее участия в постуральном балансе. Через 6 мес. — отсутствие болевого синдрома, устойчивость параметров стабилометрии, значимое улучшение проприоцептивной и опорной функций. На основании результатов исследования сделаны выводы о хондропротективных и репаративных свойствах препарата: применение ГР-02 ХР у спортсменов высокой квалификации приводит к исчезновению болевого синдрома в суставе при посттравматическом гонартрозе и к объективному улучшению биомеханических показателей; высокая стабильность полученных результатов к концу исследования свидетельствует о стойкости эффектов внутрисуставного применения препарата, а улучшение опорной функции конечности на стороне поражения к концу исследования — о повышении проприоцептивного контроля и улучшении координации движений [23].
Согласно материалам клинического пилотного моноцентрового проспективного неконтролируемого открытого исследования (II фаза), А. В. Людчиком, Н. М. Ковшель и С. Е. Ровдо дана оценка эффективности и безопасности препаратов ГР-02 ХР и ГР-10 ХР (во флаконах) при различных проявлениях дорсопатий [8, 25]. Исследование проведено на базе неврологического отделения ГП «Медицинский центр — МТЗ» (Республика Беларусь, Минск). В исследовании приняли участие 52 пациента (19 мужчин, 33 женщины) в возрасте 32–80 лет. Рефлекторные формы дорсопатий были следующими: люмбоишиалгии, торакалгии, цервикобрахиалгии и цервикокраниалгии. Клинические проявления нейродистрофических и миофасциальных синдромов и энтезопатий: миофасциальный синдром перикраниальной локализации, артроз и периартроз фасеточных суставов, артроз и периартроз реберно-грудинных суставов, очаги уплотнения мягких тканей, окружающих сустав, и в зоне прикрепления мышц пояса верхних или нижних конечностей, плечелопаточный периартрит, эпикондилит, карпальный синдром, артроз и периартроз крестцово-подвздошного сочленения, перикоксартроз, перигонартроз. В 58% случаев наблюдались артроз и периартроз фасеточных суставов.
В ходе исследования проведена локальная инъекционная терапия указанными препаратами — 315 процедур. У 31 пациента выполнялось последовательное воздействие по причине наличия у них множественных зон. Для пациентов с острой стадией процесса (n=13) схема лечения включала в себя: ГР-10 ХР на первых процедурах до стихания болевого синдрома, далее ГР-02 ХР в дозе ≤0,5 мл на 1 точку инъекции, 4–6 процедур на курс с интервалом в 2–3 нед.; для пациентов с затянувшимся процессом со склонностью к хронизации (n=39): ГР-02 ХР в течение всего курса в дозе ≤0,5 мл на 1 точку инъекции, 4–6 процедур на курс с интервалом в 2–3 нед. Выбор точек введения проводили, применяя схему расположения стандартных точек медикаментозных околосуставных/паравертебральных/миофасциальных блокад, а в случае латентных или активных миофасциальных триггеров перед каждой процедурой осуществляли индивидуальный подбор точек (триггерную диагностику). Все пациенты получали курсовое инъекционное лечение без сопутствующего фармакологического лечения, и лишь в 2 случаях с выраженным болевым синдромом при плечелопаточном периартрите был назначен сопутствующий курс нестероидного противовоспалительного препарата (НПВП). Все пациенты вели обычный образ жизни с повседневными статодинамическими и психо-эмоциональными нагрузками. В задачи данного исследования не входило проведение полного курса инъекций больным с конкретными нозологическими формами и отслеживанием отдаленных результатов лечения. Динамику состояния оценивали каждые 15–20 дней для процедур и через 45 дней после окончания курса.
Эффективность проведенного курса терапии в 23,1% случаев оценена как значительное улучшение состояния (полное купирование или выраженное уменьшение боли, восстановление функции); в 66,7% — как умеренное улучшение (значимое снижение интенсивности боли и улучшение функции, требующее продолжения лечения); в 2,6% — как сомнительный результат (уменьшение интенсивности боли на 1–2 дня или боль возвращалась к исходному уровню по истечении 1 нед.); в 7,6% эффект отсутствовал. Таким образом, можно констатировать, что инъекции ГР-02/10 ХР эффективны в 89,8%. В подавляющем большинстве случаев инъекции хорошо переносились пациентами и не сопровождались какими-либо значимыми побочными эффектами.
Авторы исследования акцентировали внимание на том, что при плечелопаточном периартрите спонтанная боль в плечевом суставе проходила или значительно уменьшалась после 1–2 инъекций, увеличивался объем активных движений при синдроме «замороженного плеча», уменьшалась болезненность при пальпации периартикулярных тканей. Отмечено, что при введении ГР-10 ХР при точном попадании в триггерную точку болевой синдром может уходить «на кончике иглы». Другим клинически значимым фактом оказались результаты при миофасциальном болевом синдроме с дисфункцией перикраниальных мышц: введение препаратов в триггерные точки прикрепления мышц к костям черепа в области затылка и виска купировало приступы головной боли; у пациентов с головной болью напряжения или цервикокраниалгией, страдавших ежедневными или частыми головными болями, приступы прекращались на период от 5–7 дней до 1–1,5 мес.
Интересным выводом авторов исследования является то, что при проведении лечения периартроза крупных синовиальных суставов (тазобедренного и коленного), ассоциированного с артрозом, большая эффективность должна достигаться при сочетании периартикулярных и внутрисуставных инъекций. Данный эффект можно объяснить тем, что болевой синдром при остеоартрите в большинстве случаев носит ноцицептивный характер (болевая импульсация от внутрисуставных болевых рецепторов), являясь следствием процессов деструкции и воспаления в суставной полости (в меньшей степени — от связочных, фасциальных и периостальных триггеров). Именно поэтому при артрозе и околосуставных изменениях следует акцентировать внимание на внутрисуставной вискосапплементирующей терапии. Таким образом, можно заключить, что комплексный подход к локальной терапии данного состояния может включать околосуставные инъекции, что с успехом было показано А. В. Людчиком и соавт.
В течение всего периода наблюдения была доказана хорошая переносимость инъекционной терапии данными препаратами при условии правильно выбранной тактики лечения и соблюдения техники введения в периартикулярные или мышечные ткани. Было отмечено, что курсовая монотерапия препаратами линии Гиалрипайер хондрорепарант® обладает анталгическим эффектом и позволяет увеличить или восстановить объем движений уже после 1–2 инъекций.
Среди нежелательных явлений отмечены: умеренная локальная боль от вкола иглы в течение нескольких дней после процедуры; усиление имеющегося у пациента болевого синдрома сразу после инъекции и сохранение его в последующем; некоторое обострение процесса после первоначального улучшения (обычно на 2–3 день) с последующим хорошим регрессом к 7 дню. По мнению авторов исследования, различная степень выраженности данных проявлений является разнородной картиной единого патогенетического состояния у лиц в остром периоде заболевания с выраженным болевым синдромом — наличием острых воспалительных изменений в тканях. Известно, что метаболиты ГК в условиях ярко выраженного воспалительного процесса обладают не противо-, а провоспалительной активностью и способны инициировать обострение. Анализируя такой паттерн, можно заключить, что перед началом курсовой терапии ГР-02/10 ХР требуется проводить оценку остроты воспалительного процесса в тканях и в случае необходимости предварительно назначать индивидуально подобранное противовоспалительное лечение, физиотерапию.
Таким образом, на основании полученных результатов исследования авторами сделаны выводы: препараты ГР-02 ХР и ГР-10 ХР являются эффективными средствами профилактики нейродистрофических и дегенеративных изменений тканей организма; обладают лечебным действием и эффективны при миофасциальных и нейродистрофических проявлениях дорсопатий вертебральной и экстравертебральной локализации, хронических воспалительных заболеваниях связочного аппарата суставов, посттравматических артрозах и реабилитации травматологических больных. Введение препаратов хорошо переносится больными и не дает серьезных побочных эффектов; стойкий лечебный эффект достигается без применения гормональных препаратов и НПВП; лечение показано пациентам как с подострой, так и с хронической стадиями заболевания [25].
Заключение
Использование молекулы ГК в качестве транспортного депо при локальной коррекции метаболизма (функциональной активности клеток) может эффективно применяться как метод лечения и профилактики дегенеративных изменений соединительнотканных структур опорно-двигательного аппарата человека.
В ряде проведенных исследований показана высокая эффективность применения препаратов линии Гиалрипайер хондрорепарант® при дегенеративно-дистрофических изменениях в суставах, патологии околосуставных тканей, посттравматических изменениях опорно-двигательного аппарата, компрессионно-ишемической невропатии, проявляющихся, в первую очередь, болевым синдромом.
Применяемая схема назначения ГР-02/10 ХР при внутрисуставном введении: ГР-02 ХР в дозе 2,0 мл, 3 инъекции на курс, интервал между инъекциями 2 нед. [23]; при внесуставном введении: в острой стадии процесса ГР-10 ХР на первых процедурах до стихания болевого синдрома, далее ГР-02 ХР в дозе ≤0,5 мл на 1 точку инъекции, 4–6 процедур на курс с интервалом в 2–3 нед.; для пациентов с хроническим процессом ГР-02 ХР в течение всего курса в дозе ≤0,5 мл на 1 точку инъекции, 4–6 процедур на курс с интервалом в 2–3 нед. [25]. Межкурсовой интервал составляет 6–12 мес. Доза, кратность применения и длительность курса устанавливаются врачом индивидуально. Интервал между курсами может быть изменен в зависимости от показаний.
ГР-02 ХР и ГР-10 ХР могут быть рекомендованы как препараты для немедикаментозных блокад в подострой или хронической стадиях заболеваний опорно-двигательного аппарата внутрисуставной и внесуставной локализации при отсутствии ярких проявлений воспалительного компонента.













