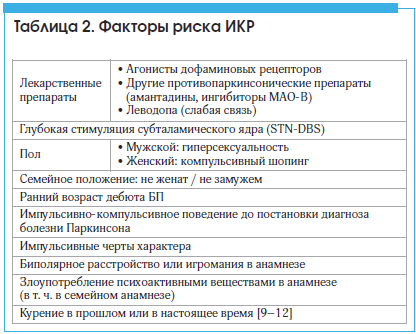
–Ш–Ъ–† –Є–Љ–µ—О—В —З–µ—В–Ї—Г—О —Б–≤—П–Ј—М —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–≥–Њ–љ–Є—Б—В–Њ–≤ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –Ф–Ф–° –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ —Б –±—Л—Б—В—А–Њ–і–µ–є—Б—В–≤—Г—О—Й–µ–є –≤—Л—Б–Њ–Ї–Њ–∞–Ї—В–Є–≤–љ–Њ–є –і–Њ—Д–∞–Љ–Є–љ-–Ј–∞–Љ–µ—Б—В–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є, –љ–∞–њ—А–Є–Љ–µ—А, —Б –њ—А–Є–µ–Љ–Њ–Љ –ї–µ–≤–Њ–і–Њ–њ—Л. –Ф—А—Г–≥–Є–µ —Д–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞ –Ш–Ъ–† –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 2 [6вАУ12].
–≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—П –Ш–Ъ–† –Є –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –Ш–Ъ–†, –њ—А–Є –С–Я
–†–µ–Ј—Г–ї—М—В–∞—В—Л –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ —В–Њ–Љ, —З—В–Њ –Ш–Ъ–† —З–∞—Й–µ –≤—Б—В—А–µ—З–∞—О—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Я, —З–µ–Љ –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є –≤ —Ж–µ–ї–Њ–Љ –Є–ї–Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –ї–Є—Ж –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ—Л [13, 14]. –•–Њ—В—П –≤ –Њ–і–љ–Њ–Љ –љ–µ–і–∞–≤–љ–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ –Њ–±—А–∞—В–љ–Њ–µ [15].–Т –Ї—А–Њ—Б—Б-—Б–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –С–Я —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —Д–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞–љ–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є –Ш–Ъ–† —З–∞—Б—В–Њ—В–∞ –Є–≥—А–Њ–Љ–∞–љ–Є–Є —Б–Њ—Б—В–∞–≤–Є–ї–∞ 1,7вАУ7,0%, –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ–≥–Њ –≥–Є–њ–µ—А—Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П вАУ 3,5%, –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ–≥–Њ —И–Њ–њ–Є–љ–≥–∞ вАУ 0,4вАУ3,0% [2, 8, 16вАУ18]. –Ш–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ–µ –њ–µ—А–µ–µ–і–∞–љ–Є–µ —В–∞–Ї–ґ–µ –Њ–њ–Є—Б—Л–≤–∞–ї–Њ—Б—М –њ—А–Є –С–Я, –Њ–і–љ–∞–Ї–Њ –≤ –њ–µ—А–≤—Л—Е —А–∞–±–Њ—В–∞—Е –њ–Њ –Ш–Ъ–† –µ–≥–Њ —З–∞—Б—В–Њ—В–∞ –љ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–ї–∞—Б—М [4, 19]. –Ъ—А—Г–њ–љ–µ–є—И–µ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –Ш–Ъ–† –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ —Б —Г—З–∞—Б—В–Є–µ–Љ 3090 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Я, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О, –≤ 46 —Ж–µ–љ—В—А–∞—Е –њ–Њ –ї–µ—З–µ–љ–Є—О —Н–Ї—Б—В—А–∞–њ–Є—А–∞–Љ–Є–і–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≤ –°–®–Р –Є –Ъ–∞–љ–∞–і–µ (–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ DOMINION) [20]. –Ф–ї—П –Є–Ј—Г—З–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л 4-—Е –Њ—Б–љ–Њ–≤–љ—Л—Е –≤–Є–і–Њ–≤ –Ш–Ъ–† –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–Є—Б—М –њ–Њ–ї—Г—Б—В—А—Г–Ї—В—Г—А–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є–љ—В–µ—А–≤—М—О, –∞ —В–∞–Ї–ґ–µ –ї–Є–±–Њ –Њ—Ж–µ–љ–Њ—З–љ–∞—П —И–Ї–∞–ї–∞, –ї–Є–±–Њ —Д–Њ—А–Љ–∞–ї—М–љ—Л–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є–µ –Ї—А–Є—В–µ—А–Є–Є. –Ю–і–Є–љ –Є–ї–Є –±–Њ–ї–µ–µ –≤–Є–і –Ш–Ъ–† –±—Л–ї –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ —Г 13,6% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (–∞–Ј–∞—А—В–љ—Л–µ –Є–≥—А—Л –≤ 5,0% —Б–ї—Г—З–∞–µ–≤, –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ–µ —Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–µ –њ–Њ–≤–µ–і–µ–љ–Є–µ вАУ –≤ 3,5%, –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ—Л–µ –њ–Њ–Ї—Г–њ–Ї–Є вАУ –≤ 5,7%, —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–Њ –њ–Є—Й–µ–≤–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П вАУ –≤ 4,3%). 3,9% —Г—З–∞—Б—В–љ–Є–Ї–Њ–≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Є–Љ–µ–ї–Є 2 –Є –±–Њ–ї–µ–µ –≤–Є–і–∞ –Ш–Ъ–†. –Р–љ–∞–ї–Њ–≥–Є—З–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –±—Л–ї–Є –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ—Л –≤ –Ї—А—Г–њ–љ–Њ–Љ –∞–Ј–Є–∞—В—Б–Ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є [21].
–Т –љ–µ–±–Њ–ї—М—И–Њ–Љ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ –Њ–і–љ–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б —Г—З–∞—Б—В–Є–µ–Љ 226 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —З–∞—Б—В–Њ—В–∞ –Ш–Ъ–† —Б–Њ—Б—В–∞–≤–Є–ї–∞ 15% [22].
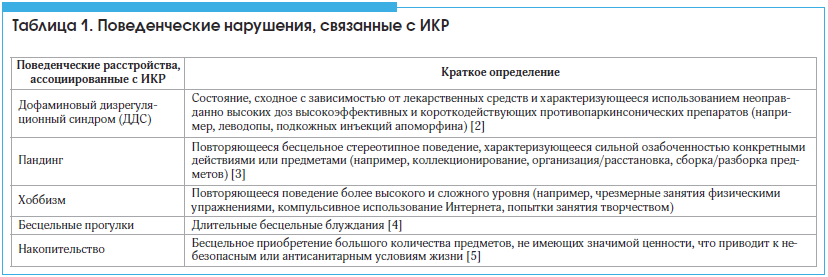
–Ф–Ф–° –Є –і—А—Г–≥–Є–µ –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Ш–Ъ–†, –љ–µ –±—Л–ї–Є —В–∞–Ї –њ–Њ–і—А–Њ–±–љ–Њ –Є–Ј—Г—З–µ–љ—Л, –Ї–∞–Ї –Њ—Б–љ–Њ–≤–љ—Л–µ –≤–Є–і—Л –љ–∞—А—Г—И–µ–љ–Є–є –Є–Љ–њ—Г–ї—М—Б–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –≤–њ–µ—А–≤—Л–µ –±—Л–ї –Њ–њ–Є—Б–∞–љ —Д–µ–љ–Њ–Љ–µ–љ –і–Њ—Д–∞–Љ–Є–љ–Њ–≤–Њ–є –і–Є–Ј—А–µ–≥—Г–ї—П—Ж–Є–Є, –∞–≤—В–Њ—А—Л –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–ї–Є 15 —Б–ї—Г—З–∞–µ–≤ –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є. –Ю–і–љ–∞–Ї–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ—В—Б—Г—В—Б—В–≤—Г—О—В –і–∞–љ–љ—Л–µ –њ–Њ–њ–µ—А–µ—З–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Є –Ї—Г–Љ—Г–ї—П—В–Є–≤–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є –Ф–Ф–°. –І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –њ–∞–љ–і–Є–љ–≥–∞, —В–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Я, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –љ–∞ —В–µ—А–∞–њ–Є–Є —Б –≤—Л—Б–Њ–Ї–Њ–є —Н–Ї–≤–Є–≤–∞–ї–µ–љ—В–љ–Њ–є –і–Њ–Ј–Њ–є –ї–µ–≤–Њ–і–Њ–њ—Л, –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –Ї—А–Є—В–µ—А–Є—П–Љ –њ–∞–љ–і–Є–љ–≥–∞ –Њ—В–≤–µ—З–∞—О—В 14% –±–Њ–ї—М–љ—Л—Е [3], –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –≤ –µ—Й–µ –±–Њ–ї–µ–µ –Ї—А—Г–њ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –С–Я, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –і–ї—П –∞–љ–∞–ї–Є–Ј–∞ –љ–µ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї–∞—Б—М —Б—В—А–Њ–≥–Њ –Њ—В–Њ–±—А–∞–љ–љ–∞—П –≥—А—Г–њ–њ–∞, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –њ–∞–љ–і–Є–љ–≥–∞ —Б–Њ—Б—В–∞–≤–Є–ї–∞ 1,4% [23]. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –і–ї—П –њ–∞–љ–і–Є–љ–≥–∞, –∞ —В–∞–Ї–ґ–µ –і–ї—П –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ш–Ъ–† (–љ–∞–њ—А–Є–Љ–µ—А, –≥–Є–њ–µ—А—Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ—Б—В–Є) –љ–µ —Б—Г—Й–µ—Б—В–≤—Г–µ—В –Њ–±—Й–µ–њ—А–Є–љ—П—В—Л—Е –і–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Є—Е –Ї—А–Є—В–µ—А–Є–µ–≤. –≠—В–Њ –Љ–Њ–ґ–µ—В –Њ–±—К—П—Б–љ—П—В—М –≤–∞—А–Є–∞—Ж–Є–Є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В–Є, –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ—Л–µ –і–ї—П –Љ–љ–Њ–≥–Є—Е –Є–Ј —Н—В–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤.
–Э–∞—А—Г—И–µ–љ–Є–µ –Є–Љ–њ—Г–ї—М—Б–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Є –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л
–Р–≥–Њ–љ–Є—Б—В—Л –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤
–£–ґ–µ –≤ –њ–µ—А–≤—Л—Е –њ—Г–±–ї–Є–Ї–∞—Ж–Є—П—Е —Б–ї—Г—З–∞–µ–≤ –Ш–Ъ–† –Є –Ї—А–Њ—Б—Б-—Б–µ–Ї—Ж–Є–Њ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –Њ–±—Б—Г–ґ–і–∞–ї–∞—Б—М —Б–≤—П–Ј—М –љ–∞—А—Г—И–µ–љ–Є–є –Є–Љ–њ—Г–ї—М—Б–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –њ—А–Є –С–Я –Є –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ —Б –∞–≥–Њ–љ–Є—Б—В–∞–Љ–Є –і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–Р–Ф–†). –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DOMINION [20] –Ш–Ъ–† –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —З–∞—Й–µ –≤—Б—В—А–µ—З–∞–ї–Є—Б—М —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Р–Ф–† (17,1%), –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –љ–µ –њ—А–Є–љ–Є–Љ–∞—О—Й–Є–Љ–Є —Н—В—Г –≥—А—Г–њ–њ—Г –њ—А–µ–њ–∞—А–∞—В–Њ–≤ (6,9%). –Ы–µ—З–µ–љ–Є–µ –Р–Ф–† –њ—А–Є –С–Я –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–ї–Њ—Б—М —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —И–∞–љ—Б–Њ–≤ —А–∞–Ј–≤–Є—В–Є—П –Ш–Ъ–† –≤ 2вАУ3 —А–∞–Ј–∞. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ—А–∞–Љ–Є–њ–µ–Ї—Б–Њ–ї –Є —А–Њ–њ–Є–љ–Є—А–Њ–ї (2 –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е –Р–Ф–†), —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –Ш–Ъ–† –±—Л–ї–∞ —Б–Њ–њ–Њ—Б—В–∞–≤–Є–Љ–Њ–є (17,7 –Є 15,5% —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ). –Я—А–Є–µ–Љ —Н—В–Є—Е –љ–µ—Н—А–≥–Њ–ї–Є–љ–Њ–≤—Л—Е –Р–Ф–† –≤—В–Њ—А–Њ–≥–Њ –њ–Њ–Ї–Њ–ї–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ –Ј–љ–∞—З–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ш–Ъ–†. –Ш—Е –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–∞—П —Б–µ–ї–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є D2-–њ–Њ–і–Њ–±–љ—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (—А–µ—Ж–µ–њ—В–Њ—А—Л D3 –Є D2), –Ї–Њ—В–Њ—А—Л–µ –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Њ–љ–љ–Њ —Б–≤—П–Ј–∞–љ—Л —Б –Љ–µ–Ј–Њ–Ї–Њ—А—В–Є–Ї–Њ–ї–Є–Љ–±–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є, –≤–µ—А–Њ—П—В–љ–Њ, –Є –Њ–±—К—П—Б–љ—П—О—В –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ –±–ЊћБ–ї—М—И—Г—О —З–∞—Б—В–Њ—В—Г –Ш–Ъ–† –њ—А–Є –њ—А–Є–µ–Љ–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –С—Л–ї–∞ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ–∞ —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –∞–љ—В–Є–њ—Б–Є—Е–Њ—В–Є–Ї–Њ–Љ –∞—А–Є–њ–Є–њ—А–∞–Ј–Њ–ї–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є —П–≤–ї—П–µ—В—Б—П —З–∞—Б—В–Є—З–љ—Л–Љ –∞–≥–Њ–љ–Є—Б—В–Њ–Љ —А–µ—Ж–µ–њ—В–Њ—А–∞ D3, –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ш–Ъ–† [24]. –І—В–Њ –ґ–µ –Ї–∞—Б–∞–µ—В—Б—П —А–Њ–ї–Є –і–Њ–Ј—Л –Р–Ф–†, —В–Њ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е —А–∞–±–Њ—В–∞—Е –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ —З–µ—В–Ї–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Љ–µ–ґ–і—Г –і–Њ–Ј–Њ–є –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–Њ–≥–Њ –Р–Ф–† –Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ш–Ъ–† [25, 26]. –Ю–і–љ–∞–Ї–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DOMINION —В–∞–Ї–∞—П —Б–≤—П–Ј—М –љ–µ –љ–∞–±–ї—О–і–∞–ї–∞—Б—М. –°—Г—Й–µ—Б—В–≤—Г–µ—В –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–µ –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М—Б—В–≤–Њ —В–Њ–≥–Њ, —З—В–Њ –ї–µ—З–µ–љ–Є–µ –Р–Ф–† –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П (–≤ –≤–Є–і–µ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–є —Д–Њ—А–Љ—Л [27], –њ–ї–∞—Б—В—Л—А—П [27, 28] –Є–ї–Є –њ–Њ–і–Ї–Њ–ґ–љ–Њ–є –њ–Њ–Љ–њ—Л [29]) —Б–љ–Є–ґ–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ш–Ъ–†, —Е–Њ—В—П –і–ї—П –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П —Н—В–Њ–є –≥–Є–њ–Њ—В–µ–Ј—Л –љ–µ–Њ–±—Е–Њ–і–Є–Љ—Л –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–µ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П.–Ы–µ–≤–Њ–і–Њ–њ–∞, –∞–Љ–∞–љ—В–∞–і–Є–љ—Л –Є –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Ь–Р–Ю-–Т
–Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DOMINION –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –ї–µ–≤–Њ–і–Њ–њ—Л, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј–∞—Е [20, 26], –Є –∞–Љ–∞–љ—В–∞–і–Є–љ–∞ [30] —В–∞–Ї–ґ–µ –±—Л–ї–Њ —Б–≤—П–Ј–∞–љ–Њ —Б —А–∞–Ј–≤–Є—В–Є–µ–Љ –Ш–Ъ–†, –Њ–і–љ–∞–Ї–Њ –≤ –Љ–µ–љ—М—И–µ–є —Б—В–µ–њ–µ–љ–Є, —З–µ–Љ –ї–µ—З–µ–љ–Є–µ –Р–Ф–†. –Т –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —В–∞–Ї–ґ–µ –±—Л–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—П –Љ–µ–ґ–і—Г –Ш–Ъ–† –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –∞–Љ–∞–љ—В–∞–і–Є–љ–∞ [31]. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –µ—Б—В—М —Б–Њ–Њ–±—Й–µ–љ–Є–µ –Њ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ–є —Б–≤—П–Ј–Є –Љ–µ–ґ–і—Г –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–Љ –Љ–Њ–љ–Њ–∞–Љ–Є–љ–Њ–Ї—Б–Є–і–∞–Ј—Л-B (MAO-B), –Њ—Б–Њ–±–µ–љ–љ–Њ —А–∞–Ј–∞–≥–Є–ї–Є–љ–Њ–Љ, –Є –Ш–Ъ–† –њ—А–Є –С–Я [32]. –Э–∞–±–ї—О–і–µ–љ–Є—П –Ј–∞ –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є, –њ–Њ–ї—Г—З–∞—О—Й–Є–Љ–Є –Є–љ—В—А–∞–і—Г–Њ–і–µ–љ–∞–ї—М–љ—Г—О –Є–љ—Д—Г–Ј–Є—О –≥–µ–ї—П –ї–µ–≤–Њ–і–Њ–њ—Л-–Ї–∞—А–±–Є–і–Њ–њ—Л, —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В –Њ –±–Њ–ї–µ–µ –љ–Є–Ј–Ї–Є—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П—Е –Ш–Ъ–† [33], —З—В–Њ –њ–ї–∞–љ–Є—А—Г–µ—В—Б—П –њ–Њ–і—В–≤–µ—А–і–Є—В—М –≤ –і–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е.–Э–∞—А—Г—И–µ–љ–Є–µ –Є–Љ–њ—Г–ї—М—Б–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –Є –≥–ї—Г–±–Њ–Ї–∞—П —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ (DBS)
–°–≤—П–Ј—М –Љ–µ–ґ–і—Г DBS –Є –Ш–Ъ–† –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В—Б—П —Б–ї–Њ–ґ–љ–Њ–є –Є –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤–Њ–є [34]. –†–∞–љ–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ DBS c—Г–±—В–∞–ї–∞–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ —П–і—А–∞ (STN DBS) –∞—Б—Б–Њ—Ж–Є–Є—А—Г–µ—В—Б—П —Б —Г–ї—Г—З—И–µ–љ–Є–µ–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ш–Ъ–†, —З—В–Њ, –≤–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, –Њ–±—К—П—Б–љ—П–µ—В—Б—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–Љ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ–Љ –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –Р–Ф–†, –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є [35, 36]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –±–Њ–ї–µ–µ –њ–Њ–Ј–і–љ–Є–µ –Ї—А–Њ—Б—Б-—Б–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ –Є –њ—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ DBS —Б–∞–Љ–∞ –њ–Њ —Б–µ–±–µ –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М –Є–ї–Є —Г—Б—Г–≥—Г–±–ї—П—В—М –Ш–Ъ–† [37], —Е–Њ—В—П –∞–љ–∞–ї–Є–Ј —В–∞–Ї–Є—Е —Б–ї—Г—З–∞–µ–≤ –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –Љ–љ–Њ–≥–Є–µ –Є–Ј —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Њ–і–Њ–ї–ґ–∞–ї–Є –њ–Њ–ї—Г—З–∞—В—М —В—Г –ґ–µ –Є–ї–Є –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї—Г—О –і–Њ–Ј—Г –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ—Б–ї–µ –Њ–њ–µ—А–∞—Ж–Є–Є [38]. –Я—А–Є –Є–Ј—Г—З–µ–љ–Є–Є –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д—Г–љ–Ї—Ж–Є–є –љ–∞ —Д–Њ–љ–µ DBS –њ–∞—Ж–Є–µ–љ—В—Л —Б –С–Я –±–µ–Ј –Ш–Ъ–† –≤ –њ–µ—А–Є–Њ–і —Б –≤–Ї–ї—О—З–µ–љ–љ—Л–Љ —Б—В–Є–Љ—Г–ї—П—В–Њ—А–Њ–Љ –±—Л–ї–Є –±–Њ–ї–µ–µ –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ—Л –≤ –њ—А–Є–љ—П—В–Є–Є —А–µ—И–µ–љ–Є–є [39]. –Р–≤—В–Њ—А—Л –і—А—Г–≥–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є, —З—В–Њ DBS —Г—Б–Є–ї–Є–≤–∞–µ—В –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ—Б—В—М, –њ—А–µ–ґ–і–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –љ–µ–Њ–±–і—Г–Љ–∞–љ–љ–Њ–µ —А–µ–∞–≥–Є—А–Њ–≤–∞–љ–Є–µ –≤ –Ї–Њ–љ—Д–ї–Є–Ї—В–љ—Л—Е —Б–Є—В—Г–∞—Ж–Є—П—Е, –Њ–і–љ–∞–Ї–Њ —Г–ї—Г—З—И–∞–µ—В –Є–љ–≥–Є–±–Є—А—Г—О—Й–Є–є –Ї–Њ–љ—В—А–Њ–ї—М –≤ –њ—А–Њ—Ж–µ—Б—Б–µ —Б–∞–Љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є [40].–Р—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Ш–Ъ–† —Б –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–Љ–Є –Є –і—А—Г–≥–Є–Љ–Є –љ–µ–Љ–Њ—В–Њ—А–љ—Л–Љ–Є —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –С–Я
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ—А–Є –С–Я –Љ–Њ–≥—Г—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л, –≤ –љ–µ–Ї–Њ—В–Њ—А–Њ–є —Б—В–µ–њ–µ–љ–Є —Б—Е–Њ–і–љ—Л–µ –њ–Њ —Б–≤–Њ–Є–Љ –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ —Б –Ш–Ъ–†. –Ґ–∞–Ї–Є–Љ –њ—А–Є–Љ–µ—А–Њ–Љ —П–≤–ї—П–µ—В—Б—П –Њ–±—Б–µ—Б—Б–Є–≤–љ–Њ-–Ї–Њ–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–Њ (–Ю–Ъ–†), –Ї–Њ—В–Њ—А–Њ–µ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ–Њ–≤—В–Њ—А–µ–љ–Є–µ–Љ –љ–∞–≤—П–Ј—З–Є–≤—Л—Е –Є —Г—В–Њ–Љ–Є—В–µ–ї—М–љ—Л—Е –і–µ–є—Б—В–≤–Є–є (–љ–∞–њ—А–Є–Љ–µ—А, —Б—З–µ—В, –њ–Њ–≤—В–Њ—А–µ–љ–Є–µ —Б–ї–Њ–≤, –њ–Њ–≤—В–Њ—А—П—О—Й–Є–µ—Б—П –њ—А–Њ–≤–µ—А–Ї–Є —Б–Њ–±—Б—В–≤–µ–љ–љ—Л—Е –і–µ–є—Б—В–≤–Є–є), –љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –љ–∞ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —В—А–µ–≤–Њ–≥–Є, –≤—Л–Ј–≤–∞–љ–љ–Њ–є –љ–∞–≤—П–Ј—З–Є–≤—Л–Љ–Є –Љ—Л—Б–ї—П–Љ–Є. –Ю–Ъ–† –њ—А–Є –С–Я –≤—Б—В—А–µ—З–∞–µ—В—Б—П –±–Њ–ї–µ–µ —З–∞—Б—В–Њ, —З–µ–Љ –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є, –Њ–і–љ–∞–Ї–Њ, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –Ш–Ъ–†, –љ–µ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є–Є –Ю–Ъ–† —Б –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є [41].–Т –Ї—А—Г–њ–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Љ–µ—В–Њ–і–∞ ¬Ђ—Б–ї—Г—З–∞–є вАУ –Ї–Њ–љ—В—А–Њ–ї—М¬ї, —Б–Њ–Њ–±—Й–∞–ї–Њ—Б—М, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Я –Є –Ш–Ъ–†, —Г—З–∞—Б—В–≤–Њ–≤–∞–≤—И–Є—Е –і–Њ —Н—В–Њ–≥–Њ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DOMINION, –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –і–µ–њ—А–µ—Б—Б–Є—П –Є —В—А–µ–≤–Њ–≥–∞, –Ю–Ъ–†, –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ—Б—В—М –Є —Б–Ї–ї–Њ–љ–љ–Њ—Б—В—М –Ї –њ–Њ–Є—Б–Ї—Г –љ–Њ–≤–Є–Ј–љ—Л [42]. –Ф—А—Г–≥–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–Є —В–∞–Ї–ґ–µ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–ї–Є –∞—Б—Б–Њ—Ж–Є–∞—Ж–Є—О –Љ–µ–ґ–і—Г —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Ш–Ъ–† –Є –і–µ–њ—А–µ—Б—Б–Є–µ–є [2, 43вАУ45], —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В—М—О [46], –њ—Б–Є—Е–Њ–Ј–Њ–Љ [26], –∞–љ–≥–µ–і–Њ–љ–Є–µ–є (–љ–µ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Є—Б–њ—Л—В—Л–≤–∞—В—М —Г–і–Њ–≤–Њ–ї—М—Б—В–≤–Є–µ) [47] –Є –∞–ї–µ–Ї—Б–Є—В–Є–Љ–Є–µ–є, –Ї–Њ—В–Њ—А–∞—П –њ—А–Њ—П–≤–ї—П–µ—В—Б—П —В—А—Г–і–љ–Њ—Б—В—П–Љ–Є –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є, –Њ–њ–Є—Б–∞–љ–Є–Є, —А–∞–Ј–ї–Є—З–µ–љ–Є–Є –Є –Є–і–µ–љ—В–Є—Д–Є–Ї–∞—Ж–Є–Є —Б–Њ–±—Б—В–≤–µ–љ–љ—Л—Е –Є —З—Г–ґ–Є—Е —Н–Љ–Њ—Ж–Є–є [48]. –Т –љ–µ–і–∞–≤–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–Љ —А–Њ—Б—Б–Є–є—Б–Ї–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Њ–і–љ–Њ—Ж–µ–љ—В—А–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –С–Я –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–Ъ–† –±—Л–ї–∞ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –±–ЊћБ–ї—М—И–∞—П —З–∞—Б—В–Њ—В–∞ –љ–µ —В–Њ–ї—М–Ї–Њ –і–µ–њ—А–µ—Б—Б–Є–Є, –љ–Њ –Є –љ–µ–є—А–Њ—В–Є—Ж–Є–Ј–Љ–∞ [49]. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–Ъ–† –њ—А–Є –С–Я —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–µ–љ–∞ –±–ЊћБ–ї—М—И–∞—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –љ–∞—А—Г—И–µ–љ–Є–є —Б–љ–∞, –∞ –Є–Љ–µ–љ–љ–Њ —Е—Г–і—И–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–љ–∞, –і–љ–µ–≤–љ–∞—П —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, —Б–Є–љ–і—А–Њ–Љ –±–µ—Б–њ–Њ–Ї–Њ–є–љ—Л—Е –љ–Њ–≥ [50, 51], —Е—Г–і—И–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –њ–Њ —И–Ї–∞–ї–µ —Б–љ–∞ PDSS [49]. –Ш–љ—В–µ—А–µ—Б–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ –љ–µ–і–∞–≤–љ–µ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –±—Л–ї–∞ –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–љ–∞ —Б–Є–ї—М–љ–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Б–Є–Љ–њ—В–Њ–Љ–∞–Љ–Є –Ш–Ъ–† –Є –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –њ–Њ–≤–µ–і–µ–љ–Є—П –≤ —Д–∞–Ј—Г —Б–љ–∞ —Б –±—Л—Б—В—А—Л–Љ –і–≤–Є–ґ–µ–љ–Є–µ–Љ –≥–ї–∞–Ј, –Ї–Њ—В–Њ—А–∞—П –љ–µ –Ј–∞–≤–Є—Б–µ–ї–∞ –Њ—В —В–Є–њ–∞ –њ—А–Є–љ–Є–Љ–∞–µ–Љ–Њ–≥–Њ –Р–Ф–†, –і–µ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е –Є–ї–Є –і—А—Г–≥–Є—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї [52].
–Э–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—П –Ш–Ъ–†
–Ь–µ—Е–∞–љ–Є–Ј–Љ—Л —А–∞–Ј–≤–Є—В–Є—П –Ш–Ъ–† –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –і–Њ –Ї–Њ–љ—Ж–∞ –љ–µ –Є–Ј—Г—З–µ–љ—Л. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П –≤ —Д—Г–љ–Ї—Ж–Є–Њ–љ–Є—А–Њ–≤–∞–љ–Є–Є –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –њ—Г—В–µ–є, –Ї–Њ—В–Њ—А—Л–µ –љ–∞–±–ї—О–і–∞—О—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ш–Ъ–† –њ—А–Є –С–Я, —В–∞–Ї–ґ–µ –±—Л–ї–Є –њ–Њ–Ї–∞–Ј–∞–љ—Л –Є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є–Ј–Љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –њ–Є—Й–µ–≤–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б—В—А–∞—Б—В—М—О –Ї –∞–Ј–∞—А—В–љ—Л–Љ –Є–≥—А–∞–Љ –Є –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ–Љ –њ—Б–Є—Е–Њ–∞–Ї—В–Є–≤–љ—Л–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є. –Ф–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤ –Њ—Б–љ–Њ–≤–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П –ї–µ–ґ–Є—В –і–Є—Б—Д—Г–љ–Ї—Ж–Є—П –Љ–µ–Ј–Њ–Ї–Њ—А—В–Є–Ї–Њ–ї–Є–Љ–±–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Ь–µ–Ј–Њ–ї–Є–Љ–±–Є—З–µ—Б–Ї–Є–є –Є –Љ–µ–Ј–Њ–Ї–Њ—А—В–Є–Ї–∞–ї—М–љ—Л–є –њ—Г—В–Є (–і–≤–∞ –љ–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л—Е –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е –њ—Г—В–Є –Љ–Њ–Ј–≥–∞) –Њ—В–≤–µ—З–∞—О—В –Ј–∞ –њ—А–Њ—Ж–µ—Б—Б –Њ–±—Г—З–µ–љ–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –њ–Њ–Њ—Й—А–µ–љ–Є—П –Є –Ј–∞ –њ—А–Є–љ—П—В–Є–µ –Є—Б–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е —А–µ—И–µ–љ–Є–є —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ. –Ь–µ–Ј–Њ–Ї–Њ—А—В–Є–Ї–∞–ї—М–љ—Л–є –њ—Г—В—М —А–µ–≥—Г–ї–Є—А—Г–µ—В –њ—А–Є–љ—П—В–Є–µ —А–µ—И–µ–љ–Є–є, —Б–≤—П–Ј–∞–љ–љ—Л—Е —Б –Њ—Ж–µ–љ–Ї–Њ–є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є –Ј–љ–∞—З–Є–Љ–Њ—Б—В–Є –Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–є —Ж–µ–љ–љ–Њ—Б—В–Є –њ—А–Є–љ—П—В–Њ–≥–Њ —А–µ—И–µ–љ–Є—П. –Ь–µ–Ј–Њ–Ї–Њ—А—В–Є–Ї–Њ–ї–Є–Љ–±–Є—З–µ—Б–Ї–∞—П –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П —Б–µ—В—М —Б–≤—П–Ј—Л–≤–∞–µ—В –Ї–ї—О—З–µ–≤—Л–µ –Ї–Њ—А–Ї–Њ–≤—Л–µ –Є –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤—Л–µ –Њ–±–ї–∞—Б—В–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–µ–љ—В—А–Њ–Љ–µ–і–Є–∞–ї—М–љ—Г—О –њ—А–µ—Д—А–Њ–љ—В–∞–ї—М–љ—Г—О –Ї–Њ—А—Г, –≤–µ–љ—В—А–∞–ї—М–љ—Л–є —Б—В—А–Є–∞—В—Г–Љ, –≤–µ–љ—В—А–∞–ї—М–љ—Л–є —В–µ–≥–Љ–µ–љ—В—Г–Љ –Є –∞–Љ–Є–≥–і–∞–ї—Г [53], –Є –Є–≥—А–∞–µ—В —А–µ—И–∞—О—Й—Г—О —А–Њ–ї—М –≤ —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –Є –њ–Њ–і–Ї—А–µ–њ–ї–µ–љ–Є–Є –Њ–±—Г—З–µ–љ–Є—П [54вАУ56].–Я—А–Њ–≤–Њ–Ї–∞—Ж–Є—П –Ш–Ъ–† –љ–∞ —Д–Њ–љ–µ –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ —А–µ—Ж–µ–њ—В–Њ—А–љ—Л–Љ –њ—А–Њ—Д–Є–ї–µ–Љ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞. –Я–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–µ–≤–Њ–і–Њ–њ–Њ–є –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Р–Ф–† –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є –Є–Љ–µ—О—В –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –∞–Ї—В–Є–≤–∞—Ж–Є–Є —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –і–Њ—Д–∞–Љ–Є–љ–∞ D3:D2 –Є D3:D1 [57]. D3-–і–Њ—Д–∞–Љ–Є–љ–Њ–≤—Л–µ —А–µ—Ж–µ–њ—В–Њ—А—Л —Б–Ї–Њ–љ—Ж–µ–љ—В—А–Є—А–Њ–≤–∞–љ—Л –≤ –≤–µ–љ—В—А–∞–ї—М–љ–Њ–Љ —Б—В—А–Є–∞—В—Г–Љ–µ, –±–ї–µ–і–љ–Њ–Љ —И–∞—А–µ, –≤–µ–љ—В—А–∞–ї—М–љ–Њ–Љ –Њ—В–і–µ–ї–µ —Б–Ї–Њ—А–ї—Г–њ—Л –Є –Љ–µ–і–Є–∞–ї—М–љ–Њ–Љ –і–Њ—А–Ј–∞–ї—М–љ–Њ–Љ —П–і—А–µ —В–∞–ї–∞–Љ—Г—Б–∞, —Г—З–∞—Б—В–≤—Г—О—В –≤ –Љ–µ–і–Є–∞—Ж–Є–Є –њ–Њ –Љ–µ–Ј–Њ–ї–Є–Љ–±–Є—З–µ—Б–Ї–Є–Љ –њ—Г—В—П–Љ, —Б–≤—П–Ј–∞–љ–љ—Л–Љ —Б –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ–Є –њ–Њ–Њ—Й—А–µ–љ–Є—П/–Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є [58]. –Э–∞–њ—А–Њ—В–Є–≤, —А–µ—Ж–µ–њ—В–Њ—А—Л D1 –Є D2 –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —А–∞—Б–њ–Њ–ї–∞–≥–∞—О—В—Б—П –≤ –і–Њ—А–Ј–∞–ї—М–љ–Њ–Љ —Б—В—А–Є–∞—В—Г–Љ–µ –Є —Г—Б–Є–ї–Є–≤–∞—О—В –Љ–Њ—В–Њ—А–љ—Л–µ –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є —З–µ—А–µ–Ј –љ–Є–≥—А–Њ—Б—В—А–Є–∞–ї—М–љ—Л–µ –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–µ –њ—Г—В–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ –њ—А–µ–і–њ–Њ–ї–∞–≥–∞—В—М, —З—В–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л–µ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Р–Ф–† –±—Г–і—Г—В –љ–µ–њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –∞–Ї—В–Є–≤–Є—А–Њ–≤–∞—В—М –Љ–µ–Ј–Њ–ї–Є–Љ–±–Є—З–µ—Б–Ї–Є–µ, –∞ –љ–µ –і–Њ—А–Ј–∞–ї—М–љ—Л–µ –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–µ –њ—Г—В–Є –Є, —Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М–љ–Њ, —Б –±–Њ–ї—М—И–µ–є –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М—О –±—Г–і—Г—В –Є–љ–і—Г—Ж–Є—А–Њ–≤–∞—В—М –Ш–Ъ–† –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –ї–µ–≤–Њ–і–Њ–њ–Њ–є –Є –і—А—Г–≥–Є–Љ–Є –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є.
–Ф–Є–∞–≥–љ–Њ—Б—В–Є–Ї–∞ –Ш–Ъ–† –Є –Љ–µ—В–Њ–і—Л –Њ—Ж–µ–љ–Ї–Є
–Я–Њ–Љ–Є–Љ–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—В–µ—А–≤—М—О –і–ї—П –Њ—Ж–µ–љ–Ї–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ш–Ъ–† –њ—А–Є –С–Я –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤—Л—Е –Є–љ—Б—В—А—Г–Љ–µ–љ—В–Њ–≤. –Ю–і–Є–љ –Є–Ј –љ–Є—Е вАУ –Њ–њ—А–Њ—Б–љ–Є–Ї MIDI (Minnesota Impulsive Disorders Interview) [59], –Ї–Њ—В–Њ—А—Л–є –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л—П–≤–Є—В—М –љ–µ–Ї–Њ—В–Њ—А—Л–µ –≤–Є–і—Л –Ш–Ъ–†, –≤—Б—В—А–µ—З–∞—О—Й–Є–µ—Б—П –њ—А–Є –С–Я. –Ф—А—Г–≥–Є–Љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–Њ–Љ —П–≤–ї—П—О—В—Б—П –Њ–њ—А–Њ—Б–љ–Є–Ї QUIP (Questionnaire for Impulsive-Compulsive Disorders in ParkinsonвАЩs Disease) [60] –Є –≤–µ—А—Б–Є—П —Н—В–Њ–≥–Њ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞ –≤ –≤–Є–і–µ –Њ—Ж–µ–љ–Њ—З–љ–Њ–є —И–Ї–∞–ї—Л (QUIP-RS) [61], –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –Ї–∞–Ї –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–Љ, —В–∞–Ї –Є —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –±—Л–ї —А–∞–Ј—А–∞–±–Њ—В–∞–љ —Б–Ї—А–Є–љ–Є–љ–≥–Њ–≤—Л–є –Њ–њ—А–Њ—Б–љ–Є–Ї DDS-PC (Dopamine Dysregulation Syndrome-Patient and Caregiver Inventory) –і–ї—П –Њ—Ж–µ–љ–Ї–Є –Ф–Ф–° [62]. –®–Є—А–Њ–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ–∞—П —И–Ї–∞–ї–∞ MDS-UPDRS (Movement Disorder Society-Unified ParkinsonвАЩs Disease Rating Scale) –≤–Ї–ї—О—З–∞–µ—В –≤ —Б–µ–±—П –Њ–і–Є–љ –њ—Г–љ–Ї—В (–Є–≥—А–Њ–Љ–∞–љ–Є—П, –≥–Є–њ–µ—А—Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–µ –њ–Њ–≤–µ–і–µ–љ–Є–µ, —Е–Њ–±–±–Є–Ј–Љ, –њ–∞–љ–і–Є–љ–≥ –Є –Ф–Ф–°) [63], —Е–Њ—В—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є, —З—В–Њ —Н—В–Њ—В –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –≤–Њ–њ—А–Њ—Б –љ–µ —П–≤–ї—П–µ—В—Б—П –≤–∞–ї–Є–і–љ—Л–Љ –≤ –Ї–∞—З–µ—Б—В–≤–µ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞ –Њ—Ж–µ–љ–Ї–Є –Ш–Ъ–† [64]. –Ґ–∞–Ї–ґ–µ –Ш–Ъ–† —Г—З–Є—В—Л–≤–∞—О—В—Б—П –≤ —И–Ї–∞–ї–µ Ardouin, –њ—А–µ–і—Б—В–∞–≤–ї—П—О—Й–µ–є —Б–Њ–±–Њ–є –њ–Њ–ї—Г—Б—В—А—Г–Ї—В—Г—А–Є—А–Њ–≤–∞–љ–љ–Њ–µ –Є–љ—В–µ—А–≤—М—О –Є–Ј 21 –њ—Г–љ–Ї—В–∞, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ—Ж–µ–љ–Є—В—М –Њ–±—Й–µ–µ –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ, –≤–Ї–ї—О—З–∞—П –і–µ–њ—А–µ—Б—Б–Є—О, –≥–Є–њ–Њ–Љ–∞–љ–Є–∞–Ї–∞–ї—М–љ–Њ–µ –Є–ї–Є –Љ–∞–љ–Є–∞–Ї–∞–ї—М–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ, —В—А–µ–≤–Њ–≥—Г, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, –≥–Є–њ–µ—А—Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ—Б—В—М, –њ—Б–Є—Е–Њ—В–Є—З–µ—Б–Ї–Є–µ —Б–Є–Љ–њ—В–Њ–Љ—Л, –∞–њ–∞—В–Є—О, –љ–µ–Љ–Њ—В–Њ—А–љ—Л–µ —Д–ї—Г–Ї—В—Г–∞—Ж–Є–Є, –Ш–Ъ–† –Є —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Ш–Ъ–† –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П [65]. –Э–∞–Ї–Њ–љ–µ—Ж, –і–ї—П –Њ—Ж–µ–љ–Ї–Є —В—П–ґ–µ—Б—В–Є –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ш–Ъ–† –±—Л–ї–∞ —Б–Њ–Ј–і–∞–љ–∞ —И–Ї–∞–ї–∞ PICS (ParkinsonвАЩs Impulse Control Scale), –Ј–∞–њ–Њ–ї–љ—П–µ–Љ–∞—П –Ї–ї–Є–љ–Є—Ж–Є—Б—В–Њ–Љ. –Ф–∞–љ–љ—Л–є –Є–љ—Б—В—А—Г–Љ–µ–љ—В –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л—П–≤–Є—В—М –Ї–∞–Ї —Б–Є–љ–і—А–Њ–Љ–∞–ї—М–љ—Л–µ, —В–∞–Ї –Є —Б—Г–±—Б–Є–љ–і—А–Њ–Љ–∞–ї—М–љ—Л–µ —Д–Њ—А–Љ—Л –Ш–Ъ–† –Є –Њ–±–ї–∞–і–∞–µ—В –≤—Л—Б–Њ–Ї–Њ–є —А–µ—В–µ—Б—В–Њ–≤–Њ–є –љ–∞–і–µ–ґ–љ–Њ—Б—В—М—О –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ [66].–Ъ–Њ—А—А–µ–Ї—Ж–Є—П –Ш–Ъ–†
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Њ–њ—Л—В –њ–Њ–Ї–∞–Ј—Л–≤–∞–µ—В, —З—В–Њ –Ш–Ъ–† –Љ–Њ–≥—Г—В –Є—Б—З–µ–Ј–∞—В—М –њ–Њ—Б–ї–µ —Б–љ–Є–ґ–µ–љ–Є—П –і–Њ–Ј—Л –њ—А–Є–љ–Є–Љ–∞–µ–Љ–Њ–≥–Њ –Р–Ф–†, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –њ–Њ–ї–љ–Њ–є –Њ—В–Љ–µ–љ–µ –њ—А–µ–њ–∞—А–∞—В–∞, –і–∞–ґ–µ –µ—Б–ї–Є –і–ї—П —Н—В–Њ–≥–Њ —В—А–µ–±—Г–µ—В—Б—П –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –і–Њ–Ј—Л –ї–µ–≤–Њ–і–Њ–њ—Л [20, 67]. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –Љ–љ–Њ–≥–Є–µ –њ–∞—Ж–Є–µ–љ—В—Л –љ–µ —Е–Њ—В—П—В –Є–ї–Є –љ–µ –Љ–Њ–≥—Г—В –њ—А–µ–Ї—А–∞—В–Є—В—М —В–µ—А–∞–њ–Є—О –Р–Ф–† –ї–Є–±–Њ –Є–Ј-–Ј–∞ –Љ–Њ—В–Њ—А–љ–Њ–≥–Њ —Г—Е—Г–і—И–µ–љ–Є—П, –ї–Є–±–Њ –Є–Ј-–Ј–∞ –њ–Њ—П–≤–ї–µ–љ–Є—П —Б–Є–љ–і—А–Њ–Љ–∞ –Њ—В–Љ–µ–љ—Л –Р–Ф–†. –°–Є–љ–і—А–Њ–Љ –Њ—В–Љ–µ–љ—Л –Р–Ф–† вАУ —Н—В–Њ —Б–ї–Њ–ґ–љ—Л–є, –љ–µ—А–µ–і–Ї–Њ —В—П–ґ–µ–ї—Л–є —Б–Є–љ–і—А–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є —Б–њ–µ—Ж–Є—Д–Є—З–µ–љ —В–Њ–ї—М–Ї–Њ –і–ї—П —Н—В–Њ–є –≥—А—Г–њ–њ—Л –њ—А–Њ—В–Є–≤–Њ–њ–∞—А–Ї–Є–љ—Б–Њ–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є –њ–Њ—Н—В–Њ–Љ—Г –љ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–Љ—П–≥—З–µ–љ –ї–µ–≤–Њ–і–Њ–њ–Њ–є –Є–ї–Є –і—А—Г–≥–Є–Љ–Є –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є.–Ъ –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –љ–∞–Ї–Њ–њ–ї–µ–љ–Њ –Њ—З–µ–љ—М –Љ–∞–ї–Њ –і–∞–љ–љ—Л—Е –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –Є–Ј—Г—З–µ–љ–Є—О –≤–ї–Є—П–љ–Є—П –љ–µ–є—А–Њ–њ—Б–Є—Е–Є–∞—В—А–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–ї–Є –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ –Ш–Ъ–† –њ—А–Є –С–Я [6]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –љ–∞–±–ї—О–і–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Њ—В–≤–µ—В–∞ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –Ї–ї–∞—Б—Б—Л –ї–µ–Ї–∞—А—Б—В–≤, –≤–Ї–ї—О—З–∞—П —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞, –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В –±—Г–њ—А–Њ–њ–Є–Њ–љ, –∞–љ—В–Є–њ—Б–Є—Е–Њ—В–Є—З–µ—Б–Ї–Є–µ —Б—А–µ–і—Б—В–≤–∞, —Б—В–∞–±–Є–ї–Є–Ј–∞—В–Њ—А—Л –љ–∞—Б—В—А–Њ–µ–љ–Є—П –Є –њ—А–Њ—В–Є–≤–Њ—Б—Г–і–Њ—А–Њ–ґ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –Ј–Њ–љ–Є—Б–∞–Љ–Є–і. –Т –љ–µ–±–Њ–ї—М—И–Њ–Љ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Њ–Њ–±—Й–∞–ї–Њ—Б—М –Њ –њ–Њ–ї—М–Ј–µ –∞–Љ–∞–љ—В–∞–і–Є–љ–∞ –≤ –Ї–∞—З–µ—Б—В–≤–µ —Б—А–µ–і—Б—В–≤–∞ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Ш–Ъ–† –њ—А–Є –С–Я [68], –Њ–і–љ–∞–Ї–Њ —В–∞–Ї–ґ–µ —Б–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –∞–Љ–∞–љ—В–∞–і–Є–љ –±—Л–ї –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ —Б –љ–∞–ї–Є—З–Є–µ–Љ –Ш–Ъ–†, –≤–Ї–ї—О—З–∞—П –Є–≥—А–Њ–Љ–∞–љ–Є—О, –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є DOMINION [30], –∞ —В–∞–Ї–ґ–µ –≤ –љ–µ–і–∞–≤–љ–Њ –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ–љ–Њ–є –љ–µ–±–Њ–ї—М—И–Њ–є —Б–µ—А–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–ї—Г—З–∞–µ–≤ [31].
–Р–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –Њ–њ–Є–Њ–Є–і–љ—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ (–Љ—О –Є –Ї–∞–њ–њ–∞), —В–∞–Ї–Є–µ –Ї–∞–Ї –љ–∞–ї—В—А–µ–Ї—Б–Њ–љ –Є –љ–∞–ї–Љ–µ—Д–µ–љ, –њ—А–Њ–і–µ–Љ–Њ–љ—Б—В—А–Є—А–Њ–≤–∞–ї–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–∞ –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є–≥—А–Њ–Љ–∞–љ–Є–Є, –≥–Є–њ–µ—А—Б–µ–Ї—Б—Г–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П, –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–Љ–∞ –Є –Є–Љ–њ—Г–ї—М—Б–Є–≤–љ—Л—Е –њ–Њ–Ї—Г–њ–Њ–Ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±–µ–Ј –С–Я [69, 70]. –Я—А–Є –С–Я –љ–µ–±–Њ–ї—М—И–Њ–µ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–µ –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –љ–∞–ї—В—А–µ–Ї—Б–Њ–љ–∞ –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Ш–Ъ–† –љ–µ –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≤ –њ–µ—А–≤–Є—З–љ–Њ–є –Ї–Њ–љ–µ—З–љ–Њ–є —В–Њ—З–Ї–µ (–њ–Њ –Њ—Ж–µ–љ–Ї–µ –Ї–ї–Є–љ–Є—Ж–Є—Б—В–∞), –љ–Њ –≤—Л—П–≤–Є–ї–Њ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –і–ї—П –љ–∞–ї—В—А–µ–Ї—Б–Њ–љ–∞ –њ—А–Є –Ј–∞–њ–Њ–ї–љ–µ–љ–Є–Є —Б–∞–Љ–Є–Љ –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –Њ—Ж–µ–љ–Њ—З–љ–Њ–є —И–Ї–∞–ї—Л —В—П–ґ–µ—Б—В–Є —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ш–Ъ–† [71].
–Т –љ–∞–±–ї—О–і–∞—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ—А–Є —В–µ—А–∞–њ–Є–Є —Б –њ–Њ–Љ–Њ—Й—М—О –Є–љ—В—А–∞–і—Г–Њ–і–µ–љ–∞–ї—М–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –≥–µ–ї—П –ї–µ–≤–Њ–і–Њ–њ—Л-–Ї–∞—А–±–Є–і–Њ–њ—Л —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–µ –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –Ш–Ъ–† –Љ–Њ–≥—Г—В —Г–Љ–µ–љ—М—И–∞—В—М—Б—П –Є–ї–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –Є—Б—З–µ–Ј–∞—В—М [72]. –Р –≤ –Њ—В–Ї—А—Л—В–Њ–Љ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≥–µ–ї—П –ї–µ–≤–Њ–і–Њ–њ—Л-–Ї–∞—А–±–Є–і–Њ–њ—Л –Є –∞–њ–Њ–Љ–Њ—А—Д–Є–љ–∞ –љ–∞ —Д–Њ–љ–µ –Є–љ—Д—Г–Ј–Є–Є –ї–µ–≤–Њ–і–Њ–њ—Л –љ–µ –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –љ–Є –Њ–і–љ–Њ–≥–Њ –љ–Њ–≤–Њ–≥–Њ —Б–ї—Г—З–∞—П –Ш–Ъ–† [73].
–І—В–Њ –Ї–∞—Б–∞–µ—В—Б—П –љ–µ—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Њ–≤ –ї–µ—З–µ–љ–Є—П, —В–Њ –≤ —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–Љ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є, –≤ –Ї–Њ—В–Њ—А–Њ–Љ –Є–Ј—Г—З–∞–ї–∞—Б—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ–∞—П –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П (–Ъ–Я–Ґ), –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–ї–Њ –µ–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ –≤ –≥—А—Г–њ–њ–µ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ъ–Я–Ґ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Ї–Њ–љ—В—А–Њ–ї—М–љ–Њ–є –≥—А—Г–њ–њ–Њ–є, –≤ –Ї–Њ—В–Њ—А–Њ–є –Ъ–Я–Ґ –љ–µ –њ—А–Є–Љ–µ–љ—П–ї–∞—Б—М [74]. –Т –Њ—З–µ–љ—М –љ–µ–±–Њ–ї—М—И–Њ–є —Б–µ—А–Є–Є —Б–ї—Г—З–∞–µ–≤ —Б–Њ–Њ–±—Й–∞–ї–Њ—Б—М –Њ –≤—А–µ–Љ–µ–љ–љ–Њ–Љ —Г–ї—Г—З—И–µ–љ–Є–Є –њ—А–Њ—П–≤–ї–µ–љ–Є–є –њ–∞–љ–і–Є–љ–≥–∞ –љ–∞ —Д–Њ–љ–µ –њ–Њ–≤—В–Њ—А—П—О—Й–µ–є—Б—П —В—А–∞–љ—Б–Ї—А–∞–љ–Є–∞–ї—М–љ–Њ–є –Љ–∞–≥–љ–Є—В–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –і–Њ—А—Б–Њ–ї–∞—В–µ—А–∞–ї—М–љ–Њ–є –њ—А–µ—Д—А–Њ–љ—В–∞–ї—М–љ–Њ–є –Ї–Њ—А—Л [75].
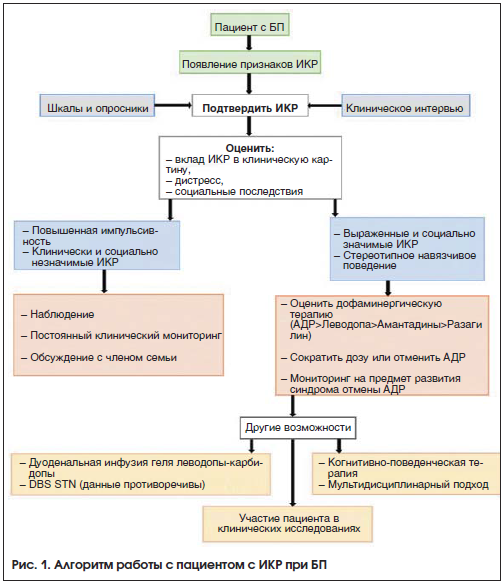
–Я—А–Є –≤—Л—П–≤–ї–µ–љ–Є–Є –Ш–Ъ–† –њ—А–Є –С–Я –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–є –∞–ї–≥–Њ—А–Є—В–Љ —А–∞–±–Њ—В—Л —Б –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ –љ–∞ —А–Є—Б—Г–љ–Ї–µ 1.