Распространенность
Частота встречаемости интраоперационных и послеоперационных инсультов зависит от типа и сложности проводимого хирургического вмешательства. Риск возникновения инсульта после общехирургических операций очень низок, в то время как кардиоваскулярные операции, в том числе комбинированные, сопряжены с высокой вероятностью его развития (табл. 1) [1–7]. Большое значение придается и продолжительности хирургического вмешательства. Кроме того, инсульты чаще развиваются после экстренных, а не плановых операций [1].
Несмотря на успехи современной хирургии и улучшение качества ухода за послеоперационными больными, частота встречаемости интраоперационных и послеоперационных инсультов не снижается, что объясняют старением населения и увеличением числа пациентов с сопутствующими заболеваниями, которым предстоит операция. Возникновение инсультов во время и после операций продлевает сроки госпитализации, обусловливает инвалидизацию, требует длительного лечения, а также может привести к летальному исходу [7].
Патофизиология
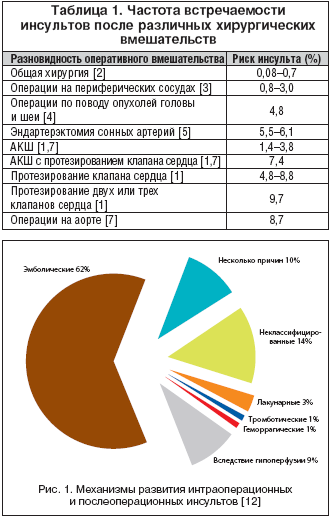
Результаты радиологических и патологоанатомических исследований говорят о том, что интраоперационные и послеоперационные инсульты являются в основном ишемическими и эмболическими [8–10]. Так, по данным исследования, которое было проведено у 388 пациентов с инсультами, развившимися после аорто–коронарного шунтирования (АКШ), геморрагический инсульт выявляется в 1% случаев, а эмболический – в 62% (рис. 1) [11]. Сроки возникновения эмболических инсультов характеризуются бимодальным распределением: примерно 45% таких инсультов развиваются на следующий день после операции [1,11], а оставшиеся 55% – после выхода из анестезии, начиная со второго дня [1,11]. Ранняя эмболия обусловлена вмешательствами на сердце и аорте или высвобождением твердых частиц из аппарата искусственного кровообращения [1,7,13]. Отсроченная эмболия чаще происходит на фоне фибрилляции предсердий в послеоперационном периоде, инфаркта миокарда, вызванного дисбалансом между потреблением и расходом кислорода, и коагулопатий [13]. Хирургическая травма и ассоциированное с ней повреждение тканей провоцирует усиление свертываемости крови. Согласно результатам различных исследований, после операции система свертывания крови стимулируется, а фибринолиз подавляется, о чем свидетельствует подавление активности тканевого активатора плазминогена и усиление активности ингибитора активатора плазминогена 1 типа, а также повышение содержания продуктов деградации фибриногена – комплекса тромбин–антитромбин, белка–предшественника тромба и D–димера – сразу после хирургического вмешательства и вплоть до 14–21 дня послеоперационного периода [14–16]. Общая анестезия, дегидратация, постельный режим, стаз в послеоперационном периоде, отказ от антитромбоцитарной и антикоагулянтной терапии во время и после операции еще больше усиливает состояние гиперкоагуляции, вызванное хирургическим вмешательством, и повышает риск возникновения тромботических явлений, в том числе и инсульта.
После АКШ наблюдаются непродолжительные и длительные когнитивные расстройства, проявляющиеся в форме кратковременной потери памяти, ограничения физической активности и психомоторной заторможенности [7]. Причины этих явлений комплексны, их провоцируют ишемическое повреждение вследствие микроэмболизации, хирургическая травма, предшествующие сосудистые изменения и колебания температуры во время операции.
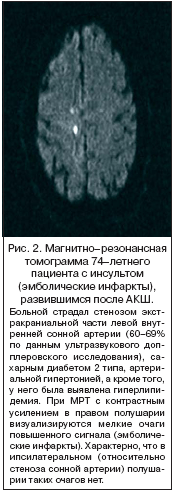
В противоположность традиционным представлениям при операциях на сердце, а также вмешательствах по поводу стеноза сонных артерий развитие инсульта не связано с гипоперфузией. Искусственная гипотензия, обусловленная анестезией, не оказывает отрицательного влияния на перфузию головного мозга и не увеличивает риск интраоперационных и послеоперационных инсультов из–за гипоперфузии при вмешательствах по поводу стеноза сонных артерий [6,11,15]. У большинства таких пациентов чаще возникают эмболические инсульты на противоположной стороне или двусторонние инсульты (рис. 2), т.е. их появление нельзя объяснить только за счет стеноза сонных артерий [6]. По данным другого исследования, лишь 9% инсультов после АКШ происходит в зонах гипоперфузии головного мозга [11]. Как и следовало ожидать, большинство таких инсультов случилось в первый день после операции. При гипоперфузии отсроченные инсульты зачастую развиваются на фоне дегидратации в послеоперационном периоде или кровопотери. Реже инсульт провоцирует воздушная, жировая или парадоксальная эмболия, а также нарушение целостности стенки артерии при проведении анестезии или выполнении операций в области шеи (табл. 2).
Стратификация риска
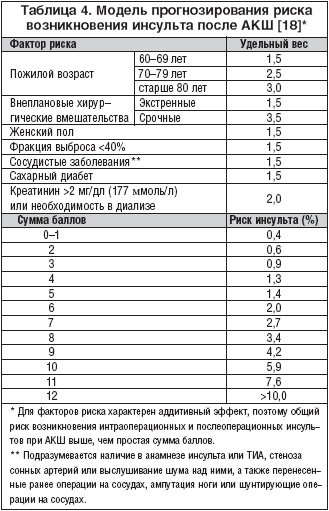
Повышение риска инсульта во время и после хирургических вмешательств связано со статусом пациента и особенностями самой операции (табл. 3) [2,4,6,8,13, 15,16]. Для оптимизации лечения у каждого больного перед операций необходимо соотнести эффективность с потенциальным риском. Существует несколько моделей для стратификации риска интраоперационных и послеоперационных инсультов [7,17]. Используя методику ступенчатого перехода, исследователи из Группы по изучению сердечно–сосудистых заболеваний севера Новой Англии разработали модель для прогнозирования риска развития инсульта после АКШ, в которой каждый из 7 признаков, оцениваемых до операции, имеет свой уровень значимости. Эти признаки были выделены на основании клинических наблюдений за 33062 пациентами, которым предстояло АКШ [17]. Основные данные по этой прогностической модели суммированы в таблице 4 [18].
Коррекция факторов риска
Осуществляя различные диагностические и лечебные мероприятия, можно скорректировать факторы риска, чтобы предотвратить интраоперационные и послеоперационные инсульты и минимизировать показатели заболеваемости. Серьезным фактором риска является наличие в анамнезе инсульта или транзиторной ишемической атаки (ТИА) [2,4, 6–8,12,13,17]. Поэтому очень важно подробно собрать анамнез, а при наличии указаний на инсульт или ТИА, произошедшие в предыдущие 6 месяцев – постараться установить их причину и провести соответствующее лечение. Это приобретает особое значение в тех случаях, если такая оценка не проводилась или была неполной, или же если после инсульта/ТИА в неврологическом статусе пациента произошло ухудшение. Зачастую в первые дни после инсульта резервы кровоснабжения головного мозга снижены, поэтому до проведения планового хирургического вмешательства должно пройти достаточное время для того, чтобы гемодинамика и неврологический статус больного успели стабилизироваться.
Симптоматический стеноз сонных артерий также ассоциируется с высоким риском интраоперационных и послеоперационных инсультов [6,19]. В этих случаях выполняют ультразвуковое доплеровское исследование сонных артерий; если симптоматический стеноз сонных артерий возник не позднее, чем за 6 месяцев до момента обследования, перед кардиоваскулярной операцией целесообразно предпринять реваскуляризирующее вмешательство [20]. У пациентов с сочетанным поражением сердца и сонных артерий, которым предстоит экстренная операция на сердце (у таких пациентов вероятность развития осложнений и гибели из–за заболевания сердца гораздо выше, чем риск инсульта), можно провести комбинированное вмешательство (реваскуляризация сонных артерий одновременно с АКШ) или две последовательные операции в обратной последовательности (реваскуляризация сонных артерий после АКШ). Однако комбинированный метод ассоциируется с большей распространенностью инсультов [23]. Безопасность эндартерэктомии по сравнению со стентированием сонных артерий дискутируется. Предварительные результаты исследований по этому вопросу свидетельствует о том, что при сочетанном симптоматическом стенозе сонных артерий и поражении коронарных сосудов у пациентов, которым на первом этапе предстоит реваскуляризация сонных артерий, лучше, по–видимому, выполнить стентирование [22].
Влияние бессимптомного стеноза сонных артерий, в особенности монолатерального, на вероятность развития интраоперационных и послеоперационных инсультов, зачастую преувеличено. Данные научной литературы за период с 1970 по 2000 гг. показывают, что риск возникновения инсульта после АКШ в целом составляет 2%, при бессимптомном стенозе просвета одной из общих сонных артерий на 50–99% – 3%, при двустороннем стенозе просвета обеих общих сонных артерий на 50–99% – 5%, а при окклюзии сонных артерий – 7% [6]. В 60% случаев развитие интраоперационных и послеоперационных инсультов у больных со стенозом сонных артерий связано с другими причинами [6].
Бессимптомный стеноз сонных артерий можно заподозрить при предоперационном обследовании на основании выслушивания шума в области сосудов шеи. Поскольку выслушивание такого шума само по себе не сопряжено с высоким риском инсульта и не коррелирует с выраженностью стеноза сонных артерий [23], проведение ультразвукового допплеровского исследования в этих ситуациях не показано. Однако если в анамнезе имеются указания на ТИА, то выполнение такого исследования может быть вполне обоснованным. Далее, лишь немногие данные указывают на необходимость осуществления профилактической реваскуляризации по стандартной методике у пациентов с бессимптомным стенозом сонных артерий, которым предстоит обширная кардиоваскулярная операция [24].
Проведение реваскуляризации сонных артерий до выполнения кардиоваскулярного хирургического вмешательства, как правило, нецелесообразно, поскольку риск возникновения интраоперационных и послеоперационных инсультов и инфаркта миокарда во время этой процедуры повышается в 2 раза, а вероятность развития инсульта во время более обширной операции практически не уменьшается [6,19,20]. Тем не менее у некоторых пациентов с гемодинамически значимым выраженным бессимптомным стенозом сонных артерий (в особенности двусторонним) целесообразно осуществить реваскуляризацию сонных артерий перед плановой операцией на сердце. Таким образом, выбор тактики ведения при выявлении бессимптомного стеноза сонных артерий должен быть дифференцированным. Перед операцией следует, как минимум, провести углубленное неврологическое обследование, подробно собрать анамнез (стараясь обнаружить симптомы ТИА, о которых пациент раньше не упоминал), а также выполнить компьютерную томографию (КТ) или магнитно–резонансную томографию (МРТ) головного мозга с целью исключить «молчащие» ипсилатеральные инфаркты. Дополнительные методы обследования, такие как ультразвуковое допплеровское исследование сосудов головного мозга, КТ–ангиография или магнитно–резонансная ангиография, помогают выявить микроэмболии, определить скорость кровотока в сосудах головного мозга, обнаружить гемодинамически значимый стеноз сонных артерий [25,26] и отобрать тех больных, которым перед более обширной операцией может быть показана реваскуляризация сонных артерий. Однако клиническая и экономическая целесообразность исследовать гемодинамику до операции на сердце многими оспаривается, и поэтому до того, как включить эти диагностические процедуры в стандартные протоколы предоперационного обследования пациентов со стенозом сонных артерий, их нужно еще усовершенствовать и ратифицировать.
Атеросклероз аорты – это объективный прогностический фактор риска интраоперационных и послеоперационных инсультов, особенно у пациентов, которым предстоит операция на сердце и реваскуляризация левой венечной артерии [1,13]. Уточнить тактику хирургического лечения позволяет чреспищеводная эхокардиография или интраоперационное эпиаортальное ультразвуковое исследование, с помощью которого можно определить размеры и локализацию бляшек в аорте и на основании полученных данных изменить зону катетеризации аорты или наложения зажима с целью «обойти» кальцинированную бляшку. Проведение катетеризации аорты [27] или внутриаортальной фильтрации [28] под контролем эхокардиографии во время АКШ снижает риск интраоперационных и послеоперационных инсультов.
Систолическая дисфункция увеличивает вероятность развития инсульта во время и после операции, особенно при сопутствующей фибрилляции предсердий [13]. Эхокардиография, проводимая в предоперационном периоде для оценки фракции выброса, визуализации внутрисердечных эмболов и выявления признаков атеросклероза аорты, дает возможность стратифицировать риск инсульта и изменить тактику лечения пациентов с сердечной недостаточностью, фибрилляцией предсердий или при подозрении на пороки клапанов сердца, если на следующем этапе предполагается реваскуляризация левой венечной артерии.
Фибрилляция предсердий развивается у 30–50% пациентов, перенесших операцию на сердце. Чаще всего она возникает на второй и четвертый дни после хирургического вмешательства и служит основной причиной интраоперационных и послеоперационных инсультов [1,8,9,13,17,18,29]. Электролитный дисбаланс и повышение объема внутрисосудистой жидкости, наблюдающиеся в послеоперационном периоде, усиливают эктопическую активность предсердий, что предрасполагает к появлению аритмий (табл. 5) [29]. Поэтому очень важно на протяжении, как минимум, трех дней после операции на сердце проводить мониторинг сердечной деятельности для исключения аритмий, а также корректировать электролитный дисбаланс и объем внутрисосудистой жидкости. Частоту встречаемости послеоперационных фибрилляции предсердий и инсультов можно снизить за счет профилактического введения амиодарона и b–адреноблокаторов, которое начинают за 5 дней до хирургического вмешательства [30]. Пациентам с уже существующей фибрилляцией предсердий назначают антиаритмические препараты или лекарственные средства, контролирующие частоту сердечных сокращений, которые продолжают давать и в послеоперационном периоде, дополняя при необходимости внутривенным введением. Никаких специальных клинических испытаний, посвященных изучению целесообразности использования антикоагулянтов при вновь возникшей в послеоперационном периоде фибрилляции предсердий (которая зачастую спонтанно исчезает через 4–6 недель), не проводилось. Пациентам с высоким риском развития интраоперационных и послеоперационных инсультов (например, при наличии инсульта или ТИА в анамнезе), у которых после хирургического вмешательства возникла фибрилляция предсердий, эксперты Американской коллегии торакальной медицины рекомендуют начинать гепаринотерапию и проводить ее в течение 30 дней после восстановления нормального синусового ритма [31].
Прекращение приема варфарина или других антитромбоцитарных средств перед операцией повышает риск интраоперационных и послеоперационных инсультов [32, 33]. Вероятность их развития особенно высока при наличии ишемической болезни сердца [33]. Изучение исходов хирургических вмешательств у больных, нуждающихся в длительной терапии варфарином, свидетельствует о том, что частота встречаемости тромбоэмболий варьирует в зависимости от тактики лечения: при прекращении приема варфарина в отсутствие внутривенного введения гепарина она составляет 0,6%, а в случае внутривенного введения гепарина тромбоэмболий не бывает [34]. При приеме варфарина в терапевтической дозировке значительные кровотечения на фоне стоматологических манипуляций наблюдаются в 0,2% случаев, а при пункциях суставов, операциях по поводу катаракты, эндоскопии и колоноскопии с биопсией или без таковой кровотечений вообще не наблюдается.
Клинические исследования в группе больных с высоким риском тромбоэмболий, которым предстояло эндопротезирование коленного или тазобедренного суставов, продемонстрировали, что прием варфарина в небольшой терапевтической дозировке (международное нормализованное отношение от 1,8 до 2,1) в предоперационном периоде безопасен и является эффективным методом профилактики эмболических явлений [35]. Эти данные позволяют предположить, что в ходе подготовки больного к стоматологическим манипуляциям, артроцентезам, операциям по поводу катаракты, диагностическим эндоскопическим процедурам и даже ортопедическим операциям нет необходимости отменять антитромбоцитарные средства или антикоагулянты. Если же от приема антикоагулянтов перед проведением других инвазивных вмешательств все же приходится отказываться, то эти сроки, по возможности, должны быть минимальными. После отмены варфарина рекомендуется начать гепаринотерапию и уже в раннем послеоперационном периоде возобновить лечение антикоагулянтами. Особенно это касается пациентов с высоким риском тромбоэмболий (например, при наличии системных эмболий или фибрилляции предсердий в анамнезе, а также искусственных клапанов сердца) [36].
Продолжительность хирургического вмешательства по возможности следует сократить. Более длительные вмешательства ассоциированы с большим риском развития интраоперационных и послеоперационных инсультов. Кроме того, при выборе хирургической тактики необходимо учитывать и профиль риска у данного конкретного больного. Среди пациентов с низкой фракцией выброса риск возникновения инсульта при проведении ангиопластики коронарных сосудов меньше, чем при АКШ [37]. В группе больных с атеросклерозом аорты использование аппарата искусственного кровообращения во время АКШ повышает вероятность развития инсульта по сравнению с выполнением АКШ без этого устройства [38]. При атеросклерозе дуги аорты предпочтительна бесконтактная («no–touch») технология АКШ, не связанная с манипуляциями на восходящей части дуги аорты [39].
Также необходимо принимать во внимание метод оказания анестезиологического пособия и разновидность используемого препарата. Регионарная анестезия сопряжена с меньшей вероятностью развития послеоперационных осложнений, чем общая анестезия [40]. Есть данные, что изофлуран и тиопентал натрия могут обладать нейропротекторным действием [41].
Активно дискутируется и вопрос о том, каким должен быть оптимальный уровень артериального давления (АД) в ходе хирургического вмешательства [12, 17]. Так, согласно результатам одного из исследований, частота встречаемости сердечно–сосудистых и неврологических осложнений (в том числе инсульта) гораздо ниже, если среднее АД в ходе АКШ поддерживается в интервале 80–100 мм рт.ст., а не 50–60 мм рт.ст. (т.е. повышенное среднее АД более безопасно для проведения АКШ и улучшает исходы) [42]. Уровень АД во время операции нужно оценивать в сочетании с его значением в предоперационном периоде; изменение АД на 20 мм рт.ст. и более (20% и более) по сравнению с предоперационным уровнем ассоциируется с высоким риском интраоперационных и послеоперационных осложнений [43]. Приведение интраоперационных и послеоперационных показателей АД в соответствие с его предоперационными значениями позволяет снизить вероятность возникновения инсульта и летального исхода [27].
Температура тела также влияет на послеоперационные исходы. Если в ходе АКШ температура тела поддерживается на уровне не выше 31,4–33,1°С, то частота встречаемости интраоперационных и послеоперационных инсультов заметно уменьшается [44]. Однако в этих случаях выше вероятность смерти больного. Таким образом, чтобы избежать быстрого согревания и гипертермии после завершения АКШ и минимизировать тем самым риск появления когнитивных расстройств в послеоперационном периоде, наиболее целесообразно поддерживать гипотермию на уровне 34°С [44].
Гипергликемия (как во время, так и после операции) коррелирует с высокой распространенностью фибрилляции предсердий, инсульта и смерти [45]. В ходе операции и в послеоперационном периоде необходимо строго контролировать содержание глюкозы в крови. Введение инсулина и калия во время и после операции с целью поддержания концентрации глюкозы не выше 140 мг/дл (7,8 ммоль/л) улучшает исходы хирургического вмешательства [46].
И в предоперационном, и в послеоперационном периодах всегда нужно проводить профилактику и лечение инфекций и воспалительных процессов. Лейкоцитоз сопряжен с высоким риском инсультов, плохими исходами и возможностью развития фибрилляции предсердий после хирургического вмешательства [47,48].
Систолическая дисфункция и аритмии, возникающие в послеоперационном периоде, ассоциированы с высокой частотой встречаемости инсультов [1, 7–9]. Поэтому после операции нужно не только восстанавливать электролитный баланс и объем внутрисосудистой жидкости, но и четко отслеживать симптомы сердечной недостаточности и аритмий. В послеоперационном периоде показана ранняя мобилизация пациента и проведение мероприятий, направленных на профилактику тромбоза глубоких вен нижних конечностей. После шунтирования со сбросом крови справа налево иногда развивается парадоксальная эмболия, которая может стать причиной инсульта.
Наконец, есть данные, что прием антитромбоцитарных средств после хирургических вмешательств на сердце и сонных артериях снижает распространенность интраоперационных и послеоперационных инсультов, не повышая при этом частоту осложнений, связанных с кровотечениями [49, 50]. Кроме того, в предоперационном периоде вне зависимости от показателей липидного профиля целесообразно назначать статины, что позволяет уменьшить риск инсультов у пациентов, которым предстоит кардиоваскулярная операция [51].
Лечение
Пациентам, которые ранее перенесли обширные операции, внутривенное введение тканевого активатора плазминогена противопоказано из–за высокого риска кровотечений. Альтернативой для таких больных служат внутриартериальное введение тканевого активатора плазминогена и эндоваскулярная механическая ретракция сгустка. Результаты серии экспериментов свидетельствуют о том, что внутриартериальное введение тромболитиков не позднее, чем через 6 часов после инсульта, является достаточно безопасной процедурой [52,53]. По данным исследования, проводившегося среди 36 пациентов, которым после инсульта внутриартериально вводили тканевой активатор плазминогена, частичную или полную реканализацию удалось осуществить в 80% случаев, причем у 38% больных симптоматика полностью купировалась или же осталось лишь незначительное ограничение трудоспособности. Показатели смертности в этой группе оказались аналогичны таковым у непрооперированных пациентов, которым проводили внутриартериальный тромболизис [53]. Кровотечения из операционной раны, большинство из которых были незначительными, наблюдались в 17% случаев. У 25% больных произошли внутричерепные кровоизлияния, однако ухудшения в неврологическом статусе отмечены только в 8% случаев. Наиболее часто внутричерепные кровоизлияния возникали после трепанации черепа. Применение методов механической тромбэктомии или эмболэктомии после интраоперационных и послеоперационных инсультов подробно не изучено. Однако в послеоперационном периоде использование этих методов может быть целесообразно, особенно в тех случаях, когда внутриартериальный тромболизис противопоказан. Наличие ограничений к проведению подобных процедур лишний раз подчеркивает необходимость своевременно диагностировать интраоперационные и послеоперационные инсульты и немедленно приглашать на консультацию невролога.
Перспективы
Идея предоперационной профилактики инсульта привлекает все большее внимание. Эффективность нейропротекторов, как средств профилактики инсульта и когнитивных расстройств после АКШ, оценивали лишь в ходе нескольких рандомизированных испытаний [54–56]. Считается, что назначение в предоперационном периоде статинов [51] или b–адреноблокаторов [30] снижает распространенность инсультов и когнитивных расстройств после АКШ. Кроме того, есть данные (хотя и противоречивые), что таким же действием обладает антифибринолитический препарат апротинин/контрикал [56]. Полученные результаты свидетельствуют о том, что нейропротекторное лечение, проводимое в предоперационном периоде, может быть эффективно в плане профилактики инсультов, но требует дальнейшего изучения. Чтобы сформулировать наиболее оптимальные стратегии профилактики и лечения интраоперационных и послеоперационных инсультов, нужно дополнительно провести рандомизированные контролируемые испытания.
Реферат подготовлен Е.Б. Третьяк
по материалам статьи M. Selim «Perioperative stroke»
The New England Journal of Medicine Vol. 356: pp. 706–713, No.7, February 15, 2007


Литература
1. Bucerius J, Gummert JF, Borger MA, et al. Stroke after cardiac surgery: a risk factor analysis of 16,184 consecutive adult patients. Ann Thorac Surg 2003;75:472–478. [Free Full Text]
2. Kam PC, Calcroft RM. Peri–operative stroke in general surgical patients. Anaesthesia 1997;52:879–883. [CrossRef][ISI][Medline]
3. Gutierrez IZ, Barone DL, Makula PA, Currier C. The risk of perioperative stroke in patients with asymptomatic carotid bruits undergoing peripheral vascular surgery. Am Surg 1987;53:487–489. [ISI][Medline]
4. Nosan DK, Gomez CR, Maves MD. Perioperative stroke in patients undergoing head and neck surgery. Ann Otol Rhinol Laryngol 1993;102:717–723. [ISI][Medline]
5. Bond R, Rerkasem K, Shearman CP, Rothwell PM. Time trends in the published risks of stroke and death due to endarterectomy for symptomatic carotid stenosis. Cerebrovasc Dis 2004;18:37–46. [ISI][Medline]
6. Naylor AR, Mehta Z, Rothwell PM, Bell PR. Carotid artery disease and stroke during coronary artery bypass: a critical review of the literature. Eur J Vasc Endovasc Surg 2002;23:283–294. [CrossRef][ISI][Medline]
7. McKhann GM, Grega MA, Borowicz LM Jr, Baumgartner WA, Selnes OA. Stroke and encephalopathy after cardiac surgery: an update. Stroke 2006;37:562–571. [Free Full Text]
8. Limburg M, Wijdicks EF, Li H. Ischemic stroke after surgical procedures: clinical features, neuroimaging, and risk factors. Neurology 1998;50:895–901. [Abstract]
9. Restrepo L, Wityk RJ, Grega MA, et al. Diffusion– and perfusion–weighted magnetic resonance imaging of the brain before and after coronary artery bypass grafting surgery. Stroke 2002;33:2909–2915. [Free Full Text]
10. Brooker RF, Brown WR, Moody DM, et al. Cardiotomy suction: a major source of brain lipid emboli during cardiopulmonary bypass. Ann Thorac Surg 1998;65:1651–1655. [Free Full Text]
11. Likosky DS, Marrin CA, Caplan LR, et al. Determination of etiologic mechanisms of strokes secondary to coronary artery bypass graft surgery. Stroke 2003;34:2830–2834. [Free Full Text]
12. Likosky DS, Caplan LR, Weintraub RM, et al. Intraoperative and postoperative variables associated with strokes following cardiac surgery. Heart Surg Forum 2004;7:E271–E276. [CrossRef][ISI][Medline]
13. Hogue CW Jr, Murphy SF, Schechtman KB, Davila–Roman VG. Risk factors for early or delayed stroke after cardiac surgery. Circulation 1999;100:642–647. [Medline]
14. Dixon B, Santamaria J, Campbell D. Coagulation activation and organ dysfunction following cardiac surgery. Chest 2005;128:229–236. [CrossRef][ISI][Medline]
15. Paramo JA, Rifon J, Llorens R, Casares J, Paloma MJ, Rocha E. Intra– and postoperative fibrinolysis in patients undergoing cardiopulmonary bypass surgery. Haemostasis 1991;21:58–64. [ISI][Medline]
16. Hinterhuber G, Bohler K, Kittler H, Quehenberger P. Extended monitoring of hemostatic activation after varicose vein surgery under general anesthesia. Dermatol Surg 2006;32:632–639. [CrossRef][ISI][Medline]
17. van Wermeskerken GK, Lardenoye JW, Hill SE, et al. Intraoperative physiologic variables and outcome in cardiac surgery: Part II. Neurologic outcome. Ann Thorac Surg 2000;69:1077–1083. [Free Full Text]
18. Charlesworth DC, Likosky DS, Marrin CA, et al. Development and validation of a prediction model for strokes after coronary artery bypass grafting. Ann Thorac Surg 2003;76:436–443. [Free Full Text]
19. Gerraty RP, Gates PC, Doyle JC. Carotid stenosis and perioperative stroke risk in symptomatic and asymptomatic patients undergoing vascular or coronary surgery. Stroke 1993;24:1115–1118. [Abstract]
20. Chaturvedi S, Bruno A, Feasby T, et al. Carotid endarterectomy –– an evidence–based review: report of the Therapeutics and Technology Assessment Subcommittee of the American Academy of Neurology. Neurology 2005;65:794–801. [Free Full Text]
21. Das SK, Brow TD, Pepper J. Continuing controversy in the management of concomitant coronary and carotid disease: an overview. Int J Cardiol 2000;74:47–65. [CrossRef][ISI][Medline]
22. Yadav JS, Wholey MH, Kuntz RE, et al. Protected carotid–artery stenting versus endarterectomy in high–risk patients. N Engl J Med 2004;351:1493–1501. [Free Full Text]
23. Mackey AE, Abrahamowicz M, Langlois Y, et al. Outcome of asymptomatic patients with carotid disease. Neurology 1997;48:896–903. [Abstract]
24. Birincioglu CL, Bayazit M, Ulus AT, Bardakci H, Kucuker SA, Tasdemir O. Carotid disease is a risk factor for stroke in coronary bypass operations. J Card Surg 1999;14:417–423. [ISI][Medline]
25. Molloy J, Markus HS. Asymptomatic embolization predicts stroke and TIA risk in patients with carotid artery stenosis. Stroke 1999;30:1440–1443. [Free Full Text]
26. Soinne L, Helenius J, Tatlisumak T, et al. Cerebral hemodynamics in asymptomatic and symptomatic patients with high–grade carotid stenosis undergoing carotid endarterectomy. Stroke 2003;34:1655–1661. [Free Full Text]
27. Gold JP, Torres KE, Maldarelli W, Zhuravlev I, Condit D, Wasnick J. Improving outcomes in coronary surgery: the impact of echo–directed aortic cannulation and perioperative hemodynamic management in 500 patients. Ann Thorac Surg 2004;78:1579–1585. [Free Full Text]
28. Wimmer–Greinecker G. Reduction of neurologic complications by intra–aortic filtration in patients undergoing combined intracardiac and CABG procedures. Eur J Cardiothorac Surg 2003;23:159–164. [Free Full Text]
29. Lahtinen J, Biancari F, Salmela E, et al. Postoperative atrial fibrillation is a major cause of stroke after on–pump coronary artery bypass surgery. Ann Thorac Surg 2004;77:1241–1244. [Free Full Text]
30. Crystal E, Garfinkle MS, Connolly SS, Ginger TT, Sleik K, Yusuf SS. Interventions for preventing post–operative atrial fibrillation in patients undergoing heart surgery. Cochrane Database Syst Rev 2004;4:CD003611–CD003611. [Medline]
31. Epstein AE, Alexander JC, Gutterman DD, Maisel W, Wharton JM. Anticoagulation: American College of Chest Physicians guidelines for the prevention and management of postoperative atrial fibrillation after cardiac surgery. Chest 2005;128:Suppl 2:24S–27S. [CrossRef][ISI][Medline]
32. Maulaz AB, Bezerra DC, Michel P, Bogousslavsky J. Effect of discontinuing aspirin therapy on the risk of brain ischemic stroke. Arch Neurol 2005;62:1217–1220. [Free Full Text]
33. Genewein U, Haeberli A, Straub PW, Beer JH. Rebound after cessation of oral anticoagulant therapy: the biochemical evidence. Br J Haematol 1996;92:479–485. [CrossRef][ISI][Medline]
34. Dunn AS, Turpie AG. Perioperative management of patients receiving oral anticoagulants: a systematic review. Arch Intern Med 2003;163:901–908. [Free Full Text]
35. Larson BJ, Zumberg MS, Kitchens CS. A feasibility study of continuing dose–reduced warfarin for invasive procedures in patients with high thromboembolic risk. Chest 2005;127:922–927. [CrossRef][ISI][Medline]
36. Dunn AS, Wisnivesky J, Ho W, Moore C, McGinn T, Sacks HS. Perioperative management of patients on oral anticoagulants: a decision analysis. Med Decis Making 2005;25:387–397. [Free Full Text]
37. O'Keefe JH Jr, Allan JJ, McCallister BD, et al. Angioplasty versus bypass surgery for multivessel coronary artery disease with left ventricular ejection fraction < or = 40%. Am J Cardiol 1993;71:897–901. [CrossRef][ISI][Medline]
38. Sharony R, Grossi EA, Saunders PC, et al. Propensity case–matched analysis of off–pump coronary artery bypass grafting in patients with atheromatous aortic disease. J Thorac Cardiovasc Surg 2004;127:406–413. [Free Full Text]
39. Lev–Ran O, Braunstein R, Sharony R, et al. No–touch aorta off–pump coronary surgery: the effect on stroke. J Thorac Cardiovasc Surg 2005;129:307–313. [Free Full Text]
40. Breen P, Park KW. General anesthesia versus regional anesthesia. Int Anesthesiol Clin 2002;40:61–71. [Medline]
41. Turner BK, Wakim JH, Secrest J, Zachary R. Neuroprotective effects of thiopental, propofol, and etomidate. AANA J 2005;73:297–302. [Medline]
42. Gold JP, Charlson ME, Williams–Russo P, et al. lmprovement of outcomes after coronary artery bypass: a randomized trial comparing intraoperative high versus low mean arterial pressure. J Thorac Cardiovasc Surg 1995;110:1302–1311. [Free Full Text]
43. Charlson ME, MacKenzie CR, Gold JP, Ales KL, Topkins M, Shires GT. Intraoperative blood pressure: what patterns identify patients at risk for postoperative complications? Ann Surg 1990;212:567–580. [ISI][Medline]
44. Rees K, Beranek–Stanley M, Burke M, Ebrahim S. Hypothermia to reduce neurological damage following coronary artery bypass surgery. Cochrane Database Syst Rev 2001;1:CD002138–CD002138. [Medline]
45. Gandhi GY, Nuttall GA, Abel MD, et al. Intraoperative hyperglycemia and perioperative outcomes in cardiac surgery patients. Mayo Clin Proc 2005;80:862–866. [ISI][Medline]
46. Krinsley JS. Effect of an intensive glucose management protocol on the mortality of critically ill adult patients. Mayo Clin Proc 2004;79:992–1000. [Erratum, Mayo Clin Proc 2005;80:1101.] [ISI][Medline]
47. Albert AA, Beller CJ, Walter JA, et al. Preoperative high leukocyte count: a novel risk factor for stroke after cardiac surgery. Ann Thorac Surg 2003;75:1550–1557. [Free Full Text]
48. Lamm G, Auer J, Weber T, Berent R, Ng C, Eber B. Postoperative white blood cell count predicts atrial fibrillation after cardiac surgery. J Cardiothorac Vasc Anesth 2006;20:51–56. [CrossRef][ISI][Medline]
49. Mangano DT. Aspirin and mortality from coronary bypass surgery. N Engl J Med 2002;347:1309–1317. [Free Full Text]
50. Engelter S, Lyrer P. Antiplatelet therapy for preventing stroke and other vascular events after carotid endarterectomy. Cochrane Database Syst Rev 2003;3:CD001458–CD001458. [Medline]
51. Durazzo AE, Machado FS, Ikeoka DT, et al. Reduction in cardiovascular events after vascular surgery with atorvastatin: a randomized trial. J Vasc Surg 2004;39:967–975. [CrossRef][ISI][Medline]
52. Moazami N, Smedira NG, McCarthy PM, et al. Safety and efficacy of intraarterial thrombolysis for perioperative stroke after cardiac operation. Ann Thorac Surg 2001;72:1933–1937. [Free Full Text]
53. Chalela JA, Katzan I, Liebeskind DS, et al. Safety of intra–arterial thrombolysis in the postoperative period. Stroke 2001;32:1365–1369. [Free Full Text]
54. Taggart DP, Browne SM, Wade DT, Halligan PW. Neuroprotection during cardiac surgery: a randomised trial of a platelet activating factor antagonist. Heart 2003;89:897–900. [Free Full Text]
55. Arrowsmith JE, Harrison MJ, Newman SP, Stygall J, Timberlake N, Pugsley WB. Neuroprotection of the brain during cardiopulmonary bypass: a randomized trial of remacemide during coronary artery bypass in 171 patients. Stroke 1998;29:2357–2362. [Free Full Text]
56. Sedrakyan A, Treasure T, Elefteriades JA. Effect of aprotinin on clinical outcomes in coronary artery bypass graft surgery: a systematic review and meta–analysis of randomized clinical trials. J Thorac Cardiovasc Surg 2004;128:442–448. [Free Full Text]












