–ù–Α―É―΅–Ϋ–Α―è –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ–Α ―¹–Η–Φ–Ω–Ψ–Ζ–Η―É–Φ–Α –±―΄–Μ–Α ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Α–Ϋ–Α ―¹ ―Ü–Β–Μ―¨―é –Ψ–±–Φ–Β–Ϋ–Α –Ψ–Ω―΄―²–Ψ–Φ –Φ–Β–Ε–¥―É ―¹–Ω–Β―Ü–Η–Α–Μ–Η―¹―²–Α–Φ–Η –Η –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ–Η―è –Ϋ–Ψ–≤–Β–Ι―à–Β–Ι –≤–Α–Ε–Ϋ–Ψ–Ι –Η–Ϋ―³–Ψ―Ä–Φ–Α―Ü–Η–Η.
–û–±―â–Β–Ι ―Ü–Β–Μ―¨―é –±―΄–Μ–Ψ ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Ω–Ψ–Ϋ–Η–Φ–Α–Ϋ–Η―è –Ω―É―²–Β–Ι –Φ–Β–¥–Η–Κ–Α–Φ–Β–Ϋ―²–Ψ–Ζ–Ϋ–Ψ–Ι –Κ–Ψ―Ä―Ä–Β–Κ―Ü–Η–Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι –Η –Ψ–±–Μ–Β–≥―΅–Β–Ϋ–Η―è ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤, –Α ―²–Α–Κ–Ε–Β –Ω–Ψ–≤―΄―à–Β–Ϋ–Η―è –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η ―É ―¹–Α–Φ―΄―Ö ―Ä–Α–Ζ–Ϋ―΄―Ö –≥―Ä―É–Ω–Ω –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤.
–£ ―Ä–Α–Φ–Κ–Α―Ö –Κ–Ψ–Ϋ―³–Β―Ä–Β–Ϋ―Ü–Η–Η –±―΄–Μ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ ―¹–Η–Φ–Ω–Ψ–Ζ–Η―É–Φ –Η–Ζ 4 –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α―²–Β–Μ―¨–Ϋ―΄―Ö ―¹–Β―¹―¹–Η–Ι. –ù–Η–Ε–Β –Ω―Ä–Η–≤–Ψ–¥―è―²―¹―è –Κ–Μ―é―΅–Β–≤―΄–Β –Φ–Ψ–Φ–Β–Ϋ―²―΄ –¥–Ψ–Κ–Μ–Α–¥–Ψ–≤ –≤–Β–¥―É―â–Η―Ö ―¹–Ω–Β―Ü–Η–Α–Μ–Η―¹―²–Ψ–≤.
–ü–Β―Ä–≤–Α―è ―΅–Α―¹―²―¨ –Κ–Ψ–Ϋ―³–Β―Ä–Β–Ϋ―Ü–Η–Η –Ω―Ä–Ψ―Ö–Ψ–¥–Η–Μ–Α –Ω–Ψ–¥ –Ω―Ä–Β–¥―¹–Β–¥–Α―²–Β–Μ―¨―¹―²–≤–Ψ–Φ –Ω―Ä–Ψ―³–Β―¹―¹–Ψ―Ä–Α –™–Β―Ä–Φ–Α–Ϋ–Α –ö–Η–Ϋ–≥–Φ–Α (–ù–Η–¥–Β―Ä–Μ–Α–Ϋ–¥―΄) –Η –±―΄–Μ–Α –Ω–Ψ―¹–≤―è―â–Β–Ϋ–Α –≤–Β―Ä―²–Η–≥–Ψ
–Η –≤–Β―Ä―²–Η–≥–Ψ, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι
–Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι
–û―Ü–Β–Ϋ–Κ–Α –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι ―É –Ω–Ψ―¹―²–Β–Μ–Η –±–Ψ–Μ―¨–Ϋ–Ψ–≥–Ψ
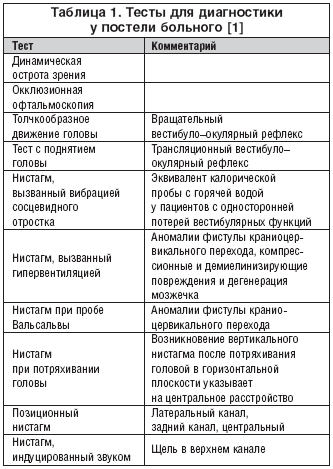
–î–Μ―è –Ω―Ä–Α–Κ―²–Η–Κ―É―é―â–Β–≥–Ψ –Ϋ–Β–≤―Ä–Ψ–Μ–Ψ–≥–Α –≤―¹–Β–≥–¥–Α –Κ―Ä–Α–Ι–Ϋ–Β ―¹–Μ–Ψ–Ε–Ϋ–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ–Η―²―¨, ―É –Κ–Ψ–≥–Ψ –Η–Ζ –Ψ–≥―Ä–Ψ–Φ–Ϋ–Ψ–≥–Ψ ―΅–Η―¹–Μ–Α –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ε–Α–Μ–Ψ–±–Α–Φ–Η –Ϋ–Α –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β –Η–Μ–Η –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Β ―Ä–Α–≤–Ϋ–Ψ–≤–Β―¹–Η―è –Η–Φ–Β–Β―²―¹―è –Η―¹―²–Η–Ϋ–Ϋ–Ψ–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Β ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Ψ –Η –Κ–Α–Κ–Ψ–≥–Ψ –Ψ–Ϋ–Ψ –≥–Β–Ϋ–Β–Ζ–Α – –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η–Μ–Η ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–≥–Ψ. –ö–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–Β –Ψ–±―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ζ–Α―΅–Α―¹―²―É―é ―è–≤–Μ―è–Β―²―¹―è –Κ–Μ―é―΅–Β–≤―΄–Φ –¥–Μ―è –Ψ―²–≤–Β―²–Α –Ϋ–Α ―ç―²–Ψ―² –≤–Ψ–Ω―Ä–Ψ―¹. –î―ç–≤–Η–¥ –½–Η (–ë–Ψ–Μ―¨–Ϋ–Η―Ü–Α –î–Ε–Ψ–Ϋ–Α –Ξ–Ψ–Ω–Κ–Η–Ϋ―¹–Α, –ë–Α–Μ―²–Η–Φ–Ψ―Ä, –Γ–®–ê) –Ω―Ä–Β–¥―¹―²–Α–≤–Η–Μ ―Ä―è–¥ –≤–Η–¥–Β–Ψ–Φ–Α―²–Β―Ä–Η–Α–Μ–Ψ–≤ (–Ψ–Ω–Η―¹–Α–Ϋ―΄ –≤ ―²–Α–±–Μ–Η―Ü–Β 1) –Ω–Ψ ―¹–Η―¹―²–Β–Φ–Ϋ–Ψ –Ω―Ä–Η–Φ–Β–Ϋ―è–Β–Φ―΄–Φ ―²–Β―¹―²–Α–Φ, ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Α–Ϋ–Ϋ―΄–Φ –Ϋ–Α –Ψ―¹–Ϋ–Ψ–≤–Β ―³–Η–Ζ–Η–Ψ–Μ–Ψ–≥–Η–Η –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η ―¹―²–Α―²–Η―΅–Β―¹–Κ–Η―Ö –Η –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η―Ö ―³―É–Ϋ–Κ―Ü–Η–Ι –≤–Β―¹―²–Η–±―É–Μ–Ψ––Ψ–Κ―É–Μ―è―Ä–Ϋ―΄―Ö ―Ä–Β―³–Μ–Β–Κ―¹–Ψ–≤ –Η –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ―΄―Ö –Μ–Α–±–Η―Ä–Η–Ϋ―²–Ϋ―΄―Ö ―΅―É–≤―¹―²–≤–Η―²–Β–Μ―¨–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤. –î–Α–Ϋ–Ϋ―΄–Β ―²–Β―¹―²―΄ –≤―¹–Β–≥–¥–Α –≤―΄―è–≤―è―² –Α–Ϋ–Ψ–Φ–Α–Μ–Η―é –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄, ―΅―²–Ψ –Ω―Ä–Ψ―è―¹–Ϋ–Η―² –¥–Η–Α–≥–Ϋ–Ψ–Ζ –Η–Μ–Η ―É–Κ–Α–Ε–Β―² –Ϋ–Α –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨ –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Β–≥–Ψ –Ψ–±―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è.
–û―²–Ψ–Ϋ–Β–≤―Ä–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Β –Ψ–±―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ―É –Ω–Ψ―¹―²–Β–Μ–Η –±–Ψ–Μ―¨–Ϋ–Ψ–≥–Ψ –≤–Κ–Μ―é―΅–Α–Β―² –Ψ―Ü–Β–Ϋ–Κ―É –Κ–Α–Κ ―¹―²–Α―²–Η―΅–Β―¹–Κ–Η―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ―΄―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Β–Φ ―²–Ψ–Ϋ―É―¹–Α –Ω―Ä–Η –Ϋ–Β–Ω–Ψ–¥–≤–Η–Ε–Ϋ–Ψ–Ι –≥–Ψ–Μ–Ψ–≤–Β, ―²–Α–Κ –Η –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η―Ö, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ–Α―Ö ―¹ –Α–Ϋ–Ψ–Φ–Α–Μ―¨–Ϋ―΄–Φ–Η –Ψ―²–≤–Β―²–Α–Φ–Η –≤–Ψ –≤―Ä–Β–Φ―è –¥–≤–Η–Ε–Β–Ϋ–Η―è –≥–Ψ–Μ–Ψ–≤―΄. –Γ–Ω–Ψ–Ϋ―²–Α–Ϋ–Ϋ―΄–Ι –Ϋ–Η―¹―²–Α–≥–Φ – –Ψ–¥–Η–Ϋ –Η–Ζ –≥–Μ–Α–Ζ–Ϋ―΄―Ö ―Ä–Β―³–Μ–Β–Κ―¹–Ψ–≤, –Ω―Ä–Η–Ζ–Ϋ–Α–Κ ―¹―²–Α―²–Η―΅–Β―¹–Κ–Η―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι ―²–Ψ–Ω–Η―΅–Β―¹–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Ϋ–Α ―É―Ä–Ψ–≤–Ϋ–Β –Ω–Ψ–Μ―É–Κ―Ä―É–Ε–Ϋ―΄―Ö –Κ–Α–Ϋ–Α–Μ–Ψ–≤ (–ü–ö). –î–Μ―è –≤―΄―è–≤–Μ–Β–Ϋ–Η―è –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ –Ϋ–Η―¹―²–Α–≥–Φ–Α –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ ―É―¹―²―Ä–Α–Ϋ–Η―²―¨ ―³–Η–Κ―¹–Α―Ü–Η―é –≤–Ζ–Ψ―Ä–Α –Ω―É―²–Β–Φ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è ―ç–Κ–≤–Η–≤–Α–Μ–Β–Ϋ―²–Α –Ω―Ä–Ψ–±―΄ –†–Ψ–Φ–±–Β―Ä–≥–Α –¥–Μ―è –≥–Μ–Α–Ζ ―¹ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ –Ψ―΅–Κ–Ψ–≤ –Λ―Ä–Β–Ϋ―Ü–Β–Μ―è. –ü–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η–Ι –Ϋ–Η―¹―²–Α–≥–Φ – ―²–Ψ–Μ―΅–Κ–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ–Β –¥–≤–Η–Ε–Β–Ϋ–Η–Β –≥–Μ–Α–Ζ–Ϋ―΄―Ö ―è–±–Μ–Ψ–Κ ―¹ –Ψ–¥–Ϋ–Ψ–Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Ϋ―΄–Φ–Η –Φ–Β–¥–Μ–Β–Ϋ–Ϋ―΄–Φ–Η ―³–Α–Ζ–Α–Φ–Η, ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É―é―â–Β–Β―¹―è –Ω–Ψ―¹―²–Ψ―è–Ϋ–Ϋ–Ψ–Ι ―¹–Κ–Ψ―Ä–Ψ―¹―²―¨―é, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄–Ι –Ϋ–Η―¹―²–Α–≥–Φ –Φ–Ψ–Ε–Β―² –Η–Φ–Β―²―¨ –≤–Ψ–Μ–Ϋ–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ―É―é ―³–Ψ―Ä–Φ―É – ―¹ –≤–Ψ–Ζ―Ä–Α―¹―²–Α―é―â–Β–Ι ―¹–Κ–Ψ―Ä–Ψ―¹―²―¨―é. –ü―Ä–Η –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η―Ö –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è―Ö –Ϋ–Η―¹―²–Α–≥–Φ ―É―¹–Η–Μ–Η–≤–Α–Β―²―¹―è –Η–Μ–Η –Ω–Ψ―è–≤–Μ―è–Β―²―¹―è –Ω―Ä–Η ―É–¥–Α–Μ–Β–Ϋ–Η–Η ―³–Η–Κ―¹–Α―Ü–Η–Η –≤–Ζ–Ψ―Ä–Α [–Ω―Ä–Η–Ζ–Ϋ–Α–Κ –†–Ψ–Φ–±–Β―Ä–≥–Α –≤–Β―¹―²–Η–±―É–Μ–Ψ––Ψ–Κ―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ ―Ä–Β―³–Μ–Β–Κ―¹–Α (–£–û–†)]. –ü–Ψ–Μ–Ϋ–Α―è –Ψ–¥–Ϋ–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ―è―è –Ω–Ψ―²–Β―Ä―è –Μ–Α–±–Η―Ä–Η–Ϋ―²–Ϋ–Ψ–Ι ―³―É–Ϋ–Κ―Ü–Η–Η –≤―΄–Ζ―΄–≤–Α–Β―² ―¹–Φ–Β―à–Α–Ϋ–Ϋ―΄–Ι –≥–Ψ―Ä–Η–Ζ–Ψ–Ϋ―²–Α–Μ―¨–Ϋ–Ψ–―²–Ψ―Ä―¹–Η–Ψ–Ϋ–Ϋ―΄–Ι –Ϋ–Η―¹―²–Α–≥–Φ. –ß–Η―¹―²―΄–Ι –≤–Β―Ä―²–Η–Κ–Α–Μ―¨–Ϋ―΄–Ι –Η–Μ–Η ―΅–Η―¹―²―΄–Ι ―²–Ψ―Ä―¹–Η–Ψ–Ϋ–Ϋ―΄–Ι (–≤―Ä–Α―â–Α―²–Β–Μ―¨–Ϋ―΄–Ι) –Ϋ–Η―¹―²–Α–≥–Φ –Ϋ–Β –Φ–Ψ–Ε–Β―² –Ψ–±―ä―è―¹–Ϋ―è―²―¨―¹―è –≤–Ψ–≤–Μ–Β―΅–Β–Ϋ–Η–Β–Φ –Ψ–¥–Ϋ–Ψ–≥–Ψ –Κ–Α–Ϋ–Α–Μ–Α –Η–Μ–Η –Ψ–¥–Ϋ–Ψ–≥–Ψ –Μ–Α–±–Η―Ä–Η–Ϋ―²–Α, –≤ ―¹–≤―è–Ζ–Η ―¹ ―΅–Β–Φ ―¹–Μ–Β–¥―É–Β―² –Ω―Ä–Β–¥–Ω–Ψ–Μ–Ψ–Ε–Η―²―¨ ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄–Ι –≥–Β–Ϋ–Β–Ζ.
–£ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι ―³―É–Ϋ–Κ―Ü–Η―è –£–û–† –Ψ―Ü–Β–Ϋ–Η–≤–Α–Β―²―¹―è –Ω―É―²–Β–Φ –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η―è –≤–Μ–Η―è–Ϋ–Η―è –Ω–Ψ–≤–Ψ―Ä–Ψ―²–Α –≥–Ψ–Μ–Ψ–≤―΄ –Ϋ–Α –Ψ―¹―²―Ä–Ψ―²―É –Ζ―Ä–Β–Ϋ–Η―è, –Ω―É―²–Β–Φ –Ϋ–Α–±–Μ―é–¥–Β–Ϋ–Η―è –Ζ–Α –¥–≤–Η–Ε–Β–Ϋ–Η―è–Φ–Η –≥–Μ–Α–Ζ–Ϋ―΄―Ö ―è–±–Μ–Ψ–Κ –≤ –Ψ―²–≤–Β―² –Ϋ–Α –Ϋ–Η–Ζ–Κ–Ψ– –Η –≤―΄―¹–Ψ–Κ–Ψ―΅–Α―¹―²–Ψ―²–Ϋ–Ψ–Β –≤―Ä–Α―â–Β–Ϋ–Η–Β –≥–Ψ–Μ–Ψ–≤–Ψ–Ι –Η –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –Κ–Α–Μ–Ψ―Ä–Η―΅–Β―¹–Κ–Ψ–≥–Ψ ―²–Β―¹―²–Α ―É –Ω–Ψ―¹―²–Β–Μ–Η –±–Ψ–Μ―¨–Ϋ–Ψ–≥–Ψ. –£―΄―¹–Ψ–Κ–Ψ―΅–Α―¹―²–Ψ―²–Ϋ―΄–Ι –£–û–† –Φ–Ψ–Ε–Β―² –±―΄―²―¨ ―É―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ –Ω―É―²–Β–Φ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –±―΄―¹―²―Ä–Ψ–≥–Ψ –≤―Ä–Α―â–Β–Ϋ–Η―è –≥–Ψ–Μ–Ψ–≤–Ψ–Ι. –ü―Ä–Η –Η–Ϋ―²–Α–Κ―²–Ϋ–Ψ–Φ –£–û–† –±―É–¥–Β―² ―¹–Ψ―Ö―Ä–Α–Ϋ―è―²―¨―¹―è ―É―¹―²–Ψ–Ι―΅–Η–≤―΄–Ι –≤–Ζ–Ψ―Ä. –Θ –Ω–Α―Ü–Η–Β–Ϋ―²–Α ―¹ –Ψ–¥–Ϋ–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Η–Φ –Ω―Ä–Α–≤–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Η–Φ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β–Φ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ –Α–Ω–Ω–Α―Ä–Α―²–Α ―²–Ψ–Μ―΅–Κ–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ–Β –¥–≤–Η–Ε–Β–Ϋ–Η–Β –≥–Ψ–Μ–Ψ–≤―΄ –≤–Ω―Ä–Α–≤–Ψ –≤―΄–Ζ–Ψ–≤–Β―² –Ϋ–Α―Ä–Α―¹―²–Α―é―â–Β–Β –±―΄―¹―²―Ä–Ψ–Β ―¹–Κ–Α―΅–Κ–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ–Β –¥–≤–Η–Ε–Β–Ϋ–Η–Β –≥–Μ–Α–Ζ–Ϋ―΄―Ö ―è–±–Μ–Ψ–Κ. –Θ –Ϋ–Β–Κ–Ψ―²–Ψ―Ä―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι –Φ–Ψ–Ζ–Ε–Β―΅–Κ–Α –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Α–Ϋ–Ψ–Φ–Α–Μ―¨–Ϋ–Α―è –Ψ―¹―¨ –≤―Ä–Α―â–Β–Ϋ–Η―è –≥–Μ–Α–Ζ–Ϋ―΄―Ö ―è–±–Μ–Ψ–Κ –Ω―Ä–Η –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –£–û–†; –±–Ψ–Μ–Β–Β ―²–Η–Ω–Η―΅–Ϋ–Α –≤–Ψ―¹―Ö–Ψ–¥―è―â–Α―è –Φ–Β–¥–Μ–Β–Ϋ–Ϋ–Α―è ―³–Α–Ζ–Α, –Ω–Β―Ä–Β―Ö–Ψ–¥―è―â–Α―è –≤ –≥–Ψ―Ä–Η–Ζ–Ψ–Ϋ―²–Α–Μ―¨–Ϋ―É―é ―Ä–Ψ―²–Α―Ü–Η―é, ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Ψ–Φ ―΅–Β–≥–Ψ ―è–≤–Μ―è–Β―²―¹―è –Ϋ–Η―¹―Ö–Ψ–¥―è―â–Β–Β –Κ–Ψ―Ä―Ä–Β–Κ―²–Η―Ä―É―é―â–Β–Β –±―΄―¹―²―Ä–Ψ–Β ―¹–Κ–Α―΅–Κ–Ψ–Ψ–±―Ä–Α–Ζ–Ϋ–Ψ–Β –¥–≤–Η–Ε–Β–Ϋ–Η–Β –≥–Μ–Α–Ζ. –ü―Ä–Η –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α –Ϋ–Α―΅–Α–Μ―¨–Ϋ–Α―è –Φ–Β–¥–Μ–Β–Ϋ–Ϋ–Α―è ―³–Α–Ζ–Α –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Α –≤ ―¹―²–Ψ―Ä–Ψ–Ϋ―É –Η–Ϋ―²–Α–Κ―²–Ϋ–Ψ–≥–Ψ ―É―Ö–Α, –≤ ―ç―²–Ψ–Φ ―¹–Μ―É―΅–Α–Β –Ϋ–Α–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η–Β –Ϋ–Η―¹―²–Α–≥–Φ–Α –Ϋ–Β –Φ–Ψ–Ε–Β―² –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α―²―¨―¹―è –¥–Μ―è –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η―è –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ–≥–Ψ ―É―Ö–Α. –£–Φ–Β―¹―²–Ψ ―ç―²–Ψ–≥–Ψ ―²―Ä–Β–±―É–Β―²―¹―è –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η–Β –Α―É–¥–Η–Ψ–≥―Ä–Α–Φ–Φ―΄ –Η ―¹–Μ―É―Ö–Ψ–≤―΄―Ö ―²–Β―¹―²–Ψ–≤.
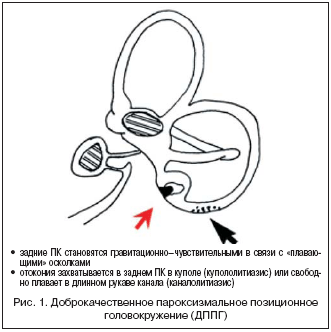
–Θ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –¥–Ψ–±―Ä–Ψ–Κ–Α―΅–Β―¹―²–≤–Β–Ϋ–Ϋ―΄–Φ –Ω–Α―Ä–Ψ–Κ―¹–Η–Ζ–Φ–Α–Μ―¨–Ϋ―΄–Φ –Ω–Ψ–Ζ–Η―Ü–Η–Ψ–Ϋ–Ϋ―΄–Φ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ (–î–ü–ü–™) (―Ä–Η―¹. 1) ―²–Β―¹―² –î–Η–Κ―¹–Α––Ξ–Ψ–Μ–Ω–Α–Ι–Κ–Α –Φ–Ψ–Ε–Β―² –Ω―Ä–Ψ–≤–Ψ―Ü–Η―Ä–Ψ–≤–Α―²―¨ –≤–Β―Ä―²–Η–≥–Ψ –Η –Ϋ–Η―¹―²–Α–≥–Φ, –Ω–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –Ψ―²–Ψ–Κ–Ψ–Ϋ–Η–Α–Μ―¨–Ϋ―΄–Β –Ψ–±–Μ–Ψ–Φ–Κ–Η –Ω―Ä–Ψ―Ö–Ψ–¥―è―² ―΅–Β―Ä–Β–Ζ –Κ–Α–Ϋ–Α–Μ, –≤―΄–Ζ―΄–≤–Α―è –¥–≤–Η–Ε–Β–Ϋ–Η–Β ―ç–Ϋ–¥–Ψ–Μ–Η–Φ―³―΄, –≤–Ψ–Ζ–±―É–Ε–¥–Α―è ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Η –Ω―Ä–Ψ–≤–Ψ―Ü–Η―Ä―É―è –Ψ―²–≤–Β―². –™–Η–Ω–Β―Ä–≤–Β–Ϋ―²–Η–Μ―è―Ü–Η―è –Φ–Ψ–Ε–Β―² –≤―΄–Ζ―΄–≤–Α―²―¨ –Ϋ–Η―¹―²–Α–≥–Φ –Η ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄–Β ―¹ ―²―Ä–Β–≤–Ψ–≥–Ψ–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ –Ω―Ä–Η ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è―Ö. –ü–Ψ―¹–Μ–Β –Ψ–¥–Ϋ–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Β–≥–Ψ –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ –Α–Ω–Ω–Α―Ä–Α―²–Α –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥–Η―² ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ–Ψ–Β –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η–Β ―Ä–Α–≤–Ϋ–Ψ–≤–Β―¹–Η―è –¥–Μ―è ―É―¹―²―Ä–Α–Ϋ–Β–Ϋ–Η―è ―¹–Ω–Ψ–Ϋ―²–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Ϋ–Η―¹―²–Α–≥–Φ–Α. –ù–Η―¹―²–Α–≥–Φ, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ―΄–Ι –≥–Η–Ω–Β―Ä–≤–Β–Ϋ―²–Η–Μ―è―Ü–Η–Β–Ι, –Φ–Ψ–Ε–Β―² –Η–Ϋ–Ψ–≥–¥–Α –Ϋ–Α–±–Μ―é–¥–Α―²―¨―¹―è –Ω―Ä–Η –Ω–Β―Ä–Η–Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―³–Η―¹―²―É–Μ–Α―Ö –Η–Μ–Η –Η―à–Β–Φ–Η–Η, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ–Ψ–Ι –≤–Α–Ζ–Ψ–Κ–Ψ–Ϋ―¹―²―Ä–Η–Κ―²–Ψ―Ä–Α–Φ–Η; –≥–Η–Ω–Β―Ä–≤–Β–Ϋ―²–Η–Μ―è―Ü–Η―è ―²–Α–Κ–Ε–Β –Φ–Ψ–Ε–Β―² –≤―΄–Ζ―΄–≤–Α―²―¨ –Η–Μ–Η ―É―¹–Η–Μ–Η–≤–Α―²―¨ –Ϋ–Η―¹―Ö–Ψ–¥―è―â–Η–Ι –Ϋ–Η―¹―²–Α–≥–Φ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι –Φ–Ψ–Ζ–Ε–Β―΅–Κ–Α. –ù–Η―¹―²–Α–≥–Φ, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ―΄–Ι –Ω―Ä–Ψ–±–Ψ–Ι –£–Α–Μ―¨―¹–Α–Μ―¨–≤―΄, –Φ–Ψ–Ε–Β―² –≤–Ψ–Ζ–Ϋ–Η–Κ–Α―²―¨ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Α–Ϋ–Ψ–Φ–Α–Μ–Η―è–Φ–Η –Κ―Ä–Α–Ϋ–Η–Ψ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Β―Ö–Ψ–¥–Α, ―â–Β–Μ―¨―é –≤–Β―Ä―Ö–Ϋ–Β–≥–Ψ –Κ–Α–Ϋ–Α–Μ–Α, –Ω–Β―Ä–Η–Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η–Φ–Η ―³–Η―¹―²―É–Μ–Α–Φ–Η –Η –Α–Ϋ–Ψ–Φ–Α–Μ–Η―è–Φ–Η ―Ü–Β–Ω–Η ―¹–Μ―É―Ö–Ψ–≤―΄―Ö –Κ–Ψ―¹―²–Ψ―΅–Β–Κ. –ö–Ψ–Φ–Ω―Ä–Β―¹―¹–Η―è –Κ–Ψ–Ζ–Β–Μ–Κ–Α ―É―à–Ϋ–Ψ–Ι ―Ä–Α–Κ–Ψ–≤–Η–Ϋ―΄ –Η–Μ–Η ―¹–Η–Μ―¨–Ϋ―΄–Ι ―à―É–Φ (―³–Β–Ϋ–Ψ–Φ–Β–Ϋ –Δ―É–Μ–Μ–Η–Ψ) –Φ–Ψ–≥―É―² –≤―΄–Ζ–≤–Α―²―¨ –Ϋ–Η―¹―²–Α–≥–Φ –Ω―Ä–Η –Ω–Β―Ä–Η–Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Η―Ö ―³–Η―¹―²―É–Μ–Α―Ö, –≤–Κ–Μ―é―΅–Α―è ―â–Β–Μ―¨ –≤–Β―Ä―Ö–Ϋ–Β–≥–Ψ –Κ–Α–Ϋ–Α–Μ–Α –Η–Μ–Η –Α–Ϋ–Ψ–Φ–Α–Μ–Η–Η ―¹–Μ―É―Ö–Ψ–≤―΄―Ö –Κ–Ψ―¹―²–Ψ―΅–Β–Κ. –£–Η–±―Ä–Α―Ü–Η―è ―¹–Ψ―¹―Ü–Β–≤–Η–¥–Ϋ–Ψ–≥–Ψ –Ψ―²―Ä–Ψ―¹―²–Κ–Α –Φ–Ψ–Ε–Β―² –≤―΄–Ζ–≤–Α―²―¨ –Ϋ–Η―¹―²–Α–≥–Φ –Ω―Ä–Η ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α―Ö, –≤–Κ–Μ―é―΅–Α―è –Ψ–¥–Ϋ–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ―é―é –Ω–Ψ―²–Β―Ä―é –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―³―É–Ϋ–Κ―Ü–Η–Η –Η ―³–Η―¹―²―É–Μ―΄.
–ü―Ä–Ψ―²–Η–≤–Ψ―Ä–Β―΅–Η–Β –Φ–Β–Ε–¥―É –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ―΄–Φ ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι,
–Η –Ζ–Ϋ–Α―΅–Β–Ϋ–Η–Β–Φ ―à–Β–Η –¥–Μ―è –Ψ―Ä–Η–Β–Ϋ―²–Η―Ä–Ψ–≤–Α–Ϋ–Η―è
–î–Μ―è –Ω–Ψ–¥–¥–Β―Ä–Ε–Α–Ϋ–Η―è ―Ä–Α–≤–Ϋ–Ψ–≤–Β―¹–Η―è –Η –Ω―Ä–Α–≤–Η–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ―Ä–Η–Β–Ϋ―²–Η―Ä–Ψ–≤–Α–Ϋ–Η―è –≤ –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤–Β ―΅–Β–Μ–Ψ–≤–Β–Κ –Ζ–Α–≤–Η―¹–Η―² –≤ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Ι ―¹―²–Β–Ω–Β–Ϋ–Η –Ψ―² –Ω–Ψ–Μ–Ϋ–Ψ―²―΄ –Η ―¹–Ψ–±―¹―²–≤–Β–Ϋ–Ϋ–Ψ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η―è –Ψ–±―Ä–Α―²–Ϋ–Ψ–Ι ―¹–≤―è–Ζ–Η –¥–≤–Η–≥–Α―²–Β–Μ―¨–Ϋ–Ψ–Ι –Κ–Ψ–Φ–Α–Ϋ–¥―΄. –€―ç–Ϋ―¹ –€–Α–≥–Ϋ―É―¹―¹–Ψ–Ϋ (–Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―²―¹–Κ–Α―è –±–Ψ–Μ―¨–Ϋ–Η―Ü–Α –¦―É–Ϋ–¥–Α, –®–≤–Β―Ü–Η―è) –Ψ–±―ä―è―¹–Ϋ–Η–Μ, ―΅―²–Ψ –Φ―΄ –Η―¹–Ω―΄―²―΄–≤–Α–Β–Φ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β, –Κ–Ψ–≥–¥–Α –≤–Ψ–Ζ–Ϋ–Η–Κ–Α–Β―² ―¹–Β–Ϋ―¹–Ψ―Ä–Ϋ–Ψ–Β –Ϋ–Β―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Η–Β, –Κ–Ψ–≥–¥–Α ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β ―¹–Β–Ϋ―¹–Ψ―Ä–Ϋ―΄–Β ―¹–Η―¹―²–Β–Φ―΄ –¥–Α―é―² –Ω―Ä–Ψ―²–Η–≤–Ψ―Ä–Β―΅–Η–≤―΄–Β –¥–Α–Ϋ–Ϋ―΄–Β –Ψ –¥–≤–Η–Ε–Β–Ϋ–Η–Η ―²–Β–Μ–Α –Η ―ç―²–Ψ ―Ä–Β–≥―É–Μ–Η―Ä―É–Β―²―¹―è –Ψ―΅–Β–Ϋ―¨ ―¹–Μ–Ψ–Ε–Ϋ―΄–Φ–Η ―¹–Η―¹―²–Β–Φ–Α–Φ–Η. –î–≤–Η–Ε–Β–Ϋ–Η―è –≥–Ψ–Μ–Ψ–≤―΄ –≤ –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤–Β ―Ä–Α―¹–Ω–Ψ–Ζ–Ϋ–Α―é―²―¹―è –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ–Ψ–Ι, –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ―΄–Φ–Η ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Α–Φ–Η –Η –Ω―Ä–Ψ–Ω―Ä–Η–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Α–Φ–Η, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ –Φ–Β―Ö–Α–Ϋ–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄ –Ψ–Ω―Ä–Β–¥–Β–Μ―è―é―² –¥–≤–Η–Ε–Β–Ϋ–Η–Β ―΅–Α―¹―²–Β–Ι ―²–Β–Μ–Α –Ω–Ψ –Ψ―²–¥–Β–Μ―¨–Ϋ–Ψ―¹―²–Η –Ψ―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ ―²―É–Μ–Ψ–≤–Η―â–Α, –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è –Η –Ω–Ψ–¥–Μ–Β–Ε–Α―â–Β–Ι –Ω–Ψ–≤–Β―Ä―Ö–Ϋ–Ψ―¹―²–Η. –î–Μ―è –Ψ–±―Ä–Α–±–Ψ―²–Κ–Η –Η–Ϋ―³–Ψ―Ä–Φ–Α―Ü–Η–Η –Ψ―² –Ζ―Ä–Η―²–Β–Μ―¨–Ϋ―΄―Ö –Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –≤ –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ–Ψ–Φ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Β ―΅–Β–Μ–Ψ–≤–Β–Κ –≤ –≤–Β―Ä―²–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Φ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Η –¥–Ψ–Μ–Ε–Β–Ϋ –Ω–Ψ–Μ―É―΅–Α―²―¨ –Η–Ϋ―³–Ψ―Ä–Φ–Α―Ü–Η―é –Ψ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Η –≥–Ψ–Μ–Ψ–≤―΄ –Ψ―²–Ϋ–Ψ―¹–Η―²–Β–Μ―¨–Ϋ–Ψ ―²―É–Μ–Ψ–≤–Η―â–Α. –‰–Ϋ―³–Ψ―Ä–Φ–Α―Ü–Η―è –¥–Ψ–Μ–Ε–Ϋ–Α –≤ ―²–Ψ–Ι –Η–Μ–Η –Η–Ϋ–Ψ–Ι ―¹―²–Β–Ω–Β–Ϋ–Η –Ζ–Α–≤–Η―¹–Β―²―¨ –Ψ―² –Ω―Ä–Ψ–Ω―Ä–Η–Ψ―Ü–Β–Ω―²–Η–≤–Ϋ–Ψ–Ι –Α―³―³–Β―Ä–Β–Ϋ―²–Α―Ü–Η–Η –Ψ―² ―à–Β–Ι–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α, –Ϋ–Ψ ―²–Α–Κ–Ε–Β –¥–Ψ–Μ–Ε–Ϋ–Ψ –Ω―Ä–Β–¥―¹―²–Α–≤–Μ―è―²―¨―¹―è –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ―΄–Φ –≤―΄―è–≤–Μ–Β–Ϋ–Η–Β –Ϋ–Β–Κ–Ψ―²–Ψ―Ä–Ψ–≥–Ψ –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η―è –Φ–Β–Ε–¥―É –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ–Η –Η ―à–Β–Ι–Ϋ―΄–Φ–Η ―Ä–Β―³–Μ–Β–Κ―¹–Α–Φ–Η. –Δ–Α–Κ–Ψ–Β –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β ―É–Ε–Β ―Ö–Ψ―Ä–Ψ―à–Ψ –Η–Ζ–≤–Β―¹―²–Ϋ–Ψ –Η –Ψ–Ω–Η―¹–Α–Ϋ–Ψ ―É –Ε–Η–≤–Ψ―²–Ϋ―΄―Ö, ―΅–Β–≥–Ψ –Ϋ–Β–Μ―¨–Ζ―è ―¹–Κ–Α–Ζ–Α―²―¨ –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η –Μ―é–¥–Β–Ι.
–î–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ, ―΅―²–Ψ ―É ―΅–Β–Μ–Ψ–≤–Β–Κ–Α ―¹―É―â–Β―¹―²–≤―É–Β―² –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β –Φ–Β–Ε–¥―É –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι –Η ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –Η–Ϋ―³–Ψ―Ä–Φ–Α―Ü–Η–Β–Ι. –ü―Ä–Η―΅–Β–Φ ―ç―²–Ψ –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β –Ψ―²–Ϋ–Ψ―¹–Η―²―¹―è –Κ –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ–Ψ–Φ―É –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―é ―²–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, ―΅―²–Ψ ―Ä–Β–≥―É–Μ―è―Ü–Η―è ―¹–Ψ ―¹―²–Ψ―Ä–Ψ–Ϋ―΄ –Κ–Ψ―Ä―΄ –Κ–Α–Ε–Β―²―¹―è –Φ–Β–Ϋ–Β–Β –≤–Β―Ä–Ψ―è―²–Ϋ–Ψ–Ι. –Δ–Α–Κ–Ε–Β –≤–Ψ–Ζ–Φ–Ψ–Ε–Ϋ–Ψ –Ω–Ψ–Κ–Α–Ζ–Α―²―¨, ―΅―²–Ψ ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ―΄–Β –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ―΄–Β ―ç–Κ―¹–Ω–Β―Ä–Η–Φ–Β–Ϋ―²–Α–Μ―¨–Ϋ–Ψ –Η–Μ–Η –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β–Φ, –Φ–Ψ–≥―É―² –≤–Μ–Η―è―²―¨ –Ϋ–Α –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ―΄–Ι –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨ –Η –Ψ―Ä–Η–Β–Ϋ―²–Α―Ü–Η―é. –£ ―¹–Ψ–Ψ―²–≤–Β―²―¹―²–≤–Η–Η ―¹ –¥–Α–Ϋ–Ϋ―΄–Φ–Η –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –Μ–Β―΅–Β–Ϋ–Η―è ―à–Β–Ι–Ϋ–Ψ–Ι –Φ–Η–Ψ―³–Α―¹―Ü–Η–Α–Μ―¨–Ϋ–Ψ–Ι –±–Ψ–Μ–Η –Η–Μ–Η –≥―Ä―΄–Ε–Η –¥–Η―¹–Κ–Α ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ –Φ–Ψ–Ε–Ϋ–Ψ –Ω―Ä–Β–¥–Ω–Ψ–Μ–Ψ–Ε–Η―²―¨, ―΅―²–Ψ –Φ–Β―¹―²–Ϋ–Ψ–Β –Μ–Β―΅–Β–Ϋ–Η–Β ―à–Β–Ι–Ϋ–Ψ–≥–Ψ ―¹–Β–≥–Φ–Β–Ϋ―²–Α –≤–Μ–Η―è–Β―² –Ϋ–Α –≤–Ψ―¹–Ω―Ä–Η–Ϋ–Η–Φ–Α–Β–Φ–Ψ–Β –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β –Η –Ζ–Α―Ä–Β–≥–Η―¹―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄–Ι –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ―΄–Ι –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨. –¦–Β―΅–Β–Ϋ–Η–Β ―à–Β–Ι–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É–Β―² ―É–Μ―É―΅―à–Β–Ϋ–Η―é –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―è. –£–Φ–Β―¹―²–Β ―¹ ―²–Β–Φ ―¹–Β–Ι―΅–Α―¹ ―¹―΅–Η―²–Α–Β―²―¹―è, –Ω–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –≥–Μ―É–±–Ψ–Κ–Η–Β –Φ―΄―à―Ü―΄ ―à–Β–Η –Η–Φ–Β―é―² ―¹–Α–Φ―É―é –±–Ψ–Μ―¨―à―É―é –≤ ―΅–Β–Μ–Ψ–≤–Β―΅–Β―¹–Κ–Ψ–Φ ―²–Β–Μ–Β –Ω–Μ–Ψ―²–Ϋ–Ψ―¹―²―¨ –Φ―΄―à–Β―΅–Ϋ―΄―Ö –≤–Β―Ä–Β―²–Β–Ϋ, –Ψ–Ϋ–Η –Φ–Ψ–≥―É―² ―Ä–Α–±–Ψ―²–Α―²―¨ –Κ–Α–Κ ―¹–Β–Ϋ―¹–Ψ―Ä–Ϋ―΄–Ι –Ψ―Ä–≥–Α–Ϋ –≤ –¥–Ψ–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Β –Κ –Η―Ö ―Ä–Ψ–Μ–Η –≤ –≤―΄–Ω–Ψ–Μ–Ϋ–Β–Ϋ–Η–Η –¥–≤–Η–Ε–Β–Ϋ–Η―è. –ù–Α ―Ä–Η―¹―É–Ϋ–Κ–Β 2 –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ –≥–Η–Ω–Ψ―²–Β―²–Η―΅–Β―¹–Κ–Η–Ι –Ω–Ψ―Ä–Ψ―΅–Ϋ―΄–Ι –Κ―Ä―É–≥ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι, –≤ –Κ–Ψ―²–Ψ―Ä–Ψ–Φ ―²―Ä–Β–≤–Ψ–≥–Α –≤–Ϋ–Ψ―¹–Η―² –≤–Κ–Μ–Α–¥ –≤ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β ―΅–Β―Ä–Β–Ζ ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β –Ϋ–Α–Ω―Ä―è–Ε–Β–Ϋ–Η―è –Φ―΄―à―Ü –Η –±–Ψ–Μ―¨, –Κ–Ψ―²–Ψ―Ä―΄–Β, –≤ ―¹–≤–Ψ―é –Ψ―΅–Β―Ä–Β–¥―¨, –Φ–Ψ–¥―É–Μ–Η―Ä―É―é―² ―Ä–Β–≥―É–Μ―è―Ü–Η―é –Φ―΄―à–Β―΅–Ϋ–Ψ–≥–Ψ ―²–Ψ–Ϋ―É―¹–Α –Η –≤–Ψ–Ζ–±―É–Ε–¥–Α―é―² –Ω―Ä–Ψ–Ω―Ä–Η–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä―΄. –û–¥–Ϋ–Α–Κ–Ψ –Ϋ–Β―¹–Φ–Ψ―²―Ä―è –Ϋ–Α –Ω―Ä–Ψ–≥―Ä–Β―¹―¹ –≤ ―ç―²–Ψ–Ι –Ψ–±–Μ–Α―¹―²–Η –≤―¹–Β –Β―â–Β –Ϋ–Β ―¹―É―â–Β―¹―²–≤―É–Β―² –¥–Η–Α–≥–Ϋ–Ψ―¹―²–Η―΅–Β―¹–Κ–Η―Ö ―²–Β―¹―²–Ψ–≤ –¥–Μ―è –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è, –≤―΄–Ζ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι. –ö ―¹–Ψ–Ε–Α–Μ–Β–Ϋ–Η―é, –≤ –Ϋ–Α―¹―²–Ψ―è―â–Β–Β –≤―Ä–Β–Φ―è –Β–¥–Η–Ϋ―¹―²–≤–Β–Ϋ–Ϋ―΄–Ι –Ω―É―²―¨ –¥–Μ―è ―É―¹―²–Α–Ϋ–Ψ–≤–Κ–Η ―Ü–Β―Ä–≤–Η–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –≥–Β–Ϋ–Β–Ζ–Α –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è – ―ç―²–Ψ –Η―¹―΅–Β–Ζ–Ϋ–Ψ–≤–Β–Ϋ–Η–Β –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è –Ω–Ψ―¹–Μ–Β –Μ–Β―΅–Β–Ϋ–Η―è –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è ―à–Β–Η.
–£―²–Ψ―Ä–Α―è –Ψ–±―Ä–Α–Ζ–Ψ–≤–Α―²–Β–Μ―¨–Ϋ–Α―è ―¹–Β―¹―¹–Η―è –Κ–Ψ–Ϋ―³–Β―Ä–Β–Ϋ―Ü–Η–Η –Ω―Ä–Ψ―Ö–Ψ–¥–Η–Μ–Α –Ω–Ψ–¥ –Ω―Ä–Β–¥―¹–Β–¥–Α―²–Β–Μ―¨―¹―²–≤–Ψ–Φ –€–Α―É―Ä–Η–Κ–Ψ –™–Α–Ϋ–Α–Ϋ―Ü–Α (–ë―Ä–Α–Ζ–Η–Μ–Η―è) –Η –±―΄–Μ–Α –Ω–Ψ―¹–≤―è―â–Β–Ϋ–Α –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α –Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ –Η –Φ–Ψ–Ζ–Ε–Β―΅–Κ–Ψ–≤―΄–Φ
―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α–Φ
–ü―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Α―è –Ψ―Ü–Β–Ϋ–Κ–Α –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α
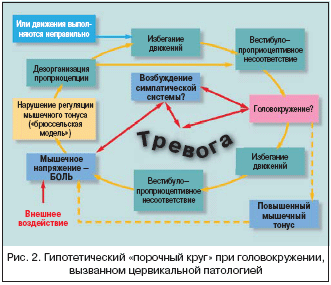
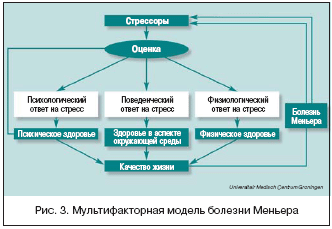
–ë–Ψ–Μ–Β–Ζ–Ϋ―¨ –€–Β–Ϋ―¨–Β―Ä–Α – –Η–Ϋ–≤–Α–Μ–Η–¥–Η–Ζ–Η―Ä―É―é―â–Β–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ–Ψ–Β ―¹ ―Ä–Α–Ζ–≤–Η―²–Η–Β–Φ –Ω–Ψ―²–Β–Ϋ―Ü–Η–Α–Μ―¨–Ϋ–Ψ ―²―è–Ε–Β–Μ―΄―Ö –Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι –Η (―É –≤–Ψ―¹–Ω―Ä–Η–Η–Φ―΅–Η–≤―΄―Ö –Η–Ϋ–¥–Η–≤–Η–¥―É―É–Φ–Ψ–≤) –Ψ―¹―²―Ä―΄–Φ –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η―Ä–Ψ–≤–Α–Ϋ–Η–Β–Φ ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤, –Ζ–Α–Ω―É―â–Β–Ϋ–Ϋ–Ψ–≥–Ψ ―¹―²―Ä–Β―¹―¹–Ψ–≤―΄–Φ–Η ―¹–Η―²―É–Α―Ü–Η―è–Φ–Η. –ë–Ψ–Μ–Β–Ζ–Ϋ―¨ ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É–Β―²―¹―è –Ω–Ψ―¹―²–Ψ―è–Ϋ–Ϋ―΄–Φ –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤–Η–Β–Φ –Φ–Β–Ε–¥―É –Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Φ–Η, ―³–Η–Ζ–Η―΅–Β―¹–Κ–Η–Φ–Η ―³–Α–Κ―²–Ψ―Ä–Α–Φ–Η –Η ―³–Α–Κ―²–Ψ―Ä–Α–Φ–Η –Ψ–Κ―Ä―É–Ε–Α―é―â–Β–Ι ―¹―Ä–Β–¥―΄: –±―΄–Μ–Ψ –≤―΄–¥–≤–Η–Ϋ―É―²–Ψ –Ω―Ä–Β–¥–Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β, ―΅―²–Ψ ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ –±–Ψ–Μ–Β–Ζ–Ϋ–Η ―É―Ö―É–¥―à–Α―é―² ―ç–Φ–Ψ―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ―΄–Ι ―¹―²–Α―²―É―¹, –Κ–Ψ―²–Ψ―Ä―΄–Ι, –≤ ―¹–≤–Ψ―é –Ψ―΅–Β―Ä–Β–¥―¨, ―¹–Ϋ–Η–Ε–Α–Β―² –≤–Ψ―¹–Ω―Ä–Η―è―²–Η–Β ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤. –≠―²–Ψ―² «–Ω–Ψ―Ä–Ψ―΅–Ϋ―΄–Ι –Κ―Ä―É–≥» –Μ―É―΅―à–Β –≤―¹–Β–≥–Ψ –Ψ―²―Ä–Α–Ε–Β–Ϋ –≤ –Φ―É–Μ―¨―²–Η―³–Α–Κ―²–Ψ―Ä–Ϋ–Ψ–Ι –Φ–Ψ–¥–Β–Μ–Η –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α, –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Ϋ–Ψ–Ι –Ϋ–Α ―Ä–Η―¹―É–Ϋ–Κ–Β 3.
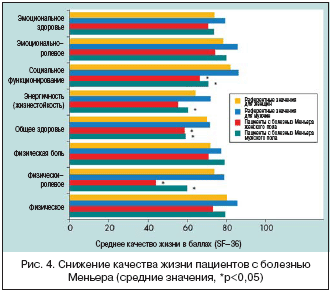
–ù–Η–Ϋ–Κ–Β –£–Α–Ϋ –ö―Ä―É–Ι–Ε―¹–Β–Ϋ (–Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―² –™―Ä–Ψ–Ϋ–Η–Ϋ–≥–Β–Ϋ–Α, –ù–Η–¥–Β―Ä–Μ–Α–Ϋ–¥―΄) –Ω―Ä–Β–¥―¹―²–Α–≤–Η–Μ–Α –¥–Α–Ϋ–Ϋ―΄–Β –Η–Ζ ―¹–Ψ–±―¹―²–≤–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Ω–Ψ –Ψ―Ü–Β–Ϋ–Κ–Β –Ω–Ψ–≤―¹–Β–¥–Ϋ–Β–≤–Ϋ―΄―Ö ―¹―²―Ä–Β―¹―¹–Ψ–≤, –±–Ψ―Ä―¨–±―΄ ―¹ –Ϋ–Η–Φ–Η, –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ–Ψ―¹―²–Η, ―³–Η–Ζ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η –Ω―¹–Η―Ö–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ζ–¥–Ψ―Ä–Ψ–≤―¨―è –Η –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α. –£―¹–Β–≥–Ψ –≤ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω–Ψ―¹–Μ–Β–¥–Ψ–≤–Α―²–Β–Μ―¨–Ϋ–Ψ –±―΄–Μ–Η –≤–Κ–Μ―é―΅–Β–Ϋ―΄ 110 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―É―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Ϋ–Ψ–Ι –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α, –Η–Ζ –Κ–Ψ―²–Ψ―Ä―΄―Ö 74% –Η–Φ–Β–Μ–Η –Ψ–¥–Ϋ–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Β –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β, 61% ―¹–Ψ―¹―²–Α–≤–Η–Μ–Η –Φ―É–Ε―΅–Η–Ϋ―΄, ―¹―Ä–Β–¥–Ϋ–Η–Ι –≤–Ψ–Ζ―Ä–Α―¹―² –±―΄–Μ 52±6,11 –Μ–Β―² –Η ―¹―Ä–Β–¥–Ϋ―è―è –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –±–Ψ–Μ–Β–Ζ–Ϋ–Η 8,2±6,5 –Μ–Β―². –ü–Α―Ü–Η–Β–Ϋ―²―΄ –Ψ―Ü–Β–Ϋ–Η–≤–Α–Μ–Η―¹―¨ ―¹ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ Dutch Daily Hassles List, Coping Inventory for Stressful Situations (CISS – ―¹―Ä–Β–¥―¹―²–≤–Α –±–Ψ―Ä―¨–±―΄ ―¹–Ψ ―¹―²―Ä–Β―¹―¹–Ψ–≤―΄–Φ–Η ―¹–Η―²―É–Α―Ü–Η―è–Φ–Η), Symptoms Checklist 90 (SCL–90 – –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ –Ω–Ψ ―¹–Η–Φ–Ω―²–Ψ–Φ–Α–Φ), NEO Five Factor Inventory (NEO–FFI – –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ –Ω–Ψ 5 ―³–Α–Κ―²–Ψ―Ä–Α–Φ), General Health Questionnaire (GHQ–12 – –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ –Ω–Ψ –Ψ–±―â–Β–Φ―É ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η―é –Ζ–¥–Ψ―Ä–Ψ–≤―¨―è) –Η the Short Form Health Survey 36 (SF–36 – –Κ–Ψ―Ä–Ψ―²–Κ–Α―è ―³–Ψ―Ä–Φ–Α –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ–Α –Ω–Ψ –Ζ–¥–Ψ―Ä–Ψ–≤―¨―é). –ü―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨ –Η ―¹―É–±―ä–Β–Κ―²–Η–≤–Ϋ–Α―è ―²―è–Ε–Β―¹―²―¨ ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ –Ω–Ψ–¥―¹―΅–Η―²―΄–≤–Α–Μ–Α―¹―¨ ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ–Α. –£ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ –≥―Ä―É–Ω–Ω–Ψ–Ι –Ζ–¥–Ψ―Ä–Ψ–≤―΄―Ö –Μ―é–¥–Β–Ι ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η, ―΅―²–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²―΄ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α –Η–Φ–Β–Μ–Η –±–Ψ–Μ―¨―à–Β–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –Ω–Ψ–≤―¹–Β–¥–Ϋ–Β–≤–Ϋ―΄―Ö ―¹―²―Ä–Β―¹―¹–Ψ–≤, –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Μ–Η ―¹―²―Ä–Α―²–Β–≥–Η–Η –±–Ψ―Ä―¨–±―΄ –Φ–Β–Ϋ–Β–Β ―΅–Α―¹―²–Ψ –Η –Ψ–±–Μ–Α–¥–Α–Μ–Η –±o–Μ―¨―à–Β–Ι –Ω―¹–Η―Ö–Ψ–Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι (–Ϋ–Α–Ω―Ä–Η–Φ–Β―Ä, ―²―Ä–Β–≤–Ψ–≥–Α –Η –¥–Β–Ω―Ä–Β―¹―¹–Η―è) –Η ―Ö―É–¥―à–Η–Φ –Κ–Α―΅–Β―¹―²–≤–Ψ–Φ –Ε–Η–Ζ–Ϋ–Η (―Ä–Η―¹. 4) –ù–Η–Κ–Α–Κ–Η―Ö –Α–Ϋ–Ψ–Φ–Α–Μ–Η–Ι –≤ –Η–Ϋ–¥–Η–≤–Η–¥―É–Α–Μ―¨–Ϋ–Ψ―¹―²–Η –≤―΄―è–≤–Μ–Β–Ϋ–Ψ –Ϋ–Β –±―΄–Μ–Ψ. –Θ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –±–Ψ–Μ–Β–Β ―²―è–Ε–Β–Μ―΄–Φ–Η ―¹–Η–Φ–Ω―²–Ψ–Φ–Α–Φ–Η –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Μ–Α―¹―¨ –±o–Μ―¨―à–Α―è –Ω―¹–Η―Ö–Ψ–Ω–Α―²–Ψ–Μ–Ψ–≥–Η―è –Η ―Ö―É–¥―à–Β–Β –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η, ―΅–Β–Φ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Μ–Β–≥–Κ–Η–Φ–Η ―¹–Η–Φ–Ω―²–Ψ–Φ–Α–Φ–Η.
–£–Α–Ε–Ϋ–Α―è –¥–Β―²–Α–Μ―¨ –¥–Α–Ϋ–Ϋ–Ψ–Ι ―Ä–Α–±–Ψ―²―΄ –≤ ―²–Ψ–Φ, ―΅―²–Ψ –Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Ι –Ω―Ä–Ψ―³–Η–Μ―¨ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α ―¹―Ä–Α–≤–Ϋ–Η–Φ ―¹ ―²–Α–Κ–Ψ–≤―΄–Φ –Ω―Ä–Η –¥―Ä―É–≥–Η―Ö ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η –Ψ―¹–Μ–Α–±–Μ―è―é―â–Η―Ö –Ζ–¥–Ψ―Ä–Ψ–≤―¨–Β –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è―Ö. –‰―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ―²–Α–Κ–Ε–Β –≤―΄―è–≤–Η–Μ–Ψ, ―΅―²–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²―΄ ―¹ –±o–Μ―¨―à–Β–Ι –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –±–Ψ–Μ–Β–Ζ–Ϋ–Η –Η–Φ–Β–Μ–Η –±o–Μ―¨―à–Β–Β –Κ–Ψ–Μ–Η―΅–Β―¹―²–≤–Ψ –Ω–Ψ–≤―¹–Β–¥–Ϋ–Β–≤–Ϋ―΄―Ö ―¹―²―Ä–Β―¹―¹–Ψ–≤ –Η ―Ö―É–¥―à–Β–Β –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ –Ω–Α―Ü–Η–Β–Ϋ―²―΄ ―¹ –±–Ψ–Μ–Β–Β ―²―è–Ε–Β–Μ―΄–Φ–Η ―¹–Η–Φ–Ω―²–Ψ–Φ–Α–Φ–Η –Η–Φ–Β–Μ–Η –±o–Μ―¨―à–Η–Β –Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β –Ω―Ä–Ψ–±–Μ–Β–Φ―΄ –Η ―Ö―É–¥―à–Β–Β –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η. –≠―²–Η ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ –Ψ―¹–≤–Β―²–Η–Μ–Η –Ω―Ä–Ψ–±–Μ–Β–Φ―É –Η –Ω―Ä–Ψ–Η–Μ–Μ―é―¹―²―Ä–Η―Ä–Ψ–≤–Α–Μ–Η –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨ –Η–Ϋ―²–Β–Ϋ―¹–Η―³–Η–Κ–Α―Ü–Η–Η –Ω―¹–Η―Ö–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Ψ–Ι –Ω–Ψ–¥–¥–Β―Ä–Ε–Κ–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ ―ç―²–Ψ–Ι –Η–Ϋ–≤–Α–Μ–Η–¥–Η–Ζ–Η―Ä―É―é―â–Β–Ι –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é.
–€–Β–¥–Η–Κ–Α–Φ–Β–Ϋ―²–Ψ–Ζ–Ϋ–Ψ–Β –Μ–Β―΅–Β–Ϋ–Η–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö
–Η –Φ–Ψ–Ζ–Ε–Β―΅–Κ–Ψ–≤―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤
–€–Η―Ö–Α―ç–Μ―¨ –®―²―Ä―É–Ω–Ω (–Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―² –€―é–Ϋ–Η―Ö–Α, –™–Β―Ä–Φ–Α–Ϋ–Η―è) –Ω―Ä–Β–¥―¹―²–Α–≤–Η–Μ –Ψ–±–Ζ–Ψ―Ä ―²–Β–Κ―É―â–Β–≥–Ψ ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η―è –Φ–Β–¥–Η–Κ–Α–Φ–Β–Ϋ―²–Ψ–Ζ–Ϋ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄―Ö –Η –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η―Ö –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤.
–ü–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α
–£–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Ι –Ϋ–Β–≤―Ä–Η―² – –≤―²–Ψ―Ä–Α―è –Ω–Ψ ―΅–Α―¹―²–Ψ―²–Β –Ω―Ä–Η―΅–Η–Ϋ–Α –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ –≤–Β―Ä―²–Η–≥–Ψ, –≤―΄–Ζ―΄–≤–Α–Β―²―¹―è ―Ä–Β–Α–Κ―²–Η–≤–Α―Ü–Η–Β–Ι herpes simplex ―²–Η–Ω–Α 1. –£ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Ω–Μ–Α―Ü–Β–±–Ψ––Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Η–Ζ―É―΅–Α–Μ–Ψ―¹―¨, –Φ–Ψ–≥―É―² –Μ–Η –Κ–Ψ―Ä―²–Η–Κ–Ψ―¹―²–Β―Ä–Ψ–Η–¥―΄, –Ω―Ä–Ψ―²–Η–≤–Ψ–≤–Η―Ä―É―¹–Ϋ―΄–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄ –Η–Μ–Η –Η―Ö –Κ–Ψ–Φ–±–Η–Ϋ–Α―Ü–Η―è ―É–Μ―É―΅―à–Η―²―¨ –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η–Β –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―³―É–Ϋ–Κ―Ü–Η–Η [2]. –‰–Ζ 141 ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Α 38 –Ω–Ψ–Μ―É―΅–Α–Μ–Η –Ω–Μ–Α―Ü–Β–±–Ψ, 35 –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ (100 –Φ–≥ ―É–Φ–Β–Ϋ―¨―à–Α–Β–Φ―΄–Ι –Κ–Α–Ε–¥―΄–Ι ―²―Ä–Β―²–Η–Ι –¥–Β–Ϋ―¨ –Ϋ–Α 20 –Φ–≥), 33 –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä (1 –≥ 3 ―Ä–Α–Ζ–Α –≤ ―¹―É―²–Κ–Η –≤ ―²–Β―΅–Β–Ϋ–Η–Β 7 –¥–Ϋ–Β–Ι) –Η 35 –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ + –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä. –¦–Β―΅–Β–Ϋ–Η–Β –Ϋ–Α―΅–Η–Ϋ–Α–Μ–Ψ―¹―¨ –≤ ―²–Β―΅–Β–Ϋ–Η–Β 3 –¥–Ϋ–Β–Ι –Ω–Ψ―¹–Μ–Β –Ω–Ψ―è–≤–Μ–Β–Ϋ–Η―è ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤. –Γ―Ä–Β–¥–Ϋ–Β–Β (± –Κ–≤–Α–¥―Ä–Α―²–Η―΅–Ϋ–Ψ–Β –Ψ―²–Κ–Μ–Ψ–Ϋ–Β–Ϋ–Η–Β – –ö–û) ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―³―É–Ϋ–Κ―Ü–Η–Η ―΅–Β―Ä–Β–Ζ 12 –Φ–Β―¹―è―Ü–Β–≤ –Ψ―²―¹―Ä–Ψ―΅–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Η–Ψ–¥–Α ―¹–Ψ―¹―²–Α–≤–Η–Μ–Ψ 39,6±28,1% –≤ –≥―Ä―É–Ω–Ω–Β –Ω–Μ–Α―Ü–Β–±–Ψ, 62,4±16,9% – –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ–Α, 36,0±26,7% – –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä–Α –Η 59,2±24,1% – –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ–Α –Ω–Μ―é―¹ –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä. –½–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Β ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –±―΄–Μ–Ψ –≤―΄―è–≤–Μ–Β–Ϋ–Ψ –Ω―Ä–Η –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Η –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ–Α (―Ä<0,001), –Ϋ–Ψ –Ϋ–Β –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä–Α (―Ä=0,43). –≠―²–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω―Ä–Ψ–¥–Β–Φ–Ψ–Ϋ―¹―²―Ä–Η―Ä–Ψ–≤–Α–Μ–Ψ, ―΅―²–Ψ –Φ–Ψ–Ϋ–Ψ―²–Β―Ä–Α–Ω–Η―è –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ–Ψ–Φ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ ―É–Μ―É―΅―à–Η–Μ–Α –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η–Β –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―³―É–Ϋ–Κ―Ü–Η–Η ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ –Ϋ–Β–≤―Ä–Η―²–Ψ–Φ, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä–Ψ–Φ – –Ϋ–Β―². –ö–Ψ–Φ–±–Η–Ϋ–Α―Ü–Η―è –Φ–Β―²–Η–Μ–Ω―Ä–Β–¥–Ϋ–Η–Ζ–Ψ–Μ–Ψ–Ϋ–Α –Η –≤–Α–Μ–Α―Ü–Η–Κ–Μ–Ψ–≤–Η―Ä–Α –Ϋ–Β –Ω―Ä–Β–≤–Ψ―¹―Ö–Ψ–¥–Η–Μ–Α –Κ–Ψ―Ä―²–Η–Κ–Ψ―¹―²–Β―Ä–Ψ–Η–¥–Ϋ―É―é –Φ–Ψ–Ϋ–Ψ―²–Β―Ä–Α–Ω–Η―é. –ù–Α –Ψ―¹–Ϋ–Ψ–≤–Β –¥–Α–Ϋ–Ϋ―΄―Ö –Ω―Ä–Ψ―¹–Ω–Β–Κ―²–Η–≤–Ϋ–Ψ–≥–Ψ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è ―¹–Ω–Β―Ü–Η―³–Η―΅–Ϋ―΄–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β ―É–Ω―Ä–Α–Ε–Ϋ–Β–Ϋ–Η―è ―²–Α–Κ–Ε–Β –Φ–Ψ–≥―É―² ―É–Μ―É―΅―à–Η―²―¨ –≤–Β―¹―²–Η–±―É–Μ–Ψ―¹–Ω–Η–Ϋ–Α–Μ―¨–Ϋ―É―é ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η―é ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ψ―¹―²―Ä―΄–Φ –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η–Φ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ –Ω–Ψ–≤―Ä–Β–Ε–¥–Β–Ϋ–Η–Β–Φ [3].
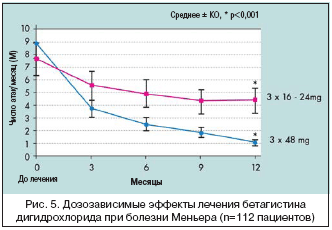
–ù–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ―É–Β―²―¹―è –Φ–Ϋ–Ψ–Ε–Β―¹―²–≤–Ψ –Φ–Β―²–Ψ–¥–Ψ–≤ –Μ–Β―΅–Β–Ϋ–Η―è –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α: –Ψ―² –Ψ–≥―Ä–Α–Ϋ–Η―΅–Β–Ϋ–Η―è –Ω–Ψ―²―Ä–Β–±–Μ–Β–Ϋ–Η―è ―¹–Ψ–Μ–Η, –≤–Ψ–¥―΄, –Κ–Ψ―³–Β–Η–Ϋ–Α –Η –Α–Μ–Κ–Ψ–≥–Ψ–Μ―è –¥–Ψ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―è –¥–Η―É―Ä–Β―²–Η–Κ–Ψ–≤ –Η ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄―Ö –Α–Ϋ–Κ―¹–Η–Ψ–Μ–Η―²–Η–Κ–Ψ–≤. –£–≤–Β–¥–Β–Ϋ–Η–Β –≥–Β–Ϋ―²–Α–Φ–Η―Ü–Η–Ϋ–Α ―΅–Β―Ä–Β–Ζ –±–Α―Ä–Α–±–Α–Ϋ–Ϋ―É―é –Ω–Β―Ä–Β–Ω–Ψ–Ϋ–Κ―É – ―¹–Β–Ι―΅–Α―¹ ―Ä–Β–¥–Κ–Ψ –Η―¹–Ω–Ψ–Μ―¨–Ζ―É–Β–Φ–Α―è –Φ–Α–Ϋ–Η–Ω―É–Μ―è―Ü–Η―è, –Α ―ç–Ϋ–¥–Ψ–Μ–Η–Φ―³–Α―²–Η―΅–Β―¹–Κ–Α―è –Ψ–Ω–Β―Ä–Α―Ü–Η―è –Ϋ–Α –Φ–Β―à–Ψ―΅–Κ–Β –Ω―Ä–Η–Ζ–Ϋ–Α–Ϋ–Α –Ϋ–Β―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ–Ι. –ü–Β―Ä–Ψ―Ä–Α–Μ―¨–Ϋ―΄–Ι –Ω―Ä–Η–Β–Φ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α ―ç―³―³–Β–Κ―²–Η–≤–Β–Ϋ –≤ ―¹–Ψ–Κ―Ä–Α―â–Β–Ϋ–Η–Η ―΅–Α―¹―²–Ψ―²―΄ –Η ―²―è–Ε–Β―¹―²–Η –Α―²–Α–Κ –≤–Β―Ä―²–Η–≥–Ψ, ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Ϋ―΄―Ö –¥–Μ―è –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α. –ë–Β―²–Α–≥–Η―¹―²–Η–Ϋ, ―¹―²―Ä―É–Κ―²―É―Ä–Ϋ―΄–Ι –Α–Ϋ–Α–Μ–Ψ–≥ –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α, –Ψ–±–Μ–Α–¥–Α–Β―² ―΅–Α―¹―²–Η―΅–Ϋ–Ψ ―¹–≤–Ψ–Ι―¹―²–≤–Α–Φ–Η –Α–≥–Ψ–Ϋ–Η―¹―²–Α –≥–Η―¹―²–Α–Φ–Η–Ϋ–Ψ–≤―΄―Ö –ù1–―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ –Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ – ―¹–≤–Ψ–Ι―¹―²–≤–Α–Φ–Η –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η―¹―²–Α –ù3–―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤, ―΅―²–Ψ –Ω―Ä–Ψ–≤–Ψ―Ü–Η―Ä―É–Β―² –Η ―É―¹–Η–Μ–Η–≤–Α–Β―² ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―É―é –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―É―é –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―Ü–Η―é. –ü―Ä–Β–¥–Ω–Ψ–Μ–Α–≥–Α–Μ–Ψ―¹―¨, ―΅―²–Ψ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ –¥–Β–Ι―¹―²–≤―É–Β―² –Ω―É―²–Β–Φ ―É–Μ―É―΅―à–Β–Ϋ–Η―è ―Ü–Η―Ä–Κ―É–Μ―è―Ü–Η–Η –Κ―Ä–Ψ–≤–Η –≤–Ψ –≤–Ϋ―É―²―Ä–Β–Ϋ–Ϋ–Β–Φ ―É―Ö–Β –Η ―É―¹–Η–Μ–Η–≤–Α–Β―² –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η–Β –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α –≤ –Φ–Ψ–Ζ–≥―É, –Κ–Α–Κ –Η –≤ –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η―Ö ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Α―Ö –Μ–Α–±–Η―Ä–Η–Ϋ―²–Α. –ë–Β―²–Α–≥–Η―¹―²–Η–Ϋ –Ψ–±–Μ–Α–¥–Α–Β―² ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄–Φ –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Ψ–Φ –¥–Β–Ι―¹―²–≤–Η―è –Ω―É―²–Β–Φ ―É―¹–Η–Μ–Β–Ϋ–Η―è ―¹–Η–Ϋ―²–Β–Ζ–Α –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α –≤ ―²―É–±–Β―Ä–Ψ–Φ–Α–Φ–Φ–Η–Μ–Μ―è―Ä–Ϋ–Ψ–Φ ―è–¥―Ä–Β –Ζ–Α–¥–Ϋ–Β–≥–Ψ –≥–Η–Ω–Ψ―²–Α–Μ–Α–Φ―É―¹–Α –Η –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η―è –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α –≤ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Φ ―è–¥―Ä–Β ―΅–Β―Ä–Β–Ζ –Α–Ϋ―²–Α–≥–Ψ–Ϋ–Η–Ζ–Φ –ù3––Α―É―²–Ψ―Ä–Β―Ü–Β–Ω―²–Ψ―Ä–Ψ–≤ [4–6]. –î–Α–Ϋ–Ϋ―΄–Β –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ―΄–Ι ―É―¹–Ω–Β―Ö –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è –≤―΄―¹–Ψ–Κ–Η–Φ–Η –¥–Ψ–Ζ–Α–Φ–Η –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α (–Ϋ–Α–Ω―Ä–Η–Φ–Β―Ä, 48 –Φ–≥/―¹―É―². ―²―Ä–Η ―Ä–Α–Ζ–Α –≤ –¥–Β–Ϋ―¨ –≤ ―²–Β―΅–Β–Ϋ–Η–Β 6–12 –Φ–Β―¹―è―Ü–Β–≤) –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η―è ―΅–Η―¹–Μ–Α –Α―²–Α–Κ (―Ä–Η―¹. 5). –Θ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Η–Ϋ–≤–Α–Μ–Η–¥–Η–Ζ–Η―Ä―É―é―â–Β–Ι –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ ―²–Α–Κ–Ε–Β –Ψ―²―¹―Ä–Ψ―΅–Η–Μ –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ―¹―²―¨ –≤ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι –Ϋ–Β–≤―Ä―ç–Κ―²–Ψ–Φ–Η–Η –Η ―É―¹–Η–Μ–Η–Μ –Ω–Ψ―¹–Μ–Β–Ψ–Ω–Β―Ä–Α―Ü–Η–Ψ–Ϋ–Ϋ―É―é –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―É―é –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―Ü–Η―é [7].
–ü―Ä–Β–¥–≤–Α―Ä–Η―²–Β–Μ―¨–Ϋ–Α―è –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Α―è –Ψ―Ü–Β–Ϋ–Κ–Α –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Α, ―΅―²–Ψ –Κ–Α―Ä–±–Α–Φ–Α–Ζ–Β–Ω–Η–Ϋ –Ζ–Ϋ–Α―΅–Η–Φ–Ψ ―¹–Ϋ–Η–Ε–Α–Β―² ―΅–Η―¹–Μ–Ψ –Α―²–Α–Κ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö –Ω–Α―Ä–Ψ–Κ―¹–Η–Ζ–Φ–Ψ–≤, –Κ–Ψ―²–Ψ―Ä―΄–Β ―Ö–Α―Ä–Α–Κ―²–Β―Ä–Η–Ζ―É―é―²―¹―è –Ω–Ψ–≤―²–Ψ―Ä–Ϋ―΄–Φ–Η –Κ–Ψ―Ä–Ψ―²–Κ–Η–Φ–Η –Α―²–Α–Κ–Α–Φ–Η –≤–Β―Ä―²–Η–≥–Ψ, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ―΄―Ö ―¹ –Ϋ–Β–Ι―Ä–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ–Ψ–Ι –Ω–Β―Ä–Β–Κ―Ä–Β―¹―²–Ϋ–Ψ–Ι –Κ–Ψ–Φ–Ω―Ä–Β―¹―¹–Η–Β–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ –Ϋ–Β―Ä–≤–Α [8].
–Π–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β –Η ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄–Β –Ψ–Κ―É–Μ–Ψ–Φ–Ψ―²–Ψ―Ä–Ϋ―΄–Β ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α
–£ ―Ö–Ψ–¥–Β –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –±―΄–Μ–Η –≤―΄―è–≤–Μ–Β–Ϋ―΄ –Ϋ–Ψ–≤―΄–Β –Ω–Ψ–¥―Ö–Ψ–¥―΄ –Κ –Μ–Β―΅–Β–Ϋ–Η―é ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄―Ö –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö –Η ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄―Ö –Ψ–Κ―É–Μ–Ψ–Φ–Ψ―²–Ψ―Ä–Ϋ―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤. –ù–Β–¥–Α–≤–Ϋ–Η–Β ―Ä–Α–±–Ψ―²―΄ –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η, ―΅―²–Ψ –±–Μ–Ψ–Κ–Α―²–Ψ―Ä―΄ –Κ–Α–Μ–Η–Β–≤―΄―Ö –Κ–Α–Ϋ–Α–Μ–Ψ–≤ 3,4––¥–Η–Α–Φ–Η–Ϋ–Ψ–Ω–Η―Ä–Η–¥–Η–Ϋ –Η 4––Α–Φ–Η–Ϋ–Ψ–Ω–Η―Ä–Η–¥–Η–Ϋ (–≤ ―Ö–Ψ―Ä–Ψ―à–Ψ –Ω–Β―Ä–Β–Ϋ–Ψ―¹–Η–Φ―΄―Ö –¥–Ψ–Ζ–Η―Ä–Ψ–≤–Κ–Α―Ö 5–10 –Φ–≥ 3 ―Ä–Α–Ζ–Α –≤ ―¹―É―²–Κ–Η) ―ç―³―³–Β–Κ―²–Η–≤–Ϋ―΄ –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η–Ι, ―Ä–Α–Ϋ–Β–Β ―Ä–Α―¹―¹–Φ–Α―²―Ä–Η–≤–Α–Β–Φ―΄―Ö, –Κ–Α–Κ ―²―Ä―É–¥–Ϋ–Ψ –Ω–Ψ–¥–¥–Α―é―â–Η―Ö―¹―è –Μ–Β―΅–Β–Ϋ–Η―é, ―²–Α–Κ–Η–Β –Κ–Α–Κ –Ϋ–Η―¹―Ö–Ψ–¥―è―â–Η–Ι –Ϋ–Η―¹―²–Α–≥–Φ [9,10], –≤–Ψ―¹―Ö–Ψ–¥―è―â–Η–Ι –Ϋ–Η―¹―²–Α–≥–Φ [11] –Η –Ω–Β―Ä–Η–Ψ–¥–Η―΅–Β―¹–Κ–Α―è –Α―²–Α–Κ―¹–Η―è 26 ―²–Η–Ω–Α [12]. –£–Μ–Η―è–Ϋ–Η–Β ―ç―²–Η―Ö –±–Μ–Ψ–Κ–Α―²–Ψ―Ä–Ψ–≤ –Κ–Α–Μ–Η–Β–≤―΄―Ö –Κ–Α–Ϋ–Α–Μ–Ψ–≤ –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –Ψ―²–Ϋ–Β―¹–Β–Ϋ–Ψ –Κ ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η―é –≤–Ψ–Ζ–±―É–¥–Η–Φ–Ψ―¹―²–Η –Κ–Μ–Β―²–Ψ–Κ –ü―É―Ä–Κ–Η–Ϋ―¨–Β –Φ–Ψ–Ζ–Ε–Β―΅–Κ–Α. –î―Ä―É–≥–Η–Β ―³–Α―Ä–Φ–Α–Κ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄, –≤―¹–Β ―΅–Α―â–Β –Η―¹–Ω–Ψ–Μ―¨–Ζ―É–Β–Φ―΄–Β –≤ –Ω―Ä–Α–Κ―²–Η–Κ–Β – ―ç―²–Ψ b––±–Μ–Ψ–Κ–Α―²–Ψ―Ä―΄ –Ω―Ä–Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι –Φ–Η–≥―Ä–Β–Ϋ–Η –Η–Μ–Η ―¹–Β–Μ–Β–Κ―²–Η–≤–Ϋ―΄–Β –Η–Ϋ–≥–Η–±–Η―²–Ψ―Ä―΄ –Ω–Ψ–≤―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ –Ζ–Α―Ö–≤–Α―²–Α ―¹–Β―Ä–Ψ―²–Ψ–Ϋ–Η–Ϋ–Α –Ω―Ä–Η ―³–Ψ–±–Η―΅–Β―¹–Κ–Ψ–Φ –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ–Ψ–Φ –≤–Β―Ä―²–Η–≥–Ψ [13], ―Ö–Ψ―²―è –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Β–Β –≤―¹–Β –Β―â–Β ―²―Ä–Β–±―É–Β―² –¥–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨―¹―²–≤ –≤ –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è―Ö.
–Δ―Ä–Β―²―¨―è ―΅–Α―¹―²―¨ ―¹–Η–Φ–Ω–Ψ–Ζ–Η―É–Φ–Α –Ω―Ä–Ψ―Ö–Ψ–¥–Η–Μ–Α –Ω–Ψ–¥
–Ω―Ä–Β–¥―¹–Β–¥–Α―²–Β–Μ―¨―¹―²–≤–Ψ–Φ –Λ–Β―Ä–Ϋ–Α–Ϋ–¥–Ψ –£–Α–Ζ –™–Α―Ä―Ü–Η–Α (–ü–Ψ―Ä―²―É–≥–Α–Μ–Η―è) –Η –±―΄–Μ–Α –Ω–Ψ―¹–≤―è―â–Β–Ϋ–Α –Ω–Ψ–Ε–Η–Μ―΄–Φ –Ω–Α―Ü–Η–Β–Ϋ―²–Α–Φ –Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Η
–Θ―¹–Μ–Ψ–≤–Η―è –Η –Ω–Ψ―¹–Μ–Β–¥―¹―²–≤–Η―è –Ω–Α–¥–Β–Ϋ–Η–Ι ―¹―Ä–Β–¥–Η –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ–Η ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α–Φ–Η
–ü–Α–¥–Β–Ϋ–Η―è –Κ―Ä–Α–Ι–Ϋ–Β ―΅–Α―¹―²―΄ ―¹―Ä–Β–¥–Η –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Η ―¹–≤―è–Ζ–Α–Ϋ―΄ ―¹–Ψ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ―΄–Φ ―É―Ö―É–¥―à–Β–Ϋ–Η–Β–Φ –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η, ―É–≤–Β–Μ–Η―΅–Β–Ϋ–Η–Β–Φ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Β–Φ–Ψ―¹―²–Η –Η ―¹―²–Ψ–Η–Φ–Ψ―¹―²–Η –Μ–Β―΅–Β–Ϋ–Η―è. –£ –Ϋ–Β–¥–Α–≤–Ϋ–Β–Φ –Ω–Β―Ä–Β–Κ―Ä–Β―¹―²–Ϋ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η, –≤–Κ–Μ―é―΅–Η–≤―à–Β–Φ 4003 –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (65 –Μ–Β―² –Η –±–Ψ–Μ–Β–Β), ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ϋ–Ψ―¹―²―¨ –Ω–Α–¥–Β–Ϋ–Η–Ι ―¹–Ψ―¹―²–Α–≤–Η–Μ–Α 34,8%, –Ϋ–Ψ –±―΄–Μ–Α –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –≤―΄―à–Β ―¹―Ä–Β–¥–Η –Ε–Β–Ϋ―â–Η–Ϋ (40,1%), ―΅–Β–Φ –Φ―É–Ε―΅–Η–Ϋ. –Θ 12,1% –±―΄–Μ–Η –Ω–Β―Ä–Β–Μ–Ψ–Φ―΄ [14]. –û–Κ–Ψ–Μ–Ψ 60% –Ω–Β―Ä–Β–Μ–Ψ–Φ–Ψ–≤ ―É –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹–Μ―É―΅–Α–Ι–Ϋ―΄, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ 20% –≤–Ψ–Ζ–Ϋ–Η–Κ–Α―é―² –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –Ϋ–Β–≤―Ä–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι –Η 20% – –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤. –£–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α –≤―΄―Ä–Α–Ε–Α―é―²―¹―è –≤ ―¹–Ϋ–Η–Ε–Β–Ϋ–Ϋ–Ψ–Φ –Ω–Ψ―¹―²―É―Ä–Α–Μ―¨–Ϋ–Ψ–Φ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Β ―¹ –Ϋ–Β―¹―²–Α–±–Η–Μ―¨–Ϋ–Ψ―¹―²―¨―é –Ω–Ψ–Ζ―΄ –≤–Ψ –≤―Ä–Β–Φ―è –Ω–Β―Ä–Β―Ö–Ψ–¥–Ϋ―΄―Ö –¥–≤–Η–Ε–Β–Ϋ–Η–Ι, ―²–Α–Κ–Η―Ö –Κ–Α–Κ –Ω–Β―Ä–Β―Ö–Ψ–¥ –Η–Ζ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η―è –Μ–Β–Ε–Α –≤ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η–Β ―¹–Η–¥―è –Η ―¹―²–Ψ―è [15]. –Θ –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ–Η ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α–Φ–Η 53,1% –Ω–Α–¥–Β–Ϋ–Η–Ι –Ϋ–Α–Ω―Ä―è–Φ―É―é ―¹–≤―è–Ζ–Α–Ϋ―΄ ―¹ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ –Η –≤–Β―Ä―²–Η–≥–Ψ [16]. –î–Α–Ϋ–Ϋ―΄–Β, –Η–Ζ–Μ–Ψ–Ε–Β–Ϋ–Ϋ―΄–Β –ü–Β–¥―Ä–Ψ –¦―É–Η–Ζ –€–Α–Ϋ–≥–Α–±–Β–Ι―Ä–Α –ê–Μ―¨–±–Β―Ä–Ϋ–Α―Ü (–Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―² –Γ–Α–Ϋ––ü–Α―É–Μ–Ψ, –ë―Ä–Α–Ζ–Η–Μ–Η―è), –Ω–Ψ–Ζ–≤–Ψ–Μ―è―é―² –≥–Ψ–≤–Ψ―Ä–Η―²―¨ –Ψ ―²–Ψ–Φ, ―΅―²–Ψ –Η–Ϋ―³–Ψ―Ä–Φ–Α―Ü–Η―è –Ω–Ψ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α–Φ ―É –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Φ–Ψ–Ε–Β―² –Ψ–±–Β―¹–Ω–Β―΅–Η―²―¨ ―Ä–Α–Ζ―Ä–Α–±–Ψ―²–Κ―É ―Ä―É–Κ–Ψ–≤–Ψ–¥―¹―²–≤ –¥–Μ―è –Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―â–Β–Ϋ–Η―è –Ω–Α–¥–Β–Ϋ–Η–Ι.
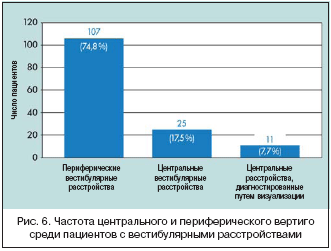
–ê–Ϋ–Α–Μ–Η–Ζ –Η―¹―²–Ψ―Ä–Η–Ι –±–Ψ–Μ–Β–Ζ–Ϋ–Η 681 –Ω–Ψ–Ε–Η–Μ–Ψ–≥–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Α (–Ψ–±―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ―΄ ―¹ 1990 –Ω–Ψ 2007 –≥., ―¹―Ä–Β–¥–Ϋ–Η–Ι –≤–Ψ–Ζ―Ä–Α―¹―² 72 –≥–Ψ–¥–Α, 62,2% –Ε–Β–Ϋ―â–Η–Ϋ) –≤―΄―è–≤–Η–Μ, ―΅―²–Ψ 143 (21%) –Η–Φ–Β–Μ–Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è. –ü–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β –Ω―Ä–Ψ–±–Μ–Β–Φ―΄ –≤―΄―è–≤–Μ–Β–Ϋ―΄ –≤ 107 ―¹–Μ―É―΅–Α―è―Ö (74,8%), –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ –Ψ―¹―²–Α–≤―à–Η–Β―¹―è 36 ―¹–Μ―É―΅–Α–Β–≤ –Ψ―²–Ϋ–Ψ―¹–Η–Μ–Η―¹―¨ –Κ ―Ü–Β–Ϋ―²―Ä–Α–Μ―¨–Ϋ―΄–Φ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Φ ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α–Φ (25,2%) (―Ä–Η―¹. 6). –£―¹–Β–≥–Ψ ―É 19 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ (13,2%) –±―΄–Μ–Ψ –±–Ψ–Μ–Β–Β –Ψ–¥–Ϋ–Ψ–≥–Ψ –Ω–Α–¥–Β–Ϋ–Η―è. –ù–Α–Η–±–Ψ–Μ–Β–Β ―΅–Α―¹―²–Ψ –Ω–Α–¥–Β–Ϋ–Η―è ―¹–Μ―É―΅–Α–Μ–Η―¹―¨ –≤ –≤–Α–Ϋ–Ϋ–Ψ–Ι –Κ–Ψ–Φ–Ϋ–Α―²–Β, –¥–Ψ–Φ–Α –Ϋ–Ψ―΅―¨―é, –Η ―΅–Η―¹–Μ–Ψ –Ω–Α–¥–Β–Ϋ–Η–Ι ―É–≤–Β–Μ–Η―΅–Η–≤–Α–Μ–Ψ―¹―¨ –Ζ–Η–Φ–Ψ–Ι –≤ ―¹–≤―è–Ζ–Η ―¹ –±–Ψ–Μ–Β–Β –≤―΄―Ä–Α–Ε–Β–Ϋ–Ϋ―΄–Φ ―ç–Ϋ―É―Ä–Β–Ζ–Ψ–Φ. –û–¥–Η–Ϋ –Ω–Α―Ü–Η–Β–Ϋ―² ―É–Ω–Α–Μ –≤–Ψ –≤―Ä–Β–Φ―è –Η–≥―Ä―΄ –≤ –≥–Ψ–Μ―¨―³, –¥―Ä―É–≥–Ψ–Ι – –Ω―Ä–Ψ–≥―É–Μ–Κ–Η –Ϋ–Α ―É–Μ–Η―Ü–Β, –¥―Ä―É–≥–Ψ–Ι – –Ϋ–Α –≤―΄―Ö–Ψ–¥–Β –Η–Ζ ―Ä–Β―¹―²–Ψ―Ä–Α–Ϋ–Α –Ω–Ψ―¹–Μ–Β ―É–Ε–Η–Ϋ–Α. –Θ 4 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –±―΄–Μ–Η ―¹–Ω–Ψ–Ϋ―²–Α–Ϋ–Ϋ―΄–Β –Ω–Α–¥–Β–Ϋ–Η―è, ―É 5 –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –±―΄–Μ–Η –Ω–Β―Ä–Β–Μ–Ψ–Φ―΄, ―É –Ψ–¥–Ϋ–Ψ–≥–Ψ –Η–Ζ –Κ–Ψ―²–Ψ―Ä―΄―Ö –Φ–Ϋ–Ψ–Ε–Β―¹―²–≤–Β–Ϋ–Ϋ―΄–Β (–Η–Ζ––Ζ–Α –Ω–Ψ–≤―²–Ψ―Ä–Ϋ―΄―Ö –Ω–Α–¥–Β–Ϋ–Η–Ι). –ù–Α–Η–±–Ψ–Μ–Β–Β ―΅–Α―¹―²―΄–Ι –Ω–Β―Ä–Β–Μ–Ψ–Φ – ―à–Β–Ι–Κ–Η –±–Β–¥―Ä–Α, –Ϋ–Ψ ―É –Ψ–¥–Ϋ–Ψ–≥–Ψ –Ω–Α―Ü–Η–Β–Ϋ―²–Α –±―΄–Μ –Ω–Β―Ä–Β–Μ–Ψ–Φ –≥―Ä―É–¥–Ϋ–Ψ–≥–Ψ –Ψ―²–¥–Β–Μ–Α –Ω–Ψ–Ζ–≤–Ψ–Ϋ–Ψ―΅–Ϋ–Η–Κ–Α. –ù–Β–Ψ–±―Ö–Ψ–¥–Η–Φ–Ψ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Η–Β –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι ―¹ ―Ü–Β–Μ―¨―é –Ω―Ä–Β–¥–Ψ―²–≤―Ä–Α―â–Β–Ϋ–Η―è –Ω–Α–¥–Β–Ϋ–Η–Ι –≤ –≤―΄―¹–Ψ–Κ–Ψ–≤–Ψ―¹–Ω―Ä–Η–Η–Φ―΅–Η–≤–Ψ–Ι –Ω–Ψ–Ω―É–Μ―è―Ü–Η–Η. –£–Ψ––Ω–Β―Ä–≤―΄―Ö, –Κ–Μ–Η–Ϋ–Η―Ü–Η―¹―²―΄ –¥–Ψ–Μ–Ε–Ϋ―΄ –±―΄―²―¨ –±–Ψ–Μ―¨―à–Β –Ψ―¹–≤–Β–¥–Ψ–Φ–Μ–Β–Ϋ―΄ –Ψ ―Ä–Η―¹–Κ–Β –Ω–Α–¥–Β–Ϋ–Η―è ―É –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω―Ä–Η―΅–Β–Φ –±–Ψ–Μ―¨―à–Η–Ι –Α–Κ―Ü–Β–Ϋ―² –¥–Ψ–Μ–Ε–Β–Ϋ –±―΄―²―¨ ―¹–¥–Β–Μ–Α–Ϋ –Ϋ–Α –¥–Η–Α–≥–Ϋ–Ψ―¹―²–Η–Κ–Β –Η –Μ–Β―΅–Β–Ϋ–Η–Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤. –ü―Ä–Α–≤–Η–Μ―¨–Ϋ―΄–Ι –¥–Η–Α–≥–Ϋ–Ψ–Ζ –Η –Μ–Β―΅–Β–Ϋ–Η–Β –Φ–Β―²–Α–±–Ψ–Μ–Η―΅–Β―¹–Κ–Η―Ö –Ϋ–Α―Ä―É―à–Β–Ϋ–Η–Ι (–Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ –≥–Η–Ω–Ψ–≥–Μ–Η–Κ–Β–Φ–Η–Η) ―²–Α–Κ–Ε–Β –Ϋ–Β–Φ–Α–Μ–Ψ–≤–Α–Ε–Ϋ―΄ –¥–Μ―è ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η―è ―΅–Α―¹―²–Ψ―²―΄ –Ω–Α–¥–Β–Ϋ–Η–Ι. –ü–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –≤ –≥―Ä―É–Ω–Ω–Β –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―΅–Α―â–Β –≤―¹―²―Ä–Β―΅–Α–Β―²―¹―è –Ω–Ψ–Μ–Η–Ω―Ä–Α–≥–Φ–Α–Ζ–Η―è, –Ϋ–Β–Ψ–±―Ö–Ψ–¥–Η–Φ ―²―â–Α―²–Β–Μ―¨–Ϋ―΄–Ι –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨ –Ϋ–Α–Ζ–Ϋ–Α―΅–Α–Β–Φ―΄―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, –Ψ―¹–Ψ–±–Β–Ϋ–Ϋ–Ψ –¥–Η―É―Ä–Β―²–Η–Κ–Ψ–≤. –£―¹–Β –Ω―Ä–Β–Ω–Α―Ä–Α―²―΄ –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –≥–Η–Ω–Β―Ä―²–Ψ–Ϋ–Η–Η ―¹–Ϋ–Η–Ε–Α―é―² ―Ü–Β―Ä–Β–±―Ä–Α–Μ―¨–Ϋ―΄–Ι –Κ―Ä–Ψ–≤–Ψ―²–Ψ–Κ, –¥–Η―É―Ä–Β―²–Η–Κ–Η –Η b––±–Μ–Ψ–Κ–Α―²–Ψ―Ä―΄ –≤―΄–Ζ―΄–≤–Α―é―² ―¹–Α–Φ–Ψ–Β –±–Ψ–Μ―¨―à–Ψ–Β ―¹–Ϋ–Η–Ε–Β–Ϋ–Η–Β ―Ü–Β―Ä–Β–±―Ä–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Κ―Ä–Ψ–≤–Ψ―²–Ψ–Κ–Α –Η –Φ–Ψ–≥―É―² –±―΄―²―¨ –Ϋ–Α–Ω―Ä―è–Φ―É―é ―¹–≤―è–Ζ–Α–Ϋ―΄ ―¹ –Ω–Α–¥–Β–Ϋ–Η―è–Φ–Η. –û–¥–Ϋ–Α–Κ–Ψ ―¹–Α–Φ–Ψ–Ι –≤–Α–Ε–Ϋ–Ψ–Ι ―è–≤–Μ―è–Β―²―¹―è ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Α―è –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Α―è ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η―è –Ω–Ψ–Ε–Η–Μ―΄―Ö –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤.
–£–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Α―è –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―Ü–Η―è ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄
–ü–Α―Ü–Η–Β–Ϋ―²―΄ ―¹ –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄ –Ε–Α–Μ―É―é―²―¹―è –Ϋ–Α –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β –Η –Ϋ–Β―É―¹―²–Ψ–Ι―΅–Η–≤–Ψ―¹―²―¨, –Ψ―¹―Ü–Η–Μ–Μ–Ψ–Ω―¹–Η―é, –Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ―¹―²–≤–Β–Ϋ–Ϋ―É―é –¥–Β–Ζ–Ψ―Ä–Η–Β–Ϋ―²–Α―Ü–Η―é, –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –Ψ―â―É―â–Β–Ϋ–Η―è –≤–Β―Ä―²–Η–Κ–Α–Μ―¨–Ϋ–Ψ–≥–Ψ –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η―è, ―²–Ψ―à–Ϋ–Ψ―²―É –Η ―Ä–≤–Ψ―²―É. –ü–Ψ―¹–Κ–Ψ–Μ―¨–Κ―É –Ϋ–Β–Ι―Ä–Ψ–≤–Β–≥–Β―²–Α―²–Η–≤–Ϋ–Α―è ―¹–Η–Φ–Ω―²–Ψ–Φ–Α―²–Η–Κ–Α –Η―¹―΅–Β–Ζ–Α–Β―² –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Ϋ–Β―¹–Κ–Ψ–Μ―¨–Κ–Η―Ö –¥–Ϋ–Β–Ι –Ω–Ψ―¹–Μ–Β –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η―è –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄, –Ω–Ψ―¹―²―É―Ä–Ψ––Μ–Ψ–Κ–Ψ–Φ–Ψ―²–Ψ―Ä–Ϋ―΄–Β, –Ψ–Κ―É–Μ–Ψ–Φ–Ψ―²–Ψ―Ä–Ϋ―΄–Β –Η –Ω–Β―Ä―Ü–Β–Ω―²–Η–≤–Ϋ―΄–Β ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ ―²―Ä–Β–±―É―é―² –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Η –¥–Μ―è –Ω–Ψ–Μ–Ϋ–Ψ–Ι –Η–Μ–Η ―΅–Α―¹―²–Η―΅–Ϋ–Ψ–Ι –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―Ü–Η–Η. –€–Η―Ö–Α―ç–Μ―¨ –¦–Α–Κ―É―Ä, –Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―² de Provence, –€–Α―Ä―¹–Β–Μ―¨, –Λ―Ä–Α–Ϋ―Ü–Η―è, ―¹–¥–Β–Μ–Α–Μ –Ψ–±–Ζ–Ψ―Ä –Ω―Ä–Β–Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –Η –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ–Η―Ö –¥–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―¨―¹―²–≤ ―²–Ψ–≥–Ψ, –Κ–Α–Κ –Φ–Ψ–Ε–Β―² –±―΄―²―¨ –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Α –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Α―è ―³―É–Ϋ–Κ―Ü–Η―è ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ψ–¥–Ϋ–Ψ―¹―²–Ψ―Ä–Ψ–Ϋ–Ϋ–Η–Φ –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Η–Β–Φ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―¹–Η―¹―²–Β–Φ―΄, –Η –Ψ–±―ä―è―¹–Ϋ–Η–Μ –Ω―Ä–Η–Ϋ―Ü–Η–Ω―΄, –Κ–Ψ―²–Ψ―Ä―΄–Φ–Η –¥–Ψ–Μ–Ε–Ϋ―΄ ―Ä―É–Κ–Ψ–≤–Ψ–¥―¹―²–≤–Ψ–≤–Α―²―¨―¹―è –≤―Ä–Α―΅–Η –Ω―Ä–Η –Μ–Β―΅–Β–Ϋ–Η–Η –Η ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –Ω–Ψ―²–Β―Ä–Β–Ι –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―³―É–Ϋ–Κ―Ü–Η–Ι.
–û―¹–Ϋ–Ψ–≤–Ϋ―΄–Β –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ―΄, –Μ–Β–Ε–Α―â–Η–Β –≤ –Ψ―¹–Ϋ–Ψ–≤–Β –¥–≤―É―Ö –≥–Μ–Α–≤–Ϋ―΄―Ö ―²–Β–Ψ―Ä–Η–Ι –Ω–Ψ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―Ü–Η–Η (―¹―²–Α―²–Η―΅–Β―¹–Κ–Ψ–Ι –Η –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Ψ–Ι), –Ω―Ä–Ψ–Η–Μ–Μ―é―¹―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ―΄ –Ϋ–Α ―Ä–Η―¹―É–Ϋ–Κ–Β 7. –Γ―²–Α―²–Η―΅–Β―¹–Κ–Η–Ι –¥–Β―³–Η―Ü–Η―², –Ω―Ä–Ψ–Η–Μ–Μ―é―¹―²―Ä–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄–Ι –Ζ–¥–Β―¹―¨ ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α, –Κ–Ψ―²–Ψ―Ä―΄–Φ –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Α –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Α―è –Ϋ–Β–≤―Ä―ç–Κ―²–Ψ–Φ–Η―è, –Ω–Ψ–Μ–Ϋ–Ψ―¹―²―¨―é –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Η―Ä―É–Β―²―¹―è ―¹–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Β–Φ – ―Ä–Β–Ζ―É–Μ―¨―²–Α―², –Κ–Ψ―²–Ψ―Ä―΄–Ι –Φ–Ψ–Ε–Ϋ–Ψ –Ψ–±―ä―è―¹–Ϋ–Η―²―¨ –Ω–Μ–Α―¹―²–Η―΅–Β―¹–Κ–Η–Φ–Η –Η–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è–Φ–Η, –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥―è―â–Η–Φ–Η –≤ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Φ ―è–¥―Ä–Β ―¹―²–≤–Ψ–Μ–Α –Φ–Ψ–Ζ–≥–Α. –ù–Α–Ω―Ä–Ψ―²–Η–≤, –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η–Ι –¥–Β―³–Β–Κ―² ―É –¥–Α–Ϋ–Ϋ–Ψ–Ι –≥―Ä―É–Ω–Ω―΄ –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ –Ψ―¹―²–Α–Β―²―¹―è –Ω–Μ–Ψ―Ö–Ψ ―¹–Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ―΄–Φ ―¹–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Β–Φ, ―΅―²–Ψ ―É–Κ–Α–Ζ―΄–≤–Α–Β―² –Ϋ–Α ―²–Ψ, ―΅―²–Ψ –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η–Β –¥–Η–Ϋ–Α–Φ–Η―΅–Β―¹–Κ–Η―Ö –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄―Ö ―³―É–Ϋ–Κ―Ü–Η–Ι –Ω―Ä–Ψ–Η―¹―Ö–Ψ–¥–Η―² –≤ ―Ä–Β–Ζ―É–Μ―¨―²–Α―²–Β –Ζ–Α–Φ–Β―â–Α―é―â–Η―Ö –Ω―Ä–Ψ―Ü–Β―¹―¹–Ψ–≤.
–ï―¹―²―¨ –¥–Α–Ϋ–Ϋ―΄–Β, ―΅―²–Ψ –Ϋ–Α―΅–Α–Μ–Ψ ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Η –Ϋ–Α ―Ä–Α–Ϋ–Ϋ–Η―Ö ―¹―Ä–Ψ–Κ–Α―Ö, –Ω―Ä–Β–¥–Ω–Ψ―΅―²–Β–Ϋ–Η–Β –Α–Κ―²–Η–≤–Ϋ–Ψ–Ι ―²―Ä–Β–Ϋ–Η―Ä–Ψ–≤–Κ–Η –Η –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―è ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Ψ–Ϋ–Ϋ―΄―Ö –Ω―Ä–Ψ–≥―Ä–Α–Φ–Φ ―¹ ―É–Ω―Ä–Α–Ε–Ϋ–Β–Ϋ–Η―è–Φ–Η, –≤―΄–Ω–Ψ–Μ–Ϋ―è–Β–Φ―΄―Ö –≤ ―¹―²–Α–Ϋ–¥–Α―Ä―²–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Ι, –Ϋ–Ψ –Φ–Β–Ϋ―è―é―â–Β–Ι―¹―è –Ψ–Κ―Ä―É–Ε–Α―é―â–Β–Ι –Ψ–±―¹―²–Α–Ϋ–Ψ–≤–Κ–Β, –Η ―²―Ä–Β–Ϋ–Η―Ä–Ψ–≤–Κ–Η, –Α–¥–Α–Ω―²–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Ι –Κ –Κ–Α–Ε–¥–Ψ–Φ―É –Κ–Ψ–Ϋ–Κ―Ä–Β―²–Ϋ–Ψ–Φ―É –Ω–Α―Ü–Η–Β–Ϋ―²―É – –≥–Μ–Α–≤–Ϋ―΄–Β –Ω―Ä–Α–Κ―²–Η―΅–Β―¹–Κ–Η–Β ―à–Α–≥–Η –≤ ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤. –Δ–Α–Κ–Ε–Β ―Ä–Β–Κ–Ψ–Φ–Β–Ϋ–¥―É–Β―²―¹―è –Η–Ζ–±–Β–≥–Α―²―¨ –¥–Μ–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –Φ–Β–¥–Η–Κ–Α–Φ–Β–Ϋ―²–Ψ–Ζ–Ϋ–Ψ–≥–Ψ –Μ–Β―΅–Β–Ϋ–Η―è ―¹ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ ―¹ ―¹–Β–¥–Α―²–Η–≤–Ϋ―΄–Φ ―ç―³―³–Β–Κ―²–Ψ–Φ: ―¹–Μ–Β–¥―É–Β―² –Ϋ–Α–Ζ–Ϋ–Α―΅–Α―²―¨ ―¹―Ä–Β–¥―¹―²–≤–Α, ―É―¹–Κ–Ψ―Ä―è―é―â–Η–Β –Ω―Ä–Ψ―Ü–Β―¹―¹ –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η―è. –û–¥–Ϋ–Η–Φ –Η–Ζ ―²–Α–Κ–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ ―è–≤–Μ―è–Β―²―¹―è –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ.
–™–Η―¹―²–Α–Φ–Η–Ϋ ―è–≤–Μ―è–Β―²―¹―è –Ϋ–Β–Ι―Ä–Ψ–Φ–Ψ–¥―É–Μ―è―²–Ψ―Ä–Ϋ―΄–Φ ―²―Ä–Α–Ϋ―¹–Φ–Η―²―²–Β―Ä–Ψ–Φ, –Κ–Ψ―²–Ψ―Ä―΄–Ι ―Ä–Β–≥―É–Μ–Η―Ä―É–Β―² ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β ―Ü–Β―Ä–Β–±―Ä–Α–Μ―¨–Ϋ―΄–Β ―³―É–Ϋ–Κ―Ü–Η–Η, –≤–Κ–Μ―é―΅–Α―è –±–Ψ–¥―Ä―¹―²–≤–Ψ–≤–Α–Ϋ–Η–Β, –Η –Κ–Α―Ä–¥–Η–Ψ–≤–Α―¹–Κ―É–Μ―è―Ä–Ϋ―É―é –¥–Β―è―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨. –ù–Β–Κ–Ψ―²–Ψ―Ä―΄–Β ―É―΅–Β–Ϋ―΄–Β –Ω–Ψ–¥―΅–Β―Ä–Κ–Η–≤–Α―é―², ―΅―²–Ψ –≥–Η―¹―²–Α–Φ–Η–Ϋ ―Ä–Β–≥―É–Μ–Η―Ä―É–Β―² ―²–Α–Κ–Ε–Β ―Ä–Α–Ζ–Μ–Η―΅–Ϋ―΄–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β ―³―É–Ϋ–Κ―Ü–Η–Η. –î–Ψ –Ω–Ψ―¹–Μ–Β–¥–Ϋ–Β–≥–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Η –±―΄–Μ–Ψ ―Ä–Α―¹–Ω―Ä–Ψ―¹―²―Ä–Α–Ϋ–Β–Ϋ–Ψ ―É–±–Β–Ε–¥–Β–Ϋ–Η–Β, ―΅―²–Ψ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α, ―¹―²―Ä―É–Κ―²―É―Ä–Ϋ–Ψ–≥–Ψ –Α–Ϋ–Α–Μ–Ψ–≥–Α –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α, ―¹–≤―è–Ζ–Α–Ϋ–Α ―²–Ψ–Μ―¨–Κ–Ψ ―¹ –≤–Μ–Η―è–Ϋ–Η–Β–Φ –Ϋ–Α ―¹–Ψ―¹―É–¥–Η―¹―²―΄–Ι –Κ–Ψ–Φ–Ω–Ψ–Ϋ–Β–Ϋ―² –≤–Ϋ―É―²―Ä–Β–Ϋ–Ϋ–Β–≥–Ψ ―É―Ö–Α. –Γ–Β–Ι―΅–Α―¹ –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ, ―΅―²–Ψ, –Ω–Ψ–Φ–Η–Φ–Ψ –¥–Β–Ι―¹―²–≤–Η―è –Ϋ–Α ―¹–Ψ―¹―É–¥―΄ –≤–Ϋ―É―²―Ä–Β–Ϋ–Ϋ–Β–≥–Ψ ―É―Ö–Α, –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Η–Β –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β ―΅―É–≤―¹―²–≤–Η―²–Β–Μ―¨–Ϋ―΄–Β –Κ–Μ–Β―²–Κ–Η –Η –≤–Ψ–Ζ–±―É–Ε–¥–Α―é―â–Β–≥–Ψ ―ç―³―³–Β–Κ―²–Α –Ϋ–Α –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Ϋ–Β–Ι―Ä–Ψ–Ϋ–Ψ–≤ –Κ–Ψ―Ä―²–Η–Κ–Α–Μ―¨–Ϋ―΄―Ö –Η ―¹―É–±–Κ–Ψ―Ä―²–Η–Κ–Α–Μ―¨–Ϋ―΄―Ö ―¹―²―Ä―É–Κ―²―É―Ä, –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ –Η–Ϋ―²–Β–Ϋ―¹–Η–≤–Ϋ–Ψ –≤–Ζ–Α–Η–Φ–Ψ–¥–Β–Ι―¹―²–≤―É–Β―² ―¹ –≥–Η―¹―²–Α–Φ–Η–Ϋ–Β―Ä–≥–Η―΅–Β―¹–Κ–Ψ–Ι ―¹–Η―¹―²–Β–Φ–Ψ–Ι, ―É–≤–Β–Μ–Η―΅–Η–≤–Α―è ―¹–Η–Ϋ―²–Β–Ζ –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α –Η –≤―΄―¹–≤–Ψ–±–Ψ–Ε–¥–Β–Ϋ–Η–Β –≤ ―²―É–±–Β―Ä–Ψ–Φ–Α–Φ–Φ–Η–Μ―è―Ä–Ϋ–Ψ–Φ ―è–¥―Ä–Β –Ζ–Α–¥–Ϋ–Β–≥–Ψ –≥–Η–Ω–Ψ―²–Α–Μ–Α–Φ―É―¹–Α. –£–Μ–Η―è–Ϋ–Η–Β –≥–Η―¹―²–Α–Φ–Η–Ϋ–Α –Ϋ–Α –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Β –Κ–Μ–Β―²–Κ–Η –Ω–Ψ―Ä–Α–Ε–Β–Ϋ–Ϋ–Ψ–Ι ―¹―²–Ψ―Ä–Ψ–Ϋ―΄ –Φ–Ψ–Ε–Β―² –≤–Ϋ–Ψ―¹–Η―²―¨ –≤–Κ–Μ–Α–¥ –≤ –Ω–Β―Ä–Β–±–Α–Μ–Α–Ϋ―¹–Η―Ä–Ψ–≤–Κ―É –Ϋ–Β–Ι―Ä–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η –Φ–Β–Ε–¥―É –¥–≤―É–Φ―è ―¹―²–Ψ―Ä–Ψ–Ϋ–Α–Φ–Η, –Α ―ç―²–Ψ –Κ–Μ―é―΅–Β–≤–Ψ–Ι –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ –≤ –≤–Ψ―¹―¹―²–Α–Ϋ–Ψ–≤–Μ–Β–Ϋ–Η–Η –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―³―É–Ϋ–Κ―Ü–Η–Η. –£–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―΄–Ι –¥–Β―³–Η―Ü–Η―² ―²―Ä–Β–±―É–Β―² –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–≥–Ψ –≤―Ä–Β–Φ–Β–Ϋ–Η –¥–Μ―è –Κ–Ψ–Φ–Ω–Β–Ϋ―¹–Α―Ü–Η–Η, –Η ―ç―²–Η –¥–Μ–Η―²–Β–Μ―¨–Ϋ―΄–Β –Α–¥–Α–Ω―²–Η–≤–Ϋ―΄–Β –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ―΄ –Φ–Ψ–≥―É―² –±―΄―²―¨ ―É―¹–Η–Μ–Β–Ϋ―΄ ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é ―³–Α―Ä–Φ–Α–Κ–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö –≥–Η―¹―²–Α–Φ–Η–Ϋ–Β―Ä–≥–Η―΅–Β―¹–Κ–Η―Ö –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤, ―²–Α–Κ–Η―Ö –Κ–Α–Κ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ. –†–Α–±–Ψ―²―΄ –Ϋ–Α –Ε–Η–≤–Ψ―²–Ϋ―΄―Ö –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Η, ―΅―²–Ψ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ –¥–Β–Ι―¹―²–≤―É–Β―² –Ϋ–Α –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ―É―é –Α–¥–Α–Ω―²–Α―Ü–Η―é –Ψ―²–Μ–Η―΅–Ϋ–Ψ –Ψ―² –Ω―Ä–Β–Ω–Α―Ä–Α―²–Ψ–≤ ―¹ ―¹–Β–¥–Α―²–Η–≤–Ϋ―΄–Φ–Η ―ç―³―³–Β–Κ―²–Α–Φ–Η [17] .
–Ξ–Ψ―²―è –Ϋ–Α ―¹–Β–≥–Ψ–¥–Ϋ―è―à–Ϋ–Η–Ι –¥–Β–Ϋ―¨ ―²―Ä–Β–±―É–Β―²―¹―è –±–Ψ–Μ―¨―à–Β –¥–Α–Ϋ–Ϋ―΄―Ö –Ψ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Β, –±―΄–Μ–Η ―¹–¥–Β–Μ–Α–Ϋ―΄ –≤–Α–Ε–Ϋ―΄–Β ―à–Α–≥–Η –≤ –Ω–Ψ–Ϋ–Η–Φ–Α–Ϋ–Η–Η –Β–≥–Ψ –Φ–Β―¹―²–Α –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α, ―Ä–Ψ–¥―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Ι –Η ―Ä–Α–Ζ―ä―è―¹–Ϋ–Β–Ϋ–Η–Η –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Α –Β–≥–Ψ –¥–Β–Ι―¹―²–≤–Η―è.
–ü–Ψ―¹–Μ–Β–¥–Ϋ―è―è, –Ζ–Α–Κ–Μ―é―΅–Η―²–Β–Μ―¨–Ϋ–Α―è ―¹–Β―¹―¹–Η―è
–Κ–Ψ–Ϋ―³–Β―Ä–Β–Ϋ―Ü–Η–Η –±―΄–Μ–Α –Ω–Ψ―¹–≤―è―â–Β–Ϋ–Α –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―é –Η –Κ–Α―΅–Β―¹―²–≤―É –Ε–Η–Ζ–Ϋ–Η. –û–Ϋ–Α –Ω―Ä–Ψ―Ö–Ψ–¥–Η–Μ–Α –Ω–Ψ–¥
–Ω―Ä–Β–¥―¹–Β–¥–Α―²–Β–Μ―¨―¹―²–≤–Ψ–Φ –ï–≤–≥–Β–Ϋ–Η–Ψ –€–Η―Ä–Α (–‰―²–Α–Μ–Η―è)
–ö–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η –Μ―é–¥–Β–Ι ―¹ ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η–Φ
–≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ –Η –≤–Β―Ä―²–Η–≥–Ψ
–Ξ―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Ψ–Β –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β –Η –≤–Β―Ä―²–Η–≥–Ψ –Φ–Ψ–≥―É―² –±―΄―²―¨ ―΅―Ä–Β–Ζ–≤―΄―΅–Α–Ι–Ϋ―΄–Φ –¥–Η―¹―²―Ä–Β―¹―¹–Ψ–Φ –Η –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –≤–Μ–Η―è―²―¨ –Ϋ–Α –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η –Μ―é–¥–Β–Ι, ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –¥–Α–Ϋ–Ϋ–Ψ–Ι –Ω–Α―²–Ψ–Μ–Ψ–≥–Η–Β–Ι. –Ξ–Ψ―²―è ―¹―Ä–Β–¥–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α –≤―΄―è–≤–Μ–Β–Ϋ –≤―΄―¹–Ψ–Κ–Η–Ι ―É―Ä–Ψ–≤–Β–Ϋ―¨ –¥–Η―¹―²―Ä–Β―¹―¹–Α –Η ―É–Φ―¹―²–≤–Β–Ϋ–Ϋ–Ψ–≥–Ψ ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α, –Ϋ–Α–Κ–Ψ–Ω–Μ–Β–Ϋ–Ψ –Φ–Α–Μ–Ψ –¥–Α–Ϋ–Ϋ―΄―Ö –Ψ –Κ–Ψ–≥–Ϋ–Η―²–Η–≤–Ϋ―΄―Ö –Η ―ç–Φ–Ψ―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ―΄―Ö –Ω―Ä–Ψ―Ü–Β―¹―¹–Α―Ö, –Κ–Ψ―²–Ψ―Ä―΄–Β –≤–Β–¥―É―² –Κ ―ç―²–Η–Φ –Η―¹―Ö–Ψ–¥–Α–Φ –Η –Κ–Ψ―²–Ψ―Ä―΄–Β –Ω–Ψ―²–Β–Ϋ―Ü–Η–Α–Μ―¨–Ϋ–Ψ –Φ–Ψ–≥―É―² –≤–Μ–Η―è―²―¨ –Ϋ–Α –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤. –Γ–Α―Ä–Α –ö–Η―Ä–±–Η (–Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―² –Γ–Α―É―³–Κ―ç–Φ–Ω―²–Ψ–Ϋ–Α, –£–Β–Μ–Η–Κ–Ψ–±―Ä–Η―²–Α–Ϋ–Η―è) –Ω―Ä–Β–¥―¹―²–Α–≤–Η–Μ–Α ―Ä–Α–±–Ψ―²―΄, –≤ –Κ–Ψ―²–Ψ―Ä―΄―Ö ―¹–¥–Β–Μ–Α–Ϋ–Α –Ω–Ψ–Ω―΄―²–Κ–Α –Ψ―²–≤–Β―²–Η―²―¨ –Ϋ–Α 2 –≤–Α–Ε–Ϋ―΄―Ö –≤–Ψ–Ω―Ä–Ψ―¹–Α: ―΅―²–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ―è–Β―² –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η –Η ―΅―²–Ψ –Φ–Ψ–Ε–Ϋ–Ψ ―¹–¥–Β–Μ–Α―²―¨ –¥–Μ―è –Β–Β ―É–Μ―É―΅―à–Β–Ϋ–Η―è.
–£ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Η–Ζ―É―΅–Α–Μ–Α―¹―¨ ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η―è –±―É–Κ–Μ–Β―²–Ψ–≤ –Ω–Ψ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–Ι ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η–Η (–£–†) –Η ―²–Β―Ö–Ϋ–Η–Κ–Β ―É–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η―è ―¹―²―Ä–Β―¹―¹–Ψ–Φ –¥–Μ―è –Μ–Β―΅–Β–Ϋ–Η―è –≤–Β―Ä―²–Η–≥–Ψ –Η –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è –Ω―Ä–Η –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α [18]. –£―¹–Β–≥–Ψ 360 ―΅–Μ–Β–Ϋ–Ψ–≤ –Ψ–±―â–Β―¹―²–≤–Α –€–Β–Ϋ―¨–Β―Ä–Α –Ω―Ä–Η–Ϋ―è–Μ–Η ―É―΅–Α―¹―²–Η–Β –≤ ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–Φ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–Φ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –¥–≤―É―Ö –±―É–Κ–Μ–Β―²–Ψ–≤ –Ω–Ψ ―¹–Α–Φ–Ψ–Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―é – «–£–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Α―è ―Ä–Β–Α–±–Η–Μ–Η―²–Α―Ü–Η―è» –Η «–Θ–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η–Β ―¹―²―Ä–Β―¹―¹–Ψ–Φ». –ë―É–Κ–Μ–Β―²―΄ –±―΄–Μ–Η –Ϋ–Α–Ω–Η―¹–Α–Ϋ―΄ ―¹ –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Ϋ–Η–Β–Φ ―²–Β–Ψ―Ä–Η–Ι –Ω–Ψ ―É–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η―é ―¹–Η–Φ–Ω―²–Ψ–Φ–Α–Φ–Η (–Η―Ö –Φ–Ψ–Ε–Ϋ–Ψ –Ϋ–Α–Ι―²–Η –Ϋ–Α ―¹–Α–Ι―²–Β info@menieres.org.uk). –ß–Β―Ä–Β–Ζ 6 –Φ–Β―¹―è―Ü–Β–≤ –Ψ―²―¹―Ä–Ψ―΅–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Η–Ψ–¥–Α –Ω–Α―Ü–Η–Β–Ϋ―²―΄, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η–Β –£–†, ―¹–Ψ–Ψ–±―â–Η–Μ–Η –Ψ–± ―É–Μ―É―΅―à–Β–Ϋ–Η–Η ―¹–Η–Φ–Ω―²–Ψ–Φ–Α―²–Η–Κ–Η, –Φ–Ϋ–Β―¹―²–Η―΅–Β―¹–Κ–Η―Ö –Ω―Ä–Ψ―Ü–Β―¹―¹–Ψ–≤, ―²―Ä–Β–≤–Ψ–≥–Η –Η –¥–Β–Ω―Ä–Β―¹―¹–Η–Η –Η –Ϋ–Β–≥–Α―²–Η–≤–Ϋ―΄―Ö ―É–±–Β–Ε–¥–Β–Ϋ–Η–Ι –Ψ ―¹–Η–Φ–Ω―²–Ψ–Φ–Α―Ö, –≤ ―²–Ψ –≤―Ä–Β–Φ―è –Κ–Α–Κ –Ω–Α―Ü–Η–Β–Ϋ―²―΄ –≤ –≥―Ä―É–Ω–Ω–Β –Ω–Ψ ―É–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η―é ―¹―²―Ä–Β―¹―¹–Ψ–Φ ―¹–Ψ–Ψ–±―â–Η–Μ–Η –Ψ–± ―É–Μ―É―΅―à–Β–Ϋ–Η–Η ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤, –Φ–Ϋ–Β―¹―²–Η―΅–Β―¹–Κ–Η―Ö –Ω―Ä–Ψ―Ü–Β―¹―¹–Ψ–≤ –Η –Ϋ–Β–≥–Α―²–Η–≤–Ϋ―΄―Ö ―É–±–Β–Ε–¥–Β–Ϋ–Η–Ι –Ψ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Η.
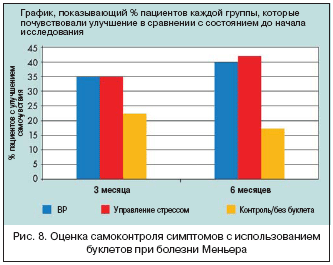
–ö–Α–Κ –Ω–Ψ–Κ–Α–Ζ–Α–Ϋ–Ψ –Ϋ–Α ―Ä–Η―¹―É–Ϋ–Κ–Β 8, 45 ―΅–Β–Μ–Ψ–≤–Β–Κ (37,5%) –≥―Ä―É–Ω–Ω―΄ –£–† –Η 47 (39,2%) –≥―Ä―É–Ω–Ω―΄ ―É–Ω―Ä–Α–≤–Μ–Β–Ϋ–Η―è ―¹―²―Ä–Β―¹―¹–Ψ–Φ ―¹–Ψ–Ψ–±―â–Η–Μ–Η –Ψ–± ―É–Μ―É―΅―à–Β–Ϋ–Η–Η –≤ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ 19 (15,8%) –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨–Ϋ–Ψ–Ι –≥―Ä―É–Ω–Ω―΄. –î–Α–Ϋ–Ϋ―΄–Β –±―É–Κ–Μ–Β―²―΄ –Ω–Ψ ―¹–Α–Φ–Ψ–Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―é –Ω―Ä–Β–¥–Μ–Α–≥–Α―é―² –Ϋ–Β–¥–Ψ―Ä–Ψ–≥–Ψ–Ι –Η –Μ–Β–≥–Κ–Ψ –≤―΄–Ω–Ψ–Μ–Ϋ―è–Β–Φ―΄–Ι –Φ–Β―²–Ψ–¥, –Ω–Ψ–Φ–Ψ–≥–Α―é―â–Η–Ι –Μ―é–¥―è–Φ ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α –±–Ψ―Ä–Ψ―²―¨―¹―è ―¹ ―¹–Η–Φ–Ω―²–Ψ–Φ–Α–Φ–Η –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è.
–î–≤–Α –¥–Α–Μ―¨–Ϋ–Β–Ι―à–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –Ω―Ä–Ψ–≤–Ψ–¥–Η–Μ–Η―¹―¨ ―¹ ―Ü–Β–Μ―¨―é –≤―΄―è–≤–Μ–Β–Ϋ–Η―è –≤–Μ–Η―è–Ϋ–Η―è ―²―Ä–Β–≤–Ψ–≥–Η –Η –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Ψ–≤ –¥–Η―¹―²―Ä–Β―¹―¹–Α –Ϋ–Α –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η. –‰―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω–Ψ ―²―Ä–Β–≤–Ψ–≥–Β –±―΄–Μ–Ψ –Ω―Ä–Ψ–≤–Β–¥–Β–Ϋ–Ψ –≤ ―Ä–Α–Φ–Κ–Α―Ö ―Ä–Α–Ϋ–¥–Ψ–Φ–Η–Ζ–Η―Ä–Ψ–≤–Α–Ϋ–Ϋ–Ψ–≥–Ψ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä―É–Β–Φ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –¥–≤―É―Ö –±―É–Κ–Μ–Β―²–Ψ–≤ –Ω–Ψ ―¹–Α–Φ–Ψ–Μ–Β―΅–Β–Ϋ–Η―é, –Ψ–Ω–Η―¹–Α–Ϋ–Ϋ–Ψ–≥–Ψ –≤―΄―à–Β. 358 ―É―΅–Α―¹―²–Ϋ–Η–Κ–Ψ–≤ –Ζ–Α–Ω–Ψ–Μ–Ϋ–Η–Μ–Η –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ, –≤–Κ–Μ―é―΅–Β–Ϋ–Ϋ―΄–Ι –≤ –Ω―Ä–Β–±―É–Κ–Μ–Β―² –Η –Ω–Ψ―¹―²–±―É–Κ–Μ–Β―² (3 –Φ–Β―¹―è―Ü–Α) –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è. –™–Μ–Α–≤–Ϋ―΄–Φ–Η –≤―΄–≤–Ψ–¥–Α–Φ–Η –±―΄–Μ–Η –Ω–Ψ–Μ–Ψ–Ε–Β–Ϋ–Η―è, –Ϋ–Α –Κ–Ψ―²–Ψ―Ä―΄―Ö –Ϋ―É–Ε–Ϋ–Ψ ―¹–¥–Β–Μ–Α―²―¨ –Α–Κ―Ü–Β–Ϋ―² –¥–Μ―è ―²–Ψ–≥–Ψ, ―΅―²–Ψ–±―΄ –Ω–Ψ–Φ–Ψ―΅―¨ –Ω–Α―Ü–Η–Β–Ϋ―²–Α–Φ:
– –Ω–Ψ–Ϋ―è―²―¨ –Η―Ö –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η–Β –Η –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ ―Ä–Α–±–Ψ―²―΄ ―¹–Η―¹―²–Β–Φ―΄ ―Ä–Α–≤–Ϋ–Ψ–≤–Β―¹–Η―è;
– –Ω–Ψ–Ϋ―è―²―¨, ―΅―²–Ψ –±–Ψ–Μ–Β–Β –Μ–Β–≥–Κ–Η–Β ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è –Ϋ–Β –≤―¹–Β–≥–¥–Α –Ψ–Ζ–Ϋ–Α―΅–Α―é―², ―΅―²–Ψ ―¹–Κ–Ψ―Ä–Ψ –±―É–¥–Β―² –Α―²–Α–Κ–Α (–Ψ–Ϋ–Η –Φ–Ψ–≥―É―² –Ω―Ä–Ψ―¹―²–Ψ –≤–Ψ–Ζ–Ϋ–Η–Κ–Α―²―¨ –Ω–Ψ―¹–Μ–Β –Α―²–Α–Κ–Η –Η –Φ–Ψ–≥―É―² –±―΄―²―¨ –Ψ–±–Μ–Β–≥―΅–Β–Ϋ―΄ ―¹ –Ω–Ψ–Φ–Ψ―â―¨―é –£–†);
– ―É–Μ―É―΅―à–Η―²―¨ –Η―Ö ―¹–Α–Φ–Ψ–Ψ―â―É―â–Β–Ϋ–Η–Β –Η –±–Ψ―Ä–Ψ―²―¨―¹―è ―¹ –Ϋ–Β–Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ–Ψ―¹―²―¨―é, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ–Ψ–Ι ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é;
– –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ–Η―Ä–Ψ–≤–Α―²―¨ –Η―Ö ―³–Η–Ζ–Η―΅–Β―¹–Κ–Η–Β ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ ―²―Ä–Β–≤–Ψ–≥–Η.
–£ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Α –¥–Η―¹―²―Ä–Β―¹―¹–Α, 800 ―΅–Μ–Β–Ϋ–Ψ–≤ –Ψ–±―â–Β―¹―²–≤–Α –€–Β–Ϋ―¨–Β―Ä–Α –Η 484 ―΅–Μ–Β–Ϋ–Α ―¹–Β–Φ–Β–Ι –Η –¥―Ä―É–Ζ–Β–Ι (–Κ–Α–Κ –Κ–Ψ–Ϋ―²―Ä–Ψ–Μ―¨–Ϋ–Α―è –≥―Ä―É–Ω–Ω–Α) –Ζ–Α–Ω–Ψ–Μ–Ϋ–Η–Μ–Η –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ–Η –¥–Μ―è –≤―΄―è–≤–Μ–Β–Ϋ–Η―è –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η―è –Κ –±–Ψ–Μ–Β–Ζ–Ϋ–Η –€–Β–Ϋ―¨–Β―Ä–Α –Φ–Β―Ö–Α–Ϋ–Η–Ζ–Φ–Ψ–≤, –Ψ―²–Ϋ–Ψ―¹―è―â–Η―Ö―¹―è –Κ –¥―Ä―É–≥–Η–Φ ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η–Φ –Ζ–Α–±–Ψ–Μ–Β–≤–Α–Ϋ–Η―è–Φ, –Η –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η―è, ―΅―²–Ψ –≤–Μ–Η―è–Β―² –Ϋ–Α –¥–Η―¹―²―Ä–Β―¹―¹ (―²―Ä–Β–≤–Ψ–≥–Α, –¥–Β–Ω―Ä–Β―¹―¹–Η―è –Η–Μ–Η ―É–Φ―¹―²–≤–Β–Ϋ–Ϋ–Ψ–Β ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Ψ). –≠―²–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –Ω–Ψ–Κ–Α–Ζ–Α–Μ–Ψ, ―΅―²–Ψ –Ψ―²―¹―É―²―¹―²–≤–Η–Β ―²–Ψ–Μ–Β―Ä–Α–Ϋ―²–Ϋ–Ψ―¹―²–Η –Κ –Ϋ–Β–Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ–Ψ―¹―²–Η, –Ϋ–Β–≥–Α―²–Η–≤–Ϋ―΄–Β ―É–±–Β–Ε–¥–Β–Ϋ–Η―è –Ψ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Η –Η ―³–Η–Ζ–Η―΅–Β―¹–Κ–Ψ–Ι –Α–Κ―²–Η–≤–Ϋ–Ψ―¹―²–Η, –≤–Ψ―¹–Ω―Ä–Η―è―²–Η–Η –±–Ψ–Μ–Β–Ζ–Ϋ–Η, ―²―Ä–Β–≤–Ψ–≥–Α –Ψ –Ζ–¥–Ψ―Ä–Ψ–≤―¨–Β –Η ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ –Ω–Ψ―¹―²―²―Ä–Α–≤–Φ–Α―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ ―¹―²―Ä–Β―¹―¹–Ψ―Ä–Ϋ–Ψ–≥–Ψ ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α –Φ–Ψ–≥―É―² –Η–≥―Ä–Α―²―¨ ―Ä–Ψ–Μ―¨ –≤ ―Ä–Α–Ζ–≤–Η―²–Η–Η –¥–Η―¹―²―Ä–Β―¹―¹–Α –Η ―É–Φ―¹―²–≤–Β–Ϋ–Ϋ–Ψ–≥–Ψ ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤–Α ―É –Μ―é–¥–Β–Ι ―¹ –±–Ψ–Μ–Β–Ζ–Ϋ―¨―é –€–Β–Ϋ―¨–Β―Ä–Α.
–Δ–Α–Κ–Η–Φ –Ψ–±―Ä–Α–Ζ–Ψ–Φ, ―Ä–Β–Ζ―É–Μ―¨―²–Α―²―΄ ―ç―²–Η―Ö –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Ι –≤–Ϋ–Β―¹–Μ–Η –Ω–Ψ–Μ–Ψ–Ε–Η―²–Β–Μ―¨–Ϋ―΄–Ι –≤–Κ–Μ–Α–¥ –≤ ―É–Μ―É―΅―à–Β–Ϋ–Η–Β –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η –Μ―é–¥–Β–Ι ―¹ ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η–Φ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ –Η –≤–Β―Ä―²–Η–≥–Ψ, ―¹–Ω–Ψ―¹–Ψ–±―¹―²–≤―É―è ―Ä–Α–Ζ–≤–Η―²–Η―é –±–Ψ–Μ–Β–Β ―³–Η–Ζ–Η–Ψ–Μ–Ψ–≥–Η―΅–Β―¹–Κ–Η―Ö –≤–Φ–Β―à–Α―²–Β–Μ―¨―¹―²–≤ –¥–Μ―è –Ω–Ψ–Φ–Ψ―â–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Α–Φ ―¹ ―Ö―Ä–Ψ–Ϋ–Η―΅–Β―¹–Κ–Η–Φ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η–Β–Φ –Η –≤–Β―Ä―²–Η–≥–Ψ, –Η―¹–Ω―΄―²―΄–≤–Α―é―â–Η―Ö –¥–Η―¹―²―Ä–Β―¹―¹.
–‰―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β OSVaLD: –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η–Β –≤–Μ–Η―è–Ϋ–Η―è –ë–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―². –Ϋ–Α –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≤–Β―Ä―²–Η–≥–Ψ
–†–Β–Ζ―É–Μ―¨―²–Α―²―΄ –≤–Α–Ε–Ϋ–Ψ–≥–Ψ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –±―΄–Μ–Η –Ω―Ä–Β–¥―¹―²–Α–≤–Μ–Β–Ϋ―΄ –≤ ―¹–Α–Φ―΄–Ι –Ω–Β―Ä–≤―΄–Ι ―Ä–Α–Ζ –™–Β―Ä–Φ–Η–Ϋ–Η–Ψ –ü–Β―Ä–Β–Ζ –™–Α―Ä―Ä–Η–Κ–≤–Β―¹ (–Θ–Ϋ–Η–≤–Β―Ä―¹–Η―²–Β―² –£–Α–Μ–Β–Ϋ―¹–Η–Η, –‰―¹–Ω–Α–Ϋ–Η―è) –Ϋ–Α –Φ–Β–Ε–¥―É–Ϋ–Α―Ä–Ψ–¥–Ϋ–Ψ–Ι –Κ–Ψ–Ϋ―³–Β―Ä–Β–Ϋ―Ü–Η–Η –Ω–Ψ –Ω―Ä–Ψ–±–Μ–Β–Φ–Α–Φ –Ϋ–Α―Ä―É―à–Β–Ϋ–Η―è ―Ä–Α–≤–Ϋ–Ψ–≤–Β―¹–Η―è. OSVaLD (–ù–Α–±–Μ―é–¥–Α―²–Β–Μ―¨–Ϋ–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β ―¹―Ä–Β–¥–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –Ψ―² –Ω–Ψ–≤―²–Ψ―Ä–Ϋ–Ψ–≥–Ψ –Ω–Β―Ä–Η―³–Β―Ä–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –≤–Β―¹―²–Η–±―É–Μ―è―Ä–Ϋ–Ψ–≥–Ψ –≤–Β―Ä―²–Η–≥–Ψ, –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η ―ç―³―³–Β–Κ―²–Α –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―². –Ϋ–Α –Κ–Α―΅–Β―¹―²–≤–Ψ –Ε–Η–Ζ–Ϋ–Η –Η ―¹–Η–Φ–Ω―²–Ψ–Φ―΄ –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è), 3––Φ–Β―¹―è―΅–Ϋ–Ψ–Β, –Ψ―²–Κ―Ä―΄―²–Ψ–Β, –Φ–Ϋ–Ψ–≥–Ψ–Ϋ–Α―Ü–Η–Ψ–Ϋ–Α–Μ―¨–Ϋ–Ψ–Β –Ω–Ψ―¹―²–Φ–Α―Ä–Κ–Β―²–Η–Ϋ–≥–Ψ–≤–Ψ–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Β –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―². (2*24 –Φ–≥ –Η–Μ–Η 3*16 –Φ–≥) –≤ –Μ–Β―΅–Β–Ϋ–Η–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤ ―¹ –≤–Β―Ä―²–Η–≥–Ψ –Ω―Ä–Ψ–¥–Ψ–Μ–Ε–Η―²–Β–Μ―¨–Ϋ–Ψ―¹―²―¨―é –Φ–Β–Ϋ–Β–Β 5 –Μ–Β―². –Π–Β–Μ―¨―é –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è –±―΄–Μ–Ψ –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Η–Β –¥–Η―¹–Κ–Ψ–Φ―³–Ψ―Ä―²–Α –Ψ―² –±–Ψ–Μ–Β–Ζ–Ϋ–Η, ―¹–≤―è–Ζ–Α–Ϋ–Ϋ–Ψ–≥–Ψ ―¹ –≤–Β―Ä―²–Η–≥–Ψ, –Ψ–Ω―Ä–Β–¥–Β–Μ–Β–Ϋ–Ϋ–Ψ–≥–Ψ –Ω–Ψ ―à–Κ–Α–Μ–Β Dizziness Handicap Inventory (DHI – ―à–Κ–Α–Μ–Α –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η –≥–Ψ–Μ–Ψ–≤–Ψ–Κ―Ä―É–Ε–Β–Ϋ–Η―è –Η –Φ–Ϋ–Β―¹―²–Η―΅–Β―¹–Κ–Η―Ö ―³―É–Ϋ–Κ―Ü–Η–Ι), Short Form–36 (SF–36 – –Ψ–Ω―Ä–Ψ―¹–Ϋ–Η–Κ –Ω–Ψ –Κ–Α―΅–Β―¹―²–≤―É –Ε–Η–Ζ–Ϋ–Η), Hospital Anxiety and Depression Scale (HADS – –≥–Ψ―¹–Ω–Η―²–Α–Μ―¨–Ϋ–Α―è ―à–Κ–Α–Μ–Α ―²―Ä–Β–≤–Ψ–≥–Η –Η –¥–Β–Ω―Ä–Β―¹―¹–Η–Η). –‰–Ζ–Φ–Β–Ϋ–Β–Ϋ–Η―è –≤ DHI, SF–36, HADS –Φ–Β–Ε–¥―É –Η―¹―Ö–Ψ–¥–Ϋ―΄–Φ–Η –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è–Φ–Η –Η ―¹–Ω―É―¹―²―è 3 –Φ–Β―¹―è―Ü–Α –Η―¹–Ω–Ψ–Μ―¨–Ζ–Ψ–≤–Α–Μ–Η―¹―¨ –¥–Μ―è –Ψ―Ü–Β–Ϋ–Κ–Η ―²–Β―Ä–Α–Ω–Β–≤―²–Η―΅–Β―¹–Κ–Ψ–≥–Ψ ―ç―³―³–Β–Κ―²–Α –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α. –£ –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η–Η –Ω―Ä–Η–Ϋ―è–Μ–Ψ ―É―΅–Α―¹―²–Η–Β –±–Ψ–Μ–Β–Β 2 ―²―΄―¹. ―΅–Β–Μ–Ψ–≤–Β–Κ (n=2028) –Η–Ζ 13 ―¹―²―Ä–Α–Ϋ 4 –Κ–Ψ–Ϋ―²–Η–Ϋ–Β–Ϋ―²–Ψ–≤ (–Γ–Β–≤–Β―Ä–Ϋ–Α―è –Η –°–Ε–Ϋ–Α―è –ê–Φ–Β―Ä–Η–Κ–Α, –ê–Ζ–Η―è –Η –ï–≤―Ä–Ψ–Ω–Α).
–®–Κ–Α–Μ–Α DHI –Ϋ–Β–Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ –≤–Α―Ä―¨–Η―Ä–Ψ–≤–Α–Μ–Α –≤ –Ζ–Α–≤–Η―¹–Η–Φ–Ψ―¹―²–Η –Ψ―² –¥–Η–Α–≥–Ϋ–Ψ–Ζ–Α, –Η –±–Α–Μ–Μ―΄ –Ω―Ä–Ψ–≥―Ä–Β―¹―¹–Η–≤–Ϋ–Ψ ―É–Μ―É―΅―à–Α–Μ–Η―¹―¨ –Ω–Ψ –≤―¹–Β–Φ –Κ–Α―²–Β–≥–Ψ―Ä–Η―è–Φ –≤ ―²–Β―΅–Β–Ϋ–Η–Β –Η―¹―¹–Μ–Β–¥–Ψ–≤–Α–Ϋ–Η―è. –Θ–Μ―É―΅―à–Β–Ϋ–Η–Β ―²–Α–Κ–Ε–Β –±―΄–Μ–Ψ –Ψ―²–Φ–Β―΅–Β–Ϋ–Ψ –Η –Ω–Ψ ―à–Κ–Α–Μ–Β SF–36. –½–Ϋ–Α―΅–Β–Ϋ–Η–Β –¥–Μ―è –Ϋ–Ψ―Ä–Φ–Α–Μ―¨–Ϋ–Ψ–Ι –Ω–Ψ–Ω―É–Μ―è―Ü–Η–Η ―¹–Ψ―¹―²–Α–≤–Μ―è–Β―² 50 (―΅–Β–Φ –Ϋ–Η–Ε–Β –±–Α–Μ–Μ, ―²–Β–Φ ―Ö―É–Ε–Β ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η–Β –Ω–Α―Ü–Η–Β–Ϋ―²–Α). –û―΅–Β–≤–Η–¥–Ϋ–Ψ, ―΅―²–Ψ –Ω―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―². ―¹–≤―è–Ζ–Α–Ϋ–Ψ ―¹–Ψ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ―΄–Φ ―É–Μ―É―΅―à–Β–Ϋ–Η–Β–Φ –Ω–Ψ ―³–Η–Ζ–Η―΅–Β―¹–Κ–Η–Φ –Η –Ω―¹–Η―Ö–Η―΅–Β―¹–Κ–Η–Φ –Ω–Ψ–Κ–Α–Ζ–Α―²–Β–Μ―è–Φ –Ζ–¥–Ψ―Ä–Ψ–≤―¨―è, ―¹–Ω―É―¹―²―è 1 –Φ–Β―¹―è―Ü –Η 3 –Φ–Β―¹―è―Ü–Α –Ω–Ψ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η―é ―¹ –Η―¹―Ö–Ψ–¥–Ϋ―΄–Φ–Η –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è–Φ–Η. –ê–Ϋ–Α–Μ–Η–Ζ HADS –≤―΄―è–≤–Η–Μ –Ζ–Ϋ–Α―΅–Η―²–Β–Μ―¨–Ϋ–Ψ–Β ―É–Μ―É―΅―à–Β–Ϋ–Η–Β ―¹–Ψ―¹―²–Ψ―è–Ϋ–Η―è ―É –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, –Ω–Ψ–Μ―É―΅–Α–≤―à–Η―Ö –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ 48 –Φ–≥ –≤ ―¹―É―²–Κ–Η –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η –Κ–Α–Κ ―à–Κ–Α–Μ―΄ ―²―Ä–Β–≤–Ψ–≥–Η, ―²–Α–Κ –Η –¥–Β–Ω―Ä–Β―¹―¹–Η–Η, ―¹–Ω―É―¹―²―è 1 –Η 3 –Φ–Β―¹―è―Ü–Α –≤ ―¹―Ä–Α–≤–Ϋ–Β–Ϋ–Η–Η ―¹ –Η―¹―Ö–Ψ–¥–Ϋ―΄–Φ–Η –Ζ–Ϋ–Α―΅–Β–Ϋ–Η―è–Φ–Η.
OSVaLD –Ω–Ψ–¥―²–≤–Β―Ä–Ε–¥–Α–Β―² –Κ–Μ–Η–Ϋ–Η―΅–Β―¹–Κ―É―é ―ç―³―³–Β–Κ―²–Η–≤–Ϋ–Ψ―¹―²―¨ –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―². –≤ –Ψ―²–Ϋ–Ψ―à–Β–Ϋ–Η–Η ―É–Μ―É―΅―à–Β–Ϋ–Η―è –Κ–Α―΅–Β―¹―²–≤–Α –Ε–Η–Ζ–Ϋ–Η –Ω–Α―Ü–Η–Β–Ϋ―²–Ψ–≤, ―¹―²―Ä–Α–¥–Α―é―â–Η―Ö –Ψ―² –Φ–Α–Ϋ–Η―³–Β―¹―²–Α―Ü–Η–Η –≤–Β―Ä―²–Η–≥–Ψ. –ü―Ä–Η–Φ–Β–Ϋ–Β–Ϋ–Η–Β –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―². –Α―¹―¹–Ψ―Ü–Η–Η―Ä–Ψ–≤–Α–Μ–Ψ―¹―¨ ―¹ ―Ä–Β–¥―É–Κ―Ü–Η–Β–Ι ―É–Φ―¹―²–≤–Β–Ϋ–Ϋ―΄―Ö ―Ä–Α―¹―¹―²―Ä–Ψ–Ι―¹―²–≤ (DHI), ―É–Μ―É―΅―à–Β–Ϋ–Η–Β–Φ ―³–Η–Ζ–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Η –Ω―¹–Η―Ö–Η―΅–Β―¹–Κ–Ψ–≥–Ψ –Ζ–¥–Ψ―Ä–Ψ–≤―¨―è (SF–36) –Η ―É–Φ–Β–Ϋ―¨―à–Β–Ϋ–Η–Β–Φ ―¹–Η–Φ–Ω―²–Ψ–Φ–Ψ–≤ ―²―Ä–Β–≤–Ψ–≥–Η –Η –¥–Β–Ω―Ä–Β―¹―¹–Η–Η (HADS). OSVaLD ―²–Α–Κ–Ε–Β –Ω–Ψ–¥―²–≤–Β―Ä–¥–Η–Μ –Ω―Ä–Β–≤–Ψ―¹―Ö–Ψ–¥–Ϋ―΄–Ι –Ω―Ä–Ψ―³–Η–Μ―¨ –±–Β–Ζ–Ψ–Ω–Α―¹–Ϋ–Ψ―¹―²–Η –±–Β―²–Α–≥–Η―¹―²–Η–Ϋ–Α 48 –Φ–≥/―¹―É―².
–†–Β―³–Β―Ä–Α―² –Ω–Ψ–¥–≥–Ψ―²–Ψ–≤–Μ–Β–Ϋ –ï.–ê. –ö–Μ–Η–Φ–Ψ–≤–Ψ–Ι –Ω–Ψ –Φ–Α―²–Β―Ä–Η–Α–Μ–Α–Φ ―¹―²–Α―²―¨–Η «International Conference on Balance Disturbances», International Medical News, Nr.01/February 2008