–£—Б–њ–µ—И–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Є –≤–љ–µ–і—А–µ–љ–Є–µ –≤ –Љ–µ–і–Є—Ж–Є–љ—Б–Ї—Г—О –љ–∞—Г–Ї—Г –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –і–µ—Б—П—В–Є–ї–µ—В–Є—П –љ–Њ–≤–µ–є—И–Є—Е —В–µ—Е–љ–Њ–ї–Њ–≥–Є–є –Ј–∞–ї–Њ–ґ–Є–ї–Њ –Њ—Б–љ–Њ–≤—Г —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –њ—А–Є–љ—Ж–Є–њ–Є–∞–ї—М–љ–Њ –љ–Њ–≤—Л—Е –Ї–Њ–љ—Ж–µ–њ—Ж–Є–є –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П (–Э–Ь–Ъ) –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, –њ–Њ–і—Е–Њ–і–Њ–≤ –Ї –Є—Е –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—О –Є –ї–µ—З–µ–љ–Є—О. –Ю–њ—А–µ–і–µ–ї–µ–љ–Њ, —З—В–Њ —Б—В—А–∞—В–µ–≥–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П–Љ–Є –≤ —В–µ—А–∞–њ–Є–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —П–≤–ї—П–µ—В—Б—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –≥–µ–Љ–Њ–њ–µ—А—Д—Г–Ј–Є–Є –Є –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—Ж–Є—П.
–Э–∞—Б—В–Њ—П—Й–∞—П —А–∞–±–Њ—В–∞ –љ–∞–њ—А–∞–≤–ї–µ–љ–∞ –љ–∞ —А–∞—Б–Ї—А—Л—В–Є–µ –љ–Њ–≤—Л—Е —Д—Г–љ–і–∞–Љ–µ–љ—В–∞–ї—М–љ—Л—Е —Б—В–Њ—А–Њ–љ –і–µ–є—Б—В–≤–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ –∞—Б–њ–µ–Ї—В–∞—Е –µ–≥–Њ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ–Њ–≥–Њ, –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –Є –≥–µ–Љ–Њ–Ї–Њ—А—А–µ–Ї—В–Њ—А–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Э–Ь–Ъ.
–Я–Њ–і –љ–∞–±–ї—О–і–µ–љ–Є–µ–Љ –љ–∞—Е–Њ–і–Є–ї–Є—Б—М 124 –њ–∞—Ж–Є–µ–љ—В–∞ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –≤–Є–і–∞–Љ–Є –Э–Ь–Ъ (—Б–Љ. —В–∞–±–ї.).

–Я—А–Є –Њ—Ж–µ–љ–Ї–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г—З–Є—В—Л–≤–∞–ї–Є –і–∞–љ–љ—Л–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –і–Њ –Є –љ–∞ —Д–Њ–љ–µ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Я–Њ–Љ–Є–Љ–Њ —В—А–∞–і–Є—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —Б —Ж–µ–ї—М—О –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є –і–Є–∞–≥–љ–Њ–Ј–∞ –≤—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –±—Л–ї–Є –њ—А–Њ–Є–Ј–≤–µ–і–µ–љ—Л –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П (–Ъ–Ґ), –∞ –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Є –Љ–∞–≥–љ–Є—В–љ–Њ–—А–µ–Ј–Њ–љ–∞–љ—Б–Ї–∞—П —В–Њ–Љ–Њ–≥—А–∞—Д–Є—П (–Ь–†–Ґ) –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–∞—П –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є—П (–£–Ч–Ф–У) –Є/–Є–ї–Є –і—Г–њ–ї–µ–Ї—Б–љ–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–Њ–ї–Њ–≤—Л (–Ь–Р–У), –≠–Ъ–У, –≠—Е–Њ–Ъ–У, –≠–≠–У, –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є–µ. –£ —А—П–і–∞ –±–Њ–ї—М–љ—Л—Е –Њ—Б—Г—Й–µ—Б—В–≤–ї–µ–љ–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –Љ–µ—В–Њ–і–Њ–Љ –Њ–і–љ–Њ—Д–Њ—В–Њ–љ–љ–Њ–є —Н–Љ–Є—Б—Б–Є–Њ–љ–љ–Њ–є –Ї–Њ–Љ–њ—М—О—В–µ—А–љ–Њ–є —В–Њ–Љ–Њ–≥—А–∞—Д–Є–Є (–Ю–§–≠–Ъ–Ґ).
–Я—А–Њ–Є–Ј–≤–Њ–і–Є–ї–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞:
- –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Љ–µ—В–Њ–і–Њ–Љ G. Born [7,9] –њ—А–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –Р–Ф–§ –≤ –Ї–Њ–љ–µ—З–љ–Њ–є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є 1,2x10–6 –Љ–Ь (–Р–Ф–§––Р–Ґ);
- –≤–∞–Ј–Њ– –Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ – –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ (–Я–УI2) –≤ –±–µ–і–љ–Њ–є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞–Љ–Є –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є –Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ (–Ґ—Е–Р2) –≤ –±–Њ–≥–∞—В–Њ–є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞–Љ–Є –њ–ї–∞–Ј–Љ–µ –Ї—А–Њ–≤–Є [3].
–†–∞—Б—Б—З–Є—В—Л–≤–∞–ї—Б—П —В–∞–Ї–ґ–µ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П 6––Ї–µ—В–Њ––Я–УF1a/–Ґ—Е–Т2, –Њ—В—А–∞–ґ–∞—О—Й–Є–є –≤–µ–ї–Є—З–Є–љ—Г –Є —Е–∞—А–∞–Ї—В–µ—А –Ї–Њ–љ–µ—З–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Є–Ј—Г—З–∞–µ–Љ—Л—Е —А–∞–Ј–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –±–Є–Њ—А–µ–≥—Г–ї—П—В–Њ—А–Њ–≤ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞.
–Р—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ—Л–є, –∞ –Є–Љ–µ–љ–љ–Њ –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–є, –њ–Њ—В–µ–љ—Ж–Є–∞–ї —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є–Ј—Г—З–∞–ї–Є —Б –њ–Њ–Љ–Њ—Й—М—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є «–Љ–∞–љ–ґ–µ—В–Њ—З–љ–Њ–є» –њ—А–Њ–±—Л (–Ь–Я), –Њ—Б–љ–Њ–≤–∞–љ–љ–Њ–є –љ–∞ —Б–Њ–Ј–і–∞–љ–Є–Є –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є (3–5 –Љ–Є–љ) –ї–Њ–Ї–∞–ї—М–љ–Њ–є –Є—И–µ–Љ–Є–Є —Б–Њ—Б—Г–і–Њ–≤ —А—Г–Ї–Є, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б—В–Є–Љ—Г–ї—П—Ж–Є–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –Є –≤—Л–і–µ–ї–µ–љ–Є—П —Н–љ–і–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –Є –љ–µ–Ї–Њ—В–Њ—А—Л—Е –і—А—Г–≥–Є—Е –≤–µ—Й–µ—Б—В–≤ –Є–Ј —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П [1]. –Т—Л—И–µ—Г–Ї–∞–Ј–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є –≤ –њ—А–Њ–±–∞—Е –Ї—А–Њ–≤–Є, –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–Њ –Є –њ–Њ—Б–ї–µ –Ь–Я.
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є –Љ–µ—В–Њ–і–Њ–Љ –Ю–§–≠–Ъ–Ґ –њ–Њ—Б–ї–µ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П —А–∞–і–Є–Њ—Д–∞—А–Љ–њ—А–µ–њ–∞—А–∞—В–∞ —Ж–µ—А–µ—В–µ–Ї 740 –Ь–С–Ї –Ґ—Б99m. –¶–µ—А–µ—В–µ–Ї —П–≤–ї—П–µ—В—Б—П –ї–Є–њ–Є–і–Њ—А–∞—Б—В–≤–Њ—А–Є–Љ—Л–Љ –Љ–∞–Ї—А–Њ—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–Љ –∞–Љ–Є–љ–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є —Б—А–∞–Ј—Г –ґ–µ –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є –њ–Њ—Б—В—Г–њ–∞–µ—В –≤ –Љ–Њ–Ј–≥, —А–∞—Б–њ—А–µ–і–µ–ї—П—П—Б—М —В–∞–Љ –њ—А–Њ–њ–Њ—А—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—О –Є –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —З–∞—Б–Њ–≤ —Б–Њ—Е—А–∞–љ—П—П –њ–Њ—Б—В–Њ—П–љ–љ—Г—О –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–Є –≤–Є–Ј—Г–∞–ї—М–љ–Њ –Є –њ–Њ–ї—Г–Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ. –Т–Є–Ј—Г–∞–ї—М–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ –≤–Ї–ї—О—З–∞–ї–∞ –њ—А–Њ—Б–Љ–Њ—В—А –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е —В–Њ–Љ–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–Є—Е —Б—А–µ–Ј–Њ–≤ –≤ –∞–Ї—Б–Є–∞–ї—М–љ–Њ–є –њ—А–Њ–µ–Ї—Ж–Є–Є. –Я–Њ–ї—Г–Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ—Г—О –Њ—Ж–µ–љ–Ї—Г –њ—А–Њ–≤–Њ–і–Є–ї–Є –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є –њ—А–Њ–≥—А–∞–Љ–Љ–µ «CORTIQAL». –≠—В–∞ –њ—А–Њ–≥—А–∞–Љ–Љ–∞ –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –њ–Њ–≤–µ—А—Е–љ–Њ—Б—В—М –Љ–Њ–Ј–≥–∞ –≤ —Н–Ї–≤–∞—В–Њ—А–Є–∞–ї—М–љ–Њ–є –њ–ї–Њ—Б–Ї–Њ—Б—В–Є –≤ –≤–Є–і–µ –Ї–∞—А—В—Л, –Є–Ј–Њ–±—А–∞–ґ–∞—О—Й–µ–є –Њ–±–∞ –њ–Њ–ї—Г—И–∞—А–Є—П –Љ–Њ–Ј–≥–∞ –Є –≤–Ї–ї—О—З–∞—О—Й–µ–є 9 —А–µ–≥–Є–Њ–љ–Њ–≤: –њ–µ—А–µ–і–љ–µ—Д—А–Њ–љ—В–∞–ї—М–љ—Л–є, —Б—А–µ–і–љ–µ—Д—А–Њ–љ—В–∞–ї—М–љ—Л–є, –Ј–∞–і–љ–µ—Д—А–Њ–љ—В–∞–ї—М–љ—Л–є, –њ–∞—А–Є–µ—В–∞–ї—М–љ—Л–є, —В–µ–Љ–њ–Њ—А–Њ–њ–∞—А–Є–µ—В–∞–ї—М–љ—Л–є, —В–µ–Љ–њ–Њ—А–Њ–Њ–Ї—Ж–Є–њ–Є—В–∞–ї—М–љ—Л–є, –њ–µ—А–Є—Б–Є–ї—М–≤–Є–∞—А–љ—Л–є, —В–µ–Љ–њ–Њ—А–∞–ї—М–љ—Л–є –Є –Њ–±–ї–∞—Б—В—М –Љ–Њ–Ј–ґ–µ—З–Ї–∞. –Ю—Ж–µ–љ–Є–≤–∞–ї–Є –≤–µ–ї–Є—З–Є–љ—Г –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –≤ –Ї–∞–ґ–і–Њ–Љ –Є–Ј —А–µ–≥–Є–Њ–љ–Њ–≤ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —А–µ—Д–µ—А–µ–љ—В–љ–Њ–є –Ј–Њ–љ–µ, –≤ –Ї–∞—З–µ—Б—В–≤–µ –Ї–Њ—В–Њ—А–Њ–є –≤—Л–±—А–∞–љ –Љ–Њ–Ј–ґ–µ—З–Њ–Ї.
–Ю—Ж–µ–љ–Ї–∞ –і–Є–љ–∞–Љ–Є–Ї–Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є—Е –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ–Њ–Ї–∞–Ј–∞–ї–∞, —З—В–Њ –≤ —В–Њ–є –Є–ї–Є –Є–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ 80% —Б–ї—Г—З–∞–µ–≤. –Ю—Б–ї–Њ–ґ–љ–µ–љ–Є–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –љ–µ –±—Л–ї–Њ.
–Я—А–Є —А–∞—Б—Б–Љ–Њ—В—А–µ–љ–Є–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—Л–ї–Њ –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ, —З—В–Њ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –µ–≥–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞–Є–±–Њ–ї—М—И–µ–µ –Є—Е —З–Є—Б–ї–Њ (31%) —Б–≤—П–Ј–∞–љ–Њ —Б –љ–∞–ї–Є—З–Є–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —Б–Њ—З–µ—В–∞–љ–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є – –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –≤ —Б—В–∞–і–Є–Є —В—П–ґ–µ–ї—Л—Е —А–∞–Ј–≤–µ—А–љ—Г—В—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Я–Њ–і–Њ–±–љ—Л–Љ –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –∞–і–µ–Ї–≤–∞—В–љ–Њ–є –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–°–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –≤ –њ–Њ–і–≥—А—Г–њ–њ–∞—Е –±–Њ–ї—М–љ—Л—Е, —Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ—Л—Е –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–µ–є –Њ—З–∞–≥–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≤ —В–Њ–Љ –Є–ї–Є –Є–љ–Њ–Љ —Б–Њ—Б—Г–і–Є—Б—В–Њ–Љ –±–∞—Б—Б–µ–є–љ–µ (–і–∞–љ–љ—Л–µ –Ъ–Ґ/–Ь–†–Ґ), –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –љ–∞–Є–±–Њ–ї—М—И–Є–є –њ—А–Њ—Ж–µ–љ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞–±–ї—О–і–∞–ї—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Њ—З–∞–≥–∞–Љ–Є –≤ –Ј–Њ–љ–µ —Б–Љ–µ–ґ–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є–ї–Є –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ––±–∞–Ј–Є–ї—П—А–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л – 86% —Б–ї—Г—З–∞–µ–≤; –њ—А–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–Є –Љ–Њ–Ј–≥–∞ –≤ –Ј–Њ–љ–µ –Ї–∞—А–Њ—В–Є–і–љ–Њ–≥–Њ –±–∞—Б—Б–µ–є–љ–∞ —А–∞–Ј–≤–Є—В–Є–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤ 74% —Б–ї—Г—З–∞–µ–≤.
–Ю—Ж–µ–љ–Є–≤–∞—П —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е –≤ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –≤–Є–і–∞ –Э–Ь–Ъ, —Г–і–∞–ї–Њ—Б—М —Г—Б—В–∞–љ–Њ–≤–Є—В—М, —З—В–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –Є–Љ–µ–ї –Љ–µ—Б—В–Њ —Г –≤—Б–µ—Е (100%) –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—А–µ—Е–Њ–і—П—Й–Є–Љ–Є –Э–Ь–Ъ, –≤ 87% –љ–∞–±–ї—О–і–µ–љ–Є–є –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Э–Ь–Ъ –Є –≤ 67% —Б–ї—Г—З–∞–µ–≤ —Б—А–µ–і–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ.
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –њ–Њ–±—Г–і–Є–ї–Є –љ–∞—Б –Ї –њ—А–Њ–≤–µ–і–µ–љ–Є—О –±–Њ–ї–µ–µ –і–µ—В–∞–ї—М–љ–Њ–≥–Њ –Є–Ј—Г—З–µ–љ–Є—П –∞—Б–њ–µ–Ї—В–Њ–≤ –і–µ–є—Б—В–≤–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –≤ –Њ—Б—В—А–Њ–є —Б—В–∞–і–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є.
–Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Љ–љ–Њ–≥–Њ–њ–ї–∞–љ–Њ–≤—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –і–µ–є—Б—В–≤–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –љ–∞ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤–Ї–ї—О—З–∞—О—В –Ї–∞–Ї –∞–љ—В–Є–≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ, —В–∞–Ї –Є –Є–љ–≥–Є–±–Є—А–Њ–≤–∞–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, —З—В–Њ —А–µ–∞–ї–Є–Ј—Г–µ—В—Б—П, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –±–ї–∞–≥–Њ–і–∞—А—П –±–ї–Њ–Ї–Є—А–Њ–≤–∞–љ–Є—О —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –љ–Њ—А–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –Є —Б–≤—П–Ј–∞–љ–Њ —Б –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ–Њ–≥–Њ —Ж–Р–Ь–§, –Ї–Њ—В–Њ—А—Л–є –Њ–њ–Њ—Б—А–µ–і—Г–µ—В –Љ–Њ–ї–µ–Ї—Г–ї—П—А–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –љ–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В—Л –Є –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ—Г—О —Б–Є—Б—В–µ–Љ—Г —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є [3]. –Т –Њ—Б—В—А–Њ–є —Б—В–∞–і–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –≥–Є–њ–µ—А–∞–≥—А–µ–≥–∞—Ж–Є—П —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –љ–∞ —Д–Њ–љ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –≤—Б–µ–≥–Њ –њ—Г–ї–∞ –љ–µ–є—А–Њ–≥—Г–Љ–Њ—А–∞–ї—М–љ—Л—Е —А–µ–≥—Г–ї—П—В–Њ—А–Њ–≤, –≤–Ї–ї—О—З–∞—П –Ї–∞—В–µ—Е–Њ–ї–∞–Љ–Є–љ—Л –Є –њ—А–Њ—Б—В–∞–љ–Њ–Є–і—Л. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Ї–∞–Ї –±—Л–ї–Њ –љ–∞–Љ–Є —А–∞–љ–µ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, –≤ –Њ—Б—В—А–µ–є—И–µ–є —Д–∞–Ј–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ —Г—Б–Є–ї–µ–љ–Є–µ –≥–µ–Љ–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–Є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ–Љ–Њ–µ –і–Є—Б–±–∞–ї–∞–љ—Б–Њ–Љ –Љ–µ–ґ–і—Г –њ—А–Њ–∞–≥—А–µ–≥–∞–љ—В–Њ–Љ —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–Љ –Є –Љ–Њ—Й–љ—Л–Љ —Н–љ–і–Њ–≥–µ–љ–љ—Л–Љ –∞–љ—В–Є–∞–≥—А–µ–≥–∞–љ—В–Њ–Љ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–Њ–Љ, —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б –њ—А–Є–Ј–љ–∞–Ї–∞–Љ–Є –Є—Б—В–Њ—Й–µ–љ–Є—П –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П [2,4]. –Т—Л—П–≤–ї–µ–љ–Є–µ —Д–∞–Ї—В–∞ —Б–љ–Є–ґ–µ–љ–Є—П –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —А–µ–Ј–µ—А–≤–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л —Г –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А—Л–Љ–Є –Э–Ь–Ъ —Б—В–∞–≤–Є—В –Ј–∞–і–∞—З—Г –њ–Њ–Є—Б–Ї–∞ –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –љ–µ —В–Њ–ї—М–Ї–Њ –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–Љ–Є —Б–≤–Њ–є—Б—В–≤–∞–Љ–Є, –љ–Њ –Є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –љ–Њ—А–Љ–∞–ї–Є–Ј–Њ–≤–∞—В—М –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П. –≠—В–Њ —П–≤–Є–ї–Њ—Б—М –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –Њ—Ж–µ–љ–Ї–Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Б —Г—З–µ—В–Њ–Љ –µ–≥–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ –≤–ї–Є—П–љ–Є—П –љ–∞ –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П.
–Ш–Ј—Г—З–∞–ї–Є –∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Г—О –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ (–Р–Ф–§––Р–Ґ), –∞ —В–∞–Ї–ґ–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—О –Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ –Є –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞ –і–Њ –Є –њ–Њ—Б–ї–µ 10––і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –Є–љ—К–µ–Ї—Ж–Є–є –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ –і–Њ–Ј–µ 20 –Љ–≥ –љ–∞ 250 –Љ–ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Г 17 –±–Њ–ї—М–љ—Л—Е –≤ –Њ—Б—В—А–µ–є—И–µ–є —Д–∞–Ј–µ –Є–љ—Б—Г–ї—М—В–∞. –С—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤ –њ–µ—А–≤—Л–µ —Б—Г—В–Ї–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ —Г–Љ–µ—А–µ–љ–љ–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —А–µ–Ј–Ї–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –љ–∞ —Д–Њ–љ–µ –≥–Є–њ–µ—А–њ—А–Њ–і—Г–Ї—Ж–Є–Є —В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–∞ (—А–Є—Б. 1). –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –µ—Б–ї–Є –њ—А–Є –Ь–Я —Г –Ј–і–Њ—А–Њ–≤—Л—Е –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ —Б–љ–Є–ґ–µ–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П, —В–Њ —Г –±–Њ–ї—М–љ—Л—Е –љ–∞–±–ї—О–і–∞–ї–∞—Б—М –Є–љ–≤–µ—А—В–Є—А–Њ–≤–∞–љ–љ–∞—П —А–µ–∞–Ї—Ж–Є—П, —В.–µ. —А–µ–Ј–Ї–Њ–µ –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ (–љ–∞ 40–50%) —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ –Ї–Њ—Н—Д—Д–Є—Ж–Є–µ–љ—В–∞. –Я–Њ—Б–ї–µ 10––і–љ–µ–≤–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Њ–±–љ–∞—А—Г–ґ–µ–љ–Њ –њ–Њ–љ–Є–ґ–µ–љ–Є–µ –∞–≥—А–µ–≥–∞—Ж–Є–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ —А–Њ—Б—В –≤–µ–ї–Є—З–Є–љ—Л –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П. –Я—А–Є —Н—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –Є—Б—Е–Њ–і–љ–Њ–є –њ—А–Њ–±–µ —Н—В–∞ –≤–µ–ї–Є—З–Є–љ–∞ –і–Њ—Б—В–Є–≥–∞–ї–∞ 62% –Њ—В –Ї–Њ–љ—В—А–Њ–ї—П, –∞ –њ–Њ—Б–ї–µ –Ь–Я –Њ–љ–∞ –њ—А–Є–±–ї–Є–ґ–∞–ї–∞—Б—М –Ї –љ–Њ—А–Љ–µ. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–µ—З–µ–љ–Є–µ –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –≤ –Њ—Б—В—А–Њ–Љ –њ–µ—А–Є–Њ–і–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї –≤—Л—П–≤–ї—П–µ–Љ–Њ–Љ—Г —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Ј–∞—Й–Є—В–љ–Њ–≥–Њ –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –µ–≥–Њ –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ (—А–Є—Б. 1).

–†–Є—Б. 1. –°–Њ—Б—В–Њ—П–љ–Є–µ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є (–њ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –Р–Ф–§-–Р–Ґ –Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П 6-–Ї–µ—В–Њ –Я–УF1a/–Ґ–•–Т2 –њ–Њ—Б–ї–µ –Ь–Я) —Г –±–Њ–ї—М–љ—Л—Е —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ
–І—В–Њ –ґ–µ —Б–ї—Г–ґ–Є–ї–Њ –њ—А–Є—З–Є–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г —З–∞—Б—В–Є –±–Њ–ї—М–љ—Л—Е —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ–Є –Є–љ—Б—Г–ї—М—В–∞–Љ–Є? –Ф–ї—П –њ–Њ–Є—Б–Ї–∞ –Њ—В–≤–µ—В–∞ –љ–∞ —Н—В–Њ—В –≤–Њ–њ—А–Њ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–ї–Њ—Б—М –≤–∞–ґ–љ—Л–Љ —Б–Њ–њ–Њ—Б—В–∞–≤–Є—В—М —Н—Д—Д–µ–Ї—В –ї–µ—З–µ–љ–Є—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ–Њ–і—В–Є–њ–∞–Љ–Є –Є–љ—Б—Г–ї—М—В–∞. –†–∞–љ–µ–µ –љ–∞–Љ–Є –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≥–µ—В–µ—А–Њ–≥–µ–љ–љ—Л–µ –њ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞–Љ —А–∞–Ј–≤–Є—В–Є—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –Э–Ь–Ъ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –≤ —Г—Б–ї–Њ–≤–Є—П—Е –Њ–і–љ–Њ–љ–∞–њ—А–∞–≤–ї–µ–љ–љ—Л—Е –њ–Њ —Е–∞—А–∞–Ї—В–µ—А—Г, –љ–Њ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ–Њ —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–є —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ –Ї—А–Њ–≤–Є –Є —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ [4]. –С—Л–ї –њ—А–Њ–≤–µ–і–µ–љ –∞–љ–∞–ї–Є–Ј —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ —Б–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–Є —Б –µ–≥–Њ –≤–ї–Є—П–љ–Є–µ–Љ –љ–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ —Г –±–Њ–ї—М–љ—Л—Е –і–≤—Г—Е –≥—А—Г–њ–њ: —Б –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–Љ –≥–µ–љ–µ–Ј–Њ–Љ –Є–љ—Б—Г–ї—М—В–∞ (–њ–µ—А–≤–∞—П –≥—А—Г–њ–њ–∞) –Є —Б –ї–∞–Ї—Г–љ–∞—А–љ—Л–Љ –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ (–≤—В–Њ—А–∞—П –≥—А—Г–њ–њ–∞). –Т—Л–±–Њ—А —Н—В–Є—Е –і–≤—Г—Е –њ–Њ–і—В–Є–њ–Њ–≤ —Б–≤—П–Ј–∞–љ —Б –і–Є–∞–Љ–µ—В—А–∞–ї—М–љ–Њ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–ї–Њ–ґ–љ—Л–Љ —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л –Љ–Њ–Ј–≥–∞ –Є, —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ–Њ, —Б –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–є —А–∞–Ј–ї–Є—З–љ–Њ–є –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є. –Х—Б–ї–Є –њ–∞—Ж–Є–µ–љ—В—Л –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ—Л —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –љ–∞–ї–Є—З–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–Њ–ї–Њ–≤—Л (–Ь–Р–У), —В–Њ –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤—В–Њ—А–Њ–є –≥—А—Г–њ–њ—Л —Е–∞—А–∞–Ї—В–µ—А–љ–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Љ–µ–ї–Ї–Є—Е –∞—А—В–µ—А–Є–є/–∞—А—В–µ—А–Є–Њ–ї.–°–Њ–њ–Њ—Б—В–∞–≤–ї–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤—Л—П–≤–Є–ї–Њ –±–Њ–ї—М—И–Є–є –њ—А–Њ—Ж–µ–љ—В –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б –ї–∞–Ї—Г–љ–∞—А–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ.
–Р–љ–∞–ї–Є–Ј –≥–µ–Љ–Њ—А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ–∞—А–∞–Љ–µ—В—А–Њ–≤ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Г –±–Њ–ї—М–љ—Л—Е —Б –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –і–Њ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї—Б—П —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–µ–љ–љ—Л–є –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, —З—В–Њ –њ—А–Њ—П–≤–ї—П–ї–Њ—Б—М —А–µ–Ј–Ї–Є–Љ –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є–µ–Љ –Р–Ф–§––Р–Ґ –Є —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –≤–µ–ї–Є—З–Є–љ—Л –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –і–Њ 50% –≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б –Є—Б—Е–Њ–і–љ—Л–Љ –µ–≥–Њ –Ј–љ–∞—З–µ–љ–Є–µ–Љ –њ—А–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –њ—А–Њ–±—Л. –Я—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –њ—А–Є–≤–Њ–і–Є–ї–Њ –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Є —Б—В–µ–њ–µ–љ–Є –Є–љ–≤–µ—А—В–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Ї –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –њ–Њ–Ј–Є—В–Є–≤–љ—Л–Љ —Б–і–≤–Є–≥–∞–Љ –≤ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–Љ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є–Є –≤ –Њ—В–≤–µ—В –љ–∞ –Ь–Я, –љ–Њ –љ–µ —Г—Б—В—А–∞–љ—П–ї–Њ –њ–Њ–ї–љ–Њ—Б—В—М—О –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є—П –µ–≥–Њ —В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ––≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞.
–£ –±–Њ–ї—М–љ—Л—Е —Б –ї–∞–Ї—Г–љ–∞—А–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –Є—Б—Е–Њ–і–љ–Њ, –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П, –њ—А–Њ—П–≤–ї—П–≤—И–µ–µ—Б—П –≤ –љ–µ–∞–і–µ–Ї–≤–∞—В–љ–Њ–є —А–µ–∞–Ї—Ж–Є–Є –Є–Ј—Г—З–∞–µ–Љ—Л—Е —Б–Є—Б—В–µ–Љ –љ–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г (—А–Є—Б. 2). –Я–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є–ї–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–Њ–∞–≥—А–µ–≥–∞–љ—В–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П, –≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Ј–∞ —Б—З–µ—В —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞. –Я—А–Є —Н—В–Њ–Љ –≤–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–µ—А–≤–Њ–є –≥—А—Г–њ–њ—Л –љ–Њ—А–Љ–∞–ї—М–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≤–µ–ї–Є—З–Є–љ—Л –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –≤—Л—П–≤–ї—П–ї–Њ—Б—М –≤ –њ—А–Њ–±–∞—Е –Ї—А–Њ–≤–Є –Ї–∞–Ї –і–Њ, —В–∞–Ї –Є –њ–Њ—Б–ї–µ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –љ–∞–≥—А—Г–Ј–Ї–Є.

–†–Є—Б. 2. –°–Њ—Б—В–Њ—П–љ–Є–µ —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є (–њ–Њ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –Р–Ф–§-–Р–Ґ –Є —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П 6-–Ї–µ—В–Њ –Я–УF1a/–Ґ–•–Т2 –њ–Њ—Б–ї–µ –Ь–Я) —Г –±–Њ–ї—М–љ—Л—Е —Б –∞—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–Љ –Є –ї–∞–Ї—Г–љ–∞—А–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–∞–Љ–Є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ –Њ—Б—В—А–µ–є—И–µ–є —Д–∞–Ј–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є –Љ–µ—А–µ, –њ–Њ––≤–Є–і–Є–Љ–Њ–Љ—Г, —Б–≤—П–Ј–∞–љ —Б–Њ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М—О –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Њ—В–Є–≤–Њ–і–µ–є—Б—В–≤–Њ–≤–∞—В—М —Г—Б–Є–ї–µ–љ–Є—О –≥–µ–Љ–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–∞—Ж–Є–Є, —Б—В–Є–Љ—Г–ї–Є—А—Г–µ–Љ–Њ–є, —Б –Њ–і–љ–Њ–є —Б—В–Њ—А–Њ–љ—Л, —Б–і–≤–Є–≥–Њ–≤—Л–Љ–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П–Љ–Є –њ–Њ—В–Њ–Ї–∞ –Ї—А–Њ–≤–Є (–Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –љ–∞–ї–Є—З–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –≤ —Б—В–µ–љ–Ї–∞—Е –Ь–Р–У) –Є, —Б –і—А—Г–≥–Њ–є – –Љ–Њ—Й–љ—Л–Љ –≤—Л–±—А–Њ—Б–Њ–Љ —В—А–Њ–Љ–±–Њ–њ–ї–∞—Б—В–Є—З–µ—Б–Ї–Є—Е —Б–Њ–µ–і–Є–љ–µ–љ–Є–є –Є–Ј –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ–Њ–є —В–Ї–∞–љ–Є –Љ–Њ–Ј–≥–∞, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є—Е –њ—А–Њ–Ї–Њ–∞–≥—Г–ї—П–љ—В–љ—Г—О –љ–∞–њ—А–∞–≤–ї–µ–љ–љ–Њ—Б—В—М –Є –і–Є—Б–±–∞–ї–∞–љ—Б —Д–∞–Ї—В–Њ—А–Њ–≤ –≥—Г–Љ–Њ—А–∞–ї—М–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є –≥–µ–Љ–Њ—Б—В–∞–Ј–∞.–С–Њ–ї–µ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–є –≥–µ–Љ–Њ—А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В —Г –±–Њ–ї—М–љ—Л—Е —Б –ї–∞–Ї—Г–љ–∞—А–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ —Б–≤—П–Ј–∞–љ, –Њ—З–µ–≤–Є–і–љ–Њ, —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –Њ—З–∞–≥–Њ–≤—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –≤–µ—Й–µ—Б—В–≤–∞ –Љ–Њ–Ј–≥–∞ –Є –≥—А—Г–±—Л—Е —Б—В–µ–љ–Њ–Ј–Є—А—Г—О—Й–Є—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є –Ь–Р–У. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–є –≥–µ–љ–µ–Ј –Є–љ—Б—Г–ї—М—В–∞ —З–∞—Й–µ —Б–Њ–њ—А—П–ґ–µ–љ —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –≥–Њ–ї–Њ–≤—Л, —З—В–Њ –Є –Њ–±—Г—Б–ї–Њ–≤–ї–Є–≤–∞–µ—В –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–µ —А–∞–Ј–≤–Є—В–Є–µ –Ї—А—Г–њ–љ–Њ–Њ—З–∞–≥–Њ–≤–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≤–µ—Й–µ—Б—В–≤–∞ –Љ–Њ–Ј–≥–∞, –њ–Њ–љ—П—В–љ–Њ, —З—В–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є—П –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –Ј–∞—В—А—Г–і–љ–µ–љ–∞. –≠—В–Њ –≤ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–є –Љ–µ—А–µ –Њ–±—К—П—Б–љ—П–µ—В –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є—Е —Б—Е–µ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е. –Я—А–Є —Н—В–Њ–Љ –≤–µ—А–Њ—П—В–љ–Њ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–Є—В—М, —З—В–Њ –±–Њ–ї—М–љ—Л–Љ —Б –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ—Л–є –Ї—Г—А—Б –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –њ—А–µ–њ–∞—А–∞—В–∞, —В–∞–Ї –Ї–∞–Ї —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –і–∞–љ–љ–Њ–є –≥—А—Г–њ–њ—Л –њ–Њ–Ј–Є—В–Є–≤–љ–∞—П —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –Њ—В—З–µ—В–ї–Є–≤–Њ –љ–∞–Љ–µ—З–∞–µ—В—Б—П –ї–Є—И—М –Ї 10––Љ—Г –і–љ—О –ї–µ—З–µ–љ–Є—П.
–Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –Ъ–∞–≤–Є–љ—В–Њ–љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Я–Њ –і–∞–љ–љ—Л–Љ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П –Ь–Р–У (–≤ —Г—Б–ї–Њ–≤–Є—П—Е «–Њ—Б—В—А–Њ–≥–Њ –Њ–њ—Л—В–∞» – –і–Њ –Є –њ–Њ—Б–ї–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–є –Є–љ—Д—Г–Ј–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞), –Ъ–∞–≤–Є–љ—В–Њ–љ –Њ–і–Є–љ–∞–Ї–Њ–≤–Њ –≤–ї–Є—П–ї –љ–∞ –Ї—А–Њ–≤–Њ—В–Њ–Ї –≤ –Ј–і–Њ—А–Њ–≤–Њ–Љ –Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ–Њ–Љ –њ–Њ–ї—Г—И–∞—А–Є—П—Е –Љ–Њ–Ј–≥–∞, —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ —Д–µ–љ–Њ–Љ–µ–љ–∞ «–Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—П».
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Ъ–∞–≤–Є–љ—В–Њ–љ —П–≤–ї—П–µ—В—Б—П —Ж–µ–љ–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ –≤ –њ–µ—А–µ—З–љ–µ –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–≤, –њ—А–Є–Љ–µ–љ—П–µ–Љ—Л—Е –њ—А–Є –Њ—Б—В—А—Л—Е –Э–Ь–Ъ, –љ–µ —В–Њ–ї—М–Ї–Њ –±–ї–∞–≥–Њ–і–∞—А—П —Б–≤–Њ–Є–Љ –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б–≤–Њ–є—Б—В–≤–∞–Љ, –љ–Њ –Є –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –Є–Ј–Љ–µ–љ—П—О—Й–Є–є –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ—Л–є, –∞–љ—В–Є–∞–≥—А–µ–≥–∞—Ж–Є–Њ–љ–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –њ—А–Є –ї–∞–Ї—Г–љ–∞—А–љ—Л—Е –Є–љ—Б—Г–ї—М—В–∞—Е.
–С—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –Є–Ј—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ –ї–µ—З–µ–љ–Є–Є 65 –±–Њ–ї—М–љ—Л—Е —Б –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є (–Ф–≠). –≠—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є –Ф–≠ —П–≤–ї—П–ї–Є—Б—М: –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–∞—П –±–Њ–ї–µ–Ј–љ—М (18 —Б–ї—Г—З–∞–µ–≤), —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–Њ–љ–Є—П (5 —Б–ї—Г—З–∞–µ–≤), –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–Њ–љ–Є—П –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ (30 —Б–ї—Г—З–∞–µ–≤), –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–∞—П –і–Є—Б—В–Њ–љ–Є—П —Б —В—А–∞–љ–Ј–Є—В–Њ—А–љ–Њ–є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є (12 —Б–ї—Г—З–∞–µ–≤). –†–∞—Б–њ—А–µ–і–µ–ї–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –Ф–≠ –њ–Њ —Б—В–∞–і–Є—П–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –±—Л–ї–Њ —Б–ї–µ–і—Г—О—Й–Є–Љ: I —Б—В–∞–і–Є—П – 22 –њ–∞—Ж–Є–µ–љ—В–∞, II —Б—В–∞–і–Є—П – 21 –њ–∞—Ж–Є–µ–љ—В, III —Б—В–∞–і–Є—П – 22 –њ–∞—Ж–Є–µ–љ—В–∞ [5].
–°–Є–Љ–њ—В–Њ–Љ—Л –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –≤—Л—П–≤–ї—П–ї–Є—Б—М —Г 43 –Є–Ј 65 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є –±—Л–ї–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л–Љ–Є –Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є, –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б—В–∞—В–Є–Ї–Є, –њ–Њ—Е–Њ–і–Ї–Є –Є –Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є–Є, —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –≤—Л—Б—И–Є—Е –Ї–Њ—А–Ї–Њ–≤—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –Љ–Њ–Ј–ґ–µ—З–Ї–Њ–≤—Л–Љ–Є –Є –≤–µ—Б—В–Є–±—Г–ї—П—А–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О —З–µ—А–µ–њ–љ–Њ––Љ–Њ–Ј–≥–Њ–≤–Њ–є –Є–љ–љ–µ—А–≤–∞—Ж–Є–Є. –Я—А–Є —Н—В–Њ–Љ —Г 15 –Є–Ј –љ–Є—Е –Њ—З–∞–≥–Њ–≤–∞—П –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–∞—П –Љ–Є–Ї—А–Њ—Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–∞ –≤—Л—П–≤–ї—П–ї–∞—Б—М –њ—А–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б—В–∞—В—Г—Б–∞ –Є –љ–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї–∞—Б—М —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Д—Г–љ–Ї—Ж–Є–Є. –°—Г–±—К–µ–Ї—В–Є–≤–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л –±—Л–ї–Є –≤–µ–і—Г—Й–Є–Љ–Є –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Г 27 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ—А–Є—З–µ–Љ —Г 18 –Є–Ј –љ–Є—Е –Њ–љ–Є –±—Л–ї–Є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є, –∞ —Г 9 – –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л–Љ–Є.
–Т—Л—П–≤–ї–µ–љ–љ—Л–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г 30 –Є–Ј 43 –±–Њ–ї—М–љ—Л—Е —Б I –Є II —Б—В–∞–і–Є–µ–є –Ф–≠ –Є –≤ 6 –љ–∞–±–ї—О–і–µ–љ–Є—П—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б III —Б—В–∞–і–Є–µ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Њ–њ—А–µ–і–µ–ї—П–ї—Б—П –њ–Њ—Б–ї–µ 3–4 –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –Є –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ —Г–≤–µ–ї–Є—З–Є–≤–∞–ї—Б—П, –і–Њ—Б—В–Є–≥–∞—П –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ –Ї –Ї–Њ–љ—Ж—Г –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П. –Ю—В–Љ–µ—З–µ–љ–Њ, —З—В–Њ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –±—Л–ї–Њ –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ, —З–µ–Љ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ –Ъ–∞–≤–Є–љ—В–Њ–љ–∞.
–Ю–њ—А–µ–і–µ–ї–µ–љ–∞ –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –њ—А–Є –∞–љ–∞–ї–Є–Ј–µ –µ–≥–Њ –і–µ–є—Б—В–≤–Є—П –љ–∞ —В–µ –Є–ї–Є –Є–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Б–Є–љ–і—А–Њ–Љ—Л. –Т –љ–∞–Є–±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є —Н—Д—Д–µ–Ї—В –і–µ–є—Б—В–≤–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤—Л—А–∞–ґ–µ–љ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –љ–∞—А—Г—И–µ–љ–Є–є –≤—Л—Б—И–Є—Е –Ї–Њ—А–Ї–Њ–≤—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –њ–∞–Љ—П—В–Є, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ––≤–Њ–ї–µ–≤–Њ–є —Б—Д–µ—А—Л, –∞ —В–∞–Ї–ґ–µ –∞—Б—В–µ–љ–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Т –±–Њ–ї–µ–µ —З–µ–Љ 50% –љ–∞–±–ї—О–і–µ–љ–Є–є –Є–Љ–µ–ї –Љ–µ—Б—В–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –њ—А–Є –≤–µ—Б—В–Є–±—Г–ї–Њ––Љ–Њ–Ј–ґ–µ—З–Ї–Њ–≤—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е. –Т –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї —Н—В–Њ–Љ—Г, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е, –њ—А–Њ–ї–µ—З–µ–љ–љ—Л—Е –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ, —Б—В–µ–њ–µ–љ—М –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —Ж–µ—Д–∞–ї–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ю–њ—А–µ–і–µ–ї–µ–љ–љ—Л–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –љ–∞–±–ї—О–і–∞–ї—Б—П –њ—А–Є –љ–∞—А—Г—И–µ–љ–Є—П—Е –і–≤–Є–≥–∞—В–µ–ї—М–љ–Њ–є —Б—Д–µ—А—Л. –Ю–±—К–µ–Ї—В–Є–≤–љ–Њ –±–Њ–ї—М–љ—Л–µ —Б—В–∞–љ–Њ–≤–Є–ї–Є—Б—М –±–Њ–ї–µ–µ —Б–Њ–±—А–∞–љ–љ—Л–Љ–Є, –Ї–Њ–љ—В–∞–Ї—В–љ—Л–Љ–Є, —Г–Љ–µ–љ—М—И–∞–ї–∞—Б—М –Є—Е —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–∞—П –ї–∞–±–Є–ї—М–љ–Њ—Б—В—М, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–ї–Њ—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Њ–є –≠–≠–У –Є —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —В–µ—Б—В–Њ–≤.
–Ф–ї—П –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –≤–ї–Є—П–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –љ–∞ –њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ—Л–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Љ–Њ–Ј–≥–∞ —Г 11 –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В – 52,3±2,1 –≥–Њ–і–∞) –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Љ–µ—В–Њ–і–Њ–Љ –Ю–§–≠–Ъ–Ґ (—А–Є—Б. 3) –і–Њ –Є –њ–Њ—Б–ї–µ –Ї—Г—А—Б–∞ –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –њ—А–µ–њ–∞—А–∞—В–∞. –Я—А–Є –Њ—Ж–µ–љ–Ї–µ —Д–Њ–љ–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Г –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –і–Є—Д—Д—Г–Ј–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –Ї–∞–Ї –≤ –Ї–Њ—А–Ї–Њ–≤—Л—Е –Њ–±–ї–∞—Б—В—П—Е, —В–∞–Ї –Є –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –±–µ–ї–Њ–≥–Њ –≤–µ—Й–µ—Б—В–≤–∞ –Љ–Њ–Ј–≥–∞, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –ї–Њ–±–љ—Л—Е –Є –≤–Є—Б–Њ—З–љ—Л—Е –і–Њ–ї—П—Е. –Я—А–Є —Н—В–Њ–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –љ–Њ—Б–Є–ї–Њ –Љ–Њ–Ј–∞–Є—З–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Я–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї—Г—А—Б–∞ –Є–љ—Д—Г–Ј–Є–Њ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ —Г —Н—В–Є—Е –ґ–µ –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б—В–µ–њ–µ–љ–Є –њ–µ—А—Д—Г–Ј–Є–Є –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –њ–Њ –≤—Б–µ–Љ —А–µ–≥–Є–Њ–љ–∞–Љ –Ї–∞–Ї –≤ –Ї–Њ—А–Ї–Њ–≤—Л—Е –Њ—В–і–µ–ї–∞—Е, —В–∞–Ї –Є –≤ –±–µ–ї–Њ–Љ –≤–µ—Й–µ—Б—В–≤–µ –Љ–Њ–Ј–≥–∞, —З—В–Њ —Б–ї–µ–і—Г–µ—В —А–∞—Б—Ж–µ–љ–Є—В—М –Ї–∞–Ї –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є–µ –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –њ—А–µ–њ–∞—А–∞—В–∞. –Э–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Њ—Б–Њ–±–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –≤—Л—П–≤–ї—П–µ–Љ–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ –њ—А–µ–ґ–і–µ –≤—Б–µ–≥–Њ –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М –≤ –Є—Б—Е–Њ–і–љ–Њ –љ–∞–Є–±–Њ–ї–µ–µ «—Б–Ї–Њ–Љ–њ—А–Њ–Љ–µ—В–Є—А–Њ–≤–∞–љ–љ—Л—Е» –≥–Є–њ–Њ–њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ—Л—Е –Њ–±–ї–∞—Б—В—П—Е. –Я–Њ—Б–ї–µ –Њ–±—А–∞–±–Њ—В–Ї–Є –і–∞–љ–љ—Л—Е –њ–Њ –њ—А–Њ–≥—А–∞–Љ–Љ–µ «CORTIQAL» –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –≤ –Ј–Њ–љ–∞—Е —Б –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —А–µ–і—Г–Ї—Ж–Є–µ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —А–µ–њ–µ—А—Д—Г–Ј–Є–Њ–љ–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –±—Л–ї–∞ –≤—Л—И–µ – —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–є «—Д–µ–љ–Њ–Љ–µ–љ, –Њ–±—А–∞—В–љ—Л–є –Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—О». –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —В–µ–љ–і–µ–љ—Ж–Є—П –Ї —Б–≥–ї–∞–ґ–Є–≤–∞–љ–Є—О –Љ–µ–ґ—А–µ–≥–Є–Њ–љ–∞—А–љ–Њ–є –∞—Б–Є–Љ–Љ–µ—В—А–Є–Є –Ј–∞ —Б—З–µ—В –≤—Л—А–∞–≤–љ–Є–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –≤ –Њ—В–і–µ–ї—М–љ—Л—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –Њ–±–ї–∞—Б—В—П—Е (–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–є —Н—Д—Д–µ–Ї—В).

–Ы–µ—З–µ–љ–Є–µ –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–≤–µ–ї–Є—З–µ–љ–Є—О –Љ–Њ–Ј–≥–Њ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –Ј–Њ–љ–∞—Е –Є—Б—Е–Њ–і–љ–Њ–є –≥–Є–њ–Њ–њ–µ—А—Д—Г–Ј–Є–Є.–≠—В–Њ—В –Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–є —Н—Д—Д–µ–Ї—В –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —З—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е.
–†–Є—Б. 3 –Э–µ–є—А–Њ–≥—А–∞—Д–Є—З–µ—Б–Ї–∞—П –Њ—Ж–µ–љ–Ї–∞ –Љ–µ—В–Њ–і–Њ–Љ –Ю–§–≠–Ъ–Ґ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ
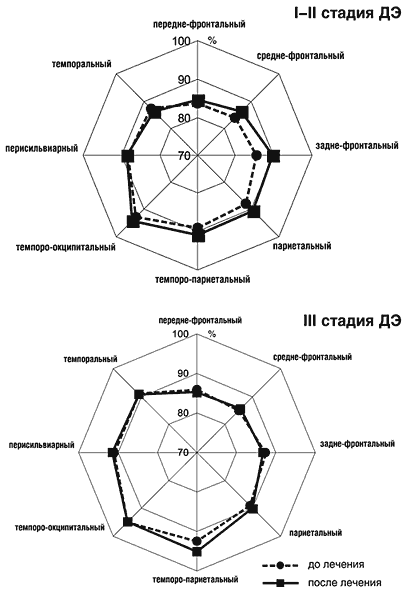
–†–Є—Б. 4. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ–є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є —Г –±–Њ–ї—М–љ—Л—Е —Б –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ
–Т—Л–≤–Њ–і—Л1. –Я–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –њ—А–Є –Њ—Б—В—А—Л—Е –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Э–Ь–Ъ. –Я—А–Є —Н—В–Њ–Љ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –Њ—В–Љ–µ—З–µ–љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤:
1. –Я–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –њ—А–Є –Њ—Б—В—А—Л—Е –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Э–Ь–Ъ. –Я—А–Є —Н—В–Њ–Љ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В –Љ–Њ–љ–Њ—В–µ—А–∞–њ–Є–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –Њ—В–Љ–µ—З–µ–љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤:- —Б –њ—А–µ—Е–Њ–і—П—Й–Є–Љ–Є –Э–Ь–Ъ,
- —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є —Б–Њ—З–µ—В–∞–љ–љ–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є,
- —Б –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–µ–є –Њ—З–∞–≥–∞ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Љ–Њ–Ј–≥–∞ –≤ –Ј–Њ–љ–∞—Е —Б–Љ–µ–ґ–љ–Њ–≥–Њ –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –Є –≤ –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ––±–∞–Ј–Є–ї—П—А–љ–Њ–є —Б–Є—Б—В–µ–Љ–µ.
2. –Я–Њ–ї—Г—З–µ–љ—Л –љ–Њ–≤—Л–µ –і–∞–љ–љ—Л–µ –Њ –≥–µ–Љ–Њ–Ї–Њ—А—А–µ–Ї—В–Њ—А–љ—Л—Е –Є –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е —Б–≤–Њ–є—Б—В–≤–∞—Е –Ъ–∞–≤–Є–љ—В–Њ–љ–∞. –Т –Њ—Б—В—А–µ–є—И–µ–Љ –њ–µ—А–Є–Њ–і–µ –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞ –Ї—Г—А—Б –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л—Е –Є–љ—Д—Г–Ј–Є–є –њ—А–µ–њ–∞—А–∞—В–∞ –Њ–±—Й–µ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –љ–µ –Љ–µ–љ–µ–µ 10 –і–љ–µ–є –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–ї—Г—З—И–µ–љ–Є—О –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї –Ї—А–Њ–≤–Є –Є –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є—О –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Н–љ–і–Њ—В–µ–ї–Є—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–Њ–і–Є—Д–Є–Ї–∞—Ж–Є–Є —Г—А–Њ–≤–љ—П –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –љ–∞–і –љ–Є–Љ–Є.
3. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ–∞ –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞, –њ—А–Є–Љ–µ–љ—П–µ–Љ–Њ–≥–Њ –≤ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Є–Є —Б –њ—А–Є–љ—П—В—Л–Љ–Є —Б—Е–µ–Љ–∞–Љ–Є —В–µ—А–∞–њ–Є–Є, –Њ—В –≤–µ–і—Г—Й–µ–≥–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ–∞ —А–∞–Ј–≤–Є—В–Є—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞, —Б –Њ—В—З–µ—В–ї–Є–≤—Л–Љ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ–Љ —Г –±–Њ–ї—М–љ—Л—Е —Б –ї–∞–Ї—Г–љ–∞—А–љ—Л–Љ –Є–љ—Б—Г–ї—М—В–Њ–Љ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –±–Њ–ї—М–љ—Л–Љ–Є —Б –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –Ю–Э–Ь–Ъ.
–Т—Л—П–≤–ї–µ–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–µ —В–Є–њ—Л —А–µ–∞–Ї—Ж–Є–є —В—А–Њ–Љ–±–Њ—Ж–Є—В–∞—А–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –≤ –Њ—В–≤–µ—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ, –Њ–±–Њ—Б–љ–Њ–≤—Л–≤–∞—О—Й–Є–µ –µ–≥–Њ —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї—Г—О –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В—М. –Я—А–Є –ї–∞–Ї—Г–љ–∞—А–љ–Њ–Љ –Є–љ—Б—Г–ї—М—В–µ –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–µ —В–Њ–ї—М–Ї–Њ —Г—Б—В—А–∞–љ–µ–љ–Є–µ —Д–Њ–љ–Њ–≤–Њ–є –≥–Є–њ–µ—А–∞–≥—А–µ–≥–∞–±–µ–ї—М–љ–Њ—Б—В–Є —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤, –љ–Њ —В–∞–Ї–ґ–µ –≤ –Њ—В–≤–µ—В –љ–∞ –љ–∞–≥—А—Г–Ј–Њ—З–љ—Г—О –њ—А–Њ–±—Г –њ–Њ–і–∞–≤–ї—П–µ—В—Б—П –Є—Е –њ–∞—А–∞–і–Њ–Ї—Б–∞–ї—М–љ—Л–є –њ—А–Њ–∞–≥—А–µ–≥–∞–љ—В–љ—Л–є –Њ—В–≤–µ—В –Є –≤–Њ–Ј—А–∞—Б—В–∞–µ—В –≤–µ–ї–Є—З–Є–љ–∞ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–≥–Њ —Б–Њ–Њ—В–љ–Њ—И–µ–љ–Є—П –≤—Б–ї–µ–і—Б—В–≤–Є–µ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є —Н–љ–і–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–∞. –Я—А–Є –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Њ–Љ –Є–љ—Б—Г–ї—М—В–µ –ї–µ—З–µ–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ–Њ —Б—В–∞–љ–і–∞—А—В–љ–Њ–є —Б—Е–µ–Љ–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —Б—В–µ–њ–µ–љ–Є –Є–љ–≤–µ—А—В–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞ —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –љ–∞ —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –љ–∞–≥—А—Г–Ј–Ї—Г, –Њ–і–љ–∞–Ї–Њ –њ–Њ–ї–љ–Њ—Б—В—М—О –љ–µ —Б–≥–ї–∞–ґ–Є–≤–∞–µ—В –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є—П —В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ––≤–∞–Ј–Њ–Ї–Њ–љ—Б—В—А–Є–Ї—В–Њ—А–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ –≤ –њ—А–Њ—Б—В–∞—Ж–Є–Ї–ї–Є–љ–—В—А–Њ–Љ–±–Њ–Ї—Б–∞–љ–Њ–≤–Њ–Љ –±–∞–ї–∞–љ—Б–µ.
–Я–Њ–Ї–∞–Ј–∞–љ–∞ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М —А–∞–Ј—А–∞–±–Њ—В–Ї–Є –Љ–µ—В–Њ–і–Є–Ї –±–Њ–ї–µ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ (–≤ —Б—А–∞–≤–љ–µ–љ–Є–Є —Б–Њ —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ) –Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –њ—А–Є –∞—В–µ—А–Њ—В—А–Њ–Љ–±–Њ—В–Є—З–µ—Б–Ї–Њ–Љ –≤–∞—А–Є–∞–љ—В–µ –њ–Њ—Б–ї–µ–і–љ–µ–≥–Њ.
4. –Я–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –Э–Ь–Ъ. –Э–∞–Є–±–Њ–ї–µ–µ –Њ—В—З–µ—В–ї–Є–≤—Л–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Л—П–≤–ї–µ–љ —Г –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ I –Є II —Б—В–∞–і–Є—П–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В—М—О –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –Љ–µ–љ–µ–µ 10 –ї–µ—В. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –љ–∞—З–Є–љ–∞—В—М —В–µ—А–∞–њ–Є—О –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –≤ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —А–∞–љ–љ–Є–µ —Б—А–Њ–Ї–Є –Њ—В –Љ–Њ–Љ–µ–љ—В–∞ –≤–µ—А–Є—Д–Є–Ї–∞—Ж–Є–Є –і–Є–∞–≥–љ–Њ–Ј–∞.
–Т–Љ–µ—Б—В–µ —Б —В–µ–Љ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –Ї —А–µ–≥—Г–ї—П—Ж–Є–Є –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–љ–Њ–≥–Њ –Ї–Њ–љ—В—А–Њ–ї—П –≥–µ–Љ–∞—В–Њ–≤–∞–Ј–∞–ї—М–љ—Л—Е –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–є –Њ–њ—А–∞–≤–і—Л–≤–∞–µ—В –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Є –њ—А–Є –±–Њ–ї–µ–µ —В—П–ґ–µ–ї—Л—Е —Д–Њ—А–Љ–∞—Е –±–Њ–ї–µ–Ј–љ–Є —Б —Ж–µ–ї—М—О –њ–Њ–≤—Л—И–µ–љ–Є—П –∞—В—А–Њ–Љ–±–Њ–≥–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ —Н–љ–і–Њ—В–µ–ї–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б—В–µ–љ–Ї–Є –Є —Г–ї—Г—З—И–µ–љ–Є—П —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є. –С–Њ–ї—М–љ—Л–Љ —Б —В—П–ґ–µ–ї—Л–Љ–Є —Д–Њ—А–Љ–∞–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ (III —Б—В–∞–і–Є—П –Ф–≠) –њ–Њ–Ї–∞–Ј–∞–љ–Њ –љ–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ —Б –Ї—Г—А—Б–Њ–≤–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ –≤ –Є–љ—М–µ–Ї—Ж–Є–Њ–љ–љ–Њ–є —Д–Њ—А–Љ–µ.
5. –Э–∞ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –і–Њ–Ї–∞–Ј–∞—В–µ–ї—М–љ–Њ–є –±–∞–Ј–µ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М —В–µ—А–∞–њ–Є–Є –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ, —Б –Њ—В—Б—Г—В—Б—В–≤–Є–µ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –≤–Ї–ї—О—З–∞—П «—Б–Є–љ–і—А–Њ–Љ –Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—П». –Ґ–∞–Ї–ґ–µ –≤–љ–Њ–≤—М –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ –Њ–±—А–∞—В–љ—Л–є –Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—О –Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В.
6. –£—Б—В–∞–љ–Њ–≤–ї–µ–љ –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Э–Ь–Ъ. –Ь–µ—В–Њ–і–Њ–Љ –Ю–§–≠–Ъ–Ґ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ф–≠ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–Њ–Љ –≤–µ—А–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Љ–Њ–Ј–≥–Њ–≤–Њ–є –њ–µ—А—Д—Г–Ј–Є–Є, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –Ј–Њ–љ–∞—Е –Є–Ј–љ–∞—З–∞–ї—М–љ–Њ–є –≥–Є–њ–Њ–њ–µ—А—Д—Г–Ј–Є–Є. –≠—В–Њ—В –Љ–Њ–і—Г–ї–Є—А—Г—О—Й–Є–є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–є —Н—Д—Д–µ–Ї—В –±—Л–ї –±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –љ–∞ —А–∞–љ–љ–Є—Е —Б—В–∞–і–Є—П—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, —З—В–Њ –≤–љ–Њ–≤—М –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ —А–∞–љ–љ–µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Ъ–∞–≤–Є–љ—В–Њ–љ–∞ —Г –і–∞–љ–љ–Њ–є –Ї–∞—В–µ–≥–Њ—А–Є–Є –±–Њ–ї—М–љ—Л—Е.
1. –С–∞–ї—Г–і–∞ –Т.–Я., –Ф–µ—П–љ–Њ–≤ –Ш.–Ш., –С–∞–ї—Г–і–∞ –Ь.–Т. –Є –і—А. –Я—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ —В—А–Њ–Љ–±–Њ–Ј–Њ–≤ / –Я–Њ–і —А–µ–і. –Т.–Я. –С–∞–ї—Г–і—Л. – –°–∞—А–∞—В–Њ–≤: –Ш–Ј–і––≤–Њ –°–∞—А–∞—В–Њ–≤—Б–Ї–Њ–≥–Њ —Г–љ–—В–∞, 1992. – 176 —Б.
2. –Ш–Њ–љ–Њ–≤–∞ –Т.–У. –Я–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є–µ –∞—Б–њ–µ–Ї—В—Л –≥–µ–Љ–Њ—А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б—Б. –і–—А–∞ –Љ–µ–і. –љ–∞—Г–Ї. – –Ь., 1994. – 46 —Б.
3. –°—Г—Б–ї–Є–љ–∞ –Ч.–Р. –Ш—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є —Б–Є—Б—В–µ–Љ–∞ –њ—А–Њ—Б—В–∞–љ–Њ–Є–і–Њ–≤ (–Ї–ї–Є–љ–Є–Ї–Њ––±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ): –Ф–Є—Б—Б. –і–—А–∞ –Љ–µ–і. –љ–∞—Г–Ї. – –Ь., 1990. – 339 —Б.
4. –Ґ–∞–љ–∞—И—П–љ –Ь.–Ь. –Ш—И–µ–Љ–Є—З–µ—Б–Ї–Є–µ –Є–љ—Б—Г–ї—М—В—Л –Є –Њ—Б–љ–Њ–≤–љ—Л–µ —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –≥–µ–Љ–Њ—А–µ–Њ–ї–Њ–≥–Є–Є, –≥–µ–Љ–Њ—Б—В–∞–Ј–∞ –Є —Д–Є–±—А–Є–љ–Њ–ї–Є–Ј–∞: –Р–≤—В–Њ—А–µ—Д. –і–Є—Б—Б. –і–—А–∞ –Љ–µ–і. –љ–∞—Г–Ї. – –Ь., 1997. – 48 —Б.
5. –®–Љ–Є–і—В –Х.–Т. –Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ // –Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–њ–∞—В–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. – 1985. – вДЦ9. – –°. 1–6.
6. Antiplatelet Trialists’ Collaboration. Collaborativ–µ overview of randomised trialists of antiplatelet therapy – I. Prevention of death, myocardial infarction and stroke by prolonged antiplatelet therapy in various categories of patients // B. M. J. – 1994. – Vol. 308. – P. 81–106.
7. Born G. Aggregation of blood platelets by adenosine diphosphate and reversal // Nature. – 1962. – Vol. 194. – вДЦ9. – P. 927–929.
8. Backhaus C., Karkoutly C., Welsch M., Kriegstein J. A mouse model of focal cerebral ischemia for screening n–µuroprot–µctive drug effects // J. Pharmacol. Methods. – 1992. – Vol. 27. – P. 27–32.
9. O’Brien J.R. Variability in the aggregation of human platelets by adrenaline // Nature. – 1964. – Vol. 202. – P. 1188–1190.
10. Krieglstein J., Rischke R. Vinpocetine increases the neuroprotective effect of adenosine in vitro // Eur. J. Pharmacol. – 1991. – Vol. 205. – P. 7–10.
11. Molnar P., Erd S.L. Vinpocetine is as potent as phenytoin to block voltage–gated Na+ channels in rat cortical neurons // Eur. J. Pharmacol. – 1995. – Vol. 273. – P. 303–306.
12. Rischke R., Krieglstein J. Protective effects of vinpocetine against brain damage caused by focal or global cerebral ischemia. In: Krieglstein J., Oberpichler H., editor(s). Pharmacology of Cerebral Ischemia. – Stuttgart: Wissenschaftliche Veriagsgesellschaft, 1990. – P. 527–532.
13. Rischke R., Krieglstein J. Effects of vinpocetine on local cerebral blood flow and glucose utilization seven days after forebrain ischaemia in the rat // Pharmacology. – 1990. – Vol. 41. – P. 153–160.
14. Sauer D., Rischke R., Beck T. et al. Vinpocetine prevents ischemic cell damage in rat hippocampus // Life Sciences. – 1988. – Vol. 43. – P. 1733–1739.
15. Tamaki N., Kusunoki T., Matsumoto S. The effect of vinpocetine on cerebral blood flow in patients with cerebrovascular disorders // Ther. Hung. – 1985. – Vol. 33. – P. 13–21.












