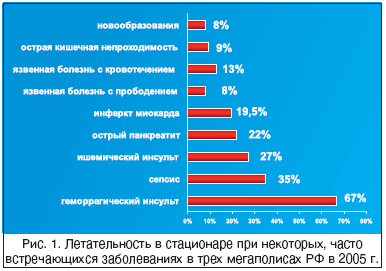
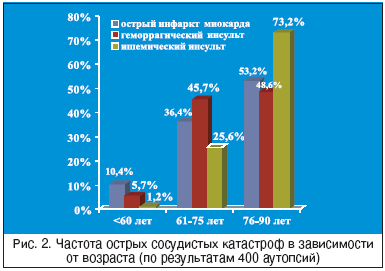
По нашим данным, частота летального мозгового инсульта увеличивается в 1,8–2,0 раза с каждым последующим десятилетием жизни (рис. 2). Инвалидизация после инсульта составляет 3,2 на 100 тыс. населения, а к труду возвращается не более 20% больных, перенесших инсульт, причем 1/3 заболевших – люди трудоспособного возраста. Среди всех видов инсульта преобладают ишемические поражения мозга.
Исследования острейшей стадии ишемического инсульта, проведенные в последние 2 десятилетия, показали отсутствие прямого тождества между острой фокальной церебральной ишемией, подразумевающей последовательность и потенциальную обратимость метаболических изменений в ткани мозга, и инфарктом мозга – сформировавшегося морфологического очага. Область мозга с наиболее значительным снижением кровотока (менее 10 мл/100 г в 1 мин.) становится необратимо поврежденной через 5–8 мин. после появления первых клинических симптомов, однако на протяжении нескольких часов по периферии этой зоны сохраняется ишемизированная, но живая ткань – пенумбра, или зона ишемической полутени. В этой зоне метаболизм сохранен на более низком уровне, присутствуют лишь функциональные изменения. Длительность существования этой области индивидуальна у каждого больного и определяет границы временного периода («терапевтическое окно»), в пределах которого проводимые лечебные мероприятия наиболее эффективны. На этом основании предложена схема (рис. 3) последовательных этапов «ишемического каскада» на основе их причинно–следственных связей и значимости для терапии: 1) снижение мозгового кровотока; 2) энергетический дефицит; 3) глутаматная «эксайтотоксичность»; 4) внутриклеточное накопление кальция; 5) активация внутриклеточных ферментов; 6) повышение синтеза окиси азота и развитие оксидантного стресса; 7) экспрессия генов раннего реагирования; 8) отдаленные последствия ишемии (реакция местного воспаления, микрососудистые нарушения, повреждения гематоэнцефалического барьера); 9) апоптоз.
В течение первых 3 часов с момента острого нарушения мозгового кровообращения максимально выражен энергетический дефицит в ишемизированной ткани, через 3–6 часов – глутаматная эксайтотоксичность, нарушения кальциевого гомеостаза и лактат–ацидоз, угасающие к концу 1–х суток. Отдаленные последствия ишемии начинают проявляться на 2–3–м часу, становятся максимальными через 12–36 часов (оксидантный стресс и локальное воспаление) и на 2–3–и сутки (апоптоз), но сохраняются длительно (в течение нескольких месяцев), способствуя в постинсультном периоде прогрессированию процессов атерогенеза и диффузного повреждения ткани головного мозга (энцефалопатии).
Каждый этап ишемического каскада является потенциальной мишенью для терапевтических воздействий, при этом чем раньше прерывается каскад, тем большего эффекта можно ожидать от терапии. В соответствии с имеющимися представлениями о развитии «ишемического каскада», в настоящее время выделяют 2 взаимодополняющих направления в ведении больных с ишемическим инсультом:
• максимально раннее восстановление кровотока (реперфузия)
• защита мозговой ткани от ишемического поражения (нейропротекция).
Улучшение перфузии ткани мозга воздействует на 1–й этап каскада, нейропротективная терапия – на 2–8–й его этапы (табл. 1).
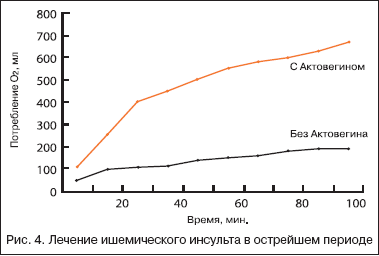
Поскольку проведение активной реперфузионной терапии возможно лишь в стационаре, после нейровизуализирующего исследования, позволяющего исключить геморрагический компонент поражения, оценить размеры ишемизированной области и патогенетический вариант инсульта, становится понятным преимущество другого направления терапии – нейропротекции (синонимы: цитопротекция, метаболическая защита мозга). Эта терапия может использоваться на догоспитальном этапе при появлении первых симптомов инсульта, даже при возможном геморрагическом его характере (рис. 4).
Улучшение перефузии ткани мозга:
• гемодилюция
• антиагрегантная терапия
• антикоагулянтная терапия гепарином
• плазма
• биореологические препараты
• rtPA – в первые 3 часа!
Нейропротективная терапия:
Противоишемические препараты:
• регуляторы аминацидергических систем (снижение эксайтотоксичности)
• антиоксиданты
• корректоры энергетического метаболизма
• нейротрофические и нейромодуляторные препараты
Нейропротективная терапия:
факты и перспективы
Основная цель нейропротективной терапии – сократить объем очага поражения ткани головного мозга при острых цереброваскулярных событиях и при хронической прогрессирующей энцефалопатии [Wahlgren NG, Ahmed N., 2004].
В «идеальном» варианте при остром инсульте цель нейропротекции заключается в предотвращении прогрессировании ишемического каскада, происходящего в клетках головного мозга. При хронической энцефалопатии – выживание клеток, в условиях хронической гипоксии.
Финалом патобиохимического каскада при острой ишемии, как и при хронической ситуации, является апоптоз клеток головного мозга, который происходит вследствие резкого энергетического дефицита клетки (рис. 3).
Таким образом, основная задача нейропротективной терапии – препятствие прогрессирующему энергетическому дефициту.
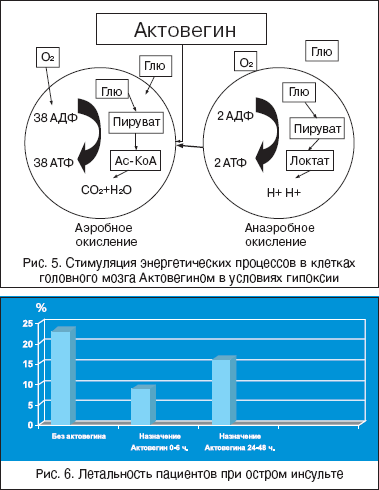
Центральный биохимический механизм энергетического дефицита клетки – это перестройка с аэробного пути окисления глюкозы (с выгодным количеством энергии) на анаэробный (с дефицитом энергии) (рис. 5).
Данные теоретические предпосылки определяют главное свойство нейропротективных препаратов – способствование активации аэробного пути окисления глюкозы.
Особенности применения нейропротекторов в раннем периоде инсульта заключаются в:
• увеличении доли транзиторных ишемических атак и «малых» инсультов среди острых нарушений мозгового кровообращения по ишемическому типу;
• значительном уменьшении размеров инфаркта мозга;
• удлинении периода «терапевтического окна», расширяющее возможности для тромболитической терапии;
• осуществлении защиты от реперфузионного повреждения.
Все нейропротекторы по своим фармакологическим особенностям разделены на следующие группы:
1) антагонисты глутамата и различных модуляторных участков глутаматных рецепторов (глицин, рилузол, лубелузол);
2) антагонисты кальция (нимодипин);
3) антиоксиданты и их предшественники (Актовегин, мексидол, эмоксипин, a–токоферол, карнозин, милдронат и др.);
4) ингибиторы ферментов (аллопуринол, тормозящий активность ксантинолоксидазы, депренил – ингибитор МАО–В, нитро–L–аргинин – блокатор NO–синтетазы);
5) энергокорректоры (Актовегин, реамберин, цитофлавин).
По результатам экспериментальных работ, проведенных на моделях острой фокальной ишемии, основным направлением первичной нейропротекции является прерывание быстрых механизмов глутамат–кальциевого каскада с целью коррекции дисбаланса возбуждающих и тормозных нейротрансмиттерных систем и активации естественных тормозных процессов. Этот вид нейропротекции должен быть начат с первых минут ишемии и продолжаться на протяжении первых 3 дней инсульта, особенно активно в первые 12 ч. Антагонисты NMDA–рецепторов были первыми нейропротективными препаратами, которые в экспериментальных условиях значительно (на 40–70%) ограничивали область инфаркта мозга, прежде всего за счет сохранения живой зоны «ишемической полутени». Блокада рецепторов может осуществляться конкурентными и неконкурентными антагонистами. Единственными безопасными и, по результатам второй фазы испытаний, эффективными неконкурентными антагонистами NMDA–рецепторов на сегодняшний день являются препараты магния, регулирующие кальциевый ток через вольтаж–чувствительные и агонист–зависимые каналы. Испытания магнезии при остром инсульте показали ее безопасность, отсутствие значимых побочных эффектов, снижение 30–дневной летальности на 10% (30% против 40% в контроле) и ранней летальности на 5,7%.
Естественным активатором тормозных нейротрансмиттерных систем является препарат глицин. Наряду с нейротрансмиттерным глицин также обладает общеметаболическим действием, связывает низкомолекулярные токсичные продукты (альдегиды, кетоны), в больших количествах образующиеся в процессе ишемии. Сублингвальное применение глицина в первые дни инсульта в дозе 20 мг/кг массы тела (в среднем 1–2 г/сут.) полностью безопасно и позволяет обеспечить противоишемическую защиту мозга у больных с различной локализацией сосудистого поражения и разной тяжестью состояния.
Большую значимость в развитии процессов ишемического повреждения ткани мозга имеет недостаточность трофического обеспечения. Уровень трофического обеспечения определяет альтернативный выбор между генетическими программами апоптоза и антиапоптозной защиты, влияет на механизмы некротических и репаративных процессов. Естественной защитной реакцией мозга в первые минуты ишемии является синтез трофических факторов и рецепторов к ним. При быстрой и активной экспрессии генов, кодирующих нейротрофины (факторы роста), ишемия мозга может длительно не приводить к инфарктным изменениям. В случае же формирования ишемического повреждения высокий уровень трофических факторов обеспечивает регресс неврологического дефицита даже при сохранении морфологического дефекта, его вызвавшего. Таким образом, важной стратегией вторичной нейропротекции является разработка и внедрение препаратов с выраженными нейротрофическими и ростовыми свойствами. Факторы роста, представляющие собой эндогенные полипептиды, являются идеальными претендентами для лечения инсульта, так как обладают нейропротективными, репаративными и пролиферативными свойствами.
Однако значительные размеры полипептидной молекулы нейротрофина не позволяют ему проникать через гематоэнцефалический барьер, что ограничивает возможности его терапевтического применения. Большое внимание уделяется изучению свойств низкомолекулярных нейропептидов. Эти соединения свободно проникают через гематоэнцефалический барьер, оказывают многостороннее действие на ЦНС и характеризуются высокой эффективностью и выраженной направленностью действия при условии их очень малой концентрации в организме.
В последние годы большое внимание было уделено изучению свойств нейропептидов, структурно связанных с адренокортикотропным гормоном (АКТГ). Было показано, что АКТГ–подобные пептиды влияют на текучесть синаптических мембран, модулируют рецепторные функции, воздействуя на процессы фосфорилирования белков, тормозят активацию микроглии и избыточный синтез нейротоксичных цитокинов и лигандов к NMDA–рецепторам, обладают самостоятельным нейротрофическим эффектом.
В РФ был создан синтетический аналог фрагмента АКТГ(4–10) – препарат семакс, представляющий собой гептапептид (Met–Glu–His–Phe–Pro–Gly–Pro), лишенный гормональной активности. Семакс является эндогенным регулятором функций ЦНС и обладает нейромодуляторной и нейротрофической активностью, а также выраженным ноотропным эффектом.
Проведенные клинико–иммунобиохимические исследования подтвердили сильное нейропротективное действие семакса, основными компонентами которого являются иммуномодуляция, торможение глиальных реакций воспаления, улучшение трофического обеспечения мозга, торможение синтеза оксида азота и других реакций оксидантного стресса.
В клинической практике РФ чаще всего используются следующие лекарственные препараты: Актовегин, церебролизин, эмоксипин и мексидол.
Эмоксипин – производное тригидроксипиридина, структурный аналог витамина В6. Основными эффектами эмоксипина являются торможение перекисного окисления липидов и активация антиоксидантной системы, изменение активности мембран–связанных ферментов, модификация метаболической, рецепторной и транспортной функций клеточных мембран. При его применении внутривенно (капельно по 15 мл 1% раствора в течение 10 дней, а затем внутримышечно по 5 мл 1% раствора в течение 14 дней) установлено его благоприятное действие на регресс неврологических нарушений и нормализацию паттерна ЭЭГ.
Отечественным антиоксидантом является мексидол – соль эмоксипина и янтарной кислоты. Препарат тормозит перекисное окисление липидов и свободнорадикальные процессы, увеличивает концентрацию восстановленной формы глутатиона, активирует эндогенную антиоксидантную систему супероксиддисмутазы и церулоплазмин, предупреждает снижение активности глутатион–зависимых ферментов (глутатионпероксидазы, глутатионредуктазы), в результате чего достоверно уменьшается выраженность процессов оксидантного стресса. Доклинические испытания продемонстрировали безопасность мексидола при применении его в суточной дозе до 100 мг/кг и эффективность препарата при разных вариантах церебральной гипоксии, в том числе циркуляторной гипоксии (ишемии).
Клиническая эффективность мексидола проявляется регрессом общемозговых нарушений (в том числе расстройств сознания) и значимо более быстрым, по сравнению с группой плацебо, восстановлением двигательных функций, редукцией признаков вазомоторной нестабильности.
Широко известный и много десятилетий используемый в России и странах СНГ препарат церебролизин – водный раствор освобожденного от белка гидролизата мозга (активная фракция представлена пептидами, молекулярный вес которых не превышает 10 000 дальтон), стандартно входит в курс лечения больных с острыми нарушениями мозгового кровообращения. Дозировка препарата в продолжение последних 5–7 лет постепенно увеличивалась с 1 мл внутримышечно до 20–30 мл внутривенно, в последних фармакологических справочниках указывается однократная дозировка 60 мл церебролизина внутривенно. Можно отметить, что такие большие различия в дозировке не могут давать объективную картину клинической и фармакологической эффективности препарата.
Многочисленные и крайне разноречивые литературные данные не позволяют до настоящего времени сделать однозначные выводы о клинической эффективности препарата, несмотря на прекрасные экспериментальные данные о возможностях нейропротекции и стимуляции дифференциации нейронов, поддержании их жизнедеятельности в процессе старения, приостановке процессов нейродегенерации, улучшении когнитивных функций.
В рандомизированном двойном слепом плацебо–контролируемом исследовании [Ladurner G, Kalvach P, Moessler H., 2005] эффективности церебролизина в терапии инсульта также не показано никаких преимуществ препарата перед плацебо.
Особое место среди нейропротекторов принадлежит Актовегину (высокоочищенный гемодиализат, вырабатываемый из телячьей крови). Помимо неорганических электролитов и других микроэлементов, он содержит 30% органических веществ (олигопептиды, аминокислоты, нуклеозиды, промежуточные продукты углеводного и жирового обмена, липиды, олигосахариды). Молекулярная масса органических соединений составляет менее 5000 Да. В растворе Актовегина содержится значительное количество незаменимых микро– и макроэлементов – натрий, фосфор, кальций, магний, медь и др. Данный факт представляет особый интерес, т.к. многие из этих микроэлементов являются каталитическими центрами различных ферментов головного мозга. Помимо этого, входящий в состав Актовегина магний является нейроседативным ионом (табл. 2).
По современным представлениям Актовегин оказывает выраженное антигипоксическое действие за счет следующих механизмов:
1. Прямое инсулиноподобное действие, приводящее к усилению транспорта глюкозы внутрь клеток. Как было показано в экспериментальных исследованиях, инозитолфосфатолигосахариды, входящие в состав Актовегина, повышают транспорт 3–0–метилглюкозы в клетки в 5 раз.
2. Активизация ферментов, катализирующих реакции гликолиза и окислительного фосфорилирования, таких как пируватдегидрогеназа, сукцинатдегидрогеназа, цитохром–С–оксидаза.
Под влиянием Актовегина значительно улучшается диффузия и утилизация кислорода как в нейрональных структурах, так и в клетках организма в целом, прежде всего в альвеолярной системе легких. Это значительно улучшает оксигенацию во всей микроциркулярной системе, в коже, а также в слизистых оболочках желудочно–кишечного тракта, что позволяет уменьшить выраженность вторичных трофических расстройств, и особенно важно у больных с обширными ишемическими и диффузными гипоксическими повреждениями мозга. Под действием Актовегина в клетках значительно повышается обмен высокоэнергетических фосфатов, прежде всего АТФ, повышается устойчивость церебральных структур к гипоксии, уменьшается выраженность диффузных постишемических повреждений.
Помимо антигипоксического действия, Актовегин обладает свойствами мощного непрямого антиоксиданта, реализующимися благодаря активации ключевого фермента эндогенной антиоксидантной системы – супероксиддисмутазы. К настоящему времени антигипоксический и антиоксидантный эффекты Актовегина были подробно исследованы.
В серии лабораторных и клинических тестов было установлено, что под влиянием Актовегина:
• усиливается транспорт глюкозы через биологические мембраны в условиях гипоксического повреждения культуры клеток;
• увеличивается эффективность потребления кислорода клетками в условиях гипоксии (рис. 5);
• увеличивается интенсивность аэробного гликолиза и окислительного фосфорилирования в культуре клеток, подвергшихся гипоксии;
• значительно повышается энергетический статус ишемизированных клеток;
• улучшается утилизация кислых продуктов обмена (лактата), нормализуется кислотность и уменьшается отек тканей
• обеспечивается блокада перекисного окисления липидов в биологических мембранах;
• обеспечиваются мембрано– и цитопротекторный эффекты за счет сохранения массопереноса;
• происходит «включение» субстратов препарата в химические синтезы;
• наблюдается эндотелиотропное и ангиопротекторное действие, улучшается мироциркуляция, повышается пролиферация фибробластов и активность макрофагов;
• отмечается увеличение синтеза коллагена;
• осуществляется системное противоишемическое действие и устраняется гипоперфузия органов без отрицательного влияния на системную гемодинамику;
• сохраняется активность антиоксидантных систем на клинической модели острого инфаркта миокарда.
Актовегин, действуя как комплексный (нейротропный и системный) активатор метаболизма, обладающий выраженным органопротекторным и иммуномодулирующим действием, позволяет осуществлять комплексную защиту организма в условиях ишемии и гипоксии, стабилизировать церебральный кровоток на основе поддержания системного кровообращения и адекватного функционирования основных буферных систем организма.
Таким образом, Актовегин является единственным истинным антигипоксическим препаратом, улучшающим энергетический обмен ишемизированных нервных клеток и позволяющим предотвратить развитие всего каскада ишемического повреждения. Помимо этого, неоспоримыми преимуществами Актовегина являются: универсальный органонеспецифический механизм противоишемического действия, большое количество форм выпуска, практически полное отсутствие противопоказаний и побочных эффектов при применении при различных нозологиях у разных групп пациентов.
Накоплен большой клинический опыт применения Актовегина.
Так, в исследованиях Румянцевой С.А. и соавт. (2003), продемонстрировано значительное снижение летальности пациентов, получающих Актовегин при остром инсульте, особенно при назначении препарата в первые 6 часов заболевания (рис. 6).
В работах van Alberta (1983), показано снижение летальности на 8,7% у пожилых пациентов при назначении Актовегина при остром инсульте.
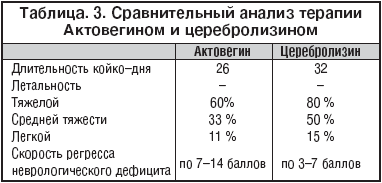
В других работах Румянцевой С.А. показаны преимущества применения Актовегина у больных старше 70 лет с ишемическим инсультом по сравнению с церебролизином. Они заключались в снижении летальности, сокращении длительности пребывания больных в стационаре, активации состояния сознания и скорости регресса очаговых неврологических симптомов при средней и легкой степени тяжести инсульта (табл. 3). Также в данном исследовании было продемонстрировано, что в большинстве случаев под воздействием Актовегина отмечалась активация энергетического метаболизма головного мозга в виде активации суммарной мощности спектров ЭЭГ и активации a–ритма и медленных волн. В случаях применения церебролизина указанных реакций не отмечалось.
Проведенное нами клиническое исследование эффективности терапии инсульта при включении Актовегина в комплексную терапию также продемонстрировало снижение летальности и большую регрессию неврологического дефицита, по сравнению с группой контроля.
Оценивалась динамика восстановления витальных функций, степени функциональных нарушений к 14 суткам от развития нарушения мозгового кровообращения, общей длительности пребывания в стационаре, тяжести исходов заболевания и частоты соматических осложнений. Первая доза: раствор Актовегина для инъекций – 10 мл (400 мг), вводили в/в струйно вводился врачами скорой помощи, в стационаре продолжали ежедневные инфузии раствора Актовегина в течение 14 дней. В результате лечения через 2 недели у большего числа пациентов в группе Актовегина по сравнению с группой контроля нормализовалось общее состояние (табл. 4).
При оценке функционального статуса пациентов в соответствии со шкалой Бартел в группе Актовегина оказалось достоверно большее число пациентов с индексом в пределах 75–100 баллов, то есть больных, практически полностью восстановивших свои функциональные возможности, по сравнению с группой контроля (табл. 5).
Результаты тестирования по шкале Бартел в целом подтвердились при клинической оценке исхода острого нарушения мозгового кровообращения лечащим врачом (табл. 6). Так, полное восстановление функций и нормализация неврологического статуса произошли у 45% пациентов в группе Актовегина, в отличие от 25% случаев в группе сравнения (p<0,05).
Таким образом, применение Актовегина для фармакотерапии острого инсульта более эффективно, чем традиционно принятое ведение, и способствует значимо лучшему восстановлению неврологических функций к 14–м суткам заболевания.
Другим перспективным препаратом для использования при острых и хронических нарушениях мозгового кровообращения является кортексин. Кортексин представляет собой лиофилизат, полученный путем уксуснокислой экстракции из коры головного мозга крупного рогатого скота или свиней, содержащий низкомолекулярные активные нейропептиды, молекулярный вес которых не превышает 10 000 дальтон, достаточный для проникновения через ГЭБ.
Кортексин обладает тканеспецифическим многофункциональным действием на головной мозг, что проявляется в метаболической регуляции, нейропротекции, функциональной нейромодуляции, нейротрофической активности, улучшении внутриклеточного синтеза белка.
Кортексин регулирует процессы перекисного окисления липидов в клетках головного мозга, снижает образование свободных радикалов, блокирует процессы свободнорадикального окисления. Препарат устраняет дисбаланс тормозных и возбуждающих аминокислот, обладает умеренным GABA–ергическим действием.
Препарат оказывает положительное действие при нарушении когнитивных функций, улучшает концентрацию внимания, кратковременную память, способность к обучению, ускоряет восстановление функций головного мозга после стрессорных воздействий, регулирует уровень серотонина и допамина. Стимулирует процесс умственной деятельности, не оказывая избыточного активирующего влияния, восстанавливает биоэлектрическую активность головного мозга. Кортексин также стимулирует репаративные процессы в головном мозге.
В клинике внутренних болезней широко используются и ряд других препаратов, обладающим цитопротективным эффектом в условиях ишемии. Одним из них является милдронат, нашедший свое место прежде всего в комплексном лечении ишемической болезни сердца. Милдронат оказывает оптимизирующее действие на процессы окисления жирных кислот, что предотвращает накопление их токсичных недоокисленных остатков в кардиомиоцитах, находящихся в состоянии ишемии. Однако ввиду особенностей энергетического метаболизма нервных клеток, не использующих жирные кислоты в качестве субстрата окисления, милдронат не может быть рекомендован для применения при различных цереброваскулярных заболеваниях из–за отсутствия точек приложения своего действия.
В целом сравнительный анализ данной группы препаратов (табл. 7) показал, что наиболее изученными нейропротекторами являются Актовегин и церебролизин.
Однако в связи со своим механизмом комплексного антиишемического, нейропротективного действия особую актуальность приобретает Актовегин – препарат, объединяющий все терапевтические возможности влияния на поврежденную ткань мозга. При этом большее число положительных доказательств в отношении клинической эффективности в комплексной терапии цереброваскулярных заболеваний также имеет Актовегин, а его эффективность показана как для острых цереброваскулярных событий, так и хронических.
Ряд дополнительных преимуществ Актовегина, экономическая составляющая и стандартизация доз препарата позволяют рекомендовать его широкому кругу пациентов. Именно поэтому Актовегин вошел в стандарт медицинской помощи при инсульте на догоспитальном этапе. Стандарт был утвержден приказом № 643 Минсоцздравразвития от 5 сентября 2006 года. Скорейшее его внедрение в практику позволит уменьшить летальность в остром периоде заболевания и повысить эффективность реабилитационных мероприятий.