В настоящее время существует ряд инструментальных методик, позволяющих оценить структурное и функциональное состояние головного мозга. К ним относятся ангиографические, компьютерно–томографические и магнитно–резонансные методы и их модификации. Необходимо указать на трудоемкость, дороговизну и небезопасность проведения этих методик у ургентных больных.
Под нашим наблюдением находилось 426 пациентов в различных стационарах г. Москвы. Больных с инсультом было 279, из них с инфарктом мозга 187, с внутримозговым кровоизлияниям – 38, с субарахноидальным кровоизлиянием – 54.
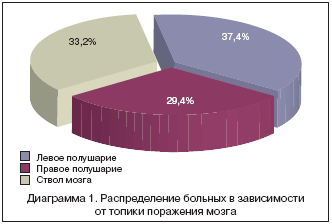
Большинство больных с инфарктом мозга различной топики наблюдалось на базе ГКБ № 6. 59,2% всех больных были с ишемическим поражением; средний возраст 57,85±7,61 года; летальность в этой группе составила 41,2% (диагр. 1).
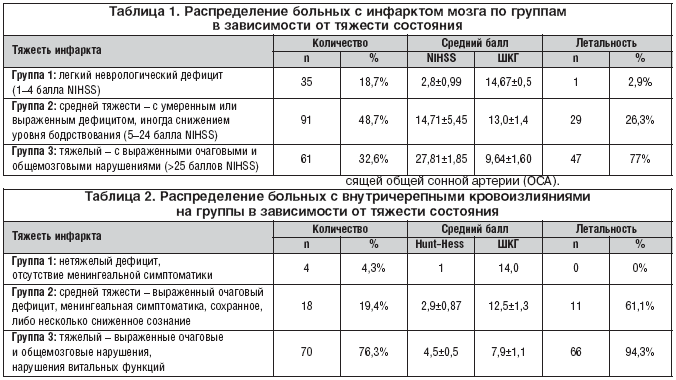
Распределение больных с инфарктом мозга в зависимости от тяжести состояния представлено в таблице 1.
Средний возраст в группе больных с геморрагическим инсультом – 49,3±6,8 года.
Обследовано 92 пациента, из них:
– с внутримозговым кровоизлиянием на базе ГКБ № 6 – 71%, летальность – 73,7%;
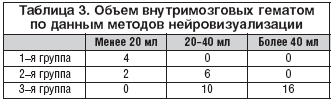
– с субарахноидальным кровоизлиянием – 42,6%, летальность 90,7%. Распределение больных с геморрагическим инсультом по тяжести состояния и по объему внутримозговой гематомы представлены в таблицах 2 и 3.
Среди больных преобладали пациенты с тяжелым или средне–тяжелым состоянием при поступлении.
Необходимо отметить, что столь высокие цифры летальности при инсульте обусловлены спецификой работы в условиях отделений реанимации, нейрореанимации, нейрохирургической реанимации, где находится наиболее тяжелый контингент больных. К примеру, летальность в группах легкого и средне–тяжелого течения инфаркта составила 2,9 и 26,9% соответственно.
Следует также уточнить, что пациенты, осмотренные в других стационарах г. Москвы, – а это НИИ СП, б–ца им. Боткина, ГКБ №№ 1, 7, 13, 15, 24, 33, 36, 57, 64 и др., – в рамках работы МНДБ, как правило находились в состоянии комы не менее II степени.
Всем 426 больным выполнена Эхо–Эс и Эхо–Пг, УЗДГ и ТКД, большинству в динамике; ДС выполнена 268 пациентам, ТТГ – 300, ЦО – 263, ЭЭГ – 236, БИМ – 291 пациенту.
Исследование ауторегуляции проведено 296 пациентам.
Исследования проводились при поступлении, а далее на 2–е, 3–и, 4–е, 5–е, 7–е, 14–е, 21–е сут. заболевания, а также при изменении состояния в ту или иную сторону, поэтому общее количество проведенных процедур подсчитать трудно. В течение 1–х сут. всем больным проводился мониторинг ТКД, ЦО, БИМ. Мониторинг ЭЭГ проводился при работе в рамках протокола констатации смерти мозга.
В результате клинико–инструментального мониторинга получены следующие данные.
Ишемический инсульт
При инфаркте головного мозга, обусловленном стеноокклюзирующим процессом в сонных или позвоночных артериях, чрезвычайно информативен метод дуплексного сканирования, позволяющий визуализировать строение сосудистой стенки, обычное или атипичное расположение сосуда, его извитость или гипоплазию, уровень и симметрию каротидных бифуркаций, наличие или отсутствие клапанов яремных вен, диаметры продольного и поперечного сечения магистральных артерий головы (МАГ), атеросклеротические включения или тромбы – от начальных проявлений уплотнения сосудистой стенки до окклюзирующих поражений с подробной характеристикой атероматозных бляшек сонных и/или позвоночных артерий с регистрацией объемного кровотока по МАГ. Основными диагностическими критериями при этом служат:
– гемодинамическая значимость стеноза – определение процента стеноза по площади поперечного сечения и по диаметру сосуда;
– эмбологенность атеросклеротической бляшки – определяется ее структурой, равномерной или разрыхленной поверхностью, степенью спаянности с подлежащими тканями.
Атеросклеротические бляшки, стеноз внутренних сонных артерий (ВСА) более чем на 70%, являются гемодинамически значимыми, что подтверждается явным падением линейной скорости кровотока (ЛСК) по гомолатеральной средней мозговой артерии (СМА) на фоне снижения объемной скорости кровотока в приносящей общей сонной артерии (ОСА).
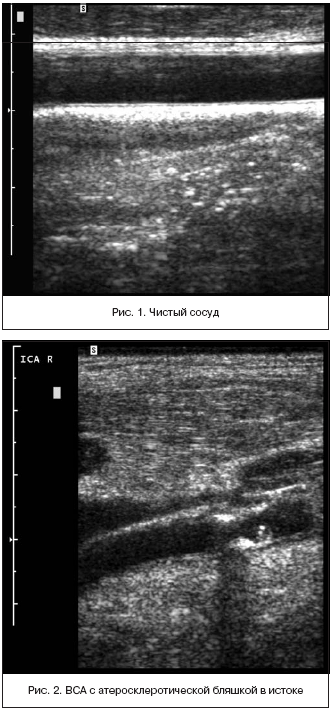
При этом наиболее частыми являются гетерогенные плотные атеросклеротические бляшки, гомогенные мягкие наблюдаются реже (рис. 1 и 2); они могут явиться источником церебральных микроэмболов, которые характеризуются значительно большей частотой при мягких «нестабильных» с изъязвлениями и кровоизлияниями, чем при плотных кальцифицированных.
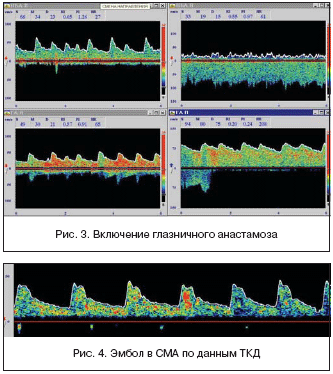
В наблюдениях, где имеется гомолатеральная окклюзия в истоке ВСА, наружная сонная артерия (НСА) зачастую становится основной коллатералью для глазничной артерии (ГА) (рис. 3). Поток по ней резко усиливается, появляется высокоамплитудный свистящий сигнал, т.е. регистрируется доплерограмма периферической артерии. В последствии обязательным является изменение направления потока в ГА на ретроградный, что четко подтверждается компрессией ветвей шунтирующей кровь НСА – пережатие ипсилатеральной височной и/или подчелюстной артерии, ослабляет или вовсе прекращает регистрацию потока по ГА. Эти изменения достаточно просто регистрируются при УЗДГ.
УЗ–методы чрезвычайно информативны при выявлении разных подтипов инсульта. Так, при выраженных сочетанных сужениях истоков сонных и/или позвоночных артерий (ПА) более 70% просвета ДС регистрирует субкритические параметры церебральной перфузии вкупе с грубыми стенозами проксимальных сегментов ВСА и /или ПА. Тотальный мозговой кровоток с нормальных 700 мл/мин. падает до 350–210 мл/мин. Это характерно для развития инсультов по типу сосудисто–мозговой недостаточности, особенно при снижении артериального давления.
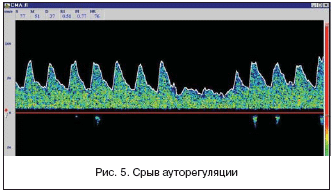
Иное дело эмболический генез инсульта (рис. 4). При нем решающую роль играет не столько степень сужения приносящей артерии, сколько наличие в ее стенке изъязвившихся эмбологенных атером.
При таких формах ОНМК прекрасный диагностический тандем – ДС и ТКД–мониторинг. На этапе церебральной васкуляризации ДС определяет наличие, сторонность, толщину, строение и, главное, характер поверхности атеросклеротической бляшки. Если она является источником эмболий, то мониторинг гомолатеральной СМА позволяет подтвердить наличие, частоту и даже вероятный субстрат эмбола. Следует помнить о том, что в ряде подобных ситуаций, особенно сочетающихся с нарушением сердечного ритма, необходимо иметь в виду возможность кардиальной эмболии.
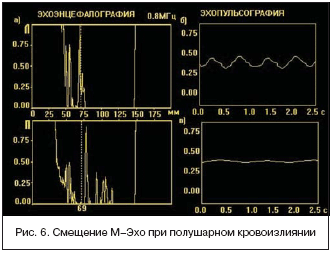
Следует отметить, что нарушения ауторегуляции наблюдались нами не только при патологических паттернах, свидетельствующих о нарушениях регионарной перфузии либо вследствие стено–окклюзирующего поражения, отека мозга, либо вследствие реканализации (рис. 5). Подобные явления мы отмечали и при магистральном потоке, что может свидетельствовать о сохраняющихся циркуляторных нарушениях в очаге поражения.
При повторных исследованиях: в 1–й группе сохранялись подобные значения индексов в течение всего острого периода инфаркта. Клинически здесь отмечался положительный эффект в виде снижения дефицита до 1–2 баллов у 15 больных. У 13 больных сохранялся стойкий неврологический дефицит прежней степени. Это больные с лакунарными инфарктами, поражением функционально значимых зон. Таким образом, в данной группе несмотря на отсутствие или негрубое нарушение коэффициента ауторегуляции наличие паттерна нормального магистрального кровотока нельзя с уверенностью констатировать функциональный исход инфаркта по данным ТКД.
Во 2–й группе при наличии положительной динамики, увеличении ЛСК в зоне инфаркта к 5–7–м сут. отмечалось увеличение реактивности до нормальных значений на интактной стороне. На стороне поражения показатели ауторегуляции оставались нарушенными, однако указанные изменения становились менее выраженными (КА до 0,87). При отсутствии восстановления нарушения ауторегуляции, как правило, сохранялись в той же степени. При отрицательной динамике отмечалось нарастание нарушений ауторегуляции наряду со снижением ЛСК, увеличением индексов периферического сопротивления.
В 3–й группе отмечались грубые нарушения ауторегуляции, а в случае положительной динамики – уменьшение выраженности ауторегуляторных нарушений на интактной стороне.
Следует отметить, что более выраженные нарушения ауторегуляции на стороне поражения во 2–й и 3–й группах могут быть связаны не только с объемами очага поражения и зоны перифокального отека, но и более грубым стеноокклюзирующим поражением, снижением церебрального перфузионного резерва (ЦПР).
Смещение срединных структур при проведении Эхо–Эс у больных с инфарктом головного мозга, без признаков стено–окклюзирующего поражения МАГ выявлялось достаточно редко, не превышало 3 мм, соответствовало ухудшению клинической картины, развивалось преимущественно на 3–5–е сут. заболевания. При продолженном тромбозе сонной артерии, особенно при разобщении Виллизиева круга, выявлялась равномерная дислокация, распространяющаяся как на передние (прозрачная перегородка), так и на задние (III желудочек, эпифиз) отделы М–Эха. Особое значение в оценке данных Эхо–Эс имеет время проведения исследования. По нашим данным, в единичных случаях дислокация срединных структур возникала через несколько часов, значительно чаще – на 3–4–е сут. заболевания. Особенно грозным прогностическим признаком являлось появление и увеличение дислокации срединных структур в сочетании с падением сатурации и увеличением индекса термодинамического потенциала. Указанное сочетание результатов нейрофизиологического мониторинга свидетельствовало о наступлении грозных неврологических осложнений в виде развития и усугубления отека мозга, развития вторичных ишемических нарушений.
Пациенты с геморрагическим инсультом
Ранжируя значение УЗ– и Т–приемов в диагностике и курации больных с геморрагическим инсультом, мы остановились на следующем.
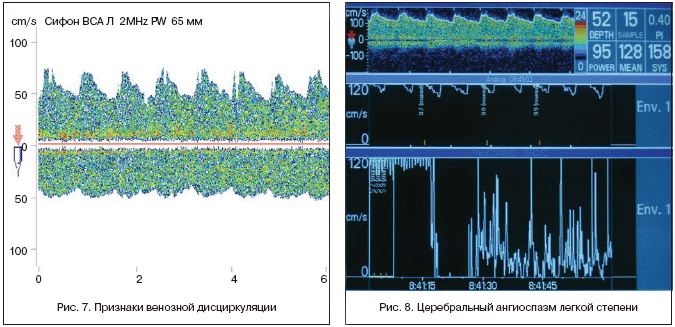
1. Наиболее значимым является метод Эхо–Эс, позволяющий уже в первые минуты поступления пациента на уровне приемного отделения, или даже в машине СМП, заподозрить наличие острого объемного поражения головного мозга, и на раннем этапе спланировать возможную тактику ведения пациента (рис. 6). При полушарных геморрагиях с дислокацией срединных структур менее 4 мм прогноз, как правило, благоприятный. При увеличении смещения М–Эхо более 6 мм в 97% случаев заболевание закончилось летально. При стволовых локализациях кровоизлияния смещение М–Эхо возникает достаточно редко и не превышает 2 мм. Основными косвенными признаками вероятного субтенториального поражения являлись резкое расширение основания сигнала от III желудочка, расщепление вершины М–Эха, в сочетании с гипертрофированными сигналами от бокового желудочка, ундулирующая пульсация стенок III желудочка.
2. Менее значимым является комплекс доплерографических методик. При ДС и УЗДГ показатели ЛСК по МАГ были несколько выше, чем у группы больных с инфарктами. Значительно ярче проявлялись признаки венозной дисциркуляции по глазничным и яремным венам, соответствующие стороне поражения (рис. 7). При ТКД в 40,2% случаев регистрировался односторонний, а в 30,4% – 2–сторонний паттерн затрудненной перфузии. Еще в 58,6% регистрировалось усиление скоростей по базальным венам до 20–25 см/с.
Незаменимым и едва ли не единственным прижизненным способом распознавания церебрального спазма является использование ТКД (рис. 8).
Данное исследование чрезвычайно полезно для выбора тактики консервативного или оперативного лечения, прогноза субарахноидального кровоизлияния (САК). У 63,2% больных с САК и 42,1% больных с внутримозговым кровоизлиянием (ВМК) зафиксированы доплерографические признаки ангиоспазма, причем более выраженными они были в группе больных с САК.
3. Динамика показателей ТТГ, ЦО и БИМ мало отличалась от параметров в группе больных с инфарктом мозга и коррелировала только с тяжестью состояния и, соответственно, со степенью выраженности осложнений основного заболевания. Следует лишь отметить, что при корпоральной ТТГ у больных с правополушарной локализацией геморрагии со стороны парализованных конечностей термоасимметрия была на 0,1–0,3 °С выше, чем у больных с инфарктом мозга. Продольный термальный градиент был значительно большим у больных с ВМК в правое полушарие – до 0,5 °С, при 0,3 °С у больных с поражением левого полушария.
Что касается медикаментозной терапии инсульта, важно выбирать те лекарственные препараты, которые оказывают выраженный терапевтический эффект, ускоряют восстановительную динамику, и чье применение обосновано с точки зрения фармакоэкономики. Примером такого препарата является Мексидол, применяемый в нашей стране в течение уже 10 лет. Обладая антигипоксическим, антиоксидантным, нейропректорным действием, Мексидол незаменим в условиях лечения в неврологической клинике, поскольку является эффективным как при ишемическом, так и при геморрагическом инсульте. Это немаловажно в условиях недифференцированной терапии, когда определение характера инсульта требует дополнительных методов нейровизуализации. Кроме того, данный вопрос требует решения в кратчайшие сроки. Известно, что наиболее эффективным при лечении острого ишемического инсульта для определения его этиологии является тромболизис. Однако в условиях современной российской медицины эта процедура является малореальной: при отсутствии круглосуточных и неоднократных для одного пациента нейровизуализационных методов исследования данный метод лечения становится практически неприменим. Следует отметить, что Мексидол продемонстрировал высокую эффективность при лечении пациентов с острым ишемическим инсультом, согласно результатам двойного слепого плацебо–контролируемого исследования (В.И. Скворцова и соавт., 2006). Было установлено, что максимально раннее начало лечения (желательно – в первые часы от момента развития инсульта) достоверно ускоряет восстановительную динамику и улучшает исход заболевания.
В лечении геморрагического инсульта приоритетен нейрохирургичекий метод. Следовательно, использование препаратов, обладающих недифферинцированным действием (а Мексидол совершенно неоспоримо является таким препаратом), даже в условиях специализированного стационара выходит на первый план.
Необходимость тщательного мультифакториального мониторинга в остром периоде любой церебральной катастрофы в настоящее время не вызывает сомнения, причем с целью не только теоретической – исследование различных патологических изменений, происходящих в динамике заболевания. На настоящем этапе развития медицины, когда лечение становится более интенсивным, интервенционным, нейромониторинг необходим для более точного и дифференцированного подхода к терапии, фармакологической или хирургической, определения риска различных вмешательств, оценки прогноза заболевания. При комплексном подходе различные методики мониторинга дополняют друг друга, повышая точность исследования. Необходимо отметить, что при любом варианте инсульта использование Мексидола в качестве препарата первого выбора абсолютно оправданно.
Литература
1. Гусев Е.И., Коновалов А.Н., Беляков В.В. и др. Методы исследования в неврологии и нейрохирургии. – М.: Нолидж, 2000. – 330 с.
2. Карлов В.А., Стулин И.Д., Богин Ю.Н. Ультразвуковая и тепловизионная диагностика сосудистых поражений нервной системы. – М.: Медицина, 1986. – 260 с.
3. Кунцевич Г.И. Ультразвуковые методы исследования магистральных артерий шеи и артерий виллизиева круга // Методы исследования в неврологии и нейрохирургии; под ред. Е.И. Гусева. – М.: Нолидж, 2000. – С. 145–209.
4. Лелюк В.Г., Лелюк С.Э. Ультразвуковая ангиология. – М.: Реальное время, 2003. – 322 с.
5. Никитин Ю.М., Труханов А.И., Агаджанова Л.П., и др. Ультразвуковая доплерографичекая диагностика сосудистых заболеваний. – М.: ВИДАР, 1998. – 432 с.
6. Патология сонных артерий и проблема ишемического инсульта. Клинические, ультразвуковые и гемодинамические аспеты / Под. ред. Д.Н. Джибладзе. М., 2002. 207 с.
7. Подлеснова Е.Ю. Анатомические и функциональные состовляющие церебровасклярного резерва у больных инсультом // Журнал неврологии и психиатрии им. С.С.Корсакова, – 2003 г. – Вып. № 9 – с. 152.
8. Свистов Д.В. Доплерографическая оценка ауторегуляции кровоснабжения головного мозга в норме и при нейрохирургической патологии // Современные подходы к лечению нервных и психических заболеваний. – СПб. – 2000. – с. 330.
9. Скворцова В.И., Стаховская Л.В., Нарциссов Я.Р. и соавт. Рандомизированное двойное слепое плацебо–контролируемое исследование эффективности и безопасности мексидола в комплексной терапии ишемического инсульта в остром периоде. Журнал им. С.К Корсакова. 2006; 18: 52–59.
10. Стулин И.Д., Мусин Р.С., Сурикова И.Л. и др. Роль инструментального мониторинга в диагностике и прогнозировании ОНМК // Журнал неврологии и психиатрии им. С.С.Корсакова, выпуск 9, приложение к журналу 2003, с.154.
11. Суслина З.А., Верещагин Н.В., Пирадов М.А. Подтипы ишемических нарушений мозгового кровообращения: диагностика и лечение // Консилиум медикум. – 2001. – Т. 3. – №5. – С. 221–227.
12. Шахнович А.Р., Шахнович В.А. Диагностика нарушений мозгового кровообращения. Транскраниальная допплерография. М., АСТК 1996. 436 с.
13. Шахнович В.А. Ишемия мозга: Нейросонология. М.: АСТК, 2002. 298 с.
14. Шевченко Ю.Л., Одинак М.М., Кузнецов А.Н., Ерофеев А.А. Кардиогенный и ангиогенный церебральный эмболический инсульт. М., «Гэотар–Медиа», 2006, 270 с.
15. Akopov S., Whitman G.T. Hemodynamic Studies in Early Ischemic Stroke Serial Transcranial Doppler and Magnetic Resonance Angiography Evaluation // Stroke. 2002;33:1274–1279.
16. Alexandrov AV, Demchuk AM, Wein TH, Grotta JC. Yield of Transcranial Doppler in acute cerebral ischemia. Stroke 1999;30:1604–1609.
17. Barrett K.M, Ackerman R.H., Gahn G., Romero J.M., Candia M. Basilar and middle cerebral artery reserve: a comparative study using transcranial Doppler and breath–holding techniques. Stroke. 2001;32:2793–2796.
18. Chernyshev O.Y., Garami Z., Calleja S., Song J., Campbell M.S., Noser E.A., Shaltoni H., Chin–I Chen, Iguchi Y., Grotta J.C., Alexandrov A.V. Yield and Accuracy of Urgent Combined Carotid/Transcranial Ultrasound Testing in Acute Cerebral Ischemia//Stroke. 2005;36:32.












