–Ъ.–Љ.–љ. –Р.–Т. –Ь–Њ—Б–Ї–≤–Є–љ
–Э–∞—Г—З–љ–Њ-–Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—М—Б–Ї–Є–є —Ж–µ–љ—В—А —Б–Є—Б—В–µ–Љ–љ—Л—Е –њ—Б–Є—Е–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–є, –Ь–Њ—Б–Ї–≤–∞–Ґ–µ—А–Љ–Є–љ «–њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞» –Њ–±—К–µ–і–Є–љ—П–µ—В –Љ–љ–Њ–ґ–µ—Б—В–≤–Њ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, —Б–∞–Љ—Л–Љ–Є —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ–Є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —П–≤–ї—П—О—В—Б—П —В—А–µ–≤–Њ–≥–∞, —З—Г–≤—Б—В–≤–Њ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –љ–∞–њ—А—П–ґ–µ–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є—П —Б–љ–∞, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, –љ–µ–∞–і–µ–Ї–≤–∞—В–љ—Л–µ –Є —А–∞–Ј–љ—Л–µ –њ–Њ –Љ–Њ–і–∞–ї—М–љ–Њ—Б—В–Є —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є. –Э–µ—А–µ–і–Ї–Њ –≤—Б—В—А–µ—З–∞—О—В—Б—П –Є —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–µ –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–µ –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ – —Д–Њ–±–Є–Є, –њ–∞–љ–Є—З–µ—Б–Ї–Є–µ –∞—В–∞–Ї–Є.
–Ю–њ–Є—Б–∞–љ–Є–µ –њ–Њ–і–Њ–±–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–µ–Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ —Е—Г–і–Њ–ґ–µ—Б—В–≤–µ–љ–љ–Њ–є –Є –Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –ї–Є—В–µ—А–∞—В—Г—А–µ –≤ —В–µ—З–µ–љ–Є–µ –Љ–љ–Њ–≥–Є—Е —Б—В–Њ–ї–µ—В–Є–є. –Ґ–∞–Ї, —Г–ґ–µ –≤ 1894 –≥–Њ–і—Г –Ч. –§—А–µ–є–і –≤ —А–∞–±–Њ—В–µ «–Ю–њ—А–∞–≤–і–∞–љ–Є–µ –Њ—В–і–µ–ї–µ–љ–Є—П –Њ—В –љ–µ–≤—А–∞—Б—В–µ–љ–Є–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤: —В—А–µ–≤–Њ–ґ–љ—Л–µ –љ–µ–≤—А–Њ–Ј—Л» —Г–Ї–∞–Ј—Л–≤–∞–ї –љ–∞ —Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —Г–Ї–∞–Ј—Л–≤–∞—П, —З—В–Њ —В—А–µ–≤–Њ–≥–∞ –Є –њ–∞–љ–Є–Ї–∞, –Ї–∞–Ї –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П —Б—В–µ–њ–µ–љ—М –µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є, –Љ–Њ–≥—Г—В –±—Л—В—М –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ—Л —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ –Њ–і–љ–Њ–є –Є–ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Д—Г–љ–Ї—Ж–Є–є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞. –Я—А–Є —Н—В–Њ–Љ –њ–∞—Ж–Є–µ–љ—В –Љ–Њ–ґ–µ—В –Њ—Й—Г—Й–∞—В—М —Б–µ—А–і—Ж–µ–±–Є–µ–љ–Є–µ, —Б–ґ–∞—В–Є–µ –≥–Њ—А–ї–∞, –Њ—Й—Г—Й–µ–љ–Є–µ –љ–µ—Е–≤–∞—В–Ї–Є –≤–Њ–Ј–і—Г—Е–∞, –±–Њ–ї–Є –≤ –Њ–±–ї–∞—Б—В–Є —Б–µ—А–і—Ж–∞ –Є —В–∞–Ї –і–∞–ї–µ–µ. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ–Њ–ґ–љ–Њ –љ–∞–±–ї—О–і–∞—В—М –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Г—О —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ—Б—В—М –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б –љ–∞–њ—А—П–ґ–µ–љ–љ—Л–Љ —А–Є—В–Љ–Њ–Љ —Б–Њ–≤—А–µ–Љ–µ–љ–љ–Њ–є –ґ–Є–Ј–љ–Є, –∞ —В–∞–Ї–ґ–µ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ —Б—В—А–µ—Б—Б–Њ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В–Є –≤ —Г—Б–ї–Њ–≤–Є—П—Е –і–µ—Д–Є—Ж–Є—В–∞ –≤—А–µ–Љ–µ–љ–Є, –Є–Ј–±—Л—В–Ї–∞ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –Ї–∞–Ї —Б–ї–µ–і—Б—В–≤–Є–µ —Б—В—А–µ–Љ–Є—В–µ–ї—М–љ–Њ–є —Г—А–±–∞–љ–Є–Ј–∞—Ж–Є–Є. –І–∞—Б—В–Њ—В–∞ —Н—В–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–∞ –Є —Б–Њ—Б—В–∞–≤–ї—П–µ—В, –њ–Њ –і–∞–љ–љ—Л–Љ —А–∞–Ј–љ—Л—Е –∞–≤—В–Њ—А–Њ–≤, 10–20% –≤ –њ–Њ–њ—Г–ї—П—Ж–Є–Є [7]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –∞–і–µ–Ї–≤–∞—В–љ–∞—П —В–µ—А–∞–њ–Є—П —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Є–Љ–µ–µ—В –±–Њ–ї—М—И—Г—О —Б–Њ—Ж–Є–∞–ї—М–љ—Г—О –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М. –Ґ–∞–Ї, –≤ —А—П–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –њ–∞—Ж–Є–µ–љ—В—Л, —Б—В—А–∞–і–∞—О—Й–Є–µ –њ–µ—А–Љ–∞–љ–µ–љ—В–љ—Л–Љ–Є –Є–ї–Є –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–Љ–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, –Є–Љ–µ—О—В –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–є —Г—А–Њ–≤–µ–љ—М —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞, –≤–і–≤–Њ–µ –≤–Њ–Ј—А–∞—Б—В–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Є–љ—Б—Г–ї—М—В–∞, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ – —А–Є—Б–Ї –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є, –Є–љ—Д–∞—А–Ї—В–∞ –Љ–Є–Њ–Ї–∞—А–і–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Њ–±—Й–µ–є –њ–Њ–њ—Г–ї—П—Ж–Є–µ–є [5,12]. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П —Б—Г–Є—Ж–Є–і–∞ –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –Њ–љ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 20% –і–ї—П –ї–Є—Ж —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Є –Њ–Ї–Њ–ї–Њ 6% –і–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і—А—Г–≥–Њ–є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є [7]. –Ю—Б–Њ–±–µ–љ–љ–Њ —З–∞—Б—В–Њ —Б—Г–Є—Ж–Є–і–∞–ї—М–љ—Л–µ —В–µ–љ–і–µ–љ—Ж–Є–Є –њ—А–Њ—Б–ї–µ–ґ–Є–≤–∞—О—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е —З—Г–≤—Б—В–≤–Њ —А–∞–Ј–і—А–∞–ґ–µ–љ–Є—П –Є —В—А–µ–≤–Њ–≥–Є —Б–Њ—З–µ—В–∞–µ—В—Б—П —Б —Н–њ–Є–Ј–Њ–і–Є—З–µ—Б–Ї–Є–Љ–Є –њ–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є –∞—В–∞–Ї–∞–Љ–Є –Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–ї–Є—В–µ–ї—М–љ–Њ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є–Љ–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –њ—А–Є —В—А–∞–љ—Б—Д–Њ—А–Љ–∞—Ж–Є–Є –≤ —В—А–µ–≤–Њ–ґ–љ—Г—О –і–µ–њ—А–µ—Б—Б–Є—О.
–Ф—А—Г–≥–Є–Љ –љ–µ –Љ–µ–љ–µ–µ –≤–∞–ґ–љ—Л–Љ —Б–Њ—Ж–Є–∞–ї—М–љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —П–≤–ї—П–µ—В—Б—П –≤–Њ–Ј—А–∞—Б—В–∞–љ–Є–µ —А–Є—Б–Ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –∞–ї–Ї–Њ–≥–Њ–ї—П –Є –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є—П —Н—В–Є–Љ–Є –≤–µ—Й–µ—Б—В–≤–∞–Љ–Є –њ—А–Є —Б–Є–љ–і—А–Њ–Љ–µ –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Ґ–∞–Ї, –њ–Њ—Б—В–Њ—П–љ–љ–Њ–µ —Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –∞–ї–Ї–Њ–≥–Њ–ї—П —Г —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 24,3%, –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –≤–Њ–Ј–љ–Є–Ї–∞–µ—В —Г 8,7% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ј–ї–Њ—Г–њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–∞–Љ–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ —Г 26% –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –і—А—Г–≥–Є–Љ–Є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є – —Г 17% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [10].
–§–∞–Ї—В–Њ—А—Л, –њ—А–Є–≤–Њ–і—П—Й–Є–µ –Ї —А–∞–Ј–≤–Є—В–Є—О –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –љ–∞ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–Ї–Њ–љ—З–∞—В–µ–ї—М–љ–Њ –љ–µ —П—Б–љ—Л. –Э–µ—Б–Њ–Љ–љ–µ–љ–љ–Њ, –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ—О—В –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –ї–Є—З–љ–Њ—Б—В–Є. –Ю–±—Б—Г–ґ–і–∞–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–∞—П —А–Њ–ї—М –љ–∞—А—Г—И–µ–љ–Є–є –∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є. –Ґ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ locus coeruleus, —П–≤–ї—П—П—Б—М –Њ–і–љ–Њ–є –Є–Ј –љ–∞–і—Б–µ–≥–Љ–µ–љ—В–∞—А–љ—Л—Е —Б—В—А—Г–Ї—В—Г—А –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є, –∞—Д—Д–µ—А–µ–љ—В–љ–Њ –Є —Н—Д—Д–µ—А–µ–љ—В–љ–Њ –њ—А–Њ–µ—Ж–Є—А—Г–µ—В—Б—П –љ–∞ –±–Њ–ї—М—И–Њ–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —Б–Њ–Ј–і–∞–≤–∞—П —И–Є—А–Њ–Ї—Г—О —Б–µ—В—М –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Њ–є –Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ї–∞–Ј—Л–≤–∞—О—В, —З—В–Њ —В—А–µ–≤–Њ–ґ–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–µ—А–∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О. –Ъ–Њ—Б–≤–µ–љ–љ–Њ —Н—В–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–∞–µ—В —В–∞–Ї–ґ–µ –Є —В–Њ—В —Д–∞–Ї—В, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–∞ –њ—А–µ—Б–Є–љ–∞–њ—В–Є—З–µ—Б–Ї–Є—Е a2––∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤, —З—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—К—П—Б–љ–µ–љ–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ–Љ –Ј–∞—Й–Є—В–љ—Л—Е, –∞–љ—Б–Ї–Є–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤. [9]. –Т —Е–Њ–і–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–ї–Њ—Б—М, —З—В–Њ –њ—Б–Є—Е–Њ–≤–µ—В–µ—В–∞—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Њ–≥—Г—В —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В—А–∞–љ—Д–Њ—А–Љ–∞—Ж–Є–Є –∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ–њ—Г–ї—П—Ж–Є–Є –∞–і—А–µ–љ–Њ—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ —Б –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М—О [11]. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –Љ–љ–Њ–≥–Њ–Ї—А–∞—В–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –љ–µ –њ–Њ–і—В–≤–µ—А–і–Є–ї–Є –і–∞–љ–љ—Г—О –≥–Є–њ–Њ—В–µ–Ј—Г.
–Ч–љ–∞—З–Є—В–µ–ї—М–љ–∞—П —А–Њ–ї—М –≤ —А–∞–Ј–≤–Є—В–Є–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Њ—В–і–∞–µ—В—Б—П —Б–љ–Є–ґ–µ–љ–Є—О —Г—А–Њ–≤–љ—П g-–∞–Љ–Є–љ–Њ–Љ–∞—Б–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–У–Р–Ь–Ъ), —П–≤–ї—П—О—Й–µ–є—Б—П –Њ–і–љ–Є–Љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е —В–Њ—А–Љ–Њ–Ј–љ—Л—Е –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ (—А–Є—Б. 1). –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –У–Р–Ь–Ъ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –≥–ї—Г—В–∞–Љ–∞—В (–њ—А–Є —Н—В–Њ–Љ –≤–Њ–Ј–Љ–Њ–ґ–љ–∞ –Ї–∞–Ї –њ—А—П–Љ–∞—П, —В–∞–Ї –Є –Њ–±—А–∞—В–љ–∞—П —А–µ–∞–Ї—Ж–Є–Є), –і–∞–ї–µ–µ –≥–ї—Г—В–∞–Љ–∞—В –њ–Њ–і –і–µ–є—Б—В–≤–Є–µ–Љ –≥–ї—Г—В–∞–Љ–∞—В–і–µ–≥–Є–і—А–Њ–≥–µ–љ–∞–Ј—Л —А–∞—Б—Й–µ–њ–ї—П–µ—В—Б—П –і–Њ —Г—А–Њ–≤–љ—П a––Ї–µ—В–Њ–≥–ї—Г—В–∞—А–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л. –Ф–ї—П —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є–є —В–Є–њ–Є—З–љ–∞ –Њ–±—А–∞—В–љ–∞—П —А–µ–∞–Ї—Ж–Є—П, —В–Њ –µ—Б—В—М –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ –≥–ї—Г—В–∞–Љ–∞—В–∞ –Є –і–∞–ї–µ–µ –У–Р–Ь–Ъ. –Я—А–µ–і–њ–Њ–ї–∞–≥–∞–µ—В—Б—П, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ–≥–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Љ–Њ–ґ–µ—В —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞—В—М –Њ—Б–Њ–±–∞—П —Д–Њ—А–Љ–∞ –≥–ї—Г—В–∞–Љ–∞—В–і–µ–≥–Є–і—А–Њ–≥–µ–љ–∞–Ј—Л, –і–∞—О—Й–∞—П –≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –њ—А—П–Љ—Г—О —А–µ–∞–Ї—Ж–Є—О, —З—В–Њ –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞–Ї–Њ–њ–ї–µ–љ–Є—О –≥–ї—Г—В–∞–Љ–∞—В–∞ –Є —Б–љ–Є–ґ–µ–љ–Є—О –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –У–Р–Ь–Ъ. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Г—О —А–Њ–ї—М –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–ґ–µ—В –Є–≥—А–∞—В—М —Б–љ–Є–ґ–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Є –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –Є—Е —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Ї —Б–≤—П–Ј—Л–≤–∞–љ–Є—О —Б —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–Є–Љ–Є –Љ–µ–і–Є–∞—В–Њ—А–∞–Љ–Є [10].
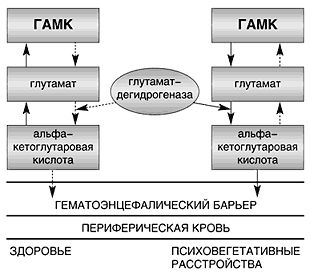
–†–Є—Б. 1. –Ь–µ—В–∞–±–Њ–ї–Є–Ј–Љ g-–∞–Љ–Є–љ–Њ–Љ–∞—Б–ї—П–љ–Њ–є –Ї–Є—Б–ї–Њ—В—Л —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є
–Ь–µ–і–Є–∞—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е –Љ–Њ–≥—Г—В –±—Л—В—М —И–Є—А–Њ–Ї–Њ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Њ—В–і–µ–ї–∞—Е –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—А–Є —Н—В–Њ–Љ –њ—А–µ–Њ–±–ї–∞–і–∞–љ–Є–µ —В—А–µ–≤–Њ–ґ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Љ–Њ–ґ–µ—В –±—Л—В—М —А–µ–Ј—Г–ї—М—В–∞—В–Њ–Љ –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –ї–Є–Љ–±–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Я–∞—А–Њ–Ї—Б–Є–Ј–Љ—Л –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —А–µ–≥—Г–ї–Є—А—Г—О—Й–µ–≥–Њ –≤–ї–Є—П–љ–Є—П —А–µ—В–Є–Ї—Г–ї—П—А–љ–Њ–є —Д–Њ—А–Љ–∞—Ж–Є–Є –Є —Б–≤—П–Ј–Є –µ–µ —Б –і—А—Г–≥–Є–Љ–Є –љ–∞–і—Б–µ–≥–Љ–µ–љ—В–∞—А–љ—Л–Љ–Є –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П–Љ–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —А–µ–≥—Г–ї—П—Ж–Є–Є.–§–Њ–±–Є–Є, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –Є–Љ–µ—О—В –±–Њ–ї–µ–µ —Б–ї–Њ–ґ–љ—Л–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П. –У–µ–љ–µ–Ј —Д–Њ–±–Є–є —Б–≤—П–Ј–∞–љ, –≤ —В–Њ–Љ —З–Є—Б–ї–µ, —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–≥–Њ –њ–Њ–≤–µ–і–µ–љ–Є—П –Є –Є–Ј–Љ–µ–љ–µ–љ–љ—Л—Е –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –і–∞–љ–љ–Њ–Љ —Б–ї—Г—З–∞–µ –Љ–Њ–ґ–љ–Њ –≥–Њ–≤–Њ—А–Є—В—М –Њ –Ј–∞–Є–љ—В–µ—А–µ—Б–Њ–≤–∞–љ–љ–Њ—Б—В–Є –Ї–Њ—А—Л –±–Њ–ї—М—И–Є—Е –њ–Њ–ї—Г—И–∞—А–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [9]. –°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ–∞—П —Б–Є—Б—В–µ–Љ–∞ –Љ–Њ–ґ–µ—В –љ–µ —В–Њ–ї—М–Ї–Њ —Б–ї—Г–ґ–Є—В—М –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ —А–µ–∞–ї–Є–Ј–∞—Ж–Є–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –њ—Б–Є—Е–Њ–≤–µ—В–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –љ–Њ –Є —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ —Г—З–∞—Б—В–≤–Њ–≤–∞—В—М –≤ –Є—Е —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є. –Ґ–∞–Ї, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–µ —Г—З–∞—Б—В–Є–µ –Љ–µ—В–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л –≤ —А–∞–Ј–≤–Є—В–Є–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Т —З–∞—Б—В–љ–Њ—Б—В–Є, –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –≤–≤–µ–і–µ–љ–Є–µ —Е–Њ–ї–µ—Ж–Є—Б—В–Њ–Ї–Є–љ–Є–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞–µ—В —Г—А–Њ–≤–µ–љ—М —В—А–µ–≤–Њ–≥–Є –љ–µ —В–Њ–ї—М–Ї–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ–≥–∞—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –љ–Њ –Є —Г –Ј–і–Њ—А–Њ–≤—Л—Е –Є—Б–њ—Л—В—Г–µ–Љ—Л—Е [9]. –≠—В–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–≥—Г—В –±—Л—В—М –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ—Л –Ї–∞–Ї –Ї–Њ–љ–Ї—Г—А–µ–љ—В–љ—Л–Љ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ–Љ —Г–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ –Љ–µ–і–Є–∞—В–Њ—А–∞ —Б –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤—Л–Љ–Є —А–µ—Ж–µ–њ—В–Њ—А–∞–Љ–Є, —В–∞–Ї –Є –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ–є —Б—В–Є–Љ—Г–ї—П—Ж–Є–µ–є –Љ–µ—В–∞—Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Т —Н—В–Њ–Љ —Б–ї—Г—З–∞–µ –њ–µ—А–≤–Є—З–љ–Њ —В—А–µ–≤–Њ–ґ–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Љ–Њ–≥—Г—В —А–µ–∞–ї–Є–Ј–Њ–≤–∞—В—М—Б—П –љ–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–Љ —Г—А–Њ–≤–љ–µ. –Ґ–Њ–ї—М–Ї–Њ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ–Љ —Б—Г—Й–µ—Б—В–≤–Њ–≤–∞–љ–Є–Є —В—А–µ–≤–Њ–ґ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –≤ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –Љ–Њ–≥—Г—В –≤–Њ–≤–ї–µ–Ї–∞—В—М—Б—П —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л.
–Ш—Б—Е–Њ–і—П –Є–Ј –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–≥–Њ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–µ –Љ–µ—Б—В–Њ –≤ –ї–µ—З–µ–љ–Є–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Њ—В–≤–Њ–і–Є—В—Б—П —В—А–∞–љ–Ї–≤–Є–ї–Є–Ј–∞—В–Њ—А–∞–Љ – –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–Љ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–∞ [4]. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –њ—А–Є—Е–Њ–і–Є—В—Б—П –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ —Н—В–Њ—В —Б–њ–Њ—Б–Њ–± –ї–µ—З–µ–љ–Є—П –і–∞–ї–µ–Ї–Њ –љ–µ –Є–і–µ–∞–ї–µ–љ, –≤ –њ–µ—А–≤—Г—О –Њ—З–µ—А–µ–і—М –Є–Ј––Ј–∞ —А–∞–Ј–≤–Є–≤–∞—О—Й–Є—Е—Б—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ъ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ –њ–Њ–±–Њ—З–љ—Л–Љ —Н—Д—Д–µ–Ї—В–∞–Љ –Њ—В–љ–Њ—Б—П—В—Б—П –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–љ–Є–Љ–∞–љ–Є—П, –љ–∞—А—Г—И–µ–љ–Є–µ –Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є–Є. –£—З–Є—В—Л–≤–∞—П —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–є —Б–Є–љ–і—А–Њ–Љ —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г —А–∞–±–Њ—В–∞—О—Й–Є—Е –ї—О–і–µ–є, –Њ—З–µ–≤–Є–і–љ–Њ –≤–ї–Є—П–љ–Є–µ —Г–Ї–∞–Ј–∞–љ–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–∞ —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –І–∞—Б—В–Њ —А–∞–Ј–≤–Є–≤–∞—О—Й–µ–µ—Б—П —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –і–µ–Ј–∞–і–∞–њ—В–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є. –Ъ–∞–Ї —Г–њ–Њ–Љ–Є–љ–∞–ї–Њ—Б—М –≤—Л—И–µ, —Д–∞–Ї—В–Њ—А –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–≥–Њ —А–∞–Ј–≤–Є—В–Є—П –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—Б–Њ–±–µ–љ–љ–Њ —Б–µ—А—М–µ–Ј–µ–љ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, —Г—З–Є—В—Л–≤–∞—П –Є—Е –њ–µ—А–≤–Є—З–љ—Г—О –ї–Є—З–љ–Њ—Б—В–љ—Г—О –њ—А–µ–і—А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є, –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є –Є –љ–∞—А–Ї–Њ—В–Є—З–µ—Б–Ї–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є [10]. –Я—А–Є –Њ—Ж–µ–љ–Ї–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–∞–Љ–Є –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Е–Њ—А–Њ—И–Є–є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –њ–Њ—Б–ї–µ 8 –љ–µ–і–µ–ї—М —В–µ—А–∞–њ–Є–Є –Є –і–ї–Є—В—Б—П –Њ–Ї–Њ–ї–Њ 3 –Љ–µ—Б—П—Ж–µ–≤, –њ–Њ—Б–ї–µ —З–µ–≥–Њ –і–∞–ґ–µ –њ—А–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–Є –і–Њ–Ј—Л –њ—А–Є–љ–Є–Љ–∞–µ–Љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –љ–∞—Б—В—Г–њ–∞–µ—В —Б—В–Њ–є–Ї–Њ–µ —Г—Е—Г–і—И–µ–љ–Є–µ. –Я—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ —Б—Г—Й–µ—Б—В–≤—Г—О—В –≥—А–∞–љ–Є—Ж—Л —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –і–Њ–Ј—Л –≤ —Б–≤—П–Ј–Є —Б –њ–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г–Ї–∞–Ј–∞–љ–љ–Њ–є —Д–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –≥—А—Г–њ–њ—Л –≤ –≤–Є–і–µ —Г–≥–љ–µ—В–µ–љ–Є—П –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –і—Л—Е–∞—В–µ–ї—М–љ–Њ–≥–Њ —Ж–µ–љ—В—А–∞ –Є —Б–љ–Є–ґ–µ–љ–Є—П —Б–Њ–Ї—А–∞—В–Є—В–µ–ї—М–љ–Њ–є —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –Љ–Є–Њ–Ї–∞—А–і–∞. –£–Ї–∞–Ј–∞–љ–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л —В–∞–Ї–ґ–µ –љ–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –і–Њ—Б—В–Є–≥–∞—В—М –∞–і–µ–Ї–≤–∞—В–љ—Л—Е –і–Њ–Ј —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є –і—Л—Е–∞—В–µ–ї—М–љ–Њ–є –Є —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–µ—А–µ—З–Є—Б–ї–µ–љ–љ—Л–µ —Д–∞–Ї—В—Л –љ–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –њ—А–Є–Ј–љ–∞—В—М –њ–Њ–ї–љ–Њ—Б—В—М—О —Г–і–Њ–≤–ї–µ—В–≤–Њ—А–Є—В–µ–ї—М–љ—Л–Љ –Љ–µ—В–Њ–і –ї–µ—З–µ–љ–Є—П –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤–Њ–≥–Њ —А—П–і–∞ –Є –Ј–∞—Б—В–∞–≤–ї—П—О—В –≤—А–∞—З–µ–є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В—М –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ—Л–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤.
–Т –њ—А–Њ–≥—А–∞–Љ–Љ—Г —Б–Є—Б—В–µ–Љ–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –≤–Ї–ї—О—З–µ–љ–Є–µ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є—Е –Љ–µ—В–Њ–і–Є–Ї, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Г—О —В–µ—А–∞–њ–Є—О, –Љ–µ—В–Њ–і –њ—Б–Є—Е–Њ—Б–µ–Љ–∞–љ—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є, –њ–Њ–Ј–≤–Њ–ї—П—О—Й–Є—Е —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —В—А–∞–љ—Б—Д–Њ—А–Љ–Є—А–Њ–≤–∞—В—М —Б–Њ—Ж–Є–∞–ї—М–љ–Њ––±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Б–Є—Б—В–µ–Љ—Г –њ–∞—Ж–Є–µ–љ—В–∞. –Т —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –Є —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–Љ–µ–љ—П–ї–Є—Б—М –Љ–µ—В–Њ–і—Л –±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Њ–±—А–∞—В–љ–Њ–є —Б–≤—П–Ј–Є (biofeedback). –Ю—Б–Њ–±—Г—О –њ—А–Њ–±–ї–µ–Љ—Г –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В –њ–∞—Ж–Є–µ–љ—В—Л —Б –Њ—А–≥–∞–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–Љ–Є—Б—П —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –њ—Б–Є—Е–Њ–њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —А–µ–∞–Ї—Ж–Є–є –Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є —Б—Д–µ—А—Л. –Я—А–Є –Є—Е –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤—Л—П–≤–ї–µ–љ–Є–µ –і–Њ–Љ–Є–љ–Є—А—Г—О—Й–µ–є –њ—А–Є—З–Є–љ—Л, –Ј–∞–њ—Г—Б–Ї–∞—О—Й–µ–є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–є –Ї–∞—Б–Ї–∞–і.
–Э–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ–Є –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–Љ–Є –Љ–µ—В–Њ–і–Є–Ї–∞–Љ–Є, –Ї–Њ—А—А–µ–Ї—В–Є—А—Г—О—Й–Є–Љ–Є –њ—Б–Є—Е–Њ—Б–µ–Љ–∞–љ—В–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П, –≤—Л–Ј–≤–∞–љ–љ—Л–µ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л–Љ —Б—В—А–µ—Б—Б–Њ–Љ, —П–≤–ї—П—О—В—Б—П —Б–Є—Б—В–µ–Љ–љ—Л–µ –њ—Б–Є—Е–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–Є, –Ї–Њ—А—А–µ–Ї—В–Є—А—Г—О—Й–Є–µ –≤–ї–Є—П–љ–Є–µ –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л—Е —Б—В–Є–Љ—Г–ї–Њ–≤ (–≤–µ—А–±–∞–ї—М–љ—Л—Е –Є –љ–µ–≤–µ—А–±–∞–ї—М–љ—Л—Е) –Є –њ—Б–Є—Е–Њ—Б–µ–Љ–∞–љ—В–Є—З–µ—Б–Ї–Є—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ (—Б–Љ—Л—Б–ї–Њ–≤—Л—Е –Ј–љ–∞—З–µ–љ–Є–є, –Њ–њ—А–µ–і–µ–ї—П—О—Й–Є—Е –≤–љ—Г—В—А–µ–љ–љ—О—О –Ї–∞—А—В–Є–љ—Г –Љ–Є—А–∞ –њ–∞—Ж–Є–µ–љ—В–∞), –Є –Њ–њ—В–Є–Љ–Є–Ј–Є—А—Г—О—Й–Є–µ —Б–Њ—Ж–Є–∞–ї—М–љ–Њ––±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О —Б–Є—Б—В–µ–Љ—Г –њ–∞—Ж–Є–µ–љ—В–∞. –Т–∞–ґ–љ—Л–Љ –Є—В–Њ–≥–Њ–Љ –њ—А–Є–Љ–µ–љ—П–µ–Љ–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ —П–≤–ї—П–µ—В—Б—П –Њ–њ—В–Є–Љ–Є–Ј–∞—Ж–Є—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Њ–љ–љ—Л—Е –њ–Њ–ї–µ–є –Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ––±–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є—Б—В–µ–Љ, –Њ–Ї—А—Г–ґ–∞—О—Й–Є—Е –њ–∞—Ж–Є–µ–љ—В–∞. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Б–Є—Б—В–µ–Љ–љ—Л—Е –њ—Б–Є—Е–Њ—В–µ—Е–љ–Њ–ї–Њ–≥–Є–є —Г 72 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ [2,3] –њ–Њ–Ї–∞–Ј–∞–ї–Њ —Б—В–Њ–є–Ї–Є–є –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Л–є —Н—Д—Д–µ–Ї—В —Б—В–∞–±–Є–ї–Є–Ј–∞—Ж–Є–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –≤ 84%. –С—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–µ—А–Є–Њ–і–Њ–≤ —Б–Є—В—Г–∞—В–Є–≤–љ–Њ–є –Є –ї–Є—З–љ–Њ—Б—В–љ–Њ–є —В—А–µ–≤–Њ–≥–Є, –љ–µ–Љ–Њ—В–Є–≤–Є—А–Њ–≤–∞–љ–љ–Њ–є –∞–≥—А–µ—Б—Б–Є–Є, –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є. –Ю—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є –љ–∞–≤—П–Ј—З–Є–≤—Л—Е —Б–Њ—Б—В–Њ—П–љ–Є–є –Є —А–µ–∞–Ї—Ж–Є–є –Њ–±—Б–µ—Б—Б–Є–≤–љ–Њ–—Д–Њ–±–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Г–Ї–∞–Ј–∞–љ–љ—Л–є –Љ–µ—В–Њ–і –ї–µ—З–µ–љ–Є—П —Б–ї–µ–і—Г–µ—В –њ—А–Є–Ј–љ–∞—В—М —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ –Є —Ж–µ—Б–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ.
–Я—А–Њ–≤–µ–і–µ–љ–Є–µ –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Љ–Њ–ґ–µ—В —Б–Њ—З–µ—В–∞—В—М—Б—П —Б –њ—А–Є–µ–Љ–Њ–Љ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –љ–µ –Њ–±–ї–∞–і–∞—О—Й–Є—Е –њ–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –≤ –≤–Є–і–µ –Ј–∞–Љ–µ–і–ї–µ–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є. –Ъ —В–∞–Ї–Є–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, –Њ—В–љ–Њ—Б—П—В—Б—П –љ–µ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–µ —Б–Њ–µ–і–Є–љ–µ–љ–Є—П –Є —А–∞—Б—В–Є—В–µ–ї—М–љ—Л–µ –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ. –Т —Н—В–Њ–Љ –∞—Б–њ–µ–Ї—В–µ –±–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –њ—А–µ–і—Б—В–∞–≤–ї—П–µ—В –Я–µ—А—Б–µ–љ, –≤ —Б–Њ—Б—В–∞–≤ –Ї–Њ—В–Њ—А–Њ–≥–Њ –≤—Е–Њ–і—П—В —Н–Ї—Б—В—А–∞–Ї—В—Л –≤–∞–ї–µ—А–Є–∞–љ—Л, –Љ–µ–ї–Є—Б—Б—Л, –Љ—П—В—Л –њ–µ—А–µ—З–љ–Њ–є, –Њ–±–ї–∞–і–∞—О—Й–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –∞–љ–Ї—Б–Є–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М—О.
–Я—А–Њ–≤–µ–і–µ–љ–љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї–Є –≤—Л—Б–Њ–Ї—Г—О —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Я–µ—А—Б–µ–љ–∞ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є —В—А–µ–≤–Њ–ґ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –≤ —А–∞–Љ–Ї–∞—Е –њ—Б–Є—Е–Њ–≤–µ—В–µ—В–∞—В–Є–≤–љ–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –Ґ–∞–Ї, –±—Л–ї–Њ –њ—А–Њ–≤–µ–і–µ–љ–Њ –њ–ї–∞—Ж–µ–±–Њ– –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ–Њ–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б–њ—Л—В–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Г–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —Г 93 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ –≤ —Б—В—А—Г–Ї—В—Г—А–µ –љ–µ–≤—А–Њ—В–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —В—А–µ–≤–Њ–ґ–љ–Њ–≥–Њ —А—П–і–∞ [1]. –Т –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –≤–Ї–ї—О—З–µ–љ—Л 62 –ґ–µ–љ—Й–Є–љ—Л –Є 31 –Љ—Г–ґ—З–Є–љ–∞. –Т–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤–∞—А—М–Є—А–Њ–≤–∞–ї –Њ—В 16 –і–Њ 62 –ї–µ—В, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б–њ—Л—В–∞–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б–Њ—Б—В–∞–≤–Є–ї 34,5 –ї–µ—В. –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –±—Л–ї–Є —А–∞–Ј–і–µ–ї–µ–љ—Л –љ–∞ 2 –≥—А—Г–њ–њ—Л. –Т –њ–µ—А–≤—Г—О –≥—А—Г–њ–њ—Г –≤–Њ—И–ї–Є 47 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (30 –ґ–µ–љ—Й–Є–љ, 17 –Љ—Г–ґ—З–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 34,8 –ї–µ—В), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Я–µ—А—Б–µ–љ –§–Њ—А—В–µ –≤ –і–Њ–Ј–µ 1 –Ї–∞–њ—Б—Г–ї–∞ (125 –Љ–≥) 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М. –Т—В–Њ—А—Г—О –≥—А—Г–њ–њ—Г —Б–Њ—Б—В–∞–≤–Є–ї–Є 46 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (32 –ґ–µ–љ—Й–Є–љ—Л, 14 –Љ—Г–ґ—З–Є–љ, —Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 35,0 –ї–µ—В), –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –њ–ї–∞—Ж–µ–±–Њ –њ–Њ 1 –Ї–∞–њ—Б—Г–ї–µ 2 —А–∞–Ј–∞ –≤ –і–µ–љ—М. –Я–ї–∞—Ж–µ–±–Њ –Є –Я–µ—А—Б–µ–љ –§–Њ—А—В–µ –±—Л–ї–Є –Є–і–µ–љ—В–Є—З–љ—Л –њ–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є —Д–Њ—А–Љ–µ –Є –≤–Є–і—Г —Г–њ–∞–Ї–Њ–≤–Ї–Є. –Ъ—Г—А—Б –ї–µ—З–µ–љ–Є—П —Б–Њ—Б—В–∞–≤–Є–ї 28 –і–љ–µ–є. –Ю–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ –і–ї—П –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –Є—Б–њ—Л—В–∞–љ–Є–µ –±—Л–ї–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –њ—А–Є–µ–Љ–∞ –Ї–∞–Ї–Є—Е––ї–Є–±–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і–µ–ї—М, –њ—А–µ–і—И–µ—Б—В–≤—Г—О—Й–Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є—О –Я–µ—А—Б–µ–љ–∞.
–Т —А–∞–Љ–Ї–∞—Е –љ–∞—Б—В–Њ—П—Й–µ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–ї—Б—П –Љ–µ—В–Њ–і –∞–љ–Ї–µ—В–Є—А–Њ–≤–∞–љ–Є—П – –∞–љ–Ї–µ—В—Л –Њ—Ж–µ–љ–Ї–Є —Б–Њ—Б—В–Њ—П–љ–Є—П –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –Њ—Ж–µ–љ–Ї–Є –Ї–∞—З–µ—Б—В–≤–∞ —Б–љ–∞, –Њ—Ж–µ–љ–Ї–Є –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є, –∞ —В–∞–Ї–ґ–µ —И–Ї–∞–ї–∞ –ґ–Є–Ј–љ–µ–љ–љ—Л—Е —Б–Њ–±—Л—В–Є–є –•–Њ–ї–Љ—Б–∞ –Є –†–µ—П, –≤–Є–Ј—Г–∞–ї—М–љ–∞—П –∞–љ–∞–ї–Њ–≥–Њ–≤–∞—П —И–Ї–∞–ї–∞ –і–ї—П —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є –Њ—Ж–µ–љ–Ї–Є —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П, —И–Ї–∞–ї—Л –°–њ–Є–ї–±–µ—А–≥–µ—А–∞, –С–µ–Ї–∞. –Я—А–Њ–≤–Њ–і–Є–ї—Б—П –∞–љ–∞–ї–Є–Ј —Г—А–Њ–≤–љ—П –≤–љ–Є–Љ–∞–љ–Є—П –Є —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–Њ—А—А–µ–Ї—В—Г—А–љ–Њ–є –њ—А–Њ–±—Л –С—Г—А–і–Њ–љ–∞ –Є –њ—А–Њ–±—Л –®—Г–ї—М—В–µ.
–Ю—Б–љ–Њ–≤–љ—Л–Љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—П–≤–ї–µ–љ–Є—П–Љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –≤–Ї–ї—О—З–µ–љ–љ—Л—Е –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Є –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —В—А–µ–≤–Њ–ґ–љ–Њ—Б—В—М, —З—Г–≤—Б—В–≤–Њ –≤–љ—Г—В—А–µ–љ–љ–µ–≥–Њ –љ–∞–њ—А—П–ґ–µ–љ–Є—П, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, —Д–Њ–±–Є–Є. –£ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–≥–Њ —З–Є—Б–ї–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Њ—В–Љ–µ—З–∞–ї–Є—Б—М —В–∞–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П, –Ї–∞–Ї –≥–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П (74%), –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М (67%), –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М (53%), —З—Г–≤—Б—В–≤–Њ –љ–µ—Е–≤–∞—В–Ї–Є –≤–Њ–Ј–і—Г—Е–∞ (80%), –љ–µ—Б–Є—Б—В–µ–Љ–љ–Њ–µ –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ (68%), —В—А—Г–і–љ–Њ—Б—В–Є –Ј–∞—Б—Л–њ–∞–љ–Є—П (74%), –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Л–µ –Ї–∞—А–і–Є–∞–ї–≥–Є–Є (62%).
–Р–љ–∞–ї–Є–Ј –∞–љ–Ї–µ—В–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ –Є–Љ–µ–ї–Є—Б—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ —В—А–µ–≤–Њ–ґ–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Є –љ–∞—А—Г—И–µ–љ–Є—П —Б–љ–∞, –ї–µ–≥–Ї–Є–є —Г—А–Њ–≤–µ–љ—М –і–µ–њ—А–µ—Б—Б–Є–Є. –Т—Б–µ –њ–∞—Ж–Є–µ–љ—В—Л –Њ—В–Љ–µ—З–∞–ї–Є —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –љ–∞ —Д–Њ–љ–µ —Б—Г—Й–µ—Б—В–≤—Г—О—Й–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є.
–Р–љ–∞–ї–Є–Ј –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є —З–µ—А–µ–Ј –Њ–і–љ—Г –љ–µ–і–µ–ї—О –ї–µ—З–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞–ї —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —А–µ–∞–Ї—В–Є–≤–љ–Њ–є —В—А–µ–≤–Њ–≥–Є, –Ї–Њ—В–Њ—А–∞—П –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –≤ –Њ–±–µ–Є—Е –Є—Б—Б–ї–µ–і—Г–µ–Љ—Л—Е –≥—А—Г–њ–њ–∞—Е. –Э–∞ 28 –і–µ–љ—М —В–µ—А–∞–њ–Є–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Њ–±—Й–µ–є —Б–ї–∞–±–Њ—Б—В–Є, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В–Є, —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є, —В—А–µ–≤–Њ–≥–Є, —З—Г–≤—Б—В–≤–∞ –љ–µ—Е–≤–∞—В–Ї–Є –≤–Њ–Ј–і—Г—Е–∞, –∞ —В–∞–Ї–ґ–µ –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Л—Е –Ї–∞—А–і–Є–∞–ї–≥–Є–є. –£–ї—Г—З—И–µ–љ–Є–µ —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П –њ–Њ –≤–Є–Ј—Г–∞–ї—М–љ–Њ–є –∞–љ–∞–ї–Њ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ –і–Њ—Б—В–Є–≥–ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є –≤ –Њ–±–µ–Є—Е –≥—А—Г–њ–њ–∞—Е, –Њ–і–љ–∞–Ї–Њ —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –∞–љ–∞–ї–Є–Ј –њ–Њ–ї—Г—З–µ–љ–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–ї, —З—В–Њ –і–Є–љ–∞–Љ–Є–Ї–∞ –і–∞–љ–љ–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –±—Л–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ –±–Њ–ї—М—И–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Я–µ—А—Б–µ–љ. –Э–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Я–µ—А—Б–µ–љ–Њ–Љ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ —Г—А–Њ–≤–љ—П —В—А–µ–≤–Њ–≥–Є, –њ—А–Є —Н—В–Њ–Љ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М —Г–Ї–∞–Ј–∞–љ–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –њ—А—П–Љ–Њ –Ј–∞–≤–Є—Б–µ–ї–∞ –Њ—В –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є. –С—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –≤ –≥—А—Г–њ–њ–µ –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Я–µ—А—Б–µ–љ. –£ —Н—В–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —В–∞–Ї–ґ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –Є —В—П–ґ–µ—Б—В–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є. –Р–љ–∞–ї–Є–Ј –∞–љ–Ї–µ—В–љ—Л—Е –і–∞–љ–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞–ї –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Я–µ—А—Б–µ–љ. –Т –≥—А—Г–њ–њ–µ –њ–ї–∞—Ж–µ–±–Њ —Н—В–Њ—В –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М –љ–µ –і–Њ—Б—В–Є–≥ —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–є –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ—Б—В–Є.
–Я–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –≤ –≥—А—Г–њ–њ–µ, –њ—А–Є–љ–Є–Љ–∞–≤—И–µ–є –Я–µ—А—Б–µ–љ, –љ–µ –±—Л–ї–Њ. –Т–∞–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –њ–Њ–ї—Г—З–∞—О—Й–Є—Е –Я–µ—А—Б–µ–љ, –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є—П –≤–љ–Є–Љ–∞–љ–Є—П –Є —Г—Б–Є–ї–µ–љ–Є—П –і–љ–µ–≤–љ–Њ–є —Б–Њ–љ–ї–Є–≤–Њ—Б—В–Є. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –±—Л–ї–∞ —Е–Њ—А–Њ—И–µ–є –Є –µ–≥–Њ –њ—А–Є–µ–Љ –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї –≤–ї–Є—П–љ–Є—П –љ–∞ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –±–Њ–ї—М–љ—Л—Е.
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Љ–Њ–ґ–љ–Њ —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і, —З—В–Њ –Я–µ—А—Б–µ–љ –Љ–Њ–ґ–µ—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –≤ —В–µ—А–∞–њ–Є–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е –Є –њ–Њ—Б—В—В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е —Б—В—А–µ—Б—Б–Њ–≤—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –У–ї–∞–≤–љ—Л–Љ –Њ–±—А–∞–Ј–Њ–Љ —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П —Б—В–µ–њ–µ–љ—М —В–∞–Ї–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–∞–Ї —А–µ–∞–Ї—В–Є–≤–љ–∞—П –Є –ї–Є—З–љ–Њ—Б—В–љ–∞—П —В—А–µ–≤–Њ–≥–∞, –љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞, –і–µ–њ—А–µ—Б—Б–Є—П, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і –Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –∞–љ–Ї—Б–Є–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е –Є –≤–µ–≥–µ—В–Њ—В—А–Њ–њ–љ—Л—Е —Б–≤–Њ–є—Б—В–≤–∞—Е –њ—А–µ–њ–∞—А–∞—В–∞. –£–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є–Є —Б–Њ—Ж–Є–∞–ї—М–љ–Њ–є –∞–і–∞–њ—В–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є —Г–Ї–∞–Ј–∞–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Є –Љ–Њ–ґ–µ—В –±—Л—В—М –Ї–Њ—Б–≤–µ–љ–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ —Б—В–Њ–є–Ї–Њ—Б—В–Є –њ–Њ–ї—Г—З–µ–љ–љ–Њ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞. –Т–∞–ґ–љ—Л–Љ–Є –њ—А–µ–і—Б—В–∞–≤–ї—П—О—В—Б—П –і–∞–љ–љ—Л–µ –Њ–± –Њ—В—Б—Г—В—Б—В–≤–Є–Є –≤–ї–Є—П–љ–Є—П –њ—А–Є–µ–Љ–∞ –Я–µ—А—Б–µ–љ–∞ –љ–∞ —Г—А–Њ–≤–µ–љ—М —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –∞ —В–∞–Ї–ґ–µ –Є —В–Њ, —З—В–Њ –Я–µ—А—Б–µ–љ –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В –і–љ–µ–≤–љ–Њ–є —Б–Њ–љ–ї–Є–≤–Њ—Б—В–Є. –Т—Б–µ —Н—В–Њ –њ–Њ–Ј–≤–Њ–ї—П–µ—В —Б–і–µ–ї–∞—В—М –≤—Л–≤–Њ–і –Њ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ–Њ–≥–Њ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—А–∞–њ–Є–Є –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–µ –Ї–Њ—В–Њ—А—Л—Е –і–Њ–Љ–Є–љ–Є—А—Г—О—В –њ—А–Њ—П–≤–ї–µ–љ–Є—П —В—А–µ–≤–Њ–≥–Є.
–°–ї–µ–і—Г–µ—В –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ –Њ–±—П–Ј–∞—В–µ–ї—М–љ—Л–Љ —Г—Б–ї–Њ–≤–Є–µ–Љ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П —Б—В–Њ–є–Ї–Њ–≥–Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –Њ—В –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –њ–∞—Ж–Є–µ–љ—В–∞–Љ –Љ–µ—В–Њ–і–Є–Ї –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є, –Є—Е –Ї–Њ—В–Њ—А—Л—Е –љ–∞–Є–±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–є –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –Љ–Њ–ґ–љ–Њ –њ—А–Є–Ј–љ–∞—В—М –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ—Г—О –њ—Б–Є—Е–Њ—Б–µ–Љ–∞–љ—В–Є—З–µ—Б–Ї—Г—О –Ї–Њ—А—А–µ–Ї—Ж–Є—О.
1. –Т–Њ–Ј–љ–µ—Б–µ–љ—Б–Ї–∞—П –Ґ.–У., –§–µ–і–Њ—В–Њ–≤–∞ –Р.–Т., –§–Њ–Ї–Є–љ–∞ –Э.–Ь. –Я–µ—А—Б–µ–љ–—Д–Њ—А—В–µ –≤ –ї–µ—З–µ–љ–Є–Є —В—А–µ–≤–Њ–ґ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —Г –±–Њ–ї—М–љ—Л—Е –њ—Б–Є—Е–Њ–≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ.//–Ы–µ—З–µ–љ–Є–µ –љ–µ—А–≤–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–є. – —Б. 38–41.
2. –°–Љ–Є—А–љ–Њ–≤ –Ш.–Т., –Ь–Њ—Б–Ї–≤–Є–љ –Р.–Т. –Я—А–Њ–≥—А–∞–Љ–Љ–∞ –Є–љ–і–Є–≤–Є–і—Г–∞–ї—М–љ–Њ–є –њ—Б–Є—Е–Њ—Б–µ–Љ–∞–љ—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є.//–†–Ь–Ц. – 2000. – N 9. – —Б. 24–27.
3. –°–Љ–Є—А–љ–Њ–≤ –Ш.–Т., –Ь–Њ—Б–Ї–≤–Є–љ –Р.–Т., –Э–µ–ґ–і–∞–љ–Њ–≤ –Ш.–Ъ. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Љ–µ—В–Њ–і–∞ –њ—Б–Є—Е–Њ—Б–µ–Љ–∞–љ—В–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є.//–Ы–µ—З–µ–±–љ–∞—П –њ—А–∞–Ї—В–Є–Ї–∞. – 2000. – N 5. – —Б. 34–35.
4. –°–Љ—Г–ї–µ–≤–Є—З –Р.–С., –Ф—А–Њ–±–Є—И–µ–≤–∞ –Ь.–Ѓ., –Ш–≤–∞–љ–Њ–≤ –°.–Т. –Ґ—А–∞–љ–Ї–≤–Є–ї–Є–Ј–∞—В–Њ—А—Л – –њ—А–Њ–Є–Ј–≤–Њ–і–љ—Л–µ –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤ –≤ –њ—Б–Є—Е–Є–∞—В—А–Є—З–µ—Б–Ї–Њ–є –Є –Њ–±—Й–µ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ. – –Ь., – –Ш–Ґ–Р–†––Ґ–Р–°–°. – 1999. – 63 —Б.
5. Bajwa W.K., Asnis G.M., Sanderson W.C., et al. High cholesterol levels in patients with anxiety disorders.//Am. J. Psychiatry. – 1996. – V. 149. – N. 3. – p. 376–378.
6. Beck A.T., et al. An inventory for measurig depression.//Arch. Gen. Psychiat. – 1961. – V. 5. – P. 561–571.
7. Beck A.T., Steer R.A., Sanderson W.C., et al. Panic Disorder and suicidal ideation and behavior: discrepant findings in psychiatric outpatients.//Am. J. Psychiatry. – 1995. – V. 151. – V. 9. – p.1195–1199.
8. Efficacy of the preparation Persen–forte for treatment and prophylaxis of posttraumatic stress disorders (PSD) occurring with persons having been under stress conditions for a long time/
9. Redmond D.E. New and old evidence for the involvement of a brain norepinephrine system in anxiety.//Phenomenology and treatment of Anxiety. Edited by Fann W.E., Jamaica, NY, Spectrum Press, – 1994.
10. Stewart S.H., Pihl R.O. Chronic Use of Alcohol and/or Benzodiazepines may account for evidence of altered benzodiazepine receptor sensitivity in anxiety disorder.//Arch. Gen. Psychiatry. – 1995. – V. 49. – p. 329–333.
11. Wang Z.W., Crowe R.R., Noyes R.J. Adrenergic receptor genes as candidate genes for affective disorder: a linkage study.//Am. J. Psychiatry. – 1992. – V. 149. – P. 470–474.
12. Weissman M.M., Markowitz J.S., Ouelette R., et al. Panic Disorder and cardiovascular/cerebrovascular problems: results from community survey.//Am. J. Psychiatry. – 1996. – V. 153. – N. 11. – p. 1504–1508.












