–†–∞—Б—Б–µ—П–љ–љ—Л–є —Б–Ї–ї–µ—А–Њ–Ј (PC) –Њ—В–љ–Њ—Б–Є—В—Б—П –Ї —З–Є—Б–ї—Г –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л (–¶–Э–°). –Ґ–Њ–ї—М–Ї–Њ –≤ –†–Њ—Б—Б–Є–Є –љ–∞—Б—З–Є—В—Л–≤–∞–µ—В—Б—П –±–Њ–ї–µ–µ 150 —В—Л—Б—П—З —В–∞–Ї–Є—Е –±–Њ–ї—М–љ—Л—Е, –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Є–Ј –Ї–Њ—В–Њ—А—Л—Е – –ї—О–і–Є –Љ–Њ–ї–Њ–і–Њ–≥–Њ —В—А—Г–і–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. PC – –∞—Г—В–Њ–Є–Љ–Љ—Г–љ–љ–Њ–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ, –Њ—Б–љ–Њ–≤–љ—Л–Љ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–Љ –Ї–Њ—В–Њ—А–Њ–≥–Њ —П–≤–ї—П–µ—В—Б—П –∞—Г—В–Њ–∞–≥—А–µ—Б—Б–Є—П –њ—А–Њ—В–Є–≤ –Љ–Є–µ–ї–Є–љ–∞ –¶–Э–°. –Ю–і–љ–∞–Ї–Њ, –Ї–∞–Ї –њ–Њ–Ї–∞–Ј–∞–ї–Є –љ–µ–і–∞–≤–љ–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –њ—А–Є PC –њ–Њ–і–≤–µ—А–≥–∞—О—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ –Њ–±–Њ–ї–Њ—З–Ї–Є –њ—А–Њ–≤–Њ–і–љ–Є–Ї–Њ–≤ –¶–Э–°, –љ–Њ –Є —Б–∞–Љ–Є –∞–Ї—Б–Њ–љ—Л. –Ш–Љ–µ–љ–љ–Њ –∞–Ї—Б–Њ–љ–∞–ї—М–љ–∞—П –і–µ–≥–µ–љ–µ—А–∞—Ж–Є—П —П–≤–ї—П–µ—В—Б—П –њ—А–Є—З–Є–љ–Њ–є —А–∞–Ј–≤–Є—В–Є—П –∞—В—А–Њ—Д–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ–≥–Њ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–Є—Ж–Є—В–∞, –њ—А–Є–≤–Њ–і—П—Й–µ–≥–Њ –Ї –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є –±–Њ–ї—М–љ—Л—Е. –Ю—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–µ–љ —В–Њ—В —Д–∞–Ї—В, —З—В–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –∞–Ї—Б–Њ–љ–Њ–≤ –љ–∞—З–Є–љ–∞–µ—В—Б—П —Г–ґ–µ –љ–∞ –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є –±–Њ–ї–µ–Ј–љ–Є, —З—В–Њ –і–Є–Ї—В—Г–µ—В –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П —А–∞–љ–љ–µ–є –∞–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є PC.
–Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, –Є —Б–µ–≥–Њ–і–љ—П —Н—В–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Њ—Б—В–∞–µ—В—Б—П –љ–µ–Є–Ј–ї–µ—З–Є–Љ—Л–Љ. –Э–Њ –µ—Б–ї–Є —А–∞–љ–µ–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П –њ–Њ–Љ–Њ—Й—М –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б PC —Б–≤–Њ–і–Є–ї–∞—Б—М –ї–Є—И—М –Ї –њ–Њ–њ—Л—В–Ї–∞–Љ –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є—П –Њ–±–Њ—Б—В—А–µ–љ–Є–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є –њ—А–Њ–≤–µ–і–µ–љ–Є—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П, —В–Њ –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є –њ–Њ—П–≤–Є–ї–Є—Б—М –њ—Г—В–Є –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ —В–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–Ј–љ–Є. –≠—В–Њ —Б—В–∞–ї–Њ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–Љ –±–ї–∞–≥–Њ–і–∞—А—П –≤–љ–µ–і—А–µ–љ–Є—О –≤ –њ—А–∞–Ї—В–Є–Ї—Г —Б—А–µ–і—Б—В–≤ –њ—А–µ–≤–µ–љ—В–Є–≤–љ–Њ–є (–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–µ–є) —В–µ—А–∞–њ–Є–Є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≤–µ–і–µ—В –Ї —Г–Љ–µ–љ—М—И–µ–љ–Є—О —З–Є—Б–ї–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є–є –±–Њ–ї–µ–Ј–љ–Є, –і–µ–ї–∞–µ—В –Є—Е –Љ–µ–љ–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ–Є –Є –Ј–∞–Љ–µ–і–ї—П–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є —Ж–µ–ї—М—О –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е PC. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, —Б–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є –њ–Њ–і—Е–Њ–і –Ї –ї–µ—З–µ–љ–Є—О PC —Б–Њ—Б—В–Њ–Є—В –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Њ–±–Њ—Б—В—А–µ–љ–Є–є, –Ї—Г–њ–Є—А–Њ–≤–∞–љ–Є–Є –Є—Е –Є –њ—А–Њ–≤–µ–і–µ–љ–Є–Є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є.
–Я—А–µ–≤–µ–љ—В–Є–≤–љ–∞—П (–Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–∞—П) —В–µ—А–∞–њ–Є—П
–Ъ –њ—А–µ–њ–∞—А–∞—В–∞–Љ, —Б–љ–Є–ґ–∞—О—Й–Є–Љ —З–∞—Б—В–Њ—В—Г –Њ–±–Њ—Б—В—А–µ–љ–Є–є PC, –Њ—В–љ–Њ—Б—П—В—Б—П b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ—Л –Є –Ї–Њ–њ–∞–Ї—Б–Њ–љ.
–Я—А–Є–Љ–µ–љ–µ–љ–Є–µ b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤, –Њ–±–ї–∞–і–∞—О—Й–Є—Е –∞–љ—В–Є–≤–Є—А—Г—Б–љ—Л–Љ –Є –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—И–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ, –њ—А–Є PC –Њ—Б–љ–Њ–≤–∞–љ–Њ –љ–∞ –њ—А–µ–і–њ–Њ–ї–Њ–ґ–µ–љ–Є–Є –Њ —А–Њ–ї–Є –≤ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–Є —Н—В–Њ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—А—Б–Є—Б—В–Є—А—Г—О—Й–µ–є –Є–ї–Є –ї–∞—В–µ–љ—В–љ–Њ–є –≤–Є—А—Г—Б–љ–Њ–є –Є–љ—Д–µ–Ї—Ж–Є–Є —Г –ї—О–і–µ–є —Б –Є–Ј–Љ–µ–љ–µ–љ–љ–Њ–є –Є–Љ–Љ—Г–љ–љ–Њ–є —Б–Є—Б—В–µ–Љ–Њ–є. b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ—Л –Њ–±–ї–∞–і–∞—О—В –Њ—З–µ–љ—М —И–Є—А–Њ–Ї–Є–Љ —Б–њ–µ–Ї—В—А–Њ–Љ –і–µ–є—Б—В–≤–Є—П, –Њ—Б–љ–Њ–≤–љ—Л–Љ–Є –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П–Љ–Є –Ї–Њ—В–Њ—А–Њ–≥–Њ –њ—А–Є –ї–µ—З–µ–љ–Є–Є PC —П–≤–ї—П—О—В—Б—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –љ–∞ —А–µ–њ–ї–Є–Ї–∞—Ж–Є—О –≤–Є—А—Г—Б–Њ–≤ –Є —Б—В–Є–Љ—Г–ї—П—Ж–Є—П –≤—Л—А–∞–±–Њ—В–Ї–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤.
–Ъ b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞–Љ, –њ—А–Є–Љ–µ–љ—П—О—Й–Є–Љ—Б—П –≤ –ї–µ—З–µ–љ–Є–Є PC, –Њ—В–љ–Њ—Б—П—В—Б—П –±–µ—В–∞—Д–µ—А–Њ–љ, –∞–≤–Њ–љ–µ–Ї—Б –Є —А–µ–±–Є—Д. –Т—Б–µ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ —Б–љ–Є–ґ–∞—О—В —З–∞—Б—В–Њ—В—Г –Њ–±–Њ—Б—В—А–µ–љ–Є–є –њ—А–Є —А–µ–Љ–Є—В—В–Є—А—Г—О—Й–µ–Љ —В–µ—З–µ–љ–Є–Є PC –Є –Ј–∞–Љ–µ–і–ї—П—О—В –љ–∞—А–∞—Б—В–∞–љ–Є–µ –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є. –Ш—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–Њ–Ї—А–∞—Й–µ–љ–Є—О —З–Є—Б–ї–∞ –≥–Њ—Б–њ–Є—В–∞–ї–Є–Ј–∞—Ж–Є–є –Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Ї—Г—А—Б–Њ–≤ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –њ—А–Є–Љ–µ—А–љ–Њ –≤ 30%.
–Э–∞–Є–±–Њ–ї—М—И–Є–є –Њ–њ—Л—В –љ–∞–Ї–Њ–њ–ї–µ–љ –њ–Њ –ї–µ—З–µ–љ–Є—О PC –±–µ—В–∞—Д–µ—А–Њ–љ–Њ–Љ. –≠—В–Њ —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–є b-–Є–љ—В–µ—Д–µ—А–Њ–љ-1–∞, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–є –Ї—Г–ї—М—В—Г—А–Њ–є –Ї–Є—И–µ—З–љ–Њ–є –њ–∞–ї–Њ—З–Ї–Є. –С–µ—В–∞—Д–µ—А–Њ–љ –љ–µ —В–Њ–ї—М–Ї–Њ —Б–Њ–Ї—А–∞—Й–∞–µ—В —З–Є—Б–ї–Њ —Н–Ї–Ј–∞—Ж–µ—А–±–∞—Ж–Є–є –њ—А–Є —А–µ–Љ–Є—В—В–Є—А—Г—О—Й–µ–Љ —В–µ—З–µ–љ–Є–Є PC, –љ–Њ –Є –Ј–∞–Љ–µ–і–ї—П–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ—А–Є –≤—В–Њ—А–Є—З–љ–Њ-–њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–є –µ–≥–Њ —Д–Њ—А–Љ–µ, –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–є –Ї–∞–Ї —Б –Њ–±–Њ—Б—В—А–µ–љ–Є—П–Љ–Є, —В–∞–Ї –Є –±–µ–Ј –љ–Є—Е. –Я—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і–Є—В—Б—П –±–Њ–ї—М–љ—Л–Љ–Є —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ, –њ–Њ–і–Ї–Њ–ґ–љ–Њ, –≤ –і–Њ–Ј–µ 8 –Љ–ї–љ –Ь–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Х–і–Є–љ–Є—Ж (ME). –£ –±–Њ–ї—М–љ—Л—Е, –љ–µ –Њ—В–≤–µ—З–∞—О—Й–Є—Е –љ–∞ —Б—В–∞–љ–і–∞—А—В–љ—Л–µ –і–Њ–Ј—Л –±–µ—В–∞—Д–µ—А–Њ–љ–∞, –њ—А–Є –≤—Л—Б–Њ–Ї–Њ–є —Б—В–µ–њ–µ–љ–Є –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –±–Њ–ї—М—И–µ–є –і–Њ–Ј—Л – 12 –Љ–ї–љ ME.
–Р–≤–Њ–љ–µ–Ї—Б – —З–µ–ї–Њ–≤–µ—З–µ—Б–Ї–Є–є —А–µ–Ї–Њ–Љ–±–Є–љ–∞–љ—В–љ—Л–є b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ-1–∞, –≤—Л—А–∞–±–∞—В—Л–≤–∞–µ–Љ—Л–є –Ї—Г–ї—М—В—Г—А–Њ–є –Ї–ї–µ—В–Њ–Ї –Љ–ї–µ–Ї–Њ–њ–Є—В–∞—О—Й–µ–≥–Њ. –≠—В–Њ—В –њ—А–µ–њ–∞—А–∞—В –Є–Љ–µ–µ—В —В–Њ –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–Њ, —З—В–Њ –≤–≤–Њ–і–Є—В—Б—П 1 —А–∞–Ј –≤ –љ–µ–і–µ–ї—О. –Ю–љ –њ—А–Є–Љ–µ–љ—П–µ—В—Б—П –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ, –≤ –і–Њ–Ј–µ 6 –Љ–ї–љ ME.
–†–µ–±–Є—Д – —В–∞–Ї–ґ–µ b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ-1a, –≤–≤–Њ–і–Є—В—Б—П –њ–Њ–і–Ї–Њ–ґ–љ–Њ, 3 —А–∞–Ј–∞ –≤ –љ–µ–і–µ–ї—О. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤ –і–≤—Г—Е –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е – 6 –Љ–ї–љ ME –Є 12 –Љ–ї–љ ME. –†–∞–Ј–љ–Є—Ж–∞ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П —А–µ–±–Є—Д–Њ–Љ –≤ —А–∞–Ј–љ—Л—Е –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –љ–µ–і–Њ—Б—В–Њ–≤–µ—А–љ–∞.
–Я—А–Є –ї–µ—З–µ–љ–Є–Є b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–∞–Љ–Є –љ–∞–Є–±–Њ–ї–µ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —З–∞—Б—В–Њ—В–∞ –Њ–±–Њ—Б—В—А–µ–љ–Є–є —Б–љ–Є–ґ–∞–µ—В—Б—П –љ–∞ 2-–є –≥–Њ–і –ї–µ—З–µ–љ–Є—П, —В–Њ –µ—Б—В—М —Б–Њ –≤—А–µ–Љ–µ–љ–µ–Љ –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞. –Э–∞–Ј–љ–∞—З–µ–љ–Є–µ –±–µ—В–∞—Д–µ—А–Њ–љ–∞ –Є —А–µ–±–Є—Д–∞ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–µ–є –і–Њ 5,5 –±–∞–ї–ї–Њ–≤ –њ–Њ —И–Ї–∞–ї–µ EDSS (Expanded Disability Status Scale), –∞–≤–Њ–љ–µ–Ї—Б–∞ – –і–Њ 4,0 –±–∞–ї–ї–Њ–≤, –љ–Њ –≤ –ї—О–±–Њ–Љ —Б–ї—Г—З–∞–µ –±–Њ–ї—М–љ–Њ–є –і–Њ–ї–ґ–µ–љ –±—Л—В—М —Е–Њ–і—П—З–Є–Љ.
–Т—Б–µ b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ—Л –≤—Л–Ј—Л–≤–∞—О—В –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —И–Є—А–Њ–Ї–Є–є —Б–њ–µ–Ї—В—А –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤ –љ–∞—З–∞–ї–µ –ї–µ—З–µ–љ–Є—П. –Э–∞–Є–±–Њ–ї–µ–µ —Б—Г—Й–µ—Б—В–≤–µ–љ–љ—Л–Љ–Є –Є–Ј –љ–Є—Е —П–≤–ї—П—О—В—Б—П –Љ–µ—Б—В–љ—Л–µ –Ї–Њ–ґ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є (–Є–љ–Њ–≥–і–∞ –≤–њ–ї–Њ—В—М –і–Њ –љ–µ–Ї—А–Њ–Ј–∞) –Є –≥—А–Є–њ–њ–Њ–њ–Њ–і–Њ–±–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л (–њ–Њ–≤—Л—И–µ–љ–Є–µ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, –љ–µ–і–Њ–Љ–Њ–≥–∞–љ–Є–µ, –Љ–Є–∞–ї–≥–Є–Є) – “–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤—Л–є –≥—А–Є–њ–њ”. –Ю–і–љ–∞–Ї–Њ —Н—В–Є —П–≤–ї–µ–љ–Є—П —Б–Њ –≤—А–µ–Љ–µ–љ–µ–Љ –Є—Б—З–µ–Ј–∞—О—В, –∞ –Є—Е –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Љ–Њ–ґ–љ–Њ –њ—А–µ–і—Г–њ—А–µ–і–Є—В—М. –С–Њ–ї–Є –Є –Ї–Њ–ґ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ –Љ–µ—Б—В–µ –Є–љ—К–µ–Ї—Ж–Є–Є –Љ–Њ–≥—Г—В –±—Л—В—М —Г–Љ–µ–љ—М—И–µ–љ—Л —Б–Њ–±–ї—О–і–µ–љ–Є–µ–Љ –њ—А–∞–≤–Є–ї –Є—Е –њ—А–Њ–≤–µ–і–µ–љ–Є—П (—Б–Љ–µ–љ–Њ–є –Ј–Њ–љ –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞), –њ—А–Њ—В–Є—А–∞–љ–Є–µ–Љ —Н—В–Њ–є –Њ–±–ї–∞—Б—В–Є –Ї—Г—Б–Њ—З–Ї–Њ–Љ –ї—М–і–∞ –і–Њ –Є –њ–Њ—Б–ї–µ –Є–љ—К–µ–Ї—Ж–Є–Є. –Ъ–Њ–ґ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –њ—А–Њ—П–≤–ї—П—О—В—Б—П –Љ–µ–љ—М—И–µ, –µ—Б–ї–Є —В—Й–∞—В–µ–ї—М–љ–Њ —А–∞—Б—В–≤–Њ—А—П—В—М –њ—А–µ–њ–∞—А–∞—В –Є –њ–µ—А–µ–і –≤–≤–µ–і–µ–љ–Є–µ–Љ —Б–Њ–≥—А–µ–≤–∞—В—М –µ–≥–Њ –і–Њ –Ї–Њ–Љ–љ–∞—В–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л. “–Ш–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤—Л–є –≥—А–Є–њ–њ” –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤ –љ–∞—З–∞–ї–µ –ї–µ—З–µ–љ–Є—П —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е, –љ–Њ –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –њ–Њ—З—В–Є —Г –≤—Б–µ—Е –њ—А–Њ—Е–Њ–і–Є—В, —З—В–Њ –≤–∞–ґ–љ–Њ –Њ–±—К—П—Б–љ–Є—В—М –±–Њ–ї—М–љ–Њ–Љ—Г. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Н—В–Є —Б–Є–Љ–њ—В–Њ–Љ—Л –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –ї–µ–≥–Ї–Њ –љ–Є–≤–µ–ї–Є—А–Њ–≤–∞—В—М –≤–≤–µ–і–µ–љ–Є–µ–Љ –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ –љ–Њ—З—М –Є –њ—А–Є–µ–Љ–Њ–Љ –Ј–∞ —З–∞—Б –і–Њ –Є–љ—К–µ–Ї—Ж–Є–Є –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ –Є–ї–Є 2-3-—А–∞–Ј–Њ–≤—Л–Љ –њ—А–Є–µ–Љ–Њ–Љ –≤ —Б—Г—В–Ї–Є –Є–±—Г–њ—А–Њ—Д–µ–љ–∞ –Є–ї–Є –њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ–∞. –Т —Ж–µ–ї—П—Е –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ —В–∞–Ї–ґ–µ –і–≤—Г–Ї—А–∞—В–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –і–Њ–Ј—Л –≤–Њ –≤—А–µ–Љ—П –њ–µ—А–≤—Л—Е –≤–≤–µ–і–µ–љ–Є–є –њ—А–µ–њ–∞—А–∞—В–∞.
–Ф—А—Г–≥–Є–Љ–Є –Ј–љ–∞—З–Є–Љ—Л–Љ–Є –њ–Њ–±–Њ—З–љ—Л–Љ–Є –і–µ–є—Б—В–≤–Є—П–Љ–Є –±–µ—В–∞—Д–µ—А–Њ–љ–∞ —П–≤–ї—П–µ—В—Б—П —В–Њ, —З—В–Њ –Њ–љ —Г—Б–Є–ї–Є–≤–∞–µ—В —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В—М –Є –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤—В—М —А–∞–Ј–≤–Є—В–Є–µ –і–µ–њ—А–µ—Б—Б–Є–Є. –Я–Њ–≤—Л—И–µ–љ–Є–µ –Љ—Л—И–µ—З–љ–Њ–≥–Њ —В–Њ–љ—Г—Б–∞ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г —В–µ—Е –±–Њ–ї—М–љ—Л—Е, —Г –Ї–Њ—В–Њ—А—Л—Е –Њ–љ –±—Л–ї –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—А–∞–ґ–µ–љ –Є –і–Њ –љ–∞—З–∞–ї–∞ —В–µ—А–∞–њ–Є–Є. –Я—А–Є –љ–∞—А–∞—Б—В–∞–љ–Є–Є —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В–Є —Б–ї–µ–і—Г–µ—В —Г–≤–µ–ї–Є—З–Є—В—М –і–Њ–Ј—Г –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤. –†–∞–Ј–≤–Є—В–Є–µ –і–µ–њ—А–µ—Б—Б–Є–Є —В—А–µ–±—Г–µ—В –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ –Є–ї–Є –і–∞–ґ–µ –њ–µ—А–µ—А—Л–≤–∞ –≤ –ї–µ—З–µ–љ–Є–Є.
–£ –∞–≤–Њ–љ–µ–Ї—Б–∞ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В—М –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Љ–µ–љ—М—И–µ. –≠—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ–±—К—П—Б–љ–µ–љ–Њ —В–µ–Љ, —З—В–Њ –Њ–љ –≤–≤–Њ–і–Є—В—Б—П –≤–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ, –∞ –љ–µ –њ–Њ–і–Ї–Њ–ґ–љ–Њ. –Ъ–Њ–ґ–∞ – –∞–Ї—В–Є–≤–љ—Л–є –Є–Љ–Љ—Г–љ–љ—Л–є –Њ—А–≥–∞–љ —Б –Є–Љ–Љ—Г–љ–Њ–Ї–Њ–Љ–њ–µ—В–µ–љ—В–љ—Л–Љ–Є –Ї–ї–µ—В–Ї–∞–Љ–Є, –Ї–Њ—В–Њ—А—Л–µ –Њ–њ–Њ—Б—А–µ–і—Г—О—В –≥—Г–Љ–Њ—А–∞–ї—М–љ—Л–µ –Є –Ї–ї–µ—В–Њ—З–љ—Л–µ –Є–Љ–Љ—Г–љ–љ—Л–µ –Њ—В–≤–µ—В—Л. –Ь—Л—И—Ж—Л –ґ–µ –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є “—В–Є—Е–Є”.
–Ф—А—Г–≥–Є–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ—А–µ–≤–µ–љ—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –Њ—В–ї–Є—З–љ—Л–Љ –њ–Њ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Г –і–µ–є—Б—В–≤–Є—П –Њ—В b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤, —П–≤–ї—П–µ—В—Б—П –Ї–Њ–њ–∞–Ї—Б–Њ–љ. –≠—В–Њ – –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–є –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –њ—А–µ–њ–∞—А–∞—В, –Њ–±–ї–∞–і–∞—О—Й–Є–є –∞–љ—В–Є–≥–µ–љ—Б–њ–µ—Ж–Є—Д–Є—З–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –Ю–љ —Б–Њ—Б—В–Њ–Є—В –Є–Ј 4 –∞–Љ–Є–љ–Њ–Ї–Є—Б–ї–Њ—В – –≥–ї—Г—В–∞–Љ–Є–љ–∞, –ї–Є–Ј–Є–љ–∞, –∞–ї–∞–љ–Є–љ–∞ –Є —В–Є—А–Њ–Ј–Є–љ–∞. –Я—А–µ–њ–∞—А–∞—В –њ–Њ–і–∞–≤–ї—П–µ—В –Ї–ї–µ—В–Њ—З–љ–Њ-–Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є –Њ—В–≤–µ—В –љ–∞ –Њ–і–Є–љ –Є–Ј –Њ—Б–љ–Њ–≤–љ—Л—Е –∞—Г—В–Њ–∞–љ—В–Є–≥–µ–љ–Њ–≤ –¶–Э–° – –Њ—Б–љ–Њ–≤–љ–Њ–є –±–µ–ї–Њ–Ї –Љ–Є–µ–ї–Є–љ–∞. –Т–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤–Є–µ –Ґ-–Ї–ї–µ—В–Њ–Ї —Б –Ї–Њ–њ–∞–Ї—Б–Њ–љ–Њ–Љ, –≤–Љ–µ—Б—В–Њ –Њ—Б–љ–Њ–≤–љ–Њ–≥–Њ –±–µ–ї–Ї–∞ –Љ–Є–µ–ї–Є–љ–∞, –≤–µ–і–µ—В –Ї –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О —Б—Г–њ—А–µ—Б—Б–Њ—А–љ—Л—Е –Ї–Њ–њ–∞–Ї—Б–Њ–љ-—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є—Е –Ґ-–Ї–ї–µ—В–Њ–Ї. –≠—В–Є –Ї–ї–µ—В–Ї–Є, –њ—А–Њ–љ–Є–Ї–∞—П –≤ –¶–Э–°, —Б–µ–Ї—А–µ—В–Є—А—Г—О—В –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ —Д–∞–Ї—В–Њ—А—Л, –Ї–Њ—В–Њ—А—Л–µ —В–Њ—А–Љ–Њ–Ј—П—В —А–∞–Ј–≤–Є—В–Є–µ –Є–Љ–Љ—Г–љ–љ–Њ–≥–Њ –Њ—В–≤–µ—В–∞, –њ—А–Є–≤–Њ–і—П—Й–µ–≥–Њ –Ї –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є. –Я—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і—П—В –µ–ґ–µ–і–љ–µ–≤–љ–Њ, –њ–Њ–і–Ї–Њ–ґ–љ–Њ, –≤ –і–Њ–Ј–µ 20 –Љ–≥ –Њ–љ –≤—Л–Ј—Л–≤–∞–µ—В –ї–Є—И—М –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –њ–Њ–±–Њ—З–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ –≤–Є–і–µ –њ–Њ–Ї—А–∞—Б–љ–µ–љ–Є—П –Є —Г–њ–ї–Њ—В–љ–µ–љ–Є—П –≤ –Љ–µ—Б—В–µ –Є–љ—К–µ–Ї—Ж–Є–є, –Є —Г –љ–µ–±–Њ–ї—М—И–Њ–≥–Њ —З–Є—Б–ї–∞ –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞—О—В—Б—П —Б–Є—Б—В–µ–Љ–љ—Л–µ –њ–Њ—Б—В–Є–љ—К–µ–Ї—Ж–Є–Њ–љ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є –≤ –≤–Є–і–µ –Њ–±—Й–µ–є –≥–Є–њ–µ—А–µ–Љ–Є–Є, –Њ—Й—Г—Й–µ–љ–Є—П —Б—В—П–≥–Є–≤–∞–љ–Є—П –≤ –≥—А—Г–і–љ–Њ–є –Ї–ї–µ—В–Ї–µ, –Њ–і—Л—И–Ї–Є, —Б–µ—А–і—Ж–µ–±–Є–µ–љ–Є—П. –≠—В–Є —П–≤–ї–µ–љ–Є—П –њ—А–Њ—Е–Њ–і—П—В —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Љ–Є–љ—Г—В, –љ–µ —В—А–µ–±—Г—П –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є.
–Ю–њ—Л—В–∞ —Б–Њ–≤–Љ–µ—Б—В–љ–Њ–≥–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є—П b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤ –Є –Ї–Њ–њ–∞–Ї—Б–Њ–љ–∞ –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–µ—В, –љ–Њ –і–Њ–Ї–∞–Ј–∞–љ–∞ –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В—М –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –љ–∞ –Є—Е —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–∞–Љ–Є (–≤ —Б–ї—Г—З–∞–µ –≤–Њ–Ј–љ–Є–Ї—И–µ–≥–Њ –Њ–±–Њ—Б—В—А–µ–љ–Є—П).
–Э–∞–Є–±–Њ–ї–µ–µ –≤–∞–ґ–љ—Л–µ –≤–Њ–њ—А–Њ—Б—Л, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–µ –њ—А–Є –љ–∞–Ј–љ–∞—З–µ–љ–Є–Є –њ—А–µ–≤–µ–љ—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є: –Ї–Њ–Љ—Г –љ–∞–Ј–љ–∞—З–∞—В—М —Н—В–Њ –ї–µ—З–µ–љ–Є–µ, –Ї–Њ–≥–і–∞ –µ–≥–Њ –љ–∞—З–Є–љ–∞—В—М –Є –Ї–Њ–≥–і–∞ –њ—А–µ–Ї—А–∞—Й–∞—В—М, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є —Н—В–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П?
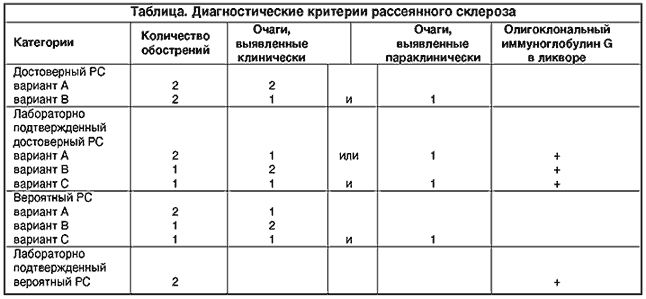
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–µ—Б–Њ–Љ–љ–µ–љ–љ—Л–Љ–Є –њ–Њ–Ї–∞–Ј–∞–љ–Є—П–Љ–Є –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О —Б—А–µ–і—Б—В–≤ –Љ–Њ–і–Є—Д–Є—Ж–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є —П–≤–ї—П—О—В—Б—П –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–є PC (—Б–Љ. —В–∞–±–ї.), —А–µ–Љ–Є—В—В–Є—А—Г—О—Й–µ–µ —В–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П (–і–ї—П –±–µ—В–∞—Д–µ—А–Њ–љ–∞ —В–∞–Ї–ґ–µ –Є –≤—В–Њ—А–Є—З–љ–Њ-–њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–є PC), –≤–Њ–Ј—А–∞—Б—В –њ–∞—Ж–Є–µ–љ—В–∞ –Њ—В 18 –і–Њ 50 –ї–µ—В, –љ–µ–≥—А—Г–±–∞—П –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є—П. –Э–∞—З–Є–љ–∞—В—М —В–∞–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В –Ї–∞–Ї –Љ–Њ–ґ–љ–Њ —А–∞–љ—М—И–µ, —В–∞–Ї –Ї–∞–Ї –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –∞–Ї—Б–Њ–љ–Њ–≤, –≤–µ–і—Г—Й–µ–µ –≤ –і–∞–ї—М–љ–µ–є—И–µ–Љ –Ї —А–∞–Ј–≤–Є—В–Є—О –љ–µ–Њ–±—А–∞—В–Є–Љ–Њ–≥–Њ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ—Д–µ–Ї—В–∞, –љ–∞—З–Є–љ–∞–µ—В—Б—П —Г–ґ–µ –љ–∞ –љ–∞—З–∞–ї—М–љ–Њ–є —Б—В–∞–і–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П. –Я—А–µ–Ї—А–∞—Й–∞—В—М –ґ–µ –ї–µ—З–µ–љ–Є–µ —Н—В–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Є–ї–Є –Ј–∞–Љ–µ–љ—П—В—М –Є—Е —Б–ї–µ–і—Г–µ—В –њ—А–Є –љ–µ–њ–µ—А–µ–љ–Њ—Б–Є–Љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–∞—Е –Є –≤ —Б–ї—Г—З–∞–µ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П. –Ю—В—Б—Г—В—Б—В–≤–Є–µ–Љ —Н—Д—Д–µ–Ї—В–∞ —Б–ї–µ–і—Г–µ—В —Б—З–Є—В–∞—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є—П 3 –Ї—Г—А—Б–Њ–≤ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Ј–∞ 1 –≥–Њ–і –Є–ї–Є –љ–µ—Г–Ї–ї–Њ–љ–љ–Њ–µ –љ–∞—А–∞—Б—В–∞–љ–Є–µ –Є–љ–≤–∞–ї–Є–і–Є–Ј–∞—Ж–Є–Є –≤ —В–µ—З–µ–љ–Є–µ 6 –Љ–µ—Б—П—Ж–µ–≤ –ї–µ—З–µ–љ–Є—П.
–Т –Ї–∞—З–µ—Б—В–≤–µ –∞–ї—М—В–µ—А–љ–∞—В–Є–≤–љ–Њ–є –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є –њ—А–µ–і–ї–Њ–ґ–µ–љ–Њ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞ G. –Ю–љ —В–∞–Ї–ґ–µ –≤–ї–Є—П–µ—В –љ–∞ —З–∞—Б—В–Њ—В—Г –Њ–±–Њ—Б—В—А–µ–љ–Є–є –Є –љ–∞—А–∞—Б—В–∞–љ–Є–µ –Є–љ–≤–∞–ї–Є–і–Є–Ј—Ж–Є–Є. –Я—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і—П—В –Є–Ј —А–∞—Б—З–µ—В–∞ 0,2-0,4 –≥/–Ї–≥ –≤ —В–µ—З–µ–љ–Є–µ 5 –і–љ–µ–є, –∞ –Ј–∞—В–µ–Љ –≤ —В–∞–Ї–Њ–є –ґ–µ –і–Њ–Ј–µ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ –Ї–∞–ґ–і—Л–µ 2 –Љ–µ—Б—П—Ж–∞. –Я—А–µ–і–ї–∞–≥–∞—О—В—Б—П –Є –і—А—Г–≥–Є–µ —Б—Е–µ–Љ—Л –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П – 1 –≥/–Ї–≥ –µ–ґ–µ–Љ–µ—Б—П—З–љ–Њ. –Ю–і–љ–∞–Ї–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –±–Њ–ї—М—И–Є—Е –і–Њ–Ј –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–±—Г–ї–Є–љ–∞ —Б–≤—П–Ј–∞–љ–Њ —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ-—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є –њ–Њ—З–µ—З–љ—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –∞ —В–∞–Ї–ґ–µ —В—А–Њ–Љ–±–Њ—Н–Љ–±–Њ–ї–Є–Є. –Т –њ–µ—А–≤—Л–µ —З–∞—Б—Л –њ–Њ—Б–ї–µ –Є–љ—Д—Г–Ј–Є–Є –Љ–Њ–≥—Г—В –Њ—В–Љ–µ—З–∞—В—М—Б—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –Љ–Є–∞–ї–≥–Є—П, –Њ–Ј–љ–Њ–±, –ї–Є—Е–Њ—А–∞–і–Ї–∞. –≠—В–Є —П–≤–ї–µ–љ–Є—П –Ї—Г–њ–Є—А—Г—О—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ —Б–Ї–Њ—А–Њ—Б—В–Є –≤–≤–µ–і–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞, –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤ –Є –∞–љ—В–Є–≥–Є—Б—В–∞–Љ–Є–љ–љ—Л—Е —Б—А–µ–і—Б—В–≤. –Т–љ—Г—В—А–Є–≤–µ–љ–љ—Л–є –Є–Љ–Љ—Г–љ–Њ–≥–ї–Њ–Њ–±—Г–ї–Є–љ —Г—Б–њ–µ—И–љ–Њ –њ—А–Є–Љ–µ–љ—П–ї—Б—П —Г –±–µ—А–µ–Љ–µ–љ–љ—Л—Е –ґ–µ–љ—Й–Є–љ —Б PC –і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П –њ–Њ—Б–ї–µ—А–Њ–і–Њ–≤–Њ–≥–Њ –Њ–±–Њ—Б—В—А–µ–љ–Є—П.
–Ъ—Г–њ–Є—А–Њ–≤–∞–љ–Є–µ –Њ–±–Њ—Б—В—А–µ–љ–Є–є
–Т –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –ї–µ—З–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е –Њ–±–Њ—Б—В—А–µ–љ–Є–є PC –≤—Л—Б–Њ–Ї–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –Љ–µ—В–Є–ї–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –≤—Л—В–µ—Б–љ–Є–ї–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –∞–і—А–µ–љ–Њ–Ї–Њ—А—В–Є–Ї–Њ—В—А–Њ–њ–љ–Њ–≥–Њ –≥–Њ—А–Љ–Њ–љ–∞ –Є –µ–≥–Њ —Б–Є–љ—В–µ—В–Є—З–µ—Б–Ї–Є—Е –∞–љ–∞–ї–Њ–≥–Њ–≤. –С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –Њ–±–Њ—Б—В—А–µ–љ–Є–є —Б–Њ–≤–њ–∞–і–∞–µ—В –њ–Њ –≤—А–µ–Љ–µ–љ–Є —Б –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є–µ–Љ –љ–Њ–≤—Л—Е –∞–Ї—В–Є–≤–љ—Л—Е –Њ—З–∞–≥–Њ–≤ –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є, –≤—Л—П–≤–ї—П–µ–Љ—Л—Е –њ—А–Є –Ь–†–Ґ-–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Є —Б–њ–Є–љ–љ–Њ–Љ –Љ–Њ–Ј–≥–µ, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г–µ—В –Њ –љ–Њ–≤–Њ–є –≤–Њ–ї–љ–µ –≤–Њ—Б–њ–∞–ї–µ–љ–Є—П. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–Њ–≤ —Г—Б–Ї–Њ—А—П–µ—В –Є—Е –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ. –Ю–і–љ–∞–Ї–Њ –њ–Њ—Б–ї–µ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—П –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –Љ–Њ–ґ–µ—В –љ–∞–±–ї—О–і–∞—В—М—Б—П –љ–Њ–≤–∞—П –≤—Б–њ—Л—И–Ї–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –±–Њ–ї–µ–Ј–љ–Є, —З—В–Њ —В–∞–Ї–ґ–µ –Њ—В—А–∞–ґ–∞—О—В –і–∞–љ–љ—Л–µ –Ь–†–Ґ. –≠—В–Њ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–≤—П–Ј–∞–љ–Њ —Б–Њ —Б–Ї–Њ—А–Њ—Б—В—М—О –Њ—В–Љ–µ–љ—Л –≥–Њ—А–Љ–Њ–љ–Њ–≤, –њ–Њ—Н—В–Њ–Љ—Г –љ–∞–Є–±–Њ–ї–µ–µ –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–≤–µ–і–µ–љ–Є–µ “–њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є–Є” —Б –≤–љ—Г—В—А–Є–≤–µ–љ–љ—Л–Љ –≤–≤–µ–і–µ–љ–Є–µ–Љ –Љ–µ—В–Є–ї–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –Є –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –њ–µ—А–µ—Е–Њ–і–Њ–Љ –љ–∞ –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–љ–µ–є: –≤ —В–µ—З–µ–љ–Є–µ 3-7 –і–љ–µ–є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –≤–≤–Њ–і—П—В 1-2 –≥ –Љ–µ—В–Є–ї–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ (–њ—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і—П—В —Б 400-500 –Љ–ї —Д–Є–Ј. —А–∞—Б—В–≤–Њ—А–∞ –≤ —В–µ—З–µ–љ–Є–µ 1-2 —З–∞—Б–Њ–≤), –Ј–∞—В–µ–Љ –љ–∞–Ј–љ–∞—З–∞—О—В –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ – 4 –і–љ—П –њ–Њ 200 –Љ–≥, 4 –і–љ—П –њ–Њ 100 –Љ–≥, 2 –і–љ—П –њ–Њ 50 –Љ–≥ –Є –і–∞–ї–µ–µ, —Б–љ–Є–ґ–∞—П –і–Њ–Ј—Г –Ї–∞–ґ–і—Л–є –і–µ–љ—М –љ–∞ 10 –Љ–≥. –Я—А–µ–і–ї–∞–≥–∞—О—В—Б—П –Є –і—А—Г–≥–Є–µ —Б—Е–µ–Љ—Л –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –њ–Њ—Б–ї–µ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П –≥–Њ—А–Љ–Њ–љ–∞ – 2 –і–љ—П –њ–Њ 80 –Љ–≥, 2 –і–љ—П –њ–Њ 60 –Љ–≥, 2 –і–љ—П –њ–Њ 40 –Љ–≥ —Б –њ–Њ—Б–ї–µ–і—Г—О—Й–Є–Љ –µ–ґ–µ–і–љ–µ–≤–љ—Л–Љ —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –і–Њ–Ј—Л –љ–∞ 5-10 –Љ–≥. –Ґ–∞–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –Њ–±—Л—З–љ–Њ —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П. –Я—А–µ–њ–∞—А–∞—В –≤—Б–µ–≥–і–∞ –љ–∞–Ј–љ–∞—З–∞—О—В –µ–і–Є–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –≤ –њ–µ—А–≤—Г—О –њ–Њ–ї–Њ–≤–Є–љ—Г –і–љ—П. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –њ–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –±–µ—Б—Б–Њ–љ–љ–Є—Ж–∞ –Є –ї–µ–≥–Ї–∞—П —Н–є—Д–Њ—А–Є—П, —В—А–µ–≤–Њ–≥–∞, –Љ–µ—В–∞–ї–ї–Є—З–µ—Б–Ї–Є–є –њ—А–Є–≤–Ї—Г—Б –≤–Њ —А—В—Г –≤–Њ –≤—А–µ–Љ—П –Є–љ—Д—Г–Ј–Є–Є, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –∞–њ–њ–µ—В–Є—В–∞, —В–Њ—И–љ–Њ—В–∞, –ґ–µ–ї—Г–і–Њ—З–љ–Њ-–Ї–Є—И–µ—З–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞, –≥–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є, –Љ–Є–∞–ї–≥–Є–Є, –Є–Ї–Њ—В–∞. –†–µ–ґ–µ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –±–Њ–ї–µ–µ —Б–µ—А—М–µ–Ј–љ—Л–µ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П – —А–∞–Ј–≤–Є—В–Є–µ –њ—Б–Є—Е–Њ–Ј–∞, —Б–µ—А–і–µ—З–љ—Л—Е –∞—А–Є—В–Љ–Є–є, –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є. –≠—В–Њ —В—А–µ–±—Г–µ—В –±—Л—Б—В—А–Њ–є –Є –Ї–≤–∞–ї–Є—Д–Є—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є, –њ–Њ—Н—В–Њ–Љ—Г –ї–µ—З–µ–љ–Є–µ –≥–ї—О–Ї–Њ–Ї–Њ—А—В–Є–Ї–Њ–Є–і–∞–Љ–Є –љ—Г–ґ–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е. –Ф–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —Г–ї—М—Ж–µ—А–Њ–≥–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ —Б –љ–Є–Љ–Є –≤ –Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ–Љ –њ–Њ—А—П–і–Ї–µ —Б–ї–µ–і—Г–µ—В –љ–∞–Ј–љ–∞—З–Є—В—М –±–ї–Њ–Ї–∞—В–Њ—А—Л –Э2-–≥–Є—Б—В–∞–Љ–Є–љ–Њ–≤—Л—Е —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤. –Ф–ї—П –≤–Њ—Б–њ–Њ–ї–љ–µ–љ–Є—П –њ–Њ—В–µ—А—М –Ї–∞–ї–Є—П –Є –Ї–∞–ї—М—Ж–Є—П –љ–∞–Ј–љ–∞—З–∞—О—В –∞—Б–њ–∞—А–Ї–∞–Љ, –њ–∞–љ–∞–љ–≥–Є–љ, —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В —Г–њ–Њ—В—А–µ–±–ї—П—В—М –≤ –њ–Є—Й—Г –±–∞–љ–∞–љ—Л. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Б–ї–µ–і—Г–µ—В –Њ–≥—А–∞–љ–Є—З–Є—В—М –њ–Њ—В—А–µ–±–ї–µ–љ–Є–µ –ґ–Є–і–Ї–Њ—Б—В–Є –Є –њ—А–Є–Љ–µ–љ—П—В—М –Ї–∞–ї–Є–є—Б–±–µ—А–µ–≥–∞—О—Й–Є–µ –Љ–Њ—З–µ–≥–Њ–љ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ (—Б–њ–Є—А–Њ–љ–Њ–ї–∞–Ї—В–Њ–љ). –Ш–љ–Њ–≥–і–∞ –њ–Њ—Б–ї–µ –Њ—В–Љ–µ–љ—Л –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г—Е—Г–і—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П, –≤ —Н—В–Є—Е —Б–ї—Г—З–∞—П—Е –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –≤–љ–Њ–≤—М –љ–∞–Ј–љ–∞—З–Є—В—М 20-40 –Љ–≥ –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –Є –Њ–њ—П—В—М –Љ–µ–і–ї–µ–љ–љ–Њ —Б–љ–Є–ґ–∞—В—М –µ–≥–Њ –і–Њ–Ј—Г.
–Ф–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –љ–µ–±–Њ–ї—М—И–Є—Е –і–Њ–Ј —Б—В–µ—А–Њ–Є–і–Њ–≤ –љ–µ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —В–∞–Ї –Ї–∞–Ї –≤–µ—Б—М–Љ–∞ –≤–µ—А–Њ—П—В–љ–Њ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е –Є–Ј–≤–µ—Б—В–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є –њ—А–Є –Њ—В—Б—Г—В—Б—В–≤–Є–Є –Ј–љ–∞—З–Є–Љ–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є. –Ш–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ–µ (–±–µ–Ј –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–≥–Њ –≤–≤–µ–і–µ–љ–Є—П) –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –≤—Л—Б–Њ–Ї–Є—Е –і–Њ–Ј –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ (1-1,5 –Љ–≥/–Ї–≥) –і–∞–µ—В –Ї—А–∞—В–Ї–Њ–≤—А–µ–Љ–µ–љ–љ—Л–є —А–µ–Ј—Г–ї—М—В–∞—В, –љ–Њ, –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ—А–Њ–≤–µ–і–µ–љ–Є–µ–Љ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ–є –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є–Є, –њ—А–Є–≤–Њ–і–Є—В –Ї –±–Њ–ї—М—И–µ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ.
–У–Њ—А–Љ–Њ–љ–∞–ї—М–љ–∞—П –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є—П –љ–µ —В–Њ–ї—М–Ї–Њ –Ї—Г–њ–Є—А—Г–µ—В –Њ–±–Њ—Б—В—А–µ–љ–Є—П PC, –љ–Њ –Є –Ј–∞–Љ–µ–і–ї—П–µ—В —А–∞–Ј–≤–Є—В–Є–µ –Ї–∞–Ї —А–µ–Љ–Є—В—В–Є—А—Г—О—Й–µ–≥–Њ, —В–∞–Ї –Є –≤—В–Њ—А–Є—З–љ–Њ-–њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–≥–Њ PC. –Я–∞—Ж–Є–µ–љ—В–∞–Љ —Б —Н—В–Њ–є —Д–Њ—А–Љ–Њ–є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Љ–Њ–ґ–љ–Њ –њ—А–Њ–≤–Њ–і–Є—В—М —В–∞–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ 1-2 —А–∞–Ј–∞ –≤ –≥–Њ–і –Є–ї–Є –≤–≤–Њ–і–Є—В—М –Ї–∞–ґ–і—Л–µ 2 –Љ–µ—Б—П—Ж–∞ –њ–Њ 500 –Љ–≥ –Љ–µ—В–Є–ї–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –≤ —В–µ—З–µ–љ–Є–µ 3 –і–љ–µ–є. –Т–љ—Г—В—А–Є–≤–µ–љ–љ–∞—П –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–∞—П –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є—П –њ–Њ–Ї–∞–Ј–∞–љ–∞ –Є –њ—А–Є –ї–µ—З–µ–љ–Є–Є –Љ–Њ–љ–Њ—Б–Є–Љ–њ—В–Њ–Љ–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є PC, –≤ —З–∞—Б—В–љ–Њ—Б—В–Є, —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–≥–Њ –љ–µ–≤—А–Є—В–∞. –Т–µ—Б—М–Љ–∞ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –µ–≥–Њ –≤–≤–µ–і–µ–љ–Є–µ–Љ –і–µ–Ї—Б–∞–Љ–µ—В–∞–Ј–Њ–љ–∞ —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Љ–љ–Њ–≥–Є–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї—П–Љ–Є —Б—З–Є—В–∞–µ—В—Б—П –љ–µ—Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ—Л–Љ. –Ю–і–љ–Њ–є –Є–Ј —Б—Е–µ–Љ –і–ї—П –ї–µ—З–µ–љ–Є—П —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–≥–Њ –љ–µ–≤—А–Є—В–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–ї–µ–і—Г—О—Й–∞—П: –≤ —В–µ—З–µ–љ–Є–µ 3 –і–љ–µ–є –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ, –Ї–∞–ґ–і—Л–µ 6 —З–∞—Б–Њ–≤ –≤–≤–Њ–і—П—В –њ–Њ 250 –Љ–≥ –Љ–µ—В–Є–ї–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –љ–∞ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ —А–∞—Б—В–≤–Њ—А–µ —Е–ї–Њ—А–Є–і–∞ –љ–∞—В—А–Є—П, –Ј–∞—В–µ–Љ –≤ —В–µ—З–µ–љ–Є–µ 10 –і–љ–µ–є –љ–∞–Ј–љ–∞—З–∞—О—В –њ–µ—А–Њ—А–∞–ї—М–љ—Л–є –њ—А–Є–µ–Љ –њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ –Є–Ј —А–∞—Б—З–µ—В–∞ 1 –Љ–≥/–Ї–≥ –Є –≤ —В–µ—З–µ–љ–Є–µ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е 3 –і–љ–µ–є –±—Л—Б—В—А–Њ —Б–љ–Є–ґ–∞—О—В —Н—В—Г –і–Њ–Ј—Г. –Х—Б–ї–Є —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ—Л–є –љ–µ–≤—А–Є—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –±–Њ–ї—М—О –≤ –≥–ї–∞–Ј–љ–Њ–Љ —П–±–ї–Њ–Ї–µ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤.
–£ –±–Њ–ї—М–љ—Л—Е —Б –Њ—Б—В—А—Л–Љ–Є, —В—П–ґ–µ–ї—Л–Љ–Є –∞—В–∞–Ї–∞–Љ–Є PC, –љ–µ –њ–Њ–і–і–∞—О—Й–Є–Љ–Є—Б—П –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—О –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–љ–Њ–є —В–µ—А–∞–њ–Є–Є, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –њ–ї–∞–Ј–Љ–∞—Д–µ—А–µ–Ј–∞. –Х–≥–Њ –Љ–Њ–ґ–љ–Њ —В–∞–Ї–ґ–µ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞—В—М —Б –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є –Є –і—А—Г–≥–Њ–є –Є–Љ–Љ—Г–љ–Њ—Б—Г–њ—А–µ—Б—Б–Њ—А–љ–Њ–є —В–µ—А–∞–њ–Є–µ–є. –Я—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —В–∞–Ї–Њ–≥–Њ –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ 2 –љ–µ–і–µ–ї—М –і–Њ 5 —А–∞–Ј –Њ–±–Љ–µ–љ–Є–≤–∞–µ—В—Б—П 1,5 –Њ–±—К–µ–Љ–∞ –њ–ї–∞–Ј–Љ—Л –Ј–∞ –Ї–∞–ґ–і—Л–є —Б–µ–∞–љ—Б; –њ–Њ—Б–ї–µ –њ—А–Њ—Ж–µ–і—Г—А—Л –њ–ї–∞–Ј–Љ–∞—Д–µ—А–µ–Ј–∞ –≤–љ—Г—В—А–Є–≤–µ–љ–љ–Њ –Ї–∞–њ–µ–ї—М–љ–Њ –≤–≤–Њ–і–Є—В—Б—П 500-1000 –Љ–≥ –Љ–µ—В–Є–ї–њ—А–µ–і–љ–Є–Ј–Њ–ї–Њ–љ–∞ —Б 400 –Љ–ї —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ —А–∞—Б—В–≤–Њ—А–∞ —Е–ї–Њ—А–Є–і–∞ –љ–∞—В—А–Є—П. –Я—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–µ–Љ –Ї –њ—А–Є–Љ–µ–љ–µ–љ–Є—О –њ–ї–∞–Ј–Љ–∞—Д–µ—А–µ–Ј–∞ —П–≤–ї—П–µ—В—Б—П —П–Ј–≤–µ–љ–љ–∞—П –±–Њ–ї–µ–Ј–љ—М. –Э–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л–Љ–Є –њ–Њ–±–Њ—З–љ—Л–Љ–Є —П–≤–ї–µ–љ–Є—П–Љ–Є –Њ–±–Љ–µ–љ–љ–Њ–≥–Њ –њ–µ—А–µ–ї–Є–≤–∞–љ–Є—П –њ–ї–∞–Ј–Љ—Л —П–≤–ї—П—О—В—Б—П –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–Њ—В–Њ–љ–Є—П –Є –њ–µ—А–Є–Њ—А–∞–ї—М–љ—Л–µ –њ–∞—А–µ—Б—В–µ–Ј–Є–Є. –Я–ї–∞–Ј–Љ–∞—Д–µ—А–µ–Ј –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –њ—А–Є —В—П–ґ–µ–ї—Л—Е –∞—В–∞–Ї–∞—Е PC, –љ–µ–ґ–µ–ї–Є –њ—А–Є –ї–µ–≥–Ї–Є—Е.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ –Є–Љ–µ—О—Й–Є–µ—Б—П –і–∞–љ–љ—Л–µ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ –≤–ї–Є—П–љ–Є–Є –љ–∞ —В–µ—З–µ–љ–Є–µ PC –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Ж–Є—В–Њ—Б—В–∞—В–Є–Ї–Њ–≤ (–∞–Ј–∞—В–Є–Њ–њ—А–Є–љ–∞, –Љ–µ—В–Њ—В—А–µ–Ї—Б–∞—В–∞, —Ж–Є–Ї–ї–Њ—Д–Њ—Б—Д–∞–Љ–Є–і–∞, —Ж–Є–Ї–ї–Њ—Б–њ–Њ—А–Є–љ–∞ –Р), —Б–ї–µ–і—Г–µ—В –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Њ–њ—А–∞–≤–і–∞–љ–Њ –ї–Є—И—М –њ—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–Њ–є –Є –і—А—Г–≥–Њ–є –Є–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–є —В–µ—А–∞–њ–Є–Є. –Я—А–Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–Љ —Н—Д—Д–µ–Ї—В–µ —Н—В–Є –њ—А–µ–њ–∞—А–∞—В—Л –≤—Л–Ј—Л–≤–∞—О—В –Њ—З–µ–љ—М –Љ–љ–Њ–≥–Њ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤, –Є –±–Њ–ї—М–љ—Л–Љ —Б —Е–Њ—А–Њ—И–Є–Љ –њ—А–Њ–≥–љ–Њ–Ј–Њ–Љ –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Ї–∞—В–µ–≥–Њ—А–Є—З–µ—Б–Ї–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Њ.
–Я—А–Є –Њ–±–Њ—Б—В—А–µ–љ–Є—П—Е, –∞ —В–∞–Ї–ґ–µ –≤ —Б—В–∞–і–Є–Є —А–µ–Љ–Є—Б—Б–Є–Є –љ–∞–Ј–љ–∞—З–∞—О—В –Є “–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї—Г—О” —В–µ—А–∞–њ–Є—О, –≤–Ї–ї—О—З–∞—О—Й—Г—О –љ–Њ–Њ—В—А–Њ–њ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (—Ж–µ—А–µ–±—А–Њ–ї–Є–Ј–Є–љ, –њ–Є—А–∞—Ж–µ—В–∞–Љ, –њ–Є—А–Є—В–Є–љ–Њ–ї), –ї–Є–њ–Њ—В—А–Њ–њ–љ—Л–µ (—Н—Б—Б–µ–љ—Ж–Є–∞–ї–µ), —Б–Њ—Б—Г–і–Є—Б—В—Л–µ (–њ–µ–љ—В–Њ–Ї—Б–Є—Д–Є–ї–ї–Є–љ, –≤–Є–љ–њ–Њ—Ж–µ—В–Є–љ) –Є –≤–Є—В–∞–Љ–Є–љ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–≥—А—Г–њ–њ—Л –Т –Є —В–Њ–Ї–Њ—Д–µ—А–Њ–ї). –¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М –Є—Е –љ–∞–Ј–љ–∞—З–µ–љ–Є—П –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М—О –њ–Њ–і–і–µ—А–ґ–∞–љ–Є—П —Д—Г–љ–Ї—Ж–Є–Є –∞–Ї—Б–Њ–љ–Њ–≤ –Є –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –∞–Ї—Б–Њ–љ–Њ–њ–∞—В–Є–Є.
–°–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П
–І—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ–Њ –Є –≤ –њ–µ—А–Є–Њ–і –Љ–µ–ґ–і—Г –Њ–±–Њ—Б—В—А–µ–љ–Є—П–Љ–Є –њ—А–Њ–≤–Њ–і–Є—В—М –∞–Ї—В–Є–≤–љ—Г—О, –∞–і–µ–Ї–≤–∞—В–љ—Г—О —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї—Г—О —В–µ—А–∞–њ–Є—О. –Ф–ї—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –ґ–µ —Б –њ–µ—А–≤–Є—З–љ–Њ-–њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–Є–Љ —В–µ—З–µ–љ–Є–µ–Љ PC –Њ–љ–∞ —З–∞—Б—В–Њ —П–≤–ї—П–µ—В—Б—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ —Б–њ–Њ—Б–Њ–±–Њ–Љ –Њ–±–ї–µ–≥—З–µ–љ–Є—П –Є—Е —Б–Њ—Б—В–Њ—П–љ–Є—П. –Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Љ–µ—О—В—Б—П –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —А–µ–∞–ї—М–љ–Њ–≥–Њ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П –љ–∞ –Њ—Б–љ–Њ–≤–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П.
–Ф–ї—П –Љ–љ–Њ–≥–Є—Е –±–Њ–ї—М–љ—Л—Е PC –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є –њ—А–Њ–±–ї–µ–Љ–Њ–є —П–≤–ї—П–µ—В—Б—П –Њ–±—Й–∞—П —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, –≤—Б—В—А–µ—З–∞—О—Й–∞—П—Б—П –≤ 75-92% —Б–ї—Г—З–∞–µ–≤. –≠—В–Њ—В —Б–Є–Љ–њ—В–Њ–Љ —З–∞—Б—В–Њ –љ–µ–і–Њ–Њ—Ж–µ–љ–Є–≤–∞–µ—В—Б—П –Є –љ–µ—А–µ–і–Ї–Њ –њ—А–Є–љ–Є–Љ–∞–µ—В—Б—П –Ј–∞ “–Ї–∞–њ—А–Є–Ј” –Є–ї–Є –њ—А–Њ—П–≤–ї–µ–љ–Є–µ “–љ–µ–≤—А–Њ–Ј–∞”. –£—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М –љ–µ —Б–≤—П–Ј–∞–љ–∞ —Б–Њ —Б—В–µ–њ–µ–љ—М—О –њ–∞—А–µ–Ј–∞, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г—Б—Г–≥—Г–±–ї—П–µ—В—Б—П –≤ –ґ–∞—А—Г –Є –њ—А–Є –њ—А–Є–љ—П—В–Є–Є –≥–Њ—А—П—З–µ–є –≤–∞–љ–љ—Л. –Ф–ї—П –µ–µ –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –Њ—З–µ–љ—М –≤–∞–ґ–љ—Л–Љ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–µ –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є –Є –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е —Д–Є–Ј–Є—З–µ—Б–Ї–Є—Е —Г–њ—А–∞–ґ–љ–µ–љ–Є–є (—З—А–µ–Ј–Љ–µ—А–љ–∞—П —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞ –Љ–Њ–ґ–µ—В —Г—Б—Г–≥—Г–±–ї—П—В—М —Н—В–Њ—В —Б–Є–Љ–њ—В–Њ–Љ). –Я—А–µ–њ–∞—А–∞—В–Њ–Љ –≤—Л–±–Њ—А–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П –∞–Љ–∞–љ—В–∞–і–Є–љ. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ–є –і–Њ–Ј–Њ–є —П–≤–ї—П–µ—В—Б—П 100 –Љ–≥ –≤ —Б—Г—В–Ї–Є. –Ф–ї—П —Г–≤–µ–ї–Є—З–µ–љ–Є—П –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В–Є –µ–≥–Њ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В “–Ї–∞–љ–Є–Ї—Г–ї—Л” –љ–∞ 1-2 –і–љ—П –≤ –љ–µ–і–µ–ї—О. –Я—А–Є –µ–≥–Њ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Б–µ–ї–µ–≥–Є–ї–Є–љ – –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–є –њ—А–µ–њ–∞—А–∞—В - –≤ –і–Њ–Ј–µ 5 –Љ–≥/—Б—Г—В.
–І–∞—Б—В—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –њ—А–Є PC —П–≤–ї—П–µ—В—Б—П –Є–љ—В–µ–љ—Ж–Є–Њ–љ–љ—Л–є –Є –њ–Њ—Б—В—Г—А–∞–ї—М–љ—Л–є —В—А–µ–Љ–Њ—А. –Ф—А–Њ–ґ–∞–љ–Є–µ –Љ–Њ–ґ–µ—В –±—Л—В—М –Њ—З–µ–љ—М –≤—Л—А–∞–ґ–µ–љ–љ—Л–Љ –Є –≤–Њ–Ј–љ–Є–Ї–∞—В—М –і–∞–ґ–µ –њ—А–Є –љ–∞–Љ–µ—А–µ–љ–Є–Є –і–≤–Є–ґ–µ–љ–Є—П, –µ—Й–µ –і–Њ –µ–≥–Њ –љ–∞—З–∞–ї–∞, —П–≤–ї—П—П—Б—М –Њ—Б–љ–Њ–≤–љ—Л–Љ –Є–љ–≤–∞–ї–Є–і–Є–Ј–Є—А—Г—О—Й–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ. –Ъ —Б–Њ–ґ–∞–ї–µ–љ–Є—О, —Б–њ–Њ—Б–Њ–±—Л –Ї–Њ—А—А–µ–Ї—Ж–Є–Є —В—А–µ–Љ–Њ—А–∞ –њ—А–Є PC –Љ–∞–ї–Њ—Н—Д—Д–µ–Ї—В–Є–≤–љ—Л. –Э–µ–Ї–Њ—В–Њ—А–Њ–µ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Є–Ј–Њ–љ–Є–∞–Ј–Є–і, –Ї–Њ—В–Њ—А—Л–є –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –≤–ї–Є—П–µ—В –љ–∞ –њ–Њ—Б—В—Г—А–∞–ї—М–љ–Њ–µ, —З–µ–Љ –љ–∞ –Є–љ—В–µ–љ—Ж–Є–Њ–љ–љ–Њ–µ –і—А–Њ–ґ–∞–љ–Є–µ. –Ш–Ј–Њ–љ–Є–∞–Ј–Є–і –њ—А–Є–Љ–µ–љ—П—О—В –≤ –і–Њ–Ј–µ 800-1200 –Љ–≥/—Б—Г—В –≤ —Б–Њ—З–µ—В–∞–љ–Є–Є —Б–Њ 100 –Љ–≥ –њ–Є—А–Є–і–Њ–Ї—Б–Є–љ–∞ (–і–ї—П –њ—А–µ–і—Г–њ—А–µ–ґ–і–µ–љ–Є—П —А–∞–Ј–≤–Є—В–Є—П –њ–Њ–ї–Є–љ–µ–≤—А–Њ–њ–∞—В–Є–Є). –Я–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –Є–Ј–Њ–љ–Є–∞–Ј–Є–і–∞ —П–≤–ї—П—О—В—Б—П –Њ–±—А–∞—В–Є–Љ–Њ–µ –љ–∞—А—Г—И–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–µ—З–µ–љ–Є, —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, –ї–Є—Е–Њ—А–∞–і–Ї–∞, —Б—Л–њ—М, —В–Њ—И–љ–Њ—В–∞, —Г—Б–Є–ї–µ–љ–Є–µ –±—А–Њ–љ—Е–Є–∞–ї—М–љ–Њ–є —Б–µ–Ї—А–µ—Ж–Є–Є. –≠—В–Є —П–≤–ї–µ–љ–Є—П –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–љ—Г—В—М —Г–ґ–µ –њ—А–Є –і–Њ–Ј–µ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ 600 –Љ–≥ –Є, —Г—З–Є—В—Л–≤–∞—П –љ–µ —Б—В–Њ–ї—М –Ј–∞–Љ–µ—В–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –Є–Ј–Њ–љ–Є–∞–Ј–Є–і–∞ –љ–∞ –і—А–Њ–ґ–∞–љ–Є–µ, –љ–µ—А–µ–і–Ї–Њ –Ј–∞—Б—В–∞–≤–ї—П—О—В –Њ—В–Ї–∞–Ј–∞—В—М—Б—П –Њ—В –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П. –Э–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —В—А–µ–Љ–Њ—А –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≥–µ–Ї—Б–∞–Љ–Є–і–Є–љ, –Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ, –Ї–ї–Њ–љ–∞–Ј–µ–њ–∞–Љ. –Ф–ї—П –ї–µ—З–µ–љ–Є—П –і—А–Њ–ґ–∞–љ–Є—П –њ—А–Є PC –њ—А–µ–і–ї–Њ–ґ–µ–љ –Є –Њ–љ–і–∞–љ—Б–µ—В—А–Њ–љ, –±–ї–Њ–Ї–Є—А—Г—О—Й–Є–є —Ж–µ–љ—В—А–∞–ї—М–љ—Л–µ –Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ 5–Э–Ґ–Ч-—А–µ—Ж–µ–њ—В–Њ—А—Л –Є —П–≤–ї—П—О—Й–Є–є—Б—П, —В–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –∞–љ—В–∞–≥–Њ–љ–Є—Б—В–Њ–Љ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞. –Я–Њ–њ—Л—В–Ї–Є –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і—А–Њ–ґ–∞–љ–Є—П –і–Њ–ї–ґ–љ—Л –±—Л—В—М –і–Њ–њ–Њ–ї–љ–µ–љ—Л —А–∞–Ј–ї–Є—З–љ—Л–Љ–Є –Љ–µ—В–Њ–і–∞–Љ–Є —А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є – —Г–њ—А–∞–ґ–љ–µ–љ–Є—П–Љ–Є –љ–∞ –Ї–Њ–Њ—А–і–Є–љ–∞—Ж–Є—О; –њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ —В—А–µ–Љ–Њ—А–µ —А—Г–Ї –Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М —Д–Є–Ї—Б–∞—Ж–Є—О –љ–∞ –Ј–∞–њ—П—Б—В—М—П—Е –љ–µ–±–Њ–ї—М—И–Є—Е –≥—А—Г–Ј–Њ–≤ –≤ 400-600 –≥. –Ю–і–љ–∞–Ї–Њ, —Н—В–Њ –Љ–Њ–ґ–µ—В —Г—Б–Є–ї–Є—В—М –Є–Љ–µ—О—Й—Г—О—Б—П —Б–ї–∞–±–Њ—Б—В—М –Є —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, –∞ –Є–љ–Њ–≥–і–∞ –Є —Г—Б–Є–ї–Є—В—М —В—А–µ–Љ–Њ—А. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е —Б–ї—Г—З–∞—П—Е –њ—А–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ–Љ –і—А–Њ–ґ–∞–љ–Є–Є –њ—А–Њ–≤–Њ–і—П—В —Б—В–µ—А–µ–Њ—В–∞–Ї—Б–Є—З–µ—Б–Ї–Є–µ –Њ–њ–µ—А–∞—Ж–Є–Є – —В–∞–ї–∞–Љ–∞—В–Њ–Љ–Є—О –Є–ї–Є —Б—В–Є–Љ—Г–ї—П—Ж–Є—О –≤–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Є–љ—В–µ—А–Љ–µ–і–Є–∞–ї—М–љ–Њ–≥–Њ —П–і—А–∞ –Ј—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –±—Г–≥—А–∞.
–Ю–і–Є–љ –Є–Ј —Б–∞–Љ—Л—Е —З–∞—Б—В—Л—Е –Є –Є–љ–≤–∞–ї–Є–і–Є–Ј–Є—А—Г—О—Й–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ PC – –њ–Њ–≤—Л—И–µ–љ–Є–µ –Љ—Л—И–µ—З–љ–Њ–≥–Њ —В–Њ–љ—Г—Б–∞ –њ–Њ —Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–Љ—Г —В–Є–њ—Г. –°–њ–∞—Б—В–Є—З–љ–Њ—Б—В—М –Љ–Њ–ґ–µ—В –і–∞–ґ–µ –±–Њ–ї—М—И–µ –Ј–∞—В—А—Г–і–љ—П—В—М –і–≤–Є–ґ–µ–љ–Є—П, —З–µ–Љ —Б–ї–∞–±–Њ—Б—В—М. –° —В–µ—З–µ–љ–Є–µ–Љ –≤—А–µ–Љ–µ–љ–Є –њ–Њ–≤—Л—И–µ–љ–љ—Л–є —В–Њ–љ—Г—Б –≤ —Б–≥–Є–±–∞—В–µ–ї—М–љ—Л—Е –≥—А—Г–њ–њ–∞—Е –Љ—Л—И—Ж –Љ–Њ–ґ–µ—В –њ—А–Є–≤–µ—Б—В–Є –Ї —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—О –Ї–Њ–љ—В—А–∞–Ї—В—Г—А. –Ю—Б–љ–Њ–≤–Њ–є –ї–µ—З–µ–љ–Є—П —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В–Є –і–Њ–ї–ґ–љ–Њ —П–≤–ї—П—В—М—Б—П –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –Ы–§–Ъ, –Љ–∞—Б—Б–∞–ґ–∞ –Є —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–Є–Є. –§–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –ї–Є—И—М –і–Њ–њ–Њ–ї–љ—П–µ—В —Н—В–Є –Љ–µ—В–Њ–і—Л, –∞ –љ–µ –Ј–∞–Љ–µ–љ—П–µ—В –Є—Е. –Ф–Њ –љ–∞—З–∞–ї–∞ –∞–љ—В–Є—Б–њ–∞—Б—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –љ—Г–ґ–љ–Њ –Њ—Ж–µ–љ–Є—В—М –µ–µ –≤–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П –≤ –≤–Є–і–µ —Г—Б–Є–ї–µ–љ–Є—П —Б–ї–∞–±–Њ—Б—В–Є. –Ю–±—Й–Є–Љ –њ—А–∞–≤–Є–ї–Њ–Љ —Н—В–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –љ–∞—З–∞–ї–Њ —Б –Љ–∞–ї—Л—Е –і–Њ–Ј —Б –њ–Њ—Б—В–µ–њ–µ–љ–љ—Л–Љ –Є—Е —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј—Л, –љ–∞ –Ї–Њ—В–Њ—А–Њ–є –њ–Њ–ї—Г—З–µ–љ –ґ–µ–ї–∞–µ–Љ—Л–є —Н—Д—Д–µ–Ї—В. –Я—А–Є –љ–∞–ї–Є—З–Є–Є —Г –±–Њ–ї—М–љ–Њ–≥–Њ –љ–Њ—З–љ—Л—Е –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л—Е –Љ—Л—И–µ—З–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–≤ —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –Њ–і–љ–Њ–Ї—А–∞—В–љ–Њ–µ –љ–∞–Ј–љ–∞—З–µ–љ–Є–µ –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–∞ –љ–∞ –љ–Њ—З—М. –Ф–ї—П —Б–љ–Є–ґ–µ–љ–Є—П —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В–Є –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –њ—А–Є–Љ–µ–љ—П—О—В –±–∞–Ї–ї–Њ—Д–µ–љ. –≠—В–Њ—В –њ—А–µ–њ–∞—А–∞—В —З–∞—Б—В–Є—З–љ–Њ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є, –њ–Њ—Н—В–Њ–Љ—Г –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –Є –Ї–∞–ґ–і—Л–µ 6 –Љ–µ—Б—П—Ж–µ–≤ —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–µ—А—П—В—М –µ–µ —Д—Г–љ–Ї—Ж–Є—О. –Э–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ –±–∞–Ї–ї–Њ—Д–µ–љ–∞ – 5 –Љ–≥/—Б—Г—В, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П – 100 –Љ–≥/—Б—Г—В. –Ц–µ–ї–∞—В–µ–ї—М–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М –Є–Ј–љ–∞—З–∞–ї—М–љ—Г—О –і–Њ–Ј—Г (–Ї–∞–Ї –Є —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –µ–µ) –љ–∞ –љ–Њ—З—М, —З—В–Њ–±—Л —Г–Љ–µ–љ—М—И–Є—В—М –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л: —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, —Б–ї–∞–±–Њ—Б—В—М, —В–Њ—И–љ–Њ—В—Г, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ. –Э—Г–ґ–љ–Њ –њ–Њ–Љ–љ–Є—В—М, —З—В–Њ —А–µ–Ј–Ї–∞—П –Њ—В–Љ–µ–љ–∞ –±–∞–Ї–ї–Њ—Д–µ–љ–∞ –Љ–Њ–ґ–µ—В —Б–њ—А–Њ–≤–Њ—Ж–Є—А–Њ–≤–∞—В—М —Б—Г–і–Њ—А–Њ–ґ–љ—Л–µ –њ—А–Є–њ–∞–і–Ї–Є. –Ф—А—Г–≥–Є–Љ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ —Г–Љ–µ–љ—М—И–µ–љ–Є—П —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В–Є —П–≤–ї—П–µ—В—Б—П —В–Є–Ј–∞–љ–Є–і–Є–љ. –Ю–љ —В–∞–Ї–ґ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –љ–µ–Њ–±—Е–Њ–і–Є–Љ –Ї–Њ–љ—В—А–Њ–ї—М –µ–µ —Д—Г–љ–Ї—Ж–Є–є –њ–µ—А–µ–і –љ–∞—З–∞–ї–Њ–Љ —В–µ—А–∞–њ–Є–Є –Є –Ј–∞—В–µ–Љ —З–µ—А–µ–Ј 1, 3 –Є 6 –Љ–µ—Б—П—Ж–µ–≤ –ї–µ—З–µ–љ–Є—П. –Э–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ —В–Є–Ј–∞–љ–Є–і–Є–љ–∞ 2-4 –Љ–≥/—Б—Г—В, –µ–µ –Љ–Њ–ґ–љ–Њ —Г–і–≤–∞–Є–≤–∞—В—М –Ї–∞–ґ–і—Л–µ 3 –і–љ—П, –љ–Њ –Њ–±—Й–∞—П —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ –љ–µ –і–Њ–ї–ґ–љ–∞ –њ—А–µ–≤—Л—И–∞—В—М 36 –Љ–≥. –Я—А–µ–њ–∞—А–∞—В –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М —Б—Г—Е–Њ—Б—В—М –≤–Њ —А—В—Г, —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ. –°–Њ–љ–ї–Є–≤–Њ—Б—В—М –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —В–Є–Ј–∞–љ–Є–і–Є–љ–∞ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В —З–∞—Й–µ, —З–µ–Љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є –±–∞–Ї–ї–Њ—Д–µ–љ–Њ–Љ, –љ–Њ —Г—Б–Є–ї–µ–љ–Є–µ —Б–ї–∞–±–Њ—Б—В–Є, –љ–∞–њ—А–Њ—В–Є–≤, –Њ—В–Љ–µ—З–∞–µ—В—Б—П —А–µ–ґ–µ. –Ь–Њ–ґ–љ–Њ –≤ –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї —Н—В–Є–Љ –њ—А–µ–њ–∞—А–∞—В–∞–Љ –љ–∞–Ј–љ–∞—З–Є—В—М –і–Є–∞–Ј–µ–њ–∞–Љ. –Х–≥–Њ –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ – 2 –Љ–≥/—Б—Г—В, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П – 40 –Љ–≥/—Б—Г—В. –Я–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є –і–Є–∞–Ј–µ–њ–∞–Љ–∞ —П–≤–ї—П—О—В—Б—П —Б–Њ–љ–ї–Є–≤–Њ—Б—В—М –Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П. –†–µ–Ј–Ї–∞—П –Њ—В–Љ–µ–љ–∞ –µ–≥–Њ —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –≤—Л–Ј–≤–∞—В—М —Н–њ–Є–ї–µ–њ—В–Є—З–µ—Б–Ї–Є–µ –њ—А–Є–њ–∞–і–Ї–Є. –Я—А–Є –≤—Л—А–∞–ґ–µ–љ–љ—Л—Е —В–Њ–љ–Є—З–µ—Б–Ї–Є—Е —Б–њ–∞–Ј–Љ–∞—Е –њ—А–Є–Љ–µ–љ—П—О—В –±–Њ—В—Г–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —В–Њ–Ї—Б–Є–љ –Р. –Я—А–µ–њ–∞—А–∞—В –≤–≤–Њ–і–Є—В—Б—П –љ–µ–њ–Њ—Б—А–µ–і—Б—В–≤–µ–љ–љ–Њ –≤ —Б–њ–∞–Ј–Љ–Є—А–Њ–≤–∞–љ–љ—Л–µ –Љ—Л—И—Ж—Л. –Я–∞—А–µ–Ј —Н—В–Є—Е –Љ—Л—И—Ж –љ–∞—З–Є–љ–∞–µ—В —А–∞–Ј–≤–Є–≤–∞—В—М—Б—П —З–µ—А–µ–Ј 24-72 —З–∞—Б–∞ –њ–Њ—Б–ї–µ –≤–≤–µ–і–µ–љ–Є—П —В–Њ–Ї—Б–Є–љ–∞, –і–Њ—Б—В–Є–≥–∞—П –Љ–∞–Ї—Б–Є–Љ—Г–Љ–∞ –љ–∞ 5-14 –і–µ–љ—М, –Є –і–ї–Є—В—Б—П 12-16 –љ–µ–і–µ–ї—М. –Я—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ–Љ –њ–µ—А–Њ—А–∞–ї—М–љ–Њ–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Љ–Є–Њ—А–µ–ї–∞–Ї—Б–∞–љ—В–Њ–≤ –і–ї—П –ї–µ—З–µ–љ–Є—П –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–є —Б–њ–∞—Б—В–Є—З–љ–Њ—Б—В–Є —Г –Њ–±–µ–Ј–і–≤–Є–ґ–µ–љ–љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–Є–Љ–µ–љ—П—О—В —Н–љ–і–Њ–ї—О–Љ–±–∞–ї—М–љ–Њ–µ –≤–≤–µ–і–µ–љ–Є–µ –±–∞–Ї–ї–Њ—Д–µ–љ–∞ –Є —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Є–µ –Љ–µ—В–Њ–і—Л –ї–µ—З–µ–љ–Є—П: –њ–µ—А–µ—Б–µ—З–µ–љ–Є–µ —Б—Г—Е–Њ–ґ–Є–ї–Є–є –њ—А–Є–≤–Њ–і—П—Й–Є—Е –Љ—Л—И—Ж –±–µ–і–µ—А, –њ–µ—А–µ–і–љ–Є—Е –Є –Ј–∞–і–љ–Є—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞.
–С–Њ–ї–µ–µ –њ–Њ–ї–Њ–≤–Є–љ—Л –±–Њ–ї—М–љ—Л—Е PC –љ–∞ –Њ–њ—А–µ–і–µ–ї–µ–љ–љ–Њ–Љ —Н—В–∞–њ–µ —А–∞–Ј–≤–Є—В–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є—Б–њ—Л—В—Л–≤–∞—О—В –±–Њ–ї–Є, —А–∞–Ј–ї–Є—З–љ—Л–µ –њ–Њ —Е–∞—А–∞–Ї—В–µ—А—Г –Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є. –С–Њ–ї–µ–≤—Л–µ —Б–Є–љ–і—А–Њ–Љ—Л –њ—А–Є PC –±—Л–≤–∞—О—В –Њ—Б—В—А—Л–Љ–Є (–љ–µ–≤—А–∞–ї–≥–Є—П —В—А–Њ–є–љ–Є—З–љ–Њ–≥–Њ –љ–µ—А–≤–∞, —В–Њ–љ–Є—З–µ—Б–Ї–Є–µ —Б–њ–∞–Ј–Љ—Л), –њ–Њ–і–Њ—Б—В—А—Л–Љ–Є (–њ—А–Є —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–Љ –љ–µ–≤—А–Є—В–µ, –≥–µ–Љ–Њ—А—А–∞–≥–Є—З–µ—Б–Ї–Њ–Љ —Ж–Є—Б—В–Є—В–µ) –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є. –Я–Њ–ї–Њ–≤–Є–љ—Г –≤—Б–µ—Е –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ —Б–Њ—Б—В–∞–≤–ї—П—О—В —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –±–Њ–ї–Є –≤ –≤–Є–і–µ –і–Є–Ј–µ—Б—В–µ–Ј–Є–є –≤ –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е –Є –±–Њ–ї–µ–є –≤ —Б–њ–Є–љ–µ. –Ф–Њ—А–Ј–∞–ї–≥–Є—П —З–∞—Й–µ –≤—Б–µ–≥–Њ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –љ–∞—А—Г—И–µ–љ–љ–Њ–є —Б—В–∞—В–Є–Ї–Њ–є —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–Њ–Ј—Л. –Ы–µ—З–µ–љ–Є–µ –Ј–∞–≤–Є—Б–Є—В –Њ—В —Е–∞—А–∞–Ї—В–µ—А–∞ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞. –≠—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —Б—А–µ–і—Б—В–≤–Њ–Љ –ї–µ—З–µ–љ–Є—П –љ–µ–≤—А–∞–ї–≥–Є–Є —В—А–Њ–є–љ–Є—З–љ–Њ–≥–Њ –љ–µ—А–≤–∞ –њ—А–Є PC, –Ї–∞–Ї –Є –Є–і–Є–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–∞–ї–≥–Є–Є –µ–≥–Њ, —П–≤–ї—П–µ—В—Б—П –Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ. –•–Њ—А–Њ—И–µ–µ –і–µ–є—Б—В–≤–Є–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Є –і—А—Г–≥–Є–µ –њ—А–Њ—В–Є–≤–Њ—Б—Г–і–Њ—А–Њ–ґ–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л – —Д–µ–љ–Є—В–Њ–Є–љ, –≥–∞–±–∞–њ–µ–љ—В–Є–љ –Є –ї–∞–Љ–Њ—В—А–Є–і–ґ–Є–љ. –С–Њ–ї–Є –њ—А–Є —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–Љ –љ–µ–≤—А–Є—В–µ —Е–Њ—А–Њ—И–Њ –Ї—Г–њ–Є—А—Г—О—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤, –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л—Е –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є, –њ—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є, –Ї–Њ—А—В–Є–Ї–Њ—Б—В–µ—А–Њ–Є–і–Њ–≤. –Я—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –ґ–≥—Г—З–Є—Е –љ–µ–≤—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї—П—Е –љ–∞–Є–±–Њ–ї–µ–µ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ—Л —В—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л, –∞ —В–∞–Ї–ґ–µ –У–Р–Ь–Ъ-–µ—А–≥–Є—З–µ—Б–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л. –•–Њ—А–Њ—И–Є–є —Н—Д—Д–µ–Ї—В –њ—А–Є —В–∞–Ї–Њ–≥–Њ —А–Њ–і–∞ –±–Њ–ї—П—Е –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞–љ–љ–∞—П —В–µ—А–∞–њ–Є—П —Б –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –Ї–ї–Њ–Љ–Є–њ—А–∞–Љ–Є–љ–∞ (10-25 –Љ–≥/—Б—Г—В), –≥–∞–ї–Њ–њ–µ—А–Є–і–Њ–ї–∞ (0,5-1,0 –Љ–≥/—Б—Г—В) –Є –Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ–∞ (100-200 –Љ–≥/—Б—Г—В). –С–Њ–ї–Є –≤ —Б–њ–Є–љ–µ —Е–Њ—А–Њ—И–Њ –Ї—Г–њ–Є—А—Г—О—В—Б—П –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–Љ–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Є–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є. –Ф–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ–Њ–Ј—Л –Є —Г–Ї—А–µ–њ–ї–µ–љ–Є—П –њ–∞—А–∞–≤–µ—А—В–µ–±—А–∞–ї—М–љ—Л—Е –Љ—Л—И—Ж –Љ–Њ–≥—Г—В –±—Л—В—М –њ–Њ–ї–µ–Ј–љ—Л –Љ–∞—Б—Б–∞–ґ, —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–Є—П, –Ы–§–Ъ. –Ф–ї—П —Б–љ—П—В–Є—П –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л—Е –Љ—Л—И–µ—З–љ—Л—Е —Б–њ–∞–Ј–Љ–Њ–≤ –Є—Б–њ–Њ–ї—М–Ј—Г—О—В –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ—Л –Є –∞–љ—В–Є–Ї–Њ–љ–≤—Г–ї—М—Б–∞–љ—В—Л. –С–Њ–ї—М –≤ –Љ–µ—Б—В–∞—Е –Є–љ—К–µ–Ї—Ж–Є–є –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є b-–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤ —Б–љ–Є–Љ–∞—О—В –Љ–µ—Б—В–љ—Л–Љ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –ї–Є–і–Њ–Ї–∞–Є–љ–∞, –∞ –і–Є—Д—Д—Г–Ј–љ—Л–µ –Љ—Л—И–µ—З–љ—Л–µ –±–Њ–ї–Є (“–Є–љ—В–µ—А—Д–µ—А–Њ–љ–Њ–≤—Л–є –≥—А–Є–њ–њ”) —Е–Њ—А–Њ—И–Њ –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г—О—В—Б—П –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–Љ–Є –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є. –Я—А–Є –±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л—Е —Б–њ–∞–Ј–Љ–∞—Е –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ. –Я—Б–Є—Е–Њ–≥–µ–љ–љ—Л–µ –±–Њ–ї–Є —А–µ–∞–≥–Є—А—Г—О—В –љ–∞ –ї–µ—З–µ–љ–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–∞–Љ–Є. –У–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є –њ—А–Є PC, –Є–Љ–µ—О—Й–Є–µ —З–∞—Й–µ –≤—Б–µ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А –≥–Њ–ї–Њ–≤–љ—Л—Е –±–Њ–ї–µ–є –љ–∞–њ—А—П–ґ–µ–љ–Є—П, –ї–µ—З–∞—В —В–∞–Ї –ґ–µ, –Ї–∞–Ї –≥–Њ–ї–Њ–≤–љ—Л–µ –±–Њ–ї–Є —Н—В–Њ–≥–Њ —В–Є–њ–∞ —Г –±–Њ–ї—М–љ—Л—Е –±–µ–Ј –†–°.
–Т–µ—Б—М–Љ–∞ —З–∞—Б—В—Л–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ PC —П–≤–ї—П–µ—В—Б—П –і–µ–њ—А–µ—Б—Б–Є—П. –Я–Њ –≤—Б–µ–є –≤–Є–і–Є–Љ–Њ—Б—В–Є, –і–µ–њ—А–µ—Б—Б–Є—П –њ—А–Є PC –Љ—Г–ї—М—В–Є—Д–∞–Ї—В–Њ—А–Є–∞–ї—М–љ–∞. –Я—А–Є—З–Є–љ–∞–Љ–Є –µ–µ –Љ–Њ–≥—Г—В –±—Л—В—М —А–µ–∞–Ї—Ж–Є—П –љ–∞ –±–Њ–ї–µ–Ј–љ—М, —Б–∞–Љ–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Є –њ–Њ–±–Њ—З–љ—Л–µ —Н—Д—Д–µ–Ї—В—Л –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –і–µ–њ—А–µ—Б—Б–Є–Є –ґ–µ–ї–∞—В–µ–ї—М–љ–Њ —Б–Њ—З–µ—В–∞–љ–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–љ–Њ–є –Є –њ—Б–Є—Е–Њ—В–µ—А–∞–њ–Є–Є. –І–∞—Й–µ –≤—Б–µ–≥–Њ –љ–∞–Ј–љ–∞—З–∞—О—В –∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ (–љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ – 25 –Љ–≥, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П – 150-–Ч00 –Љ–≥). –Э–Њ –Є –і—А—Г–≥–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л —В–∞–Ї–ґ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –њ—А–Є PC, –Ї–∞–Ї –Є –њ—А–Є –і–µ–њ—А–µ—Б—Б–Є—П—Е –Є–љ–Њ–≥–Њ –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є—П, —Е–Њ—В—П –Є—Е –њ–Њ–±–Њ—З–љ—Л–µ —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є–Є—З–µ—Б–Ї–Є–µ —Н—Д—Д–µ–Ї—В—Л (—Б—Г—Е–Њ—Б—В—М —Б–ї–Є–Ј–Є—Б—В—Л—Е, –љ–∞—А—Г—И–µ–љ–Є–µ –∞–Ї–Ї–Њ–Љ–Њ–і–∞—Ж–Є–Є, –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–∞—П –≥–Є–њ–Њ—В–µ–љ–Ј–Є—П, —В–∞—Е–Є–Ї–∞—А–і–Є—П) –њ—А–Є —Н—В–Њ–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–Є –Љ–Њ–≥—Г—В –≤–Њ–Ј–љ–Є–Ї–∞—В—М –њ—А–Є –Љ–µ–љ—М—И–Є—Е –і–Њ–Ј–Є—А–Њ–≤–Ї–∞—Е. –Я—А–Є —Н—В–Њ–Љ –љ—Г–ґ–љ–Њ —Г—З–Є—В—Л–≤–∞—В—М –Є —В–Њ, —З—В–Њ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Њ–є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ–Њ–≥—Г—В —Г—Б—Г–≥—Г–±–ї—П—В—М –Ј–∞–і–µ—А–ґ–Ї—Г –Љ–Њ—З–Є, –љ–∞—А—Г—И–µ–љ–Є–µ –Ј—А–µ–љ–Є—П, –Ј–∞—В—А—Г–і–љ–µ–љ–Є–µ –≥–ї–Њ—В–∞–љ–Є—П (–Є–Ј-–Ј–∞ —Б—Г—Е–Њ—Б—В–Є –≤–Њ —А—В—Г). –Я–Њ—Н—В–Њ–Љ—Г –і–ї—П –ї–µ—З–µ–љ–Є—П –і–µ–њ—А–µ—Б—Б–Є–Є —Г –±–Њ–ї—М–љ—Л—Е PC —А–µ–Ї–Њ–Љ–µ–љ–і—Г—О—В –њ—А–Є–Љ–µ–љ—П—В—М —Б–µ–ї–µ–Ї—В–Є–≤–љ—Л–µ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞, –ї–Є—И–µ–љ–љ—Л–µ —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —Б–≤–Њ–є—Б—В–≤ – —В—А–∞–Ј–∞–і–Њ–љ (–љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ – 50 –Љ–≥, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П – 150-600 –Љ–≥), —Б–µ—А—В—А–∞–ї–Є–љ (–љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ – 25 –Љ–≥, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П – 50 –Љ–≥), —Д–ї—Г–Њ–Ї—Б–µ—В–Є–љ (–љ–∞—З–∞–ї—М–љ–∞—П –Є —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П –і–Њ–Ј—Л – 20 –Љ–≥), –њ–∞—А–Њ–Ї—Б–µ—В–Є–љ (–љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ – 20 –Љ–≥, —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–∞—П – 50 –Љ–≥) –Є —В.–і. –≠—В–Є –њ—А–µ–њ–∞—А–∞—В—Л —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –Є —З–∞—Й–µ –≤—Б–µ–≥–Њ —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б—П—В—Б—П. –Э–∞—З–Є–љ–∞—В—М –ї–µ—З–µ–љ–Є–µ —Б–ї–µ–і—Г–µ—В —Б –Љ–Є–љ–Є–Љ–∞–ї—М–љ—Л—Е –љ–∞—З–∞–ї—М–љ—Л—Е –і–Њ–Ј, –Љ–µ–і–ї–µ–љ–љ–Њ –њ–Њ–≤—Л—И–∞—П –Є—Е —З–µ—А–µ–Ј 3-5 –і–љ–µ–є. –Ф–ї—П –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –ґ–µ–ї–∞–µ–Љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞ –љ—Г–ґ–љ–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–µ–і–µ–ї—М. –Х—Б–ї–Є —З–µ—А–µ–Ј 4-5 –љ–µ–і–µ–ї—М —Н—Д—Д–µ–Ї—В–∞ –Њ—В –ї–µ—З–µ–љ–Є—П –љ–µ—В –Є–ї–Є —З–µ—А–µ–Ј 6-8 –љ–µ–і–µ–ї—М –Њ—В–Љ–µ—З–∞–µ—В—Б—П –ї–Є—И—М –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ –і–µ–є—Б—В–≤–Є–µ –њ—А–µ–њ–∞—А–∞—В–∞, –∞ —В–∞–Ї–ґ–µ –≤ —Б–ї—Г—З–∞–µ –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —В—А—Г–і–љ–Њ –њ–µ—А–µ–љ–Њ—Б–Є–Љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —П–≤–ї–µ–љ–Є–є, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –Љ–µ–љ—П—В—М –њ—А–µ–њ–∞—А–∞—В. –Т —Б–ї—Г—З–∞–µ –ґ–µ —Е–Њ—А–Њ—И–µ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —В–µ—А–∞–њ–Є—О —Б–ї–µ–і—Г–µ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В—М –і–Њ 6 –Љ–µ—Б—П—Ж–µ–≤, –∞ –Ј–∞—В–µ–Љ –≤–љ–Њ–≤—М –Њ—Ж–µ–љ–Є—В—М —Б–Њ—Б—В–Њ—П–љ–Є–µ –±–Њ–ї—М–љ–Њ–≥–Њ –і–ї—П —А–µ—И–µ–љ–Є—П –≤–Њ–њ—А–Њ—Б–∞ –Њ–± –Њ—В–Љ–µ–љ–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–∞ –Є–ї–Є –њ—А–Њ–і–Њ–ї–ґ–µ–љ–Є–Є –µ–≥–Њ –њ—А–Є–µ–Љ–∞.
–Я—А–Є —В—А–µ–≤–Њ–ґ–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е –і–ї—П –љ–µ–і–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–Є—В—М –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ—Л (–і–Є–∞–Ј–µ–њ–∞–Љ – 2-10 –Љ–≥/—Б—Г—В, –∞–ї–њ—А–Њ–Ј–∞–ї–∞–Љ – 3-4 –Љ–≥/—Б—Г—В, –Ї–ї–Њ–љ–∞–Ј–µ–њ–∞–Љ – 4-6 –Љ–≥/—Б—Г—В, –ї–Њ—А–∞–Ј–µ–њ–∞–Љ – 3-4 –Љ–≥/—Б—Г—В). –Ю—Б–Њ–±–µ–љ–љ–Њ –Њ–љ–Є –њ–Њ–ї–µ–Ј–љ—Л –љ–∞ –Ї–Њ—А–Њ—В–Ї–Є–є –њ–µ—А–Є–Њ–і –њ—А–Є —Б–Њ–Њ–±—Й–µ–љ–Є–Є –±–Њ–ї—М–љ–Њ–Љ—Г –і–Є–∞–≥–љ–Њ–Ј–∞ PC.
–Э–µ—А–µ–і–Ї–Њ —В–µ—З–µ–љ–Є–µ PC —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В —А–∞–Ј–ї–Є—З–љ—Л–µ –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–µ —Б–Є–љ–і—А–Њ–Љ—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –±—Л—В—М —Б–µ–љ—Б–Њ—А–љ—Л–Љ–Є, –Љ–Њ—В–Њ—А–љ—Л–Љ–Є –Є —Б–Љ–µ—И–∞–љ–љ—Л–Љ–Є. –Ъ –љ–Є–Љ –Њ—В–љ–Њ—Б—П—В —Б–Є–Љ–њ—В–Њ–Љ –Ы–µ—А–Љ–Є—В—В–∞, —Б–Є–Љ–њ—В–Њ–Љ –£—В–≥–Њ—Д—Д–∞, –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–є –Ј—Г–і, –ї–Є—Ж–µ–≤—Г—О –Љ–Є–Њ–Ї–Є–Љ–Є—О, —В–Њ–љ–Є—З–µ—Б–Ї–Є–µ —Б–њ–∞–Ј–Љ—Л, –і–Є–Ј–∞—А—В—А–Є—О, —Б–њ–∞–Ј–Љ –Ї–Њ–љ–≤–µ—А–≥–µ–љ—Ж–Є–Є –Є —В.–і. –≠—В–Є –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–µ —Б–Є–Љ–њ—В–Њ–Љ—Л —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –Љ–∞–ї–Њ–є –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М—О (–Њ–±—Л—З–љ–Њ –љ–µ –±–Њ–ї–µ–µ 2 –Љ–Є–љ—Г—В) –Є –±–Њ–ї—М—И–Њ–є —З–∞—Б—В–Њ—В–Њ–є – –і–Њ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е —Б–Њ—В–µ–љ –≤ –і–µ–љ—М, —З–∞—Б—В–Њ –њ—А–Њ–≤–Њ—Ж–Є—А—Г—О—В—Б—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л–Љ–Є —В—А–Є–≥–≥–µ—А–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є – –і–≤–Є–ґ–µ–љ–Є–µ–Љ, —Б—В—А–µ—Б—Б–Њ–Љ, —Б–µ–љ—Б–Њ—А–љ—Л–Љ–Є —Б—В–Є–Љ—Г–ї–∞–Љ–Є, –≥–Є–њ–µ—А–≤–µ–љ—В–Є–ї—П—Ж–Є–µ–є. –Т—Б–µ —Н—В–Є –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤ –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ —Е–Њ—А–Њ—И–Њ –њ–Њ–і–і–∞—О—В—Б—П –ї–µ—З–µ–љ–Є—О –і–∞–ґ–µ –љ–µ–±–Њ–ї—М—И–Є–Љ–Є –і–Њ–Ј–∞–Љ–Є –Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ–∞ – 50-100 –Љ–≥/—Б—Г—В –Є–ї–Є –≥–∞–±–∞–њ–µ–љ—В–Є–љ–∞ – 100-–Ч00 –Љ–≥/—Б—Г—В. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –і–Њ–Ј—Г –Љ–Њ–ґ–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—В—М –і–Њ –і–Њ—Б—В–Є–ґ–µ–љ–Є—П –ґ–µ–ї–∞–µ–Љ–Њ–≥–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞. –Я—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—В–Њ—А–Њ–≥–Њ —А—П–і–∞ –і–ї—П –ї–µ—З–µ–љ–Є—П –њ–Њ–і–Њ–±–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —П–≤–ї—П—О—В—Б—П —Д–µ–љ–Є—В–Њ–Є–љ, —Д–µ–љ–Њ–±–∞—А–±–Є—В–∞–ї, –Ї–ї–Њ–љ–∞–Ј–µ–њ–∞–Љ, –∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ –Є –і—А. –Х—Б–ї–Є —В–∞–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ, –њ–Њ–Ї–∞–Ј–∞–љ–∞ –≥–Њ—А–Љ–Њ–љ–∞–ї—М–љ–∞—П –њ—Г–ї—М—Б-—В–µ—А–∞–њ–Є—П.
–£ –њ–Њ–і–∞–≤–ї—П—О—Й–µ–≥–Њ —З–Є—Б–ї–∞ –±–Њ–ї—М–љ—Л—Е PC –Є–Љ–µ—О—В—Б—П —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є—П. –Ч–∞—З–∞—Б—В—Г—О –Њ–љ–Є —П–≤–ї—П—О—В—Б—П –Њ—Б–љ–Њ–≤–љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –љ–∞—А—Г—И–µ–љ–Є—П –љ–∞—Б—В—А–Њ–µ–љ–Є—П, —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–∞—П –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є. –° –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —В–Њ—З–Ї–Є –Ј—А–µ–љ–Є—П –љ–∞—А—Г—И–µ–љ–Є—П –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е PC –Љ–Њ–ґ–љ–Њ —А–∞–Ј–і–µ–ї–Є—В—М –љ–∞ —В—А—Г–і–љ–Њ—Б—В–Є —Г–і–µ—А–ґ–∞–љ–Є—П –Љ–Њ—З–Є –Є —В—А—Г–і–љ–Њ—Б—В–Є –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є—П –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П. –Э–µ—А–µ–і–Ї–Њ –Є–Љ–µ–µ—В—Б—П –Є —Б–Њ—З–µ—В–∞–љ–Є–µ —Н—В–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –С–Њ–ї—М—И–Є–љ—Б—В–≤—Г –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—А—Г—И–µ–љ–љ—Л–Љ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–µ–Љ –Љ–Њ–ґ–љ–Њ –њ–Њ–Љ–Њ—З—М –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ. –Я—А–Є –Є–Љ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –њ–Њ–Ј—Л–≤–∞—Е –љ–∞ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–µ –љ–∞–Ј–љ–∞—З–∞—О—В: —В–Њ–ї—В–µ—А–Њ–і–Є–љ (4 –Љ–≥), –∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ (25-50 –Љ–≥), –љ–Є—Д–µ–і–Є–њ–Є–љ, –Њ–Ї—Б–Є–±—Г—В–Є–љ–Є–љ (2,5-10 –Љ–≥). –Я—А–Є —В—А—Г–і–љ–Њ—Б—В—П—Е –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є—П –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П –љ–∞–Ј–љ–∞—З–∞—О—В a-–±–ї–Њ–Ї–∞—В–Њ—А – —В–µ—А–∞–Ј–Њ–Ј–Є–љ – 5-10 –Љ–≥; –њ–Њ–±–Њ—З–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ –Њ—А—В–Њ—Б—В–∞—В–Є—З–µ—Б–Ї–Њ–є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–Є. –Ь–Њ–ґ–љ–Њ –њ—А–Є–Љ–µ–љ—П—В—М —Б—А–µ–і—Б—В–≤–∞, —Г–Љ–µ–љ—М—И–∞—О—Й–Є–µ –љ–∞–њ—А—П–ґ–µ–љ–Є–µ –Љ—Л—И—Ж –љ–∞—А—Г–ґ–љ–Њ–≥–Њ —Б—Д–Є–љ–Ї—В–µ—А–∞ –Љ–Њ—З–µ–≤–Њ–≥–Њ –њ—Г–Ј—Л—А—П – —В–Є–Ј–∞–љ–Є–і–Є–љ (8 –Љ–≥), –і–Є–∞–Ј–µ–њ–∞–Љ. –Я—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ї–Њ–љ—Б–µ—А–≤–∞—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є –њ–Њ–Ї–∞–Ј–∞–љ–Њ —Е–Є—А—Г—А–≥–Є—З–µ—Б–Ї–Њ–µ –ї–µ—З–µ–љ–Є–µ.
–Я—А–Є –њ—А–µ–і—К—П–≤–ї–µ–љ–Є–Є –ґ–∞–ї–Њ–± –љ–∞ –Ј–∞–њ–Њ—А—Л –љ—Г–ґ–љ–Њ –≤—Л—П—Б–љ–Є—В—М —Г –њ–∞—Ж–Є–µ–љ—В–∞, –Ї–∞–Ї —З–∞—Б—В–Њ –±—Л–≤–∞–µ—В —Б—В—Г–ї –Є –Њ–±—К—П—Б–љ–Є—В—М, —З—В–Њ –Ї–∞–ґ–і–Њ–і–љ–µ–≤–љ–Њ–µ –Њ–њ–Њ—А–Њ–ґ–љ–µ–љ–Є–µ –Ї–Є—И–µ—З–љ–Є–Ї–∞ –љ–µ–Њ–±—П–Ј–∞—В–µ–ї—М–љ–Њ. –Т –±–Њ–ї—М—И–Є–љ—Б—В–≤–µ —Б–ї—Г—З–∞–µ–≤ –і–ї—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Ї–Є—И–µ—З–љ–Є–Ї–∞ –±–Њ–ї—М–љ—Л–Љ –і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Б–Њ–±–ї—О–і–∞—В—М –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Г—О –і–Є–µ—В—Г –Є –њ–Њ—В—А–µ–±–ї—П—В—М –±–Њ–ї—М—И–µ –ґ–Є–і–Ї–Њ—Б—В–Є (—З—В–Њ –љ–µ –≤—Б–µ–≥–і–∞ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –≤ —Б–ї—Г—З–∞—П—Е –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ—Л—Е –Є–Љ–њ–µ—А–∞—В–Є–≤–љ—Л—Е –њ–Њ–Ј—Л–≤–Њ–≤ –љ–∞ –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є–µ) –Є–ї–Є –њ—А–Є–љ–Є–Љ–∞—В—М —Б–ї–∞–±–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л.
–Т—Б–ї–µ–і –Ј–∞ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Љ–Њ—З–µ–Є—Б–њ—Г—Б–Ї–∞–љ–Є—П –њ—А–Є PC –Њ–±—Л—З–љ–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—В –Є —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П. –≠—В–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –Љ–Њ–≥—Г—В –±—Л—В—М —Б–ї–µ–і—Б—В–≤–Є–µ–Љ –њ–Њ—А–∞–ґ–µ–љ–Є—П –Њ–њ—А–µ–і–µ–ї–µ–љ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –¶–Э–°, –≤–Њ–Ј–љ–Є–Ї–∞—В—М –Є–Ј-–Ј–∞ –і—А—Г–≥–Є—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –±–Њ–ї–µ–Ј–љ–Є (—Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, —Б–њ–∞—Б—В–Є–Ї–∞, –њ–∞—А–µ–Ј—Л), –∞ —В–∞–Ї–ґ–µ –Є–Љ–µ—В—М –њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї—Г—О –Њ—Б–љ–Њ–≤—Г. –°–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –Љ—Г–ґ—З–Є–љ –њ—А–Њ—П–≤–ї—П—О—В—Б—П —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–Њ–Љ —Н—А–µ–Ї—Ж–Є–Є, —Н—П–Ї—Г–ї—П—Ж–Є–Є, —Б–љ–Є–ґ–µ–љ–Є–µ–Љ –ї–Є–±–Є–і–Њ. –£ –ґ–µ–љ—Й–Є–љ –Њ–љ–Є –Ј–∞–Ї–ї—О—З–∞—О—В—Б—П –≤ –љ–µ–≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є –і–Њ—Б—В–Є—З—М –Њ—А–≥–∞–Ј–Љ–∞, –≤ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –ї—О–±—А–Є–Ї–∞—Ж–Є–Є –Є, —А–µ–ґ–µ, –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ–Љ –њ–Њ–ї–Њ–≤–Њ–Љ –∞–Ї—В–µ. –°–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –ґ–µ–љ—Й–Є–љ –Љ–Њ–≥—Г—В –±—Л—В—М —Б–≤—П–Ј–∞–љ—Л –Є —Б –љ–∞—А—Г—И–µ–љ–Є–µ–Љ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤ –Њ–±–ї–∞—Б—В–Є –≥–µ–љ–Є—В–∞–ї–Є–є, –∞ —В–∞–Ї–ґ–µ —Б –≤—Л—Б–Њ–Ї–Є–Љ —В–Њ–љ—Г—Б–Њ–Љ –≤ –∞–і–і—Г–Ї—В–Њ—А–∞—Е –±–µ–і–µ—А.
–Я–Њ—Б–Ї–Њ–ї—М–Ї—Г —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —Г –±–Њ–ї—М–љ—Л—Е PC –Љ–Њ–≥—Г—В –Є–Љ–µ—В—М –њ—Б–Є—Е–Њ–≥–µ–љ–љ—Г—О –њ—А–Є—А–Њ–і—Г, –±–Њ–ї—М—И–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –Ї–Њ–љ—Б—Г–ї—М—В–Є—А–Њ–≤–∞–љ–Є–µ —Г —Б–µ–Ї—Б–Њ–њ–∞—В–Њ–ї–Њ–≥–∞ –Є –њ—Б–Є—Е–Њ–ї–Њ–≥–∞. –°–ї–µ–і—Г–µ—В –њ—А–Є–љ–Є–Љ–∞—В—М –≤–Њ –≤–љ–Є–Љ–∞–љ–Є–µ –Є —В–Њ, –Ї–∞–Ї–Є–µ –њ—А–µ–њ–∞—А–∞—В—Л –њ–Њ–ї—Г—З–∞–µ—В –±–Њ–ї—М–љ–Њ–є, —В–∞–Ї –Ї–∞–Ї –Љ–љ–Њ–≥–Є–µ –Є–Ј –љ–Є—Е –Љ–Њ–≥—Г—В –≤–ї–Є—П—В—М –љ–∞ —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є. –Я–Њ–±–Њ—З–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ –ї–Є–Њ—А–µ–Ј–∞–ї–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М —Б–љ–Є–ґ–µ–љ–Є–µ –ї–Є–±–Є–і–Њ, –±–µ–љ–Ј–Њ–і–Є–∞–Ј–µ–њ–Є–љ–Њ–≤ – –љ–∞—А—Г—И–µ–љ–Є–µ —Н—П–Ї—Г–ї—П—Ж–Є–Є, —В—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є—Е –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ – –љ–∞—А—Г—И–µ–љ–Є–µ —Н—А–µ–Ї—Ж–Є–Є –Є –ї—О–±—А–Є–Ї–∞—Ж–Є–Є. –Ф–ї—П –ї–µ—З–µ–љ–Є—П —Б–µ–Ї—Б—Г–∞–ї—М–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —Г –Љ—Г–ґ—З–Є–љ –≤ –њ–Њ—Б–ї–µ–і–љ–µ–µ –≤—А–µ–Љ—П –≤—Б–µ —З–∞—Й–µ –њ—А–Є–Љ–µ–љ—П—О—В —Б–Є–ї–і–µ–љ–∞—Д–Є–ї. –°–Є–ї–і–µ–љ–∞—Д–Є–ї –њ—А–Є–љ–Є–Љ–∞—О—В –≤ –і–Њ–Ј–µ 50-100 –Љ–≥ –Ј–∞ 1 —З–∞—Б –і–Њ –њ–Њ–ї–Њ–≤–Њ–≥–Њ –∞–Ї—В–∞. –Я–Њ–±–Њ—З–љ—Л–Љ–Є –і–µ–є—Б—В–≤–Є—П–Љ–Є —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ —П–≤–ї—П—О—В—Б—П –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –Ј–∞–ї–Њ–ґ–µ–љ–љ–Њ—Б—В—М –љ–Њ—Б–∞, –њ–Њ–Ї—А–∞—Б–љ–µ–љ–Є–µ –ї–Є—Ж–∞, –і–Є—Б–њ–µ–њ—Б–Є—П. –°–Є–ї–і–µ–љ–∞—Д–Є–ї –∞–±—Б–Њ–ї—О—В–љ–Њ –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ –±–Њ–ї—М–љ—Л–Љ —Б –Ї–∞—А–і–Є–∞–ї—М–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є. –Т–Њ–Ј–Љ–Њ–ґ–љ–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–Є—Б–њ–Њ—Б–Њ–±–ї–µ–љ–Є–є –і–ї—П –≤–∞–Ї—Г—Г–Љ–љ–Њ–є —Н—А–µ–Ї—Ж–Є–Є. –Ш—Б–њ–Њ–ї—М–Ј—Г—О—В –Є –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л: –Є–љ—В—А–∞—Г—А–µ—В—А–∞–ї—М–љ—Л–µ —Б–≤–µ—З–Є —Б –њ—А–Њ—Б—В–∞–≥–ї–∞–љ–і–Є–љ–Њ–Љ –Х1 –Є –Є–љ—К–µ–Ї—Ж–Є–Є —Н—В–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –Є–ї–Є –њ–∞–њ–∞–≤–µ—А–Є–љ–∞ –≤ –њ–Њ–ї–Њ–≤–Њ–є —З–ї–µ–љ. –Я–Њ–±–Њ—З–љ—Л–Љ–Є —Н—Д—Д–µ–Ї—В–∞–Љ–Є —В–∞–Ї–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –Љ–Њ–≥—Г—В –±—Л—В—М –±–Њ–ї–µ–Ј–љ–µ–љ–љ–Њ—Б—В—М –≤ –Љ–µ—Б—В–µ –Є–љ—К–µ–Ї—Ж–Є–Є –Є —Д–Є–±—А–Њ–Ј –њ–Њ–ї–Њ–≤–Њ–≥–Њ —З–ї–µ–љ–∞. –Э—Г–ґ–љ–Њ –Њ—В–Љ–µ—В–Є—В—М, —З—В–Њ —Е–Њ—В—П –љ–∞—З–∞–ї—М–љ–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Н—В–Њ–≥–Њ –Љ–µ—В–Њ–і–∞ –Њ—З–µ–љ—М –≤—Л—Б–Њ–Ї–∞, —З–µ—А–µ–Ј 2 –≥–Њ–і–∞ –µ–≥–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Њ–љ–∞ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Б–љ–Є–ґ–∞–µ—В—Б—П. –Ю—В—Б—Г—В—Б—В–≤–Є–µ –ї—О–±—А–Є–Ї–∞—Ж–Є–Є —Г –ґ–µ–љ—Й–Є–љ –Љ–Њ–ґ–љ–Њ –Ї–Њ–Љ–њ–µ–љ—Б–Є—А–Њ–≤–∞—В—М –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –Є–љ—В—А–∞–≤–∞–≥–Є–љ–∞–ї—М–љ—Л—Е —Г–≤–ї–∞–ґ–љ–Є—В–µ–ї–µ–є, –∞ —Б–љ–Є–ґ–µ–љ–Є–µ –њ–Њ—А–Њ–≥–∞ –Њ—А–≥–∞–Ј–Љ–∞ –і–Њ—Б—В–Є–≥–∞–µ—В—Б—П –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ–Љ –≤–Є–±—А–∞—В–Њ—А–Њ–≤.
–Ш, –±–µ–Ј—Г—Б–ї–Њ–≤–љ–Њ, –љ–∞ –≤—Б–µ—Е —Н—В–∞–њ–∞—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –Ї–∞–Ї –≤ —Б—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л—Е, —В–∞–Ї –Є –≤–љ–µ—Б—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л—Е —Г—Б–ї–Њ–≤–Є—П—Е, –Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ–∞—П —В–µ—А–∞–њ–Є—П –і–Њ–ї–ґ–љ–∞ –±—Л—В—М –і–Њ–њ–Њ–ї–љ–µ–љ–∞ –Љ–µ—В–Њ–і–∞–Љ–Є –љ–µ–є—А–Њ—А–µ–∞–±–Є–ї–Є—В–∞—Ж–Є–Є – –Љ–∞—Б—Б–∞–ґ–µ–Љ, —Д–Є–Ј–Є–Њ—В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ–Є –њ—А–Њ—Ж–µ–і—Г—А–∞–Љ–Є, –Ы–§–Ъ –Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ —А–∞–Ј–ї–Є—З–љ—Л—Е –њ—А–Є—Б–њ–Њ—Б–Њ–±–ї–µ–љ–Є–є –і–ї—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є. –І—А–µ–Ј–≤—Л—З–∞–є–љ–Њ –≤–∞–ґ–љ–∞ –Є —Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –њ–Њ–Љ–Њ—Й—М –±–Њ–ї—М–љ—Л–Љ PC.
–°–њ–Є—Б–Њ–Ї –ї–Є—В–µ—А–∞—В—Г—А—Л –Т—Л –Љ–Њ–ґ–µ—В–µ –љ–∞–є—В–Є –љ–∞ —Б–∞–є—В–µ http://www.rmj.ru
–Ґ–Њ–ї—В–µ—А–Њ–і–Є–љ –
–Ф–µ—В—А—Г–Ј–Є—В–Њ–ї (—В–Њ—А–≥–Њ–≤–Њ–µ –љ–∞–Ј–≤–∞–љ–Є–µ)
(Pharmacia)
1. –У—Г—Б–µ–≤ –Х.–Ш., –Ф–µ–Љ–Є–љ–∞ –Ґ.–Ы. –Є –і—А., –Ш–Љ–Љ—Г–љ–Њ–Љ–Њ–і—Г–ї–Є—А—Г—О—Й–µ–µ –ї–µ—З–µ–љ–Є–µ —А–∞—Б—Б–µ—П–љ–љ–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞. –Ь–Њ—Б–Ї–≤–∞, –Р–Ю “ –І–µ—А—В–∞–љ–Њ–≤—Б–Ї–∞—П —В–Є–њ–Њ–≥—А–∞—Д–Є—П”, 1992.
2.–У—Г—Б–µ–≤ –Х.–Ш., –Ф–µ–Љ–Є–љ–∞ –Ґ.–Ы., –С–Њ–є–Ї–Њ –Р.–Э., “ –†–∞—Б—Б–µ—П–љ–љ—Л–є —Б–Ї–ї–µ—А–Њ–Ј”, –Ь., 1997.
3.–Ф–µ–Љ–Є–љ–∞ –Ґ.–Ы., –У—Г—Б–µ–≤ –Х.–Ш. –Є –і—А., –Я–µ—А–≤—Л–є –Њ–њ—Л—В –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –Ї–Њ–њ–∞–Ї—Б–Њ–љ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —А–µ–Љ–Є—В—В–Є—А—Г—О—Й–µ–є —Д–Њ—А–Љ—Л —А–∞—Б—Б–µ—П–љ–љ–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞ –≤ –†–Њ—Б—Б–Є–Є. –Ь–∞—В–µ—А, –Ї –†–µ–≥–Є–Њ–љ, —Б–Њ–≤. “ –Т–Њ–њ—А–Њ—Б—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л”, –Ь., 1999, —Б—В—А. 127-129.
4.–Ф–µ–Љ–Є–љ–∞ –Ґ.–Ы., –Ч–∞–≤–∞–ї–Є—И–Є–љ –Ш.–Р. –Є –і—А. –Р—Б–њ–µ–Ї—В—Л –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є —А–∞—Б—Б–µ—П–љ–љ–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞. –Ь–∞—В–µ—А, –Љ–µ–ґ–і—Г–љ–∞—А. –Ї–Њ–љ—Д. “ –£–ї—Г—З—И–µ–љ–Є–µ –Ї–∞—З–µ—Б—В–≤–∞ –ґ–Є–Ј–љ–Є –Є–љ–≤–∞–ї–Є–і–Њ–≤ –±–Њ–ї—М–љ—Л—Е —А–∞—Б—Б–µ—П–љ–љ—Л–Љ —Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ –≤ —Б—В—А–∞–љ–∞—Е –Х–≤—А–Њ–њ—Л”. –°–∞–Љ–∞—А–∞, 1999,—Б—В—А.24-28.
5.–Ч–∞–≤–∞–ї–Є—И–Є–љ –Ш.–Р., –Я–µ—А–µ—Б–µ–і–Њ–≤–∞ –Р.–Т., –Ц—Г—З–µ–љ–Ї–Њ –Ґ.–Ф. –Ю—В –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ –Ї –ї–µ—З–µ–љ–Є—О —А–∞—Б—Б–µ—П–љ–љ–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞. –Ь–∞—В–µ—А, –Ї –†–µ–≥–Є–Њ–љ, —Б–Њ–≤. “ –Т–Њ–њ—А–Њ—Б—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л”. –Ь.,1999, —Б—В—А.28-38.
6. –Ы–µ—В–љ—П—П —И–Ї–Њ–ї–∞ –њ–Њ —А–∞—Б—Б–µ—П–љ–љ–Њ–Љ—Г —Б–Ї–ї–µ—А–Њ–Ј—Г. –Р–Љ—Б—В–µ—А–і–∞–Љ, 1998 –≥.
7. –†–∞—Б—Б–µ—П–љ–љ—Л–є —Б–Ї–ї–µ—А–Њ–Ј. –Ш–Ј–±—А–∞–љ–љ—Л–µ –≤–Њ–њ—А–Њ—Б—Л —В–µ–Њ—А–Є–Є –Є –њ—А–∞–Ї—В–Є–Ї–Є”, –њ–Њ–і —А–µ–і. –Ш.–Р.–Ч–∞–≤–∞–ї–Є—И–Є–љ–∞, –Ь., 2000.
8. –®–Љ–Є–і—В –Ґ.–Х., –Ц—Г—З–µ–љ–Ї–Њ –Ґ.–Ф. –Ъ–Њ–њ–∞–Ї—Б–Њ–љ - –љ–Њ–≤–Њ–µ —Б—А–µ–і—Б—В–≤–Њ –і–ї—П –ї–µ—З–µ–љ–Є—П —А–∞—Б—Б–µ—П–љ–љ–Њ–≥–Њ —Б–Ї–ї–µ—А–Њ–Ј–∞. –Т–µ—Б—В–љ–Є–Ї –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є, –Ь., 1998, 4,—Б—В—А. 15-18.
9. –®–Љ–Є–і—В –Ґ.–Х., –Ц—Г—З–µ–љ–Ї–Њ –Ґ.–Ф., –Ы—Г–Ї—М—П–љ–Њ–≤–∞ –Ъ.–°. –Я—А–Њ–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ. –і–Є—Д—Д–µ—А–µ–љ—Ж–Є–∞–ї—М–љ—Л–є –і–Є–∞–≥–љ–Њ–Ј –Є –ї–µ—З–µ–љ–Є–µ —А–µ—В—А–Њ–±—Г–ї—М–±–∞—А–љ–Њ–≥–Њ –љ–µ–≤—А–Є—В–∞ –њ—А–Є —А–∞—Б—Б–µ—П–љ–љ–Њ–Љ —Б–Ї–ї–µ—А–Њ–Ј–µ. –Ь–∞—В–µ—А, –Ї –†–µ–≥–Є–Њ–љ. —Б–Њ–≤. “–Т–Њ–њ—А–Њ—Б—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л”. M., 1999, —Б—В—А. 91-98. lO.Aisen M.L. et al. The effect of mechanical damping loads on disabling action tremor. Neurol., 1993,43,1346-1350.
11. Alam M. et al. Methylprednisolon in multiple sclerosis. A comparision of oral with intravenous therapy. J. Neurol. Neurosurg. Psych..1993,56,1219-1220.
12.Alter M. et al. Practice advisory on selection of patients with MS for treatment with betaseron. Neurology, 1994,44,15370-1540.
13.Barnes M.P. et al. Intravenous methylprednisolone for MS in relapse. J. Neurol..Neurosurg., Psych.,1985,48,157-159.
14.Bass –Т. et al. Tizanidine versus baclofen in the treatment of spasticity in patients with MS. Can.J.Neurol. Sci.,1988,15,15-19.
15.Beck R.W. Corticosteroid treatment of optic neuritis. A need to change treatment practices. Neurol.,1992,42,1133-1135.
16.Blaivas J.G. Management of bladder dysfunction in MS. Neurol.,1980,30,12-18.
17.Bozek –°.–Т. et al. A controlled trial of isoniazide therapy for action tremor in MS. Neurol.,1987,234,36-39.
18.Canadian MS Research Group. A randomized controlled trial of amantadine in fatigue associated with MS. Can.J. Neurol.Sci.,1987,14,273-278. 19-Chezzi A. Sexual dysfunction in MS. Int.MSJ.5,2,45-53.
20.Fazecas F. et al. Intravenous immunoglobuline trials in MS. Int. MSJ, 6,1,15-21.
21.Fowler C.J. et al. Treatment of lower urinary tract dysfunction in patients with MS. J. Neurol.,Nerosurg.,Psych., 1992,55,986-989.
22.Multiple sclerosis. Eds. Paty D.W.,Ebers G.C.,Philadelphia, 1997.
23.MS. Ed. Kesselring J.,1997.
24.Multiple Sclerosis Therapeutics. Eds. Rudick R.A.,Goodkin D.E..2-nd ed.,London,2000.
25.Noth J. Trends in the pathophysiology and pharmacotherapy of spasticity. J.Neurol.,1991,238,131-139.
26.0sterman P.O.,Westerberg C.E. Paroxysmal attacks in MS. Brain.1975,38,189-202/
27.Polman Ch.H. Interferon beta Ib and secondary progressive MS. Int. MSJ,5.2,40-43.
28.Poser C.M. et al. New diagnostic criteria for MS. Guidelines for research protocol. Ann. Neurol.,1984,13,227-231.
29.Schapiro R.T. Symptom management in MS/Ann. Neurol.,1994,36,5123-5129.
30. Stenager E. et al. Sexual function in MS. 10’ Congress of the European Committee for treatment and research in MS. Greece,! 994/
31.Walter E.U. et al. Management of side-effects of beta- interferon therapy in MS. Int. MSJ.5,2,65-75.
32.Whitlock F.A., Siskind M.M. Depression as a major symptom of MS. J. Neurol-.Neurosurg., Psych.,1980,43,861-865.
33. Weiner H.L., Dawson D.M. Plasmopheresis in MS. Neurol.,1980, 30, 1029-1033.












