Боль в спине непосредственно связана с дегенеративным процессом в межпозвонковом диске [K. Luoma et al., 2000], который приводит к грыжеобразованию. Патологические изменения в области диска клинически могут протекать как асимптомно, так и вызывать болевой синдром, как в области поясницы, так и ноге [S.D. Boden, D.O. Davis et al., 1990]. Дегенеративный процесс вызывает снижение высоты межпозвонкового диска и, следовательно, изменение биомеханики движений в позвоночнике. Это приводит к вовлечению в патологический процесс рядом расположенных структур (фасеточных суставов, мышц, связок). Эти процессы – патология межпозвонкового диска, дегенеративно–дистрофические изменения фасеточных суставов и связок (особенно желтых) – вызывают стенозирование позвоночного канала, которое является наиболее частой причиной болей в спине у людей пожилого возраста.
В межпозвонковых дисках дегенеративные изменения наступают значительно раньше, чем в костных и мышечных структурах. Так, начальные их проявления выявляют в возрасте 11–16 лет [N. Boos, S. Weissbach et al., 2002]. Было замечено, что дегенерация межпозвонковых дисков увеличивается с возрастом, особенно у мужчин. У 20% людей в молодом возрасте наблюдаются умеренные признаки дегенерации, тогда как к 50 годам у 10%, а к 70 годам у 60% степень изменений достигает выраженной [J. Miller, C. Schmatz, A. Schultz, 1988].
Анатомия
Межпозвонковые диски (рис. 1А) находятся между телами позвонков. Они являются основным элементом, связывающим позвоночный столб в единое целое, и составляют 1/3 его высоты (рис. 1Б). Основной функцией межпозвонковых дисков является механическая (опорная и амортизирующая). Они обеспечивают гибкость позвоночного столба при различных движениях (наклоны, вращения). В поясничном отделе позвоночника диаметр дисков в среднем составляет 4 см, а высота – 7–10 мм [L.T. Twomey, J.R. Taylor, 1987]. Межпозвонковый диск имеет сложное строение. В центральной его части находится пульпозное ядро, которое окружено хрящевым (фиброзным) кольцом. Выше и ниже пульпозного ядра располагаются замыкательные (концевые) пластинки (рис. 1 А,Б).
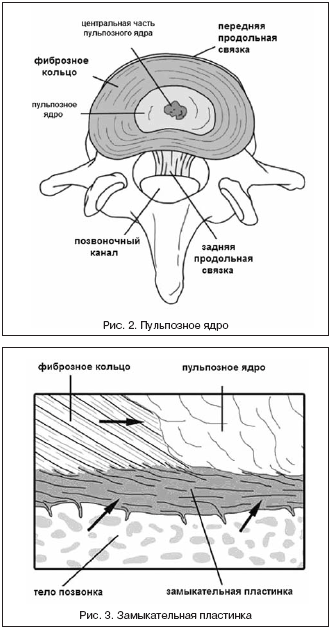
Пульпозное ядро содержит хорошо гидратированные коллагеновые (расположены беспорядочно) и эластические (расположены радиально) волокна [J. Yu et al., 2002] (рис. 2). На границе между пульпозным ядром и фиброзным кольцом (которое четко определяется до 10 лет жизни) с достаточно низкой плотностью расположены клетки, напоминающие хондроциты.
Фиброзное кольцо состоит из 20–25 колец или пластин [F. Marchand, AM. Ahmed, 1990], между которыми расположены волокна коллагена, которые направлены параллельно пластинкам и под углом 60° к вертикальной оси (рис. 1). Радиально по отношению к кольцам расположены эластические волокна, которые восстанавливают форму диска после совершившегося движения [J. Yu et al., 2002]. Клетки фиброзного кольца, расположенные ближе к центру, имеют овальную форму, тогда как на его периферии они удлиняются и располагаются параллельно коллагеновым волокнам, напоминая фибробласты. В отличие от суставного хряща, клетки диска (как пульпозного ядра, так и фиброзного кольца), имеют длинные, тонкие цитоплазматические выросты, которые достигают 30 мкм и больше [S.B. Bruehlmann et al., 2002]. Функция этих выростов остается неизвестной, однако предполагают, что они способны к восприятию механического напряжения в тканях [R.J. Errington et al., 1998].
Замыкательные (концевые) пластинки представляют собой тонкий (меньше 1 мм) слой гиалинового хряща, расположенного между телом позвонка и межпозвонковым диском. Содержащиеся в нем коллагеновые волокна расположены горизонтально [S. Roberts et al., 1989] (рис. 3).
Межпозвонковый диск здорового человека содержит кровеносные сосуды и нервы лишь во внешних пластинках фиброзного кольца [S. Roberts et al., 1995]. Замыкательная пластинка, как и любой гиалиновый хрящ, не имеет сосудов и нервов. В основном нервы идут в сопровождении сосудов, однако могут идти и независимо от них (ветви синувертебрального нерва, передней и серой коммуникантных ветвей). Синувертебральный нерв представляет собой возвратную менингиальную ветвь спинального нерва. Этот нерв выходит из спинального ганглия и проникает в межпозвонковое отверстие, где делится на восходящую и нисходящую ветви (рис. 4).
Как было показано на животных, чувствительные волокна синувертебрального нерва образованы волокнами как переднего, так и заднего корешков (рис. 5). Необходимо отметить, что передняя продольная связка иннервируется ветвями спинального ганглия. Задняя продольная связка ноцицептивную иннервацию получает от восходящих ветвей синувертебрального нерва, который также иннервирует наружные пластинки фиброзного кольца [W.E. Johnson et al., 2001].
С возрастом происходит постепенное стирание границы между фиброзным кольцом и пульпозным ядром, которое становится все более и более фиброзированным [J.A. Buckwalter, 1995]. Со временем диск морфологически становится менее структурированным – изменяются кольцевые пластинки фиброзного кольца (сливаются, раздваиваются), коллагеновые и эластические волокна располагаются все более хаотично. Часто образуются трещины, особенно в пульпозном ядре. Процессы дегенерации наблюдаются и в кровеносных сосудах и нервах диска [S. Roberts et al., 1995]. Происходит фрагментарная клеточная пролиферация (особенно в пульпозном ядре) [W.E.B. Johnson et al., 2001]. Со временем наблюдается гибель клеток межпозвонкового диска. Так, у взрослого человека количество клеточных элементов уменьшается почти в 2 раза [J.J. Trout et al., 1982]. Нужно отметить, что дегенеративные изменения межпозвонкового диска (гибель клеток, фрагментарная клеточная пролиферация, фрагментирование пульпозного ядра, изменения фиброзного кольца), выраженность которых определяется возрастом человека, достаточно сложно дифференцировать с теми изменениями, которые бы трактовались как «патологические».
Физиология
Механические свойства (и соответственно функция) межпозвонкового диска обеспечиваются межклеточной матрицей, основными компонентами которой являются коллаген и аггрекан (протеогликан). Коллагеновая сеть образована коллагеновыми волокнами I и II типа, которые составляют примерно 70% и 20% сухого веса всего диска соответственно. Коллагеновые волокна обеспечивают прочность диска и фиксируют его к телам позвонков [D.R. Eyre, H. Muir, 1977]. Аггрекан (основной протеогликан диска), состоящий из хондроитина и кератансульфата, обеспечивает диск гидратацией. Так, вес протеогликанов и воды в фиброзном кольце составляет 5 и 70%, а в пульпозном ядре – 15 и 80% соответственно. В межклеточной матрице постоянно происходят синтетические и литические (протеиназы) процессы. Тем не менее она является структурой гистологически постоянной, что обеспечивает механическую прочность межпозвонкового диска [C. Weiler et al., 2002].
Несмотря на морфологическую схожесть с суставным хрящом, межпозвонковый диск имеет ряд отличий. Так, в протеингликанах (аггрекан) диска отмечается более высокое содержание кератансульфата. Кроме того, у одного и того же человека аггреканы диска имеют меньшие размеры и более выраженные дегенеративные изменения, чем аггреканы суставного хряща [B. Johnstone et al., 1995].
Патофизиология
Основным элементом дегенерации межпозвонкового диска является уменьшение количества протеингликанов. Происходит фрагментация аггреканов, потеря глюкозаминогликанов, что приводит к падению осмотического давления и, как следствие, дегидратации диска. Однако даже в дегенерированных дисках клетки сохраняют способность к продуцированию нормальных аггреканов [R.I. Inkinen et al., 1998].
По сравнению с протеингликанами коллагеновый состав диска изменяется в меньшей степени. Так, абсолютное количество коллагена в диске, как правило, не меняется. Однако возможно перераспределение различных типов коллагеновых волокон. Кроме того, происходит процесс денатурации коллагена. Однако, по аналогии с протеингликанами, дисковые клеточные элементы сохраняют способность к синтезу здорового коллагена даже в дегенерированном межпозвонковом диске [V.C. Duance et al., 1998].
Потеря протеингликанов и дегидратация диска приводят к снижению их амортизационной и опорной функций. Межпозвонковые диски уменьшаются по высоте, постепенно начинают пролабировать в позвоночный канал. Таким образом, неправильное перераспределение осевой нагрузки на замыкательные пластинки и фиброзное кольцо может провоцировать дискогенные боли [D.S. McNally et al., 1996]. Дегенеративно–дистрофические изменения не ограничиваются только межпозвонковым диском, поскольку изменение его высоты приводит к патологическим процессам в соседних образованиях. Так, снижение опорной функции диска приводит к перегрузкам в фасеточных суставах, что способствует развитию остеоартроза и уменьшению натяжения желтых связок, что приводит к снижению их эластичности, гофрированию. Пролабирование диска, артроз фасеточных суставов и утолщение (гофрирование) желтых связок приводит к стенозу позвоночного канала [M.A. Adams et al., 1990].
В настоящее время доказано, что компрессия корешка межпозвонковой грыжей не является единственной причиной радикулярных болей, поскольку около 70% людей не испытывают болей при сдавлении корешков грыжевым выпячиванием [N. Boos et al., 1995]. Полагают, что в некоторых случаях при контакте грыжи диска и корешка происходит сенситизация последнего вследствие асептического (аутоиммунного) воспаления, источником которого являются клетки пораженного диска [K. Olmarker, B. Rydevik, 2002].
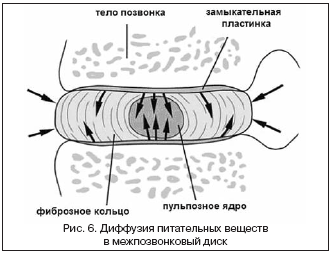
Одной из основных причин дегенерации межпозвонкового диска является нарушение адекватного питания его клеточных элементов. In vitro было показано, что клетки межпозвонкового диска достаточно чувствительны к дефициту кислорода, глюкозы и изменению pH. Нарушение функции клеток приводит к изменению состава межклеточной матрицы, что запускает и/или ускоряет дегенеративные процессы в диске. Питание клеток межпозвонкового диска происходит опосредовано, поскольку кровеносные сосуды располагаются от них на удалении до 8 мм (капилляры тел позвонков и наружных пластинок фиброзного кольца (рис. 6) [S. Holm et al., 1981].
Нарушение питания диска может быть связано со многими причинами: различными анемиями, атеросклерозом [J.P. Jones, 1997]. Кроме того, метаболические нарушения наблюдаются при перегрузках и недостаточных нагрузках на межпозвонковый диск. Полагают, что в этих случаях происходит перестройка капилляров тел позвонков и/или уплотнение замыкательных пластинок, что затрудняет диффузию питательных веществ [S. Roberts et al., 1996]. Однако необходимо отметить, что дегенеративный процесс связан только с неправильным выполнением движений при физических нагрузках, тогда как правильное их выполнение увеличивает внутридисковое содержание протеингликанов.
Выделяют несколько стадий дегенеративно–дистрофических изменений межпозвонкового диска [B.L. Sachs et al., 1987]:
• Стадия 0. Диск не изменен.
• Стадия 1. Небольшие разрывы внутренних 1/3 кольцевых пластин фиброзного кольца.
• Стадия 2. Происходит значительное разрушение диска, однако сохраняются наружные кольца фиброзного кольца, которые предотвращают грыжеобразование. Компрессии корешков нет. На этом этапе помимо болей в спине может наблюдаться ее иррадиация в ноги до уровня коленного сустава.
• Стадия 3. Наблюдаются трещины и разрывы по всему радиусу фиброзного кольца. Диск пролабирует, вызывая разрывы задней продольной связки.
В настоящее время эта классификация несколько изменена, поскольку она не предусматривала компрессионных синдромов.
Попытки создания настоящей классификации, основой для которой являлись данные компьютерной томографии, предпринимались с 1990 года и завершились в 1996 году (Schellhas):
• Стадия 0. Введенное в центр диска контрастное вещество не покидает границ пульпозного ядра (рис. 7).
• Стадия 1. На этом этапе контраст проникает до внутренней 1/3 фиброзного кольца.
• Стадия 2. Контраст распространяется на 2/3 фиброзного кольца.
• Стадия 3. Трещина по всему радиусу фиброзного кольца. Контраст проникает до внешних пластин фиброзного кольца. Полагают, что на этом этапе возникает болевой синдром, поскольку лишь внешние слои диска иннервированы.
• На 4–й стадии наблюдается распространение контраста по окружности (напоминает якорь), но не более чем на 30°. Это связано с тем, что радиальные разрывы сливаются с концентрическими.
• На 5–й стадии происходит проникновение контраста в перидуральное пространство. По–видимому, это провоцирует асептическое (аутоиммунное) воспаление в рядом расположенных мягких тканях, что иногда вызывает радикулопатию даже без явных признаков компрессии.
Механизм дискогенной боли
В 1979 году Brodsky и Binder попытались выявить механизмы возникновения дискогенных болей с помощью дискографии. Они показали, что боль возникает при введении веществ, подобных глюкозаминогликанам и молочной кислоте, при компрессии корешков, при гиперфлексии фасеточных суставов. Кроме того, они предположили, что источником боли могут быть замыкательные пластинки.
Ohnmeiss в 1997 году показал, что для возникновения болей в ноге не обязательным является полный разрыв фиброзного кольца или возникновение грыжи диска. Он доказал, что даже на 2–й стадии (когда остаются сохранными внешние пластинки фиброзного кольца) возникает боль в пояснице с иррадиацией в ногу.
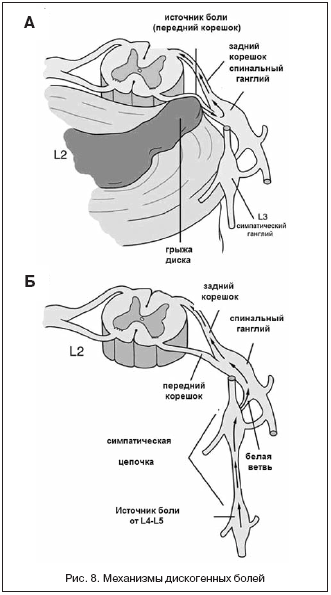
Патогенез развития дискогенных болей остается до конца не изученным. Традиционно считается, что источником боли является непосредственно тот корешок, который подвергается компрессии (рис. 8 А).
Однако в настоящее время доказано, что боль с одного уровня может исходить и из нижележащих сегментов (рис. 8 Б) [W.S. Oh, J.C. Shim, 2004]. Как показано на рисунке, патология диска L4–L5 может вызывать боль в дерматоме L2.
Лечение дискогенных болей
Большая часть основных методов как хирургического, так и консервативного лечения дискогенных болей направлена не на восстановление патологического диска, а на уменьшение симптомов заболевания. По сути, это паллиативная терапия, нацеленная на скорейшее восстановление трудоспособности пациента. Она включают в себя постельный режим (с ранней активизацией), использование нестероидных противовоспалительных препаратов, миорелаксантов, локальное введение местных анестетиков и кортикостероидов, мануальную терапию и различные способы хирургической коррекции.
Отношение к хирургическому вмешательству в мире несколько отличается и составляет лишь небольшой процент от общего числа больных, страдающих болями в спине. Так, в Великобритании оперируется один из 2000 пациентов с болью в спине, тогда как в Соединенных Штатах Америки этот показатель в 5 раз выше [J.N. Gibson et al., 2000]. При этом эффективность оперативного лечения дискогенных болей в этих странах сопоставима. Однако последние исследования показывают, что при соответствующем отборе пациентов эффективность хирургической коррекции дискогенных болей значительно повышается [P. Fritzell et al., 2001].
Хирургическая терапия включает в себя дискэктомию с артродезом, внутридисковое введение стероидов, внутридисковую декомпрессию, пластику фиброзного кольца, различные варианты лазерной терапии. В настоящее время все большее распространение получают малоинвазивные методики: пластика фиброзного кольца (электротермическая, высокочастотная), чрескожная дисковая декомпрессия (лазерная, высокочастотная, механическая), эндоскопическая чрескожная дискэктомия.
В последнее время разрабатываются новые направления в хирургии межпозвонкового диска – замена пульпозного ядра [L.M. Boyd, A.J. Carter, 2006], восстановление замыкательных пластинок [J.C. Lotz, A.J. Kim, 2005], замена диска [R.C. Huang et al., 2004].
Большие усилия исследователей направлены на возможности восстановления страдающего диска. Основная причина активного изучения возможности восстановления пораженного межпозвонкового диска обусловлена тем, что нарушение биомеханики движения (которое не корригируется симптоматической терапией) вызывает патологию рядом расположенных образований (связки, мышцы, фасеточные суставы), что приводит к развитию спинального стеноза.
Веществами, способствующими восстановлению межпозвонкового диска, являются глюкозамин и хондроитин сульфат. Их эффективность доказана как при патологии межпозвонкового диска, так и патологии хряща периферических суставов (остеоартроз) [T.E. McAlindon et al., 2000]. Предполагают, что глюкозамин и хондроитин сульфат стимулируют работу хондроцитов (биосинтез протеогликанов) и угнетают функцию литических ферментов (протеиназ). Это способствует улучшению качественного состава межклеточной матрицы и соответственно восстановлению физических свойств межпозвонкового диска. Существуют различные способы введения глюкозамина и хондроитин сульфата – пероральный, трансдермальный и интрадискальный [R. Derby et al., 2004].
Исследованию хондроитин сульфата посвящен опубликованный мета–анализ, охвативший исследования вплоть до 1999 г. [McAlindon T.E. et al., 2000]. Авторы приходят к заключению, что хондроитин сульфат оказывает умеренное или значительное воздействие на выраженность болевого синдрома и функциональную подвижность суставов при остеоартрозе по сравнению с плацебо. Данное вещество является безопасным и характеризуются минимумом побочных эффектов. В рандомизированном контролируемом сравнительном исследовании хондроитин сульфата и диклофенака, проведенном у 146 пациентов, более быстрое уменьшение выраженности клинических симптомов наблюдалось у больных, применявших нестероидные противовоспалительные препараты, однако возврат этих симптомов отмечался сразу после отмены терапии; хондроитин сульфат, напротив, характеризовался более медленным началом терапевтического действия, сохранявшемся до 3 месяцев после окончания лечения [Morreale P. et al., 1996]. Еще одно рандомизированное контролируемое исследование [Mazieres В. et al., 2001] продемонстрировало преимущества хондроитин сульфата перед плацебо у 130 пациентов с остеоартрозом коленных суставов и еще раз подтвердило сохранение терапевтического эффекта до 1 месяц после окончания лечения.
Таким образом, эффективность хондроитин сульфата была доказана только при лечении остеоартроза коленных и тазабедренных суставов и имеет степень доказательности А (EULAR, Европейская противоревматическая лига). В то же время при лечении болевых синдромов в спине (остеохондроз) масштабных, двойных слепых, плацебо контролируемых исследований не проводилось. Однако, принимая во внимание анатомо–гистологическую похожесть хрящевой ткани диска и периферических суставов можно предполагать похожую эффективность хондроитин сульфата и при остеохондрозе. Так в некоторых отечественных исследованиях была показана эффективность хондроитин сульфата при болях в спине [Н.А. Шостак et al., 2004; С.П. Филоненко et al., 2005]. Исследователями было показано достоверное уменьшение болевого синдрома и улучшения трудоспособности.
Одним из препаратов, содержащих хондроитин сульфат, является Хондроксид («Нижфарм», Россия). Одна его таблетка содержит в качестве активного компонента хондроитина сульфат – 0,25 г (сухого и 100%–го вещества) и вспомогательные вещества. При однократном приеме Хондроксида средней терапевтической дозы максимальная концентрация в плазме достигается через 3–4 ч. Накапливается, главным образом, в хрящевой ткани (максимальная концентрация в суставном хряще достигается через 48 ч.). Принимают Хондроксид внутрь, по 0,5 г (2 таблетки) 2 раза в сутки. Таблетки принимают, запивая небольшим количеством воды. Рекомендуемая продолжительность начального курса составляет 6 мес. Следует учитывать, что терапевтическое действие Хондроксида сохраняется в течение 3–5 мес. после его отмены в зависимости от локализации и стадии заболевания.
Современным и активно изучающимся направлением в терапии дегенеративно–дистрофических изменений межпозвонкового диска является клеточная терапия. Суть этого метода состоит в стимуляции (как правило, используют факторы роста) продукции межклеточной матрицы [R. Osada et al., 1996] и блокировании некоторых цитокинов, ингибирующих матричный синтез [K. Takegami et al., 2002]. Однако внутридисковое введение факторов роста и ингибиторов цитокинов не привело к восстановлению матрицы, поскольку их действие оказалось достаточно коротким. В настоящее время данный вид терапии пытаются реализовать при помощи генной инженерии [K. Nishida et al., 1999].