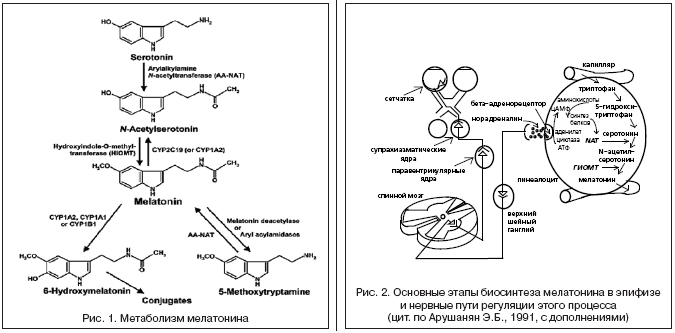
Мелатонин (М) образно называют «гормоном ночи», «Дракула–гормоном» или «биохимическим аналогом темноты».
Основные этапы биосинтеза мелатонина и временная динамика его образования сегодня хорошо изучены (рис. 2). Синтез мелатонина осуществляется в эпифизе, его источником служит триптофан, который поступает в пинеалоциты из сосудистого русла и через 5–окситриптофан превращается в серотонин. Лимитирующим фактором в синтезе гормона служит активность фермента N–ацетилтрансферазы (NАТ), контролирующего образование предшественника – N–ацетилсеротонина, в дальнейшем при участии гидроксииндол–О–метилтрансферазы (ГИОМТ) превращающегося в сам мелатонин. Принципиально важным является факт циркадианной (околосуточной) периодичности выработки в пинеалоците биологически активных соединений. Синтез мелатонина эффективно происходит только с наступлением темноты и падает в светлую фазу суток – факт, впервые показанный R. Wurtman в 1960 году. Достаточно короткого светового импульса (силой 0,1–1 lux), чтобы подавить этот процесс. В дневные часы в ткани железы, напротив, накапливается серотонин.
Дневной ритм продукции мелатонина зависит от активности NАТ в сетчатке, которая, в свою очередь, зависит от ионов кальция, дофамина и гамааминомасляной кислоты (ГАМК).
Сетчатка является независимым и важным местом продукции мелатонина, по содержанию которого она стоит на втором месте после эпифиза. По–видимому, сетчатке принадлежит определенная роль в поддержании уровня плазменного мелатонина в случае ослабления эпифизарной активности. Предполагается, что дофамин (биохимический аналог света) передает пигментному эпителию сигнал о свете, а мелатонин (биохимический аналог темноты) – о темноте, причем баланс между этими двумя нейрогормонами регулирует функцию пигментного эпителия при изменении адаптации.
На образовании мелатонина заметно сказывается целый ряд внешних и внутренних факторов. Особенно значимым надо признать длину фотопериода, поскольку величина секреции находится в обратных отношениях с продолжительностью светового дня. В случае инверсии светового режима, спустя несколько суток извращается и суточная динамика уровня мелатонина. Повреждение любого звена пути регуляции синтеза гормона, начиная с сетчатки, приводит к снижению ночной секреции мелатонина, распаду циркадианного ритма на отдельные ультрадианные составляющие. Из эндогенных факторов существенное значение могут иметь характер гормональной активности (особенно состояние гонад), а также возраст. Из–за возрастной инволюции железы наблюдается прогрессивное снижение амплитуды и величины секреции гормона на протяжении суток.
Мелатонин является многофункциональным гормоном, что определяется в том числе и значительной представленностью его рецепторов в различных образованиях головного мозга. Наиболее высоки уровень гормона и плотность мелатониновых рецепторов (МТ1, МТ2 и МТ3) в переднем гипоталамусе (преоптическая, медиобазальная области), за которыми следуют промежуточный мозг, гиппокамп, стриатум и неокортекс. Через эти рецепторы мелатонин способен ограничивать поведенческие нарушения, обусловленные стрессом, прямо вмешиваясь в работу эндокринных центров гипоталамуса и неэндокринных стресс–организующих структур мозга. Мелатониновые рецепторы описаны в различных эндокринных органах, начиная с гонад, где их содержание особенно велико, и кончая надпочечниками. Значительная плотность специализированных рецепторов обнаружена и в клетках самого эпифиза. Повышение концентрации мелатонина в крови с наступлением темноты снижает у человека температуру тела, уменьшает эмоциональную напряженность, индуцирует сон, а также незначительно угнетает функцию половых желез, что отражается в задержке пролиферации опухолевых клеток молочной и предстательной желез. Мелатонин участвует в гормональном обеспечении околосуточного и сезонного периодизма поведенческой активности.
Мелатонин является одним из самых мощных эндогенных антиоксидантов. Антиоксидантная активность мелатонина определена во всех клеточных структурах, включая ядро клетки. Мелатонин обладает протективными свойствами в отношении свободнорадикального поражения ДНК, белков и липидов. Мелатонин способен связывать свободные радикалы (гидроксил, свободный кислород, пероксинитрит и т.д.) и стимулировать активность антиоксидантной системы (ферменты супероксид дисмутаза, глутатион пероксидаза, глутатион редуктаза, глюкозо–6–фосфат ДГ). Мелатонин обеспечивает защиту клеток мозга, по меньшей мере, двумя способами: разложением пероксида водорода до воды и утилизацией свободных гидроксильных радикалов.
Доказанные биологические эффекты мелатонина многообразны: снотворный, гипотермический, антиоксидантный, противоопухолевый, адаптогенный, синхронизационный, антистрессовый, антидепрессантный, иммуномодулирующий, противосудорожный.
В целом, без отклонений в работе эпифиза (а следовательно, и в первую очередь патологии продукции М) не обходится ни одна человеческая патология. Это определяется следующими факторами:
• по мере старения организма эпифиз подвергается инволюции;
• с возрастом прогрессивно падает продукция М: уплощается, деформируется суточная кривая его плазменной концентрации;
• инволюция эпифиза и снижение синтеза мелатонина идут рука об руку со многими видами возрастной патологии;
• показана прямая зависимость от дефицита М ряда болезней нервной системы (инсомния, депрессия, невроз) и органических поражений мозга (болезнь Альцгеймера, болезнь Паркинсона и т.д.);
• эпифизарная недостаточность облегчает развитие онкологических заболеваний, иммунодефицитных состояний, ряда заболеваний внутренних органов (гипертонической болезни, ИБС, язвенной болезни желудка и двенадцатиперстной кишки и т.д.) и гинекологической патологии (дисменорея).
Исходя из вышеперечисленных биологических эффектов М следует предположить его важную роль в терапии многих неврологических заболеваний, и в первую очередь – в сосудистых нарушениях головного мозга.
Одним из важнейших звеньев патогенеза инсульта является «ишемический каскад», включающий эксайтотоксичность и оксидантный стресс. Кроме того, нарушения цикла «сон–бодрствование» встречается в 100% случаев в острейшем периоде инсульта. Они состоят из инсомнии, гиперсомнии, расстройств дыхания во сне (и прежде всего синдрома обструктивных апноэ во сне и синдрома гиповентиляции) и инверсии цикла «сон–бодрствование» (дневной сон и отсутствие ночного сна). С этих позиций М представляется очень важным препаратом, влияющим на многие звенья патогенеза инсульта, особенно с учетом отсутствия его негативного влияния на синдром «апноэ во сне».
Нами [А.М. Вейн, Я.И. Левин, Р.Л. Гасанов, 2000] проведено изучение действия ежевечернего орального приема Мелаксена (содержит 3 мг мелатонина) в течение 10 дней на субъективную оценку качества ночного сна и его объективные характеристики у 15 больных в острейшем периоде ишемического инсульта; их показатели сравнивались с таковыми у 15 здоровых добровольцев (контроль), соответственно подобранных по полу и возрасту. Все исследуемые были подвергнуты клинико–неврологическому обследованию. Для объективизации динамики восстановления применяли также Скандинавскую шкалу инсульта (СШИ). С помощью анкетных методов подробно уточняли сомнологический анамнез, субъективную оценку сна, уровень депрессии (опросник Бэк), личностной и реактивной тревоги (шкала Спилбергера). Полисомнографическое обследование до и после 10–дневного приема препарата проводилось с помощью компьютерного комплекса «Sleep Surfing» c регистрацией ЭЭГ, ЭОГ, ЭМГ. Анализ структуры сна проводился с помощью программы Центра сомнологических исследований, где, кроме стандартных параметров, изучается сегментарная структура сна.
Мозговой инсульт, как правило, приводит к грубым расстройствам ночного сна. Эти расстройства проявляются изменениями как его структуры, так и циркадных характеристик. Если в первом случае имеют место качественные изменения, проявляющиеся серьезными нарушениями механизмов генерации и поддержании сна, то во втором – либо сон становится полифазным, либо происходит его инверсия (смещение цикла «бодрствование–сон»). Действительно, у всех больных регистрировались расстройства сна различной степени выраженности. Исследования показали, что в результате приема мелатонина у больных отмечались: достоверное уменьшение длительности засыпания (с 35 до 21 минуты), представленности первой стадии – дремоты (с 12 до 8%), количества сегментов (с 89 до 66), увеличение времени второй стадии (с 32 до 44%). Индекс качества сна (интегративный показатель, чем он ниже, тем лучше структура сна) снижался с 29 до 24. Однако на фоне улучшения этих показателей сна имело место некоторое снижение длительности парадоксального сна (с 17 до 13%), при этом длительность глубокого медленного сна («дельта–сна») изменялась незначительно (с 18 до 20%). Особенностью мелатонина являлось также то, что при инверсии сна (3 пациентов) он восстанавливал нарушенный биоритм «сон–бодрствование». Отмечалось также достоверное снижение уровня депрессии. Личностная и реактивная тревожность оставались без динамики. В неврологической картине динамики не наблюдалось, что, по–видимому, связано с недостаточностью этого срока для выявления положительных сдвигов. Сделан вывод, что мелаксен оказывает положительное влияние на качество сна при его нарушениях, вызванных мозговым инсультом.
Подтверждением причинно–следственных отношений между естественной выработкой М и ухудшением мозгового кровообращения могут служить и пока еще немногочисленные результаты исследований на людях. В частности, показано, что у больных ишемическим инсультом резко дезорганизована нормальная секреторная активность эпифиза. По сравнению со здоровыми субъектами такие лица обнаруживают отсутствие ночного подъема плазменной концентрации М, что совпадает с нарушением нормального соотношения кортизол/М и дефектами в иммунном статусе, а также поведенческими расстройствами.
Но не только улучшение цикла «сон–бодрствование» делает мелатонин интересным для применения у больных инсультом. Целый ряд исследований (как экспериментальных, так и клинических) выявляет важнейшие свойства мелатонина для лечений этих пациентов:
1) мелатонин увеличивает церебральную реперфузию у крыс с экспериментальной артериальной окклюзией;
2) мелатонин уменьшает мозговой отек у крыс с экспериментальным инсультом;
3) мелатонин повышает нейропластичность в условиях стресса, вызванного экспериментальным инсультом;
4) при врожденной гипоплазии эпифиза повышается риск мозгового инсульта и инфаркта миокарда;
5) изменение иммунного статуса при инсульте, возможно связано с нарушенной ночной секрецией мелатонина;
6) мелатонин повышает нейропластичность у пожилых.
Таким образом, с учетом вышеописанного многообразия биологических эффектов мелатонина представляется, что далеко не все его возможности активно используются в современной медицине и его перспективы достаточно радужны. Несомненно, что особенности применения мелатонина в острейшем периоде церебрального инсульта, а также при хронической церебральной сосудистой патологии требуют проведения дальнейших исследований.