–Ь–µ–і–Є–Ї–Њ–—Б–Њ—Ж–Є–∞–ї—М–љ–∞—П –Ј–љ–∞—З–Є–Љ–Њ—Б—В—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–µ –≤—Л–Ј—Л–≤–∞–µ—В –љ–Є–Ї–∞–Ї–Є—Е —Б–Њ–Љ–љ–µ–љ–Є–є. –Э–∞—А—Г—И–µ–љ–Є—П –њ–∞–Љ—П—В–Є –Є –і—А—Г–≥–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–љ–Є–ґ–∞—О—В –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –љ–µ–≥–∞—В–Є–≤–љ–Њ –≤–ї–Є—П—О—В –љ–∞ –њ—А–Њ—Д–µ—Б—Б–Є–Њ–љ–∞–ї—М–љ—Г—О –і–µ—П—В–µ–ї—М–љ–Њ—Б—В—М, —Б–љ–Є–ґ–∞—О—В —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –Ї –Њ–±—Г—З–µ–љ–Є—О, –њ—А–Є–Њ–±—А–µ—В–µ–љ–Є—О –љ–Њ–≤—Л—Е –Ј–љ–∞–љ–Є–є –Є –љ–∞–≤—Л–Ї–Њ–≤, –≤—Л–Ј—Л–≤–∞—О—В —А–µ–∞–Ї—В–Є–≤–љ—Л–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞. –Т—Л—А–∞–ґ–µ–љ–љ—Л–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П (–Ъ–Э) –Њ–Ї–∞–Ј—Л–≤–∞—О—В –Њ—В—А–Є—Ж–∞—В–µ–ї—М–љ–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ —В–∞–Ї–ґ–µ –љ–∞ –Ї–∞—З–µ—Б—В–≤–Њ –ґ–Є–Ј–љ–Є —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤, –љ–µ—А–µ–і–Ї–Њ –≤—Л–љ—Г–ґ–і–∞—П –Є—Е –Љ–µ–љ—П—В—М –њ—А–Є–≤—Л—З–љ—Л–є —Г–Ї–ї–∞–і –ґ–Є–Ј–љ–Є, –≤ —А—П–і–µ —Б–ї—Г—З–∞–µ–≤ –њ—А–µ–Ї—А–∞—Й–∞—В—М –Є–ї–Є —Г–Љ–µ–љ—М—И–∞—В—М –њ—А–Њ—Д–µ—Б—Б–Є–Њ–љ–∞–ї—М–љ—Г—О –і–µ—П—В–µ–ї—М–љ–Њ—Б—В—М. –Т–µ—Б—М–Љ–∞ –Њ—Й—Г—В–Є–Љ—Л —Н–Ї–Њ–љ–Њ–Љ–Є—З–µ—Б–Ї–Є–µ –њ–Њ—В–µ—А–Є –Њ–±—Й–µ—Б—В–≤–∞, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –Њ–±—Б—Г–ґ–і–∞–µ–Љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є, –Ї–Њ—В–Њ—А—Л–µ –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–Њ–Ј—А–∞—Б—В–∞—О—В –њ—А–Є –њ–µ—А–µ—Е–Њ–і–µ –љ–∞ —Б—В–∞–і–Є—О —Г–Љ–µ—А–µ–љ–љ–Њ–є –Є —В—П–ґ–µ–ї–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є [9].
–°–ї–µ–і—Г–µ—В –њ—А–Є–Ј–љ–∞—В—М, —З—В–Њ –њ—А–Њ–±–ї–µ–Љ–∞ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Є –ї–µ—З–µ–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –њ–Њ–Ї–∞ –µ—Й–µ –≤–µ—Б—М–Љ–∞ –і–∞–ї–µ–Ї–∞ –Њ—В —Б–≤–Њ–µ–≥–Њ —А–∞–Ј—А–µ—И–µ–љ–Є—П. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ –≤ –Ї–Њ–љ—Ж–µ –•–•––љ–∞—З–∞–ї–µ –•–•I –≤–µ–Ї–∞ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –љ–Њ–≤—Л–µ –љ–∞—Г—З–љ—Л–µ –Ј–љ–∞–љ–Є—П –Њ –њ–∞—В–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є–Є –Є –љ–µ–є—А–Њ—Е–Є–Љ–Є–Є –Њ—Б–љ–Њ–≤–љ—Л—Е –і–µ–Љ–µ–љ—В–Є—А—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —З—В–Њ –њ–Њ–Ј–≤–Њ–ї–Є–ї–Њ –Њ–њ—В–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л. –Э–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –і–µ–Љ–µ–љ—Ж–Є–Є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ —Б—З–Є—В–∞–µ—В—Б—П –њ–Њ–ї–љ–Њ—Б—В—М—О –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є. –Р–Ї—В–Є–≤–љ–Њ —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –њ–Њ–і—Е–Њ–і—Л –Ї —А–∞–Ј—А–∞–±–Њ—В–Ї–µ –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –С–Р –Є –і—А—Г–≥–Є—Е —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є —Б –Ї–∞—А—В–Є–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є. –Э–∞–Ї–Њ–њ–ї–µ–љ–љ—Л–µ –Ї –љ–∞—Б—В–Њ—П—Й–µ–Љ—Г –≤—А–µ–Љ–µ–љ–Є —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –Њ–њ—А–µ–і–µ–ї–Є—В—М –Њ–њ—В–Є–Љ–∞–ї—М–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –њ–µ—А–≤–Є—З–љ–Њ–є –Є –≤—В–Њ—А–Є—З–љ–Њ–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є: –Ї–Њ—А—А–µ–Ї—Ж–Є—П –Є–Ј–≤–µ—Б—В–љ—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ —А–Є—Б–Ї–∞ –љ–∞—А—Г—И–µ–љ–Є–є –њ–∞–Љ—П—В–Є –Є –≤–љ–Є–Љ–∞–љ–Є—П –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ [1,2,11,24,26,30].
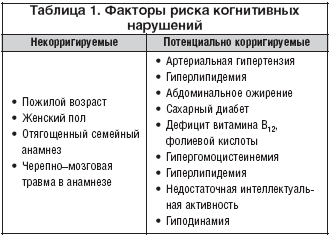
–§–∞–Ї—В–Њ—А—Л —А–Є—Б–Ї–∞
–Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є
–Э–∞–Є–±–Њ–ї–µ–µ —Б–Є–ї—М–љ—Л–Љ –Є –љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —П–≤–ї—П–µ—В—Б—П –њ–Њ–ґ–Є–ї–Њ–є –Є —Б—В–∞—А—З–µ—Б–Ї–Є–є –≤–Њ–Ј—А–∞—Б—В. –° –≤–Њ–Ј—А–∞—Б—В–Њ–Љ –≥–Њ–ї–Њ–≤–љ–Њ–є –Љ–Њ–Ј–≥ –њ—А–µ—В–µ—А–њ–µ–≤–∞–µ—В —А—П–і –Ј–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–µ –і–µ–ї–∞—О—В –µ–≥–Њ –±–Њ–ї–µ–µ —Г—П–Ј–≤–Є–Љ—Л–Љ –њ–Њ –Њ—В–љ–Њ—И–µ–љ–Є—О –Ї —А–∞–Ј–ї–Є—З–љ—Л–Љ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П–Љ. –Ґ–∞–Ї, —Б –≤–Њ–Ј—А–∞—Б—В–Њ–Љ —Г–Љ–µ–љ—М—И–∞—О—В—Б—П –Љ–∞—Б—Б–∞ –Љ–Њ–Ј–≥–∞, —З–Є—Б–ї–Њ —Б–Є–љ–∞–њ—Б–Њ–≤, –Є–Ј–Љ–µ–љ—П–µ—В—Б—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –і–Њ—Д–∞–Љ–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є, –љ–Њ—А–∞–і—А–µ–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є, –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є –Є –і—А—Г–≥–Є—Е –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ. –≠—В–Є –Є–љ–≤–Њ–ї—О—В–Є–≤–љ—Л–µ –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –Ї–Њ–љ–µ—З–љ–Њ–Љ –Є—В–Њ–≥–µ —Г–Љ–µ–љ—М—И–∞—О—В –љ–µ–є—А–Њ–љ–∞–ї—М–љ—Г—О –њ–ї–∞—Б—В–Є—З–љ–Њ—Б—В—М. –Я–Њ–і –њ–Њ—Б–ї–µ–і–љ–Є–Љ —В–µ—А–Љ–Є–љ–Њ–Љ –њ—А–Є–љ—П—В–Њ –њ–Њ–љ–Є–Љ–∞—В—М —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –љ–µ–є—А–Њ–љ–Њ–≤ –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—О —Д—Г–љ–Ї—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е —Б–≤–Њ–є—Б—В–≤ –≤ –Њ—В–≤–µ—В –љ–∞ –≤–љ–µ—И–љ–Є–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є—П. –£–Љ–µ–љ—М—И–µ–љ–Є–µ –љ–µ–є—А–Њ–љ–∞–ї—М–љ–Њ–є –њ–ї–∞—Б—В–Є—З–љ–Њ—Б—В–Є –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–љ–Є–ґ–µ–љ–Є—О –Ї–Њ–Љ–њ–µ–љ—Б–∞—В–Њ—А–љ—Л—Е –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–Њ–≥–Њ «—Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ —А–µ–Ј–µ—А–≤–∞») [1,2,8,10,11].
–Ф—А—Г–≥–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –Ї–Њ—В–Њ—А—Л–є, –Ї–∞–Ї –Є –≤–Њ–Ј—А–∞—Б—В, –љ–µ –њ–Њ–і–і–∞–µ—В—Б—П –Ї–Њ—А—А–µ–Ї—Ж–Є–Є, —П–≤–ї—П–µ—В—Б—П –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–∞—П –Њ—В—П–≥–Њ—Й–µ–љ–љ–Њ—Б—В—М. –°–∞–Љ–∞—П —З–∞—Б—В–∞—П –њ—А–Є—З–Є–љ–∞ –і–µ–Љ–µ–љ—Ж–Є–Є – –С–Р – —П–≤–ї—П–µ—В—Б—П –≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Є –і–µ—В–µ—А–Љ–Є–љ–Є—А–Њ–≤–∞–љ–љ—Л–Љ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ–Љ. –Ю—Б–Њ–±–µ–љ–љ–Њ –≤–µ–ї–Є–Ї —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –С–Р –њ—А–Є –љ–∞–ї–Є—З–Є–Є –±–ї–Є–ґ–∞–є—И–Є—Е —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤, –Ј–∞–±–Њ–ї–µ–≤—И–Є—Е –і–Њ 60 –ї–µ—В (–њ—А–µ—Б–µ–љ–Є–ї—М–љ–∞—П —Д–Њ—А–Љ–∞). –С–Р —Б–Њ —Б—В–Њ–ї—М —А–∞–љ–љ–Є–Љ –љ–∞—З–∞–ї–Њ–Љ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –∞—Г—В–Њ—Б–Њ–Љ–љ–Њ––і–Њ–Љ–Є–љ–∞–љ—В–љ—Л–Љ —В–Є–њ–Њ–Љ –њ–µ—А–µ–і–∞—З–Є –Є –≤—Л—Б–Њ–Ї–Њ–є –њ–µ–љ–µ—В—А–∞–љ—В–љ–Њ—Б—В—М—О –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –≥–µ–љ–Њ–≤. –С–Р —Б –љ–∞—З–∞–ї–Њ–Љ –њ–Њ—Б–ї–µ 60 –ї–µ—В –Њ–±—Л—З–љ–Њ —П–≤–ї—П–µ—В—Б—П —Б–њ–Њ—А–∞–і–Є—З–µ—Б–Ї–Њ–є. –Ґ–µ–Љ –љ–µ –Љ–µ–љ–µ–µ —А–Є—Б–Ї –Ј–∞–±–Њ–ї–µ—В—М —Г –±–ї–Є–ґ–∞–є—И–Є—Е —А–Њ–і—Б—В–≤–µ–љ–љ–Є–Ї–Њ–≤ —В–∞–Ї–Є—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –≤—Л—И–µ —Б—А–µ–і–љ–µ—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Њ–≥–Њ [1,2,11].
–Т–∞–ґ–љ–µ–є—И–Є–Љ —Д–∞–Ї—В–Њ—А–Њ–Љ —А–Є—Б–Ї–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —П–≤–ї—П—О—В—Б—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В–Њ–є —Б–Є—Б—В–µ–Љ—Л, –≤ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П. –Я–Њ –і–∞–љ–љ—Л–Љ –Ї—А—Г–њ–љ—Л—Е –њ–Њ–њ—Г–ї—П—Ж–Є–Њ–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–Њ–≤–µ–і–µ–љ–љ—Л—Е –≤ —А–∞–Ј–љ—Л—Е —А–µ–≥–Є–Њ–љ–∞—Е –Љ–Є—А–∞ –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –і—А—Г–≥ –Њ—В –і—А—Г–≥–∞, –±—Л–ї —Б–і–µ–ї–∞–љ —Б–Њ–≥–ї–∞—Б–Њ–≤–∞–љ–љ—Л–є –≤—Л–≤–Њ–і, —З—В–Њ –љ–∞–ї–Є—З–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є –≤ —Б—А–µ–і–љ–µ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –∞—Б—Б–Њ—Ж–Є–Є—А–Њ–≤–∞–љ–Њ —Б –њ–Њ–≤—Л—И–µ–љ–љ—Л–Љ —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –љ–∞—А—Г—И–µ–љ–Є–є –њ–∞–Љ—П—В–Є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –Є —Б—В–∞—А—З–µ—Б–Ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ. –Я—А–Є—З–µ–Љ, —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П —Б–≤—П–Ј—М –Є–Љ–µ–µ—В—Б—П –љ–µ —В–Њ–ї—М–Ї–Њ —Б —Б–Њ—Б—Г–і–Є—Б—В—Л–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –љ–Њ –Є —Б —А–Є—Б–Ї–Њ–Љ —А–∞–Ј–≤–Є—В–Є—П –С–Р. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л, –њ–Њ –Ї–Њ—В–Њ—А—Л–Љ –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П –њ—А–Њ–≤–Њ—Ж–Є—А—Г–µ—В –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є–µ –Є–ї–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї—Г—О –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є—О –С–Р, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Г—В–Њ—З–љ—П—О—В—Б—П. –Т–µ—А–Њ—П—В–љ–µ–µ –≤—Б–µ–≥–Њ, —А–µ—И–∞—О—Й–µ–µ –Ј–љ–∞—З–µ–љ–Є–µ –Є–Љ–µ–µ—В –і–µ–Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є—П —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –њ—А–Њ—В–µ–Ї–∞—О—Й–µ–≥–Њ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –ї–∞–Ї—Г–љ–∞—А–љ—Л—Е –Є–љ—Д–∞—А–Ї—В–Њ–≤ –Є/–Є–ї–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –ї–µ–є–Ї–Њ–∞—А–µ–Њ–Ј–∞ [7,15,43,46].
–Э–µ–і–∞–≤–љ–Њ –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–∞—Е–∞—А–љ—Л–є –і–Є–∞–±–µ—В 2 —В–Є–њ–∞ —В–∞–Ї–ґ–µ –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞–µ—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Я–Њ –і–∞–љ–љ—Л–Љ –†–Њ—В—В–µ—А–і–∞–Љ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –і–µ–Љ–µ–љ—Ж–Є–Є, –Є –Ї–Њ–љ–Ї—А–µ—В–љ–Њ –С–Р, –њ—А–Є–±–ї–Є–Ј–Є—В–µ–ї—М–љ–Њ –≤ 2 —А–∞–Ј–∞ –≤—Л—И–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2 —В–Є–њ–∞ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –Є—Е —Б–≤–µ—А—Б—В–љ–Є–Ї–∞–Љ–Є. –Я—А–Є —Н—В–Њ–Љ –њ–∞—Ж–Є–µ–љ—В—Л, –њ–Њ–ї—Г—З–∞—О—Й–Є–µ –Є–љ—Б—Г–ї–Є–љ, –Є–Љ–µ—О—В –љ–∞–Є–±–Њ–ї—М—И–Є–є —А–Є—Б–Ї, –Ї–Њ—В–Њ—А—Л–є –њ—А–µ–≤—Л—И–∞–µ—В —Б—А–µ–і–љ–µ—Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є–є –±–Њ–ї–µ–µ —З–µ–Љ –≤ 4 —А–∞–Ј–∞. –°—Е–Њ–і–љ—Л–µ –і–∞–љ–љ—Л–µ –±—Л–ї–Є –њ–Њ–ї—Г—З–µ–љ—Л –≤ —Е–Њ–і–µ –Ъ–∞–љ–∞–і—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –Ј–і–Њ—А–Њ–≤—М—П –њ–Њ–ґ–Є–ї—Л—Е (Canadian study of health and aging). –Я–Њ –і–∞–љ–љ—Л–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П LADIS (–µ–≤—А–Њ–њ–µ–є—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј–Є –ї–µ–є–Ї–Њ–∞—А–µ–Њ–Ј–∞ –Є –Є–љ–≤–∞–ї–Є–і–љ–Њ—Б—В–Є – leucoaraiosis and disability study), –Є–Љ–µ–µ—В—Б—П —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–∞—П —Б–≤—П–Ј—М –Љ–µ–ґ–і—Г —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ –Є —Е–∞—А–∞–Ї—В–µ—А–љ—Л–Љ –Љ–∞—А–Ї–µ—А–Њ–Љ –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ – –∞—В—А–Њ—Д–Є–µ–є –Љ–µ–і–Є–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –≤–Є—Б–Њ—З–љ—Л—Е –і–Њ–ї–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [5,6,25,34].
–У–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є—П –Є –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–µ –Њ–ґ–Є—А–µ–љ–Є–µ –≤ —Б—А–µ–і–љ–µ–Љ –≤–Њ–Ј—А–∞—Б—В–µ —В–∞–Ї–ґ–µ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –њ–Њ –Љ–µ—А–µ —Б—В–∞—А–µ–љ–Є—П. –Ч–∞–Ї–Њ–љ–Њ–Љ–µ—А–љ–Њ, —З—В–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ—Л–є —А–Є—Б–Ї –Њ—В–Љ–µ—З–∞–µ—В—Б—П –њ—А–Є —Б–Њ—З–µ—В–∞–љ–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–Є, –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є–Є, –∞–±–і–Њ–Љ–Є–љ–∞–ї—М–љ–Њ–≥–Њ –Њ–ґ–Є—А–µ–љ–Є—П –Є —Б–∞—Е–∞—А–љ–Њ–≥–Њ –і–Є–∞–±–µ—В–∞ 2 —В–Є–њ–∞, —З—В–Њ –љ–µ—А–µ–і–Ї–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–Љ «–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–Љ —Б–Є–љ–і—А–Њ–Љ–Њ–Љ [11,15,34].
–Ъ –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ —Д–∞–Ї—В–Њ—А–∞–Љ —А–Є—Б–Ї–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В–љ–Њ—Б—П—В—Б—П —В–∞–Ї–ґ–µ —З–µ—А–µ–њ–љ–Њ––Љ–Њ–Ј–≥–Њ–≤–∞—П —В—А–∞–≤–Љ–∞ –Є —Н–њ–Є–Ј–Њ–і—Л –і–µ–њ—А–µ—Б—Б–Є–Є –≤ –∞–љ–∞–Љ–љ–µ–Ј–µ, –ґ–µ–љ—Б–Ї–Є–є –њ–Њ–ї, –і–µ—Д–Є—Ж–Є—В –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –≥—А—Г–њ–њ—Л –Т –Є —Д–Њ–ї–Є–µ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л, –љ–Є–Ј–Ї–∞—П –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ–∞—П –Є —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –Љ–Њ–ї–Њ–і—Л–µ –Є —Б—А–µ–і–љ–Є–µ –≥–Њ–і—Л –ґ–Є–Ј–љ–Є (—В–∞–±–ї. 1) [1,2,11,30].
–Э–µ–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–µ –Љ–µ—В–Њ–і—Л
–њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е
–љ–∞—А—Г—И–µ–љ–Є–є
–Ъ –љ–µ–Љ–µ–і–Є–Ї–∞–Љ–µ–љ—В–Њ–Ј–љ—Л–Љ –Љ–µ—В–Њ–і–∞–Љ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Њ—В–љ–Њ—Б—П—В—Б—П –і–Є–µ—В–∞, –Њ–±–Њ–≥–∞—Й–µ–љ–љ–∞—П –њ—А–Є—А–Њ–і–љ—Л–Љ–Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–∞–Љ–Є, —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П —В—А–µ–љ–Є—А–Њ–≤–Ї–∞ –њ–∞–Љ—П—В–Є –Є –≤–љ–Є–Љ–∞–љ–Є—П –Є —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П.
–Я—А–Є—А–Њ–і–љ—Л–Љ–Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –≤–Є—В–∞–Љ–Є–љ—Л –° –Є –Х, –Ї–Њ—В–Њ—А—Л–µ —Б–Њ–і–µ—А–ґ–∞—В—Б—П –≤ —Ж–Є—В—А—Г—Б–Њ–≤—Л—Е, —А–∞—Б—В–Є—В–µ–ї—М–љ—Л—Е –Љ–∞—Б–ї–∞—Е, –Љ–Њ—А–µ–њ—А–Њ–і—Г–Ї—В–∞—Е –Є –і—А—Г–≥–Є—Е –њ—А–Њ–і—Г–Ї—В–∞—Е –њ–Є—В–∞–љ–Є—П. –Я–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–Љ —А–µ—В—А–Њ—Б–њ–µ–Ї—В–Є–≤–љ—Л–Љ –љ–∞–±–ї—О–і–µ–љ–Є—П–Љ, —В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ–∞—П «—Б—А–µ–і–Є–Ј–µ–Љ–љ–Њ–Љ–Њ—А—Б–Ї–∞—П –і–Є–µ—В–∞», –Њ–±–Њ–≥–∞—Й–µ–љ–љ–∞—П –љ–∞—В—Г—А–∞–ї—М–љ—Л–Љ–Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–∞–Љ–Є, —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ъ–Э –Є –і–µ–Љ–µ–љ—Ж–Є–Є. –° —Н—В–Њ–є —Ж–µ–ї—М—О —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –≤ —А–∞—Ж–Є–Њ–љ–µ –±–Њ–ї—М—И–µ –Њ–≤–Њ—Й–µ–є, —Д—А—Г–Ї—В–Њ–≤ –Є –Љ–Њ—А–µ–њ—А–Њ–і—Г–Ї—В–Њ–≤ [40,47].
–≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В, —З—В–Њ –ї–Є—Ж–∞ –љ–∞–њ—А—П–ґ–µ–љ–љ–Њ–≥–Њ –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ–Њ–≥–Њ —В—А—Г–і–∞ –Љ–µ–љ–µ–µ –њ–Њ–і–≤–µ—А–ґ–µ–љ—Л –Ъ–Э –Є –і–µ–Љ–µ–љ—Ж–Є–Є. –Я–∞—Ж–Є–µ–љ—В—Л –≤—Л—Б–Њ–Ї–Њ–≥–Њ –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ–Њ–≥–Њ —Г—А–Њ–≤–љ—П –Њ–±–ї–∞–і–∞—О—В –±–Њ–ї–µ–µ —А–∞–Ј–≤–Є—В—Л–Љ–Є –љ–∞–≤—Л–Ї–∞–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є, –Ї–Њ—В–Њ—А—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В –Є–Љ —Г—Б–њ–µ—И–љ–µ–µ –њ—А–µ–Њ–і–Њ–ї–µ–≤–∞—В—М —В—А—Г–і–љ–Њ—Б—В–Є, –њ–Њ—П–≤–ї—П—О—Й–Є–µ—Б—П –≤ –љ–∞—З–∞–ї–µ –і–µ–Љ–µ–љ—В–Є—А—Г—О—Й–µ–≥–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤—Л—Б–Њ–Ї–Є–є –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ—Л–є —Г—А–Њ–≤–µ–љ—М –≤ –њ—А–µ–Љ–Њ—А–±–Є–і–µ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–µ—В –±–Њ–ї—М—И—Г—О –Є–ї–Є –Љ–µ–љ—М—И—Г—О –Њ—В—Б—А–Њ—З–Ї—Г –≤—А–µ–Љ–µ–љ–Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Љ–∞–љ–Є—Д–µ—Б—В–∞—Ж–Є–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П [14,31,48].
–Ъ–∞–Ї –Ј–і–Њ—А–Њ–≤—Л–Љ –њ–Њ–ґ–Є–ї—Л–Љ, —В–∞–Ї –Є –ї–Є—Ж–∞–Љ —Б –љ–µ–≥—А—Г–±—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –њ–Њ–Ї–∞–Ј–∞–љ—Л —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П –њ–Њ —В—А–µ–љ–Є—А–Њ–≤–Ї–µ –њ–∞–Љ—П—В–Є –Є –≤–љ–Є–Љ–∞–љ–Є—П. –¶–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ—Б—В—М —В–∞–Ї–Є—Е —Г–њ—А–∞–ґ–љ–µ–љ–Є–є –±–∞–Ј–Є—А—Г–µ—В—Б—П –љ–∞ –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ–Є–Є –Њ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є—П—Е –Ї–∞–Ї –Њ –Ј–∞–њ–∞—Б–µ –Ј–љ–∞–љ–Є–є –Є –љ–∞–≤—Л–Ї–Њ–≤, –Ї–Њ—В–Њ—А—Л–µ —Д–Њ—А–Љ–Є—А—Г—О—В—Б—П –њ—А–Є–ґ–Є–Ј–љ–µ–љ–љ–Њ. –Ф—А—Г–≥–Є–Љ–Є —Б–ї–Њ–≤–∞–Љ–Є, —З–µ–ї–Њ–≤–µ–Ї –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –ґ–Є–Ј–љ–µ–і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Њ–±—Г—З–∞–µ—В—Б—П —Б—В—А–∞—В–µ–≥–Є—П–Љ –Є –љ–∞–≤—Л–Ї–∞–Љ –≤–Њ—Б–њ—А–Є—П—В–Є—П, –Њ–±—А–∞–±–Њ—В–Ї–Є, –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є—П –Є –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є. –І–µ–ї–Њ–≤–µ—З–µ—Б–Ї–∞—П –њ–∞–Љ—П—В—М –љ–µ —П–≤–ї—П–µ—В—Б—П –њ—А–Њ—Б—В—Л–Љ «—Е—А–∞–љ–Є–ї–Є—Й–µ–Љ», –Ї—Г–і–∞ —Б–Ї–ї–∞–і—Л–≤–∞–µ—В—Б—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П, –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–љ–µ—Б—В–Є—З–µ—Б–Ї–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Ј–∞–≤–Є—Б–Є—В –љ–µ –Њ—В –Њ–±—К–µ–Љ–∞ –њ–∞–Љ—П—В–Є, –Ї–Њ—В–Њ—А—Л–є –±–µ–Ј–≥—А–∞–љ–Є—З–µ–љ –Є –Љ–∞–ї–Њ –Љ–µ–љ—П–µ—В—Б—П –і–∞–ґ–µ –њ—А–Є —В—П–ґ–µ–ї—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е –Љ–Њ–Ј–≥–∞, –∞ –Њ—В –Є—Б–њ–Њ–ї—М–Ј—Г–µ–Љ—Л—Е —Б—В—А–∞—В–µ–≥–Є–є –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є—П –Є –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—П [3,11,30].
–Я—А–Њ–≥—А–∞–Љ–Љ—Л —В—А–µ–љ–Є—А–Њ–≤–Ї–Є –њ–∞–Љ—П—В–Є –≤–Ї–ї—О—З–∞—О—В –њ–Њ–≤—Л—И–µ–љ–Є–µ –Љ–Њ—В–Є–≤–∞—Ж–Є–Є –њ–∞—Ж–Є–µ–љ—В–∞ –Ї –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є—О –Є –≤–Њ—Б–њ—А–Њ–Є–Ј–≤–µ–і–µ–љ–Є—О, –Њ–±—Г—З–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–Љ —Б—В—А–∞—В–µ–≥–Є—П–Љ –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є—П (—В–∞–Ї –љ–∞–Ј—Л–≤–∞–µ–Љ—Л–Љ «–Љ–љ–µ–Љ–Њ–љ–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є–µ–Љ–∞–Љ»), —А–∞–Ј–≤–Є—В–Є–µ —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є –і–ї–Є—В–µ–ї—М–љ–Њ –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—В—М –љ–∞–і–ї–µ–ґ–∞—Й–Є–є —Г—А–Њ–≤–µ–љ—М –≤–љ–Є–Љ–∞–љ–Є—П, –∞–Ї—В–Є–≤–љ–Њ–µ –≤–Ї–ї—О—З–µ–љ–Є–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є –њ–Њ–і–і–µ—А–ґ–Ї–Є (–Ї–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ –Њ–Ї—А–∞—И–µ–љ–љ–∞—П –Є–љ—Д–Њ—А–Љ–∞—Ж–Є—П –Ј–∞–њ–Њ–Љ–Є–љ–∞–µ—В—Б—П –ї—Г—З—И–µ) –Є –≤–Њ–Њ–±—А–∞–ґ–µ–љ–Є—П. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є —В—А–µ–љ–Є—А–Њ–≤–Ї–Є –њ–∞–Љ—П—В–Є –Є –≤–љ–Є–Љ–∞–љ–Є—П –і–Њ–Ї–∞–Ј–∞–љ–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –ї–µ–≥–Ї–Њ–є –і–µ–Љ–µ–љ—Ж–Є–µ–є, –∞ —В–∞–Ї–ґ–µ –њ—А–Є –љ–µ–і–µ–Љ–µ–љ—В–љ—Л—Е (–ї–µ–≥–Ї–Є—Е –Є —Г–Љ–µ—А–µ–љ–љ—Л—Е) –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е [33,36,44].
–≠–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ –љ–∞–±–ї—О–і–µ–љ–Є—П —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В, —З—В–Њ —А–µ–≥—Г–ї—П—А–љ–∞—П —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П –∞–Ї—В–Є–≤–љ–Њ—Б—В—М —В–∞–Ї–ґ–µ —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В —Г–Љ–µ–љ—М—И–µ–љ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В–Є –і–µ–Љ–µ–љ—Ж–Є–µ–є. –Т —А—П–і–µ –∞–љ–∞–ї–Є—В–Є—З–µ—Б–Ї–Є—Е —А–∞–±–Њ—В –±—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –ї–Є—Ж–∞, —А–µ–≥—Г–ї—П—А–љ–Њ –≤—Л–њ–Њ–ї–љ—П—О—Й–Є–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Є–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П, –Є–Љ–µ—О—В –Љ–µ–љ—М—И–Є–є —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –і–µ–Љ–µ–љ—Ж–Є–Є –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ. –Т–µ—А–Њ—П—В–љ–Њ, –≤ –Њ—Б–љ–Њ–≤–µ –і–∞–љ–љ–Њ–≥–Њ —Д–µ–љ–Њ–Љ–µ–љ–∞ –ї–µ–ґ–Є—В –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ —Д–Є–Ј–Є—З–µ—Б–Ї–Є –∞–Ї—В–Є–≤–љ–Њ–≥–Њ –Њ–±—А–∞–Ј–∞ –ґ–Є–Ј–љ–Є –љ–∞ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Г—О —Б–Є—Б—В–µ–Љ—Г, –Є–љ–і–µ–Ї—Б –Љ–∞—Б—Б—Л —В–µ–ї–∞, —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Г—О —Б—Д–µ—А—Г [12,13,27,38].
–Ы–µ—З–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е
–Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–∞ –Ъ–Э
–Ъ–∞–Ї —Г–Ї–∞–Ј—Л–≤–∞–ї–Њ—Б—М –≤—Л—И–µ, –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П –Є –≥–Є–њ–µ—А–ї–Є–њ–Є–і–µ–Љ–Є—П —П–≤–ї—П—О—В—Б—П –і–Њ–Ї–∞–Ј–∞–љ–љ—Л–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —А–Є—Б–Ї–∞ –Ъ–Э, –њ—А–Є—З–µ–Љ –Ї–∞–Ї —Б–Њ—Б—Г–і–Є—Б—В–Њ–є, —В–∞–Ї –Є –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–є –њ—А–Є—А–Њ–і—Л. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ —И–Є—А–Њ–Ї–Њ –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П –≤ –ї–Є—В–µ—А–∞—В—Г—А–µ –≤–Њ–њ—А–Њ—Б, –Ї–∞–Ї–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–Є—Б–Ї —А–∞–Ј–≤–Є—В–Є—П –Ъ–Э –Њ–Ї–∞–Ј—Л–≤–∞–µ—В —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–∞—П –Є –∞–і–µ–Ї–≤–∞—В–љ–∞—П —В–µ—А–∞–њ–Є—П –і–∞–љ–љ—Л—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Њ—Б—В–Њ—П–љ–Є–є. –Т –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Ї—А—Г–њ–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е —А–∞–Ј–ї–Є—З–љ—Л—Е –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е —Б—А–µ–і—Б—В–≤ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М –і–µ–Љ–µ–љ—Ж–Є–µ–є –Є–ї–Є —В–µ–Љ–њ—Л –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –∞–љ–∞–ї–Є–Ј–Є—А–Њ–≤–∞–ї–Є—Б—М –≤ –Ї–∞—З–µ—Б—В–≤–µ –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –±–µ–Ј–Њ–њ–∞—Б–љ–Њ—Б—В–Є –Є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є (—В–∞–±–ї. 2). –Я—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –і–µ–Љ–µ–љ—Ж–Є–Є –±—Л–ї –њ–Њ–Ї–∞–Ј–∞–љ —Г –Ї–∞–ї—М—Ж–Є–µ–≤–Њ–≥–Њ –±–ї–Њ–Ї–∞—В–Њ—А–∞ –љ–Є—В—А–µ–љ–і–Є–њ–Є–љ–∞, –±–ї–Њ–Ї–∞—В–Њ—А–∞ —А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї –∞–љ–≥–Є–Њ—В–µ–љ–Ј–Є–љ—Г II —В–Є–њ–∞ —Н–њ—А–Њ—Б–∞—А—В–∞–љ–∞ –Є –њ—А–Є –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–Є –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є –њ–µ—А–Є–љ–і–Њ–њ—А–Є–ї–∞ –Є –Є–љ–і–∞–њ–∞–Љ–Є–і–∞. –Ф—А—Г–≥–Є–µ –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞–ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ –љ–∞ –Ј–∞–±–Њ–ї–µ–≤–∞–µ–Љ–Њ—Б—В—М –і–µ–Љ–µ–љ—Ж–Є–µ–є –Є–ї–Є —В–µ–Љ–њ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є [17,29,35,39,41,43,49].
–°–ї–µ–і—Г–µ—В –Њ–≥–Њ–≤–Њ—А–Є—В—М—Б—П, —З—В–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –∞–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Љ–Њ–ґ–µ—В –Њ–±—Б—Г–ґ–і–∞—В—М—Б—П –ї–Є—И—М –≤ —В–Њ–Љ —Б–ї—Г—З–∞–µ, –µ—Б–ї–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Њ–≤–Њ–і–Є–Љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–µ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є—П —Б—Г—В–Њ—З–љ–Њ–є –≤–∞—А–Є–∞–±–µ–ї—М–љ–Њ—Б—В–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П. –Ч–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –Ї–Њ–ї–µ–±–∞–љ–Є—П –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ —Б—Г—В–Њ–Ї, —Б–≤—П–Ј–∞–љ–љ—Л–µ —Б –љ–µ—А–µ–≥—Г–ї—П—А–љ—Л–Љ –Є–ї–Є –љ–µ–њ—А–∞–≤–Є–ї—М–љ—Л–Љ –њ—А–Є–µ–Љ–Њ–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Є–ї–Є —Б –Њ—А—В–Њ—Б—В–∞–Ј–Њ–Љ, –Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ —Г–≤–µ–ї–Є—З–Є–≤–∞—О—В —А–Є—Б–Ї –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –≤–∞–ґ–љ–Њ –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П —Б–ї–µ–і—Г–µ—В –і–Њ–±–Є–≤–∞—В—М—Б—П –њ–ї–∞–љ–Њ–Љ–µ—А–љ–Њ –Є –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ. –Ф–ї–Є—В–µ–ї—М–љ–∞—П –∞—А—В–µ—А–Є–∞–ї—М–љ–∞—П –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—П –≤–µ–і–µ—В –Ї –Є–Ј–Љ–µ–љ–µ–љ–Є—О —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е —Б–Њ—Б—Г–і–Њ–≤ –Є –љ–∞—А—Г—И–µ–љ–Є—О –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –∞—Г—В–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞. –Т —Н—В–Є—Е —Г—Б–ї–Њ–≤–Є—П—Е –±—Л—Б—В—А–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –њ—А–Є–≤—Л—З–љ—Л—Е –і–ї—П –±–Њ–ї—М–љ–Њ–≥–Њ —Ж–Є—Д—А –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –Љ–Њ–ґ–µ—В –њ—А–Є–≤–Њ–і–Є—В—М –Ї —Г—Б—Г–≥—Г–±–ї–µ–љ–Є—О —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –≥–Є–њ–Њ–њ–µ—А—Д—Г–Ј–Є–Є, –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Њ—Б—В—А—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Њ–Ј–≥–∞. –Ю—Б–Њ–±–µ–љ–љ–Њ –Њ–њ–∞—Б–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–µ –Є –±—Л—Б—В—А–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–≥–Њ –і–∞–≤–ї–µ–љ–Є—П –њ—А–Є –љ–∞–ї–Є—З–Є–Є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є –Ј–љ–∞—З–Є–Љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–Њ–ї–Њ–≤—Л [7,43].
–С–Њ–ї—М—И–Њ–є –Є–љ—В–µ—А–µ—Б –≤—Л–Ј—Л–≤–∞—О—В –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Б—В–∞—В–Є–љ–Њ–≤ –і–ї—П –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ. –Т –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –љ–∞–Ї–Њ–њ–ї–µ–љ–Є–µ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є–Љ–µ–µ—В –њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –љ–µ —В–Њ–ї—М–Ї–Њ –≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ –Ї—А—Г–њ–љ—Л—Е –∞—А—В–µ—А–Є–є, –љ–Њ –Є –≤ –њ—А–Њ—Ж–µ—Б—Б–µ –Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—П –≤ –њ–∞—А–µ–љ—Е–Є–Љ–µ –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —Б–µ–љ–Є–ї—М–љ—Л—Е –±–ї—П—И–µ–Ї, —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –і–ї—П –С–Р. –Ю–і–љ–∞–Ї–Њ —З–Є—Б–ї–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ—А–µ–і–њ–Њ–ї–∞–≥–∞–µ–Љ–Њ–≥–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ —Б—В–∞—В–Є–љ–Њ–≤ –≤ –Њ—В–љ–Њ—И–µ–љ–Є–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ъ–Э –љ–µ–≤–µ–ї–Є–Ї–Њ. –Ш—Е —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–∞ —Б–µ–≥–Њ–і–љ—П—И–љ–Є–є –і–µ–љ—М –љ–Њ—Б—П—В –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л–є —Е–∞—А–∞–Ї—В–µ—А [20,37,42].
–Т–∞–Ј–Њ–∞–Ї—В–Є–≤–љ–∞—П –Є –љ–µ–є—А–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –њ—А–µ–њ–∞—А–∞—В—Л, —Г–ї—Г—З—И–∞—О—Й–Є–µ —Ж–µ—А–µ–±—А–∞–ї—М–љ—Г—О –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—Ж–Є—О –Є –љ–µ–є—А–Њ–љ–∞–ї—М–љ—Л–є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ, —П–≤–ї—П—О—В—Б—П –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –љ–∞–Ј–љ–∞—З–∞–µ–Љ—Л–Љ–Є –≤ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –≤ –љ–∞—И–µ–є —Б—В—А–∞–љ–µ, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞. –Э–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –Њ—В–Љ–µ—З–∞–µ—В—Б—П —Г–ї—Г—З—И–µ–љ–Є–µ –њ–∞–Љ—П—В–Є, –≤–љ–Є–Љ–∞–љ–Є—П –Є –і—А—Г–≥–Є—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є, –Њ—Б–Њ–±–µ–љ–љ–Њ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–µ–є, —Г–ї—Г—З—И–µ–љ–Є–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –Є —Б–∞–Љ–Њ—З—Г–≤—Б—В–≤–Є—П [1–3,11]. –®–Є—А–Њ–Ї–Њ –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П –≤–µ—А–Њ—П—В–љ—Л–є –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л—Е –Є –љ–µ–є—А–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Ґ–∞–Ї, –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л–µ —Н–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –Є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±—Л–ї–Є –њ–Њ—Б–≤—П—Й–µ–љ—Л –Є–Ј—Г—З–µ–љ–Є—О –љ–µ–є—А–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ–Њ–≥–Њ —Н—Д—Д–µ–Ї—В–∞ EGB 761 (–Ь–µ–Љ–Њ–њ–ї–∞–љ—В) – —Н–Ї—Б—В—А–∞–Ї—В–∞ –ї–Є—Б—В—М–µ–≤ —А–µ–ї–Є–Ї—В–Њ–≤–Њ–≥–Њ –≥–Є–љ–Ї–≥–Њ –±–Є–ї–Њ–±—Л, —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –њ–Њ —Б–Њ–і–µ—А–ґ–∞–љ–Є—О –і–µ–є—Б—В–≤—Г—О—Й–Є—Е –≤–µ—Й–µ—Б—В–≤ (—Д–ї–∞–≤–Њ–љ–Њ–Є–і–љ—Л–µ –≥–ї–Є–Ї–Њ–Ј–Є–і—Л, –≥–Є–љ–Ї–≥–Њ–ї–Є–і—Л, –±–Є–ї–Њ–±–∞–ї–Є–і—Л). –Я–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –і–µ–є—Б—В–≤—Г—О—Й–Є–µ –≤–µ—Й–µ—Б—В–≤–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Ь–µ–Љ–Њ–њ–ї–∞–љ—В –љ–Њ—А–Љ–∞–ї–Є–Ј—Г—О—В —В–Њ–љ—Г—Б —Б–Њ—Б—Г–і–Њ–≤ –Љ–Є–Ї—А–Њ—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–≥–Њ —А—Г—Б–ї–∞, –≤ –±–Њ–ї—М—И–µ–є —Б—В–µ–њ–µ–љ–Є –≤–ї–Є—П—П –љ–∞ –њ–Њ—А–∞–ґ–µ–љ–љ—Л–µ –∞—А—В–µ—А–Є–Њ–ї—Л –Є –љ–µ –≤—Л–Ј—Л–≤–∞—П —Н—Д—Д–µ–Ї—В–∞ –Њ–±–Ї—А–∞–і—Л–≤–∞–љ–Є—П. –Ф—А—Г–≥–Є–µ –∞–Ї—В–Є–≤–љ—Л–µ –≤–µ—Й–µ—Б—В–≤–∞ EGb 761 – –≥–Є–љ–Ї–≥–Њ–ї–Є–і—Л – –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—П –љ–∞ –љ–µ–є—А–Њ–љ–∞–ї—М–љ—Г—О –Љ–µ–Љ–±—А–∞–љ—Г —Д–Њ—А–Љ–µ–љ–љ—Л—Е —Н–ї–µ–Љ–µ–љ—В–Њ–≤ –Ї—А–Њ–≤–Є, —Г–Љ–µ–љ—М—И–∞—О—В –∞–≥—А–µ–≥–∞—Ж–Є—О —В—А–Њ–Љ–±–Њ—Ж–Є—В–Њ–≤ –Є —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤. –Ґ–µ–Љ —Б–∞–Љ—Л–Љ –Ь–µ–Љ–Њ–њ–ї–∞–љ—В —Г–ї—Г—З—И–∞–µ—В —А–µ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б–≤–Њ–є—Б—В–≤–∞ –Ї—А–Њ–≤–Є, –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В —В—А–Њ–Љ–±–Њ–Њ–±—А–∞–Ј–Њ–≤–∞–љ–Є—О –Є –≤—Л–і–µ–ї–µ–љ–Є—О –њ–Њ–≤—Л—И–∞—О—Й–Є—Е —В–Њ–љ—Г—Б –≥–ї–∞–і–Ї–Њ–Љ—Л—И–µ—З–љ–Њ–є –Љ—Г—Б–Ї—Г–ї–∞—В—Г—А—Л –Љ–µ–і–Є–∞—В–Њ—А–Њ–≤ [19,23].
–Т–∞–Ј–Њ–∞–Ї—В–Є–≤–љ—Л–є –Є –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–є —Н—Д—Д–µ–Ї—В—Л –њ—А–µ–њ–∞—А–∞—В–∞ –Ь–µ–Љ–Њ–њ–ї–∞–љ—В –і–∞—О—В –Њ—Б–љ–Њ–≤–∞–љ–Є—П –і–ї—П –µ–≥–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Г –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б —Ж–µ–ї—М—О –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П –Є–ї–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М EGb 761 –Є–Ј—Г—З–∞–ї–∞—Б—М –≤ –Њ–і–љ–Њ–Љ –Є–Ј –Љ–∞—Б—И—В–∞–±–љ—Л—Е –Љ–Є—А–Њ–≤—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є –њ–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є (–Ю—А–µ–≥–Њ–љ—Б–Ї–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ), —А–µ–Ј—Г–ї—М—В–∞—В—Л –Ї–Њ—В–Њ—А–Њ–≥–Њ –±—Л–ї–Є –Њ–њ—Г–±–ї–Є–Ї–Њ–≤–∞–љ—Л –≤ 2008 –≥. –Т —Н—В–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є 118 –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж —Б—В–∞—А—И–µ 85 –ї–µ—В –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –≤ —В–µ—З–µ–љ–Є–µ 3 –ї–µ—В. –£—Б–ї–Њ–≤–Є–µ–Љ –≤–Ї–ї—О—З–µ–љ–Є—П –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –±—Л–ї–Њ –Њ—В—Б—Г—В—Б—В–≤–Є–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –љ–∞ –Є—Б—Е–Њ–і–љ–Њ–Љ –≤–Є–Ј–Є—В–µ. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –њ–ї–∞—Ж–µ–±–Њ –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М —А–∞–Ј–≤–Є—В–Є—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –±—Л–ї–∞ –±–Њ–ї—М—И–µ–є, —З–µ–Љ –љ–∞ —Д–Њ–љ–µ –∞–Ї—В–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є. –°–ї–µ–і—Г–µ—В, –Њ–і–љ–∞–Ї–Њ, –Њ–≥–Њ–≤–Њ—А–Є—В—М—Б—П, —З—В–Њ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –±—Л–ї —Б—В–∞—В–Є—Б—В–Є—З–µ—Б–Ї–Є –і–Њ—Б—В–Њ–≤–µ—А–љ—Л–Љ –ї–Є—И—М —Г —В–µ—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤, –Ї—В–Њ —Б–Њ–±–ї—О–і–∞–ї –њ—А–µ–і–њ–Є—Б–∞–љ–љ—Л–є —А–µ–ґ–Є–Љ –і–Њ–Ј–Є—А–Њ–≤–∞–љ–Є—П –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ–≥–Њ –≤—А–µ–Љ–µ–љ–Є [16].
–≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–µ–њ–∞—А–∞—В–∞ –Ь–µ–Љ–Њ–њ–ї–∞–љ—В –њ—А–Є —Г–ґ–µ —А–∞–Ј–≤–Є–≤—И–Є—Е—Б—П –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞—Е —В–∞–Ї–ґ–µ –Њ—Ж–µ–љ–Є–≤–∞–ї–∞—Б—М –≤ —Ж–µ–ї–Њ–Љ —А—П–і–µ –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ—Л—Е —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –≤ –Ї–Њ—В–Њ—А—Л—Е –њ—А–Є–љ–Є–Љ–∞–ї–Є —Г—З–∞—Б—В–Є–µ –≤ –Њ–±—Й–µ–є —Б–ї–Њ–ґ–љ–Њ—Б—В–Є –Њ–Ї–Њ–ї–Њ 2000 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –С–Р –Є–ї–Є —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є. –С—Л–ї–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П 120–240 –Љ–≥/—Б—Г—В. –і–∞–љ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ –Љ–µ–љ–µ–µ 6 –Љ–µ—Б. –Њ—В–Љ–µ—З–∞—О—В—Б—П —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤, —Г–ї—Г—З—И–µ–љ–Є–µ –њ–Њ–≤–µ–і–µ–љ–Є—П –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є —А–∞–Ј–ї–Є—З–љ–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є, –њ–Њ–≤—Л—И–µ–љ–Є–µ –Є—Е —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ—Б—В–Є –≤ –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –ґ–Є–Ј–љ–Є (—В–∞–±–ї. 3, —А–Є—Б. 1). –°–ї–µ–і—Г–µ—В –њ–Њ–і—З–µ—А–Ї–љ—Г—В—М, —З—В–Њ, —Б —Г—З–µ—В–Њ–Љ —Ж–Є—В–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є, –њ—А–µ–і–њ–Њ—З—В–Є—В–µ–ї—М–љ–µ–µ –±–Њ–ї–µ–µ –≤—Л—Б–Њ–Ї–Є–µ –і–Њ–Ј—Л –њ—А–µ–њ–∞—А–∞—В–∞ (240 –Љ–≥), —З–µ–Љ —Н—В–Њ –±—Л–ї–Њ –њ—А–Є–љ—П—В–Њ —А–∞–љ–µ–µ [21,22,28,32,45].
–Р—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–∞—П –Є –≥–ї—Г—В–∞–Љ–∞—В–µ—А–≥–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П. –°–Њ–≥–ї–∞—Б–љ–Њ –Њ–±—Й–µ–њ—А–Є–љ—П—В–Њ–Љ—Г –Љ–µ–ґ–і—Г–љ–∞—А–Њ–і–љ–Њ–Љ—Г —Б—В–∞–љ–і–∞—А—В—Г, –љ–∞ —Б—В–∞–і–Є–Є –і–µ–Љ–µ–љ—Ж–Є–Є –њ—А–Є–Њ—А–Є—В–µ—В–љ—Л –њ—А–µ–њ–∞—А–∞—В—Л –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П. –Э–∞—З–Є–љ–∞—П —Б 70–80–—Е –≥–≥. –•–• –≤–µ–Ї–∞ –±—Л–ї–Њ —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –њ–Њ–Ї–∞–Ј–∞–љ–Њ, —З—В–Њ —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Є–љ—В–µ–Ј–∞ –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–∞ —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –љ–µ–є—А–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ –і–µ—Д–µ–Ї—В–Њ–Љ –њ—А–Є –С–Р. –Т –њ–Њ—Б–ї–µ–і—Г—О—Й–µ–Љ –±—Л–ї–Њ —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Њ, —З—В–Њ –њ–Њ–і–Ї–Њ—А–Ї–Њ–≤–∞—П –∞—А—В–µ—А–Є–Њ–ї–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–∞—П —Д–Њ—А–Љ–∞ —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є, –і–µ–Љ–µ–љ—Ж–Є—П —Б —В–µ–ї—М—Ж–∞–Љ–Є –Ы–µ–≤–Є –Є –њ—А–Є –±–Њ–ї–µ–Ј–љ–Є –Я–∞—А–Ї–Є–љ—Б–Њ–љ–∞ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—В—Б—П –≤–µ—Б—М–Љ–∞ –њ–Њ—Е–Њ–ґ–Є–Љ–Є –љ–µ–є—А–Њ—В—А–∞–љ—Б–Љ–Є—В—В–µ—А–љ—Л–Љ–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ–Є. –Т—Б–µ —Н—В–Њ –њ–Њ—Б–ї—Г–ґ–Є–ї–Њ –Њ—Б–љ–Њ–≤–∞–љ–Є–µ–Љ –і–ї—П –љ–∞—З–∞–ї–∞ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј—Л (—В–µ—В—А–∞–∞–Љ–Є–љ–Њ–∞–Ї—А–Є–і–Є–љ, –Є–њ–Є–і–∞–Ї—А–Є–љ, –і–Њ–љ–µ–њ–Є–Ј–Є–ї, —А–Є–≤–∞—Б—В–Є–≥–Љ–Є–љ, –≥–∞–ї–∞–љ—В–∞–Љ–Є–љ), –њ—А–Є –і–µ–Љ–µ–љ—Ж–Є—П—Е –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В –і–∞–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –љ–∞ —Б—В–∞–і–Є–Є –ї–µ–≥–Ї–Њ–є –Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є –њ–Њ–ї–љ–Њ—Б—В—М—О –і–Њ–Ї–∞–Ј–∞–љ –Ї–∞–Ї —А–∞–љ–і–Њ–Љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ–Є, —В–∞–Ї –Є –њ–Њ–≤—Б–µ–і–љ–µ–≤–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–Њ–є. –Ю–±—Б—Г–ґ–і–∞–µ—В—Б—П —В–∞–Ї–ґ–µ –≤–µ—А–Њ—П—В–љ–∞—П —Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В—М –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є –Ј–∞–Љ–µ–і–ї—П—В—М –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–µ –і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞ –њ—А–Є –С–Р. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Є–љ–≥–Є–±–Є—В–Њ—А–Њ–≤ –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј—Л –љ–∞ —Б—В–∞–і–Є–Є –љ–µ–і–µ–Љ–µ–љ—В–љ—Л—Е (—Г–Љ–µ—А–µ–љ–љ—Л—Е) –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Є–≤–µ–ї–Є –Ї –њ—А–Њ—В–Є–≤–Њ—А–µ—З–Є–≤—Л–Љ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ [1,2,11,24,26,30].
–Ф—А—Г–≥–Є–Љ –Њ–±—Й–µ–њ—А–Є–Ј–љ–∞–љ–љ—Л–Љ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–Љ –њ–Њ–і—Е–Њ–і–Њ–Љ –Ї –і–µ–Љ–µ–љ—Ж–Є–Є —П–≤–ї—П–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –Њ–±—А–∞—В–Є–Љ–Њ–≥–Њ –±–ї–Њ–Ї–∞—В–Њ—А–∞ –Э–Ь–Ф–Р–—А–µ—Ж–µ–њ—В–Њ—А–Њ–≤ –Ї –≥–ї—Г—В–∞–Љ–∞—В—Г –Љ–µ–Љ–∞–љ—В–Є–љ—Г. –≠–Ї—Б–њ–µ—А–Є–Љ–µ–љ—В–∞–ї—М–љ—Л–µ –і–∞–љ–љ—Л–µ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤—Г—О—В, —З—В–Њ –Ї–∞–Ї –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б, —В–∞–Ї –Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Є—И–µ–Љ–Є—П –Є –≥–Є–њ–Њ–Ї—Б–Є—П, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—В—Б—П —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –≥–ї—Г—В–∞–Љ–∞—В–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л, —З—В–Њ —П–≤–ї—П–µ—В—Б—П –Њ–і–љ–Є–Љ –Є–Ј –≤–∞–ґ–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ –љ–µ–є—А–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –∞–Ї—В–Є–≤–∞—Ж–Є—П –≥–ї—Г—В–∞–Љ–∞—В–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ—А–Њ–Є—Б—Е–Њ–і–Є—В –≤ –Љ–Њ–Љ–µ–љ—В –њ—А–Њ—Ж–µ—Б—Б–∞ –Ї–Њ–љ—Б–Њ–ї–Є–і–∞—Ж–Є–Є —Б–ї–µ–і–∞ –њ–∞–Љ—П—В–Є –њ—А–Є –Ј–∞–њ–Њ–Љ–Є–љ–∞–љ–Є–Є –љ–Њ–≤–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є. –Я—А–Є –і–µ–Љ–µ–љ—В–Є—А—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П—Е —З—А–µ–Ј–Љ–µ—А–љ–∞—П –∞–Ї—В–Є–≤–∞—Ж–Є—П –≥–ї—Г—В–∞–Љ–∞—В–µ—А–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є—Б—В–µ–Љ—Л –љ–∞—А—Г—И–∞–µ—В –і–∞–љ–љ—Л–є –њ—А–Њ—Ж–µ—Б—Б, –∞ –µ–µ —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –љ–∞ —Д–Њ–љ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є—П –Љ–µ–Љ–∞–љ—В–Є–љ–∞ – —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г–µ—В –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –љ–Њ—А–Љ–∞–ї—М–љ–Њ–≥–Њ –њ–∞—В—В–µ—А–љ–∞ —Г—Б–≤–Њ–µ–љ–Є—П –љ–Њ–≤–Њ–є –Є–љ—Д–Њ—А–Љ–∞—Ж–Є–Є. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–∞—П —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Љ–µ–Љ–∞–љ—В–Є–љ–∞ —Б—З–Є—В–∞–µ—В—Б—П –і–Њ–Ї–∞–Ј–∞–љ–љ–Њ–є –њ—А–Є –і–µ–Љ–µ–љ—Ж–Є–Є —Г–Љ–µ—А–µ–љ–љ–Њ–є –Є —В—П–ґ–µ–ї–Њ–є —Б—В–µ–њ–µ–љ–Є. –Я–Њ –љ–µ–Ї–Њ—В–Њ—А—Л–Љ –і–∞–љ–љ—Л–Љ, –≤–Ї–ї—О—З–∞—П –љ–∞—И —Б–Њ–±—Б—В–≤–µ–љ–љ—Л–є –Њ–њ—Л—В, –Љ–µ–Љ–∞–љ—В–Є–љ —В–∞–Ї–ґ–µ –Љ–Њ–ґ–µ—В –±—Л—В—М —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ –љ–∞ —Б—В–∞–і–Є–Є –ї–µ–≥–Ї–Њ–є –і–µ–Љ–µ–љ—Ж–Є–Є –Є –љ–µ–і–µ–Љ–µ–љ—В–љ—Л—Е (—Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є) [1,2,11,24,30].
–Ы–µ—З–µ–љ–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є –Ї–Њ—А—А–µ–Ї—Ж–Є—П —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П. –Ъ–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В—М –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ —И–Є—А–Њ–Ї–Њ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–∞, –Є –±–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–Њ–ґ–Є–ї—Л—Е –ї—О–і–µ–є –Є–Љ–µ—О—В –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є. –Ь–љ–Њ–≥–Є–µ —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Н–Ї–Ј–Њ–≥–µ–љ–љ—Л–µ –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є –≤—Л–Ј—Л–≤–∞—О—В –Є–ї–Є —Г—Б—Г–≥—Г–±–ї—П—О—В –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж –Є–Ј––Ј–∞ —Б–Є—Б—В–µ–Љ–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤. –Я–Њ—Н—В–Њ–Љ—Г –њ—А–Є —А–∞–Ј—А–∞–±–Њ—В–Ї–µ —Б—В—А–∞—В–µ–≥–Є–Є –≤–µ–і–µ–љ–Є—П –њ–Њ–ґ–Є–ї—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Б–ї–µ–і—Г–µ—В –Њ–±—А–∞—В–Є—В—М –≤–љ–Є–Љ–∞–љ–Є–µ –љ–∞ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й—Г—О —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї—Г—О –њ–∞—В–Њ–ї–Њ–≥–Є—О, –љ–∞–ї–Є—З–Є–µ —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є, –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–є –Є–ї–Є –Є–љ–Њ–є –Є–љ—В–Њ–Ї—Б–Є–Ї–∞—Ж–Є–Є. –Э–∞–Є–±–Њ–ї–µ–µ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —Д—Г–љ–Ї—Ж–Є–Є –Њ–Ї–∞–Ј—Л–≤–∞—О—В –≥–Є–њ–Њ—В–Є—А–µ–Њ–Ј, –Т12––і–µ—Д–Є—Ж–Є—В–∞—А–љ–Њ–µ —Б–Њ—Б—В–Њ—П–љ–Є–µ, –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –њ–µ—З–µ–љ–Є –Є –њ–Њ—З–µ–Ї, —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–µ –Њ–±—Б—В—А—Г–Ї—В–Є–≤–љ—Л–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –ї–µ–≥–Ї–Є—Е, —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П —Б–µ—А–і–µ—З–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –і–ї–Є—В–µ–ї—М–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –њ—Б–Є—Е–Њ–∞–Ї—В–Є–≤–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤. –Т–Њ –≤—Б–µ—Е —Б–ї—Г—З–∞—П—Е –≤–њ–µ—А–≤—Л–µ –і–Є–∞–≥–љ–Њ—Б—В–Є—А–Њ–≤–∞–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ —Б–ї–µ–і—Г–µ—В –њ—А–Њ–≤–Њ–і–Є—В—М –ї–∞–±–Њ—А–∞—В–Њ—А–љ—Л–є —Б–Ї—А–Є–љ–Є–љ–≥ —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ–µ–љ–љ—Л—Е –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є [11,30].
–Т–µ—Б—М–Љ–∞ —З–∞—Б—В–Њ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ —Б–Њ—З–µ—В–∞—О—В—Б—П —Б —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ–Њ–≥–Њ —А—П–і–∞. –Я—А–Є —Н—В–Њ–Љ –≤–Ј–∞–Є–Љ–Њ—Б–≤—П–Ј—М –Љ–µ–ґ–і—Г –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –Є —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –Љ–Њ–ґ–µ—В –Є–Љ–µ—В—М –њ—А–Є—З–Є–љ–љ–Њ–—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–є –Є–ї–Є –њ–∞—А–∞–ї–ї–µ–ї—М–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А. –Ґ–∞–Ї, –Є–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ —В—П–ґ–µ–ї–∞—П –і–µ–њ—А–µ—Б—Б–Є—П –Љ–Њ–ґ–µ—В –≤—Л–Ј—Л–≤–∞—В—М –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –ї–Њ–±–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞. –° –і—А—Г–≥–Њ–є —Б—В–Њ—А–Њ–љ—Л, –љ–∞—З–Є–љ–∞—О—Й–Є–є—Б—П –і–µ–Љ–µ–љ—В–Є—А—Г—О—Й–Є–є –њ—А–Њ—Ж–µ—Б—Б –љ–µ—А–µ–і–Ї–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —В—А–µ–≤–Њ–ґ–љ–Њ––і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є –Ї–∞–Ї —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–є —А–µ–∞–Ї—Ж–Є–µ–є –љ–∞ –±–Њ–ї–µ–Ј–љ—М –њ—А–Є –Њ—В–љ–Њ—Б–Є—В–µ–ї—М–љ–Њ —Б–Њ—Е—А–∞–љ–љ–Њ–є –Ї—А–Є—В–Є–Ї–µ. –Э–∞–Ї–Њ–љ–µ—Ж, –љ–µ—А–µ–і–Ї–Њ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –Є —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –љ–µ —Б–≤—П–Ј–∞–љ—Л –њ—А–Є—З–Є–љ–љ–Њ–—Б–ї–µ–і—Б—В–≤–µ–љ–љ—Л–Љ–Є —Б–≤—П–Ј—П–Љ–Є, –љ–Њ –Њ–±—К–µ–і–Є–љ–µ–љ—Л –Њ–±—Й–Є–Љ –њ—Б–Є—Е–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ —Б—Г–±—Б—В—А–∞—В–Њ–Љ, —З—В–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П, –љ–∞–њ—А–Є–Љ–µ—А, –њ—А–Є –і–Є—Б—Д—Г–љ–Ї—Ж–Є–Є –ї–Њ–±–љ—Л—Е –і–Њ–ї–µ–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞. –Т –ї—О–±–Њ–Љ —Б–ї—Г—З–∞–µ, –љ–∞–ї–Є—З–Є–µ —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є —В—А–µ–±—Г–µ—В —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–Њ—А—А–µ–Ї—Ж–Є–Є. –Я—А–Є —Н—В–Њ–Љ —Б–ї–µ–і—Г–µ—В –Є–Ј–±–µ–≥–∞—В—М –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В–Њ–≤ —Б —Е–Њ–ї–Є–љ–Њ–ї–Є—В–Є—З–µ—Б–Ї–Є–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ [11,30].
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Є–Љ–µ—О—В—Б—П –љ–∞—А–∞–±–Њ—В–∞–љ–љ—Л–µ —В–µ—А–∞–њ–µ–≤—В–Є—З–µ—Б–Ї–Є–µ –њ–Њ–і—Е–Њ–і—Л –Ї –њ–∞—Ж–Є–µ–љ—В–∞–Љ —Б –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –љ–∞ –≤—Б–µ—Е —Н—В–∞–њ–∞—Е –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –њ—А–Њ—Ж–µ—Б—Б–∞. –£ –њ–Њ–ґ–Є–ї—Л—Е –ї–Є—Ж –±–µ–Ј –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Њ–є –Є—Е –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—П —П–≤–ї—П–µ—В—Б—П –њ—А–∞–≤–Є–ї—М–љ–Њ–µ –Є —Б–≤–Њ–µ–≤—А–µ–Љ–µ–љ–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —Б–µ—А–і–µ—З–љ–Њ–—Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–Є—Б—В–µ–Љ–∞—В–Є—З–µ—Б–Ї–Є–µ –Є–љ—В–µ–ї–ї–µ–Ї—В—Г–∞–ї—М–љ—Л–µ —Г–њ—А–∞–ґ–љ–µ–љ–Є—П, —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–µ –њ–Є—В–∞–љ–Є–µ –Є —Д–Є–Ј–Є—З–µ—Б–Ї–∞—П –љ–∞–≥—А—Г–Ј–Ї–∞. –Я—А–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е, –љ–µ –і–Њ—Б—В–Є–≥–∞—О—Й–Є—Е –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –і–µ–Љ–µ–љ—Ж–Є–Є, —Ж–µ–ї–µ—Б–Њ–Њ–±—А–∞–Ј–љ–Њ –њ—А–Њ–≤–µ–і–µ–љ–Є–µ –≤–∞–Ј–Њ–∞–Ї—В–Є–≤–љ–Њ–є –Є –љ–µ–є—А–Њ–Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Њ–є —В–µ—А–∞–њ–Є–Є. –£ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–µ–Љ–µ–љ—Ж–Є–µ–є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞ —П–≤–ї—П—О—В—Б—П –Є–љ–≥–Є–±–Є—В–Њ—А—Л –∞—Ж–µ—В–Є–ї—Е–Њ–ї–Є–љ—Н—Б—В–µ—А–∞–Ј—Л –Є –Љ–µ–Љ–∞–љ—В–Є–љ. –Э–∞ –≤—Б–µ—Е —Б—В–∞–і–Є—П—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –∞–Ї—В—Г–∞–ї—М–љ—Л–Љ–Є —П–≤–ї—П—О—В—Б—П –ї–µ—З–µ–љ–Є–µ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е —Б–Њ–Љ–∞—В–Є—З–µ—Б–Ї–Є—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –Є –Ї–Њ—А—А–µ–Ї—Ж–Є—П —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П.
![–Ґ–∞–±–ї–Є—Ж–∞ 2. –Р–љ—В–Є–≥–Є–њ–µ—А—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л –≤ –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–µ –і–µ–Љ–µ–љ—Ж–Є–Є [43]](/data/articles/Image/t20/n8/422-2.gif)
![–Ґ–∞–±–ї–Є—Ж–∞ 3. –Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–∞ –Ь–µ–Љ–Њ–њ–ї–∞–љ—В (EGB 761) [21,22,28,32,45]](/data/articles/Image/t20/n8/422-3.gif)
![–†–Є—Б. 1. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –њ–Њ–≤–µ–і–µ–љ—З–µ—Б–Ї–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є –љ–∞ —Д–Њ–љ–µ —В–µ—А–∞–њ–Є–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –Ь–µ–Љ–Њ–њ–ї–∞–љ—В —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –±–Њ–ї–µ–Ј–љ—М—О –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –і–µ–Љ–µ–љ—Ж–Є–µ–є (Napryeyenko et al., 2007 [32])](/data/articles/Image/t20/n8/422-4.gif)
–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –У–∞–≤—А–Є–ї–Њ–≤–∞ –°.–Ш. –§–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –±–Њ–ї–µ–Ј–љ–Є –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ // –Ь–Њ—Б–Ї–≤–∞: –Є–Ј–і––≤–Њ «–Я—Г–ї—М—Б», 2003. –115 –°.
2. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –С–Њ–ї–µ–Ј–љ—М –Р–ї—М—Ж–≥–µ–є–Љ–µ—А–∞ –Є —Б–Њ—Б—Г–і–Є—Б—В–∞—П –і–µ–Љ–µ–љ—Ж–Є—П // –Я–Њ–і —А–µ–і. –Э.–Э.–ѓ—Е–љ–Њ. – –Ь., 2002. – –°.85.
3. –Ч–∞—Е–∞—А–Њ–≤ –Т. –Т., –ѓ—Е–љ–Њ –Э. –Э. –Э–∞—А—Г—И–µ–љ–Є—П –њ–∞–Љ—П—В–Є // –Ь–Њ—Б–Ї–≤–∞: –У–µ–Њ—В–∞—А–Ь–µ–і. – 2003. – 110 –°.
4. –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т. –Т—Б–µ—А–Њ—Б—Б–Є–є—Б–Ї–∞—П –њ—А–Њ–≥—А–∞–Љ–Љ–∞ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–є —Н–њ–Є–і–µ–Љ–Є–Њ–ї–Њ–≥–Є–Є –Є —В–µ—А–∞–њ–Є–Є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ («–Я—А–Њ–Љ–µ—В–µ–є») //–Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. –2006. – –Ґ.11. – –°.27–32.
5. –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –°–Њ—Б–Є–љ–∞ –Т.–С. –Ъ–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ // –Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. – 2009. – –Ґ.14. вДЦ 4. – –°. 54–58.
6. –°–Њ—Б–Є–љ–∞ –Т.–С., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –ѓ—Е–љ–Њ –Э.–Э. –Э–µ–і–µ–Љ–µ–љ—В–љ—Л–µ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П —Г –±–Њ–ї—М–љ—Л—Е —Б–∞—Е–∞—А–љ—Л–Љ –і–Є–∞–±–µ—В–Њ–Љ 2––≥–Њ —В–Є–њ–∞ //–Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. – 2010. – –Ґ.15, вДЦ.4. ––°.25–30.
7. –°—В–∞—А—З–Є–љ–∞ –Ѓ.–Р., –Я–∞—А—Д–µ–љ–Њ–≤ –Т.–Р., –І–∞–Ј–Њ–≤–∞ –Ш.–Х., –Я—Г—Б—В–Њ–≤–Є—В–Њ–≤–∞ –Ґ.–°., –ѓ—Е–љ–Њ –Э.–Э. –Ъ–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є // –Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Є–Љ. –°.–°.–Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. – 2008. – вДЦ 4. – –°.19–23.
8. –ѓ—Е–љ–Њ –Э. –Э., –Ы–∞–≤—А–Њ–≤ –Р. –Ѓ. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ—А–Є —Б—В–∞—А–µ–љ–Є–Є // –Э–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—В–Є–≤–љ—Л–µ –±–Њ–ї–µ–Ј–љ–Є –Є —Б—В–∞—А–µ–љ–Є–µ (–†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є) / –Я–Њ–і —А–µ–і. –Ш. –Р. –Ч–∞–≤–∞–ї–Є—И–Є–љ–∞, –Э. –Э. –ѓ—Е–љ–Њ, –°. –Ш. –У–∞–≤—А–Є–ї–Њ–≤–Њ–є. – –Ь., 2001. – –°. 242 – 261.
9. –ѓ—Е–љ–Њ –Э.–Э. –Ъ–Њ–≥–љ–Є—В–Є–≤–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –≤ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є –Ї–ї–Є–љ–Є–Ї–µ. //–Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї. – 2006. – –Ґ.11. – –Я—А–Є–ї–Њ–ґ–µ–љ–Є–µ вДЦ 1. – –°. 4–12.
10. –ѓ—Е–љ–Њ –Э.–Э., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –Ы–Њ–Ї—И–Є–љ–∞ –Р.–С. –Э–∞—А—Г—И–µ–љ–Є—П –њ–∞–Љ—П—В–Є –Є –≤–љ–Є–Љ–∞–љ–Є—П –≤ –њ–Њ–ґ–Є–ї–Њ–Љ –≤–Њ–Ј—А–∞—Б—В–µ // –Ц—Г—А–љ–∞–ї –љ–µ–≤—А–Њ–ї–Њ–≥–Є–Є –Є –њ—Б–Є—Е–Є–∞—В—А–Є–Є –Є–Љ. –°.–°. –Ъ–Њ—А—Б–∞–Ї–Њ–≤–∞. – 2006. – –Ґ.106. – вДЦ 2. – –°.58–62.
11. –ѓ—Е–љ–Њ –Э.–Э., –Ч–∞—Е–∞—А–Њ–≤ –Т.–Т., –Ы–Њ–Ї—И–Є–љ–∞ –Р.–С., –Ъ–Њ–±–µ—А—Б–Ї–∞—П –Э.–Э., –Ь—Е–Є—В–∞—А—П–љ –≠.–Р. –Ф–µ–Љ–µ–љ—Ж–Є–Є. –Я—А–∞–Ї—В–Є—З–µ—Б–Ї–Њ–µ —А—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є // –Ь.: –Ь–Х–Ф–њ—А–µ—Б—Б––Є–љ—Д–Њ—А–Љ, 2010. – 272 –°.
12. Abbott R.D., White R.D., Ross G.W. et al. Walking and dementia in physically capable elderly men //JAMA. –2004. –Vol.292. – вДЦ.12. – P.1447–1453.
13. Colcombe S.J., Erickson K.I., Raz N. et al. Aerobic fitness reduces brain tissue loss in aging humans // J. Gerontol. A. Biol. Sci. Med. Sci. – 2006. –Vol.61. –N. –P.1166–1170.
14. Dartigues J.F., Gagnon M., Letenneur L. et al. Principal lifi–time occupation and cognititve impairment in French elderly cohort (PAQUID) //Am. J. Epidemiol. –1992. –Vol.135. –N.9. –P.981–988.
15. DiCarlo A., Baldereschi M., Amaducci L. Et al. Cognitive impairment without dementia in older people: prevalence, vascular risk factors, impact on disability. The Italian Longitudinal Study on Aging // J. Am. Ger. Soc. –2000. –Vol.48. – P.775–782.
16. Dodge H.H, Zitzelberger T., Oken B.S. et al.. A randomized placebo–controlled trial of ginkgo biloba for the prevention of cognitive decline. // Neurol.– 2008.– Vol.70.– P. 1809–1817.
17. Forette F., Seux M.L., Staessen J. et al. Prevention of dementia in randomized placebo–controlled systolic hypertension in Europe (SYS–EUR) trial // Lancet. –1998. –Vol. 352. – P.1347–1351.
18. Graham J.E., Rockwood K., Beattie E.L. et al. Prevalence and severity of cognitive impairment with and without dementia in an elderly population // Lancet. –1997. –Vol. 349. –P.1793–1796.
19. Halama P. Was leistet der Spezialextrakt (Egb 761) //Therapiewoche. –1990. – Vol.40. – P. 3760–3765.
20. Heart Protection Study collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20536 high–risk individuals: a randomised placebo–controlled trial // Lancet. –2002. –Vol.360. –P.7–22.
21. Ihl R., Bachinskaya N.Yu., Korczyn A. et al. Efficacy and safety of a once daily formulation of Gingko biloba extract (EGb 761) in dementia with neuropsychiatric features: a randomized controlled trial // Int. J. Ger. Psych. –2010. Epub ahead of print.
22. Kanowski S, Hoerr R. Ginkgo biloba extract EGb 761® in dementia: Intention–to–treat analysis of a 24–week, multi–center, double–blind, placebo–controlled, randomized trial. // Pharmacopsychiatry.– 2003.– Vol. 36.– P. 297–303.
23. Kleijnen J., Knipschild P. Ginkgo biloba // Lancet.–1992. – Vol.340 : Nov 7.–P.1136–1139.
24. Knopman D.S. Current treatment of mild cognitive impairment and Alzheimer’s disease // Curr. Neurol. Nerosci Rep. –2006. –Vol.6. –N.5. – P.365–371.
25. Korf ES, van Straaten E.C., de Leeuw F.E. et al. Diabetes mellitus, hypertension and medial temporal lobe atrophy: the LADIS study. // Diabet Med. – 2007.– Vol. 24(2).– P.166–171.
26. Kurshner H.S. Mild cognitive impairment: to treat or not to treat? // Curr. Neurol. Neurosci Rep. –2005. –Vol.5. –N.6. –P.455–457.
27. Laurin D., Verreault R., Linsay J. et al. Physical activity and risk of cognitive impairment and dementia in elderly persons //Arch. Neurol. –2001. –Vol.58. –N.3. –P.498–504.
28. Le Bars P.L., Katz M.M., Berman N. et al.. A placebo–controlled, double–blind, randomized trial of an extract of Ginkgo biloba for dementia. North American EGb Study Group // JAMA.– 1997.– Vol. 278.– P.1327–1332.
29. Lithel H., Hansson L., Skoog I. et al. The study on cognition and prognosis in the elderly (SCOPE): principal results of a randomized double blind intervention trial // J. Hypertention. –2003. –Vol.21. – P. 875–886.
30. Lovenstone S., Gauthier S. Management of dementia. – London: Martin Dunitz, 2001.
31. McDowell I., Xi G., Linsay J., Tierney M. Mapping the connection between education and dementia // J. Clin. Exp. Neuropsychol. –2007. –Vol.29. –N.2. –P.127–141.
32. Napryeyenko O., Borzenko I. Ginkgo biloba Special Extract in Dementia with Neuropsychiatric Features; A randomised, placebo–controlled, double–blind clinical trial // Drug research. – 2007. – Vol. 57(1). – P. 4–11.
33. Olazaran J., Muniz R., Reisberg B. et al. Benefit of cognitive–motor intervention in MCI and mild–to–moderate AD // Neurol. –2004. –Vol.63. –N.12. –P.2348–2353.
34. Ott A. et al. Association of diabetes mellitus and dementia: The Rotterdam Study// Diabetol.– 1996.– Vol. 39.– P.1392–1397.
35. Prince M.J., Bird A.S., Blizard R.A., Mann A.H. Is the cognitive function of older patients affected by anti–hypertensive treatment? Results from 54 months of the Medical Research Council’s trial of hypertension in older adults //BMJ. –1992. –Vol.304. –P.405–412.
36. Rapp S., Brenes G., Marsh A.P. Memory enhancement training for older adults with mild cognitive impairment: a preliminary study //Aging and mental health. – 2002. –Vol.6. –N.1. –P.5–11.
37. Rockwood K., Kirkland S., Hogan D.B. Use of lipid–lowering agents, indication bias and the risk of dementia in community–dwelling elderly people //Arch. Neurol. – 2002. –Vol. 59. –P. 223–227.
38. Rovio S., Kareholt I., Helkala E.L. et al. Leisure–time physical activity at midlife and the risk of dementia and Alzheimer’s disease // Lancet. Neurol. – 2005. –Vol. 4. – N.11. –P.705–711.
39. Scrader J., Luder S., Kulschevski A. et al. Morbidity and mortality after stroke – Eprosartan compared with nitrendipine for secondary prevention (MOSES) // Stroke. – 2005. –Vol. 36. –P. 1218–1226.
40. Scrameas N. Stern Y., Tang M.X. et al. Mediterranean diet and risk for Alzheimer’s disease //Ann. Neurol. – 2006. – Vol. 59. – N.6. – P.877–879.
41. SHEP Cooperative Research Group. Prevention of stroke by antihypertensive drug treatment in older persons with isolated systolic hypertension: final results of the systolic hypertension in the elderly // JAMA. –1991. – Vol. 265. –P.3255–3264.
42. Shepherd J., Blauw G., Murphy M. et al. Pravastatin in elderly individuals at risk of vascular disease (PROSPER): a randomised placebo controlled trial //Lancet. – 2002. – Vol. 360. – P.1623–1630.
43. Skoog I., Gustafson D. Clinical trials for primary prevention in dementia // Dementia therapeutic research / K.Rockwood, S.Gauthier (eds). – London a New York: Taylor a Francis. – 2006. – P.189–212.
44. Smidt I.W., Berg I.G., Deelman B.G. Memory training for remembering names: initial results in the healthy elderly // Tijdchr. Gerontol. Geriatr. – 1997. –Vol. 28. – N.4. –P.155–162.
45. Schneider L., DeKosky S., Farlow M. et al. A randomized, double–blind, placebo–controlled trial of two doses of Ginkgo biloba extract in dementia of the Alzheimer's type // Curr. Alzheimer. Res. – 2005.– Vol. 2(5).– P. 541–551.
46. Snowdon D.A., Greiner L.H., Mortimer J.A. et al. Brain infarction and the clinical expression of Alzheimer’s disease. The Nun Study // JAMA. –1997. –Vol. 277. – N.10. – P.813–817.
47. Solfrizzi V., Colacicco A.M., D’Inttrono A. et al. Dietary intake of unsaturated fatty acids and age–related cognitive decline : a 8,5 year follow–up of the Italian Longitudinal Study on Aging // Neurobiol. Aging. – 2006. –Vol. 27. –N.11. – P.1694–1704.
48. Stern Y., Alexander G.E., Prohovnik I., Mayex R. Inverse relationship between education and parietotemporal perfusion deficit in AD // Ann. Neurol. – Vol. 32. – N.3. – P.371–375.
49. Tzourio C., Andersen C., Chapman N. et al. Effects of blood pressure lowering with perindopril and indapamide therapy on dementia and cognitive decline in patients with cerebrovascular disease //Arch. Intern. Med. – 2003. –Vol.163. – P.1069–1075.












