Среди причин смерти, по данным, которые привела заместитель министра здравоохранения РФ Т.В. Яковлева, 56,7% занимают сердечно-сосудистые; 14,4% – онкологические заболевания, травмы, отравления и другие внешние причины – 10,7%. Таким образом, вклад других болезней в этот показатель по сравнению с сердечно-сосудистыми заболеваниями незначителен. При этом инсульт занимает второе место, уступая лишь ишемической болезни сердца (ИБС) с инфарктом миокарда.
В структуре инсульта 80% составляет инфаркт мозга. При этом, если при внезапной остановке мозгового кровотока потеря сознания происходит уже через 10 с, биоэлектрическое молчание на ЭЭГ – через 30–40 с, а смерть мозга – через 8–10 мин., то при инсульте процесс необратимого повреждения вещества мозга в ядре ишемии также стремителен, но в зоне ишемической полутени – участке мозга, многократно превышающем по объему область некроза, где нейроны не погибли и могут восстановить жизнедеятельность, растягивается на часы.
Наиболее доступным из современных методов лечения больных с ишемическим инсультом является системная тромболитическая терапия (ТЛТ). Вернер Хаке (W. Hacke) – один из основоположников применения ТЛТ в Европе – отмечает, что системная ТЛТ изучена значительно лучше других методов реваскуляризации. Этот метод наиболее доступен как экономически, так и технически [4, 5, 7].
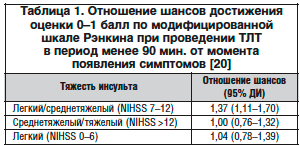
В настоящее время в сотнях медицинских организаций в России есть все необходимые условия для проведения ТЛТ. Одной из причин, препятствующих проведению ТЛТ, является сравнительно небольшой срок от момента появления первых симптомов острого нарушения мозгового кровообращения (ОНМК) до начала тромболизиса. Это всего лишь 4,5 ч. При этом не следует заблуждаться – хотя срок «от первых симптомов до иглы» максимально достигает 270 мин., каждая дополнительная минута промедления увеличивает объем безвозвратно погибшей ткани головного мозга. Поэтому чем раньше проводится ТЛТ, тем лучше результат. Именно временной интервал является «камнем преткновения» в широком применении этого метода во всем мире, в т. ч. и в нашей стране. Минимизация сроков дает наилучшие результаты (табл. 1) [20].
Наиболее эффективным методом, позволяющим снизить временной период поступления больного с инсультом в стационар и тем самым увеличить число больных, которым проводится ТЛТ, является повышение медицинской грамотности населения. Если постоянно информировать население о признаках инсульта и обучать алгоритму действий при этом состоянии, то постепенно все большее число наших пациентов будут попадать в стационар своевременно. Также важно во всех муниципальных образованиях, где врачи овладели методом ТЛТ, широко оповещать население о возможности применения нового высокоэффективного метода лечения инсульта. Без использования радио и телевидения это невозможно, поскольку целевая аудитория – люди пожилого возраста, больше слушает радио и просматривает телепередачи и меньше пользуется Интернетом, чем лица среднего возраста [3, 9, 18].
Другой фактор, уменьшающий применение ТЛТ, – распространенные заблуждения, циркулирующие как в медицинском сообществе, так и среди пациентов, об эффективности различных препаратов сосудистого и метаболического действия при ОНМК. До настоящего времени не появилось достаточных доказательств эффективности нейропротективных средств, показавших хорошие результаты в эксперименте. По мнению A. Majid (2014), причина рассогласования экспериментальных и клинических данных заключается в двойственности процессов, протекающих при инсульте. Так, активность клеток микроглии и других, участвующих в воспалительном процессе, действие металлопротеаз, процессы апоптоза и аутофагии могут носить как защитный, так и повреждающий характер в зависимости от срока их воздействия и этапа развития патологического процесса. По оценкам специалистов, не менее трети исследований потенциальных нейропротекторов дают негативные или ложноположительные результаты [13, 15]. К сожалению, приходится констатировать, что после того, как при инфаркте мозга истекает срок для проведения ТЛТ, у врача остаются возможности только для реабилитации и вторичной профилактики инсульта у данного пациента. Другие высокотехнологичные методы лечения ишемического инсульта могут осуществляться лишь в отдельных медицинских центрах.
Еще одно условие, необходимое для проведения ТЛТ, – доступность нейровизуализации. Когда в 90-е гг. прошлого века эксперты-неврологи говорили, что проведение компьютерной томографии (КТ) является обязательным для каждого больного с ОНМК в момент поступления в стационар, то это положение казалось несбыточной мечтой. Но с каждым годом аппаратов для нейровизуализации становилось все больше, а их разрешающие способности – все выше.
Следует отметить, что по мере развития методов нейровизуализации изменяются задачи, которые эти методы решают. Если вначале основная задача заключалась в определении характера инсульта – ишемический или геморрагический, то в настоящее время нейровизуализация позволяет также установить патогенетический подтип инфаркта мозга, выявить патологию сосуда, приведшего к инсульту, определить тактику лечения. Особенно важно это при преходящих нарушениях мозгового кровообращения, когда симптомов ишемии мозга уже нет, а риск повторного цереброваскулярного события неизмеримо высок.

Современные протоколы проведения РКТ и магнитно-резонансной томографии (МРТ) позволяют выявлять не только объем и характер очага инсульта, но и показывают, каковы возможности достижения положительного эффекта от ТЛТ. Так, при перфузионной РКТ возможно выявление так называемого феномена «рассогласования» – различие в объеме вещества мозга, где снижены скорость кровотока и объем крови. Эта область «рассогласования» является зоной ишемической полутени, т. е. участком мозга, который потенциально можно спасти от гибели при своевременном вмешательстве (рис. 1). Феномен «рассогласования» обнаружен и при МРТ, но здесь учитывается различие в объемах очага при исследовании диффузионно-взвешенного и перфузионно-взвешенного изображения. Таким образом, в настоящее время насущной задачей в области нейровизуализации является овладение современными приемами диагностики: для РКТ – это ангиография и перфузионное исследование, для МРТ – бесконтрастная ангиография, диффузионное и перфузионное исследования.
В настоящее время для лечения больных с ишемическим инсультом все шире стали использоваться интервенционные методы – внутриартериальные рентгеноэндоваскулярные вмешательства. Среди интраартериальных методов лечения выделяют интраартериальный тромболизис, проксимальную аспирационную тромбэктомию, дистальную тромбэктомию и стентирование (рис. 2).
Если первоначально для реканализации в основном использовали интраартериальный тромболизис, а механическое воздействие – лишь для фрагментации тромба, то сейчас все чаще используют тромбоэкстракцию после тромболизиса или без него. Для дистальной тромбэктомии созданы различные приспособления, в настоящее время обнадеживающие результаты получены при использовании устройства SOLITAIRE [22].
В результате использования интраартериальных методов лечения в ведущих клиниках США и Западной Европы определены условия достижения хорошего результата внутрисосудистого вмешательства:
- минимальный срок от развития инсульта (менее 6 ч). Таким образом, срок лечебного воздействия при ишемическом инсульте вновь несколько увеличивается до 360 мин.;
- тромбоз крупной артерии (внутренняя сонная артерия (ВСА), средняя мозговая артерия (СМА) (сегменты М1 и М2), передняя мозговая артерия (ПМА), основная артерия, позвоночная артерия). При поражении дистальных отделов сосудистых бассейнов этих артерий более эффективна системная ТЛТ;
- наличие «рассогласования» (mismatch) по данным РКТ или МРТ. Если при нейровизуализации феномен «рассогласования» отсутствует, значит зона ишемической полутени не определяется, а следовательно, не имеет смысла проводить какие-либо интервенционные методы;
- наличие хорошо развитого коллатерального кровотока, являющееся условием поддержания жизнеспособности мозгового вещества в зоне ишемической полутени [6, 16].
Швейцарские исследователи из Бернского университета [A. Galimanis и соавт., 2012] обнаружили, что у пациентов с ишемическим инсультом чаще всего выявляются окклюзии различных отделов СМА, причем более 50% всех случаев – это ствол сосуда, сегменты М1 и М2 (табл. 2).

При анализе результатов лечения этих пациентов во время выступления на Всемирном неврологическом конгрессе в Вене (2013) H. Mattle отметил, что наилучшие показатели были достигнуты у пациентов с окклюзией сегментов М1–4 СМА, в то время как при тромбозах ВСА число лиц, достигших оценки 0–2 балла по модифицированной шкале Рэнкина к 90-му дню после инсульта, было наименьшим (рис. 3). Особенно неблагоприятным был тромбоз терминальных отделов ВСА, когда одновременно блокировались бассейны СМА и ПМА. Очевидно, что для выявления этой локализации атеротромботического процесса необходимы РКТ-ангиография и быстрейшее эндоваскулярное вмешательство.
Была четко прослежена связь со сроком вмешательства – проведение реперфузионных мероприятий в срок до 6 ч позволило получить показатели 0–2 балла к 90-му дню после инсульта по модифицированной шкале Рэнкина у 60% больных. Также важным фактором, определяющим исход интраартериального вмешательства, H. Mattle считает и наличие феномена «рассогласования». При его обнаружении у 2/3 пациентов получены хорошие результаты, в то время как при его отсутствии – только у 1/4.

Из приведенных фактов можно сделать определенные выводы: если системная ТЛТ – это метод лечения больных с ишемическим инсультом, который должен применяться как можно шире во всех медицинских организациях, имеющих необходимое оборудование и, самое главное, подготовленных специалистов, то для проведения внутриартериальных вмешательств требуется определенный отбор пациентов, наличие четких показаний и отсутствие противопоказаний. Неправильно использовать рентгеноэндоваскулярные методы по принципу «вдруг поможет». Однако в основе функционирования сложной многоуровневой системы оказания помощи больным с инфарктом мозга лежит все-таки своевременное попадание пациента в стационар.
Учитывая, что наличие окклюзии крупного экстра- или интракраниального сосуда при инфаркте мозга – важный фактор для предсказания эффективности внутриартериального вмешательства, обоснован интерес к поиску различных признаков такой окклюзии. Обнаружено, что наличие оценки по шкале NIHSS от 8 до 20 баллов в первые 3 ч от момента развития симптомов инсульта с высокой вероятностью свидетельствует о страдании крупного сосуда и может быть аргументом в пользу рентгеноэндоваскулярного вмешательства (рис. 4) [8].
Но говоря об интервенционном лечении, следует обращать внимание и на признаки, которые могут предсказывать негативные результаты интраартериального вмешательства при ишемическом инсульте. В настоящее время такие предикторы неблагоприятного исхода сформулированы:
- возраст пациента более 80 лет;
- оценка более 18 баллов по шкале NIHSS;
- наличие крупного инфаркта мозга по данным РКТ-перфузии без феномена «рассогласования», при бесконтрастной РКТ – томограмма оценивается по шкале ASPECTS в 7 или менее баллов, или на МРТ в режиме диффузионно-взвешенного изображения объем очага составляет более 100 см3, что указывает на объем инфаркта мозга более 1/3 бассейна СМА [12, 14];
- гипергликемия в дебюте инсульта всегда является фактором, предрасполагающим к развитию осложнений;
- наличие сопутствующих факторов риска: артериальная гипертензия, фибрилляция предсердий, сахарный диабет. В настоящее время многие исследователи пытаются ранжировать риски интервенционных вмешательств, такими методами являются IScore (Ischemic Stroke Predictive Risk Score), THRIVE Score (Totaled Health Risks in Vascular Events) и др. [9, 19];
- наличие явных РКТ или МРТ-признаков геморрагического компонента на исходной томограмме является однозначным противопоказанием к проведению и системной ТЛТ, и внутриартериального вмешательства;
- наконец, если в результате вмешательства не достигнута реканализация, то это также является неблагоприятным прогностическим фактором.

Еще одно направление в лечении больных ишемическим инсультом – нейрохирургическое вмешательство, декомпрессивная трепанация при злокачественном течении, сопровождающемся отеком и дислокацией мозга. Этот метод повышает выживаемость при тяжелом инсульте, но, к сожалению, приводит к увеличению числа больных с инсультом, имеющих оценку по модифицированной шкале Рэнкина 4–5 баллов.
В настоящее время никаких достоверных сведений об эффективности каких-либо методов нейропротекции при инсульте, за исключением гипотермии, не получено.
Проблема лечения больных с геморрагическим инсультом – не столько неврологическая, сколько хирургическая, т. к. никаких лекарственных методов лечения кровоизлияния в мозг нет. Все, чем может помочь невролог – это базисная терапия инсульта. Сейчас во всем мире для лечения больных с внутричерепными кровоизлияниями все шире используются нейрохирургические и эндоваскулярные методы лечения.
В прошлые годы при внутримозговых кровоизлияниях проводились попытки открытого дренирования полости гематомы для уменьшения объемного воздействия и снижения токсического эффекта распада излившейся крови. При этом была показана эффективность нейрохирургического вмешательства при гематомах объемом более 30 см3, особенно при локализации в задней черепной ямке [17]. В настоящее время нейрохирургическая техника ушла по пути прогресса далеко вперед, появились системы навигации, позволяющие точно ориентироваться в полости черепа через миниатюрные фрезевые отверстия, новые доступы (например, супраорбитальный), микрохирургическая техника (рис. 5) [2, 11], гибридные операционные, когда к услугам хирургов имеется не только ангиографическая установка, но и РКТ или МРТ, и многое другое. Это позволило перейти на новый уровень нейрохирургической помощи.
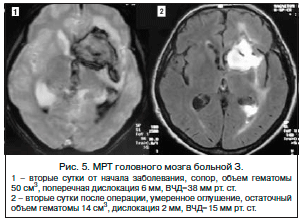
В настоящее время при геморрагическом инсульте ранняя малоинвазивная нейрохирургическая помощь показана пациентам в возрасте 50–69 лет со спонтанными внутримозговыми кровоизлияниями в течение первых 8 ч после возникновения при объеме гематомы 20–50 см3, оценке по шкале комы Глазго 9 или более [2, 21]. Очень важно подчеркнуть, что на исход нейрохирургического вмешательства оказывает влияние как срок проведения – чем раньше, тем лучше, но не позднее первых 8 ч, так и исходный уровень сознания – отсутствие тяжелой комы, свидетельствующей о необратимых процессах в веществе мозга.
Весьма перспективным методом нейромониторинга у больных с внутримозговым кровоизлиянием является ЭЭГ-мониторинг, что позволяет у части больных выявить персистирующий бессудорожный эпилептический статус как причину нарушения сознания. При этом следует отметить, что если у больных с эпилепсией видео-ЭЭГ-мониторинг уже давно показал себя как наиболее эффективный метод диагностики, то у больных с инсультом контроль ЭЭГ пока что не занял соответствующего места, хотя мы знаем об огромном числе различных ЭЭГ-феноменов у таких пациентов. Недаром С. Шорвон (S. Shorvon) заметил, что более половины больных с ОНМК переносят эпилептические припадки, которые не замечаются ни врачами, ни окружающими. Широкое использование ЭЭГ-мониторинга позволит не только выявлять бессудорожный статус, симулирующий атоническую кому при инсульте, но и даст возможность более точно оценивать состояние больного.
В отношении субарахноидального кровоизлияния следует отметить, что здесь также на первом месте находится вопрос о выявлении и выключении из кровотока внутричерепных аневризм сосудов основания мозга. В настоящее время есть два метода: нейрохирургический – клипирование аневризмы, и эндоваскулярный – эмболизация полости аневризмы. Оба метода имеют как плюсы, так и минусы, показания и противопоказания, оба активно совершенствуются. Очевидно, что в каждом конкретном случае вопрос о применении того или иного метода должен решаться коллегиально.
В заключение хотелось бы подчеркнуть, что интервенционные мероприятия при инсульте, которые в последние годы стали широко распространяться, будут постепенно становиться рутиной. По предварительным оценкам, до половины больных с инсультом нуждаются в том или ином методе хирургического или иного высокотехнологического лечения в остром периоде инсульта. Если рассматривать вопросы реабилитации и вторичной профилактики, то таких пациентов окажется еще больше.












