–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ, –Љ–Њ—А—Д–Њ–ї–Њ–≥–Є—П –Є –њ–∞—В–Њ–≥–µ–љ–µ–Ј
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П (–Ф–Э) вАУ –Ї–Њ–Љ–њ–ї–µ–Ї—Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –Є —Б—Г–±–Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤, –Ї–∞–ґ–і—Л–є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –і–Є—Д—Д—Г–Ј–љ—Л–Љ –Є–ї–Є –Њ—З–∞–≥–Њ–≤—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –Є/–Є–ї–Є –∞–≤—В–Њ–љ–Њ–Љ–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –≤ —А–µ–Ј—Г–ї—М—В–∞—В–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є—Е, —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Є –і—А—Г–≥–Є—Е –љ–∞—А—Г—И–µ–љ–Є–є, —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є—Е —Б–∞—Е–∞—А–љ–Њ–Љ—Г –і–Є–∞–±–µ—В—Г (–°–Ф). –°–ї–µ–і—Г–µ—В –Њ—В—З–µ—В–ї–Є–≤–Њ –њ–Њ–љ–Є–Љ–∞—В—М, —З—В–Њ –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ –∞–Ї—Б–Њ–љ–Њ–≤ –Ј–∞—З–∞—Б—В—Г—О –≤–µ–і–µ—В –Ї –љ–µ–є—А–Њ–і–µ–≥–µ–љ–µ—А–∞—Ж–Є–Є вАУ –њ—А–µ–Ї—А–∞—Й–µ–љ–Є—О –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Є–ї–Є –≥–Є–±–µ–ї–Є –љ–µ—А–≤–љ—Л—Е –Ї–ї–µ—В–Њ–Ї, —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–љ—Л—Е –≤ –љ–µ—А–≤–љ—Л—Е —Г–Ј–ї–∞—Е, —Б–њ–Є–љ–љ–Њ–Љ –Є –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Љ–Њ–Ј–≥–µ.–Э–µ–є—А–Њ–њ–∞—В–Є—П вИТ –Њ–і–љ–Њ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В—Л—Е —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф, –Ї–Њ—В–Њ—А–Њ–µ –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Љ–Њ–ґ–µ—В –Ј–∞—В—А–Њ–љ—Г—В—М –ї—О–±–Њ–є –Њ—В–і–µ–ї –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –њ—А–Є—З–µ–Љ –Њ–љ–∞ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –Є –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ, –Є –≤ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–µ —Б –і—А—Г–≥–Є–Љ–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Є–Љ–Є –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є—П–Љ–Є –°–Ф. –Э–∞–Є–±–Њ–ї–µ–µ —В–Є–њ–Є—З–љ–Њ–µ —Б–Њ—З–µ—В–∞–љ–Є–µ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ—В–µ—А–Є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —Б—В–Њ–њ—Л —Б –µ–µ –Є–љ—Д–µ–Ї—Ж–Є–Њ–љ–љ—Л–Љ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Є–ї–Є –Њ–±–ї–Є—В–µ—А–Є—А—Г—О—Й–Є–Љ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–Њ–Љ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є –њ—А–Є–≤–Њ–і–Є—В –Ї —В–Њ–Љ—Г, —З—В–Њ –°–Ф –Њ–Ї–∞–Ј—Л–≤–∞–µ—В—Б—П —Б–∞–Љ–Њ–є —З–∞—Б—В–Њ–є –њ—А–Є—З–Є–љ–Њ–є –љ–µ—В—А–∞–≤–Љ–∞—В–Є—З–µ—Б–Ї–Њ–є –∞–Љ–њ—Г—В–∞—Ж–Є–Є –љ–Њ–≥ –≤ –†–Њ—Б—Б–Є–Є. –І–∞—Б—В–Њ—В–∞ –Ф–Э –њ–Њ–≤—Л—И–∞–µ—В—Б—П —Б —Г–≤–µ–ї–Є—З–µ–љ–Є–µ–Љ –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –°–Ф –Є —Б—В–µ–њ–µ–љ—М—О –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –Ї–∞–Ї –њ—А–Є –°–Ф 1-–≥–Њ —В–Є–њ–∞, —В–∞–Ї –Є –њ—А–Є –°–Ф 2-–≥–Њ —В–Є–њ–∞.
–У–Є—Б—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є –љ–µ–є—А–Њ–њ–∞—В–Є—П —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г–µ—В—Б—П –њ–Њ—В–µ—А–µ–є –±–Њ–ї—М—И–Є—Е –Є –Љ–µ–ї–Ї–Є—Е –Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, —З—В–Њ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П —А–∞–Ј–ї–Є—З–љ–Њ–є —Б—В–µ–њ–µ–љ—М—О –њ–∞—А–∞–љ–Њ–і–∞–ї—М–љ–Њ–є –Є —Б–µ–≥–Љ–µ–љ—В–∞—А–љ–Њ–є –і–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–∞—Ж–Є–Є, –њ—А–Њ–ї–Є—Д–µ—А–∞—Ж–Є–Є —Б–Њ–µ–і–Є–љ–Є—В–µ–ї—М–љ–Њ–є —В–Ї–∞–љ–Є –Є —Г—В–Њ–ї—Й–µ–љ–Є–µ–Љ –Є —А–µ–і—Г–њ–ї–Є–Ї–∞—Ж–Є–µ–є –±–∞–Ј–∞–ї—М–љ–Њ–є –Љ–µ–Љ–±—А–∞–љ—Л –Ї–∞–њ–Є–ї–ї—П—А–Њ–≤ –љ–µ—А–≤–Њ–≤ –Є –Є—Е –Њ–±–ї–Є—В–µ—А–∞—Ж–Є–µ–є. –Ь–µ—Е–∞–љ–Є–Ј–Љ—Л, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ –њ—А–Є –°–Ф –љ–µ–є—А–Њ–њ–∞—В–Є—О, —А–µ–∞–ї–Є–Ј—Г—О—В—Б—П —З–µ—А–µ–Ј –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—О –Є –і—А—Г–≥–Є–µ –Љ–µ—В–∞–±–Њ–ї–Є—З–µ—Б–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞—О—Й–Є–µ –Є–љ—Б—Г–ї–Є–љ–Њ–≤—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М, –Ї–Њ—В–Њ—А—Л–µ –њ—А–Є–≤–Њ–і—П—В –Ї –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ–Њ–ї–Є–Њ–ї—М–љ–Њ–≥–Њ –њ—Г—В–Є –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –≥–ї—О–Ї–Њ–Ј—Л, –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–Є—О –±–µ–ї–Ї–Њ–≤ –Є —Б–љ–Є–ґ–∞—О—В –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї —Н–ї–Є–Љ–Є–љ–∞—Ж–Є–Є –њ—А–Њ–і—Г–Ї—В–Њ–≤ –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П. –Т –і–Њ–њ–Њ–ї–љ–µ–љ–Є–µ –Ї –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є–Є –Є –∞–Ї—В–Є–≤–∞—Ж–Є–Є –њ–Њ–ї–Є–Њ–ї—М–љ–Њ–≥–Њ –њ—Г—В–Є –≤ —А–∞–Ј–≤–Є—В–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є–Є –њ—А–Є–і–∞—О—В –Ј–љ–∞—З–µ–љ–Є–µ –Њ–Ї—Б–Є–і–∞—В–Є–≤–љ–Њ–Љ—Г —Б—В—А–µ—Б—Б—Г, –Є—И–µ–Љ–Є–Є/–≥–Є–њ–Њ–Ї—Б–Є–Є, –љ–∞—А—Г—И–µ–љ–Є—П–Љ —Б–Њ —Б—В–Њ—А–Њ–љ—Л —А–Њ—Б—В–Њ–≤—Л—Е —Д–∞–Ї—В–Њ—А–Њ–≤ –љ–µ—А–≤–Њ–≤ –Є –Є–Љ–Љ—Г–љ–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ.
–Ъ —Д–∞–Ї—В–Њ—А–∞–Љ —А–Є—Б–Ї–∞ –љ–µ–є—А–Њ–њ–∞—В–Є–Є –Њ—В–љ–Њ—Б—П—В –≤–Њ–Ј—А–∞—Б—В, –њ—А–Њ–і–Њ–ї–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М –°–Ф, –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М –≥–ї–Є–Ї–µ–Љ–Є–Є, —Г—А–Њ–≤–µ–љ—М —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –Є —В—А–Є–≥–ї–Є—Ж–µ—А–Є–і–Њ–≤, –∞—А—В–µ—А–Є–∞–ї—М–љ—Г—О –≥–Є–њ–µ—А—В–µ–љ–Ј–Є—О, –Љ–Є–Ї—А–Њ—Б–Њ—Б—Г–і–Є—Б—В—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –Є –Ї—Г—А–µ–љ–Є–µ.
–Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П –Є –њ—А–Є–љ—Ж–Є–њ—Л –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є
–Ф–Э –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А—Г–µ—В—Б—П –Ї–∞–Ї –љ–∞–±–Њ—А —Б–Є–љ–і—А–Њ–Љ–Њ–≤ (—В–∞–±–ї. 1), –Ї–∞–ґ–і—Л–є –Є–Ј –Ї–Њ—В–Њ—А—Л—Е –Є–Љ–µ–µ—В —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Є —В–µ—З–µ–љ–Є–µ. –Я–Њ—Б–Ї–Њ–ї—М–Ї—Г –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Н—В–Є—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤ –њ–µ—А–µ—Б–µ–Ї–∞—О—В—Б—П –Є —З–∞—Б—В–Њ –Њ–і–љ–Њ–≤—А–µ–Љ–µ–љ–љ–Њ –љ–∞–±–ї—О–і–∞—О—В—Б—П —Г –Њ–і–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ, —В–Њ —Н—В–Њ –љ–µ—А–µ–і–Ї–Њ –љ–µ –њ–Њ–Ј–≤–Њ–ї—П–µ—В –Њ–і–љ–Њ–Ј–љ–∞—З–љ–Њ –Ї–ї–∞—Б—Б–Є—Д–Є—Ж–Є—А–Њ–≤–∞—В—М –њ—А–Њ—П–≤–ї–µ–љ–Є–µ –Ф–Э —Г –Ї–Њ–љ–Ї—А–µ—В–љ–Њ–≥–Њ –±–Њ–ї—М–љ–Њ–≥–Њ.
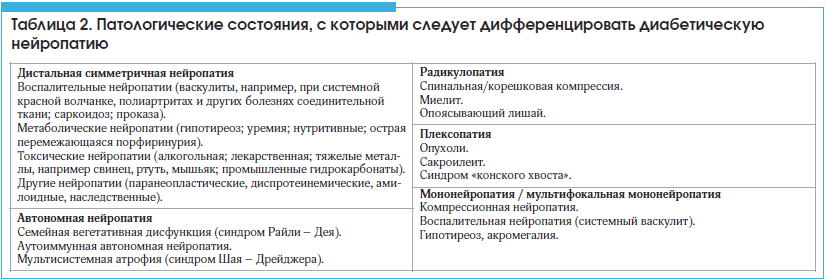
–Ъ–ї–Є–љ–Є–Ї–∞ –Ф–Э –Є–Љ–µ–µ—В —Б—Е–Њ–і—Б—В–≤–Њ —Б –Ї–ї–Є–љ–Є–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є –і—А—Г–≥–Њ–є —Н—В–Є–Њ–ї–Њ–≥–Є–Є (–∞–ї–Ї–Њ–≥–Њ–ї—М–љ–Њ–є, —В–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–є, –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ–Њ–є), –њ–Њ—Н—В–Њ–Љ—Г –µ–µ –і–Є–∞–≥–љ–Њ–Ј —Г—Б—В–∞–љ–∞–≤–ї–Є–≤–∞—О—В –Љ–µ—В–Њ–і–Њ–Љ –Є—Б–Ї–ї—О—З–µ–љ–Є—П (—В–∞–±–ї. 2).
–Т—Л–і–µ–ї—П—О—В 5 –Ї—А–Є—В–µ—А–Є–µ–≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ф–Я–Э–Я:
1) –љ–∞–ї–Є—З–Є–µ –°–Ф;
2) –і–ї–Є—В–µ–ї—М–љ–∞—П –≥–Є–њ–µ—А–≥–ї–Є–Ї–µ–Љ–Є—П вАУ –Њ–±—Л—З–љ–Њ –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –ї–µ—В;
3) –њ—А–Є–Ј–љ–∞–Ї–Є –і–Є—Б—В–∞–ї—М–љ–Њ–є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–є, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–µ–љ—Б–Њ—А–љ–Њ–є –Я–Э–Я, –љ–∞–Є–±–Њ–ї–µ–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ–є –≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е;
4) –Є—Б–Ї–ї—О—З–µ–љ—Л –і—А—Г–≥–Є–µ, –Ї—А–Њ–Љ–µ –°–Ф, –њ—А–Є—З–Є–љ—Л –Я–Э–Я;
5) –њ—А–Є–Ј–љ–∞–Ї–Є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф (—А–µ—В–Є–љ–Њ–њ–∞—В–Є—П, –љ–µ—Д—А–Њ–њ–∞—В–Є—П –Є –і—А.).
–Э–Є –Њ–і–Є–љ –Є–Ј –Ї—А–Є—В–µ—А–Є–µ–≤ –љ–µ —П–≤–ї—П–µ—В—Б—П –∞–±—Б–Њ–ї—О—В–љ—Л–Љ, –Њ–і–љ–∞–Ї–Њ –љ–∞–ї–Є—З–Є–µ 2-—Е –Є–Ј 5 –Ї—А–Є—В–µ—А–Є–µ–≤ –њ–Њ–≤—Л—И–∞–µ—В –≤–µ—А–Њ—П—В–љ–Њ—Б—В—М –і–Є–∞–≥–љ–Њ–Ј–∞ –Ф–Я–Э–Я.
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Ф–Э –≤–Ї–ї—О—З–∞—О—В –Њ—Ж–µ–љ–Ї—Г 5 –њ–∞—А–∞–Љ–µ—В—А–Њ–≤:
1) —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П: –Њ–љ–µ–Љ–µ–љ–Є–µ, –±–Њ–ї–Є, –њ–∞—А–µ—Б—В–µ–Ј–Є–Є, —Б–ї–∞–±–Њ—Б—В—М, –Ј—П–±–Ї–Њ—Б—В—М –Є –і—А.;
2) –Њ–±—К–µ–Ї—В–Є–≤–љ—Л–µ –њ—А–Є–Ј–љ–∞–Ї–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤ (—З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ—Л—Е, –і–≤–Є–≥–∞—В–µ–ї—М–љ—Л—Е, –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л—Е) вИТ –≤—Л—П–≤–ї—П—О—В—Б—П –≤ —Е–Њ–і–µ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П;
3) –і–∞–љ–љ—Л–µ –Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ —Б–µ–љ—Б–Њ—А–љ–Њ–≥–Њ —В–µ—Б—В–Є—А–Њ–≤–∞–љ–Є—П;
4) –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ —В–µ—Б—В—Л;
5) –і–∞–љ–љ—Л–µ —Н–ї–µ–Ї—В—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–≥–Њ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П (—Н–ї–µ–Ї—В—А–Њ–љ–µ–є—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є—П (–≠–Э–Ь–У), —А–µ–≥–Є—Б—В—А–∞—Ж–Є—П —Б–Њ–Љ–∞—В–Њ—Б–µ–љ—Б–Њ—А–љ—Л—Е –≤—Л–Ј–≤–∞–љ–љ—Л—Е –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–≤ (–°–°–Т–Я)).
–≠–Э–Ь–У —Б—В–Њ–Є—В —Б—А–µ–і–Є –Љ–µ—В–Њ–і–Њ–≤ –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–Є –Ф–Э –љ–∞ –њ–µ—А–≤–Њ–Љ –Љ–µ—Б—В–µ –њ–Њ –і–Њ—Б—В—Г–њ–љ–Њ—Б—В–Є –Є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В–Є. –°–љ–Є–ґ–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–Є –њ—А–Њ–≤–µ–і–µ–љ–Є—П –Є–Љ–њ—Г–ї—М—Б–∞ –њ–Њ –љ–µ—А–≤—Г –љ–µ—А–µ–і–Ї–Њ —А–µ–≥–Є—Б—В—А–Є—А—Г–µ—В—Б—П –≤ –њ–µ—А–Є–Њ–і —Г—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –і–Є–∞–≥–љ–Њ–Ј–∞ –°–Ф, –Ј–∞—В–µ–Љ, –њ–Њ –Љ–µ—А–µ –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –љ–∞–±–ї—О–і–∞–µ—В—Б—П –њ—А–Њ–≥—А–µ–і–Є–µ–љ—В–љ–Њ–µ –µ–µ —Б–љ–Є–ґ–µ–љ–Є–µ. –Т –і–Є–∞–≥–љ–Њ—Б—В–Є–Ї–µ –Р–Я–Э–Я –±–Њ–ї—М—И–Њ–є –Є–љ—Д–Њ—А–Љ–∞—В–Є–≤–љ–Њ—Б—В—М—О –Њ–±–ї–∞–і–∞–µ—В –Є–≥–Њ–ї—М—З–∞—В–∞—П —Н–ї–µ–Ї—В—А–Њ–Љ–Є–Њ–≥—А–∞—Д–Є—П: –≤ –њ–Њ—А–∞–ґ–µ–љ–љ—Л—Е –Љ—Л—И—Ж–∞—Е –≤—Л—П–≤–ї—П—О—В—Б—П –њ–Њ—В–µ–љ—Ж–Є–∞–ї—Л —Д–Є–±—А–Є–ї–ї—П—Ж–Є–є, –Њ–±–љ–∞—А—Г–ґ–Є–≤–∞–µ—В—Б—П –љ–µ–±–Њ–ї—М—И–Њ–µ –Є–Ј–Љ–µ–љ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і –Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–≤ –і–µ–є—Б—В–≤–Є—П.
–Т—Л–і–µ–ї—П—О—В —Б–ї–µ–і—Г—О—Й–Є–µ –љ–µ–є—А–Њ—Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б—В–∞–і–Є–Є –Є–Ј–Љ–µ–љ–µ–љ–Є—П –љ–µ–є—А–Њ–Љ–Њ—В–Њ—А–љ–Њ–≥–Њ –∞–њ–њ–∞—А–∞—В–∞ –њ—А–Є –і–Є—Б—В–∞–ї—М–љ–Њ–є –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є–Є (–Ф–Я–Э–Я).
1. –Я–Њ—П–≤–ї–µ–љ–Є–µ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–≤ —Д–∞—Б—Ж–Є–Ї—Г–ї—П—Ж–Є–є –≤ —Б–Њ—Б—В–Њ—П–љ–Є–Є –њ–Њ–Ї–Њ—П –Є –њ—А–Є –Є–Ј–Љ–µ–љ–µ–љ–Є–Є —В–Њ–љ—Г—Б–∞. –°–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –±–Є–Њ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–Є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–Љ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–Є –≤ –љ–µ–Ї–Њ—В–Њ—А—Л—Е –Љ—Л—И—Ж–∞—Е –і–Є—Б—В–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –љ–Є–ґ–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є.
2. –Ф–Є—Б—В–∞–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –±–Є–Њ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –Љ—Л—И—Ж. –Ш–Ј–Љ–µ–љ–µ–љ–Є—П —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П—О—В—Б—П –љ–∞ –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –≥—А—Г–њ–њ –Љ—Л—И—Ж –і–Є—Б—В–∞–ї—М–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –љ–Є–ґ–љ–Є—Е, –Ј–∞—В–µ–Љ –≤–µ—А—Е–љ–Є—Е –Ї–Њ–љ–µ—З–љ–Њ—Б—В–µ–є.
3. –Я–Њ—П–≤–ї–µ–љ–Є–µ –њ—А–Є –њ—А–Њ–Є–Ј–≤–Њ–ї—М–љ–Њ–Љ —Б–Њ–Ї—А–∞—Й–µ–љ–Є–Є —Г—А–µ–ґ–µ–љ–Є—П —З–∞—Б—В–Њ—В—Л –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–≤ –≤ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –≥—А—Г–њ–њ–∞—Е –Љ—Л—И—Ж.
4. –Ч–љ–∞—З–Є—В–µ–ї—М–љ–Њ–µ —Б–љ–Є–ґ–µ–љ–Є–µ –∞–Љ–њ–ї–Є—В—Г–і—Л –Є —Г—А–µ–ґ–µ–љ–Є–µ —З–∞—Б—В–Њ—В—Л –Ї–Њ–ї–µ–±–∞–љ–Є–є, –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–Њ–≤ –і–µ–є—Б—В–≤–Є—П.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П –Ф–Є—Б—В–∞–ї—М–љ–∞—П —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П –њ–Њ–ї–Є–љ–µ–є—А–Њ–њ–∞—В–Є—П
–°–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Б–µ–љ—Б–Њ—А–љ–∞—П (–Є–ї–Є —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–∞—П) –і–Є—Б—В–∞–ї—М–љ–∞—П –Ф–Я–Э–Я вАУ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ –≤—Б—В—А–µ—З–∞—О—Й–∞—П—Б—П (–±–Њ–ї–µ–µ 30%) —Д–Њ—А–Љ–∞ –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є –°–Ф. –Т—Л–і–µ–ї—П—О—В 3 —Б—В–∞–і–Є–Є (—В–∞–±–ї. 3) –Є 2 –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е –≤–∞—А–Є–∞–љ—В–∞ –Ф–Я–Э–Я:вАУ –Њ—Б—В—А–∞—П –±–Њ–ї–µ–≤–∞—П —Б–µ–љ—Б–Њ—А–љ–∞—П;
вАУ —Е—А–Њ–љ–Є—З–µ—Б–Ї–∞—П —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–∞—П.
–Ю—Б—В—А–∞—П –±–Њ–ї–µ–≤–∞—П —Б–µ–љ—Б–Њ—А–љ–∞—П –і–Є—Б—В–∞–ї—М–љ–∞—П
—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П –Ф–Я–Э–Я

–≠—В–∞ —Д–Њ—А–Љ–∞ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –Њ—Б—В—А–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–Љ —Б–µ–љ—Б–Њ—А–љ—Л–Љ –і–µ—Д–µ–Ї—В–Њ–Љ –≤ —Д–Њ—А–Љ–µ –і–Є—Б—В–∞–ї—М–љ—Л—Е –њ–∞—А–µ—Б—В–µ–Ј–Є–є, –≥–Є–њ–µ—А–µ—Б—В–µ–Ј–Є–є, –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–є, –∞ —В–∞–Ї–ґ–µ —З—Г–≤—Б—В–≤–∞ –ґ–ґ–µ–љ–Є—П, –њ—А–Њ—Б—В—А–µ–ї–Њ–≤, —А–µ–ґ—Г—Й–Є—Е –±–Њ–ї–µ–є –≤ –Ї–Њ–љ–µ—З–љ–Њ—Б—В—П—Е —Б –Њ—В—З–µ—В–ї–Є–≤—Л–Љ –≤–µ–≥–µ—В–∞—В–Є–≤–љ—Л–Љ —Е–∞—А–∞–Ї—В–µ—А–Њ–Љ. –С–Њ–ї–µ–≤—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П, –Ї–∞–Ї –њ—А–∞–≤–Є–ї–Њ, —Г—Б–Є–ї–Є–≤–∞—О—В—Б—П –≤ –њ–Њ–Ї–Њ–µ, –≤ –љ–Њ—З–љ–Њ–µ –≤—А–µ–Љ—П –Є —Г–Љ–µ–љ—М—И–∞—О—В—Б—П –і–љ–µ–Љ –њ—А–Є –∞–Ї—В–Є–≤–љ–Њ–є –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є. –Э–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї–Є (–ї–µ–≥–Ї–Њ–µ –њ—А–Є–Ї–Њ—Б–љ–Њ–≤–µ–љ–Є–µ –Њ–і–µ–ґ–і—Л, –њ–Њ—Б—В–µ–ї—М–љ–Њ–≥–Њ –±–µ–ї—М—П –Ї –Ї–Њ–ґ–µ) –Љ–Њ–≥—Г—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ —Г—Б–Є–ї–Є–≤–∞—В—М –±–Њ–ї—М, –≤ —В–Њ –≤—А–µ–Љ—П –Ї–∞–Ї –±–Њ–ї–µ–µ –≥—А—Г–±–Њ–µ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–µ –Є –њ–∞–ї—М–њ–∞—Ж–Є—П –љ–µ –≤—Л–Ј—Л–≤–∞—О—В –љ–µ–њ—А–Є—П—В–љ—Л—Е –Њ—Й—Г—Й–µ–љ–Є–є. –Т–Њ–Ј–Љ–Њ–ґ–љ—Л –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Ї–Њ–ґ–љ–Њ–є —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л, —Ж–≤–µ—В–∞ –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤, –ї–Њ–Ї–∞–ї—М–љ—Л–є –≥–Є–њ–µ—А–≥–Є–і—А–Њ–Ј. –°—Г—Е–Њ–ґ–Є–ї—М–љ—Л–µ —А–µ—Д–ї–µ–Ї—Б—Л –Є –≥–ї—Г–±–Њ–Ї–Є–µ –≤–Є–і—Л —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –Њ—Б—В–∞—О—В—Б—П –Є–љ—В–∞–Ї—В–љ—Л–Љ–Є. –†–∞–Ј–≤–Є—В–Є–µ —В–∞–Ї–Њ–є —Д–Њ—А–Љ—Л –Ф–Я–Э–Я —Б–≤—П–Ј–∞–љ–Њ —Б –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є–µ–Љ —В–Њ–љ–Ї–Є—Е –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –°вАУ–≤–Њ–ї–Њ–Ї–Њ–љ.
–•—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –і–Є—Б—В–∞–ї—М–љ–∞—П —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–∞—П –Ф–Я–Э–Я
–Т —В–Є–њ–Є—З–љ—Л—Е —Б–ї—Г—З–∞—П—Е —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –Љ–µ–і–ї–µ–љ–љ–Њ. –Э–∞—А—Г—И–µ–љ–Є–µ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –њ—А–Є –љ–µ–є –Љ–Њ–ґ–µ—В —Б–Њ—З–µ—В–∞—В—М—Б—П —Б —Г–Љ–µ—А–µ–љ–љ–Њ–є
–Њ–љ–µ–Љ–µ–љ–Є–µ, –њ–∞—А–µ—Б—В–µ–Ј–Є–Є, –Ј—П–±–Ї–Њ—Б—В—М, –ї–Њ–Ї–∞–ї–Є–Ј–Њ–≤–∞–љ–љ—Л–µ –≤ –њ–∞–ї—М—Ж–∞—Е —Б—В–Њ–њ, —А–∞—Б–њ—А–Њ—Б—В—А–∞–љ—П—О—Й–Є–µ—Б—П –љ–∞ –≤—Б—О —Б—В–Њ–њ—Г, –љ–Є–ґ–љ—О—О —В—А–µ—В—М –≥–Њ–ї–µ–љ–µ–є, –њ–Њ–Ј–ґ–µ вАУ –љ–∞ –Ї–Є—Б—В–Є —А—Г–Ї. –Э–∞–±–ї—О–і–∞–µ—В—Б—П —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–µ –љ–∞—А—Г—И–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–є, —В–µ–Љ–њ–µ—А–∞—В—Г—А–љ–Њ–є, —В–∞–Ї—В–Є–ї—М–љ–Њ–є –Є –≥–ї—Г–±–Њ–Ї–Њ–є —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є –≤ –Ј–Њ–љ–µ ¬Ђ–љ–Њ—Б–Ї–Њ–≤¬ї –Є ¬Ђ–њ–µ—А—З–∞—В–Њ–Ї¬ї; –≤ —В—П–ґ–µ–ї—Л—Е —Б–ї—Г—З–∞—П—Е –њ–Њ—А–∞–ґ–∞—О—В—Б—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є–µ –љ–µ—А–≤—Л —В—Г–ї–Њ–≤–Є—Й–∞, —З—В–Њ –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≥–Є–њ–µ—Б—В–µ–Ј–Є–µ–є –Ї–Њ–ґ–Є –≥—А—Г–і–Є –Є –ґ–Є–≤–Њ—В–∞. –°–љ–Є–ґ–∞—О—В—Б—П, –∞ –Ј–∞—В–µ–Љ —Г–≥–∞—Б–∞—О—В –∞—Е–Є–ї–ї–Њ–≤—Л —А–µ—Д–ї–µ–Ї—Б—Л, –Љ–Њ–≥—Г—В –≤—Л—П–≤–ї—П—В—М—Б—П –њ—А–Є–Ј–љ–∞–Ї–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–≤—А–Њ–њ–∞—В–Є–Є –Ї–Њ–љ—Ж–µ–≤—Л—Е –≤–µ—В–≤–µ–є –±–Њ–ї—М—И–µ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –Є–ї–Є –Љ–∞–ї–Њ–±–µ—А—Ж–Њ–≤–Њ–≥–Њ –љ–µ—А–≤–Њ–≤: –∞—В—А–Њ—Д–Є—П –Љ—Л—И—Ж, —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ ¬Ђ–Њ—В–≤–Є—Б–∞—О—Й–µ–є¬ї –Є–ї–Є ¬Ђ–Ї–Њ–≥—В–Є—Б—В–Њ–є¬ї —Б—В–Њ–њ—Л.
–°–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –њ—А–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Ф–Я–Э–Я –љ–µ—А–µ–і–Ї–Њ —Б–Њ—З–µ—В–∞—О—В—Б—П —Б —В—А–Њ—Д–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–Љ–Є —А–∞–Ј–≤–Є—В–Є–µ–Љ –∞–≤—В–Њ–љ–Њ–Љ–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є: —Б—Г—Е–Њ—Б—В—М—О –Є –Є—Б—В–Њ–љ—З–µ–љ–Є–µ–Љ, —А–∞—Б—В—А–µ—Б–Ї–Є–≤–∞–љ–Є–µ–Љ –Ї–Њ–ґ–Є, –≤–∞–Ј–Њ–Љ–Њ—В–Њ—А–љ—Л–Љ–Є —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞–Љ–Є, –Є–Ј–Љ–µ–љ–µ–љ–Є–µ–Љ —В–µ–Љ–њ–µ—А–∞—В—Г—А—Л –Є —Ж–≤–µ—В–∞ –Ї–Њ–ґ–љ—Л—Е –њ–Њ–Ї—А–Њ–≤–Њ–≤, –љ–∞–Є–±–Њ–ї–µ–µ —А–∞–љ–Њ –њ—А–Њ—П–≤–ї—П—О—Й–Є–Љ–Є—Б—П –≤ –Њ–±–ї–∞—Б—В–Є —Б—В–Њ–њ –Є –љ–∞–Є–±–Њ–ї–µ–µ —П—А–Ї–Њ вАУ –њ—А–Є —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л.
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Ф–Я–Э–Я –≤—Л—А–∞–ґ–µ–љ—Л —Б–ї–∞–±–Њ, –Њ–≥—А–∞–љ–Є—З–µ–љ—Л —З—Г–≤—Б—В–≤–Њ–Љ –њ—А–µ—Е–Њ–і—П—Й–µ–≥–Њ –Њ–љ–µ–Љ–µ–љ–Є—П –Є –њ–∞—А–µ—Б—В–µ–Ј–Є—П–Љ–Є —Б—В–Њ–њ. –†–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В–Є —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –Є—Б–њ–Њ–і–≤–Њ–ї—М, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –±–Њ–ї—М–љ—Л–µ –љ–µ –Њ–±—А–∞—Й–∞—О—В –≤–љ–Є–Љ–∞–љ–Є—П –љ–∞ –±–µ–Ј–±–Њ–ї–µ–Ј–љ–µ–љ–љ—Л–µ –њ–Њ—В–µ—А—В–Њ—Б—В–Є, –Њ–њ—А–µ–ї–Њ—Б—В–Є, —В—А–∞–≤–Љ—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В —Б—В–∞—В—М –Њ—Б–љ–Њ–≤–Њ–є —А–∞–Ј–≤–Є—В–Є—П —В—А–Њ—Д–Є—З–µ—Б–Ї–Є—Е —П–Ј–≤ –Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є —Б—В–Њ–њ—Л.
–Т —В—П–ґ–µ–ї—Л—Е —Б–ї—Г—З–∞—П—Е –њ–∞—А–µ—Б—В–µ–Ј–Є–Є –Є–Љ–µ—О—В —Е–∞—А–∞–Ї—В–µ—А –ґ–ґ–µ–љ–Є—П, –њ–ї–Њ—Е–Њ –ї–Њ–Ї–∞–ї–Є–Ј—Г–µ–Љ—Л—Е, –њ–Њ—Б—В–Њ—П–љ–љ—Л—Е, –Є–љ—В–µ–љ—Б–Є–≤–љ—Л—Е –±–Њ–ї–µ–є, —Г—Б–Є–ї–Є–≤–∞—О—Й–Є—Е—Б—П –њ–Њ –љ–Њ—З–∞–Љ. –С–Њ–ї–µ–≤—Л–µ –Њ—Й—Г—Й–µ–љ–Є—П –Є–љ–Њ–≥–і–∞ –љ–Њ—Б—П—В –≥–Є–њ–µ—А–њ–∞—В–Є—З–µ—Б–Ї–Є–є –Њ—В—В–µ–љ–Њ–Ї –Є –Ј–∞—З–∞—Б—В—Г—О —А–µ–Ј–Є—Б—В–µ–љ—В–љ—Л –Ї –ї–µ—З–µ–љ–Є—О. –Я—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ –њ–Њ–і–Њ–±–љ–Њ–≥–Њ —Е–∞—А–∞–Ї—В–µ—А–∞ –Њ–њ—А–µ–і–µ–ї—П–µ—В—Б—П –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Б–Є–Љ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л. –Э–µ—А–µ–і–Ї–Њ –љ–∞–±–ї—О–і–∞–µ—В—Б—П —Б–Њ—З–µ—В–∞–љ–Є–µ —Б–Є–Љ–њ–∞—В–∞–ї–≥–Є–є —Б –љ–µ–≤—А–Њ–Ј–Њ–њ–Њ–і–Њ–±–љ—Л–Љ–Є, –њ—Б–Є—Е–Њ–њ–∞—В–Њ–њ–Њ–і–Њ–±–љ—Л–Љ–Є –Є –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є.
–Р–≤—В–Њ–љ–Њ–Љ–љ–∞—П (–≤–Є—Б—Ж–µ—А–∞–ї—М–љ–∞—П) –љ–µ–є—А–Њ–њ–∞—В–Є—П
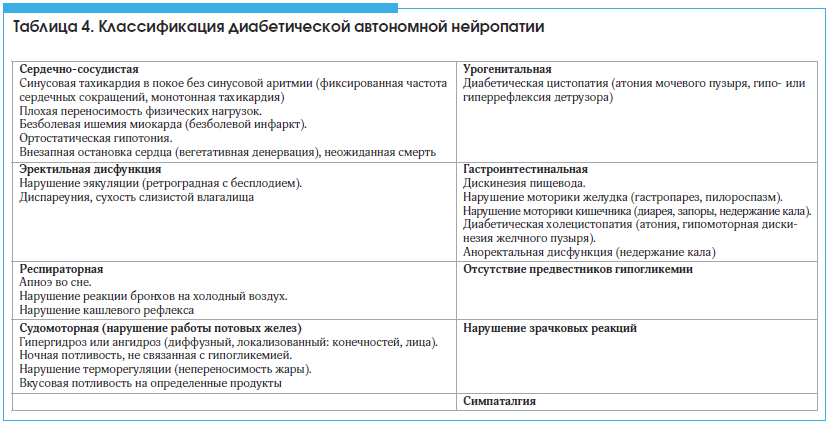
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –∞–≤—В–Њ–љ–Њ–Љ–љ–∞—П (–≤–Є—Б—Ж–µ—А–∞–ї—М–љ–∞—П, –Є–ї–Є –≤–µ–≥–µ—В–∞—В–Є–≤–љ–∞—П) –љ–µ–є—А–Њ–њ–∞—В–Є—П (–Ф–Р–Э) –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–∞ –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ —Ж–µ–љ—В—А–∞–ї—М–љ–Њ–≥–Њ –Є/–Є–ї–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ –Њ—В–і–µ–ї–Њ–≤ –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, –≤–Њ –Љ–љ–Њ–≥–Њ–Љ –Њ–њ—А–µ–і–µ–ї—П–µ—В —В–µ—З–µ–љ–Є–µ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П –Є —Б—В—А—Г–Ї—В—Г—А—Г —Б–Љ–µ—А—В–љ–Њ—Б—В–Є –њ—А–Є –°–Ф. –І–∞—Б—В–Њ—В–∞ –µ–µ —А–∞–Ј–≤–Є—В–Є—П –і–Њ—Б—В–Є–≥–∞–µ—В 40%, –∞ –њ—А–Є –і–ї–Є—В–µ–ї—М–љ–Њ—Б—В–Є –°–Ф –±–Њ–ї–µ–µ 10 –ї–µ—В –њ—А–µ–≤—Л—И–∞–µ—В 65%.–Т–µ–≥–µ—В–∞—В–Є–≤–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П, –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–µ –њ—А–Є –Ф–Р–Э, —А–∞–Ј–і–µ–ї—П—О—В—Б—П –љ–∞ –Њ—А–≥–∞–љ–Њ—Б–њ–µ—Ж–Є—Д–Є—З–µ—Б–Ї–Є–µ –Є —Б–Є—Б—В–µ–Љ–љ—Л–µ. –Т –њ—А–µ–і–µ–ї–∞—Е —Н—В–Є—Е –≥—А—Г–њ–њ –Љ–Њ–ґ–љ–Њ –≤—Л–і–µ–ї–Є—В—М —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —Д–Њ—А–Љ—Л –Ф–Р–Э, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –њ—А–Њ—П–≤–ї—П—В—М—Б—П –Ї–∞–Ї –Є–Ј–Њ–ї–Є—А–Њ–≤–∞–љ–љ–Њ, —В–∞–Ї –Є –≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П—Е (—В–∞–±–ї. 4).
–Р—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П
–Р—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П (–Р–Я–Э–Я) вАУ –Њ–і–љ–Њ –Є–Ј –њ—А–Њ—П–≤–ї–µ–љ–Є–є –Ф–Э, –≤—Б—В—А–µ—З–∞—О—Й–µ–µ—Б—П –љ–µ —З–∞—Й–µ —З–µ–Љ —Г 0,1вАУ0,3% –±–Њ–ї—М–љ—Л—Е –°–Ф, –Њ–±—Л—З–љ–Њ –≤ –≤–Њ–Ј—А–∞—Б—В–µ 50вАУ60 –ї–µ—В. –Я–µ—А–≤–Њ–љ–∞—З–∞–ї—М–љ–Њ –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–µ –Њ–±–Њ–Ј–љ–∞—З–∞–ї–Њ—Б—М –Ї–∞–Ї –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –∞–Љ–Є–Њ—В—А–Њ—Д–Є—П, –≤ –њ–Њ—Б–ї–µ–і—Г—О—Й–Є—Е –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П—Е вАУ –Ї–∞–Ї –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –∞–Љ–Є–Њ—В—А–Њ—Д–Є—П –Є –њ—А–Њ–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П. –Я—А–µ–і—А–∞—Б–њ–Њ–ї–∞–≥–∞—О—Й–Є–Љ–Є —Д–∞–Ї—В–Њ—А–∞–Љ–Є —П–≤–ї—П—О—В—Б—П –Њ—Б—В–µ–Њ—Е–Њ–љ–і—А–Њ–Ј, –і–µ—Д–Њ—А–Љ–Є—А—Г—О—Й–Є–є —Б–њ–Њ–љ–і–Є–ї–µ–Ј, –њ—А–Њ–ї–∞–±–Є—А–Њ–≤–∞–љ–Є–µ –Љ–µ–ґ–њ–Њ–Ј–≤–Њ–љ–Ї–Њ–≤—Л—Е –і–Є—Б–Ї–Њ–≤, —В—А–∞–≤–Љ—Л.–Р–Я–Э–Я –њ—А–Њ—П–≤–ї—П–µ—В—Б—П –≤–љ–µ–Ј–∞–њ–љ–Њ –≤–Њ–Ј–љ–Є–Ї–∞—О—Й–Є–Љ–Є –∞–Љ–Є–Њ—В—А–Њ—Д–Є—П–Љ–Є —З–∞—Й–µ —В–∞–Ј–Њ–≤–Њ–≥–Њ, —А–µ–ґ–µ вАУ –њ–ї–µ—З–µ–≤–Њ–≥–Њ –њ–Њ—П—Б–∞. –Т —В–Є–њ–Є—З–љ—Л—Е —Б–ї—Г—З–∞—П—Е –≤–љ–∞—З–∞–ї–µ –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –Њ—Б—В—А–∞—П –Є–ї–Є –њ–Њ–і–Њ—Б—В—А–∞—П –±–Њ–ї—М –њ–Њ—П—Б–љ–Є—З–љ–Њ-–Ї—А–µ—Б—В—Ж–Њ–≤–Њ–є –ї–Њ–Ї–∞–ї–Є–Ј–∞—Ж–Є–Є, –Є—А—А–∞–і–Є–Є—А—Г—О—Й–∞—П –≤ –љ–Њ–≥—Г, –Ј–∞—В–µ–Љ –њ—А–Є—Б–Њ–µ–і–Є–љ—П—О—В—Б—П —Б–ї–∞–±–Њ—Б—В—М –Є –∞—В—А–Њ—Д–Є—П –Љ—Л—И—Ж —В–∞–Ј–Њ–≤–Њ–≥–Њ –њ–Њ—П—Б–∞ –Є –±–µ–і—А–∞. –Я–Њ—А–∞–ґ–µ–љ–Є–µ –њ–Њ–і–≤–Ј–і–Њ—И–љ–Њ-–њ–Њ—П—Б–љ–Є—З–љ–Њ–є –Љ—Л—И—Ж—Л –Є —З–µ—В—Л—А–µ—Е–≥–ї–∞–≤–Њ–є –Љ—Л—И—Ж—Л –±–µ–і—А–∞ –њ—А–Є–≤–Њ–і–Є—В –Ї —Б–ї–∞–±–Њ—Б—В–Є —Б–≥–Є–±–∞–љ–Є—П –±–µ–і—А–∞, –љ–µ—Б—В–∞–±–Є–ї—М–љ–Њ—Б—В–Є –≤ –Ї–Њ–ї–µ–љ–љ–Њ–Љ —Б—Г—Б—В–∞–≤–µ, —А–µ–і–Ї–Њ –≤–Њ–≤–ї–µ–Ї–∞—О—В—Б—П —П–≥–Њ–і–Є—З–љ—Л–µ –Љ—Л—И—Ж—Л, –∞–і–і—Г–Ї—В–Њ—А—Л –±–µ–і—А–∞ –Є –њ–µ—А–Њ–љ–µ–∞–ї—М–љ–∞—П –≥—А—Г–њ–њ–∞. –†–µ—Д–ї–µ–Ї—В–Њ—А–љ—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ –њ—А–Њ—П–≤–ї—П—О—В—Б—П —Г–≥–љ–µ—В–µ–љ–Є–µ–Љ –Є–ї–Є –≤—Л–њ–∞–і–µ–љ–Є–µ–Љ –Ї–Њ–ї–µ–љ–љ–Њ–≥–Њ —А–µ—Д–ї–µ–Ї—Б–∞ –њ—А–Є —Б–Њ—Е—А–∞–љ–љ–Њ—Б—В–Є –Є–ї–Є –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ–Љ —Б–љ–Є–ґ–µ–љ–Є–Є –∞—Е–Є–ї–ї–Њ–≤–∞. –°–µ–љ—Б–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П –њ—А–Њ—П–≤–ї—П—О—В—Б—П –ґ–ґ–µ–љ–Є–µ–Љ, –Њ—Й—Г—Й–µ–љ–Є–µ–Љ ¬Ђ–Љ—Г—А–∞—И–µ–Ї¬ї, –±–Њ–ї—П–Љ–Є –≤ –Њ–±–ї–∞—Б—В–Є –Ї–Њ–ґ–Є –±–µ–і—А–∞, –≥–Њ–ї–µ–љ–Є –Є —Б—В–Њ–њ—Л, –љ–µ —Б–≤—П–Ј–∞–љ–љ—Л–Љ–Є —Б –і–≤–Є–ґ–µ–љ–Є—П–Љ–Є –Є —З–∞—Й–µ –њ–Њ—П–≤–ї—П—О—Й–Є–Љ–Є—Б—П –љ–Њ—З—М—О. –Ъ–∞–Ї –њ—А–∞–≤–Є–ї–Њ, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –њ—А–Њ—Ж–µ—Б—Б –Њ—Б—В–∞–µ—В—Б—П –∞—Б–Є–Љ–Љ–µ—В—А–Є—З–љ—Л–Љ. –Ы–µ—З–µ–љ–Є–µ –Р–Я–Э–Я –і–ї–Є—В–µ–ї—М–љ–Њ–µ вАУ –і–Њ 1,5вАУ2-—Е –ї–µ—В, —Б—В–µ–њ–µ–љ—М –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—П –љ–∞—А—Г—И–µ–љ–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –љ–∞—Е–Њ–і–Є—В—Б—П –≤ –њ—А—П–Љ–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В –Ї–Њ–Љ–њ–µ–љ—Б–∞—Ж–Є–Є –°–Ф.
–Ь–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є—П
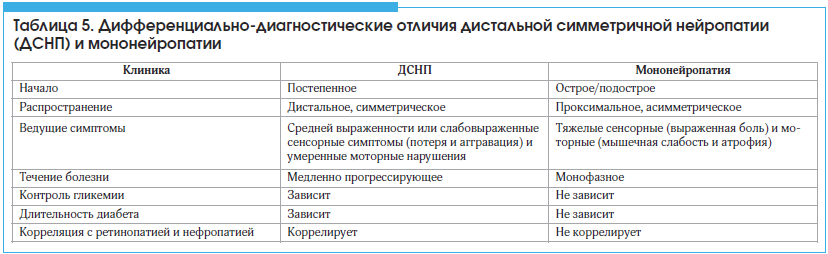
–Ф–Є–∞–±–µ—В–Є—З–µ—Б–Ї–∞—П –Љ–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є—П вАУ –њ–Њ—А–∞–ґ–µ–љ–Є–µ –Њ—В–і–µ–ї—М–љ—Л—Е –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –љ–µ—А–≤–Њ–≤, –њ—А–Є—З–Є–љ–Њ–є –Ї–Њ—В–Њ—А–Њ–≥–Њ —З–∞—Й–µ –≤—Б–µ–≥–Њ —П–≤–ї—П–µ—В—Б—П —А–∞–Ј–≤–Є—В–Є–µ –Њ—З–∞–≥–∞ –Є—И–µ–Љ–Є–Є (—А–µ–ґ–µ вАУ –Љ–Є–Ї—А–Њ–≥–µ–Љ–Њ—А—А–∞–≥–Є–Є) –≤ —Б—В–≤–Њ–ї–µ –љ–µ—А–≤–∞ –Є–ї–Є –µ–≥–Њ —Г—Й–µ–Љ–ї–µ–љ–Є–µ –≤ —Д–Є–Ј–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є —Г–Ј–Ї–Є—Е –њ—А–Њ—Б—В—А–∞–љ—Б—В–≤–∞—Е (¬Ђ–Ї–∞–њ–Ї–∞–љ–љ–∞—П¬ї, —В—Г–љ–љ–µ–ї—М–љ–∞—П –Љ–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є—П).–Я–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–∞—П –Ф–Э –Љ–Њ–ґ–µ—В –њ—А–Њ—П–≤–ї—П—В—М—Б—П –њ–Њ—А–∞–ґ–µ–љ–Є–µ–Љ –Њ—В–і–µ–ї—М–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ –Є–ї–Є –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –Є—Е –≥—А—Г–њ–њ, –Ї—А–∞–љ–Є–∞–ї—М–љ—Л—Е –љ–µ—А–≤–Њ–≤, –Ј–Њ–љ –±—А–∞—Е–Є–∞–ї—М–љ—Л—Е –Є–ї–Є –ї—О–Љ–±–Њ—Б–∞–Ї—А–∞–ї—М–љ—Л—Е —Б–њ–ї–µ—В–µ–љ–Є–є (–њ–ї–µ–Ї—Б–Њ–њ–∞—В–Є—П) –Є–ї–Є –љ–µ—А–≤–љ—Л—Е –Ї–Њ—А–µ—И–Ї–Њ–≤ (—А–∞–і–Є–Ї—Г–ї–Њ–њ–∞—В–Є—П), –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –љ–µ–Њ–ґ–Є–і–∞–љ–љ–Њ, –Њ—Б—В—А–Њ –Є –Њ–±—Л—З–љ–Њ –њ—А–Њ—Е–Њ–і–Є—В —Б–∞–Љ–Њ—Б—В–Њ—П—В–µ–ї—М–љ–Њ. –Ґ–∞–Ї–Є–µ –љ–∞—А—Г—И–µ–љ–Є—П –Њ–±—Л—З–љ–Њ –љ–∞–Ј—Л–≤–∞—О—В –Љ–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є–µ–є, –Є–ї–Є –Љ—Г–ї—М—В–Є–њ–ї–µ–Ї—Б–љ–Њ–є –Љ–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є–µ–є (—Б–Є–љ–Њ–љ–Є–Љ: —Д–Њ–Ї–∞–ї—М–љ–∞—П –Є–ї–Є –Љ—Г–ї—М—В–Є—Д–Њ–Ї–∞–ї—М–љ–∞—П). –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–µ —А–∞–Ј–ї–Є—З–Є—П –≤ –њ—А–Њ—П–≤–ї–µ–љ–Є—П—Е –і–Є—Б—В–∞–ї—М–љ–Њ–є —Б–Є–Љ–Љ–µ—В—А–Є—З–љ–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є –Є –Љ–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є–Є –њ—А–µ–і—Б—В–∞–≤–ї–µ–љ—Л –≤ —В–∞–±–ї–Є—Ж–µ 5.
–Т—Л–і–µ–ї—П—О—В —Б–ї–µ–і—Г—О—Й–Є–µ –Њ—Б–Њ–±–µ–љ–љ–Њ—Б—В–Є –Љ–Њ–љ–Њ–љ–µ–є—А–Њ–њ–∞—В–Є–Є:
вАУ —Д–Њ–Ї–∞–ї—М–љ–∞—П (–∞—Б–Є–Љ–Љ–µ—В—А–Є—З–љ–∞—П –Њ–і–љ–Њ—Б—В–Њ—А–Њ–љ–љ—П—П –Є–ї–Є –±–Є–ї–∞—В–µ—А–∞–ї—М–љ–∞—П –Љ—Л—И–µ—З–љ–∞—П —Б–ї–∞–±–Њ—Б—В—М);
вАУ –±–Њ–ї–µ–≤–∞—П (–±–Њ–ї—М вИТ –Њ–і–Є–љ –Є–Ј –љ–∞–Є–±–Њ–ї–µ–µ –Є–љ–≤–∞–ї–Є–і–Є–Ј–Є—А—Г—О—Й–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤);
вАУ –Њ—Б—В—А–∞—П –Є–ї–Є –њ–Њ–і–Њ—Б—В—А–∞—П (–≤—Б–µ —Б–Є–Љ–њ—В–Њ–Љ—Л —А–∞–Ј–≤–Є–≤–∞—О—В—Б—П –≤ —В–µ—З–µ–љ–Є–µ –љ–µ—Б–Ї–Њ–ї—М–Ї–Є—Е –і–љ–µ–є –Є–ї–Є 2-—Е –Љ–µ—Б.);
вАУ —Б–Њ —Б–њ–Њ–љ—В–∞–љ–љ—Л–Љ (–љ–µ–Ј–∞–≤–Є—Б–Є–Љ—Л–Љ –Њ—В –ї–µ—З–µ–љ–Є—П) –≤—Л–Ј–і–Њ—А–Њ–≤–ї–µ–љ–Є–µ–Љ.
–Э–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М –≤ —Б—В—А—Г–Ї—В—Г—А–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–Њ—А–Љ –Ф–Э
–Э–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М —Г –±–Њ–ї—М–љ—Л—Е –°–Ф –Ј–∞—Б–ї—Г–ґ–Є–≤–∞–µ—В –Њ—В–і–µ–ї—М–љ–Њ–≥–Њ –Њ–±—Б—Г–ґ–і–µ–љ–Є—П –≤ —Б–≤—П–Ј–Є —Б –≤—Л—Б–Њ–Ї–Њ–є —З–∞—Б—В–Њ—В–Њ–є –µ–µ –њ–Њ—П–≤–ї–µ–љ–Є—П –Є —В—А—Г–і–љ–Њ—Б—В—П–Љ–Є —В–µ—А–∞–њ–Є–Є. –Ю–љ–∞ –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ —Б—В—А—Г–Ї—В—Г—А–µ —А–∞–Ј–ї–Є—З–љ—Л—Е —Д–Њ—А–Љ –Ф–Э: –і–Є—Д—Д—Г–Ј–љ—Л—Е –Є —Д–Њ–Ї–∞–ї—М–љ—Л—Е. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, –і–ї—П –°–Ф —Е–∞—А–∞–Ї—В–µ—А–љ–∞ –Њ—Б–Њ–±–∞—П —Д–Њ—А–Љ–∞ –љ–µ–є—А–Њ–њ–∞—В–Є–Є вАУ –Њ—Б—В—А–∞—П –±–Њ–ї–µ–≤–∞—П –љ–µ–є—А–Њ–њ–∞—В–Є—П, –≤–µ–і—Г—Й–Є–Љ —Б–Є–Љ–њ—В–Њ–Љ–Њ–Љ –Ї–Њ—В–Њ—А–Њ–є —П–≤–ї—П–µ—В—Б—П –Њ—Б—В—А–∞—П –ґ–≥—Г—З–∞—П –±–Њ–ї—М (–∞–ї–ї–Њ–і–Є–љ–Є—П) –њ—А–Є –Љ–Є–љ–Є–Љ–∞–ї—М–љ–Њ–Љ —Б–µ–љ—Б–Њ–Љ–Њ—В–Њ—А–љ–Њ–Љ –і–µ—Д–Є—Ж–Є—В–µ. –Т —Ж–µ–ї–Њ–Љ, –њ–Њ –і–∞–љ–љ—Л–Љ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –∞–≤—В–Њ—А–Њ–≤, –±–Њ–ї–µ–≤–Њ–є —Б–Є–љ–і—А–Њ–Љ –њ—А–Є –Ф–Э –≤—Б—В—А–µ—З–∞–µ—В—Б—П –≤ 18вАУ20% –≤—Б–µ—Е —Б–ї—Г—З–∞–µ–≤. –Т –Ї–∞—З–µ—Б—В–≤–µ –Њ—Б–љ–Њ–≤–љ—Л—Е –Љ–µ—Е–∞–љ–Є–Ј–Љ–Њ–≤ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є—П –±–Њ–ї–Є –њ—А–Є –Ф–Э –Њ–±—Б—Г–ґ–і–∞–µ—В—Б—П –њ–Њ—А–∞–ґ–µ–љ–Є–µ —В–Њ–љ–Ї–Є—Е —Б–µ–љ—Б–Њ—А–љ—Л—Е –љ–µ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –Є —Б–ї–∞–±–Њ–Љ–Є–µ–ї–Є–љ–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л—Е –љ–µ—А–≤–љ—Л—Е –≤–Њ–ї–Њ–Ї–Њ–љ, –Њ—В–≤–µ—В—Б—В–≤–µ–љ–љ—Л—Е –Ј–∞ –±–Њ–ї–µ–≤—Г—О —З—Г–≤—Б—В–≤–Є—В–µ–ї—М–љ–Њ—Б—В—М.–Ґ–∞–Ї—В–Є–Ї–∞ –ї–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є
–§–∞—А–Љ–∞–Ї–Њ—В–µ—А–∞–њ–Є—П –±–Њ–ї–µ–≤—Л—Е —Д–Њ—А–Љ –Ф–Э –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–µ—В—Б—П –≤ 2вАУ—Е –Њ—Б–љ–Њ–≤–љ—Л—Е –љ–∞–њ—А–∞–≤–ї–µ–љ–Є—П—Е: –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ–≤—А–µ–ґ–і–µ–љ–љ—Л—Е –љ–µ—А–≤–Њ–≤ (–њ–∞—В–Њ–≥–µ–љ–µ—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П) –Є –∞–і–µ–Ї–≤–∞—В–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–µ–≤–Њ–≥–Њ —Б–Є–љ–і—А–Њ–Љ–∞ (—Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї–∞—П —В–µ—А–∞–њ–Є—П).
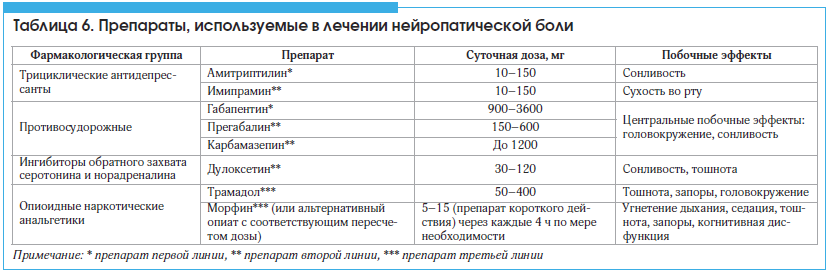
–°–Њ–≤—А–µ–Љ–µ–љ–љ—Л–µ –њ–Њ–і—Е–Њ–і—Л –Ї —В–µ—А–∞–њ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –њ—А–µ–і—Г—Б–Љ–∞—В—А–Є–≤–∞—О—В –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —А–∞–Ј–ї–Є—З–љ—Л—Е –≥—А—Г–њ–њ, –Њ–Ї–∞–Ј—Л–≤–∞—О—Й–Є—Е –≤–ї–Є—П–љ–Є–µ –љ–∞ —А–∞–Ј–ї–Є—З–љ—Л–µ –Ј–≤–µ–љ—М—П –µ–µ –њ–∞—В–Њ–≥–µ–љ–µ–Ј–∞ (—В–∞–±–ї. 6).
–Р–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л. –Ґ—А–Є—Ж–Є–Ї–ї–Є—З–µ—Б–Ї–Є–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л (–Ґ–¶–Р) –±—Л–ї–Є –њ–µ—А–≤—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є, –і–ї—П –Ї–Њ—В–Њ—А—Л—Е –њ—А–Њ–≤–µ–і–µ–љ—Л –њ–ї–∞—Ж–µ–±–Њ-–Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П, –і–Њ–Ї–∞–Ј–∞–≤—И–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤ –ї–µ—З–µ–љ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –њ—А–Є –Ф–Я–Э. –Т —Б–≤—П–Ј–Є —Б —Н—В–Є–Љ –Њ–љ–Є –Њ—В–љ–Њ—Б—П—В—Б—П –Ї –њ—А–µ–њ–∞—А–∞—В–∞–Љ –њ–µ—А–≤–Њ–≥–Њ –≤—Л–±–Њ—А–∞ –≤ —Г—Б—В—А–∞–љ–µ–љ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є. –Ґ–¶–Р –Љ–Њ–≥—Г—В –њ—А–Є–љ–Є–Љ–∞—В—М—Б—П —Б –і—А—Г–≥–Є–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –і–ї—П –ї–µ—З–µ–љ–Є—П –Ф–Э вАУ –њ—А–µ–≥–∞–±–∞–ї–Є–љ–Њ–Љ –Є –≥–∞–±–∞–њ–µ–љ—В–Є–љ–Њ–Љ. –†–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П —В–Є—В—А–Њ–≤–∞—В—М –і–Њ–Ј—Г, —З—В–Њ –Љ–Њ–ґ–µ—В –Ј–∞–љ—П—В—М –љ–µ—Б–Ї–Њ–ї—М–Ї–Њ –љ–µ–і–µ–ї—М –Є–ї–Є –Љ–µ—Б—П—Ж–µ–≤, –њ–Њ–Ї–∞ –љ–µ –±—Г–і–µ—В –і–Њ—Б—В–Є–≥–љ—Г—В–∞ —Ж–µ–ї—М –ї–µ—З–µ–љ–Є—П. –Ю–і–љ–∞–Ї–Њ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –≤ –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –Њ–≥—А–∞–љ–Є—З–µ–љ–Њ –±–Њ–ї—М—И–Є–Љ –Ї–Њ–ї–Є—З–µ—Б—В–≤–Њ–Љ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤. –Ю—Б–Њ–±–µ–љ–љ–Њ –љ–µ–ґ–µ–ї–∞—В–µ–ї—М–љ–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –њ—А–µ–њ–∞—А–∞—В–Њ–≤ —Г –±–Њ–ї—М–љ—Л—Е –њ–Њ–ґ–Є–ї–Њ–≥–Њ –≤–Њ–Ј—А–∞—Б—В–∞ —Б –Є—И–µ–Љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ—М—О —Б–µ—А–і—Ж–∞, –∞—А–Є—В–Љ–Є–µ–є, –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є –≤–љ—Г—В—А–Є–ґ–µ–ї—Г–і–Њ—З–Ї–Њ–≤–Њ–є –њ—А–Њ–≤–Њ–і–Є–Љ–Њ—Б—В–Є, –≥–ї–∞—Г–Ї–Њ–Љ–Њ–є, –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є, –Ј–∞–і–µ—А–ґ–Ї–Њ–є –Љ–Њ—З–Є, –≤–µ–≥–µ—В–∞—В–Є–≤–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О вАУ –њ—А–Њ–±–ї–µ–Љ–∞–Љ–Є, –≤–µ—Б—М–Љ–∞ —З–∞—Б—В–Њ —Б–Њ–њ—Г—В—Б—В–≤—Г—О—Й–Є–Љ–Є –°–Ф. –Э–µ —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М –Є—Е –≤–Њ –≤—А–µ–Љ—П –±–µ—А–µ–Љ–µ–љ–љ–Њ—Б—В–Є –Є –Ї–Њ—А–Љ–ї–µ–љ–Є—П –≥—А—Г–і—М—О. –Э–∞–Є–±–Њ–ї—М—И–µ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О —Б—А–µ–і–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –≥—А—Г–њ–њ—Л –Ґ–¶–Р –Њ–±–ї–∞–і–∞–µ—В –∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ вАУ —В–∞–±–ї–µ—В–Ї–Є 10 –Љ–≥ –Є 25 –Љ–≥. –Р–Љ–±—Г–ї–∞—В–Њ—А–љ—Л–Љ –±–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ 75 –Љ–≥/—Б—Г—В, —А–∞–Ј–і–µ–ї–µ–љ–љ–∞—П –љ–∞ 2 –њ—А–Є–µ–Љ–∞ –Є–ї–Є 50вАУ100 –Љ–≥ –љ–∞ –љ–Њ—З—М, —В–Є—В—А–∞—Ж–Є—П вАУ –њ–Њ 25вАУ50 –Љ–≥ –љ–∞ –љ–Њ—З—М, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П –і–Њ–Ј–∞ вАУ 50вАУ100 –Љ–≥ –љ–∞ –љ–Њ—З—М, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ вАУ 150 –Љ–≥/—Б—Г—В. –°—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л–Љ –±–Њ–ї—М–љ—Л–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ 100 –Љ–≥/—Б—Г—В, —В–Є—В—А–∞—Ж–Є—П вАУ –і–Њ 200 –Љ–≥/—Б—Г—В, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П –і–Њ–Ј–∞ вАУ 50вАУ100 –Љ–≥ –љ–∞ –љ–Њ—З—М, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ вАУ 300 –Љ–≥/—Б—Г—В. –Т–љ—Г—В—А–Є–Љ—Л—И–µ—З–љ–Њ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ 20вАУ30 –Љ–≥ 4 —А./—Б—Г—В. –Я–Њ–ґ–Є–ї—Л–Љ –њ–Њ–Ї–∞–Ј–∞–љ–∞ –і–Њ–Ј–∞ 10 –Љ–≥ 2 —А./—Б—Г—В –Є–ї–Є 20 –Љ–≥ –љ–∞ –љ–Њ—З—М. –Я—А–Є–Љ–µ–љ—П—О—В —В–∞–Ї–ґ–µ –∞–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В –Є–Љ–Є–њ—А–∞–Љ–Є–љ вАУ —В–∞–±–ї–µ—В–Ї–Є 10 –Љ–≥, 25 –Љ–≥ –Є 50 –Љ–≥. –°—В–∞—Ж–Є–Њ–љ–∞—А–љ—Л–Љ –±–Њ–ї—М–љ—Л–Љ —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ–∞ –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ 100 –Љ–≥/—Б—Г—В –≤ 2 –њ—А–Є–µ–Љ–∞, —В–Є—В—А–∞—Ж–Є—П вАУ –і–Њ 200 –Љ–≥/—Б—Г—В; –і–Њ–Ј–∞ –Љ–Њ–ґ–µ—В –±—Л—В—М –њ–Њ–≤—Л—И–µ–љ–∞ –і–Њ 250вАУ300 –Љ–≥/—Б—Г—В —З–µ—А–µ–Ј 2 –љ–µ–і., –µ—Б–ї–Є –µ—Б—В—М –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В—М. –Р–Љ–±—Г–ї–∞—В–Њ—А–љ—Л–Љ –±–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–µ—В—Б—П –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ 75 –Љ–≥/—Б—Г—В, —В–Є—В—А–∞—Ж–Є—П вАУ –њ–Њ–≤—Л—И–µ–љ–Є–µ –і–Њ 150 –Љ–≥/—Б—Г—В, –њ–Њ–і–і–µ—А–ґ–Є–≤–∞—О—Й–∞—П –і–Њ–Ј–∞ вАУ 50вАУ150 –Љ–≥/—Б—Г—В, –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ вАУ 200 –Љ–≥/—Б—Г—В.
–° —Г—З–µ—В–Њ–Љ –љ–µ–±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–≥–Њ —Б–њ–µ–Ї—В—А–∞ –њ–Њ–±–Њ—З–љ—Л—Е –і–µ–є—Б—В–≤–Є–є –Ґ–¶–Р —Г –±–Њ–ї—М–љ—Л—Е –°–Ф –≤ –њ–Њ—Б–ї–µ–і–љ–Є–µ –≥–Њ–і—Л –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –њ—А–µ–њ–∞—А–∞—В–Њ–Љ –њ–µ—А–≤–Њ–є –Њ—З–µ—А–µ–і–Є –≤—Л–±–Њ—А–∞ —Б—З–Є—В–∞–µ—В—Б—П –і—Г–ї–Њ–Ї—Б–µ—В–Є–љ.
–°–µ–ї–µ–Ї—В–Є–≤–љ—Л–є –Є–љ–≥–Є–±–Є—В–Њ—А –Њ–±—А–∞—В–љ–Њ–≥–Њ –Ј–∞—Е–≤–∞—В–∞ —Б–µ—А–Њ—В–Њ–љ–Є–љ–∞ –Є –љ–Њ—А–∞–і—А–µ–љ–∞–ї–Є–љ–∞ (–°–Ш–Ю–Ч–°–Є–Э) –і—Г–ї–Њ–Ї—Б–µ—В–Є–љ —П–≤–ї—П–µ—В—Б—П –µ–і–Є–љ—Б—В–≤–µ–љ–љ—Л–Љ –њ—А–µ–њ–∞—А–∞—В–Њ–Љ, –Ї–Њ—В–Њ—А—Л–є —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞–љ –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ —В–Њ–ї—М–Ї–Њ –і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є, –љ–Њ –Є –Ф–Э. –Ю–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й–µ–µ –і–µ–є—Б—В–≤–Є–µ –і—Г–ї–Њ–Ї—Б–µ—В–Є–љ–∞ –њ—А–Є –Ф–Э –±—Л–ї–Њ –і–Њ–Ї–∞–Ј–∞–љ–Њ –≤ –Љ–љ–Њ–≥–Њ—З–Є—Б–ї–µ–љ–љ—Л—Е –Ї–Њ–љ—В—А–Њ–ї–Є—А—Г–µ–Љ—Л—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е. –£ –±–Њ–ї—М–љ—Л—Е —Б –±–Њ–ї–µ–≤–Њ–є —Д–Њ—А–Љ–Њ–є –Ф–Э –Љ–Њ–ґ–µ—В –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ–Њ –њ–Њ–≤—Л—И–∞—В—М—Б—П –≥–ї–Є–Ї–µ–Љ–Є—П –љ–∞—В–Њ—Й–∞–Ї. –Э–∞ —Д–Њ–љ–µ –і–ї–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є (–і–Њ 52 –љ–µ–і.) –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –љ–µ–Ї–Њ—В–Њ—А–Њ–µ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–Є—А–Њ–≤–∞–љ–љ–Њ–≥–Њ –≥–µ–Љ–Њ–≥–ї–Њ–±–Є–љ–∞, –Ї–Њ—В–Њ—А–Њ–µ –љ–∞ 0,3% –њ—А–µ–≤–Њ—Б—Е–Њ–і–Є–ї–Њ —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤—Г—О—Й–µ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Г –±–Њ–ї—М–љ—Л—Е, –њ–Њ–ї—Г—З–∞–≤—И–Є—Е –Є–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ; –љ–∞–±–ї—О–і–∞–ї–Њ—Б—М —В–∞–Ї–ґ–µ –љ–µ–±–Њ–ї—М—И–Њ–µ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –≥–ї–Є–Ї–µ–Љ–Є–Є –љ–∞—В–Њ—Й–∞–Ї –Є –Њ–±—Й–µ–≥–Њ —Е–Њ–ї–µ—Б—В–µ—А–Є–љ–∞ –≤ –Ї—А–Њ–≤–Є.
–Р–љ—В–Є—Н–њ–Є–ї–µ–њ—В–Є—З–µ—Б–Ї–Є–µ (–њ—А–Њ—В–Є–≤–Њ—Б—Г–і–Њ—А–Њ–ґ–љ—Л–µ) –њ—А–µ–њ–∞—А–∞—В—Л (–Р–≠–Я) –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є —Б 1960-—Е –≥–≥., —Е–Њ—В—П –Є —Б —Г–Љ–µ—А–µ–љ–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М—О, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –њ—А–Є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Є—Е –њ–Њ—А–∞–ґ–µ–љ–Є—П—Е, —Е–∞—А–∞–Ї—В–µ—А–љ—Л—Е –і–ї—П –Ф–Э, –≤ –Њ—В–ї–Є—З–Є–µ –Њ—В —Ж–µ–љ—В—А–∞–ї—М–љ—Л—Е –±–Њ–ї–µ–є. –Р–≠–Я –±–Њ–ї–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л –њ—А–Є –Њ—Б—В—А–Њ–є –Є –њ–∞—А–Њ–Ї—Б–Є–Ј–Љ–∞–ї—М–љ–Њ–є –±–Њ–ї–Є. –Я–Њ—П–≤–ї–µ–љ–Є–µ –≤ 1990-—Е –≥–≥. –љ–Њ–≤–Њ–≥–Њ –њ—А–Њ—В–Є–≤–Њ—Б—Г–і–Њ—А–Њ–ґ–љ–Њ–≥–Њ –њ—А–µ–њ–∞—А–∞—В–∞ –≥–∞–±–∞–њ–µ–љ—В–Є–љ (–Ъ–Њ–љ–≤–∞–ї–Є—Б) –Њ—В–Ї—А—Л–ї–Њ –љ–Њ–≤—Л–µ –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –≤ –ї–µ—З–µ–љ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є. –У–∞–±–∞–њ–µ–љ—В–Є–љ –њ—А–Њ—П–≤–Є–ї —Б–µ–±—П –Ї–∞–Ї —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –Є –±–µ–Ј–Њ–њ–∞—Б–љ—Л–є –њ—А–µ–њ–∞—А–∞—В –≤ –ї–µ—З–µ–љ–Є–Є —А–∞–Ј–љ–Њ–Њ–±—А–∞–Ј–љ—Л—Е –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є—Е –±–Њ–ї–µ–≤—Л—Е —Б–Є–љ–і—А–Њ–Љ–Њ–≤, –≤ —В. —З. –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є. –Я—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –њ—А–µ–њ–∞—А–∞—В –љ–∞–Ј–љ–∞—З–∞—О—В –≤ –љ–∞—З–∞–ї—М–љ–Њ–є –і–Њ–Ј–µ 300 –Љ–≥ 1 —А./—Б—Г—В, –≤–Њ 2-–є –і–µ–љ—М вАУ –њ–Њ 300 –Љ–≥ 2 —А./—Б—Г—В, –љ–∞ 3-–є –і–µ–љ—М вАУ –њ–Њ 300 –Љ–≥ 3 —А./—Б—Г—В. –Я—А–Є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ–є –±–Њ–ї–Є –Љ–Њ–ґ–љ–Њ –љ–∞–Ј–љ–∞—З–∞—В—М —Б 1-–≥–Њ –і–љ—П –њ–Њ 300 –Љ–≥ 3 —А./—Б—Г—В. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –і–Њ–Ј—Г –Љ–Њ–ґ–љ–Њ –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Г–≤–µ–ї–Є—З–Є—В—М, –љ–Њ –љ–µ –±–Њ–ї–µ–µ —З–µ–Љ –і–Њ 3,6 –≥/—Б—Г—В. –Я—А–Є –Ф–Э –і–Њ–Ј–∞ 2,4 –≥/—Б—Г—В –Њ–±—Л—З–љ–Њ –і–Њ—Б—В–∞—В–Њ—З–љ–∞. –Ф–ї—П –±–Њ–ї—М–љ—Л—Е —Б –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є —Д—Г–љ–Ї—Ж–Є–Є –њ–Њ—З–µ–Ї —Б—Г—В–Њ—З–љ–∞—П –і–Њ–Ј–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В –њ—А–Є –Ї–ї–Є—А–µ–љ—Б–µ –Ї—А–µ–∞—В–Є–љ–Є–љ–∞ 50вАУ79 –Љ–ї/–Љ–Є–љ 600вАУ1800 –Љ–≥/—Б—Г—В, –њ—А–Є 30вАУ49 –Љ–ї/–Љ–Є–љ вАУ 300вАУ900 –Љ–≥/—Б—Г—В, –њ—А–Є 15вАУ29 –Љ–ї/–Љ–Є–љ вАУ 300вАУ600 –Љ–≥/—Б—Г—В, –њ—А–Є <15 –Љ–ї/–Љ–Є–љ вАУ 300 –Љ–≥ —З–µ—А–µ–Ј –і–µ–љ—М –Є–ї–Є –µ–ґ–µ–і–љ–µ–≤–љ–Њ. –Ф–ї—П –±–Њ–ї—М–љ—Л—Е, –љ–∞—Е–Њ–і—П—Й–Є—Е—Б—П –љ–∞ –≥–µ–Љ–Њ–і–Є–∞–ї–Є–Ј–µ, –љ–∞—З–∞–ї—М–љ–∞—П –і–Њ–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 300 –Љ–≥. –Ф–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–∞—П –і–Њ–Ј–∞ —Б–Њ—Б—В–∞–≤–ї—П–µ—В 300 –Љ–≥ –њ–Њ—Б–ї–µ –Ї–∞–ґ–і–Њ–≥–Њ 4-—З–∞—Б–Њ–≤–Њ–≥–Њ —Б–µ–∞–љ—Б–∞ –≥–µ–Љ–Њ–і–Є–∞–ї–Є–Ј–∞. –Т –і–µ–љ—М, –Ї–Њ–≥–і–∞ –≥–µ–Љ–Њ–і–Є–∞–ї–Є–Ј –љ–µ –њ—А–Њ–≤–Њ–і–Є—В—Б—П, –њ—А–µ–њ–∞—А–∞—В –љ–µ –љ–∞–Ј–љ–∞—З–∞—О—В.
–Я–Њ—Б–ї–µ –≥–∞–±–∞–њ–µ–љ—В–Є–љ–∞ –±—Л–ї –њ—А–µ–і–ї–Њ–ґ–µ–љ –і—А—Г–≥–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л–є –≤ –ї–µ—З–µ–љ–Є–Є –Ф–Э –Р–≠–Я –њ—А–µ–≥–∞–±–∞–ї–Є–љ –≤ –Ї–∞–њ—Б—Г–ї–∞—Е –њ–Њ 25 –Љ–≥, 75 –Љ–≥, 150 –Љ–≥ –Є 300 –Љ–≥. –Ю–±—Л—З–љ—Л–µ –і–Њ–Ј—Л вАУ –Њ—В 150 –Љ–≥/—Б—Г—В –і–Њ 600 –Љ–≥/—Б—Г—В –≤ 2 –њ—А–Є–µ–Љ–∞. –Я—А–Є–µ–Љ –њ–Є—Й–Є –љ–µ –≤–ї–Є—П–µ—В –љ–∞ –Ї–Є–љ–µ—В–Є–Ї—Г. –Я—А–Є –ї–µ—З–µ–љ–Є–Є –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є —Б—В–∞—А—В–Њ–≤–∞—П –і–Њ–Ј–∞ –Љ–Њ–ґ–µ—В —Б–Њ—Б—В–∞–≤–ї—П—В—М 150 –Љ–≥/—Б—Г—В. –Т –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є –Њ—В —Н—Д—Д–µ–Ї—В–∞ –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В–Є –і–Њ–Ј—Г –Љ–Њ–ґ–љ–Њ —Г–≤–µ–ї–Є—З–Є—В—М –і–Њ 300 –Љ–≥/—Б—Г—В —З–µ—А–µ–Ј 3вАУ7 –і–љ–µ–є. –Я—А–Є –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ—Б—В–Є –Љ–Њ–ґ–љ–Њ —Г–≤–µ–ї–Є—З–Є—В—М –і–Њ–Ј—Г –і–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є (600 –Љ–≥/—Б—Г—В) —З–µ—А–µ–Ј 1 –љ–µ–і. –Х—Б–ї–Є —Б–ї–µ–і—Г–µ—В –њ—А–µ–Ї—А–∞—В–Є—В—М –њ—А–Є–µ–Љ, —А–µ–Ї–Њ–Љ–µ–љ–і—Г–µ—В—Б—П –њ–Њ—Б—В–µ–њ–µ–љ–љ–Њ —Б–љ–Є–ґ–∞—В—М –і–Њ–Ј—Г –≤ —В–µ—З–µ–љ–Є–µ 1 –љ–µ–і. –Я—А–µ–≥–∞–±–∞–ї–Є–љ –љ–µ –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Є—А—Г–µ—В—Б—П –≤ –њ–µ—З–µ–љ–Є –Є –љ–µ —Б–≤—П–Ј—Л–≤–∞–µ—В—Б—П —Б –±–µ–ї–Ї–∞–Љ–Є –њ–ї–∞–Ј–Љ—Л, –њ–Њ—Н—В–Њ–Љ—Г –Њ–љ –њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є –љ–µ –≤–Ј–∞–Є–Љ–Њ–і–µ–є—Б—В–≤—Г–µ—В —Б –і—А—Г–≥–Є–Љ–Є –ї–µ–Ї–∞—А—Б—В–≤–∞–Љ–Є. –° 2015 –≥. –њ—А–µ–њ–∞—А–∞—В –њ–Њ–і–ї–µ–ґ–Є—В –њ—А–µ–і–Љ–µ—В–љ–Њ-–Ї–Њ–ї–Є—З–µ—Б—В–≤–µ–љ–љ–Њ–Љ—Г —Г—З–µ—В—Г.
–Т –і–Њ–њ–Њ–ї–љ–Є—В–µ–ї—М–љ–Њ–є —В–µ—А–∞–њ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –Љ–Њ–≥—Г—В –±—Л—В—М –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ—Л –Њ–њ–Є–Њ–Є–і–љ—Л–µ –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Є. –Т–Њ–њ—А–Њ—Б –Њ–± –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є —Б–ї–µ–і—Г–µ—В —А–∞—Б—Б–Љ–∞—В—А–Є–≤–∞—В—М –ї–Є—И—М –њ–Њ—Б–ї–µ –±–µ–Ј—Г—Б–њ–µ—И–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П –і—А—Г–≥–Є–Љ–Є —Б—А–µ–і—Б—В–≤–∞–Љ–Є —В–µ—А–∞–њ–Є–Є, —З—В–Њ —Б–≤—П–Ј–∞–љ–Њ —Б –≤—Л—Б–Њ–Ї–Њ–є —З–∞—Б—В–Њ—В–Њ–є –њ–Њ—В–µ–љ—Ж–Є–∞–ї—М–љ–Њ –Њ–њ–∞—Б–љ—Л—Е –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –њ—А–Є –Є—Е –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є, –≤ —В. —З. —Б —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ–Љ —Д–Є–Ј–Є—З–µ—Б–Ї–Њ–є –Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Њ–є –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В–Є. –Я—А–µ–њ–∞—А–∞—В–∞–Љ–Є –≤—Л–±–Њ—А–∞ –Є–Ј —Б—А–µ–і—Б—В–≤ —Н—В–Њ–є –≥—А—Г–њ–њ—Л –Љ–Њ–≥—Г—В –±—Л—В—М —В—А–∞–Љ–∞–і–Њ–ї –≤ –і–Њ–Ј–µ –і–Њ 400 –Љ–≥/—Б—Г—В, –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є—П 37,5 –Љ–≥ —В—А–∞–Љ–∞–і–Њ–ї–∞ –≥–Є–і—А–Њ—Е–ї–Њ—А–Є–і–∞ –Є 325 –Љ–≥ –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї–∞ 2вАУ6 —В–∞–±–ї./—Б—Г—В.
–Т –Ї–Њ–Љ–±–Є–љ–∞—Ж–Є–Є —Б —Г–Ї–∞–Ј–∞–љ–љ—Л–Љ–Є –њ—А–µ–њ–∞—А–∞—В–∞–Љ–Є –Љ–Њ–ґ–µ—В –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞—В—М—Б—П –∞–ї—М—Д–∞-–ї–Є–њ–Њ–µ–≤–∞—П (—В–Є–Њ–Ї—В–Њ–≤–∞—П) –Ї–Є—Б–ї–Њ—В–∞ (–Ю–Ї—В–Њ–ї–Є–њ–µ–љ), –Њ–±–ї–∞–і–∞—О—Й–∞—П —Б–Є–ї—М–љ—Л–Љ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л–Љ –і–µ–є—Б—В–≤–Є–µ–Љ –Є —Б–њ–Њ—Б–Њ–±—Б—В–≤—Г—О—Й–∞—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–Љ—Г —А–µ–≥—А–µ—Б—Б—Г –Њ—Б–љ–Њ–≤–љ—Л—Е –њ—А–Њ—П–≤–ї–µ–љ–Є–є –љ–µ–є—А–Њ–њ–∞—В–Є–Є.
–Э–µ—Б–Љ–Њ—В—А—П –љ–∞ —В–Њ —З—В–Њ –≤–Њ –Љ–љ–Њ–≥–Є—Е –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П—Е –±—Л–ї–∞ —Г–±–µ–і–Є—В–µ–ї—М–љ–Њ –і–Њ–Ї–∞–Ј–∞–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –≤—Л—И–µ–њ—А–Є–≤–µ–і–µ–љ–љ—Л—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–Њ —Б—А–∞–≤–љ–µ–љ–Є—О —Б –њ–ї–∞—Ж–µ–±–Њ, –≤ —А–µ–∞–ї—М–љ–Њ–є –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ —Г—Б—В—А–∞–љ–Є—В—М –і–Є–∞–±–µ—В–Є—З–µ—Б–Ї—Г—О –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї—Г—О –±–Њ–ї—М –љ–µ–њ—А–Њ—Б—В–Њ, –Є —В—А–µ–±—Г–µ—В—Б—П –і–Њ—Б—В–∞—В–Њ—З–љ–Њ –Љ–љ–Њ–≥–Њ —В–µ—А–њ–µ–љ–Є—П –Њ—В –±–Њ–ї—М–љ–Њ–≥–Њ –Є –≤—А–∞—З–∞, —З—В–Њ–±—Л –Њ–њ—В–Є–Љ–Є–Ј–Є—А–Њ–≤–∞—В—М –ї–µ—З–µ–љ–Є–µ –±–Њ–ї–Є. –Т —Ж–µ–ї–Њ–Љ –±–Њ–ї–µ–≤–∞—П —Д–Њ—А–Љ–∞ –љ–µ–є—А–Њ–њ–∞—В–Є–Є –ї–µ—З–Є—В—Б—П –њ–Њ–Ї–∞ –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ.
–Т–Є—В–∞–Љ–Є–љ—Л –Є –і—А—Г–≥–Є–µ –њ–Є—Й–µ–≤—Л–µ –і–Њ–±–∞–≤–Ї–Є –љ–µ –Њ–Ї–∞–Ј—Л–≤–∞—О—В —Б—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ–≥–Њ –і–µ–є—Б—В–≤–Є—П, –µ—Б–ї–Є –±–Њ–ї—М –љ–µ —Б–≤—П–Ј–∞–љ–∞ —Б –љ–µ–і–Њ—Б—В–∞—В–Ї–Њ–Љ –≤–Є—В–∞–Љ–Є–љ–Њ–≤ –Є–ї–Є –∞–ї–Ї–Њ–≥–Њ–ї–Є–Ј–Љ–Њ–Љ. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—Б—В—Л—Е –∞–љ–∞–ї—М–≥–µ—В–Є–Ї–Њ–≤, —В–∞–Ї–Є—Е –Ї–∞–Ї –њ–∞—А–∞—Ж–µ—В–∞–Љ–Њ–ї –Є–ї–Є –љ–µ—Б—В–µ—А–Њ–Є–і–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ–≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л, –љ–µ –њ–Њ–ї—Г—З–Є–ї–∞ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Є—П –њ—А–Є –Љ–µ—В–∞–∞–љ–∞–ї–Є–Ј–µ, –љ–Њ –≤–Љ–µ—Б—В–µ —Б —В–µ–Љ –≤ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –њ—А–∞–Ї—В–Є–Ї–µ –Њ–љ–Є –≤—А–µ–Љ—П –Њ—В –≤—А–µ–Љ–µ–љ–Є –љ–∞–Ј–љ–∞—З–∞—О—В—Б—П. –Р–љ–∞–ї—М–≥–µ—В–Є–Ї–Є –≤—В–Њ—А–Њ–є –ї–Є–љ–Є–Є (—В—А–∞–Љ–∞–і–Њ–ї) –≤ —В–∞–Ї–Њ–є –ґ–µ —Б—В–µ–њ–µ–љ–Є —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л, –Ї–∞–Ї –Є –Ґ–¶–Р, –љ–Њ –і–ї–Є—В–µ–ї—М–љ–Њ–µ –ї–µ—З–µ–љ–Є–µ —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–µ—В—Б—П –Њ–±—Л—З–љ—Л–Љ–Є –і–ї—П –Њ–њ–Є–∞—В–Њ–≤ –њ–Њ—Б–ї–µ–і—Б—В–≤–Є—П–Љ–Є вАУ –Њ—В–Љ–µ—З–∞—О—В—Б—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Є —Б–љ–Є–ґ–µ–љ–Є–µ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є.
–Р–љ—В–Є–і–µ–њ—А–µ—Б—Б–∞–љ—В—Л –Є—Б–њ–Њ–ї—М–Ј—Г—О—В—Б—П –≤ —Б–≤—П–Ј–Є —Б –Є—Е –∞–љ–∞–ї—М–≥–µ–Ј–Є—А—Г—О—Й–Є–Љ –і–µ–є—Б—В–≤–Є–µ–Љ. –°–Ш–Ю–Ч–°–Є–Э –Є–Љ–µ–µ—В –Љ–µ–љ—М—И–µ –њ–Њ–±–Њ—З–љ—Л—Е —Н—Д—Д–µ–Ї—В–Њ–≤ –Є –њ—А–Њ—Й–µ –і–Њ–Ј–Є—А—Г–µ—В—Б—П, –љ–Њ –Љ–µ–љ–µ–µ —Н—Д—Д–µ–Ї—В–Є–≤–µ–љ, —З–µ–Љ –Ґ–¶–Р. –°—Г–±–і–µ–њ—А–µ—Б—Б–Є–≤–љ—Л–µ –і–Њ–Ј—Л –∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ —Б–љ–Є–Љ–∞—О—В –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї—Г—О –±–Њ–ї—М: –љ–∞—З–Є–љ–∞—О—В —Б 10 –Љ–≥ –љ–∞ –љ–Њ—З—М –Є –њ–Њ–≤—Л—И–∞—О—В –і–Њ –Љ–∞–Ї—Б–Є–Љ–∞–ї—М–љ–Њ–є –і–Њ–Ј—Л 100 –Љ–≥/—Б—Г—В. –Ю–љ–Є –њ–ї–Њ—Е–Њ –њ–µ—А–µ–љ–Њ—Б—П—В—Б—П –≤ –±–Њ–ї—М—И–Є—Е –і–Њ–Ј–∞—Е, –њ—А–Є –њ—А–Є–Љ–µ–љ–µ–љ–Є–Є –Ї–Њ—В–Њ—А—Л—Е —А–∞–Ј–≤–Є–≤–∞–µ—В—Б—П –∞–љ—В–Є—Е–Њ–ї–Є–љ–µ—А–≥–Є—З–µ—Б–Ї–Є–є —Б–Є–љ–і—А–Њ–Љ (–њ–Њ—В–µ—А—П —Б–Њ–Ј–љ–∞–љ–Є—П, –≥–∞–ї–ї—О—Ж–Є–љ–∞—Ж–Є–Є). –Ю–љ–Є —В–∞–Ї–ґ–µ –Љ–Њ–≥—Г—В –≤—Л–Ј–≤–∞—В—М –љ–∞—А—Г—И–µ–љ–Є–µ –і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є —Б–µ—А–і—Ж–∞ (–±–ї–Њ–Ї–∞–і–∞ —Б–µ—А–і—Ж–∞, –≤–µ–љ—В—А–Є–Ї—Г–ї—П—А–љ—Л–µ —Н–Ї—Б—В—А–∞—Б–Є—Б—В–Њ–ї—Л, —Г–і–ї–Є–љ–µ–љ–Є–µ –Ј—Г–±—Ж–∞ QT), –њ–Њ—Н—В–Њ–Љ—Г —В—А–µ–±—Г–µ—В—Б—П –њ–µ—А–Є–Њ–і–Є—З–µ—Б–Ї–Њ–µ –≠–Ъ–У-–Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ.
–Ю–±—Л—З–љ—Л–µ –њ—А–Њ—В–Є–≤–Њ—Б—Г–і–Њ—А–Њ–ґ–љ—Л–µ —Б—А–µ–і—Б—В–≤–∞ (–Ї–∞—А–±–∞–Љ–∞–Ј–µ–њ–Є–љ, —Д–µ–љ–Є—В–Њ–Є–љ) —Н—Д—Д–µ–Ї—В–Є–≤–љ—Л, –љ–Њ —В—А–µ–±—Г–µ—В—Б—П —В—Й–∞—В–µ–ї—М–љ–∞—П —В–Є—В—А–∞—Ж–Є—П –Є—Е –і–Њ–Ј—Л, –Є –Њ–±—Л—З–љ–Њ –Њ–љ–Є –Њ—З–µ–љ—М –њ–ї–Њ—Е–Њ –њ–µ—А–µ–љ–Њ—Б—П—В—Б—П. –¶–µ–љ—В—А–∞–ї—М–љ–Њ –і–µ–є—Б—В–≤—Г—О—Й–Є–µ –∞–љ—В–∞–≥–Њ–љ–Є—Б—В—Л –≥–∞–Љ–Љ–∞-–∞–Љ–Є–љ–Њ–±—Г—В–Є—А–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –≥–∞–±–∞–њ–µ–љ—В–Є–љ –Є –њ—А–µ–≥–∞–±–∞–ї–Є–љ –њ–Њ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ј–∞–љ–Є–Љ–∞—О—В –њ—А–Њ–Љ–µ–ґ—Г—В–Њ—З–љ–Њ–µ –Љ–µ—Б—В–Њ –Љ–µ–ґ–і—Г –Ґ–¶–Р –Є –°–Ш–Ю–Ч–°–Є–Э.
R.H. Dworkin et al. –њ—А–µ–і–ї–∞–≥–∞—О—В –њ–Њ—И–∞–≥–Њ–≤—Г—О –Є–љ—Б—В—А—Г–Ї—Ж–Є—О –і–ї—П –ї–µ—З–µ–љ–Є—П –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є.
1. –Ш–Ј—Г—З–Є—В–µ –±–Њ–ї—М –Є –њ–Њ–і—В–≤–µ—А–і–Є—В–µ –µ–µ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Є–є —Е–∞—А–∞–Ї—В–µ—А. –Т—Л—П–≤–Є—В–µ –µ–µ –њ—А–Є—З–Є–љ—Л. –Ю—Ж–µ–љ–Є—В–µ –Ї–Њ–Љ–Њ—А–±–Є–і–љ–Њ—Б—В—М, –Ї–Њ—В–Њ—А–∞—П –Љ–Њ–ґ–µ—В –њ–Њ–Љ–µ—И–∞—В—М —В–µ—А–∞–њ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є. –Ю–±—К—П—Б–љ–Є—В–µ –њ–∞—Ж–Є–µ–љ—В—Г –њ—А–Њ–Є—Б—Е–Њ–ґ–і–µ–љ–Є–µ –±–Њ–ї–Є, –њ—Г—В–Є –Є –њ–µ—А—Б–њ–µ–Ї—В–Є–≤—Л –ї–µ—З–µ–љ–Є—П.
2. –Я—А–Њ–≤–Њ–і–Є—В–µ —В–µ—А–∞–њ–Є—О –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П, –≤—Л–Ј—Л–≤–∞—О—Й–µ–≥–Њ –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї—Г—О –±–Њ–ї—М.
–Э–∞—З–љ–Є—В–µ —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є—З–µ—Б–Ї—Г—О –Њ–±–µ–Ј–±–Њ–ї–Є–≤–∞—О—Й—Г—О —В–µ—А–∞–њ–Є—О:
вАУ –Ґ–¶–Р (–∞–Љ–Є—В—А–Є–њ—В–Є–ї–Є–љ) –Є–ї–Є –°–Ш–Ю–Ч–°–Є–Э (–і—Г–ї–Њ–Ї—Б–µ—В–Є–љ);
вАУ –±–ї–Њ–Ї–∞—В–Њ—А—Л –Ї–∞–ї—М—Ж–Є–µ–≤—Л—Е ќ±2-ќі –Ї–∞–љ–∞–ї–Њ–≤ (–≥–∞–±–∞–њ–µ–љ—В–Є–љ, –њ—А–µ–≥–∞–±–∞–ї–Є–љ);
вАУ –њ—А–Є –ї–Њ–Ї–∞–ї—М–љ–Њ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є вАУ –ї–Є–і–Њ–Ї–∞–Є–љ –Љ–µ—Б—В–љ–Њ;
вАУ –њ—А–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є –≤—Л—Б–Њ–Ї–Њ–є –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В–Є вАУ –Њ–њ–Є–∞—В—Л, —В—А–∞–Љ–∞–і–Њ–ї, –ї–Є–і–Њ–Ї–∞–Є–љ —Б–Є—Б—В–µ–Љ–љ–Њ.
–Ю—Ж–µ–љ–Є—В–µ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В—М –љ–µ–ї–µ–Ї–∞—А—Б—В–≤–µ–љ–љ–Њ–≥–Њ –ї–µ—З–µ–љ–Є—П.
3. –Ю—Ж–µ–љ–Є—В–µ –±–Њ–ї—М.
–Х—Б–ї–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –љ–∞ 70%, —Б–ї–µ–і—Г–µ—В –њ—А–Њ–і–Њ–ї–ґ–Є—В—М —В–µ—А–∞–њ–Є—О.
–Х—Б–ї–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –Љ–µ–љ–µ–µ —З–µ–Љ –љ–∞ 70%, –љ–µ–Њ–±—Е–Њ–і–Є–Љ–Њ –і–Њ–±–∞–≤–Є—В—М –≤—В–Њ—А–Њ–є –њ—А–µ–њ–∞—А–∞—В –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є.
–Х—Б–ї–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–∞—П –±–Њ–ї—М –љ–µ —Г–Љ–µ–љ—М—И–Є–ї–∞—Б—М –Є–ї–Є –µ–µ –Є–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М —Б–љ–Є–Ј–Є–ї–∞—Б—М —В–Њ–ї—М–Ї–Њ –љ–∞ 30%, —Б–Љ–µ–љ–Є—В–µ –њ—А–µ–њ–∞—А–∞—В –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є.
–Я—А–Є –љ–µ—Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –њ—А–µ–њ–∞—А–∞—В–Њ–≤ –њ–µ—А–≤–Њ–є –ї–Є–љ–Є–Є —Б–ї–µ–і—Г–µ—В –њ—А–Є–Љ–µ–љ—П—В—М –њ—А–µ–њ–∞—А–∞—В—Л –≤—В–Њ—А–Њ–є –Є–ї–Є —В—А–µ—В—М–µ–є –ї–Є–љ–Є–Є.
–І–∞—Б—В–Њ –њ—А–Є—Е–Њ–і–Є—В—Б—П –Ї–Њ–Љ–±–Є–љ–Є—А–Њ–≤–∞—В—М –њ—А–µ–њ–∞—А–∞—В—Л. –°—Г—Й–µ—Б—В–≤—Г–µ—В —Б—В–∞–љ–і–∞—А—В–љ—Л–є –∞–ї–≥–Њ—А–Є—В–Љ –≤—Л–±–Њ—А–∞ —В–µ—А–∞–њ–Є–Є –љ–µ–є—А–Њ–њ–∞—В–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–Є (—В–∞–±–ї. 7).













