Боли в спине, вызванные дегенеративными изменениями различных отделов позвоночника, патологией мышц спины, компрессией спинномозгового корешка и его сосудов вследствие грыжи межпозвоночного диска, развития спондилоартроза с гипертрофией межпозвонковых суставов или образования остеофитов, расценивают как неспецифические, и они составляют основную часть обращений пациентов в амбулаторной практике.
Следует помнить, что современные методы визуализации с высокой частотой позволяют определить дегенеративно-дистрофические изменения в позвоночнике даже у пациентов без болевых проявлений в спине. Так, по результатам МРТ поясничного отдела позвоночника, асимптомные грыжи межпозвонковых дисков в 30–40% случаев выявляются у лиц в возрасте до 40 лет и в 100% у лиц старше 60 лет [2, 3]. Также нет зависимости между рентгенологическими данными и клинической картиной заболевания [4]. Однако в практику российских врачей прочно вошел термин «остеохондроз» [5, 6], который может служить только предпосылкой для развития боли в спине, не являясь ее непосредственной причиной.
Диагностический поиск причины боли в первую очередь должен быть направлен на выявление симптомов специфического заболевания. Обнаружение «симптомов угрозы» при сборе анамнеза и осмотре пациента позволит врачу своевременно диагностировать серьезное, потенциально опасное для жизни заболевание [3, 7, 8].
Согласно международным стандартам, при отсутствии у пациента с болью в спине «симптомов угрозы» или радикулярной боли проведение лабораторных и инструментальных исследований (компьютерная томография (КТ), магнитно-резонансная томография (МРТ), рентгенография) необязательно, а терапия будет включать в основном препараты с анальгетическим действием [2, 3]. Группа нестероидных противовоспалительных препаратов (НПВП) является приоритетной в связи с эффективностью, доступностью и удобством применения как для купирования острой боли, так и для контроля основных проявлений хронических заболеваний позвоночника и суставов. При интенсивной боли (до 10 баллов по ВАШ (визуальная аналоговая шкала)) рациональным является назначение кеторолака; при выраженной боли, сопровождающейся болезненным гипертонусом мышц, добавляется миорелаксант (тизанидин, баклофен, толперизон); при наличии признаков центральной сенситизации используется антидепрессант (амитриптилин, флувоксамин, сертралин и др.) или антиконвульсант (карбамазепин, габапентин, прегабалин и др.).
Однако вероятность развития нежелательных явлений (НЯ) снижает приверженность терапии НПВП. Поэтому при уменьшении интенсивности боли или в случае, если боль изначально имела умеренный характер, пациенту целесообразно назначить НПВП с избирательным подавлением ЦОГ-2 для уменьшения количества неблагоприятных влияний на ЖКТ. Так, нимесулид оценивается как высокоэффективный НПВП в отношении болевых проявлений с воспалительным компонентом [9]. Эпидемиологические данные и клинические наблюдения также подтверждают благоприятное соотношение пользы и риска нимесулида (Найза) при лечении болевого синдрома [10]. Опыт применения нимесулида в нашей стране, накопленный за многие годы, свидетельствует о том, что препарат может успешно использоваться в лечении хронической и острой боли в суточной дозе ≤200 мг. Профиль безопасности удовлетворительный в отношении всех НЯ, свойственных НПВП [10]. Анализ 10 608 случаев НЯ при применении НПВП по результатам популяционного исследования показал, что НЯ со стороны ЖКТ при приеме нимесулида развивались в 10,4% случаев, а при приеме пироксикама, диклофенака и кетопрофена – почти в 2 раза чаще [11]. Сравнительный анализ побочных реакций со стороны печени, индуцированных нимесулидом и неселективными НПВП, включающий рандомизированные и постмаркетинговые клинические исследования, показал, что нимесулид вызывает повышение печеночных ферментов не чаще, чем традиционные НПВП [12]. С 1985 по 2000 г. зарегистрировано 192 значимых осложнения со стороны печени, ассоциированных с приемом нимесулида, 81 из которых наиболее серьезное. С учетом того, что к 2000 г. нимесулидом было пролечено 280 млн больных, суммарная частота опасных гепатотоксических реакций при его назначении составляла не более 0,1 на 100 000 курсов терапии [13]. По данным одного из крупных исследований, в котором проведен анализ 397 537 больных, принимавших НПВП, оказалось, что чаще всего гепатоцеллюлярная недостаточность наблюдалась при приеме флурбипрофена, ибупрофена и кеторолака (97,8, 44,6 и 33,4 случая на 100 000 пациенто-лет соответственно), для нимесулида этот показатель составил 33,1. Серьезные реакции возникают у 1 из 10 000 больных, при этом суммарная частота НЯ составляет всего 0,0001%. Проведенный под эгидой Общеевропейского органа по надзору за лекарственными средствами анализ безопасности нимесулида позволил сделать вывод, что гепатотоксичность данного препарата не выше, чем у других НПВП. Риск развития инфаркта миокарда (ИМ) на фоне приема этого препарата изучался в большом популяционном исследовании, проведенном в Финляндии. В ходе этой работы было оценено 33 309 случаев ИМ (контроль составили 138 949 лиц). Для нимесулида относительный риск развития этого тяжелого осложнения достигал 1,69, т. е. оказался близким к соответствующим значениям для мелоксикама, набуметона, этодалака и неселективных НПВП [14]. Комитет по лекарственным средствам, предназначенным для человека (Committee of Human Medicinal Products) пришел к выводу, что польза от нимесулида превышает риски от его использования, при условии, что он используется надлежащим образом. Данная организация рекомендует применять нимесулид для лечения острой боли и первичной дисменореи в максимальной суточной дозе 100 мг дважды в день и не более 15 дней подряд. Европейская комиссия также подтвердила положительный профиль безопасности нимесулида при вышеупомянутом режиме приема [15].
Что касается специфической боли в спине, то ее могут вызвать различные причины: новообразования, затрагивающие позвоночник (первичные и метастатические опухоли позвоночника, множественная миелома), сирингомиелия, деструкция позвонков и поражение нервных корешков вследствие инфекционных процессов (остеомиелит, эпидурит, туберкулезный спондилит), дисметаболические нарушения (гиперпаратиреоз, болезнь Педжета, остеопороз, остеомаляция), травматические повреждения позвонков, корешков, оболочек спинного мозга, патология внутренних органов ИМ, перикардит, пневмония, язвенная болезнь желудка и двенадцатиперстной кишки, панкреатит и др.). В таких ситуациях длительный прием анальгетиков и НПВП будет менее эффективным, что должно навести клинициста на мысль о развитии специфической боли в спине [5, 8].
Заподозрить наличие перечисленных заболеваний помогают «симптомы угрозы», к которым относят:
• начало стойкой боли в спине в возрасте до 15 и после 50 лет;
• отсутствие связи боли с движением (боль не уменьшается в покое, в положении лежа, в определенных позах);
• связь боли с травмой;
• постепенное усиление болей, ночные боли;
• наличие онкологического заболевания в анамнезе;
• возникновение боли на фоне лихорадки, снижения массы тела;
• жалобы на длительную скованность по утрам;
• симптомы поражения спинного мозга (параличи, тазовые нарушения, расстройства чувствительности);
• изменения в анализах крови, мочи;
• отсутствие ответа на консервативную терапию[2].
Неврологам и врачам других специальностей важно помнить, что причиной боли в спине могут стать различные заболевания, поэтому дифференциально-диагностический поиск необходим при ведении таких пациентов. Для иллюстрации сказанного приводим два клинических случая, истории болезни которых начинались с жалоб на боли в спине. Именно «остеохондроз» оказался в центре внимания, и попытки излечить пациентов не увенчались успехом.
Клинический случай 1.Пациентка П., 66 лет, госпитализирована в отделение гематологии и химиотерапии Республиканской клинической больницы (РКБ) г. Чебоксары 27.04.2016 г. с жалобами на значительное похудание (на 27 кг за последние 2 года), интенсивные постоянные, прогрессирующие боли в позвоночнике, ребрах, ключицах, костях таза, усиливающиеся при движениях, выраженную общую слабость, отеки нижних конечностей.
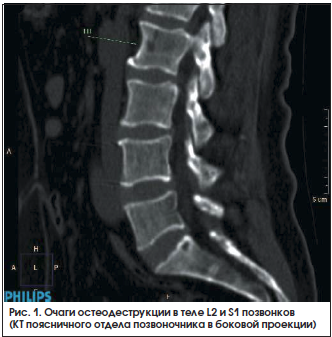
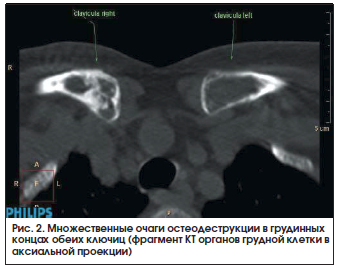
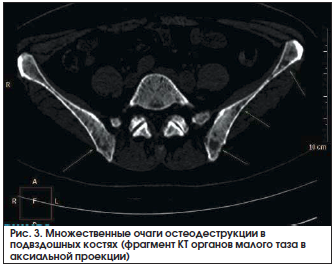
Из анамнеза заболевания: считает себя больной с октября 2013 г., когда при физической нагрузке стала отмечать появление болей в нижней части спины, при обращении к врачу-терапевту состояние было расценено как «остеохондроз поясничного отдела позвоночника». Проведение курса терапии НПВП и витаминами группы В привело к уменьшению интенсивности болей в спине, и в последующие полтора года пациентка к врачам не обращалась. Появление и нарастание общей слабости, связанные с этим (по мнению больной) частые падения, критическое снижение массы тела более чем на 20 кг при сохраненном аппетите (без соблюдения диеты), усиление болей в спине послужили поводом для повторного обращения пациентки в июне 2015 г. к врачу-терапевту. При проведении лабораторного обследования: в общем анализе крови выявлены нормохромная анемия легкой степени тяжести (гемоглобин 106 г/л) и повышение СОЭ до 99 мм/ч (по методу Вестергрена), в биохимическом анализе крови – повышение сывороточного уровня холестерина до 9,1 ммоль/л (при верхней границе нормы (ВГН) до 5,2 ммоль/л) и активности щелочной фосфатазы до 236 ЕД/л (при ВГН до 120 ЕД/л). В тот же период в общем анализе мочи выявлялась небольшая протеинурия до 0,1 г/л, а в протеинограмме – абсолютная гипогаммаглобулинемия (7,9%) при адекватном содержании общего белка в сыворотке крови (74,3 г/л). Однако изменение уровня белков в сыворотке крови и моче осталось без внимания, а диагностический поиск в первую очередь был направлен на исключение онкологического заболевания вследствие сохранения значительного повышения СОЭ. Со стороны верхних отделов желудочно-кишечного тракта, толстого кишечника, органов малого таза и молочных желез данных за онкологическое заболевание выявлено не было. Видя прогрессивное ухудшение общего состояния пациентки, продолжающуюся потерю массы тела, сохранение болей в позвоночнике и появление болей в костях таза слева, больше выраженные при движениях, родственники больной настояли на проведении КТ органов грудной клетки, брюшной полости и малого таза. При проведении в конце ноября 2015 г. КТ с контрастированием были обнаружены внутригрудная лимфаденопатия (при отсутствии увеличения забрюшинных и внутрибрюшных лимфоузлов), в костях скелета – множественные очаги остеодеструкции в телах шейных, поясничных, крестцовых позвонков (рис. 1), грудинного конца обеих ключиц (рис. 2), местами с деструкцией кортикального слоя кости, в том числе в области крыши вертлужной впадины слева размерами до 27×11×26 мм (рис. 3).
При проведении лабораторного исследования отмечались нарастание выраженности анемического синдрома (гемоглобин 85 г/л при отсутствии дефицита сывороточного уровня железа), повышение активности щелочной фосфатазы (до 256,6 ЕД/л), уровня мочевины (10,2 ммоль/л) и креатинина (114,7 мкмоль/л) в сыворотке крови, снижение скорости клубочковой фильтрации (СКФ) до 25,5 мл/мин, появление гиперкальциемии (содержание общего кальция в сыворотке крови составило 2,9 ммоль/л при ВГН до 2,55 ммоль/л). По-прежнему сохранялись повышение СОЭ (до 91–116 мм/ч), протеинурия (0,79 г/л), гипоальбуминемия и абсолютная гипогаммаглобулинемия (5,3% от общего количества белка 67,8 г/л). Назначение пероральных препаратов железа не привело к купированию анемического синдрома, уровень гемоглобина колебался в пределах от 91 до 102 г/л.
В свете выявленных изменений (диффузного остеолитического, вероятно, метастатического поражения костей скелета) и гиперкальциемии диагностический поиск был направлен на выявление первичной локализации злокачественного новообразования. В качестве альтернативных диагнозов рассматривались саркоидоз легких и внутригрудных лимфоузлов и аденома паращитовидных желез.
При проведении в декабре 2015 г. сцинтиграфии костей скелета с 99mТехнецием-Пирфотехом в Республиканском клиническом онкологическом диспансере (РКОД) г. Чебоксары были выявлены множественные, хаотично распределенные участки остеопении с сохранением кортикального слоя костей без признаков накопления радионуклида (без изменения уровня костного метаболизма) и консолидированные патологические переломы грудинного конца ключицы справа и переднего отрезка V ребра справа. Тестируемые онкомаркеры (раково-эмбриональный антиген, бета-субъединица хорионического гонадотропина человека, альфа-фетопротеин, СА 125, СА 15-3) оказались отрицательными, что позволило онкологам опровергнуть диагноз онкологического заболевания.
Для уточнения причины гиперкальциемии пациентка в декабре 2015 г. последовательно была госпитализирована в пульмонологическое и эндокринологическое отделения лечебно-профилактических учреждений г. Чебоксары. Повторное определение уровня кальция в сыворотке крови продемонстрировало сохранение гиперкальциемии (содержание общего кальция в сыворотке крови составило 3,15 ммоль/л) при неизмененном содержании фосфора в крови (1,2 ммоль/л). Выявлено более чем двукратное повышение сывороточного уровня паратиреоидного гормона (ПТГ) (до 161 пг/мл при должных референсных значениях 8,3–68,0 пг/мл). Диагноз трактовали как «вторичный гиперпаратиреоз, вероятно, на фоне паранеопластического процесса». При этом не было уделено должного внимания сохраняющейся анемии (гемоглобин 96 г/л), гипоальбуминемии и протенурии (0,5–0,79 г/л) при нарастании содержания в сыворотке крови креатинина (187 мкмоль/л) и мочевины (11,5 ммоль/л). В тот период у пациентки впервые появились и стали нарастать периферические отеки.
Проведено УЗИ щитовидной и паращитовидных желез в РКОД в январе 2016 г. Был обнаружен узел в правой доле щитовидной железы размерами 9×6 мм повышенной эхогенности, окруженный гипоэхогенным ободком с кистозными включениями. От проведения тонкоигольной аспирационной биопсии пациентка отказалась. Паращитовидные железы, равно как и шейные лимфоузлы, не визуализировались.
В стационарных и амбулаторных условиях проводилась лишь симптоматическая терапия, направленная на коррекцию анемического и гипертонического синдромов. Несмотря на проводимое лечение, сохранялись нормохромная нормоцитарная анемия средней степени тяжести (гемоглобин 84 г/л), повышение СОЭ до 120 мм/ч, нарастала гипопротеинемия (общий белок 58,3 г/л) и протеинурия (0,945 г/л).
Пациентка для верификации диагноза «первичный гиперпаратиреоз» была направлена на консультацию в Республиканский эндокринологический диспансер (РЭД) г. Чебоксары в феврале 2016 г. Повышение уровня ПТГ без гиперплазии паращитовидных желез, по данным УЗИ, и с учетом редких эпизодов нормокальциемии, по всей вероятности, носило вторичный характер на фоне снижения функции почек (хроническая болезнь почек) и дефицита витамина D. При проведении двухэнергетической рентгеновской абсорбциометрии центральных отделов скелета выявлено преимущественное снижение минеральной плотности костной ткани (МПКТ) в поясничном отделе позвоночника (L1-L4): Т–критерий составил –3,6 стандартного отклонения (SD). Учитывая нарастающую гипопротеинемию (общий белок 50,6 г/л) с гипоальбуминемией (27,2 г/л), гиперальфа-2-глобулинемией (22,3%) и гипогаммаглобулинемией (4,4%), резко выраженное снижение СКФ (до 28 мл/мин) на фоне суточной потери белка до 1,83 г/л, пациентке рекомендовано дообследование для исключения заболеваний почек и системы крови.
По мнению нефролога РКБ, поражение почек явно носило вторичный (паранеопластический) характер. В условиях поликлиники РКБ в апреле 2016 г. врачом-гематологом была проведена стернальная пункция, при этом в костном мозге было обнаружено 78,5% плазматических клеток, что явилось одним из критериев для верификации диагноза «множественной миеломы» (ММ). Больная была госпитализирована в отделение гематологии и химиотерапии РКБ для проведения первого курса полихимиотерапии.
При поступлении в стационар общее состояние расценивалось как средней степени тяжести, пациентка астенического телосложения, индекс массы тела составил 19,5 кг/м2. Кожные покровы и видимые слизистые оболочки бледные. Периферические лимфоузлы не пальпировались. Гипотрофия мышц верхних и нижних конечностей. Периферические отеки в области нижних конечностей до верхней трети голени.
При проведении лабораторных методов исследования выявлены нормохромная анемия средней степени тяжести (гемоглобин 81 г/л), повышение СОЭ (по методу Вестергрена) до 105 мм/ч, протеинурия 1,9 г/л, гиперкреатининемия (151 мкмоль/л), азотемия (мочевина сыворотки 14,2 ммоль/л), гипопротеинемия (содержание общего белка в сыворотке крови 57 г/л), диспротеинемия (альфа-2-глобулины 16,96%, гамма-глобулины 9,35%), снижение сывороточного уровня железа (7,9 мкмоль/л), гиперфибриногенемия (7,49 г/л), снижение всех основных фракций иммуноглобулинов (Ig) (IgA 0,31 мг/мл (референсные значения 0,9–2,5 мг/мл), IgM 0,03 мг/мл (референсные значения 0,6–2,8 мг/мл), IgG 2,9 мг/мл (референсные значения 8–18 мг/мл). Учитывая стойко сохраняющуюся протеинурию, для выявления моноклональных легких цепей в моче был выполнен электрофорез белков мочи с иммунофиксацией. При проведении данного метода был обнаружен белок Бенс-Джонса типа каппа.
Согласно Национальным клиническим рекомендациям по диагностике и лечению ММ [16], при установлении диагноза симптоматической ММ учитываются критерии, разработанные Международной группой по изучению ММ (IMWG) и пересмотренные в 2014 г. (табл. 1).
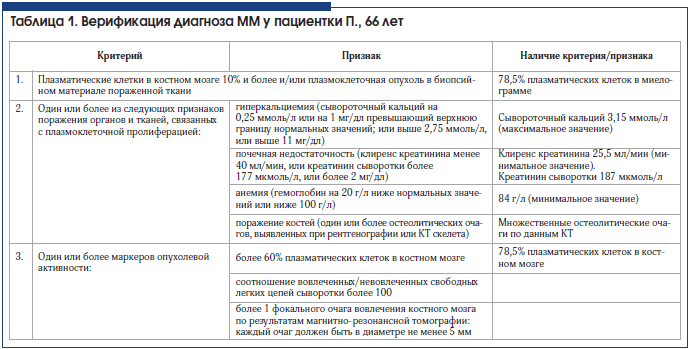
Таким образом, у пациентки П. присутствовали все 3 критерия ММ, что позволило установить диагноз злокачественного лимфопролиферативного заболевания – множественная миелома, протекающая с протеинурией Бенс-Джонса типа каппа, распространенным остеодеструктивным процессом, анемией III стадии (Durie-Salmon). Хроническая болезнь почек С4 А3 (СКФ 28 мл/мин по формуле MDRD). В условиях отделения гематологии и химиотерапии РКБ был проведен первый курс химиотерапии с включением циклофосфамида и дексаметазона.
Клинический случай 2. Пациент Ч., 53 года, считает себя больным около 3-х лет, когда стали беспокоить боли в пояснице. Травмы отрицает. За последние полтора года отмечает снижение роста с изменением осанки, резкое ограничение физической активности. Для уменьшения осевой нагрузки при ходьбе стал пользоваться тростью.
Наблюдался у участкового терапевта и врача общей практики по поводу гипертонической болезни с 2010 г., в 2012 г. проходил лечение по поводу язвенной болезни луковицы двенадцатиперстной кишки. С 2013 г. по поводу «остеохондроза», полиостеоартроза получал НПВП, миорелаксанты, «хондропротекторы» с кратковременным положительным эффектом. В общеклинических и биохимических анализах врачом первичного звена патологических изменений не выявлено, однако обращает на себя внимание гиперкальциемия (содержание общего кальция в сыворотке крови в апреле 2014 г. составило 2,99 ммоль/л). По данным МРТ пояснично-крестцового отдела позвоночника, проведенной в июне 2014 г., отмечаются дорзальные диффузные протрузии дисков L4-L5, L5-S1 размерами до 0,3 см, распространяющиеся в межпозвонковые отверстия с обеих сторон, краевые заострения замыкательных пластинок тел позвонков, грыжи Шморля тел L1, L5 позвонков, форма и размеры тел позвонков обычные, признаки дистрофических изменений в телах позвонков. Через год из-за изменения характера болей в спине (усиление болей с иррадиацией в правую ягодичную область при движении с резким ограничением движения вплоть до обездвиженности) в июле 2015 г. проведена МРТ крестцово-подвздошных сочленений и тазобедренных суставов. Выявлены признаки двустороннего сакроилеита, не сопровождавшегося изменением острофазовых показателей крови, в т. ч. изменениями в протеинограмме, и обнаружением генетического маркера серонегативных спондилоартритов (HLA-B27). Из-за сохраняющегося болевого синдрома и ухудшения состояния в марте 2016 г. был госпитализирован в ревматологическое отделение РКБ (Чебоксары). Выявлено повышение уровня кальция сыворотки до 3,32 ммоль/л (при ВГН 2,55 ммоль/л). Подозрение на манифестную форму первичного гиперпаратиреоза (ПГПТ) было подтверждено результатами исследования уровня паратгормона сыворотки крови (1912 пг/мл при ВГН 65 пг/мл), и пациент был направлен на дообследование.
Консультирован врачом-терапевтом кабинета профилактики и лечения остеопороза ФЦТОЭ и эндокринологом РЭД (Чебоксары) 04.04.2016 г. На момент осмотра предъявлял жалобы на постоянные боли в поясничной области, иррадиирующие в правую ягодичную область, усиливающиеся при длительной статической нагрузке, работе с наклоном, изменении положения тела, уменьшающиеся в положении лежа, нарушение осанки, снижение роста, боли в костях конечностей и ребер, общую слабость, снижение качества жизни.
При объективном осмотре: состояние больного расценено как относительно удовлетворительное. Положение вынужденное с опорой на трость. Обращали на себя внимание укороченное туловище, по боковым поверхностям множественные кожные складки (симптом «елки»), усиление грудного кифоза, расстояние «затылок – стена»≫ составило 6 см, ребра располагаются на гребнях подвздошных костей, выпячивание живота, болезненность при пальпации и перкуссии остистых отростков позвонков, ограничение движений в грудном, поясничном отделах позвоночника. Рост – 168 см, масса 80 кг, ИМТ 28,37 кг/м2. Отмечает снижение роста на 11 см по сравнению с ростом в молодости, что послужило поводом для проведения рентгенографии грудного и поясничного отделов позвоночника с целью выявления компрессионных переломов позвонков [17].
Щитовидная железа безболезненная, диффузно увеличена, чуть более за счет левой доли, где в нижней половине пальпируется неплотное узловое образование, неспаянное с окружающими тканями. По остальным органам и системам – без особенностей.
В общеклинических анализах крови и мочи – без патологии. В биохимическом анализе крови обращает на себя внимание гиперкальциемия (3,25 ммоль/л), гипофосфатемия (0,43 ммоль/л). На рентгенограмме, КТ поясничного отдела позвоночника выявлено выраженное снижение высоты тел Th10, Th11, Th12, L1, L2, L3 позвонков, деформация по типу «рыбьих», деформация позвоночника по типу углового кифоза с вершиной в Th12, диффузный остеопороз (рис. 4).
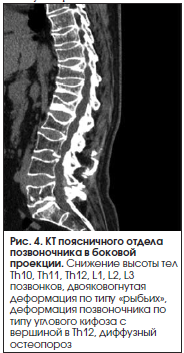
При проведении двухэнергетической рентгеновской абсорбциометрии выявлено снижение МПКТ в поясничных позвонках (L1-L4), Т-критерий составил –2,6 SD, а также снижение МПКТ в проксимальном отделе бедренной кости (neck): Т-критерий равен –4,2 SD, что соответствует тяжелой форме остеопороза [16].
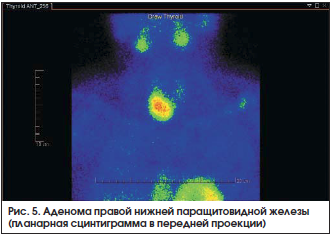
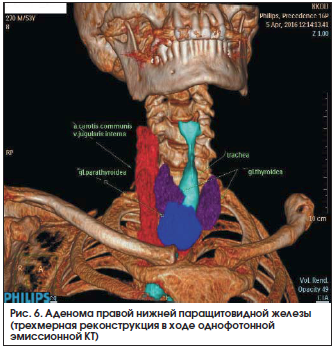
С целью дифференциальной диагностики заболеваний, сопровождающихся гиперкальциемией и изменениями МПКТ (табл. 2), проведено УЗИ щитовидной и паращитовидных желез [18]. В нижней трети левой доли обнаружено изоэхогенное образование размерами 21×12×15 мм с гипоэхогенным ободком и анэхогенным включением, при ЦДК определялся интра- и перинодальный кровоток. По нижнему контуру перешейка и правой доли визуализировалось гипоэхогенное образование размерами 40×38×22 мм диффузно неоднородной структуры с загрудинным ростом, кроме того, при ЦДК определялись сосуды с венозным и артериальным спектром кровотока внутри образования. По данным сцинтиграфии с MIBITc99m Технетрилом с последующей однофотонной эмиссионной КТ выявлены: гиперфиксация радиофармпрепарата в проекции нижнего полюса правой доли щитовидной железы (рис. 5) и овальное образование с четкими ровными контурами размерами 40×25 мм однородной структуры, локализующееся под правой долей щитовидной железы спереди от трахеи на уровне тел С5-C7 (рис. 6). Дополнительно по КТ-изображениям определялись участки деструкции в правой лопатке, акромиальном конце ключицы с нарушением целостности кортикального слоя, выраженные признаки дегенеративно-дистрофических изменений шейного отдела позвоночника, срастающийся перелом средней трети левой ключицы.
![Таблица 2. Причины гиперкальциемии [20] Таблица 2. Причины гиперкальциемии [20]](/upload/medialibrary/85d/85d3f74739755827c79cd0b6ea5f0fa0.png)
При проведении эзофагогастродуоденоскопии с целью выявления поражения органов-мишеней (табл. 3) подтверждена язвенная деформация луковицы двенадцатиперстной кишки. УЗИ почек выявило признаки нефрокальциноза (при этом нефролитиаз обнаружен не был).
![Таблица 3. Симптомы гиперкальциемии [17, 19] Таблица 3. Симптомы гиперкальциемии [17, 19]](/upload/medialibrary/f92/f92886f850e20df1e3b0a3555343e448.png)
Учитывая повторное повышение уровня кальция сыворотки крови выше ВГН на 0,25 ммоль/л, гипофосфатемию, повышение уровня паратгормона [19–21], ультразвуковые признаки аденомы правой паращитовидной железы, подтвержденные данными сцинтиграфии, выявление остеопороза по результатам остеоденситометрии, наличие компрессионных переломов тел Th10, Th11, Th12, L1, L2, L3 позвонков, язвенное поражение верхних отделов ЖКТ, пациенту был выставлен диагноз «первичный гиперпаратиреоз, манифестная костно-висцеральная форма (язвенная болезнь луковицы двенадцатиперстной кишки в стадии рубцовых изменений; вторичный остеопороз, тяжелая форма, с компрессионными переломами тел Th10, Th11, Th12, L1, L2, L3 позвонков, с преимущественным снижением МПКТ в проксимальном отделе бедра (Т-критерий –4,2 SD), средней степени тяжести. Аденома правой нижней паращитовидной железы».
В апреле 2016 г. в Республиканском клиническом госпитале для ветеранов войн (Чебоксары) выполнена паратиреоидэктомия справа и гемитиреоидэктомия слева. При патогистологическом исследовании подтверждена аденома паращитовидной железы. Ранний послеоперационный период протекал без осложнений, на 2-е сутки после операции уровень кальция сыворотки крови составил 2,42 ммоль/л, на 4-е – 2,2 ммоль/л, уровень паратиреоидного гормона снизился до 78,1 пг/мл. Пациент выписан под наблюдение хирурга и эндокринолога.
Обсуждение. Описанный случай наглядно демонстрирует развитие болей в нижней части спины вследствие низкоэнергетических компрессионных переломов тел позвонков на фоне вторичного остеопороза при аденоме паращитовидной железы, сопровождающейся развитием ПГПТ. Гиперпродукция ПТГ стимулирует резорбцию костной ткани, что проявляется развитием ведущего диагностического синдрома – синдрома гиперкальциемии, и является наиболее частой ее причиной. Причины гиперкальциемии представлены в таблице 2.
Настороженность врачей первичного звена в отношении синдрома гиперкальциемии в представленных случаях позволила бы своевременно установить диагноз и начать эффективное лечение, а также избежать таких осложнений, как прогрессирующая почечная недостаточность, компрессионные переломы тел позвонков. Считаем важным напомнить врачам первичного звена симптомы и признаки, сопровождающие синдром повышения сывороточного кальция (табл. 3).
В настоящее время ПГПТ является третьим по распространенности после сахарного диабета и патологии щитовидной железы эндокринным заболеванием и одной из наиболее частых причин остеопороза и переломов среди вторичных остеопатий. ПГПТ относится к социально значимым проблемам в связи с вовлечением в патологический процесс большинства органов и систем, высоким риском инвалидизации и преждевременной смерти, а также снижением качества жизни у пациентов вне зависимости от формы заболевания, обусловленным как наличием костно-висцеральных проявлений различной степени выраженности, так и неспецифическими нарушениями в психоэмоциональной сфере [20].
Множественная миелома — злокачественное лимфопролиферативное заболевание, характеризующееся клональной пролиферацией опухолевых плазматических клеток в костном мозге, сопровождающееся секрецией моноклонального иммуноглобулина, определяемого в сыворотке и/или в моче (М-протеин), и поражением органов-мишеней и тканей (гиперкальциемия, почечная недостаточность, анемия и литическое поражение костей). ММ составляет приблизительно 1% среди всех злокачественных опухолей и около 13% среди опухолей кроветворной и лимфоидной тканей. В России в 2009 г. впервые диагностировано 2723 случая, умер 1991 больной. Медиана общей выживаемости больных ММ за последние годы увеличилась приблизительно с 3 до 7 лет благодаря ранней диагностике и появлению новых лечебных подходов, ставших доступными для большинства пациентов [16].
Таким образом, всем пациентам с болями в нижней части спины необходимо проводить дифференциально-диагностический поиск с целью исключения специфического характера болей, направленный на выявление «симптомов угрозы» с установлением причины заболевания. Большое внимание следует уделять сбору анамнеза и данным объективного исследования. Еще великий основатель русской педиатрической школы Н.Ф. Филатов напоминал ученикам: «Не забудьте снять ребенку чулки, диагноз может быть в чулках». Так и в случае с пациентом Ч., 53 года, «диагноз был в измерении роста и во внимании к симптому гиперкальциемии».
Проведение лабораторно-инструментальной диагностики, включающей определение уровня сывороточного кальция, фосфора, щелочной фосфатазы, белковых фракций, проведение двухэнергетической рентгеновской денситометрии, позволит на ранних стадиях заподозрить остеопороз и другие метаболические заболевания скелета и своевременно начать терапию, а также предупредить развитие осложнений, приводящих к ранней инвалидизации и летальному исходу.
В случае отсутствия «симптомов угрозы» приоритетной стратегией для больного должно стать адекватное обезболивание с применением эффективных и безопасных препаратов, например нимесулида.












