Диспансерный метод – это активное динамическое наблюдение за состоянием здоровья определенных контингентов населения (здоровых и больных), взятие этих групп населения на учет с целью раннего выявления заболеваний, комплексного лечения заболевших, проведения мероприятий по оздоровлению условий их труда и быта, предупреждение развития и распространения болезней, восстановление трудоспособности и продление периода активной жизнедеятельности [1, 11].
Основная задача диспансеризации – предупреждение рецидивов, обострений и осложнений имеющихся заболеваний (вторичная профилактика) [1].
Профилактическая специализированная помощь гарантирована гражданам нашей страны Федеральным законом «Об обязательном медицинском страховании в Российской Федерации» (№ 326-ФЗ от 29.11.2010 г.). Однако этот документ не содержит рекомендаций по проведению такой профилактической работы. Единственным документом, регламентирующим работу врача-специалиста в области профилактики и диспансеризации, является приказ Министерства здравоохранения СССР от 30.05.1986 г. № 770 «О порядке проведения всеобщей диспансеризации населения». В нем изложена «Примерная схема динамического наблюдения за лицами, подлежащими наблюдению у врача-терапевта и врачей терапевтического профиля, у врача-невропатолога». Несмотря на то, что в данный документ неоднократно вносились изменения и дополнения, прописанные в нем кратность осмотров пациентов с эпилепсией, перечень необходимых мероприятий для эффективного динамического наблюдения явно устарели и не соответствуют современным представлениям об эпилептогенезе. Кроме того, названный приказ не учитывает необходимость наблюдения пациентов с доклиническими стадиями эпилепсии в виде изолированных приступов, острых ситуационных приступов в структуре различных неврологических заболеваний, а также случаев заболеваний, при которых возникновение эпилептических приступов возможно в восстановительном периоде (черепно-мозговая травма (ЧМТ), острые нарушения мозгового кровообращения (ОНМК), нейроинфекции).
В советский период предпринимались попытки профилактировать развитие эпилепсии у детей с судорожным синдромом назначением превентивной противоэпилептической терапии [А.М. Коровин, 1984; А.Ю. Ратнер, 1985]. Однако анализ современной зарубежной и отечественной литературы позволяет сделать вывод о неэффективности такого подхода [3, 4, 8].
Все это обусловливает необходимость разработки новых организационных технологий, направленных на профилактику эпилепсии, и динамического наблюдения больных в соответствии с последними достижениями в области эпилептологии.
Общеизвестно, что профилактическое лечение противоэпилептическими препаратами (ПЭП) неэффективно [8]. Понимая значение высокого уровня симптоматической эпилепсии [10, 15], специалисты разработали алгоритм ведения угрожаемых по развитию симптоматической локально обусловленной эпилепсии (СЛОЭ). С этой целью создана и внедрена модернизированная шкала эпилептогенности, в основу которой положены диагностические признаки эпилептогенности ЧМТ, предложенные Г.Н. Авакян и соавт. [3]. В ней нашли отражение вопросы клиники и диагностики посттравматической симптоматической эпилепсии. Нами разработаны унифицированные диагностические критерии шкалы эпилептогенности основных неврологических заболеваний, при которых наблюдаются эпилептические приступы (табл. 1).
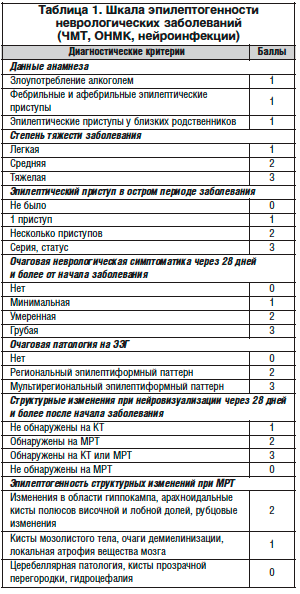
Принципиальным отличием разработанной нами шкалы от уже имеющейся является то, что диагностические признаки эпилептогенности ЧМТ позволяют рассматривать травму в качестве причины уже возникшей эпилепсии, тогда как шкала эпилептогенности основных неврологических заболеваний является прогностически-профилактической. Использование данных критериев и их оценка по балльной системе привели к изменению общепринятой схемы наблюдения за пациентами, перенесшими эти заболевания.
Материалы и методы
Нами были проанализированы данные анамнеза, клинического течения заболевания, данные инструментальных методов исследования (электроэнцефалография (ЭЭГ), компьютерная (КТ) и магнитно-резонансная (МРТ) томография) 612 пациентов, перенесших 2 и более года назад ОНМК, ЧМТ и нейроинфекции. Среди них 362 пациента (59,0%), перенесших инсульт (10 – с субарахноидальным кровоизлиянием, 30 – с внутримозговым кровоизлиянием, 322 – с инфарктом мозга), 26 (4,2%) – перенесших нейроинфекции и 224 (36,8%) – ЧМТ различной степени тяжести. Все эти пациенты обращались на амбулаторный прием в течение 12 мес. по разным причинам (ухудшение состояния, плановое лечение, очередное освидетельствование на медико-социальной экспертизе (МСЭ) и др.). В 129 (21%) случаях обратившихся выявлена СЛОЭ, которая развилась в течение 4,8±3,2 года от начала заболевания. Известно, что более чем в 80% случаев симптоматическая эпилепсия развивается в срок до 18 мес. [12, 19], поэтому нами анализировались случаи заболевания с катамнезом не менее 2-х лет.
Результаты
В ходе исследования выявлены определенные закономерности развития эпилепсии в данной группе больных. Наиболее значимыми факторами развития эпилепсии были злоупотребление алкоголем, наличие приступов в остром периоде, тяжесть заболевания, тяжесть неврологического дефицита в восстановительном периоде, эпилептиформные изменения на ЭЭГ и подтверждение структурного дефекта методами нейровизуализации. В зависимости от значимости каждого фактора ему присваивался балл (от 0 до 3), и составлялась шкала эпилептогенности основных неврологических заболеваний, представляющая собой опросник из 7 вопросов и 24 вариантов ответов, которые суммировались. Максимальная сумма баллов – 17, минимальная – 2 (табл. 1).
По данным нашего исследования, вероятность развития СЛОЭ определяется следующим образом: «сомнительно» – при сумме баллов <8 (риск развития эпилепсии составляет 1,5%±0,02%), «вероятно» – при сумме баллов ≥8 (риск – 8,1%±0,05%). Пациенты с суммой баллов >8 являются угрожаемыми по развитию СЛОЭ.
Согласно разработанному алгоритму, неврологам амбулаторной сети было предложено тестирование по шкале эпилептогенности всех пациентов, перенесших ЧМТ, ОНМК, нейроинфекции. При наличии ≥8 баллов больные направлялись для дальнейшего наблюдения в эпилептологический кабинет. Алгоритм взаимодействия невролога и эпилептолога при использовании шкалы эпилептогенности представлен на рисунке 1.
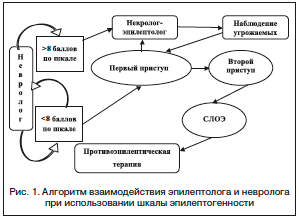
Основным условием для тестирования по шкале эпилептогенности было проведение всех необходимых инструментальных исследований (КТ, МРТ, ЭЭГ). Поэтому в исследование были включены 202 пациента, которым могли быть выполнены (с учетом тяжести состояния и возможностей лечебного учреждения) и были проведены все необходимые инструментальные исследования. Срок наблюдения составил 18 мес.
В 108 случаях (53,4%) итоговый балл оценки эпилептогенности не достигал 8, и эти пациенты продолжали наблюдаться у неврологов. У 94 пациентов (46,6%) при тестировании был зафиксирован балл оценки эпилептогенности выше 8, что расценивалось как угроза развития симптоматической эпилепсии, больные были направлены в эпилептологический кабинет. Среди них 56 пациентов после ЧМТ (25,0% от общего числа пациентов с ЧМТ), 34 – перенесших ОНМК (9,3% от общего числа пациентов с ОНМК) и 4 – после нейроинфекции (15,3% от общего числа пациентов с нейроинфекцией).
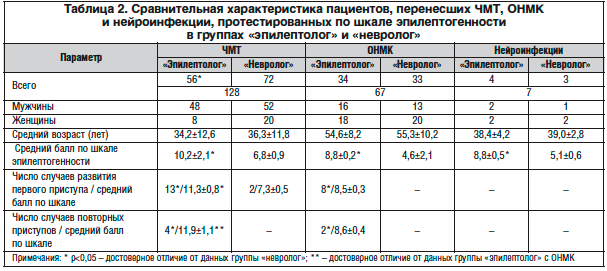
В таблице 2 представлена характеристика пациентов, протестированных по шкале эпилептогенности, которые продолжали наблюдение у невролога общей поликлинической сети (группа «невролог»), или были направлены для наблюдения в специализированные кабинеты (группа «эпилептолог»).
Анализ структуры протестированных пациентов показал однородность групп по возрасту, полу и гендерному соотношению, за исключением количества пациентов с ЧМТ (в группе наблюдения «невролог» было достоверно большее число таких пациентов). У больных, направленных к эпилептологу, средний балл оценки был достоверно выше, чем у пациентов, которые наблюдались неврологом поликлиники, особенно среди перенесших ОНМК.
Анализ результатов наблюдения в группах пациентов «невролог» и «эпилептолог» выявил, что первый эпилептический приступ развился в 23 случаях (11,3% от общего числа протестированных) в срок 7,4±4,3 мес. Причем в группе наблюдения «невролог» (общий балл оценки по шкале эпилептогенности не превышал 8 баллов), зарегистрировано 2 случая (0,9% от общего числа протестированных) дебюта приступов. Приступы развились у пациентов, перенесших ЧМТ, с общим баллом оценки 7,3±0,5. Вероятнее всего, имела место недооценка данных ЭЭГ, МРТ и анамнеза.
В группе «эпилептолог» с общим баллом оценки по шкале эпилептогенности 9,4±1,1 приступы развились в 21 случае (10,3%). Все это коррелирует с исходными данными тестирования по шкале эпилептогенности в группах и подтверждает эффективность тестирования для прогнозирования эпилептических приступов в восстановительном периоде ЧМТ, ОНМК и нейроинфекции. Обращает на себя внимание более высокий балл у пациентов, перенесших ЧМТ, в сравнении с пациентами после ОНМК и нейроинфекций.
При анализе анкет пациентов, перенесших ЧМТ, выявлено, что у них значительно чаще, чем у пациентов с ОНМК и нейроинфекцией, регистрировались факторы риска: злоупотребление алкоголем (65,0% от общего числа пациентов с ЧМТ и 14,0–17,0% от числа пациентов с ОНМК и нейроинфекцией соответственно), наследственная отягощенность (11,0% – у пациентов с ЧМТ и 2,0% – с ОНМК). Этот факт, вероятно, может объяснить более частое, в сравнении с другими пациентами, возникновение симптоматической эпилепсии после перенесенной ЧМТ [3].
Всех пациентов с первым приступом после перенесенной ЧМТ, ОНМК и нейроинфекции мы рекомендуем наблюдать по следующей схеме:
1. ЭЭГ по стандартной методике – 1 р./6 мес., а при наличии эпилептиформного паттерна – 1 р./3 мес.
2. Консультации терапевта, инфекциониста и нейрохирурга (в зависимости от основного заболевания) – 1 р./год (по показаниям – чаще).
3. Курсы нейрометаболической терапии – 1–2 р./год (в зависимости от тяжести течения основного заболевания).
4. Рациональное трудоустройство (не рекомендован труд в ночные смены и с частой сменой часовых поясов).
5. Разработка индивидуальных рекомендаций.
У 6 пациентов (2,9% от общего числа протестированных по шкале, 26,0% от числа пациентов с первым приступом в восстановительном периоде) из группы «эпилептолог» с первым приступом в течение 3±2,6 мес. зарегистрированы повторные приступы, им была назначена противоэпилептическая терапия. В 4 случаях (3,1% от числа пациентов с ЧМТ) дебютировала посттравматическая эпилепсия (средний балл по шкале – 10,9±1,1), в 2 случаях (2,9% от числа ОНМК) – постинсультная эпилепсия (инфаркт мозга со средним баллом по шкале 8,6±0,4).
При назначении ПЭП мы руководствовались общепринятыми правилами: типом эпилептических приступов, локализацией эпилептогенного очага, весом, возрастом, полом [7, 9, 13]. Длительность наблюдения за этими пациентами составила от 3 до 5,5 мес. и связана с периодом стабилизации состояния (необходимость наблюдения 2–3 межприступных интервалов [16]). 2 пациента (33%) получали топирамат в средней дозе 118±26 мг/сут, 2 – пролонгированный карбамазепин в средней дозе 817±123 мг/сут, 1 – пролонгированный вальпроат натрия в дозе 1000 мг/сут. За время наблюдения и лечения приступов и нежелательных явлений не наблюдалось. Таким пациентам рекомендуется наблюдение по следующей схеме:
1. Наблюдение неврологом-эпилептологом с кратностью посещений – 1 р./3 мес.
2. Общие анализы крови и мочи, биохимический анализ крови, терапевтический лекарственный мониторинг ПЭП – 1 р./3 мес. (по показаниям – чаще).
3. ЭЭГ – 1 р./3 мес. (по показаниям – чаще).
4. Консультация психолога, психотерапевта – 1 р./6 мес.
5. Консультация психиатра, нейрохирурга – 1 р./год (по показаниям – чаще).
6. Курсы нейрометаболической, симптоматической терапии – 1–2 р./год (в зависимости от тяжести течения основного заболевания).
7. Рациональное трудоустройство. При необходимости – консультация МСЭ с целью определения группы инвалидности и разработки программы реабилитации инвалида.
8. Решение вопросов лекарственного обеспечения (включение пациента в регистр региональных льготников или обеспечение ПЭП по программе дополнительного лекарственного обеспечения).
9. При наличии стойкой медикаментозной ремиссии через 1 год – наблюдение в общей сети и консультация эпилептолога 1 р./год.
В 62 случаях (66,0% от общего числа пациентов группы «эпилептолог») больные, у которых приступы не повторялись, продолжили наблюдение неврологом-эпилептологом городского кабинета в группе угрожаемых по развитию симптоматической эпилепсии. Этим пациентам рекомендовано:
1. ЭЭГ по стандартной методике – 1 р./12 мес., а при наличии эпилептиформного паттерна – чаще.
2. Консультация терапевта, инфекциониста и нейрохирурга (в зависимости от основного заболевания) – 1 р./год.
3. Курсы нейрометаболической терапии – 1–2 р./год (в зависимости от тяжести течения основного заболевания).
4. Рациональное трудоустройство (не рекомендован труд в ночные смены и с частой сменой часовых поясов).
5. Разработка индивидуальных рекомендаций.
Срок наблюдения составляет 18 мес. и связан с закономерностями эпилептогенеза [3, 12, 20]. Если по истечении 18 мес. приступы не развиваются, то пациенты должны быть направлены для дальнейшего наблюдения к неврологу поликлиники, им следует наблюдаться в соответствии с планом диспансерного наблюдения по основному заболеванию.
Такой план в каждом конкретном случае разрабатывается с учетом клинической ситуации. Кратность осмотров пациентов с дебютом симптоматической эпилепсии (1 р./3 мес.) обусловлена необходимостью первичного назначения ПЭП с эскалацией дозы, на которую потребуется от 7 дней до 4–8 нед., в части случаев – до 12 нед. (при применении топираматов, ламотриджинов). В дальнейшем осмотр пациентов с этой кратностью является, на наш взгляд, оптимальным, т. к. позволяет в полной мере оценить динамику эпилептического процесса.
Показание для более частого проведения ЭЭГ – наличие регионального эпилептиформного паттерна с феноменом вторичной билатеральной синхронизации. Это может являться поводом для пересмотра схемы терапии (например, замена карбамазепина на вальпроат) или коррекции дозы базового препарата. Частота консультаций специалистов терапевтического и нейрохирургического профиля обусловлена необходимостью динамического наблюдения и возможной коррекции схемы терапии (например, гипертонической болезни), решения вопроса о пластинировании дефекта свода черепа, проведения КТ или МРТ и т. д. При стабильном течении основного заболевания осмотр этими специалистами 1 р./год считаем достаточным с учетом основных звеньев эпилептогенеза [3].
Внедрение нами в поликлиническую практику тестирования по шкале эпилептогенности и ведение пациентов, угрожаемых по развитию СЛОЭ, согласно разработанному алгоритму, позволили снизить риск ее развития в 3 раза. Так, до внедрения описываемых превентивных технологий частота посттравматической эпилепсии у наблюдавшихся нами больных составляла 11%, а постинсультной эпилепсии – 10%, что сопоставимо с данными по России: 9–12% [2, 3, 6, 20] и 8,9–11% [12, 18, 23, 24] соответственно. Через 1,5 года применения предложенных нами технологий частота развития эпилепсии после ОНМК составила 3,1%, после ЧМТ – 2,9%. В процессе работы нам удалось оптимизировать помощь при впервые диагностированной симптоматической эпилепсии, сделать ее максимально ранней и эффективной. Все пациенты (6,0% от числа угрожаемых по симптоматической эпилепсии) получают ПЭП в монотерапии в среднетерапевтической дозировке (без нежелательных явлений) и находятся в состоянии стойкой медикаментозной ремиссии.
Таким образом, все вышеизложенное подтверждает необходимость продолжения работы по выявлению пациентов, угрожаемых по развитию симптоматической эпилепсии, в случае возникновения таковой – профилактирование ее трансформации в труднокурабельную резистентную форму.












