–Т –Њ—В–µ—З–µ—Б—В–≤–µ–љ–љ–Њ–є –Ї–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є–Є —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –њ–Њ–і —В–µ—А–Љ–Є–љ–Њ–Љ «–і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П» –њ–Њ–љ–Є–Љ–∞—О—В –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й—Г—О –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М –Ї—А–Њ–≤–Њ—Б–љ–∞–±–ґ–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—А–Є–≤–Њ–і—П—Й—Г—О –Ї —Б—В—А—Г–Ї—В—Г—А–љ—Л–Љ —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л–Љ –Є–Ј–Љ–µ–љ–µ–љ–Є—П–Љ –Є –≤–Њ–Ј–љ–Є–Ї–љ–Њ–≤–µ–љ–Є—О –Њ—З–∞–≥–Њ–≤—Л—Е –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —А–∞—Б—Б—В—А–Њ–є—Б—В–≤ [10]. –Ф–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П (–Ф–≠) – —Б–Є–љ–і—А–Њ–Љ –њ—А–Њ–≥—А–µ—Б—Б–Є—А—Г—О—Й–µ–≥–Њ –Љ–љ–Њ–≥–Њ–Њ—З–∞–≥–Њ–≤–Њ–≥–Њ –Є–ї–Є –і–Є—Д—Д—Г–Ј–љ–Њ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, –њ—А–Њ—П–≤–ї—П—О—Й–Є–є—Б—П –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є, –љ–µ–є—А–Њ–њ—Б–Є—Е–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ–Є –Є/–Є–ї–Є –њ—Б–Є—Е–Є—З–µ—Б–Ї–Є–Љ–Є –љ–∞—А—Г—И–µ–љ–Є—П–Љ–Є, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Є/–Є–ї–Є –њ–Њ–≤—В–Њ—А–љ—Л–Љ–Є —Н–њ–Є–Ј–Њ–і–∞–Љ–Є –Њ—Б—В—А—Л—Е –љ–∞—А—Г—И–µ–љ–Є–є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П: –і–Є—Б–≥–µ–Љ–Є—П, —В—А–∞–љ–Ј–Є—В–Њ—А–љ–∞—П –Є—И–µ–Љ–Є—З–µ—Б–Ї–∞—П –∞—В–∞–Ї–∞, –Є–љ—Б—Г–ї—М—В [4]. –Я–∞—В–Њ–≥–µ–љ–µ–Ј –Ф–≠ –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –њ–Њ—Б—В–Њ—П–љ–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –Є–ї–Є –≤–∞—А–Є–∞–љ—В–∞–Љ–Є –њ–Њ–≤—В–Њ—А–љ—Л—Е —Н–њ–Є–Ј–Њ–і–Њ–≤ –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є [2]. –Т–µ–і—Г—Й–Є–є –Љ–µ—Е–∞–љ–Є–Ј–Љ –Ф–≠ – –Є—И–µ–Љ–Є—П, —Б–≤—П–Ј–∞–љ–љ–∞—П —Б –≥–Є–њ–Њ–Ї—Б–Є–µ–є –Љ–Њ–Ј–≥–Њ–≤–Њ–є —В–Ї–∞–љ–Є. –У–Є–њ–Њ–Ї—Б–Є—П –њ—А–Є–≤–Њ–і–Є—В –Ї –љ–∞—А—Г—И–µ–љ–Є—О –∞—Г—В–Њ—А–µ–≥—Г–ї—П—Ж–Є–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П, –≤–Њ–Ј–љ–Є–Ї–∞–µ—В –≤—Б–µ –±–Њ–ї—М—И–∞—П –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М –Њ—В —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–Є—Б—В–µ–Љ–љ–Њ–є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є [8]. –Т —В–Њ –ґ–µ –≤—А–µ–Љ—П –љ–µ–Ј–∞–≤–Є—Б–Є–Љ–Њ –Њ—В –њ—А–Є—З–Є–љ –≤—Л–Ј—Л–≤–∞—О—Й–Є—Е –Є—И–µ–Љ–Є—О –Љ–Њ–Ј–≥–∞, –Є–Ј–Љ–µ–љ–µ–љ–Є—П –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ–∞ –Љ–Њ–Ј–≥–∞, –њ—А–Њ–Є—Б—Е–Њ–і—П—Й–Є–µ –≤ –Њ—В–≤–µ—В –љ–∞ –≥–Є–њ–Њ–Ї—Б–Є—О, –љ–Њ—Б—П—В —Г–љ–Є–≤–µ—А—Б–∞–ї—М–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А.
–°–Њ–≤–µ—А—И–µ–љ–љ–Њ –Њ—З–µ–≤–Є–і–љ–Њ, —З—В–Њ —Г–ї—Г—З—И–Є—В—М —А–µ–Ј—Г–ї—М—В–∞—В—Л –ї–µ—З–µ–љ–Є—П —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є, —Б–Њ–Ї—А–∞—В–Є—В—М —З–Є—Б–ї–Њ –Њ—Б–ї–Њ–ґ–љ–µ–љ–Є–є, –∞ —В–∞–Ї–ґ–µ —А–∞—Б—И–Є—А–Є—В—М –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ—Б—В–Є —В–µ—А–∞–њ–Є–Є –њ—А–Є –љ–∞–ї–Є—З–Є–Є –њ—А–Њ—В–Є–≤–Њ–њ–Њ–Ї–∞–Ј–∞–љ–Є–є –Ї —Б—В–∞–љ–і–∞—А—В–љ—Л–Љ —Б—Е–µ–Љ–∞–Љ, –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ –њ—Г—В–µ–Љ –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є—П —Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е –њ—А–µ–њ–∞—А–∞—В–Њ–≤, –≤–Њ–Ј–і–µ–є—Б—В–≤—Г—О—Й–Є—Е –љ–∞ –≤–∞–ґ–љ–µ–є—И–Є–µ –Љ–µ—Е–∞–љ–Є–Ј–Љ—Л –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є—П –Є—И–µ–Љ–Є–Є [1].
–¶–µ–ї—М—О –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П —П–≤–Є–ї–Њ—Б—М –Є–Ј—Г—З–µ–љ–Є–µ –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ —Г –±–Њ–ї—М–љ—Л—Е —Б–Љ–µ—И–∞–љ–љ–Њ–є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П.
–Ь–∞—В–µ—А–Є–∞–ї –Є –Љ–µ—В–Њ–і—Л –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П
–Т —В–µ—З–µ–љ–Є–µ 2008 –≥–Њ–і–∞ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Њ 30 –±–Њ–ї—М–љ—Л—Е —Б —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П: –Ф–≠ I – 12 (—З–µ–ї.) –Є II —Б—В–∞–і–Є–є – 18 (—З–µ–ї.), –≤ –≤–Њ–Ј—А–∞—Б—В–µ –Њ—В 46 –і–Њ 69 –ї–µ—В (—Б—А–µ–і–љ–Є–є –≤–Њ–Ј—А–∞—Б—В 57,3±0,8), –Є–Ј –љ–Є—Е 21 –ґ–µ–љ—Й–Є–љ–∞, 9 –Љ—Г–ґ—З–Є–љ. –Ю—В –≤—Б–µ—Е –±–Њ–ї—М–љ—Л—Е –±—Л–ї–Њ –њ–Њ–ї—Г—З–µ–љ–Њ –Є–љ—Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–љ–Њ–µ —Б–Њ–≥–ї–∞—Б–Є–µ –љ–∞ —Г—З–∞—Б—В–Є–µ –≤ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є. –Ш—Б–Ї–ї—О—З–∞–ї–Є—Б—М –њ–∞—Ж–Є–µ–љ—В—Л —Б –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Њ–є –Ї–∞—А—В–Є–љ–Њ–є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –Є–љ—Б—Г–ї—М—В–∞, –Њ–њ—Г—Е–Њ–ї—П–Љ–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞, —З–µ—А–µ–њ–љ–Њ––Љ–Њ–Ј–≥–Њ–≤–Њ–є —В—А–∞–≤–Љ–Њ–є –Є –≤–Њ—Б–њ–∞–ї–Є—В–µ–ї—М–љ—Л–Љ–Є –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є—П–Љ–Є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л, —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–≤—И–Є–Љ–Є—Б—П —А–∞–Ј–≤–Є—В–Є–µ–Љ –Њ—З–∞–≥–Њ–≤–Њ–є –Є –Њ–±—Й–µ–Љ–Њ–Ј–≥–Њ–≤–Њ–є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є, –∞ —В–∞–Ї–ґ–µ –±–Њ–ї—М–љ—Л–µ —Б –Њ—Б—В—А—Л–Љ –Є–љ—Д–∞—А–Ї—В–Њ–Љ –Љ–Є–Њ–Ї–∞—А–і–∞, —Б–µ—А–і–µ—З–љ–Њ–є, –њ–µ—З–µ–љ–Њ—З–љ–Њ–є –Є –њ–Њ—З–µ—З–љ–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М—О.
–С–Њ–ї—М–љ—Л–µ —Б –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –≥–Є–њ–µ—А—В–µ–љ–Ј–Є–µ–є –њ–Њ—Б—В–Њ—П–љ–љ–Њ –њ—А–Є–љ–Є–Љ–∞–ї–Є –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ—Л–µ –њ—А–µ–њ–∞—А–∞—В—Л (–≤ –Њ—Б–љ–Њ–≤–љ–Њ–Љ –Є–љ–≥–Є–±–Є—В–Њ—А—Л –Р–Я–§), —З—В–Њ –Њ–±–µ—Б–њ–µ—З–Є–≤–∞–ї–Њ –Ї–Њ—А—А–µ–Ї—Ж–Є—О –Р–Ф.
–Я–Њ—Б–ї–µ –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ–Њ–≥–Њ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є—П –±–Њ–ї—М–љ—Л–Љ –љ–∞–Ј–љ–∞—З–∞–ї—Б—П –њ—А–Є–µ–Љ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ (—В—А–Є–Љ–µ—В–∞–Ј–Є–і–Є–љ) – 1 –Ї–∞–њ—Б—Г–ї–∞ (20 –Љ–≥) —В—А–Є —А–∞–Ј–∞ –≤ —Б—Г—В–Ї–Є –≤ —В–µ—З–µ–љ–Є–µ 60 –і–љ–µ–є.
–Ґ—А–Є–Љ–µ—В–∞–Ј–Є–і–Є–љ –Њ–Ї–∞–Ј—Л–≤–∞–µ—В –∞–љ—В–Є–≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–µ –і–µ–є—Б—В–≤–Є–µ, –≤–ї–Є—П—П –љ–∞ –љ–µ–є—А–Њ–љ—Л –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –Є –Ї–∞—А–і–Є–Њ–Љ–Є–Њ—Ж–Є—В—Л, –Њ–њ—В–Є–Љ–Є–Ј–Є—А—Г—П –Є—Е –Љ–µ—В–∞–±–Њ–ї–Є–Ј–Љ. –¶–Є—В–Њ–њ—А–Њ—В–µ–Ї—В–Є–≤–љ—Л–є —Н—Д—Д–µ–Ї—В –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ –њ–Њ–≤—Л—И–µ–љ–Є–µ–Љ —Н–љ–µ—А–≥–µ—В–Є—З–µ—Б–Ї–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞, –∞–Ї—В–Є–≤–∞—Ж–Є–µ–є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ–≥–Њ –і–µ–Ї–∞—А–±–Њ–Ї—Б–Є–ї–Є—А–Њ–≤–∞–љ–Є—П –Є —А–∞—Ж–Є–Њ–љ–∞–ї—М–љ–Њ–≥–Њ –њ–Њ—В—А–µ–±–ї–µ–љ–Є—П –Ї–Є—Б–ї–Њ—А–Њ–і–∞. –Я—А–µ–њ–∞—А–∞—В –њ—А–µ–њ—П—В—Б—В–≤—Г–µ—В –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–Љ—Г –і–µ–є—Б—В–≤–Є—О —Б–≤–Њ–±–Њ–і–љ—Л—Е —А–∞–і–Є–Ї–∞–ї–Њ–≤.
–Т—Б–µ–Љ –±–Њ–ї—М–љ—Л–Љ –њ—А–Њ–≤–Њ–і–Є–ї–Њ—Б—М –Ї–Њ–Љ–њ–ї–µ–Ї—Б–љ–Њ–µ –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ, –≤–Ї–ї—О—З–∞—О—Й–µ–µ –Њ—Б–Љ–Њ—В—А –Є –љ–∞–±–ї—О–і–µ–љ–Є–µ –≤ –і–Є–љ–∞–Љ–Є–Ї–µ —Г —В–µ—А–∞–њ–µ–≤—В–∞ –Є –љ–µ–≤—А–Њ–ї–Њ–≥–∞ —Б –Њ—Ж–µ–љ–Ї–Њ–є –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –њ–Њ —И–Ї–∞–ї–µ MMSE, –≠–Ъ–У, –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –Љ–Њ–Ј–≥–Њ–≤–Њ–є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є —Б –Є—Б–њ–Њ–ї—М–Ј–Њ–≤–∞–љ–Є–µ–Љ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤—Л—Е –Љ–µ—В–Њ–і–Є–Ї: –£–Ч–Ф–У, –Ґ–Ъ–Ф–У (–њ–Њ–Ї–∞–Ј–∞—В–µ–ї–Є –ї–Є–љ–µ–є–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В–Є, –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є), —Ж–≤–µ—В–љ–Њ–µ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –≤–љ–µ—З–µ—А–µ–њ–љ—Л—Е –Њ—В–і–µ–ї–Њ–≤ –±—А–∞—Е–Є–Њ—Ж–µ—Д–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –Є —В—А–∞–љ—Б–Ї—А–∞–љ–Є–∞–ї—М–љ–Њ–µ —В—А–Є–њ–ї–µ–Ї—Б–љ–Њ–µ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є–µ –∞—А—В–µ—А–Є–є –Т–Є–ї–ї–Є–Ј–Є–µ–≤–∞ –Ї—А—Г–≥–∞, –Њ—Ж–µ–љ–Ї–∞ –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ––≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П: —Г—А–Њ–≤–µ–љ—М –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–≥–Њ –Є –Њ–Ї–Є—Б–ї–µ–љ–љ–Њ–≥–Њ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ [9], –∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л [11] –≤ –Ї—А–Њ–≤–Є – –і–Њ –ї–µ—З–µ–љ–Є—П, —З–µ—А–µ–Ј 30 –Є 60 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞.
–Ю—Ж–µ–љ–Ї—Г —Н—Д—Д–µ–Ї—В–∞ –ї–µ—З–µ–љ–Є—П –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–Љ –Є –њ–∞—Ж–Є–µ–љ—В–Њ–Љ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї–Є –њ–Њ 5––±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ: —Г—Е—Г–і—И–µ–љ–Є–µ – 0; –±–µ–Ј –і–Є–љ–∞–Љ–Є–Ї–Є – 1; –љ–µ–±–Њ–ї—М—И–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ – 2; –Ј–∞–Љ–µ—В–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ – 3; –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ – 4.
–†–µ–Ј—Г–ї—М—В–∞—В—Л
–Ш–Ј–≤–µ—Б—В–љ–Њ, —З—В–Њ –њ–Њ –Њ—Б–љ–Њ–≤–љ—Л–Љ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–Љ –њ—А–Є—З–Є–љ–∞–Љ –≤—Л–і–µ–ї—П—О—В –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї—Г—О, –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї—Г—О, —Б–Љ–µ—И–∞–љ–љ—Г—О –Є –≤–µ–љ–Њ–Ј–љ—Г—О –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ—Г—О —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—О.
–£ –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ —Б–Њ—З–µ—В–∞–љ–Є–µ —Н—В–Є–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Д–∞–Ї—В–Њ—А–Њ–≤: –≥–Є–њ–µ—А—В–Њ–љ–Є—З–µ—Б–Ї–Њ–є –±–Њ–ї–µ–Ј–љ–Є (68,2%), —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–≥–Њ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ–Ј–∞ (40,9%), –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є (54,5%).
–Ы–µ—З–µ–љ–Є–µ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є 8 –љ–µ–і–µ–ї—М —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є–ї–Њ—Б—М –±–Њ–ї—М–љ—Л–Љ–Є, —В–Њ–ї—М–Ї–Њ —Г –Њ–і–љ–Њ–≥–Њ –њ–∞—Ж–Є–µ–љ—В–∞ –њ–Њ—П–≤–Є–ї–∞—Б—М –∞–ї–ї–µ—А–≥–Є—З–µ—Б–Ї–∞—П —А–µ–∞–Ї—Ж–Є—П –Є –і–∞–ї—М–љ–µ–є—И–Є–є –њ—А–Є–µ–Љ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ –±—Л–ї –њ—А–µ–Ї—А–∞—Й–µ–љ. –Ю–і–љ–∞ –њ–∞—Ж–Є–µ–љ—В–Ї–∞ —З–µ—А–µ–Ј 30 –і–љ–µ–є –њ–Њ—Б–ї–µ –љ–∞—З–∞–ї–∞ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Л–µ—Е–∞–ї–∞ –Ј–∞ —А—Г–±–µ–ґ, –≤ —Б–≤—П–Ј–Є —Б —З–µ–Љ –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л–є –Ї–Њ–љ—В—А–Њ–ї—М —З–µ—А–µ–Ј 60 –і–љ–µ–є –љ–µ –Њ—Б—Г—Й–µ—Б—В–≤–ї—П–ї—Б—П.
–С–Њ–ї—М—И–Є–љ—Б—В–≤–Њ –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –њ—А–µ–і—К—П–≤–ї—П–ї–Є –ґ–∞–ї–Њ–±—Л –љ–∞ –≥–Њ–ї–Њ–≤–љ—Г—О –±–Њ–ї—М (93,3%), –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ (92,8%), –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –њ—А–Є —Е–Њ–і—М–±–µ (66,6%), –Њ–±—Й—Г—О —Б–ї–∞–±–Њ—Б—В—М (70%), –љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞ (60%), —Б–љ–Є–ґ–µ–љ–Є–µ –њ–∞–Љ—П—В–Є (53,3%), —Н–Љ–Њ—Ж–Є–Њ–љ–∞–ї—М–љ–Њ––≤–Њ–ї–µ–≤—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ (73,3%) – —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, —Б–ї–µ–Ј–ї–Є–≤–Њ—Б—В—М. –°—Г–±—К–µ–Ї—В–Є–≤–љ–∞—П –Њ—Ж–µ–љ–Ї–∞ 10 –Ї–ї–Є–љ–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (–≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –≥–Њ–ї–Њ–≤–Њ–Ї—А—Г–ґ–µ–љ–Є–µ, –љ–µ—Г—Б—В–Њ–є—З–Є–≤–Њ—Б—В—М –њ—А–Є —Е–Њ–і—М–±–µ, –љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞, –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М, —Б–љ–Є–ґ–µ–љ–Є–µ –њ–∞–Љ—П—В–Є, —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, –њ–Њ–≤—Л—И–µ–љ–љ–∞—П —А–∞–Ј–і—А–∞–ґ–Є—В–µ–ї—М–љ–Њ—Б—В—М, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М, —Б–ї–µ–Ј–ї–Є–≤–Њ—Б—В—М) –њ—А–Њ–Є–Ј–≤–Њ–і–Є–ї–∞—Б—М –њ–Њ 6––±–∞–ї–ї—М–љ–Њ–є —А–µ–є—В–Є–љ–≥–Њ–≤–Њ–є —И–Ї–∞–ї–µ —Б–Њ —Б—В–∞–љ–і–∞—А—В–Є–Ј–Є—А–Њ–≤–∞–љ–љ—Л–Љ–Є –Ї—А–Є—В–µ—А–Є—П–Љ–Є –Њ—Ж–µ–љ–Ї–Є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Ї–∞–ґ–і–Њ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞: —Б–Є–Љ–њ—В–Њ–Љ –Њ—В—Б—Г—В—Б—В–≤—Г–µ—В – 0; –љ–µ–Ј–љ–∞—З–Є—В–µ–ї—М–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П – 1; –ї–µ–≥–Ї–Є–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П – 2; —Г–Љ–µ—А–µ–љ–љ–Њ –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П – 3; –≤—Л—А–∞–ґ–µ–љ–љ—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П – 4; –≥—А—Г–±—Л–µ –њ—А–Њ—П–≤–ї–µ–љ–Є—П – 5. –Ю—Ж–µ–љ–Ї–∞ –Ї–∞–ґ–і–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П –љ–µ –њ—А–µ–≤—Л—И–∞–ї–∞ —Г–Љ–µ—А–µ–љ–љ–Њ–є –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —Б–Є–Љ–њ—В–Њ–Љ–∞. –°—А–∞–≤–љ–Є—В–µ–ї—М–љ—Л–є –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—М Δ –і–µ–ї—М—В–∞ –Њ—В—А–∞–ґ–∞–ї —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –Є–ї–Є —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є —В–Њ–≥–Њ –Є–ї–Є –Є–љ–Њ–≥–Њ —Б–Є–Љ–њ—В–Њ–Љ–∞ –і–Њ –Є –њ–Њ—Б–ї–µ –ї–µ—З–µ–љ–Є—П.
–Ю—Ж–µ–љ–Ї–∞ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ —З–µ—А–µ–Ј 30 –і–љ–µ–є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–∞ –Њ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–µ, –Њ–і–љ–∞–Ї–Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ (p<0,01) —Г–Љ–µ–љ—М—И–µ–љ–Є–µ —Б—Г–±—К–µ–Ї—В–Є–≤–љ–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –±—Л–ї–Њ –Њ—В–Љ–µ—З–µ–љ–Њ –њ—А–Є –Њ—Б–Љ–Њ—В—А–µ –±–Њ–ї—М–љ—Л—Е —З–µ—А–µ–Ј 60 –і–љ–µ–є, –Њ—Б–Њ–±–µ–љ–љ–Њ –Ј–љ–∞—З–Є–Љ–Њ —В–∞–Ї–Є—Е –ґ–∞–ї–Њ–±, –Ї–∞–Ї –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М, –љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞, —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В—М (—В–∞–±–ї. 1).
–Т –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–Љ —Б—В–∞—В—Г—Б–µ –≤—Л—П–≤–ї—П–ї–Є—Б—М —Б–Є–Љ–њ—В–Њ–Љ—Л –Њ—А–∞–ї—М–љ–Њ–≥–Њ –∞–≤—В–Њ–Љ–∞—В–Є–Ј–Љ–∞, –њ–Є—А–∞–Љ–Є–і–љ–∞—П –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В—М (–њ–Њ–≤—Л—И–µ–љ–Є–µ –≥–ї—Г–±–Њ–Ї–Є—Е —А–µ—Д–ї–µ–Ї—Б–Њ–≤, –∞–љ–Є–Ј–Њ—А–µ—Д–ї–µ–Ї—Б–Є—П, –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–µ —Б—В–Њ–њ–љ—Л–µ —А–µ—Д–ї–µ–Ї—Б—Л), –≤–µ—Б—В–Є–±—Г–ї–Њ––Љ–Њ–Ј–ґ–µ—З–Ї–Њ–≤—Л–µ —А–∞—Б—Б—В—А–Њ–є—Б—В–≤–∞ (–љ–Є—Б—В–∞–≥–Љ, –ї–µ–≥–Ї–Є–µ –Ї–Њ–Њ—А–і–Є–љ–∞—В–Њ—А–љ—Л–µ –љ–∞—А—Г—И–µ–љ–Є—П).
–Я—А–Є –∞–љ–∞–ї–Є–Ј–µ –і–Є–љ–∞–Љ–Є–Ї–Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ –Ј–∞ 60––і–љ–µ–≤–љ—Л–є –њ–µ—А–Є–Њ–і –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Є—Б—М –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ –љ–Є—Б—В–∞–≥–Љ–∞ (40%), —А–µ–≥—А–µ—Б—Б –Њ—А–∞–ї—М–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (33,3%), —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –≤—Л—А–∞–ґ–µ–љ–љ–Њ—Б—В–Є –Љ–Њ–Ј–ґ–µ—З–Ї–Њ–≤–Њ–є –Є –њ–Є—А–∞–Љ–Є–і–љ–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є (36,6%).
–Ю—Ж–µ–љ–Ї–∞ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е —Д—Г–љ–Ї—Ж–Є–є –њ–Њ —И–Ї–∞–ї–µ MMSE –њ—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Њ—Б–Љ–Њ—В—А–µ —Б–Њ—Б—В–∞–≤–Є–ї–∞ –≤ —Б—А–µ–і–љ–µ–Љ 24,8±1,8 –±–∞–ї–ї–∞, —З—В–Њ —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ –ї–µ–≥–Ї–Є–Љ –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л–Љ –љ–∞—А—Г—И–µ–љ–Є—П–Љ. –Ф–Њ—Б—В–Њ–≤–µ—А–љ—Л—Е –Є–Ј–Љ–µ–љ–µ–љ–Є–є —Н—В–Њ–≥–Њ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П —Г –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ.
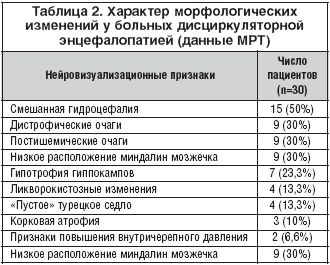
–Я—А–Є –Ь–†–Ґ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ —Г –≤—Б–µ—Е –Њ–±—Б–ї–µ–і–Њ–≤–∞–љ–љ—Л—Е –≤—Л—П–≤–ї—П–ї–Є—Б—М –њ—А–Є–Ј–љ–∞–Ї–Є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ –≥–µ–љ–µ–Ј–∞, —Г –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ –±–Њ–ї—М–љ—Л—Е –Є–Љ–µ–ї–Њ –Љ–µ—Б—В–Њ —Б–Њ—З–µ—В–∞–љ–Є–µ —Г–Ї–∞–Ј–∞–љ–љ—Л—Е –њ—А–Є–Ј–љ–∞–Ї–Њ–≤, —Г 30% –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –±—Л–ї–Њ –≤—Л—П–≤–ї–µ–љ–Њ –љ–Є–Ј–Ї–Њ–µ —А–∞—Б–њ–Њ–ї–Њ–ґ–µ–љ–Є–µ –Љ–Є–љ–і–∞–ї–Є–љ –Љ–Њ–Ј–ґ–µ—З–Ї–∞ (—В–∞–±–ї. 2).
–Ю—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П –њ–Њ —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–∞ –Њ –љ–∞–ї–Є—З–Є–Є —Г 8 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (26,7%) –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ —Б—В–µ–љ–Њ–Ј–Є—А—Г—О—Й–µ–≥–Њ –њ–Њ—А–∞–ґ–µ–љ–Є—П –њ—А–µ–, –Є —Ж–µ—А–µ–±—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є—З–µ—Б–Ї–Є –љ–µ–Ј–љ–∞—З–Є–Љ–Њ–≥–Њ. –Ю—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ –ї–Є–љ–µ–є–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В–Є –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞ (–Ы–°–Ъ) –њ–Њ –Є–љ—В—А–∞–Ї—А–∞–љ–Є–∞–ї—М–љ—Л–Љ –∞—А—В–µ—А–Є—П–Љ, –њ–Њ–≤—Л—И–µ–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, —Б–љ–Є–ґ–µ–љ–Є–µ —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, —Г –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М –њ—А–Є–Ј–љ–∞–Ї–Є –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є, –њ—А–µ–Є–Љ—Г—Й–µ—Б—В–≤–µ–љ–љ–Њ –≤ –≤–µ—А—В–µ–±—А–∞–ї—М–љ–Њ––±–∞–Ј–Є–ї—П—А–љ–Њ–Љ –±–∞—Б—Б–µ–є–љ–µ. –Я—А–Є —Б—А–∞–≤–љ–Є—В–µ–ї—М–љ–Њ–є –Њ—Ж–µ–љ–Ї–µ —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є —З–µ—А–µ–Ј 30 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ –≤—Л—П–≤–ї—П–ї–∞—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —Г 19 (67,8%) –Є–Ј 28 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –Ю—В–Љ–µ—З–µ–љ–Њ –њ–Њ–≤—Л—И–µ–љ–Є–µ –ї–Є–љ–µ–є–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В–Є —Г 9 (32,1%), –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П —Г 11 (39,3%), —Г–Љ–µ–љ—М—И–µ–љ–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є —Г 17 (60,7%); —Г 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤ (32,1%) –і–Є–љ–∞–Љ–Є–Ї–Є –љ–µ –≤—Л—П–≤–ї—П–ї–Њ—Б—М. –І–µ—А–µ–Ј 60 –і–љ–µ–є –Њ—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є –њ—А–Є —Г–ї—М—В—А–∞–Ј–≤—Г–Ї–Њ–≤–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Б–Њ–≤–њ–∞–і–∞–ї–∞ —Б —А–µ–Ј—Г–ї—М—В–∞—В–∞–Љ–Є, –њ–Њ–ї—Г—З–µ–љ–љ—Л–Љ–Є —А–∞–љ–µ–µ —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ –љ–∞ —Д–Њ–љ–µ 30––і–љ–µ–≤–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞, —В.–µ. —Б–Њ—Е—А–∞–љ—П–ї–∞—Б—М –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–∞—П –і–Є–љ–∞–Љ–Є–Ї–∞ —Г 67,8% –±–Њ–ї—М–љ—Л—Е. –Ю–і–љ–∞–Ї–Њ –Є–Ј 9 –њ–∞—Ж–Є–µ–љ—В–Њ–≤, —Г –Ї–Њ—В–Њ—А—Л—Е –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –і–Є–љ–∞–Љ–Є–Ї–Є —З–µ—А–µ–Ј 30 –і–љ–µ–є, —Г–ї—Г—З—И–µ–љ–Є–µ –±—Л–ї–Њ –Ј–∞—А–µ–≥–Є—Б—В—А–Є—А–Њ–≤–∞–љ–Њ —В–Њ–ї—М–Ї–Њ —З–µ—А–µ–Ј 60 –і–љ–µ–є –Є–Ј –љ–Є—Е: —Г 3 –±–Њ–ї—М–љ—Л—Е (10,7%) —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞–ї–Њ—Б—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Њ—В—В–Њ–Ї–∞, —Г 2 (7,1%) – –Њ—В–Љ–µ—З–∞–ї–∞—Б—М –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, —Г 4 (14,3%) –љ–∞ —Д–Њ–љ–µ 8––љ–µ–і–µ–ї—М–љ–Њ–≥–Њ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Ј–љ–∞—З–Є–Љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є –≤ –Њ—Ж–µ–љ–Њ—З–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї—П—Е –і–Њ–њ–њ–ї–µ—А–Њ–≥—А–∞—Д–Є–Є –љ–µ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М (—А–Є—Б. 1).
–Ф—Г–њ–ї–µ–Ї—Б–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ —Б–Њ—Б—В–Њ—П–љ–Є—П –±—А–∞—Е–Є–Њ—Ж–µ—Д–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є (–Ф–°) –њ—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –љ–∞–Є–±–Њ–ї–µ–µ —З–∞—Б—В–Њ —Г –±–Њ–ї—М–љ—Л—Е –Ф–≠ –љ–∞–±–ї—О–і–∞–ї–Є—Б—М –Є–Ј–Љ–µ–љ–µ–љ–Є—П –≤ –≤–Є–і–µ –љ–∞—А—Г—И–µ–љ–Є—П –і–Є—Д—Д–µ—А–µ–љ—Ж–Є—А–Њ–≤–Ї–Є –Є —Г—В–Њ–ї—Й–µ–љ–Є—П —Б—В–µ–љ–Њ–Ї —Б–Њ—Б—Г–і–∞, —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –Ї–Њ–Љ–њ–ї–µ–Ї—Б–∞ –Є–љ—В–Є–Љ–∞––Љ–µ–і–Є–∞ (–Ъ–Ш–Ь) –≤ —Б—А–µ–і–љ–µ–Љ 1,5 –Љ–Љ (1,4–1,7 –Љ–Љ), –Ј–∞ –љ–Њ—А–Љ–∞–ї—М–љ—Г—О –≤–µ–ї–Є—З–Є–љ—Г –Ъ–Ш–Ь –њ—А–Є–љ–Є–Љ–∞—О—В –Ј–љ–∞—З–µ–љ–Є–µ –≤ —Б—А–µ–і–љ–µ–Љ —А–∞–≤–љ–Њ–µ 1 –Љ–Љ (0,9–1,1 –Љ–Љ), –њ—А–Є–Ј–љ–∞–Ї–Є –Љ–∞–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є –Њ–±–љ–∞—А—Г–ґ–µ–љ—Л —Г 19 (63,3%), –≤—Л—П–≤–ї—П–µ–Љ—Л–µ –∞—В–µ—А–Њ—Б–Ї–ї–µ—А–Њ—В–Є—З–µ—Б–Ї–Є–µ –±–ї—П—И–Ї–Є, –≤—Л–Ј—Л–≤–∞—О—Й–Є–µ —Б—В–µ–љ–Њ–Ј–Є—А–Њ–≤–∞–љ–Є–µ –Љ–µ–љ–µ–µ 25%, –Њ–њ—А–µ–і–µ–ї—П–ї–Є—Б—М —Г 5 (16,6%) –±–Њ–ї—М–љ—Л—Е. –Ю—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Ї–Њ—А–Њ—Б—В–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є —Г 14 (46,7%), –њ–Њ–≤—Л—И–µ–љ–Є–µ –Є–љ–і–µ–Ї—Б–∞ –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П —Г 14 (46,7%), –њ—А–Є–Ј–љ–∞–Ї–Є –љ–∞—А—Г—И–µ–љ–Є—П –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Њ—В—В–Њ–Ї–∞ —Г 16 (53,3%), —Б–њ–Њ–љ–і–Є–ї–Њ–≥–µ–љ–љ–Њ–µ –≤–ї–Є—П–љ–Є–µ –љ–∞ –њ–Њ–Ј–≤–Њ–љ–Њ—З–љ—Г—О –∞—А—В–µ—А–Є—О – —Г 2 –њ–∞—Ж–Є–µ–љ—В–Њ–≤. –£ 2 (6,7%) –Њ–±—Б–ї–µ–і—Г–µ–Љ—Л—Е –њ—А–Є –Ф–° –Ј–љ–∞—З–Є–Љ–Њ–є –њ–∞—В–Њ–ї–Њ–≥–Є–Є –Ь–Р–У –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ. –Ъ–Њ–љ—В—А–Њ–ї—М–љ–Њ–µ –Ф–° —З–µ—А–µ–Ј 60 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ –њ–Њ–і—В–≤–µ—А–і–Є–ї–Њ –њ–Њ–Ј–Є—В–Є–≤–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г (80%) –Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ–± —Г–Љ–µ–љ—М—И–µ–љ–Є–Є –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є. –Э–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П –Њ—В–Љ–µ—З–µ–љ–∞ —Г 14 (53,8%) –Є–Ј 28, —Б–Ї–Њ—А–Њ—Б—В–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є – —Г 17 (60,7%), —Г–ї—Г—З—И–µ–љ–Є–µ –≤–µ–љ–Њ–Ј–љ–Њ–≥–Њ –Њ—В—В–Њ–Ї–∞ – —Г 12 (42,8%) –±–Њ–ї—М–љ—Л—Е.
–Т –њ–∞—В–Њ–≥–µ–љ–µ–Ј–µ –љ–∞—А—Г—И–µ–љ–Є—П —Б–Њ—Б—Г–і–Є—Б—В–Њ–є –њ—А–Њ–љ–Є—Ж–∞–µ–Љ–Њ—Б—В–Є –Є —А–∞–Ј–≤–Є—В–Є—П –≥–Є–њ–Њ–Ї—Б–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—В–Њ—П–љ–Є—П –ї–µ–ґ–∞—В –њ—А–Њ—Ж–µ—Б—Б—Л, —Е–∞—А–∞–Ї—В–µ—А–љ—Л–µ –і–ї—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Њ–Ј–≥–∞, –Њ–±—Г—Б–ї–Њ–≤–ї–µ–љ–љ—Л–µ —Б–і–≤–Є–≥–∞–Љ–Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ––≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –≤ –≥–ї—Г—В–∞—В–Є–љ––∞—Б–Ї–Њ—А–±–∞—В–љ–Њ–є —Б–Є—Б—В–µ–Љ–∞—Е –Ї—А–Њ–≤–Є [6].
–¶–µ—А–µ–±—А–∞–ї—М–љ–∞—П –Є—И–µ–Љ–Є—П –≥–µ–љ–µ—А–Є—А—Г–µ—В —Н–љ–Ј–Є–Љ—Л –Є —Б—Г–±—Б—В—А–∞—В—Л, –Ї–Њ—В–Њ—А—Л–µ –Љ–Њ–≥—Г—В –Њ–±—А–∞–Ј–Њ–≤—Л–≤–∞—В—М —Б–≤–Њ–±–Њ–і–љ—Л–µ —А–∞–і–Є–Ї–∞–ї—Л, –≤–Ї–ї—О—З–∞—О—Й–Є–µ —Ж–µ–њ–љ—Л–µ —А–µ–∞–Ї—Ж–Є–Є «–њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П». –Э–∞ —Н—В–Њ–Љ —Д–Њ–љ–µ –∞–Ї—В–Є–≤–Є–Ј–Є—А—Г–µ—В—Б—П –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–∞—П –Ј–∞—Й–Є—В–∞, –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В–∞–Љ–Є –Ї–Њ—В–Њ—А–Њ–є —П–≤–ї—П–µ—В—Б—П —Б–Є—Б—В–µ–Љ–∞ –∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –Є –≥–ї—Г—В–∞—В–Є–Њ–љ–∞. –Р—Б–Ї–Њ—А–±–Є–љ–Њ–≤–∞—П –Ї–Є—Б–ї–Њ—В–∞ —Г—З–∞—Б—В–≤—Г–µ—В –≤ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В–µ —В–Ї–∞–љ–µ–є –Њ—В –њ–Њ–≤—А–µ–ґ–і–∞—О—Й–µ–≥–Њ –і–µ–є—Б—В–≤–Є—П —А–∞–і–Є–Ї–∞–ї–Њ–≤, –≤—Л–њ–Њ–ї–љ—П—П —А–Њ–ї—М «–ї–Њ–≤—Г—И–Ї–Є». –У–ї—Г—В–∞—В–Є–Њ–љ –Є–≥—А–∞–µ—В –≤–∞–ґ–љ–µ–є—И—Г—О —А–Њ–ї—М –≤ –ґ–Є–Ј–љ–µ–і–µ—П—В–µ–ї—М–љ–Њ—Б—В–Є –Ї–ї–µ—В–Њ–Ї –Є –Њ—А–≥–∞–љ–Є–Ј–Љ–∞ –≤ —Ж–µ–ї–Њ–Љ, —П–≤–ї—П–µ—В—Б—П –Ї–ї—О—З–µ–≤—Л–Љ –≤–љ—Г—В—А–Є–Ї–ї–µ—В–Њ—З–љ—Л–Љ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–Њ–Љ.
–Ю–њ—А–µ–і–µ–ї–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л (–Р–Ъ) –≤ —Б—Л–≤–Њ—А–Њ—В–Ї–µ –Ї—А–Њ–≤–Є —Г –±–Њ–ї—М–љ—Л—Е –Ф–≠ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ (p<0,01) —Б–љ–Є–ґ–µ–љ–Є–Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–≥–Њ –њ–Њ—В–µ–љ—Ж–Є–∞–ї–∞ –∞—Б–Ї–Њ—А–±–∞—В–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л. –Ф–Њ –ї–µ—З–µ–љ–Є—П —Б–Њ–і–µ—А–ґ–∞–љ–Є–µ –Њ–±–µ–Є—Е —Д–Њ—А–Љ –Р–Ъ –±—Л–ї–Њ —Б–љ–Є–ґ–µ–љ–љ—Л–Љ: –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л –Р–Ъ —Б–Њ—Б—В–∞–≤–ї—П–ї–Њ – 0,62±0,01 –Љ–≥% (n=0,72±0,2 –Љ–≥%); –Њ–Ї–Є—Б–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л – 0,64±0,01 –Љ–≥% (n=0,81±0,11 –Љ–≥%). –Ю—Ж–µ–љ–Ї–∞ —Б–Њ—Б—В–Њ—П–љ–Є—П –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ––≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –∞—Б–Ї–Њ—А–±–∞—В–љ–Њ–≥–Њ –Ј–≤–µ–љ–∞ —Г –±–Њ–ї—М–љ—Л—Е –Ф–≠ –њ—А–Є –Њ–њ—А–µ–і–µ–ї–µ–љ–Є–Є —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –љ–∞ 30––µ —Б—Г—В–Ї–Є –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –≤—Л—П–≤–Є–ї–∞ –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Р–Ъ (0,65±0,01 –Љ–≥%), –љ–Њ —Г—А–Њ–≤–µ–љ—М –Р–Ъ –Њ—Б—В–∞–≤–∞–ї—Б—П –љ–Є–ґ–µ –љ–Њ—А–Љ—Л. –І–µ—А–µ–Ј 60 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Б–љ–Є–ґ–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Р–Ъ, —В.–µ. —Б–Њ–Њ—В–≤–µ—В—Б—В–≤–Њ–≤–∞–ї–Њ –Є—Б—Е–Њ–і–љ–Њ–Љ—Г —Г—А–Њ–≤–љ—О –і–Њ –ї–µ—З–µ–љ–Є—П. –°–Њ–і–µ—А–ґ–∞–љ–Є–µ –Њ–Ї–Є—Б–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л –∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В—Л –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ –љ–∞—А–∞—Б—В–∞–ї–Њ –Ї 60––Љ—Г –і–љ—О (0,66±0,01 –Љ–≥%), –Њ—Б—В–∞–≤–∞—П—Б—М –љ–Є–ґ–µ –љ–Њ—А–Љ—Л (—А–Є—Б. 2).
–Я—А–Є –њ–µ—А–≤–Є—З–љ–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–Є —Г –±–Њ–ї—М–љ—Л—Е –Ф–≠ –Њ–њ—А–µ–і–µ–ї—П–ї–∞—Б—М –њ–Њ–≤—Л—И–µ–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –≤ –Ї—А–Њ–≤–Є – 36,50±0,98 –Љ–≥% –њ—А–Є –љ–Њ—А–Љ–µ 27,50±0,68 –Љ–≥% –Є —Б–љ–Є–ґ–µ–љ–љ–∞—П –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –Њ–Ї–Є—Б–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л – 4,20±0,27 –Љ–≥% (–љ–Њ—А–Љ–∞ 6,60±0,28 –Љ–≥%).
–Ш—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –≤ –Ї—А–Њ–≤–Є –љ–∞ —Д–Њ–љ–µ –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ –≤—Л—П–≤–Є–ї–Њ –Є–љ—В–µ—А–µ—Б–љ—Г—О –Ј–∞–≤–Є—Б–Є–Љ–Њ—Б—В—М: –љ–∞ –њ—А–Њ—В—П–ґ–µ–љ–Є–Є –њ–µ—А–Є–Њ–і–∞ –њ—А–Є–µ–Љ–∞ –њ—А–µ–њ–∞—А–∞—В–∞ —Б–љ–Є–ґ–∞–ї–∞—Б—М –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є—П –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л – 35,7±0,53 –Љ–≥% – —З–µ—А–µ–Ј 30 –і–љ–µ–є, 35,0±0,47 –Љ–≥% – —З–µ—А–µ–Ј 60 –і–љ–µ–є, –њ—А–Є–±–ї–Є–ґ–∞—П—Б—М –Ї –љ–Њ—А–Љ–µ. –Ф–Є–љ–∞–Љ–Є–Ї–∞ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –Њ–Ї–Є—Б–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ —В–∞–Ї–ґ–µ –њ–Њ–Ї–∞–Ј–∞–ї–∞ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–µ (p<0,01) —Б–љ–Є–ґ–µ–љ–Є–µ –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –љ–Є–ґ–µ –љ–Њ—А–Љ—Л —З–µ—А–µ–Ј 30 –і–љ–µ–є – 3,94±0,11 –Љ–≥%, —З–µ—А–µ–Ј 60 –і–љ–µ–є – 3,63±0,17 –Љ–≥% (—А–Є—Б. 3).
–Ю–±—Б—Г–ґ–і–µ–љ–Є–µ
–Ґ—А–Є–Љ–µ—В–∞–Ј–Є–і–Є–љ –Є–Ј–≤–µ—Б—В–µ–љ –Ї–∞–Ї –њ—А–µ–њ–∞—А–∞—В, –Њ–±–ї–∞–і–∞—О—Й–Є–є –∞–љ—В–Є–Є—И–µ–Љ–Є—З–µ—Б–Ї–Є–Љ, –∞–љ—В–Є–∞–љ–≥–Є–љ–∞–ї—М–љ—Л–Љ —Н—Д—Д–µ–Ї—В–Њ–Љ. –Т —А—П–і–µ —А–∞–±–Њ—В —Г–Ї–∞–Ј—Л–≤–∞–ї–Є—Б—М –і–∞–љ–љ—Л–µ –Њ –±–ї–∞–≥–Њ–њ—А–Є—П—В–љ–Њ–Љ –≤–Њ–Ј–і–µ–є—Б—В–≤–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –≤ —Б–ї—Г—З–∞–µ –Є—И–µ–Љ–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ [7,13,14].
–Т –љ–∞—Б—В–Њ—П—Й–µ–є —А–∞–±–Њ—В–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–µ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є–µ –њ–Њ–Ї–∞–Ј–∞–ї–Њ, —З—В–Њ –њ—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ —Б –Њ—Ж–µ–љ–Ї–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Њ–є —Б–Є–Љ–њ—В–Њ–Љ–∞—В–Є–Ї–Є –њ—А–Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –і–Њ—Б—В–Њ–≤–µ—А–љ–Њ–Љ –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–Љ –≤–ї–Є—П–љ–Є–Є –љ–∞ —А–µ–≥—А–µ—Б—Б —В–∞–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, –Ї–∞–Ї –≥–Њ–ї–Њ–≤–љ–∞—П –±–Њ–ї—М, –Њ–±—Й–∞—П —Б–ї–∞–±–Њ—Б—В—М, –љ–∞—А—Г—И–µ–љ–Є–µ —Б–љ–∞, —Б–љ–Є–ґ–µ–љ–Є–µ —А–∞–±–Њ—В–Њ—Б–њ–Њ—Б–Њ–±–љ–Њ—Б—В–Є, —Г—В–Њ–Љ–ї—П–µ–Љ–Њ—Б—В–Є. –Ъ—А–Њ–Љ–µ —В–Њ–≥–Њ, 16 (57,1%) –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞–ї–Є —Б—В–∞–±–Є–ї—М–љ—Г—О –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—О —Ж–Є—Д—А –Р–Ф –љ–∞ —Д–Њ–љ–µ —Б–Њ—З–µ—В–∞–љ–љ–Њ–є —Б –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–° –њ–Њ–Љ–Њ—Й—М—О –Є–љ—Б—В—А—Г–Љ–µ–љ—В–∞–ї—М–љ—Л—Е –Љ–µ—В–Њ–і–Њ–≤ –±—Л–ї–Њ –њ–Њ–і—В–≤–µ—А–ґ–і–µ–љ–Њ –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ —Д—Г–љ–Ї—Ж–Є–Є —А–µ–≥—Г–ї—П—В–Њ—А–љ—Л—Е —Б–Є—Б—В–µ–Љ, –њ–Њ–≤—Л—И–µ–љ–Є–µ —Г—А–Њ–≤–љ—П –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞. –Я–Њ –і–∞–љ–љ—Л–Љ –£–Ч–Ф–У –Ь–Р–У –њ–Њ—Б–ї–µ –њ—А–Њ–≤–µ–і–µ–љ–љ–Њ–≥–Њ –Ї—Г—А—Б–∞ –ї–µ—З–µ–љ–Є—П –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М —Г–≤–µ–ї–Є—З–µ–љ–Є–µ –ї–Є–љ–µ–є–љ–Њ–є —Б–Ї–Њ—А–Њ—Б—В–Є –Ї—А–Њ–≤–Њ—В–Њ–Ї–∞, –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ—Б—Г–і–Є—Б—В–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, —Б–Њ–Ї—А–∞—Й–µ–љ–Є–µ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є. –Р–љ–∞–ї–Є–Ј —А–µ–Ј—Г–ї—М—В–∞—В–Њ–≤ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П –њ–Њ–і—В–≤–µ—А–і–Є–ї –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г, —Е–∞—А–∞–Ї—В–µ—А–Є–Ј—Г—О—Й—Г—О—Б—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–µ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П, –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є–µ–Љ —Б–Ї–Њ—А–Њ—Б—В–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є, —Г–Љ–µ–љ—М—И–µ–љ–Є–µ–Љ –Є —А–µ–≥—А–µ—Б—Б–Њ–Љ –њ—А–Є–Ј–љ–∞–Ї–Њ–≤ –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є.
–£ –±–Њ–ї—М–љ—Л—Е –Ф–≠ –њ—А–Є –Ф–° –і–Њ –ї–µ—З–µ–љ–Є—П –±—Л–ї–Є –≤—Л—П–≤–ї–µ–љ—Л –њ—А–Є–Ј–љ–∞–Ї–Є –њ–Њ–≤—Л—И–µ–љ–Є—П –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є –њ–µ—А–Є—Д–µ—А–Є—З–µ—Б–Ї–Њ–≥–Њ —Б–Њ–њ—А–Њ—В–Є–≤–ї–µ–љ–Є—П –Є —Б–љ–Є–ґ–µ–љ–Є—П —Ж–µ—А–µ–±—А–Њ–≤–∞—Б–Ї—Г–ї—П—А–љ–Њ–є —А–µ–∞–Ї—В–Є–≤–љ–Њ—Б—В–Є, —З—В–Њ —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞–ї–Њ –Њ –љ–∞–ї–Є—З–Є–Є –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є–Є. –Ъ–∞–Ї –Є–Ј–≤–µ—Б—В–љ–Њ, –Љ–Є–Ї—А–Њ–∞–љ–≥–Є–Њ–њ–∞—В–Є—П —П–≤–ї—П–µ—В—Б—П –Ј–љ–∞—З–Є–Љ–Њ–є –њ—А–Є—З–Є–љ–Њ–є –≤ —А–∞–Ј–≤–Є—В–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –Љ–Њ–Ј–≥–∞. –Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –Њ—Б–Њ–±–µ–љ–љ–Њ –≤–∞–ґ–љ—Л–Љ –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–Љ –і—Г–њ–ї–µ–Ї—Б–љ–Њ–≥–Њ —Б–Ї–∞–љ–Є—А–Њ–≤–∞–љ–Є—П, –Њ—В—А–∞–ґ–∞—О—Й–µ–≥–Њ –њ–Њ–Ј–Є—В–Є–≤–љ—Г—О –і–Є–љ–∞–Љ–Є–Ї—Г —Г –±–Њ–ї—М–љ—Л—Е –љ–∞ —Д–Њ–љ–µ –ї–µ—З–µ–љ–Є—П –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ, —П–≤–ї—П–µ—В—Б—П –≤–Є–Ј—Г–∞–ї–Є–Ј–∞—Ж–Є—П –Љ–µ–ї–Ї–Є—Е –≤–µ—В–≤–µ–є III, IV –њ–Њ—А—П–і–Ї–∞ –Љ–∞–≥–Є—Б—В—А–∞–ї—М–љ—Л—Е –∞—А—В–µ—А–Є–є –≥–Њ–ї–Њ–≤—Л.
–Т –љ–∞—Б—В–Њ—П—Й–µ–µ –≤—А–µ–Љ—П –љ–∞–Ї–∞–њ–ї–Є–≤–∞–µ—В—Б—П –≤—Б–µ –±–Њ–ї—М—И–µ —Б–≤–µ–і–µ–љ–Є–є –Њ —В–Њ–Љ, —З—В–Њ —А–Њ–ї—М —Б–Є—Б—В–µ–Љ—Л –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –њ—А–Є –Є—И–µ–Љ–Є—З–µ—Б–Ї–Є—Е –њ–Њ–≤—А–µ–ґ–і–µ–љ–Є—П—Е –Љ–Њ–Ј–≥–∞ —Б–ї–Њ–ґ–љ–∞ –Є –Љ–љ–Њ–≥–Њ–Њ–±—А–∞–Ј–љ–∞ [2,5]. –Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є –Љ–∞—В–µ—А–Є–∞–ї –ї–Є—И—М –њ–Њ–Ј–≤–Њ–ї—П–µ—В –≤—Л–і–µ–ї–Є—В—М –і–∞–љ–љ—Г—О —Б–Є—Б—В–µ–Љ—Г, –Ї–∞–Ї –Ї–Њ–Љ–њ–Њ–љ–µ–љ—В –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л –≤ –Њ—А–≥–∞–љ–Є–Ј–Љ–µ –Є —Д–∞–Ї—В–Њ—А –≤–ї–Є—П–љ–Є—П –љ–∞ —Д–Њ—А–Љ–Є—А–Њ–≤–∞–љ–Є–µ –Ј–∞—Й–Є—В–љ—Л—Е –њ—А–Є—Б–њ–Њ—Б–Њ–±–Є—В–µ–ї—М–љ—Л—Е —А–µ–∞–Ї—Ж–Є–є, –≤–Ї–ї—О—З–∞—О—Й–Є—Е—Б—П –њ—А–Є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –Є—И–µ–Љ–Є–Є [1]. –†–µ–Ј—Г–ї—М—В–∞—В—Л —Е–∞—А–∞–Ї—В–µ—А–Є—Б—В–Є–Ї–Є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ––≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–≥–Њ —А–∞–≤–љ–Њ–≤–µ—Б–Є—П –≥–ї—Г—В–∞—В–Є–Њ–љ––∞—Б–Ї–Њ—А–±–∞—В–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л –њ–Њ–і—В–≤–µ—А–ґ–і–∞—О—В, —З—В–Њ –њ—Г–ї –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–≥–Њ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –≤ –љ–∞—З–∞–ї—М–љ–Њ–Љ –њ—А–Њ—Ж–µ—Б—Б–µ —А–∞–Ј–≤–Є—В–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞ –њ–Њ–≤—Л—И–µ–љ, —З—В–Њ —Г–Ї–∞–Ј—Л–≤–∞–µ—В –љ–∞ –∞–Ї—В–Є–≤–Є–Ј–∞—Ж–Є—О –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ–Њ–є –Ј–∞—Й–Є—В—Л. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л —Б–Њ–≤–њ–∞–і–∞—О—В —Б –Љ–љ–µ–љ–Є–µ–Љ —А—П–і–∞ –∞–≤—В–Њ—А–Њ–≤, –Њ—В–Љ–µ—З–∞—О—Й–Є—Е —Г–≤–µ–ї–Є—З–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –њ—А–Є –Ф–≠ I —Б—В–∞–і–Є–Є, –љ–Њ –њ—А–Є –њ—А–Њ–≥—А–µ—Б—Б–Є—А–Њ–≤–∞–љ–Є–Є —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –Є—И–µ–Љ–Є–Є –Њ–љ –њ—А–Њ–≥—А–µ—Б—Б–Є–≤–љ–Њ –њ–∞—В–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є —Г–Љ–µ–љ—М—И–∞–µ—В—Б—П [1,6]. –Ю—Ж–µ–љ–Ї–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В–Є –∞—Б–Ї–Њ—А–±–∞—В–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л —Г –±–Њ–ї—М–љ—Л—Е –Ф–≠ –і–Њ –љ–∞—З–∞–ї–∞ –ї–µ—З–µ–љ–Є—П —Г–Ї–∞–Ј—Л–≤–∞–ї–∞ –љ–∞ —Б–љ–Є–ґ–µ–љ–Є–µ –Њ—Б–љ–Њ–≤–љ—Л—Е –њ–Њ–Ї–∞–Ј–∞—В–µ–ї–µ–є. –Я—А–Є–Љ–µ–љ–µ–љ–Є–µ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї–Њ –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є–Є –Ї–Њ–љ—Ж–µ–љ—В—А–∞—Ж–Є–Є –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–љ–Њ–є –Є —Б–љ–Є–ґ–µ–љ–Є—О –Њ–Ї–Є—Б–ї–µ–љ–љ–Њ–є —Д–Њ—А–Љ—Л –≥–ї—Г—В–∞—В–Є–Њ–љ–∞. –І–µ—А–µ–Ј 30 –і–љ–µ–є –њ—А–Є–µ–Љ–∞ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–∞ –Њ—В–Љ–µ—З–∞–ї–Њ—Б—М –њ–Њ–≤—Л—И–µ–љ–Є–µ —Б–Њ–і–µ—А–ґ–∞–љ–Є—П –Р–Ъ, –Њ–і–љ–∞–Ї–Њ —Г—А–Њ–≤–µ–љ—М –Њ—Б—В–∞–≤–∞–ї—Б—П –љ–Є–ґ–µ –љ–Њ—А–Љ—Л. –Я–Њ–ї—Г—З–µ–љ–љ—Л–µ —А–µ–Ј—Г–ї—М—В–∞—В—Л –љ–Њ—Б—П—В –њ—А–µ–і–≤–∞—А–Є—В–µ–ї—М–љ—Л–є —Е–∞—А–∞–Ї—В–µ—А, –Њ–љ–Є –Љ–Њ–≥—Г—В —Б–≤–Є–і–µ—В–µ–ї—М—Б—В–≤–Њ–≤–∞—В—М –Њ –≤–Њ–Ј–Љ–Њ–ґ–љ–Њ–Љ –≤–ї–Є—П–љ–Є–Є –њ—А–µ–њ–∞—А–∞—В–∞ –љ–∞ –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –≥–ї—Г—В–∞—В–Є–Њ–љ––∞—Б–Ї–Њ—А–±–∞—В–љ–Њ–є –Њ–Ї–Є—Б–ї–Є—В–µ–ї—М–љ–Њ––≤–Њ—Б—Б—В–∞–љ–Њ–≤–Є—В–µ–ї—М–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л.
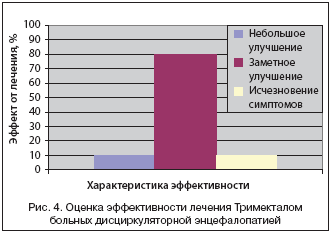
–Ю—Ж–µ–љ–Ї–∞ —Н—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В–Є –ї–µ—З–µ–љ–Є—П –±–Њ–ї—М–љ—Л—Е —Б –Ф–≠ –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞—В–µ–ї–µ–Љ –Є –њ–∞—Ж–Є–µ–љ—В–Њ–Љ —З–µ—А–µ–Ј 60 –і–љ–µ–є –њ–Њ 5––±–∞–ї–ї—М–љ–Њ–є —И–Ї–∞–ї–µ –њ–Њ–Ј–≤–Њ–ї–Є–ї–∞ —Е–∞—А–∞–Ї—В–µ—А–Є–Ј–Њ–≤–∞—В—М –њ–Њ–ї—Г—З–µ–љ–љ—Л–є —Н—Д—Д–µ–Ї—В: –љ–µ–±–Њ–ї—М—И–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ – 10%; –Ј–∞–Љ–µ—В–љ–Њ–µ —Г–ї—Г—З—И–µ–љ–Є–µ – 80%; –Є—Б—З–µ–Ј–љ–Њ–≤–µ–љ–Є–µ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤ (—А–µ–≥—А–µ—Б—Б –±–Њ–ї—М—И–Є–љ—Б—В–≤–∞ —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤) – 10%; —Г—Е—Г–і—И–µ–љ–Є—П, –Ї–∞–Ї –Є «–±–µ–Ј —Н—Д—Д–µ–Ї—В–∞», –љ–µ –Њ—В–Љ–µ—З–µ–љ–Њ –љ–Є –≤ –Њ–і–љ–Њ–Љ —Б–ї—Г—З–∞–µ (—А–Є—Б. 4).
–Ґ–∞–Ї–Є–Љ –Њ–±—А–∞–Ј–Њ–Љ, –ї–µ—З–µ–љ–Є–µ –±–Њ–ї—М–љ—Л—Е –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є I, II —Б—В–∞–і–Є–є –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і–µ–ї—М —Е–Њ—А–Њ—И–Њ –њ–µ—А–µ–љ–Њ—Б–Є—В—Б—П –њ–∞—Ж–Є–µ–љ—В–∞–Љ–Є.
–Ъ–ї–Є–љ–Є—З–µ—Б–Ї–Є–є —Н—Д—Д–µ–Ї—В —Б–Њ–њ—А–Њ–≤–Њ–ґ–і–∞–ї—Б—П –њ–Њ–ї–Њ–ґ–Є—В–µ–ї—М–љ–Њ–є –і–Є–љ–∞–Љ–Є–Ї–Њ–є —Б—Г–±—К–µ–Ї—В–Є–≤–љ—Л—Е –Є –љ–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є—Е —Б–Є–Љ–њ—В–Њ–Љ–Њ–≤, —Г 57% –±–Њ–ї—М–љ—Л—Е –Њ—В–Љ–µ—З–∞–ї–∞—Б—М —Б—В–∞–±–Є–ї—М–љ–∞—П –љ–Њ—А–Љ–∞–ї–Є–Ј–∞—Ж–Є—П —Ж–Є—Д—А –Р–Ф –љ–∞ —Д–Њ–љ–µ —Б–Њ—З–µ—В–∞–љ–љ–Њ–є —Б –Ґ—А–Є–Љ–µ–Ї—В–∞–ї–Њ–Љ –≥–Є–њ–Њ—В–µ–љ–Ј–Є–≤–љ–Њ–є —В–µ—А–∞–њ–Є–Є.
–Я—А–µ–њ–∞—А–∞—В —Б–њ–Њ—Б–Њ–±—Б—В–≤–Њ–≤–∞–ї –≤–Њ—Б—Б—В–∞–љ–Њ–≤–ї–µ–љ–Є—О –≥–µ–Љ–Њ–і–Є–љ–∞–Љ–Є–Ї–Є —Б —А–µ–≥—А–µ—Б—Б–Њ–Љ –∞—А—В–µ—А–Є–∞–ї—М–љ–Њ–є –Є –≤–µ–љ–Њ–Ј–љ–Њ–є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—Ж–Є–Є.
–Я–Њ–ї—Г—З–µ–љ–љ—Л–µ –і–∞–љ–љ—Л–µ –њ–Њ–Ј–≤–Њ–ї—П—О—В —А–µ–Ї–Њ–Љ–µ–љ–і–Њ–≤–∞—В—М –і–∞–љ–љ—Л–є –њ—А–µ–њ–∞—А–∞—В —Б —Ж–µ–ї—М—О –ї–µ—З–µ–љ–Є—П –Є –њ—А–Њ—Д–Є–ї–∞–Ї—В–Є–Ї–Є —А–∞–Ј–≤–Є—В–Є—П —Е—А–Њ–љ–Є—З–µ—Б–Ї–Њ–є –љ–µ–і–Њ—Б—В–∞—В–Њ—З–љ–Њ—Б—В–Є –Љ–Њ–Ј–≥–Њ–≤–Њ–≥–Њ –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П.



–Ы–Є—В–µ—А–∞—В—Г—А–∞
1. –Т–µ—А–ї–∞–љ –Э.–Т. –Ъ–ї–Є–љ–Є–Ї–Њ–—Д–∞—А–Љ–∞–Ї–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –∞–љ–∞–ї–Є–Ј —Б–Њ—Б—В–Њ—П–љ–Є—П —Б–Є—Б—В–µ–Љ—Л –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ –њ—А–Є —Ж–µ—А–µ–±—А–∞–ї—М–љ–Њ–є –Є—И–µ–Љ–Є–Є –Р–≤—В–Њ—А–µ—Д. –і–Є—Б—Б. –і–Њ–Ї—В. … –Љ–µ–і. –љ–∞—Г–Ї. –Ь–Њ—Б–Ї–≤–∞, 2008.– 42 —Б.
2. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т., –Я–∞—А—Д–µ–љ–Њ–≤ –Т.–Р., –°–Ї–Њ—А–Њ–Љ–µ—Ж –Р.–Р., –ѓ—Е–љ–Њ –Э.–Э. –Э–∞—А—Г—И–µ–љ–Є—П –Ї—А–Њ–≤–Њ–Њ–±—А–∞—Й–µ–љ–Є—П –≤ –≥–Њ–ї–Њ–≤–љ–Њ–Љ –Є —Б–њ–Є–љ–љ–Њ–Љ –Љ–Њ–Ј–≥–µ. –Т –Ї–љ.: –С–Њ–ї–µ–Ј–љ–Є –љ–µ—А–≤–љ–Њ–є —Б–Є—Б—В–µ–Љ—Л: –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –і–ї—П –≤—А–∞—З–µ–є. –Ь.: –Ь–µ–і–Є—Ж–Є–љ–∞, 2003.– –°. 274–291.
3. –Ф–∞–Љ—Г–ї–Є–љ –Ш.–Т. –Ф–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П: –њ–∞—В–Њ–≥–µ–љ–µ–Ј, –Ї–ї–Є–љ–Є–Ї–∞, –ї–µ—З–µ–љ–Є–µ. –Ь–µ—В–Њ–і. –†–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є. –Ь., 2005. – 48 —Б.
4. –Ф–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–∞—П —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є—П. –Ь–µ—В–Њ–і–Є—З–µ—Б–Ї–Є–µ —А–µ–Ї–Њ–Љ–µ–љ–і–∞—Ж–Є–Є /–Я–Њ–і —А–µ–і. –Э.–Э. –ѓ—Е–љ–Њ. – –Ь.:–†–Ъ–Ш –°–Њ–≤–µ—А–Њ –њ—А–µ—Б—Б, 2005. – 32 —Б.
5. –Ъ–Њ–ї–µ—Б–љ–Є—З–µ–љ–Ї–Њ –Ы.–°. —Б —Б–Њ–∞–≤. –°–Є—Б—В–µ–Љ–∞ –≥–ї—Г—В–∞—В–Є–Њ–љ–∞ —Н—А–Є—В—А–Њ—Ж–Є—В–Њ–≤ –Є –њ–ї–∞–Ј–Љ—Л –Ї—А–Њ–≤–Є –њ—А–Є –Є–љ—Б—Г–ї—М—В–∞—Е –Є –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–Є //–С–Є–Њ–Љ–µ–і–Є—Ж–Є–љ—Б–Ї–∞—П —Е–Є–Љ–Є—П: –Э–∞—Г—З–љ–Њ––њ—А–∞–Ї—В–Є—З–µ—Б–Ї–Є–є –ґ—Г—А–љ–∞–ї,2007.– –Ґ.53, вДЦ4.– –°.454–460.
6. –Ъ–Њ–ї—Б–∞–љ–Њ–≤ –Р.–С. –Ф–Є–∞–≥–љ–Њ—Б—В–Є—З–µ—Б–Ї–Њ–µ –Ј–љ–∞—З–µ–љ–Є–µ –≥–∞–Љ–Љ–∞––≥–ї—Г—В–∞–Љ–∞—В —В—А–∞–љ—Б—Д–µ—А–∞–Ј—Л –њ—А–Є —Г–Љ–µ—А–µ–љ–љ—Л—Е –Ї–Њ–≥–љ–Є—В–Є–≤–љ—Л—Е –љ–∞—А—Г—И–µ–љ–Є—П—Е —Г –њ–∞—Ж–Є–µ–љ—В–Њ–≤ —Б –і–Є—Б—Ж–Є—А–Ї—Г–ї—П—В–Њ—А–љ–Њ–є —Н–љ—Ж–µ—Д–∞–ї–Њ–њ–∞—В–Є–µ–є I –Є II —Б—В–∞–і–Є–є. –Р–≤—В–Њ—А–µ—Д.–і–Є—Б. ….–Ї–∞–љ–і.–Љ–µ–і –љ–∞—Г–Ї. –Ш–≤–∞–љ–Њ–≤–Њ, 2006. – 18 —Б.
7. –Ь–∞–Ї–Њ–ї–Ї–Є–љ –Т.–Ш., –Ю—Б–∞–і—З–Є–є –Ъ.–Ъ. –≠—Д—Д–µ–Ї—В–Є–≤–љ–Њ—Б—В—М –Є –њ–µ—А–µ–љ–Њ—Б–Є–Љ–Њ—Б—В—М —В—А–Є–Љ–µ—В–∞–Ј–Є–і–Є–љ–∞ –њ—А–Є –ї–µ—З–µ–љ–Є–Є —Б—В–∞–±–Є–ї—М–љ–Њ–є —Б—В–µ–љ–Њ–Ї–∞—А–і–Є–Є –љ–∞–њ—А—П–ґ–µ–љ–Є—П –≤ —В–µ—З–µ–љ–Є–µ 8 –љ–µ–і–µ–ї—М// –Ъ–∞—А–і–Є–Њ–ї–Њ–≥–Є—П.–2003.–43(6). – 18–22.
8. –Я—Г—В–Є–ї–Є–љ–∞ –Ь.–Т. –•—А–Њ–љ–Є—З–µ—Б–Ї–∞—П –Є—И–µ–Љ–Є—П –Љ–Њ–Ј–≥–∞//–Ы–µ—З–∞—Й–Є–є –≤—А–∞—З.– 2005.– вДЦ6.– –°. 28–33.
9. –Ґ—А–∞–≤–Є–љ–∞ –Ю.–Т. –Т –Ї–љ.: –†—Г–Ї–Њ–≤–Њ–і—Б—В–≤–Њ –њ–Њ –±–Є–Њ—Е–Є–Љ–Є—З–µ—Б–Ї–Є–Љ –Є—Б—Б–ї–µ–і–Њ–≤–∞–љ–Є—П–Љ. –Ь., 1955. –°. 253–254.
10. –®–Љ–Є–і—В –Х.–Т. –Ъ–ї–∞—Б—Б–Є—Д–Є–Ї–∞—Ж–Є—П —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –њ–Њ—А–∞–ґ–µ–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Є —Б–њ–Є–љ–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞// –Ц—Г—А–љ. –Э–µ–≤—А–Њ–њ–∞—В–Њ–ї.–Є –њ—Б–Є—Е–Є–∞—В—А.– 1985.––Ґ.85, вДЦ9.– –°. 1281–1288.
11. –®–њ–∞–Ї–Њ–≤ –Р.–Х. –Ъ –Љ–µ—В–Њ–і–Є–Ї–µ —А–∞–Ј–і–µ–ї—М–љ–Њ–≥–Њ –Њ–њ—А–µ–і–µ–ї–µ–љ–Є—П –Њ–±—Й–µ–є —А–µ–і—Г—Ж–Є—А–Њ–≤–∞–љ–љ–Њ–є –Є –і–µ–≥–Є–і—А–Њ–∞—Б–Ї–Њ—А–±–Є–љ–Њ–≤–Њ–є –Ї–Є—Б–ї–Њ—В.//–Ы–∞–±. –Ф–µ–ї–Њ, 1967,вДЦ5.– –°. 305–306.
12.–ѓ–≤–Њ—А—Б–Ї–∞—П –Т.–Р., –Ь–∞–ї–∞—Е–Њ–≤ –Т.–Т., –С–µ–ї–Њ—Г—Б –Р.–Ь. –Ш–љ—В–µ–љ—Б–Є–≤–љ–Њ—Б—В—М –њ—А–Њ—Ж–µ—Б—Б–Њ–≤ –њ–µ—А–µ–Ї–Є—Б–љ–Њ–≥–Њ –Њ–Ї–Є—Б–ї–µ–љ–Є—П –ї–Є–њ–Є–і–Њ–≤ –Є –∞–Ї—В–Є–≤–љ–Њ—Б—В—М –∞–љ—В–Є–Њ–Ї—Б–Є–і–∞–љ—В–љ—Л—Е —Д–µ—А–Љ–µ–љ—В–Њ–≤ –≤ —Н—А–Є—В—А–Њ—Ж–Є—В–∞—Е –њ—А–Є –љ–∞—З–∞–ї—М–љ—Л—Е —Д–Њ—А–Љ–∞—Е —Б–Њ—Б—Г–і–Є—Б—В—Л—Е –Ј–∞–±–Њ–ї–µ–≤–∞–љ–Є–є –≥–Њ–ї–Њ–≤–љ–Њ–≥–Њ –Љ–Њ–Ј–≥–∞.//–Э–µ–≤—А–Њ–ї–Њ–≥–Є—З–µ—Б–Ї–Є–є –≤–µ—Б—В–љ–Є–Ї.– 1995.––Ґ.XXXVII, –≤—Л–њ.3–4.– –°.15–17.
13. Iqbal S., Baziany A., Hussain M. et all. Trimetazidineas a potential neuroprotectant in transient global ischemia in gerbils: a bevioral and histological study//Brain Res.–2002.–928(1–2).–1–7.
14. Oguzhanoglu A.,Kurt T., Ortac R.,Turman B. Somatosensory evoketpotential and hystopathological investigations in ischemia–inducted brain damage: effects of trimetazidine in rats//Int.J. Neurosci.–2003.–113(4).p.447–454.












