Развитие депрессии может быть ситуационно обусловлено, однако у неврологических больных она, как правило, вызвана органическим поражением головного мозга или дисбалансом нейромедиаторных систем. Больные хроническими неврологическими заболеваниями в большей степени подвержены депрессии, чем больные с соматической патологией [15]. Неврологические заболевания, при которых может возникать депрессия, весьма многочисленны. Это расстройство входит в число частых симптомов при болезни Паркинсона, синдроме паркинсонизма, острых и хронических цереброваскулярных заболеваниях, дегенеративных деменциях, болевых синдромах, рассеянном склерозе, опухолях мозга [18,19,21,26]. Энцефалопатия, развивающаяся на поздних стадиях печеночной и почечной недостаточности, ряде эндокринных, гематологических и системных расстройств, при алкоголизме, также нередко сопровождается развитием депрессии, что связано с гипоксическим, дисметаболическим и токсическим поражением головного мозга. Депрессивные нарушения могут быть обусловлены длительным приемом лекарственных препаратов. Перечень этих препаратов достаточно велик, и многие весьма широко используются. Это b–блокаторы, блокаторы кальциевых каналов, кортикостероиды, анаболические стероиды, оральные контрацептивы, сердечные гликозиды, барбитураты, клоназепам. Нейролептическая депрессия возникает на фоне длительного приема больших доз нейролептиков (бутерофеноны, флуфеназин, хлорпромазин, рисперидон) и сопровождается экстрапирамидными расстройствами [2,6,26]. Депрессивные расстройства могут протекать под маской деменции и могут сопровождать ее развитие. При этом депрессия наблюдается часто при сосудистой деменции и реже – при болезни Альцгеймера [4].
Современный патоморфоз депрессии привел к изменению ее клинической картины, нарастанию частоты атипичных, скрытых, стертых форм. В настоящее время доля типичных случаев составляет лишь 10%, а основная масса депрессий протекает атипично. В практике врача–невролога депрессия чаще всего выступает под маской синдрома вегетативной дистонии, хронических болевых синдромов, инсомнии, нейроэндокринных расстройств [15,29,32]. К наиболее ярким проявлениям синдрома вегетативной дистонии относятся вегетативные кризы (панические атаки) [6]. Другой весьма нередкой маской депрессии являются хронические болевые синдромы, в том числе и у детей. Депрессия сопровождает и может усиливать конверсионные расстройства в рамках психогенных и психоорганических заболеваний.
Механизмы, лежащие в основе депрессии, в настоящее время активно изучаются. Показано, что в эмоциональных реакциях участвует не только лимбическая система, но и корковые структуры. Особое значение придают лобным долям головного мозга [30]. При ряде психических расстройств, которые традиционно считались “функциональными”, выявлены морфологические изменения нервной ткани, причем не только на микроструктурном уровне (в виде атрофии синапсов, укорочения дендритов и гибели части нейронов), но и на макроструктурном (в виде уменьшения объема гиппокампа и некоторых других отделов мозга). Более того, в последние годы было показано, что патологические процессы в мозге могут быть частично обратимыми под влиянием терапии препаратами, обладающими нейротрофическими и нейропротективными свойствами [15,16]. По некоторым данным, при депрессии обнаруживаются признаки гиперреактивности гипоталамо–гипофизарно–надпочечниковой системы, есть также сведения об увеличении количества нейронов, секретирующих кортикотропин–рилизинг фактор. У 33–66% больных депрессией отмечается гиперплазия надпочечников, а содержание кортизола повышено и положительно коррелирует с тяжестью состояния. Хроническая гиперкортизолемия способствует формированию инсулинорезистентности, артериальной гипертензии, гиперпродукции стероидов, гипергликемии, гиперхолестеринемии, повышающих риск сердечно–сосудистых осложнений [34]. По экспериментальным данным, в ситуациях хронического болевого, эмоционального или социального стресса (являющихся моделями депрессии) статистически достоверно уменьшается объем гиппокампа (до 10%, как и у больных депрессией), в зубчатой извилине снижается число гранулярных клеток, а в полях СА1 и СА3 гиппокампа уменьшаются размеры тел пирамидных клеток и развивается атрофия их дендритов (до 50% длины), что ведет к нарушению нормального функционирования лимбической системы и ее связей с другими отделами мозга [11]. Таким образом, последствия хронического стресса и аффективные расстройства у человека, как и сходные с депрессией нарушения поведения у животных, ассоциируются с повреждением и гибелью мозговых клеток. Эти данные согласуются с представлениями о том, что тревожные расстройства, вызванные стрессогенными факторами, могут не просто предшествовать, но и являться причиной, по крайней мере, некоторых форм депрессивных расстройств. Преимущественная локализация морфологических изменений прежде всего в лимбической системе, базальных ганглиях и ростральных отделах коры может объяснять развивающиеся при депрессии нарушения как эмоциональных, так и моторных и когнитивных функций. Предполагается, что эти морфологические изменения являются следствием цитотоксического действия ряда агентов, прежде всего возбуждающих аминокислот и, возможно, кальция [11]. Развитию эксайтотоксичности в немалой степени способствуют отмечаемое при депрессии повышенное содержание кортикостероидов (главным образом кортизола), и дефицит g–аминомасляной кислоты [2]. Не исключено, что в основе ряда нарушений лежат нейромедиаторные дисфункции, скорее всего, связанные с недостаточностью центральных серотонинергических и норадренергических структур. Некоторые авторы также упоминают в патогенезе депрессии роль гипогликемии и возможного снижения мозгового кровотока. Особое значение в патогенезе депрессии у пожилых придается сосудистому поражению субкортикально–фронтальных связей с возникновением, помимо депрессии, нарушений исполнительных функций, психомоторной заторможенности, апатии. В настоящее время рассматривается несколько патофизиологических механизмов влияния депрессии на состояние сердечно–сосудистой системы у пожилых. Одним из основных патологических процессов при депрессивных расстройствах является дисбаланс вегетативной нервной системы с активацией симпатического отдела. Повышенное выделение катехоламинов приводит к увеличению потребности миокарда в кислороде вследствие возрастания частоты сердечных сокращений, артериального давления и силы сокращения миокарда. Установлено, что появление депрессии у пациентов с заболеваниями сердечно–сосудистой системы сопровождается значимым снижением вариабельности сердечного ритма, отражая ухудшение регуляторных механизмов и снижение адаптационных возможностей организма в ответ на стресс [13,22].
Достижением нейронауки в последние годы стало доказательство, что деструктивные процессы, происходящие при аффективных расстройствах, являются частично обратимыми под влиянием успешной терапии препаратами, проявляющими нейротрофические и нейропротективные свойства [17]. Восстановление ткани мозга и его функций связывают с реорганизацией и формированием новых синапсов, удлинением и разрастанием (sprouting) дендритов и аксонов с нейрогенезом. Действие антидепрессантов при этом не ограничивается их регуляторным влиянием на содержание моноаминергических нейротрансмиттеров в синаптической щели и в пресинаптических структурах, а также на число и чувствительность постсинаптических рецепторов, но распространяется и на внутриклеточные каскады нейрохимических процессов. Одним из образуемых при этом соединений является цАМФ–элементсвязывающий белок (CREB), активирующий «поздний» ген мозгового нейротрофического фактора (англ. brain derived neurotrophic factor – BDNF), который, в свою очередь, усиливает экспрессию гена основного цитопротективного белка bcl–2, подавляющего апоптоз, что способствует восстановлению и выживанию нейронов [15].
Симптомы депрессии могут быть очевидными. Наряду с угнетенностью (в типичных случаях в виде витальной тоски) депрессия включает идеаторное и двигательное торможение со снижением мотивации к действию или тревожное возбуждение (вплоть до ажитации). Свойственная депрессивным больным психическая гипералгезия (душевная боль) сопряжена с чувством вины, снижением самооценки, суицидальными мыслями, а тягостное физическое самоощущение – с «соматическими» симптомами, такими как расстройства сна с трудностями засыпания и ранними пробуждениями; резкое снижение аппетита и массы тела; снижение либидо и нарушения менструального цикла вплоть до аменореи и др. Сниженное настроение обычно сохраняется на протяжении всего депрессивного приступа. Типичным признаком депрессии является также суточный ритм с улучшением или (реже) ухудшением самочувствия к вечеру. Атипичные проявления депрессии – это отсутствие в ряде случаев жалоб на сниженное настроение или фиксация пациента на возбудимости или тревожности, а не на сниженном настроении. Боль и психосоматические нарушения также могут быть атипичными проявлениями депрессии. Критериями диагностики маскированных депрессий являются: частое несоответствие жалоб больного характеру морфологических изменений; возможность отсутствия объективных признаков соматического заболевания; периодичность (сезонность) манифестации симптоматики заболевания; ремиттирующее течение с возможной сменой фаз обострений и рецидивов; связь самочувствия с биологическим ритмом физиологических функций (больные лучше чувствуют себя в вечернее время); частые повторные обращения за медицинской помощью; недостаточная эффективность симптоматической терапии или отсутствие таковой; улучшение самочувствия на фоне приема антидепрессантов.
Выявление депрессивных расстройств в значительной степени облегчается при использовании психометрических шкал и тестов, применение которых позволяет снизить затраты времени врача на обследование. Наиболее известными среди субъективных психометрических шкал для скрининга депрессии являются Госпитальная шкала тревоги и депрессии [A. Zigmond, 1983] шкала Цунга [W.W. Zung, 1965], опросник депрессии Бека [А. Beck, 1961] [2,3,17,20,28,34,35].
Основой диагностики депрессии является оценка анамнеза и клинических данных. Результаты параклинических методов обследования (включая нейровизуализацию) большого значения не имеют, они лишь помогают исключить неврологические или соматические причины заболевания. Выявляемость депрессии врачами общей практики не превышает 50% [16,35]. В определенной степени это обусловлено малой специфичностью клинических проявлений данного заболевания. Так, например, потеря веса и повышенная утомляемость могут отмечаться не только при депрессии, но и при онкологических заболеваниях, сахарном диабете и заболеваниях щитовидной железы.
В неврологической практике диагностика депрессии вызывает сложности не только из–за частого сочетания неврологической симптоматики и депрессии при поражении центральной нервной системы, но и из–за влияния неврологического заболевания на эмоциональное поведение больного. Так, характерная для паркинсонизма замедленность и скудость движений в сочетании с нарушением ритма и интонаций речи затрудняет правильную оценку эмоционального статуса. Еще более усложняется эта задача у больных с выраженными когнитивными или речевыми нарушениями различного генеза [4,7]. Пристального внимания заслуживают жалобы на хроническую боль – одну из наиболее частых «масок» депрессии. Сочетание депрессии и хронических болевых синдромов отмечается у 50–60 % больных.
Терапия антидепрессантами является основным методом лечения депрессивных состояний. Вопрос о начале медикаментозной терапии становится актуальным, если симптоматика сохраняется на протяжении 2–4 недель и более. Следует отметить, что около 50% случаев неэффективности терапии связано с ее неадекватным применением [5,6]. Наиболее распространенными ошибками, помимо несвоевременного начала лечения, а также недостаточного учета клинических показаний и противопоказаний к препарату, являются проведение шаблонной (без учета индивидуальных особенностей) терапии низкими дозами или, наоборот, частая смена, «жонглирование» препаратами без соблюдения экспозиции нужной длительности, или преждевременная отмена терапии, или игнорирование пациентом врачебных назначений [12]. Как известно, во многих случаях клинический эффект развивается постепенно, и подавление актуальной психопатологической симптоматики еще не означает достижения стабильной ремиссии и окончания лечения. Действие антидепрессантов обычно проявляется не сразу, а через несколько недель (обычно от 3 до 6) после начала приема, о чем надо своевременно информировать пациента. После регресса симптомов депрессии терапию продолжают 4–5 месяцев. Неэффективность лечения, связанная с истинной лекарственной резистентностью, встречается очень редко, поэтому лишь если эффект подобранного препарата в адекватной дозе не проявляется через 6–8 недель, переходят на антидепрессант другой группы. Важно подчеркнуть, что в большинстве случаев отсутствие эффекта от лечения обусловлено не истинной лекарственной резистентностью, а недостаточной дозой или небольшой продолжительностью терапии, а также несоблюдением врачебных назначений. Возможности психотерапии, которая при необходимости может дополняться антидепрессантами, в настоящее время обсуждаются, однако эффективность подобного терапевтического подхода требует дальнейшего изучения.
В неврологической практике зачастую приходится сталкиваться с ограничительной тактикой использования антидепрессантов [6]. Из числа лиц с эпидемиологическим диагнозом депрессии в амбулаторной практике (набравших более 18 баллов по шкале депрессий Центра эпидемиологических исследований) лечение получали 72,2% больных. Однако применялись, как правило, медикаментозные средства растительного происхождения и транквилизаторы. Антидепрессанты принимали лишь 8,7% больных депрессиями. Если препараты этой группы все же назначали, то, как правило, в достаточно низких суточных дозах [6]. В российском многоцентровом исследовании Компас установлено, что неврологи лишь ненамного чаще, чем другие специалисты (терапевты, кардиологи), назначают какую–либо терапию по поводу депрессивных состояний вообще (74% против 67,2 и 67,8% соответственно) и тимолептики, в частности (14,1% против 7,2 и 6,5% соответственно) [5]. Таким образом, роль медикаментозной коррекции депрессии нуждается в дополнительных обсуждениях.
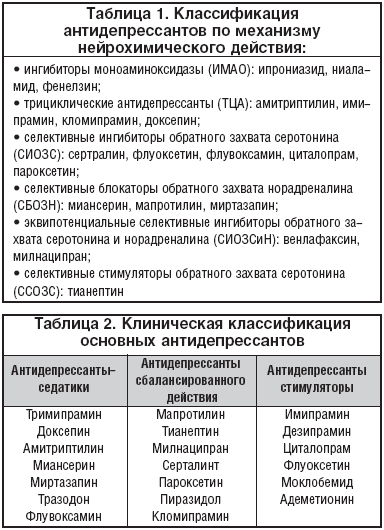
Антидепрессанты – лекарственные средства, способствующие редукции обусловленных депрессией идеаторных, двигательных и сомато–вегетативных расстройств. В основе клинического эффекта современных антидепрессантов лежит коррекция функций серотонинергической и норадренергической систем головного мозга. Весьма удобной является классификация антидепрессантов по механизму нейрохимического действия (табл. 1). Среди клинических классификаций антидепрессантов наибольшее распространение получила удобная и простая классификация П. Кильгольца с выделением препаратов с преимущественно седативным, стимулирующим или сбалансированным действием (табл. 2). Научная разработка современных антидепрессантов, с одной стороны, идет в направлении увеличения специфичности их биохимического действия. В частности, синтезируются и апробируются избирательные агонисты и антагонисты моноаминовых нейрорецепторов. Найдены вещества, избирательно воздействующие на определенные типы рецепторов (5НТ1, 5НТ2, и 5НТ3 серотониновые рецепторы). Примерами могут служить прямые агонисты 5НТ1а серотониновых рецепторов (флезиноксан, ипсапирон и др.). В то же время сохраняется тенденция к разработке средств широкого действия на различные моноаминовые системы с минимальным влиянием на рецепторы, с которыми связано развитие побочных явлений (милнаципран, венлафаксин, нефазодон, миртазапин, дулоксетин и др.). И, наконец, механизм действия некоторых препаратов с тимоаналептической активностью не связан прямо с моноаминовой системой или недостаточно ясен (например, тианептин, алпразолам, S–аденозилметионин, нейропептиды и др.) [12,17,27,33].
Среди наиболее изученных на фармацевтическом рынке за последние два десятилетия получили распространение так называемые антидепрессанты третьего поколения, являющиеся представителями нового класса фармакологических средств – селективных ингибиторов обратного захвата серотонина. К ним, в частности, относится флувоксамин [3,12,14].
В отличие от трициклических антидепрессантов селективные ингибиторы обратного захвата серотонина больше адресуются к широкому кругу депрессивных состояний невротического уровня. Они обладают большей широтой спектра психотропного действия при меньшем числе вызываемых побочных эффектов. Ядерные варианты меланхолического синдрома эндогенной депрессии с типично циркадной симптоматикой, тяжелые (психотические) депрессии и депрессивно–бредовые состояния хуже реагируют на терапию ингибиторами обратного захвата серотонина. Напротив, депрессивные состояния с обессивно–фобической, ипохондрической и тревожной симптоматикой невротического уровня лечатся достаточно успешно. Помимо депрессий с атипичной симптоматикой, была показана высокая эффективность серотонинергических антидепрессантов при тревожных и обессивно–компульсивных расстройствах в чистом виде или коморбидных с депрессией, а также при паническом расстройстве, постравматическом стрессовом расстройстве, социальной фобии, соматоформных нарушениях и других тревожных расстройствах [1,10,12,14,27].
Анализ ряда рандомизированных испытаний сравнения клинического эффекта группы селективных ингибиторов обратного нейронального захвата с трициклическими антидепрессантами, такими как имипрамин, обнаружил сходные положительные эффекты неселективных и селективных препаратов. При подведении итогов всех клинических испытаний стало ясно, что у селективных препаратов нет никаких четких преимуществ перед эталонными трициклическими антидепрессантами. Негативные же эффекты препаратов этих групп различаются существенно. Например, вероятность седативного эффекта, антихолинергического эффекта и нарушений сердечного ритма при использовании селективных ингибиторов обратного нейронального захвата серотонина меньше, чем при применении обычных антидепрессантов. С другой стороны, негативные эффекты селективных ингибиторов обратного нейронального захвата затрагивают желудочно–кишечный тракт, вызывая тошноту и диарею, а также могут привести к бессоннице, возбуждению, экстрапирамидным расстройствам (лекарственный паркинсонизм) и синдрому отмены. При сравнении негативных эффектов селективных ингибиторов обратного нейронального захвата и обычных антидепрессантов нельзя не прийти к выводу, что одна группа негативных эффектов меняется на другую и нет никакой разницы в количестве людей, которые могут принимать эти две группы антидепрессантов. В ходе 58 клинических испытаний изучались пациенты, которые прекратили прием антидепрессантов, и при этом не было обнаружено значимой разницы между селективными ингибиторами обратного нейронального захвата и обычными антидепрессантами.
Таким образом, многочисленные научные исследования этой группы препаратов, в том числе проведенные в сравнении с эталонными трициклическими антидепрессантами, традиционно используемыми в психиатрии и неврологии при лечении депрессий (амитриптилином, имипрамином, кломипрамином и др.), показали их высокую терапевтическую эффективность, сопоставимую с трициклическими соединениями, при меньшем числе побочных явлений [2,6,8,9,12,14,31,33]. Однако несмотря на принадлежность к одной группе химических соединений, спектр антидепрессивной активности различных селективных ингибиторов обратного нейронального захвата имеет свои особенности, которые определяют преимущественные показания к их индивидуальному назначению и заслуживают обсуждения.
Флувоксамин является родоначальником антидепрессантов группы селективных ингибиторов обратного захвата серотонина, первым и наиболее широко изученным препаратом этой группы. Флувоксамин зарегистрирован более чем в 80 странах, имеет самую большую (среди антидепрессантов) базу данных клинических исследований, включающую описание результатов лечения 38 тыс. пациентов. На сегодняшний день опубликовано более 5000 научных работ, посвященных изучению препарата. Препарат успешно применяется с 1983 г. в терапии депрессивных расстройств разной степени выраженности, а также так называемых пограничных психических нарушений (тревожных, панических, обсессивно–компульсивных, поведенческих и пр., в том числе у детей от 8 лет) [10]. Механизм действия флувоксамина связан с избирательным ингибированием обратного захвата серотонина нейронами головного мозга и характеризуется минимальным влиянием на норадренергическую передачу. Флувоксамин обладает невыраженной способностью связываться с a–адренергическими, b–адренергическими, гистаминергическими, мускариновыми холинергическими, дофаминергическими или серотонинергическими рецепторами. Флувоксамин обладает выраженными анксиолитическими и седативными свойствами и служит препаратом выбора для лечения депрессий в сочетании с тревогой, паникой и психомоторной ажитацией. Препарат отличает также умеренная психостимулирующая активность, следствием чего является отсутствие суицидогенности, гиперстимуляции, усиления раздражительности, нарушений сна. Мощный вегетостабилизирующий эффект флувоксамина особенно важен при лечении невротических, соматизированных депрессий и дистимий. Отсутствие поведенческой токсичности не нарушает внимание, память и когнитивные функции. Флувоксамин является эффективным антидепрессантом при лечении депрессий различного типа и различной степени выраженности. Это подтверждено, в частности, данными мета–анализа, согласно которым флувоксамин является препаратом выбора при лечении больных с тяжелой депрессией в условиях стационара. Кроме того, доказана эффективность флувоксамина в предупреждении рецидивов депрессии. После курса лечения препаратом рецидивы развивались в три раза реже, а период ремиссии до первого рецидива был в два раза продолжительнее, чем при применении плацебо. Выраженный антикверинговый эффект флувоксамина устраняет или снижает патологическое влечение к алкоголю. В психиатрической практике препарат продемонстрировал хорошую эффективность при коррекции негативной (дефицитарной) симптоматики у больных шизофренией.
В клиническом отделе эндогенных психических расстройств и аффективных состояний Научного Центра психического здоровья РАМН в разные периоды проходили клиническое изучение флуоксетин, флувоксамин, сертралин и пароксетин. Всего этими препаратами прошли курсовое лечение 129 больных эндогенной депрессией. Флувоксамин позволял снизить тяжесть депрессии в этой группе до легкой степени уже к 5 дню лечения, но как «значительный» его терапевтический эффект регистрировался после 14 дня (второй недели) лечения, а к концу курсового лечения суммарная балльная оценка симптомов депрессии по шкале Гамильтона снижалась на 64,6%. Флувоксамин показал хороший терапевтический эффект в равной мере при депрессивных состояниях легкой и средней степени тяжести, что при условии его хорошей изученности делает его препаратом выбора при данной группе состояний. Тимолептический эффект флувоксамина проявился на уровне 76,1%, тогда как седативно–анксиолитический и стимулирующий компоненты действия флувоксамина были практически одинаковыми и менее глубокими, они проявлялись на уровне 67,8 и 64,5%, соответственно [14]. Измайлова И.Г. и соавт. оценивали эффект флувоксамина в группе детей с головной болью напряжения. Начальная доза флувоксамина составляла 12,5 мг на ночь, с дальнейшим постепенным повышением дозы по 12,5 мг каждые два дня до оптимальной суточной дозы – 50–75 мг. Курс лечения составил 1,5–2 месяца. Указанную фармакотерапию сочетали с массажем, психотерапией, физиотерапией. Клинический эффект в виде уменьшения головной боли и улучшения настроения пациенты начинали отмечать к концу первой недели лечения, побочных эффектов не наблюдалось. Через 1,5 месяца терапии у 25 детей полностью купировались имевшиеся нарушения; у 5 детей отмечалось снижение интенсивности и частоты приступов цефалгии. Динамическое изучение психовегетативного статуса показало достоверное снижение астено–вегетативных и тревожно–депрессивных расстройств до близких к нормальным показателям, что подтверждает анксиолитическое, антидепрессантное, вегетотропное и мягкое антиастеническое действие препарата в детской популяции. Катамнез (6 месяцев) подтвердил сохранение достигнутых результатов у 20 детей.
Терапия антидепрессантами различной структуры традиционно давно применяется при хронической алкогольной болезни. Ряд отечественных и европейских исследователей убедительно высказываются в пользу центральной серотониновой недостаточности как основного нейрохимического механизма развития депрессии при алкоголизме. С помощью антидепрессантов можно не только воздействовать на депрессивные расстройства, но и купировать патологическое влечение к алкоголю. И в этом плане наиболее предпочтительны селективные ингибиторы обратного захвата серотонина, снижающие патологическое влечение к алкоголю. По многочисленным отечественным данным, именно флувоксамин – антидепрессант «преимущественно седативного действия с выраженными не только тимоаналептическими, но и вегетостабилизирующими и анксиолитическими эффектами» – наиболее предпочтителен при хроническом алкоголизме и наркоманиях в силу высокой коморбидности алкогольным депрессиям тревожных, фобических, сомнологических, соматовегетативных расстройствах, а также агрессивности и суицидального поведения [10].
Хорошая переносимость флувоксамина, в частности, отсутствие седативного побочного эффекта, позволяет использовать его в амбулаторной практике, без снижения качества жизни пациента. Важно подчеркнуть, что флувоксамин является не только максимально изученным, но и экономически наиболее доступным препаратом из группы селективных ингибиторов захвата серотонина. Важнейшим условием успеха лечения является рациональное сочетание фармакотерапии с социореабилитационными и психотерапевтическими мероприятиями, включая психообразовательную работу с активным вовлечением больного и его родственников в лечебный процесс.
Литература
1. Вознесенская Т.Г. Антидепрессанты в неврологической практике // Лечение нервных болезней. 2000. № 1. С. 8–13.
2. Вознесенская Т.Г. Депрессия в неврологической практике и ее лечение // Неврологический журнал. 2006. Т. 11. № 6. С. 4–11.
3. Глушков Р.Г., Андреева Н.И., Алеева Г.Н. Депрессии в общемедицинской практике // РМЖ. 2005. Т. 13. № 12. С. 858–60.
4. Дамулин И.В. Болезнь Альцгеймера и сосудистая деменция / под ред. Н.Н. Яхно. М., 2002. 85 с.
5. Депрессия в общемедицинской практике. Результаты программы Компас. //Оганов Р.Г., Ольбинская Л.И., Смулевич А.Б. и др. – Изд: Сервье, 2004.
6. Дробижев М.Ю., Воробьева О.В. Диагностика и лечение депрессий в неврологической практике: современное состояние проблемы.//Консилиум Медикум. – 2006. – №8.
7. Захаров В.В., Яхно Н.Н. Нарушения памяти. М., 2003. 160 с.
8. Краснов В.Н. Современные подходы к терапии депрессий // РМЖ. 2002. Т. 10. № 12–13. С. 553–55.
9. Крылов В.И. Антидепрессанты в общемедицинской практике. Эффективность и безопасность терапии. // «ФАРМиндекс–Практик», – 2003 – №5, с. 22–32.
10. Милопольская И.М. Коньков Е.М., Булаев В.М. Феварин в терапии хронического алкоголизма. //Консилиум Медикум. – 2006. – №3.
11. Мосолов С.Н. Биологические основы современной антипсихотической терапии // Российский психиатрический журнал, 1998, N6, с.712.
12. Мосолов С.Н. Клиническое применение современных антидепрессантов. // Медицинское информационное агенство. С.П., 1995, с. 568.
13. Оздоева Л.Д. Взаимосвязь факторов риска атеросклероза и тревожно–депрессивных состояний у мужчин из неорганизованной популяции // Кардиваскулярная терапия и профилактика. 2003. № 2(1). С. 59–64.
14. Пантелеева Г.П., Абрамова Л.И., Коренев А.Н. Сравнительная характеристика терапевтической эффективности нового поколения антидепрессантов из группы СИОЗС. //Журн. Современная психиатрия. – 1998. – 6. с. 12–16.
15. Симаненков В.И. От теории психосоматической медицины – к терапевтической практике // Медлайн–экспресс. 2006. № 4 (187). С. 3–7.
16. Смулевич А.Б. Депрессии в общей медицине. //М.: Медицинское информационное агентство, 2001. 256 с.
17. Смулевич А.Б. Подходы к терапии депрессий в общемедицинской практике // РМЖ. 2003. Т. 11. № 21. С. 1192–96.
18. Aarsland D, Cummings JL. Depression in Parkinson disease. Acta Psychiatr Scand 2002;106:161–62.
19. Alexopoulos GS. Vascular disease, depression and dementia. J Am Ger Soc 2003;51:1178–80.
20. Alexopoulos GS, Kiosses DN, Klimstra S, et al. Clinical presentation of the «depression–executive dysfunction syndrome» of late life. Am J Ger Psychiatr 2002;10:98–106.
21. Barber R. Noncognitive symptoms. In: Cerebrovascular Disease, Cognitive Impairment and Dementia. Second edition. Ed by J O’Brien et al. London, New York Martin Dunitz 2004, p. 253–69.
22. Carney R.M., Freedland K.E., Rich M.W., Jaffe A.S. Depression as a risk factor for cardiac events in established coronary heart disease: a review of possible mechanisms // Ann Behav Med 1995; 17:142–149.
23. Cipriani A, Barbui C, Geddes JR. Suicide, depression, and antidepressants. Brit Med J 2005; 330:373–74.
24. Devenand DP, Pelton GH, Roose SP. Depressive features in dementia. In: Evidence–based Dementia Practice. Ed by N Qizilbash et al. Oxford: Blackwell Sciences 2002, p. 695–98.
25. Helzer E, Pryzbeck TR. The coocurrence of alcoholism with other psychiatric disorders in the general population and its impact of treatment. I Stud Alcohol 1998; 49 (3): 219–24.
26. House A. Defining, recognizing and managing depression in neurological practice. Pract Neurol 2003;3:196–203.
27. Hyttel I. Pharmacological characterization of selective serotonin reuptake inhibitors (SSRls). Int Clin Psychopharmacol 1994; 9 (suppl. 1): 19–26.
28. Katona C. Managing depression and anxiety in the elderly patient. Eur Neuropsychopharm 2000;10(Suppl. 4):S427–S432.
29. Lipowski Z. Somatization and depression// Psychosomatics. – 1988 – Vol. 31, № 1 – P. 13 – 21.
30. Navarro V, Gasto C, Lomena F, et al. Prognostic value of frontal functional neuroimaging in lateonset severe major depression. Brit J Psychiatr 2004;184:306–11.
31. Scott J. Treatment of chronic depression. New Engl J Med 2000:342:1518–20.
32. Shenal BV, Harrison DW, Demaree HA. The neuropsychology of depression: a literature review and preliminary model. Neuropsychol Rev 2003;13:33–42.
33. Snow V, Lascher S, Mottur–Pilson C. Pharmacologic treatment of acute major depression and dysthymia. Ann Int Med 2000;132:738–42.
34. Taylor G. Emotional expressiveness and psychosomatic process// Psychosomatic medicine and contemporary psychoanalysis(Ed. G. Taylor) – 1989 – P. 73– 113.
35. Tylee A. Depression in Europe: experience from the DEPRES II survey. Eur Neuropsychopharm 2000;10(Suppl. 4):S445–S448.












